噬菌体冻干粉制剂及其制备方法、保存方法和应用
文献发布时间:2023-06-19 12:11:54
技术领域
本发明属于生物药物制剂技术领域,具体涉及一种噬菌体冻干粉制剂及其制备方法、保存方法和应用。
背景技术
我国是水产养殖大国。近年来,我国的水产养殖业获得迅猛发展。随着海水养殖规模的日益扩大和集约化养殖方式的不断推广,疾病的频繁发生对水产规模化养殖的健康发展造成了严重的威胁。水产养殖的病原体主要包括细菌、病毒、寄生虫等,其中细菌性疾病是对危害程度较为严重的一类疾病。
弧菌是能运动的芽孢短杆状细菌,广泛分布于近海岸、河口海区海水及生物体内,是海洋中最常见的细菌类群之一,同时也是引起海水养殖鱼虾细菌性疾病最重要的病原菌。弧菌的致病强度与宿主的生理状态及水质环境条件等综合因素有关,属于条件性致病菌,其主要通过口或伤口感染,产生毒素,致使伤口肌肉溃烂化脓以及内脏器官的严重病变从而导致鱼虾类的死亡。
由弧菌引起的疾病又称弧菌病,具有“流行面积广、发病率高、致死性强”等特点,是水产养殖动物的主要疾病,同时也被确定为是阻碍水产养殖业发展的重要限制性因素,给养殖业造成了巨大的危害。其中以鳗弧菌(Vibrio anguillarum)、溶藻弧菌(Vibrioalginolyticus)、哈维氏弧菌(Vibrio harveyi)、副溶血弧菌(Vibrio parahaemolyticus)和杀鲑弧菌(Vibrio salmonicida)等弧菌引起的弧菌病被认为是鱼虾类养殖中最为严重的病害之一。早期死亡综合征(EMS)或肝胰腺急性坏死综合征是一种影响虾的相当新的疾病,该病于2009年首次在中国出现,2010年传播到越南,2011年传播到马来西亚和婆罗洲北部,2012年传播到泰国。2013年,EMS首次在亚洲以外报告,出现在墨西哥-由于从亚洲进口受感染的活虾。亚利桑那大学的研究已经确定,该疾病是由细菌剂副溶血弧菌引起的,副溶血弧菌通过口腔传播并定殖于虾的胃肠道,然后产生毒素,导致虾消化器官的组织破坏和功能障碍。
目前针对水产养殖相关动物疾病的预防和控制方法主要以化学抗生素法和免疫疫苗法,其中以化学抗生素使用为主。作为当前控制水产动物疾病的主要手段,化学抗生素法具有使用方便、见效快和疗效好等优点。但是,大批量频繁使用抗生素在控制病原菌的同时,极大了助长了病原菌的耐药性,并加速了广谱耐药菌的产生。这使得致病菌的耐药性问题日益严重。此外,化学药物残留也是导致人类食源性疾病产生的重要原因之一,对人类健康造成严重危害。
噬菌体(phage,bacteriophage)又称细菌性病毒,是一类专一性裂解细菌的病毒,在环境中分布广泛、种类多样、结构简单,具有很强的宿主特异性。最重要的一点,噬菌体裂解细菌的机制不受细菌耐药性的影响,其通过受体识别从而吸附在特定宿主菌表面,将自身遗传物质注入宿主体内进行自我复制组裝,并最终通过裂解宿主菌释放子代从而实现自我的生长繁殖。
由于噬菌体的专一性和其快速增殖的特点促使其成为治疗细菌性疾病的有力工具。首先,噬菌体的治疗具有特异性,可以针对某一特定有害细菌菌株有选择性的杀灭,从而使生物体内或其生活环境的正常菌群平衡受到最小程度的影响,相比抗生素,其对环境毒副作用小,也保证了食品安全;其次,噬菌体可以随宿主菌的增殖而增殖,并在细菌感染的整个过程中发挥作用,而不像抗生素那样随时间的推移疗效逐渐降低;第三,噬菌体冻干粉制剂获取方便,价格低廉。
利用噬菌体控制致病菌早在抗生素被发现之前就有应用,但由于对噬菌体的硏究不够充分而抗生素在当时具有广谱抑菌效果,且疗效好见效快,这使得噬菌体未被广泛应用。近年来,由于抗生素滥用引发的一系列耐药菌问题,使得噬菌体重新回归人们的视野,应用噬菌体控制致病菌的研究也在科学界引起了广泛兴趣。作为应对抗生素抗性的重要武器之噬菌体的临床应用潜力巨大,如目前已有公开报道噬菌体制剂,如液体制剂和冻干制剂,但是在实际使用和研究中发现,其在应用过程中仍存在一些潜在的缺点:噬菌体主要含有蛋白质和核酸,因此确保制备后运输和储存过程中噬菌体活性尤为关键,但是目前公开报道的噬菌体制剂所含噬菌体存活性不理想,而且保存时间短,其中,冻干制剂还存在复溶后噬菌体活性不理想的问题,限制了噬菌体制剂的应用。同时弧菌噬菌体主要用于水产养殖有其特殊性,产品使用过程会扩散到整个水体,因此不应有任何对环境有害的成分,并且也需要在成本以及工艺之间做出平衡。
发明内容
本发明的目的是提供一种噬菌体冻干粉制剂及其制备方法、保存方法和应用,旨在解决现有噬菌体冻干粉制剂所含噬菌体存活性不理想、保存时间短或进一步复溶后活性不理想的等技术问题。
为了实现上述发明目的,本发明一方面,提供了一种噬菌体冻干粉制剂。本发明噬菌体冻干粉制剂由含具有生物活性的噬菌体和冻干保护剂的混合溶液经冻干处理形成的冻干混合物;其中,在所述冻干混合物中,所述噬菌体的效价为10
优选地,冻干保护剂包括多羟基化合物、高分子复合保护剂中的至少一种。
进一步优选地,多羟基化合物包括蔗糖、山梨醇中的至少一种,高分子复合保护剂包括脱脂奶粉。
优选地,噬菌体为宿主是水产类病原菌的噬菌体。
进一步优选地,水产类病原菌包括弧菌。
进一步优选地,噬菌体包括溶藻弧菌噬菌体、副溶血弧菌噬菌体和大肠杆菌噬菌体中的至少一种。
本发明另一方面,提供了本发明噬菌体冻干粉制剂的制备方法,包括如下步骤:
将含噬菌体的溶液与所述冻干保护剂按比例进行混合处理,制备成混合溶液;
将所述混合溶液进行冻干处理形成冻干混合物,得到噬菌体冻干粉制剂。
优选地,冻干处理的条件为:
冻干温度为-30℃~-40℃,时间为18~36h,真空度为0.05~0.10mbar。
优选地,含噬菌体的溶液为噬菌体原液,且所述的噬菌体原液的制备方法包括如下步骤:
对宿主菌进行扩大培养,获得宿主菌液;
将噬菌体接种至所述宿主菌液中进行噬菌体培养,获得噬菌体培养液;
将所述噬菌体培养液进行分离处理,除去包括没有裂解的宿主菌的杂质,获得所述噬菌体原液。
进一步优选地,将噬菌体接种至所述宿主菌液中是按照MOI值为1~10比例将所述噬菌体接种至所述宿主菌液中。
进一步优选地,宿主菌液中,所述宿主菌浓度为10
进一步优选地,分离处理包括对噬菌体培养液进行离心处理获得上清液和将所述上清液采用微米滤膜过滤收集滤液的步骤。
本发明再一方面,提供了本发明噬菌体冻干粉制剂的保存方法。本发明噬菌体冻干粉制剂的保存方法包括如下步骤:
将所述噬菌体冻干粉制剂于4~27℃的温度下进行保存处理。
优选地,保存处理的温度为23~27℃。
本发明又一方面,提供了本发明噬菌体冻干粉制剂在水产养殖或制备水产养殖药物中的应用。
与现有技术相比,本发明噬菌体冻干粉制剂及其制备方法、保存方法和应用存在如下技术效果:
本发明噬菌体冻干粉制剂通过将冻干保护剂与具有生物活性的噬菌体一起冻干处理,并通过控制冻干保护剂与噬菌体含量比例控制,使得冻干保护剂能够对噬菌体起到保护作用,赋予噬菌体冻干粉制剂能够长期保存,且对保存条件要求低,从而提高了本发明噬菌体冻干粉制剂的运输和储存便利性,降低了本发明噬菌体冻干粉制剂的运输和储存的经济成本,而且能够保证噬菌体冻干粉制剂经过长期保存和进行复溶后噬菌体的活性高,从而提高了噬菌体冻干粉制剂实际应用性。另外,根据噬菌体的专一性,可以根据实际病原菌的种类而灵活控制噬菌体种类,实现有针对性的细菌性病害防治,不破坏环境中的其他菌群,不会对养殖动物以及消费者产生任何影响。与抗生素相比,不会导致病原菌出现抗药性现象。其次,本发明噬菌体冻干粉制剂不含有毒有害充分,而且也无药物残留,对环境无害。
本发明噬菌体冻干粉制剂制备方法只需将冻干保护剂与噬菌体形成的混合溶液进行冻干处理即可,其工艺条件易控,制备的噬菌体冻干粉制剂活性稳定,而且有效降低了制备成本。
本发明噬菌体冻干粉制剂由于能够长期稳定保存,且对保存条件要求低,复溶后活性高,从而提高了本发明噬菌体冻干粉制剂的运输和储存便利性,降低了本发明噬菌体冻干粉制剂的运输和储存的经济成本,有效提高了其实际应用性,特别是在水产养殖或制备水产养殖药物中的应用,专一性高,防治水产病原菌针对性强,且对水体无害,无药物残留,提高了水产产品的健康安全性和环境的安全性,且降低了经济成本。
附图说明
为了更清楚地说明本申请实施例中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本申请的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动性的前提下,还可以根据这些附图获得其他的附图。
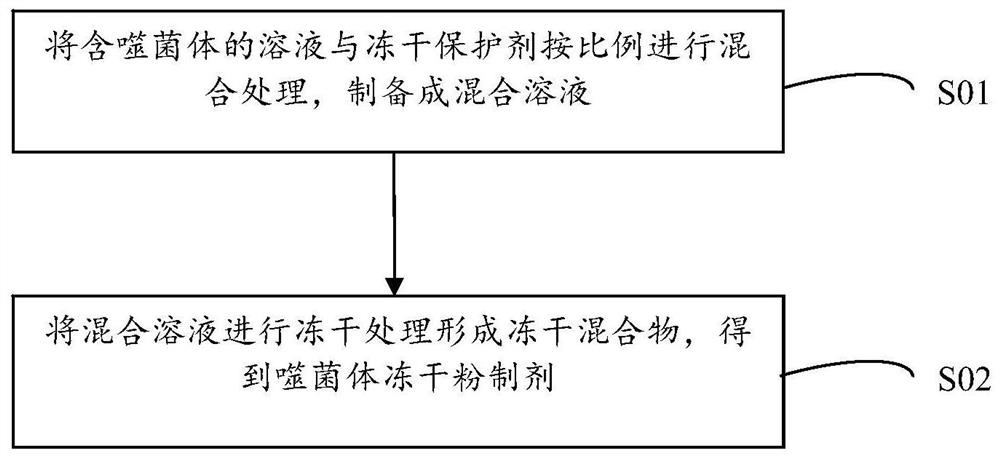
图1为本发明实施例噬菌体冻干粉制剂的制备方法流程示意图;
图2为本发明实施例1提供的溶藻弧菌噬菌体分别置于4℃、25℃±2℃环境保存6个月后效价柱状图;
图3为本发明实施例1提供的溶藻弧菌噬菌体与对照组对抑制溶藻弧菌抑菌效果曲线图。
具体实施方式
为使本发明实施例的目的、技术方案和技术效果更加清楚,对本发明实施例中的技术方案进行清楚、完整地描述,以下所描述的实施例是本发明一部分实施例,而不是全部的实施例。结合本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其它实施例,都属于本发明保护的范围。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行;所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
在本发明的描述中,术语“和/或”,描述关联对象的关联关系,表示可以存在三种关系,例如,A和/或B,可以表示:单独存在A,同时存在A和B,单独存在B的情况。其中A,B可以是单数或者复数。字符“/”一般表示前后关联对象是一种“或”的关系。
在本发明的描述中,“至少一个”是指一个或者多个,“多个”是指两个或两个以上。“以下至少一项(个)”或其类似表达,是指的这些项中的任意组合,包括单项(个)或复数项(个)的任意组合。例如,“a,b,或c中的至少一项(个)”,或,“a,b,和c中的至少一项(个)”,均可以表示:a、b、c、a-b(即a和b)、a-c、b-c、或a-b-c,其中a、b、c分别可以是单个,也可以是多个。
需要理解的是,本发明实施例中所提到的相关成分的重量不仅仅可以指代各组分的具体含量,也可以表示各组分间重量的比例关系,因此,只要是按照本发明实施例相关组分的含量按比例放大或缩小均在本发明公开的范围之内。具体地,本发明实施例中所述的重量可以是μg、mg、g、kg等化工领域公知的重量单位。
另外,除非上下文另外明确地使用,否则词的单数形式的表达应被理解为包含该词的复数形式。术语“包括”或“具有”旨在指定特征、数量、步骤、操作、元件、部分或者其组合的存在,但不用于排除存在或可能添加一个或多个其它特征、数量、步骤、操作、元件、部分或者其组合。
一方面,本发明实施例提供一种噬菌体冻干粉制剂。本发明实施例噬菌体冻干粉制剂由含具有生物活性的噬菌体和冻干保护剂的混合溶液经冻干处理形成的冻干混合物。
其中,本发明实施例噬菌体冻干粉制剂所含的噬菌体为具有生物活性的噬菌体。该具有生物活性的噬菌体是噬菌体冻干粉制剂的生物功能活性组分。这样,根据噬菌体的专一性,可以根据实际病原菌的种类而灵活控制噬菌体种类,实现有针对性的细菌性病害防治,不破坏环境中的其他菌群,不会对养殖动物以及消费者产生任何影响。与抗生素相比,不会导致病原菌出现抗药性现象。而且噬菌体冻干粉制剂不含有毒有害充分,而且也无药物残留,对环境无害。
实施例中,具有生物活性的为宿主是水产类病原菌的噬菌体。进一步地,该水产类病原菌包括但不仅仅为弧菌。此时,可以根据弧菌的种类选择对应的具有生物活性的噬菌体,从而实现本发明实施例噬菌体冻干粉制剂针对具体水产类病原菌如弧菌种类进行针对性防治与治疗。
实施例中,具有生物活性的噬菌体包括溶藻弧菌噬菌体、副溶血弧菌噬菌体和大肠杆菌噬菌体中的至少一种。具体实施例中,当噬菌体为溶藻弧菌噬菌体时,溶藻弧菌噬菌体为溶藻弧菌噬菌体ValSw4-1。根据噬菌体专一特点,当噬菌体冻干粉制剂所含的具有生物活性的噬菌体包括溶藻弧菌噬菌体如ValSw4-1时,噬菌体冻干粉制剂可以针对感染了溶藻弧菌的水产生物进行治疗或进一步防治。而且对其他菌类和水产生物无害,也无任何药物残留。
本发明实施例噬菌体冻干粉制剂所含的冻干保护剂与具有生物活性的噬菌体一起冻干处理形成冻干混合物,并通过控制冻干保护剂与噬菌体含量比例控制,使得冻干保护剂能够对噬菌体起到保护作用,赋予噬菌体冻干粉制剂能够长期保存,且对保存条件要求低,从而提高了本发明噬菌体冻干粉制剂的运输和储存便利性,降低了本发明噬菌体冻干粉制剂的运输和储存的经济成本,而且能够保证噬菌体冻干粉制剂经过长期保存和进行复溶后噬菌体的活性高,从而提高了噬菌体冻干粉制剂实际应用性。
实施例中,冻干保护剂包括多羟基化合物、高分子复合保护剂,具体实施例中,多羟基化合物包括蔗糖、山梨醇中的至少一种,高分子复合保护剂包括脱脂奶粉。经发明人研究发现,多羟基化合物具体如蔗糖、山梨醇,具有较高的玻璃化转变温度,对阻止蛋白质二级结构的改变、冻干处理过程中及贮藏期内蛋白质多肽链的伸展及聚集起着明显作用,从而能够显著提高噬菌体冻干粉制剂中噬菌体的生物活性。高分子复合保护剂如脱脂奶粉在冷冻干燥时,乳清蛋白能在菌体外形成蛋白膜,起到保护作用,且脱脂奶粉中其它成分也可提高噬菌体的冷冻干燥存活率,为冻干物提供轻而多孔的结构,因此,高分子复合保护剂如脱脂奶粉能够显著提高噬菌体冻干粉制剂中噬菌体的生物活性。
实施例中,具有生物活性的噬菌体和用于负载具有生物活性的噬菌体溶液可以是用于培养噬菌体后进行过滤处理收集的滤液。这样,采用该滤液作为溶剂载体更利于具有生物活性的噬菌体的活性稳定,与冻干保护剂组分之间起到协同增效作用,提高具有生物活性的噬菌体的生物活性的稳定,提高噬菌体冻干粉制剂在运输、储存中噬菌体的生物活性的稳定,且延长噬菌体的生物活性,从而延长噬菌体冻干粉制剂的储存时间并保证经长时间储存后依然保持高的生物活性。当然,混合溶液的溶液也可以用其他有利于噬菌体生物活性的其他试剂,如可以是但不仅仅为缓冲液。
因此,上述各实施例中噬菌体冻干粉制剂利用其所含的冻干保护剂对噬菌体起到生物活性的保护作用,以保证噬菌体的生物活性,特别是延长噬菌体的生物活性,赋予本发明实施例噬菌体冻干粉制剂在运输、储存和应用过程中的噬菌体的生物活性,实现对相应病原菌的治疗和防治的有效性和效果。而且噬菌体的专一特性,可以实现对环境中细菌性病害进行专一防治和治疗,不破坏环境中的其他菌群,不产生有毒有害成分,也无药物残留,对环境无害,不会对养殖动物以及消费者产生任何影响。而且能够对所含冻干保护剂的种类和含量的调整以提高噬菌体冻干粉制剂的生物活性稳定性和延长噬菌体的储存时间,并降低噬菌体冻干粉制剂的成本和应用成本。
另一方面,本发明实施例还提供了上文噬菌体冻干粉制剂的制备方法。本发明实施例噬菌体冻干粉制剂的制备方法流程如图1所示,包括如下步骤:
S01:将含噬菌体的溶液与冻干保护剂按比例进行混合处理,制备成混合溶液;
S02:将混合溶液进行冻干处理形成冻干混合物,得到噬菌体冻干粉制剂。
其中,步骤S01中的噬菌体为上文噬菌体冻干粉制剂所含的噬菌体,实施例中,含噬菌体的溶液可以是噬菌体原液。那么噬菌体应该是具有生物活性的噬菌体。因此,噬菌体种类如上文噬菌体冻干粉制剂所含的噬菌体种类,那么冻干保护剂也如上文噬菌体冻干粉制剂所含的冻干保护剂,为了节约篇幅,在此不再对步骤S01中的噬菌体和冻干保护剂的种类进行赘述。
实施例中,在步骤S01中混合处理过程中,含噬菌体的溶液与冻干保护剂的混合比例保证在制备的噬菌体冻干粉制剂中,噬菌体的效价为10
另外,步骤S01中混合处理可以是生物领域常规的混合处理,只要是能够使得含噬菌体的溶液与冻干保护剂混合均匀即可。如包括搅拌、振荡等。
实施例中,步骤S01中的含噬菌体的溶液为噬菌体原液时,该噬菌体原液由包括如下步骤的方法制备获得:
S011:对宿主菌进行扩大培养,获得宿主菌液;
S012:将噬菌体接种至宿主菌液中进行噬菌体培养,获得噬菌体培养液;
S013:将噬菌体培养液进行分离处理,除去包括没有裂解的宿主菌的杂质,获得噬菌体原液。
其中,步骤S011中的对宿主菌进行扩大培养可以根据宿主菌的种类或生物特性选择对应的扩大培养方法,以获得大量噬菌体宿主菌。如具体实施例中,可以按照如下扩大培养方法进行培养:
按1%~5%比例将宿主菌菌种转接于培养瓶中培养,培养条件为:温度30~37℃,转速220~250rpm,培养时间3~5个小时,使得宿主菌液浓度达到10
步骤S012中将噬菌体接种至步骤S011中的经过大量培养获得宿主菌中后,噬菌体会感染宿主菌,并在宿主菌内进行自我复制组裝,经过噬菌体培养后,以获得大量的噬菌体。在此过程中,宿主菌会随着噬菌体的自我复制而裂解,因此,在噬菌体培养过程中,宿主菌的含量会逐渐减少,而噬菌体的含量会逐渐增大。由于噬菌体的专一性,宿主菌应该是噬菌体对应的宿主菌。
实施例中,将噬菌体接种至宿主菌液中是按照MOI值为1~10比例将噬菌体接种至宿主菌液中。其中,用于接种的噬菌体可以是效价为10
步骤S012中的噬菌体培养应该是充分的,如按照上述宿主菌浓度和噬菌体接种的接种量,培养时间6~8小时,培养液逐渐变澄清,结束培养。
步骤S013中,将噬菌体培养液进行分离处理,以除去培养基和未发生裂解的宿主菌或可能的其他菌,从而获得纯的噬菌体溶液,也即是噬菌体原液。实施例中,步骤S013中的分离处理包括对噬菌体培养液进行离心处理获得上清液和将上清液采用微米滤膜过滤收集滤液的步骤。其中,微米滤膜应该是能够截留宿主菌的微米滤膜,如可以是0.22微米滤膜。
步骤S02中,经过在冻干处理过程步骤S01获得混合溶液所含的溶剂如水会被升华干燥,从而获得冻干混合物。实施例中,冻干处理的条件为:冻干温度为-30℃~-40℃,时间为18~36h,真空度为0.05~0.10mbar(5~10Pa)。具体的是先将温度调至预设的冻干温度如-30℃~-40℃,再将待冻干溶剂具体的是步骤S01中配制的混合溶液置于该预设的冻干温度中进行冻干处理。通过对该冻干处理的条件控制优化,能够有效保证混合溶液中噬菌体的活性,而且能够提高冻干处理效率。
上述本发明实施例噬菌体冻干粉制剂制备方法只需将冻干保护剂与噬菌体进行混合处理和冻干处理即可,其工艺条件易控,制备的噬菌体冻干粉制剂活性稳定,而且有效降低了制备成本。而且还能够通过对噬菌体的种类和冻干保护剂种类以及两者混合比例以实现提升噬菌体冻干粉制剂对细菌性病害的治疗和防治以及提高噬菌体冻干粉制剂的生物活性稳定性和延长储存时间。
再一方面,本发明实施例还提供了上文本发明实施例噬菌体冻干粉制剂的保存方法。本发明噬菌体冻干粉制剂的保存方法包括如下步骤:
将噬菌体冻干粉制剂于4~27℃的温度下进行保存处理。
基于上文本发明实施例噬菌体冻干粉制剂,其能够长期稳定保存,且对保存条件要求低,如能够在较宽的温度如4~27℃下进行保存,并能够有效保证噬菌体的生物活性,而且延长保存时间,从而提高了噬菌体冻干粉制剂的运输和储存便利性,降低了噬菌体冻干粉制剂的运输和储存的经济成本,有效提高了其实际应用性,并降低了其应用的成本。如经检测,上文本发明实施例噬菌体冻干粉制剂在4~27℃的温度保存6个月后,噬菌体存活率依然能够保持在91%以上。进一步,保存处理的温度为23~27℃。经检测,上文本发明实施例噬菌体冻干粉制剂在23~27℃的温度保存6个月后,噬菌体存活率仍有92%以的活性。因此,上文本发明实施例噬菌体冻干粉制剂为储存条件要求低,能够在常温下保持高生物活性,而且有效降低了储存的经济成本,同样也降低了运输的要求和经济成本,增强了本发明实施例噬菌体冻干粉制剂的应用性和降低了其应用的经济成本。
又一方面,本发明实施例提供了上文本发明噬菌体冻干粉制剂的应用,本发明噬菌体冻干粉制剂在水产养殖或制备水产养殖药物中的应用。如上文所述的,本发明实施例噬菌体冻干粉制剂由于能够长期稳定保存,且对保存条件要求低,从而提高了本发明实施例噬菌体冻干粉制剂的运输和储存便利性,并降低了本发明实施例噬菌体冻干粉制剂的运输和储存的经济成本,有效提高了其实际应用性,特别是在水产养殖或制备水产养殖药物中的应用,专一性高,防治水产病原菌针对性强,且对水体无害,无药物残留,提高了水产产品的健康安全性和环境的安全性,且降低了经济成本。
为使本发明上述实施细节和操作能清楚地被本领域技术人员理解,以及本发明实施例噬菌体冻干粉制剂及其制备方法的进步性能显著的体现,以下通过多个实施例来举例说明上述技术方案。
实施例1
本实施例提供了一种噬菌体冻干粉制剂及其制备方法,本实施例噬菌体冻干粉制剂包括溶藻弧菌噬菌体ValSw4和蔗糖冻干保护剂。其中,在噬菌体冻干粉制剂中,溶藻弧菌噬菌体ValSw4的效价为10.91×10
本实施例噬菌体冻干粉制剂制备方法包括步骤如下:
S1:溶藻弧菌噬菌体原液制备:
S11:按1%比例将溶藻弧菌菌种转接于培养瓶中培养,培养条件为:2216E培养基(2216E液体培养基经高压灭菌后冷却),温度30℃,转速220rpm,培养时间4个小时,菌液浓度为10
S12:按MOI=1向步骤S11的培养液中加入效价为10
S13:培养时间6小时,培养液开始变澄清,结束培养,获得溶藻弧菌噬菌体ValSw4-1培养液;
S14:步骤S13的噬菌体培养液经9000g离心10分钟,取上清液经0.22微米滤膜过滤获得无菌的溶藻弧菌噬菌体ValSw4-1原液,噬菌体浓度为10
S2:含有溶藻弧菌噬菌体ValSw4的原液与蔗糖冻干保存剂按照如下方法进行冻干处理,获得噬菌体冻干粉制剂:
S21:将步骤S1中的溶藻弧菌噬菌体ValSw4原液与0.3M的蔗糖按1:9比例混合,在-20℃冰箱中预冷冻3小时成固状待冷冻样品;
S22:开启Labconco冷冻干燥机制冷功能,待冷阱温度降到-40℃以下;
S23:将已凝固的待冷冻样品放入冷冻干燥机,冷冻干燥机开启抽真空模式,冷阱内气压达到0.07mbar,冷冻干燥36小时后即成溶藻弧菌噬菌体冻干粉,制得冻干粉噬菌体效价10.91×10
实施例2
本实施例提供了一种噬菌体冻干粉制剂及其制备方法,本实施例噬菌体冻干粉制剂包括溶藻弧菌噬菌体ValSw4和蔗糖冻干保护剂。其中,在噬菌体冻干粉制剂中,溶藻弧菌噬菌体ValSw4的效价为10.91×10
本实施例噬菌体冻干粉制剂制备方法包括步骤如下:
S1:溶藻弧菌噬菌体原液制备:
S11:按1%比例将溶藻弧菌菌种转接于培养瓶中培养,培养条件为:2216E培养基(2216E液体培养基经高压灭菌后冷却),温度30℃,转速220rpm,培养时间4个小时,菌液浓度为10
S12:按MOI=1向步骤S11的培养液中加入效价为10
S13:培养时间6小时,培养液开始变澄清,结束培养,获得溶藻弧菌噬菌体ValSw4-1培养液;
S14:步骤S13的噬菌体培养液经9000g离心10分钟,取上清液经0.22微米滤膜过滤获得无菌的溶藻弧菌噬菌体ValSw4-1原液,噬菌体浓度为10
S2:含有溶藻弧菌噬菌体ValSw4的原液与蔗糖冻干保存剂按照如下方法进行冻干处理,获得噬菌体冻干粉制剂:
S21:将步骤S1中的溶藻弧菌噬菌体ValSw4原液与1.0M的蔗糖按1:9比例混合,在-20℃冰箱中预冷冻3小时成固状待冷冻样品;
S22:开启Labconco冷冻干燥机制冷功能,待冷阱温度降到-40℃以下;
S23:将已凝固的待冷冻样品放入冷冻干燥机,冷冻干燥机开启抽真空模式,冷阱内气压达到0.07mbar,冷冻干燥36小时后即成溶藻弧菌噬菌体冻干粉,制得冻干粉噬菌体效价10.35×10
实施例3
本对比例提供了一种噬菌体冻干粉制剂,与实施例1相比,其冻干保护剂为山梨醇,其他不变。
本对比例噬菌体冻干粉制剂制备方法包括步骤如下:
S1:按照实施例的步骤S1制备溶藻弧菌噬菌体ValSw4原液:
S2:溶藻弧菌噬菌体ValSw4原液与山梨醇按照步骤S2中混合比例和冻干处理方法进行冻干处理,获得噬菌体冻干粉制剂。
实施例4
本对比例提供了一种噬菌体冻干粉制剂,与实施例1相比,其冻干保护剂为脱脂奶粉,其他不变。
本对比例噬菌体冻干粉制剂制备方法包括步骤如下:
S1:按照实施例的步骤S1制备溶藻弧菌噬菌体ValSw4原液;
S2:溶藻弧菌噬菌体ValSw4原液与脱脂奶粉按照步骤S2中混合比例和冻干处理方法进行冻干处理,获得噬菌体冻干粉制剂。
实施例5
本对比例提供了一种噬菌体冻干粉制剂,与实施例1相比,其噬菌体为大肠杆菌噬菌体,其他不变。
实施例6
本对比例提供了一种噬菌体冻干粉制剂,与实施例1相比,其冻干保护剂为副溶血弧菌噬菌体,其他不变。
对比例1
本对比例提供了一种噬菌体冻干粉制剂,与实施例相比,其不含蔗糖等冻干保护剂组分。
本对比例噬菌体冻干粉制剂制备方法包括步骤如下:
S1:按照实施例的步骤S1制备溶藻弧菌噬菌体ValSw4原液:
S2:溶藻弧菌噬菌体ValSw4原液按照步骤S2中冻干处理方法进行冻干处理,获得噬菌体冻干粉制剂。
对比例2
本实施例提供了一种噬菌体冻干粉制剂及其制备方法,本实施例噬菌体冻干粉制剂包括溶藻弧菌噬菌体ValSw4和蔗糖冻干保护剂。其中,在噬菌体冻干粉制剂中,溶藻弧菌噬菌体ValSw4的效价为10.91×10
本实施例噬菌体冻干粉制剂制备方法包括步骤如下:
S1:溶藻弧菌噬菌体原液制备:
S11:按1%比例将溶藻弧菌菌种转接于培养瓶中培养,培养条件为:2216E培养基(2216E液体培养基经高压灭菌后冷却),温度30℃,转速220rpm,培养时间4个小时,菌液浓度为10
S12:按MOI=1向步骤S11的培养液中加入效价为10
S13:培养时间6小时,培养液开始变澄清,结束培养,获得溶藻弧菌噬菌体ValSw4-1培养液;
S14:步骤S13的噬菌体培养液经9000g离心10分钟,取上清液经0.22微米滤膜过滤获得无菌的溶藻弧菌噬菌体ValSw4-1原液,噬菌体浓度为10
S2:含有溶藻弧菌噬菌体ValSw4的原液与蔗糖冻干保存剂按照如下方法进行冻干处理,获得噬菌体冻干粉制剂:
S21:将步骤S1中的溶藻弧菌噬菌体ValSw4原液与0.1M的蔗糖按1:9比例混合,在-20℃冰箱中预冷冻3小时成固状待冷冻样品;
S22:开启Labconco冷冻干燥机制冷功能,待冷阱温度降到-40℃以下;
S23:将已凝固的待冷冻样品放入冷冻干燥机,冷冻干燥机开启抽真空模式,冷阱内气压达到0.07mbar,冷冻干燥36小时后即成溶藻弧菌噬菌体冻干粉,制得冻干粉噬菌体效价9.95×10
噬菌体冻干粉制剂的相关性能实验
1.噬菌体冻干粉制剂所含冻干保护剂作用的比较实验:
将上述实施例1-实施例6和对比例1至对比例2的噬菌体冻干粉制剂分装后均置于25℃±2℃环境保存6个月。并按照如下方法进行检测溶藻弧菌噬菌体的效价和存活率(每组并列做7个样品,分别编号0、1、2、3、4、5、6,取均值):
间隔30天通过双层平板法测定噬菌体效价,具体方法是:从罐中取适量产品用2216E培养基10、10
表1
从表1和图2可以看出,实施例1至实施例6中含如蔗糖、山梨醇、脱脂奶粉作为冻干保护剂的噬菌体冻干粉制剂保存6个月后活性仍能具有高的存活率,如实施例1、实施例2分别高达92.59%和93.83%,活性保持90%以上,均高于对比例1中的噬菌体活性。基于成本考虑,相对实施例1和实施例2,实施例1是相对优选的。另外,对比ValSw4、大肠杆菌噬菌体和副溶血弧菌噬菌体,冻干保护对溶藻弧菌噬菌体的冻干保护作用效果相对要好,但是均能够对噬菌体起到有效的冻干保护作用,并能够在保证噬菌体冻干粉制剂于25℃±2℃环境保存6个月后依然有高的生物活性。
2.噬菌体冻干粉制剂保存温度实验:
将上述实施例1至实施例6的噬菌体冻干粉制剂分装后分别置于4℃、25℃±2℃环境保存6个月。按照1节噬菌体冻干粉制剂所含保护剂作用的比较实验中的方法分别检测溶藻弧菌噬菌体的效价和存活率(每组并列做7个样品,分别编号0、1、2、3、4、5、6,取均值)。其中,测得的实施例1的结果如图2和下述表2中所示:
表2
从表2和图2可以看出,本发明实施例溶藻弧菌噬菌体冻干粉制剂在4℃~25±2℃较宽的保存温度下均具有高的稳定性,其中,溶藻弧菌噬菌体保存6个月后依然保持在91%以上的存活率。其中,本发明实施例溶藻弧菌噬菌体冻干粉制剂中的溶藻弧菌噬菌体ValSw4-1在25±2℃环境中保存了6个月后活性最高,仍有92.59%的活性。基于本发明实施例噬菌体冻干粉制剂保存的存活率和保存以及运输的成本考虑,室温保存,如25±2℃是优选地。其他实施例提供的噬菌体冻干粉制剂保存温度实验与实施例1的接近,均在4℃和常温下具有高的存活率,其中,并理想的选择常温25±2℃下保存。
3.噬菌体冻干粉制剂的抑菌效果或生物活性实验:
将上述实施例1至实施例6提供的噬菌体冻干粉制剂分别按照如下方法进行抑菌效果实验,其中,以SM缓冲液为对照组:
1)96孔酶标板中每孔加入180μL 2216E培养基;
2)取0.5g本发明实施例噬菌体冻干粉制剂溶于1ml SM缓冲液,每孔加入10μL溶解后的噬菌体,每孔加入10μL培养到对数期的溶藻弧菌,设不加本品,加入10μL培养到对数期的溶藻弧菌及10μL SM缓冲液的对照组;
3)将酶标板放入EPOCH 2酶标仪中,30℃,线性震板,连续震荡培养24小时,每隔60分钟测定一次培养体系的OD600值。
其中,实施例1中溶藻弧菌噬菌体冻干粉制剂和对照组的测得结果如图3所示,由图3可知,本发明实施例溶藻弧菌噬菌体冻干粉制剂可抑制溶藻弧菌的生长达12小时。其他实施例提供的噬菌体冻干粉制剂基于保存温度实验的存在稳定性,其抑菌效果实验也具有高度生物活性,也可以实现长时间对对应的特异菌抑菌作用。
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
