一种人正常角膜上皮细胞的应用
文献发布时间:2023-06-19 18:27:32
技术领域
本发明涉及细胞生物学技术领域,尤其涉及一种人正常角膜上皮细胞的应用。
背景技术
目前进入临床研究和已投入市场的抗SARS-CoV-2(新型冠状病毒)药物主要分为小分子药物和中和抗体类药物,无论哪种药物的研发都需要细胞实验和动物实验提供基础理论数据。
用于SARS-CoV-2感染的细胞模型种类有限且都具备局限性,大体可分为细胞系和原代细胞两类。Vero、Huh7和稳定转染人ACE2的各种细胞系属于最常见的新型冠状病毒细胞感染模型,该类模型支持SARS-CoV-2和变异株的感染和复制,但永生化的细胞系大多来源于其他动物或癌细胞,与正常人体细胞在遗传层面和生理生化上具有差异性,并不能完全模拟病毒感染人体的全部过程。例如在Vero细胞中筛选发现的抗病毒药物羟氯喹在人体实验中发现并不具备治疗效果,原因是在人体中SARS-CoV-2利用TMPRSS2 介导感染而在Vero细胞中则利用组织蛋白酶L。原代细胞感染模型例如人Ⅱ型肺泡上皮细胞(ATⅡ)或人上呼吸道上皮细胞属于天然的SARS-CoV-2 易感细胞。但来源于人和哺乳动物的原代上皮细胞的体外培养十分困难。一方面用于原代细胞培养的细胞培养基成分复杂价格高昂,另一方面大多只能进行短期的原代培养和有限的传代培养,部分细胞甚至根本不能体外培养。而且从每个动物或活体组织样品中获得的原代细胞产量仍然很低,包括细胞的数量、直接分离或短期培养的细胞纯度都是很低的,这些原代和传代细胞的增殖速度也极为有限。以ATⅡ为例,人肺泡上皮细胞中仅有 15%的细胞为ATⅡ细胞,且在体外的分离培养中ATⅡ极易分化成为不能被病毒感染的ATⅠ,目前产业化的ATⅡ使用专用的培养基也仅能传代培养5 代,很难大规模进行病毒感染实验和药物筛选实验。
因此,现有用于SARS-CoV-2感染的细胞还有待于改进和发展。
发明内容
鉴于上述现有技术的不足,本发明的目的在于提供一种基于人正常角膜上皮细胞,该细胞支持新型冠状病毒及其变异株的感染与复制,旨在解决现有用于SARS-CoV-2感染的细胞种类有限且都具备局限性的问题。
一种人正常角膜上皮细胞在新型冠状病毒生活周期研究中的应用;所述人正常角膜上皮细胞的分类命名为人正常角膜上皮细胞HNCEC/HL-008, 保藏于中国典型培养物保藏中心,保藏编号为CCTCC NO:C201550。
可选地,所述的人正常角膜上皮细胞在新型冠状病毒生活周期研究中的应用,其中,所述新型冠状病毒包括:野生型SARS-CoV-2、B.1.617.2 突变株以及B.1.1.529.2突变株。
一种人正常角膜上皮细胞在抗病毒药物筛选与药物机制研究中的应用;所述人正常角膜上皮细胞的分类命名为人正常角膜上皮细胞 HNCEC/HL-008,保藏于中国典型培养物保藏中心,保藏编号为CCTCC NO:C201550。
可选地,所述的人正常角膜上皮细胞在抗病毒药物筛选与药物机制研究中的应用,其中,所述新型冠状病毒包括:野生型SARS-CoV-2、B.1.617.2 突变株以及B.1.1.529.2突变株。
一种人正常角膜上皮细胞在新型冠状病毒中和抗体研究中的应用;所述人正常角膜上皮细胞的分类命名为人正常角膜上皮细胞HNCEC/HL-008, 保藏于中国典型培养物保藏中心,保藏编号为CCTCC NO:C201550。
可选地,所述的人正常角膜上皮细胞在新型冠状病毒中和抗体研究中的应用,其中,所述新型冠状病毒包括:野生型SARS-CoV-2、B.1.617.2 突变株以及B.1.1.529.2突变株。
有益效果:与现有技术相比,本发明提供的人正常角膜上皮细胞具有高水平的SARS-CoV-2相关受体蛋白ACE2和TMPRSS2的表达,该细胞能够在体外长期传代培养并支持SARS-CoV-2感染复制,是国内外尚未报道过的一种新的可用于研究SARS-CoV-2及其变异株感染复制的细胞模型,可用于大规模抗病毒药物筛选和机制研究。
附图说明
图1是人正常角膜上皮细胞的ACE2蛋白免疫荧光图。
图2是人正常角膜上皮细胞的TMPRSS2蛋白免疫荧光图。
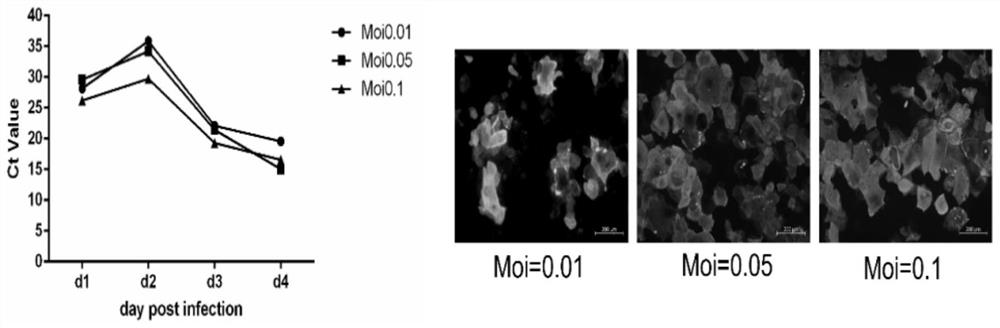
图3中是人正常角膜上皮细胞感染野生型SARS-CoV-2后病毒复制水平曲线,细胞内病毒NP蛋白免疫荧光图。
图4中4-1是人正常角膜上皮细胞感染B.1.617.2(Delta)后病毒复制水平曲线,4-2是细胞内病毒NP蛋白免疫荧光图。
图5中5-1是人正常角膜上皮细胞感染B.1.1.529.2(Omicron BA.2) 后病毒复制水平曲线,5-2是细胞内病毒NP蛋白免疫荧光图。
具体实施方式
本发明提供一种人正常角膜上皮细胞的应用,为使本发明的目的、技术方案及效果更加清楚、明确,以下对本发明进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
本发明中的人正常角膜上皮细胞分离培养自中国人的正常角膜缘组织的正常角膜上皮细胞,染色体为二倍体,STR(短串联重复序列)基因型以 22个“STR基因座/等位基因长度”来表示:Amel/X,CSF1PO/10/12, D10S1248/13/15,D12S391/18/20,D13S317/8/12,D16S539/10/11, D18S51/16/17,D19S433/13/14,D21S11/30,D2S1338/18/25,D2S441/10/11, D3S1358/15/17,D5S818/11,D6S1043/14/21.3,D7S820/9/12, D8S1179/13/15,FGA/22/25,Penta D/10/11,Penta E/11/15,TH01/9, TPOX/9/11,vWA/14。
所述的人正常角膜上皮细胞的培养条件优选为用HL培养基于37℃、5% CO
所述的人正常角膜上皮细胞的病毒感染条件优选为37℃、5% CO
所述人正常角膜上皮细胞的病毒核酸提取条件优选为天隆核酸提取仪GeneRotex 96和天隆核酸提取试剂盒,RNA反转录条件优选为TAKARA PrimeScript RTreagent KIT,Real Time PCR优选条件选为Biorad CFX 荧光定量PCR仪和iTaq UniverSYBR Green Supermix,引物序列为: Spike-forward,5-CAATGGTTTAACAGGCACAGG-3,Spike-reverse, 5-CTCAAGTGTCTGTGGATCACG-3′。
示例性地,上述人正常角膜上皮细胞的原代分离培养方法,包括如下步骤:
(1)在病人或病人监护人知情同意的情况下,收集胬肉患者手术切除的胬肉旁正常角膜缘组织样品。
(2)用95-100%(v/v)的乙醇洗分离的组织样品,再用PBS(0.01M, pH 7.4)洗,然后将组织样品放入含预冷PBS的无菌培养皿中,在解剖显微镜下,用解剖镊子和剪刀去除组织样品中残留的脂肪。
(3)将组织样品用消化液消化;优选的,所述的消化液为含胶原酶和分散酶的HL培养基。
(4)消化后的组织离心去上清,将细胞沉淀重悬于0.25%(质量体积比)胰酶-EDTA中消化。
(5)加入含10%(v/v)FBS的DMEM培养基,离心去上清。
(6)加入温水浴的分散酶和DNase I,用枪头反复吹打样品。
(7)再加入含10%(v/v)FBS的DMEM培养基,用40-70μm孔径的过滤器过滤细胞悬液,收集过滤后的细胞悬液,离心去上清。
(8)重悬细胞沉淀于HL培养基中,接种于培养瓶培养,得到人正常角膜上皮细胞。
具体地,人正常角膜上皮细胞的原代分离培养方法,
步骤(2)中,所述的预冷优选为在冰上预冷。
步骤(3)中,所述的消化液的用量优选为10倍于组织样品体积。
步骤(3)中,所述的消化的条件优选为37℃消化1-3小时。
步骤(3)中,所述的胶原酶和分散酶的浓度优选为均为0.2mg/mL。
步骤(4)中,所述的消化优选为冰上消化1小时或室温消化10分钟。
步骤(6)中,所述的温水浴优选为37℃的温水浴。
步骤(4)、(5)、(7)中,所述的离心优选为1000rpm离心5分钟。
步骤(8)中,所述的培养的条件优选为37℃、5% CO
上述人正常角膜上皮细胞的传代培养方法,包括如下步骤:
(1)当人正常角膜上皮细胞增殖至70-90%丰度时,用1×PBS(0.01M, pH 7.4)洗涤细胞,再用0.05%(质量体积比)胰酶-EDTA消化单层细胞。
(2)加入DMEM中和消化反应;离心去上清,用HL培养基重悬细胞沉淀,接种于培养瓶培养。
具体地,人正常角膜上皮细胞的传代培养方法
步骤(1)中,所述的消化的时间优选为2-5分钟。
步骤(2)中,所述的离心优选为1000rpm离心5分钟。
步骤(2)中,所述的培养的条件优选为37℃、5% CO
上述人正常角膜上皮细胞可用于人正常细胞的生理学研究,体外正常细胞的药物毒性研究和检测,角膜和角膜相关疾病包括病毒性角膜炎的发病机理研究。
本发明相对于现有技术具有如下优点和效果:
(1)本发明提供的人正常角膜上皮细胞,原代分离培养自人的正常角膜组织,该细胞未导入任何外源基因,经核型分析鉴定为人的正常二倍体细胞。经STR基因分型鉴定,是国内外从未登记注册过的一种人的正常细胞系。
(2)本发明提供的人正常角膜上皮细胞,显微镜下观察细胞的形态为排列紧密、细胞界限清晰、立体感强、多角型的上皮细胞,这种均一的细胞形态一直保持到65天,而且仍能处于增殖状态正常生长。
实施例1
人正常角膜上皮细胞ACE2蛋白的免疫荧光检测
(1)人正常角膜上皮细胞在T25或T75细胞培养瓶中生长至汇合度 70%-90%时,使用0.05%的胰蛋白酶消化制备单细胞悬液,接种于24孔板,每孔接种细胞悬液0.5mL,细胞数50000/孔,于37℃、5% CO
(2)细胞铺板24小时后吸去孔中溶液,每孔使用0.5mL室温平衡后的PBS缓冲液清洗3次。
(3)吸去PBS缓冲液后,每孔加入0.2mL 4%多聚甲醛细胞固定液室温固定20-30min,吸去多聚甲醛细胞固定液后,每孔使用0.5mL室温平衡后的PBS缓冲液清洗3次。
(4)吸去PBS缓冲液后,每孔加入0.2mL细胞通透剂(索莱宝生物),室温通透20-30min,吸去细胞通透剂后,每孔使用0.5mL室温平衡后的PBS 缓冲液清洗3次。
(5)吸去PBS缓冲液后,每孔加入0.2mL 10%(v/v)胎牛血清的PBS 缓冲液室温封闭1小时。
(6)吸去封闭液后,每孔加入0.2mL含有anti-ACE2(ab272500)的 PBS缓冲液,抗体与PBS比例为1:500(v/v),4℃孵育12小时。
(7)吸去抗体孵育液,每孔使用0.5mL室温平衡后的PBS缓冲液清洗 3次后,加入0.2mL体积比为1:1000(v/v)的山羊抗兔lgG H&L(ab150077) PBS缓冲液,室温避光孵育1小时。
(8)吸去抗体孵育液后,每孔加入0.2mL DAPI即用型溶液(索莱宝生物),室温避光孵育10min。
(9)避光条件下吸去DAPI孵育液,每孔使用0.5mL室温平衡后的PBS 缓冲液清洗3次后,重新补加0.1mL/孔的PBS缓冲液,在荧光显微镜下观察细胞核以及胞内ACE2蛋白表达量和分布。
(10)显微镜下分别使用4x、10x、20x物镜观察,每个放大倍数至少观察3个视野,每个视野至少包括>10的细胞数,具有代表性的免疫荧光图见图1,所述的人正常角膜上皮细胞具有高水平的ACE2蛋白表达。
实施例2
人正常角膜上皮细胞TMPRSS2蛋白的免疫荧光检测
实施步骤与实施例1相同,将实施例1步骤6中的anti-ACE2(ab272500) 替换为Anti-TMPRSS2(ab280567)。显微镜下分别使用4x、10x、20x物镜观察,每个放大倍数至少观察3个视野,每个视野至少包括>10的细胞数,具有代表性的免疫荧光图见图2,所述的人正常角膜上皮细胞具有高水平的 TMPRSS2蛋白表达。
实施例3
野生型新冠病毒感染实验
(1)人正常角膜上皮细胞在T25或T75细胞培养瓶中生长至汇合度 70%-90%时,使用0.05%的胰蛋白酶消化制备单细胞悬液,接种于48孔板,每孔接种细胞悬液0.2mL,细胞数40000/孔,于37℃、5% CO
(2)24小时后将细胞培养板转移至BSL-3实验室进行病毒感染实验。
(3)使用PI培养基稀释野生型SARS-CoV-2原液,最终病毒滴度分别为4000copies/mL、20000copies/mL和40000copies/mL三个滴度梯度。
(4)吸去48孔板细胞培养上清,设置病毒感染梯度组,包括:病毒感染滴度Moi=0.01、Moi=0.05和Moi=0.1,每个梯度设置3个平行孔,同时设置空白对照组3孔;Moi=0.01组每孔加入0.1mL的4000copies/mL病毒感染液,Moi=0.05每孔加入0.1mL的20000copies/mL病毒感染液, Moi=0.1组每孔加入0.1mL的40000copies/mL病毒感染液,空白对照组每孔加入0.1mL PI培养基。
(5)将48孔板转移至37℃、5% CO
(6)在感染后1、2、3、4天分别使用天隆核酸提取试剂盒提取各孔细胞上清(0.2mL/孔)核酸,并每天补加0.2mL新鲜HL培养基。
(7)在感染后第4天使用室温平衡后的PBS清洗细胞3次后,使用4%的多聚甲醛固定液浸泡48孔板,在4℃冰箱浸泡至少48h完全灭活新冠病毒后从BSL-3实验室中取出;上清核酸提取完成后使用2000mg/mL含氯消毒液和75%酒精消毒液喷洒表面后,从BSL-3实验室中取出。
病毒核酸的检测
(1)使用超微量分光光度计检测上清核酸浓度,并使用TAKARA PrimeScript RTreagent KIT反应体系进行逆转录,反应条件为:1.37℃ 15min(逆转录反应),2.85℃5s(酶失活反应),3.4℃(保持)。
(2)使用iTaq Univer SYBR Green Supermix反应体系对逆转录产物cDNA进行定量分析,反应条件为:1.95℃2min,2.95℃45s,3.60℃30s, 4.72℃45s,5.72℃10min,2-4共计40个循环。
(3)对各孔核酸的Ct值进行分析并用GraphPad Prism 6作图,见图 3所示,野生型SARS-CoV-2感染人正常角膜上皮细胞后上清中能检测到随感染时间变长而逐渐增高的病毒核酸量,且高Moi的病毒具有更高的感染效率。
细胞内病毒NP蛋白的检测
(1)吸去48孔板中的多聚甲醛固定液,使用室温平衡后的PBS清洗细胞至少3次,每孔加入0.1mL的细胞通透剂(索莱宝生物)室温透膜 20-30min。
(2)吸去细胞通透剂后,使用室温平衡后的PBS清洗细胞3次,每孔加入0.1mL 10%(v/v)胎牛血清的PBS缓冲液室温封闭1小时。
(3)吸去封闭液后,每孔加入0.1mL含有SARS-CoV-2Nucleocapsid Antibody(Sinobiological 40143-R004)的PBS缓冲液,抗体与PBS比例为1:250(v/v),4℃孵育12小时。
(4)吸去抗体孵育液,每孔使用0.2mL室温平衡后的PBS缓冲液清洗 3次后,加入0.1mL体积比为1:1000(v/v)的山羊抗兔lgG H&L(ab150077) PBS缓冲液,室温避光孵育1小时。
(5)吸去荧光二抗孵育液,在避光条件下每孔使用0.2mL室温平衡后的PBS缓冲液清洗3次后,每孔补加0.1mL PBS浸没细胞,在荧光显微镜下观察细胞内的病毒NP蛋白。
(6)使用荧光显微镜在10x物镜下对不同病毒梯度孔进行观察,每孔观察至少3个不同视野,具有代表性的免疫荧光图见图3,野生型 SARS-CoV-2感染人正常角膜上皮细胞后第4天,细胞内有高水平病毒NP蛋白表达,且随着病毒感染滴度的增高具有依赖性,图3从左至右3个图分别为Moi=0.01、Moi=0.05、Moi=0.1病毒感染滴度。
实施例4
Delta株SARS-CoV-2(B.1.617.2)感染人正常角膜上皮细胞
病毒感染、病毒核酸的检测与细胞内病毒NP蛋白的检测与实施例3相同,仅将野生型病毒替换为B.1.617.2。上清病毒核酸结果如图4-1所示,随感染时间延长,上清病毒拷贝数呈现增长趋势,高Moi=0.1组在感染后第4天Ct值升高,经镜检观察细胞出现明显CPE,导致病毒复制减弱。细胞内NP免疫荧光结果如图4-2所示,感染后第4天Moi=0.01组约有60%细胞中检测到NP蛋白存在,Moi=0.05和Moi=0.1组NP蛋白阳性率超过90%。
实施例5
奥密克戎BA.2株SARS-CoV-2(B.1.1.529.2)感染人正常角膜上皮细胞
病毒感染、病毒核酸的检测与细胞内病毒NP蛋白的检测与实施例3相同,仅将野生型病毒替换为B.1.1.529.2。上清病毒核酸结果如图5-1所示,随感染时间延长,上清病毒拷贝数呈现增长趋势,高Moi=0.05和Moi=0.1 组在感染后第4天Ct值明显比Moi=0.01组低,表明人正常角膜上皮细胞对B.1.1.529.2具有易感性。细胞内NP免疫荧光结果如图4-2所示,感染后第4天Moi=0.01组约有30%细胞中检测到NP蛋白存在,Moi=0.05和 Moi=0.1组NP蛋白阳性率约为50%。
综上所述,本发明提供的一种人正常角膜上皮细胞在SARS-CoV-2生活周期研究、抗病毒药物筛选与药物机制研究以及抗体研究中的应用。所述的人正常角膜上皮细胞具有高水平的SARS-CoV-2相关受体蛋白ACE2和 TMPRSS2的表达,该细胞能够在体外长期传代培养并支持SARS-CoV-2感染复制,是国内外尚未报道过的一种新的可用于研究SARS-CoV-2及其变异株感染复制的细胞模型,可用于大规模抗病毒药物筛选和机制研究。
应当理解的是,本发明的应用不限于上述的举例,对本领域普通技术人员来说,可以根据上述说明加以改进或变换,所有这些改进和变换都应属于本发明所附权利要求的保护范围。
