一种艾塞那肽人血清白蛋白融合蛋白的纯化方法
文献发布时间:2023-06-19 09:49:27
技术领域
本发明属于生物技术与制药工程技术领域,具体涉及一种艾塞那肽人血清白蛋白融合蛋白的纯化方法。
背景技术
艾塞那肽(Exenatide)是在南美洲钝尾毒蜥唾液中发现的一种胰高血糖素样肽-1(GLP-1)的类似物,分子量为4186.6kDa。艾塞那肽N端9个氨基酸与人糖高血糖素样肽-1高度同源,可以与人GLP-1受体结合,发挥与人GLP-1同样的生理功能,但其生物活性比人GLP-1更高更稳定,具有保护胰岛、促进胰岛素分泌、促进糖利用、减少肝糖原分解、降低血糖等作用,其促胰岛素分泌作用为血糖依赖的,不会引起低血糖反应,故被称为智慧型降血糖药,被广泛用于治疗II型糖尿病。但由于艾塞那肽的分子量小,体内半衰期只有60-90分钟,在体内维持药效时间短,患者每天需要注射2次才能达到满意的治疗效果,使用不方便,限制了其临床治疗的依从性和治疗价值。
为解决艾塞那肽药效时间短的问题,本发明的申请人将编码艾塞那肽的基因与编码人血清白蛋白基因连接在一起,构建了一个在酿酒酵母中外分泌表达艾塞那肽人血清白蛋白融合蛋白的工程酵母菌Ex-HSA/CICIM Y0600,临床试验表明,艾塞那肽人血清白蛋白融合蛋白在人体内的半衰期可长达100小时,体内药效可维持一周或更长时间,糖尿病患者只需一周注射一次艾塞那肽人血清白蛋白融合蛋白即可获得良好的治疗效果,预计艾塞那肽人血清白蛋白融合蛋白将是一个杰出的II型糖尿病长效治疗药物,是我国具有自主知识产权的1.0类创新药,将为我国II型糖尿病的患者带来福音。
由于艾塞那肽人血清白蛋白融合蛋白是一个全新的蛋白,其结构与理化特性有其特殊性,需要建立一套适合的纯化方法来制备高纯度的艾塞那肽人血清白蛋白融合蛋白,为临床制剂的规模化生产提供充足的原料药。
发明内容
为解决现有技术中存在的技术问题,本发明的目的在于提供一种艾塞那肽人血清白蛋白融合蛋白的纯化方法。
为实现上述目的,达到上述技术效果,本发明采用的技术方案为:
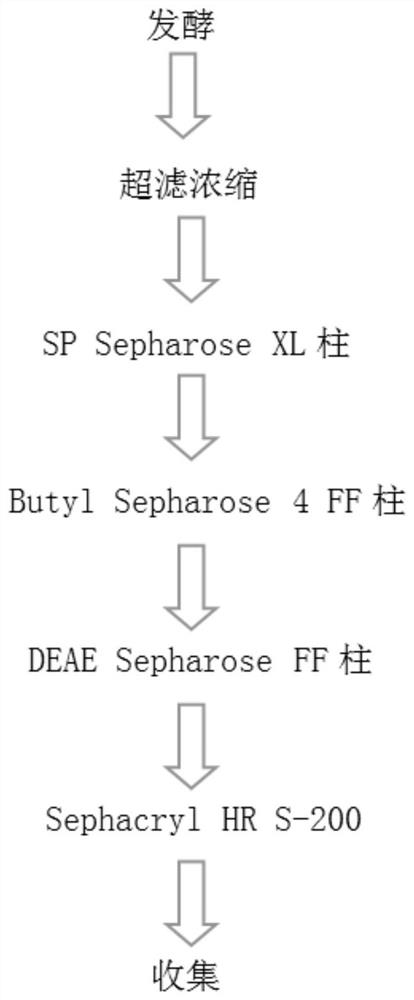
一种艾塞那肽人血清白蛋白融合蛋白的纯化方法,包括以下步骤:将重组表达的艾塞那肽人血清白蛋白融合蛋白的酵母发酵上清液经过超滤浓缩后,依次过离子柱、疏水柱和离子柱进行纯化,最后过分子筛进行除盐;所述离子柱至少为一个强阴离子柱和/或一个弱碱性阴离子柱,在两个离子柱之间用疏水柱进行一次纯化。
进一步的,所述重组表达的艾塞那肽人血清白蛋白融合蛋白的酵母发酵上清液经过超滤浓缩后,依次过SP Sepharose XL离子柱、Butyl Sepharose 4FF疏水柱、DEAESepharose FF离子柱进行纯化,随后过Sephacryl HR S-200分子筛进行除盐。
进一步的,所述SP Sepharose XL离子柱纯化步骤包括:
1)超滤与样本处理
重组表达的艾塞那肽人血清白蛋白融合蛋白的酵母发酵上清液进行超滤浓缩,得到浓缩样本,加稀释液,使电导率为2~5s/cm,随后加醋酸钠至终浓度为10-40mM,调节pH值至4.9±0.5;
2)装柱与柱处理
按照每升发酵液装柱10~20mL SP Sepharose XL树脂,水洗3~5个柱体积,再用NaOH清洗2-5个柱体积,随后水洗至pH小于9;
3)柱平衡
用平衡缓冲液平衡柱至电导率和pH与平衡缓冲液a一致;
4)上样
处理好的发酵液加载到平衡好的SP Sepharose XL离子柱中;
5)洗涤
用平衡缓冲液a清洗柱3~5个柱体积;
6)洗脱
用洗脱缓冲液a洗脱目的蛋白,收集洗脱峰。
进一步的,所述平衡缓冲液a为:5mM辛酸钠、5mM EDTA、20mM NaAC,pH为4.0-5.5,电导率小于5ms/cm;所述洗脱缓冲液a为:5mM辛酸钠、5mM EDTA、20mM NaAC、400mM NaCl,pH为4.0-5.5。
进一步的,所述Butyl Sepharose 4FF疏水柱纯化步骤包括:
1)装柱及柱处理
按照每毫升树脂吸附10-20mg蛋白样品装填Butyl Sepharose 4FF疏水柱,去乙醇,再用NaOH清洗2-5个柱体积,去碱;
2)样品处理
将SP Sepharose XL离子柱纯化后得到的艾塞那肽人血清白蛋白融合蛋白样品加NaCl至终浓度2-3M,调pH至4.0-7.0,电导率大于150ms/cm;
3)上样
将上述步骤2)处理好的样品上柱,线性流速小于150cm/h;
4)洗涤
上样完成后,用平衡缓冲液b清洗3~5个柱体积;
5)洗脱
用洗脱缓冲液b洗脱目标蛋白,收集洗脱峰。
进一步的,所述平衡缓冲液b为:20mM pH 6.5~7.5的PB、5mM辛酸钠,电导小于5ms/cm;所述洗脱缓冲液b为20mM PB、5mM辛酸钠、200mM氯化钠,pH 6.5~6.8。
进一步的,所述DEAE Sepharose FF离子柱纯化步骤包括:
1)装柱及柱处理
按照每毫升树脂吸附30~50毫克蛋白样品装柱,去乙醇,再用NaOH清洗30-90min,随后去碱;
2)样品处理
将Butyl Sepharose 4FF疏水柱层析中收集的目的洗脱峰用超滤方法脱盐,调节样品的缓冲液浓度为10-40mM PB,pH为6.0-8.0,电导小于5ms/cm;
3)上样
将处理好的DEAE Sepharose FF样品上样,线性流速为300~600cm/h;
4)洗涤
用平衡缓冲液c清洗3~5个柱体积;
5)洗脱
用洗脱缓冲液c洗脱目标蛋白,收集洗脱峰。
进一步的,所述平衡缓冲液c为:20mM pH 6.5~7.5的PB、5mM辛酸钠,电导率小于5ms/cm;所述洗脱缓冲液c为:20mM PB、5mM辛酸钠、200mM NaCl,pH 6.5~6.8。
进一步的,所述Sephacryl HR S-200分子筛除盐步骤包括:
1)装柱及柱处理
去乙醇,再用NaOH洗30-90min,随后去碱;用平衡缓冲液d平衡柱至流出液的电导率和pH与平衡缓冲液d一致;
2)上样
将DEAE洗脱液上样,上样量小于柱体积的5%,流速1-10mL/min;
3)洗涤
用平衡缓冲液d进行洗脱,收集主峰。
进一步的,所述平衡缓冲液d为:10mM PB、5mM NaCl;pH 7.0±0.5。
进一步的,所述艾塞那肽人血清白蛋白来源于艾塞那肽人血清白蛋白融合蛋白重组表达质粒转化酿酒酵母受体菌,经过发酵收集的上清液。
与现有技术相比,本发明的有益效果为:
本发明公开了一种艾塞那肽人血清白蛋白融合蛋白的纯化方法,包括以下步骤:将重组表达的艾塞那肽人血清白蛋白融合蛋白的酵母发酵上清液经过超滤浓缩后,依次过离子柱、疏水柱和离子柱进行纯化,最后过分子筛进行除盐;所述离子柱至少为一个强阴离子柱和/或一个弱碱性阴离子柱,在两个离子柱之间用疏水柱进行一次层析纯化。本发明提供的艾塞那肽人血清白蛋白融合蛋白的纯化方法,根据艾塞那肽人血清白蛋白融合蛋白的理化特性特征,建立了发酵、超滤浓缩、强阴离子胶吸附分离、疏水胶与离子交换去杂质、分子筛去内毒素除盐的优化纯化工艺,获得高纯度的重组艾塞那肽人血清白蛋白融合蛋白,纯度达到98%以上,使生产的纯化重组艾塞那肽人血清白蛋白融合蛋白的纯度符合质量标准的要求。
附图说明
图1为本发明的纯化工艺流程图;
图2为本发明HPLC分子筛法对艾塞那肽人血清白蛋白融合蛋白纯度分析图。
具体实施方式
下面对本发明的实施例进行详细阐述,以使本发明的优点和特征能更易于被本领域技术人员理解,从而对本发明的保护范围做出更为清楚明确的界定。
如图1-2所示,一种艾塞那肽人血清白蛋白融合蛋白的纯化方法,包括以下步骤:将重组表达的艾塞那肽人血清白蛋白融合蛋白的酵母发酵上清液经过超滤浓缩后,依次过离子柱、疏水柱、离子柱进行层析纯化,最后经分子筛除盐;离子柱至少为一个强阴离子柱和/或一个弱碱性阴离子柱,在两个离子柱之间用疏水柱进行一次纯化。
疏水柱前的离子柱层析交换介质为SP Sepharose XL;疏水柱层析交换介质为Butyl Sepharose 4FF;疏水柱后的离子柱层析交换介质为DEAE Sepharose FF;分子筛介质为Sephacryl HR S200。
SP Sepharose XL离子柱纯化艾塞那肽人血清白蛋白融合蛋白:
1.1、艾塞那肽人血清白蛋白来源:
艾塞那肽人血清白蛋白融合蛋白重组表达质粒转化酿酒酵母受体菌,经过发酵收集的上清液。
1.2、溶液配制
(1)超滤浓缩稀释液:2mM辛酸钠、2mM EDTA;预冷至10℃以下,备用;
(2)SP Sepharose XL离子柱平衡缓冲液a:5mM辛酸钠、5mM EDTA、20mM NaAC;pH4.9,电导小于5ms/cm;
(3)洗脱缓冲液a为:5mM辛酸钠、5mM EDTA、20mM NaAC、400mM NaCl;pH 4.9;
(4)2M NaCl溶液
(5)20%乙醇溶液
(6)0.5M NaOH。
1.3、超滤
(1)1000kDa超滤膜包过滤
按超滤机操作规范离心后的发酵液经1000kDa超滤膜包过滤进一步澄清,收集滤出液;
(2)10kDa超滤膜包超滤浓缩
将进样管路和回流管路置于1000kDa过滤后的发酵液中,透出液放置另一容器中,开启泵,回流一段时间后,调节回流阀门,进口压力为小于0.7MPa,浓缩至总体积的1/8~10左右时,不断加入超滤浓缩稀释液,超滤浓缩至电导率为2~5s/cm。以上操作始终保持发酵液处于冷却中。
1.4、SP Sepharose XL离子柱纯化步骤
(1)装柱及柱处理
按照每升发酵液装柱10~20mL SP Sepharose XL树脂,新装柱按装柱规程操作。用注射用水洗3~5个柱体积,再用0.5M NaOH清洗2个柱体积,然后用注射用水冲洗柱子至pH小于9;
(2)柱平衡
用平衡缓冲液a平衡柱至电导率和pH与平衡缓冲液a一致;
(3)上样样本处理
处理好的超滤液加醋酸钠使其终浓度为20mM,用醋酸调pH值至4.9±0.1;
(4)上样
将处理好的发酵液上柱,用平衡缓冲液a清洗柱3~5个柱体积;
(5)洗脱
用洗脱缓冲液a洗脱目的蛋白,收集洗脱峰。
Butyl Sepharose 4FF疏水柱层析纯化艾塞那肽人血清白蛋白融合蛋白
2.1、溶液配制
(1)0.5M NaOH
(2)平衡缓冲液b:20mM PB(pH 7.2)、5mM辛酸钠;电导率小于5ms/cm;
(3)洗脱缓冲液b:20mM PB、5mM辛酸钠、200mM氯化钠;pH 6.5~6.8;
(4)2M NaCl
(5)20%乙醇。
2.2、Butyl Sepharose 4FF疏水柱层析纯化步骤:
(1)装柱及柱处理
按照1mL树脂吸附10-20mg蛋白样品装填Butyl Sepharose 4FF疏水柱。用注射用水洗去乙醇,再用0.5M NaOH清洗2个柱体积,然后用注射用水洗去碱;
(2)样品处理
SP Sepharose XL样品加NaCl,使其终浓度为2.5M,调pH至5.5,电导率大于150ms/cm;
(3)上样
处理好的SP Sepharose XL样品洗脱上样,UV
(4)柱平衡
上样完成后,用平衡缓冲液b清洗柱3~5个柱体积;
(5)洗脱
用洗脱缓冲液b洗脱目标蛋白,收集洗脱峰。
DEAE Sepharose FF离子柱层析纯化艾塞那肽人血清白蛋白融合蛋白
3.1、溶液配制
(1)0.5M NaOH
(2)平衡缓冲液c:20mM PB(pH 7.2)、5mM辛酸钠;电导率小于5ms/cm;
(3)洗脱缓冲液c为:20mM PB(pH 7.2)、5mM辛酸钠、200mM氯化钠;pH 6.5~6.8。
3.2、DEAE Sepharose FF离子柱层析纯化步骤:
(1)装柱及柱处理
按照每毫升树脂吸附30~50毫克蛋白样品装柱,用注射用水洗去乙醇,再用0.5MNaOH洗60min,然后用注射用水洗去碱;
(2)样品处理
将Butyl Sepharose 4FF疏水柱层析中收集的目的洗脱峰经超滤(Diafiltration,10KD)的方法脱盐;调节样品的缓冲系统为20mM PB,pH 7.2;
(3)上样
将处理好的DEAE Sepharose FF纯化样品上样,线性流速为300~600cm/h;
(4)洗涤
上样完成后,用平衡缓冲液c清洗柱3~5个柱体积;
(5)洗脱
用洗脱缓冲液c洗脱目标蛋白,收集洗脱峰。
Sephacryl HR S-200分子筛层析去盐
4.1、溶液配制
(1)0.5M NaOH
(2)平衡缓冲液d:10mM PB,5mM NaCl;pH 7.0±0.5
(3)2M NaCl
(4)20%乙醇溶液
4.2、Sephacryl HR S-200分子筛层析去盐步骤:
(1)装柱及柱处理
柱体积1500mm(50*1000mm),流速小于8mL/min,用注射用水洗去乙醇,再用0.5MNaOH洗60min,然后用注射用水洗去碱;
(2)柱平衡
用平衡缓冲液d平衡柱至电导率和pH与平衡缓冲液d一致;
(3)上样
用DEAE Sepharose FF离子柱洗脱后样品上样,上样量小于柱体积的5%(约30~55mL),流速5mL/min;
(4)洗脱
用平衡缓冲液d进行洗脱,收集主峰;重复上样,每次上样前平衡时间必须大于4h,合并本批所有收集峰,按质量标准进行质量检测,质量检测结果显示,纯化的艾塞那肽人血清白蛋白融合蛋白符合质量标准的要求,产品纯度达到99.43%%,如图2所示。
本发明未具体描述的部分采用现有产品或现有技术即可,在此不做赘述。
以上所述仅为本发明的实施例,并非因此限制本发明的专利范围,凡是利用本发明说明书及附图内容所作的等效结构或等效流程变换,或直接或间接运用在其他相关的技术领域,均同理包括在本发明的专利保护范围内。
- 一种艾塞那肽人血清白蛋白融合蛋白的纯化方法
- 一种用于治疗儿童矮小症的重组人血清白蛋白/生长激素融合蛋白的制备纯化方法
