用于对组织进行选择性治疗的装置
文献发布时间:2023-06-19 10:14:56
本申请要求于2018年6月22日提交的题为“用于组织治疗的选择性等离子体生成”的美国临时申请序列号62/688,855的优先权,其全部内容通过引用合并于此。
背景技术
各种状况可以通过施加一定波长的光或光学能量来治疗。在不损害与靶标结构相邻的组织结构的情况下将能量传递到适当靶标结构(例如,诸如皮肤之类的组织)时存在许多挑战。这些挑战包括使用足够通量以适当波长递送能量以及能够使用光或光学能量有效且高效扫描靶标结构。
在要治疗组织实际上是透明的或缺乏对光的吸收能力的情况下,出现基于光的治疗时的挑战。迄今为止,这一挑战阻止了对具有通常无色素(例如,缺乏真黑素)毛囊(例如,金发和白发)的人使用激光脱毛技术治疗。
附加地,因为肤色较深的患者的表皮中添加的黑色素会吸收治疗光,导致不良副作用,所以这些患者通在进行基于光的治疗服务方面是有所欠缺的。
发明内容
已经开发了包括将光学能量施加到皮肤上的小型离散治疗位置的分级(fractional)途径,这些小型离散治疗位置通过健康组织分隔以促进愈合。以期望特异性准确地靶向治疗位置(例如,位于真皮层中)同时避免损害治疗位置周围(例如,表皮层中)的健康组织可能具有挑战性。例如,这需要具有高数值孔径(NA)的光学系统,用于将激光束聚焦到治疗位置。附加地,光学系统应当能够在大的受影响区域(例如,几平方厘米)上扫描聚焦光束。因此,期望开发一种光学系统,该光学系统可以具有高数值孔径,并且能够在大的受影响区域上进行扫描。进一步地,可能期望光学系统能够在合理持续时间(例如,小于一个小时)内治疗受影响区域。更进一步地,可以期望光学系统包括界面,该界面可以例如建立与治疗区域的牢固接触,稳定治疗区域,冷却治疗区域等。
过去已经尝试将掺杂剂引入到非色素沉着性区,用于使用激光进行选择性热解治疗。这种情况的示例是将金纳米壳引入皮脂腺,然后使用激光治疗痤疮。这种情况在R.Anderson的美国专利号9,687,508中进行了描述。附加地,期望掺杂不含色素的毛囊,以使具有白皙皮肤和金发的那些人可以进行激光脱毛。另外,以这种方式对组织进行掺杂和治疗局限于与掺杂剂相比较时周围组织对激光波长的吸收度低得多(接近零)的应用。在其中周围组织也吸收激光波长的情形下,需要另一方法。
肤色较暗的许多患者在使用选择性治疗靶标或发色团的基于能量的皮肤病学设备的服务方面是有所欠缺的。这是因为他们富含黑色素的表皮吸收能量以及大多数天然存在的靶标。结果,未靶向组织可以受到与靶标相同的强度的影响。因此,期望一种技术将允许具有深色皮肤类型的人享用在对组织进行掺杂选择性治疗(诸如脱毛)方面的进步。例如,通过将高NA的治疗激光聚焦到患者真皮中的位置,表皮中激光的强度远小于真皮中的焦点处的强度。附加地,可以使用在激光的波长处具有比黑色素高得多的吸收率的掺杂剂,使得在掺杂剂内而非在黑色素内出现对激光的更强烈的吸收。
某些波长的光或光学能量可以与靶标组织相互作用并且将光学能量传递到靶标组织。来自电磁辐射(EMR)(例如,激光束)的光学能量的传递可以在靶标组织中通过以下各项中的一项或多项来引起等离子体生成:电离(例如,多光子电离)、加热、激光诱导光学击穿(LIOB)、以及激光诱导热击穿(LITB)。生成的等离子体可以用于治疗靶标组织。向靶标组织添加掺杂剂可以降低LIOB所需的最小激光强度(“阈值LIOB强度”)、和/或降低LITB所需的最小激光强度(“阈值LITB强度”)。降低靶标组织的预先确定的区域(例如,靶标组织的已经添加掺杂剂的区域)的LIOB/LITB阈值强度可以允许在预先确定的区域中选择性地生成等离子体。选择性地生成等离子体可以允许对靶标组织进行选择性治疗。
因而,提供了用于基于EMR(例如,基于激光)的选择性组织治疗的改进方法、系统和设备。
一种方法包括:在靶标组织的预先确定的区域内沉积有多个掺杂剂颗粒。该方法还包括:将激光束聚焦到聚焦区域,该聚焦区域与预先确定的区域的至少一部分重叠。聚焦区域至少包括多个掺杂剂颗粒中的第一掺杂剂颗粒。该方法还包括:调整激光束的第一参数以在包括第一掺杂剂颗粒的等离子体体积内生成等离子体。
在一个实现方式中,在第一掺杂剂颗粒内生成等离子体。在另一实现方式中,经由激光诱导热击穿(LITB)在等离子体体积中生成等离子体,该激光诱导热击穿(LITB)是由于第一掺杂剂颗粒吸收激光束的一部分而引起。在又一实现方式中,激光束在聚焦区域中的最大强度低于没有掺杂剂颗粒的靶标组织的LITB阈值。
在一个实现方式中,调整激光束的第一参数包括:将激光束的最大强度设置为介于没有掺杂剂颗粒的靶标组织的LITB阈值与具有掺杂剂颗粒的靶标组织的LITB阈值之间的值。在一个实现方式中,经由激光诱导光学击穿(LIOB)在等离子体体积中生成等离子体,该激光诱导光学击穿(LIOB)是由于第一掺杂剂颗粒吸收激光束的一部分而引起。在一个实现方式中,激光束在聚焦区域中的最大强度低于没有掺杂剂颗粒的靶标组织的LITB阈值。
在一个实现方式中,调整激光束的第一参数包括:将激光束的最大强度设置为介于没有掺杂剂颗粒的靶标组织的LITB阈值与没有掺杂剂颗粒的靶标组织的LITB阈值之间的值。在另一实现方式中,调整激光束的第一参数包括:调整以下各项中的一项或多项:激光束的功率、脉冲能量、以及波长。在又一实现方式中,多个掺杂剂颗粒包括以下各项中的一项或多项:氯化钠、硅、银纳米颗粒、金属纳米复合物、树枝状分子。
在一个实现方式中,该方法还包括:沿着预先确定的区域中的第一路径扫描激光束的聚焦区域。在另一实现方式中,沿着第一路径扫描聚焦区域被配置为执行以下各项中的一项或多项:沿着第一路径破坏、消除、空化、烧蚀、变性、以及失活靶标组织。在一个实现方式中,生成的等离子体包括从第一掺杂剂颗粒生成的第一等离子体以及从靶标组织生成的第二等离子体。
在一个实现方式中,通过至少将多个掺杂剂颗粒注入靶标组织中,来在预先确定的区域中沉积多个掺杂剂颗粒。在另一实现方式中,聚焦区域的数值孔径为至少0.3。在又一实现方式中,激光束的波长基于靶标组织中的散射和吸收中的至少一者来选择。在一个实现方式中,波长介于约0.5微米与约2.0微米之间。
附图说明
根据结合附图进行的以下具体实施方式,本公开的实施例将得到更充分的理解,其中:
图1图示了治疗系统的示例性实施例;
图2是聚焦到皮肤中的真皮层的色素沉着性区域中的激光束的示意图示;
图3A是黑色素的示例性吸收度光谱图;
图3B是血红蛋白的示例性吸收度光谱图;
图4图示了黑色素和静脉血的吸收系数以及皮肤中光的散射系数与波长的曲线图;
图5是用于在靶标材料中选择性生成等离子体的示例性光学系统的示意图示;
图6是示例性光学系统的示意图示;
图7图示了治疗前的具有黑色素纹身的节段的示例性组织学;
图8图示了具有黑色素纹身的皮肤样本的示例性光谱测量;
图9图示了治疗前的具有碳纹身的节段的示例性组织学;
图10图示了具有碳纹身的皮肤样本的示例性光谱测量;
图11图示了治疗后的具有碳纹身的节段的示例性组织学;
图12是图示了用于在靶标组织中选择性地生成等离子体的方法的一个示例性实施例的流程图;
图13是示出了根据一些实施例的白猪皮的未掺杂样本和掺杂样本的图像;
图14是根据一些实施例的对照样本的毛囊的示例性放大图像;
图15是根据一些实施例的掺杂样本的毛囊的示例性放大图像;以及
图16是根据一些实施例的示出了近红外吸收色素(即,掺杂剂)对可见光和近红外光的影响的一系列示例性图像。
应当指出,附图不一定按比例绘制。附图仅旨在描绘本文中所公开的主题的典型方面,因此不应视为限制本公开的范围。本领域技术人员将会理解,本文中具体描述并且在附图中图示的系统、设备和方法是非限制性示例性实施例,并且本发明的范围仅由权利要求书限定。
具体实施方式
现在,对某些示例性实施例进行描述以提供对本文中所公开的设备和方法的结构、功能、制造和使用的原理的整体理解。附图中图示了这些实施例的一个或多个示例。本领域技术人员将会理解,本文中所具体描述且附图中所图示的设备和方法为非限制性示例性实施例,并且本发明的范围仅由权利要求书限定。结合一个示例性实施例所图示或描述的特征可以与其他实施例的特征组合。这样的修改和变化旨在包括在本发明的范围内。
下文关于诸如黄褐斑之类的皮肤的色素性状况的治疗对本公开的各个实施例进行详细讨论,以改善这种色素性状况的外观。然而,所公开的实施例可以用于治疗其他色素性状况和非色素性状况以及其他组织靶标和非组织靶标,而不受限制。色素性状况的示例可以包括但不限于发炎后色素过度沉着,眼睛周围的深色皮肤,黑眼睛,咖啡色斑,贝克尔痣,太田痣,先天性黑素细胞痣,雀斑/斑点,富含铁血黄素的结构,色素性胆结石,富含叶黄素、玉米黄质、视紫红质、类胡萝卜素、胆绿素、胆红素和血红蛋白的结构,以及含有纹身的组织。非色素性状况的示例可以包括但不限于毛囊、毛干、血管损伤、感染性状况、皮脂腺、痤疮等。
进一步地,在本公开中,实施例的名称相同的部件通常具有相似的特征,因此,在一个特定实施例中,不必对每个名称相同的部件的每个特征进行充分阐述。附加地,就在所公开的系统、设备和方法的描述中使用线性尺寸或圆形尺寸的程度而言,这样的尺寸并不旨在限制可以与这样的系统、设备和方法结合使用的形状的类型。本领域技术人员将会认识到,对于任何几何形状,可以容易确定这样的线性尺寸和圆形尺寸的等同物。系统和设备及其部件的大小和形状至少可以取决于其中系统和设备将用于其中的受试者的解剖结构、其中系统和设备将与其一起使用的部件的大小和形状、以及其中系统和设备将用于其中的方法和过程。
一般而言,对可以将电磁辐射(EMR)(例如,激光束)聚焦到组织中的治疗区域的高数值孔径(NA)光学治疗系统进行描述。聚焦激光束可以将光学能量递送到治疗区域,而不会损害周围组织。所递送的光学能量可以例如破坏皮肤的真皮层的治疗区域中的色素沉着性发色团和/或靶标,而不会影响周围区域(例如,上覆的表皮层、真皮层的其他部分等)或在未受影响区域或非靶向区域所包围的皮肤或组织的其他色素沉着性靶标区域内。在其他实现方式中,所递送的光学能量可以使得移除或更改纹身或进行血红蛋白相关治疗。
题为“用于治疗真皮黄褐斑的方法和装置(Method and Apparatus for TreatingDermal Melasma)”的美国专利申请公开号2016/0199132和题为“用于选择性治疗真皮黄褐斑的方法和装置(Method and Apparatus for Selective Treatment of DermalMelasma)”的美国临时申请号62/438,818中公开了用于使用光或光学能量治疗皮肤状况的示例性方法和设备,其中每个均通过引用而整体并入本文。
一般而言,提供了用于治疗组织中的色素性状况的系统和对应方法。如下文所更详细地讨论的,所公开的系统和方法采用诸如激光束之类的电磁辐射(EMR)以将预先确定的量的能量递送到靶标组织。EMR可以聚焦到聚焦区域,并且聚焦区域可以关于靶标组织在任何方向上平移或旋转。预先确定的量的辐射可以被配置为热破坏或以其他方式损坏表现出色素性状况的组织的部分。以这种方式,预先确定的量的能量可以递送到靶标组织内的任何位置,用于治疗色素性状况,从而改善其外观。
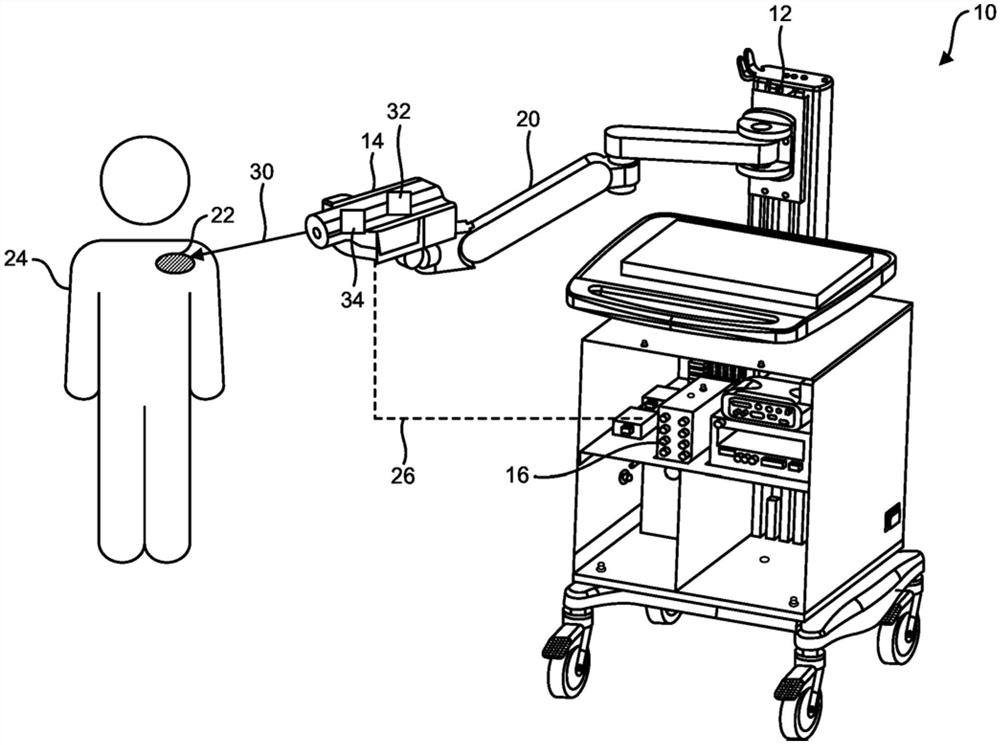
图1图示了治疗系统10的一个示例性实施例。如所示出的,治疗系统10包括安装平台12、发射器14、以及控制器16。安装平台12可以包括一个或多个操纵器或臂20。臂20可以耦合到发射器14,用于对受试者24的靶标组织22执行各种治疗。安装平台12和发射器14的操作可以由用户手动引导或使用控制器16(例如,经由用户界面)引导。在某些实施例中(未示出),发射器可以具有手持式形状因子,并且可以省略安装平台12。在其他实施例中,安装平台可以为机器人平台,并且臂可以通信耦合到控制器,用于操纵发射器。
发射器14和控制器16(以及可选地,安装平台12)可以经由通信链路26彼此通信,该通信链路26可以为任何适当类型的有线通信链路和/或无线通信链路,该任何适当类型的有线通信链路和/或无线通信链路根据任何合适通信协议携载任何适当类型的信号(例如,电信号、光学信号、红外信号等)。
控制器16的各个实施例可以被配置为控制发射器14的操作。在一个方面中,控制器16可以控制EMR 30的移动。如下文所详细讨论的,发射器14可以包括源32,该源32用于发射EMR 30;以及扫描系统34,该扫描系统34用于操纵EMR 30。作为示例,扫描系统34可以被配置为将EMR 30聚焦到聚焦区域并且在空间上平移和/或旋转该聚焦区域。控制器16可以经由通信链路26将信号发送到源32,以命令源32发射EMR 30,该EMR 30具有一个或多个选定特性,诸如波长、功率、重复率、脉冲持续时间、脉冲能量、聚焦特性(例如,聚焦体积、瑞利长度等)。在另一方面中,控制器16可以经由通信链路26将信号发送到扫描系统34,以命令扫描系统34在一个或多个平移和/或旋转操作中关于靶标组织22移动EMR 30的聚焦区域。
根据以下描述,显而易见的是,本文中所描述的系统的一个有利方面在于通过控制器16和/或扫描系统34对治疗的控制使得治疗图案能够基本上为圆或重叠圆的形式。因此,该系统的特征是利用形式为同心圆的扫描图案,而非简单沉积线性光斑图案。
本文中在诸如真皮层之类的皮肤组织内的靶标的上下文中对治疗系统10和方法的各个实施例进行了讨论。然而,所公开的实施例可以用于治疗受试者的任何位置中的任何组织,而不受限制。非皮肤组织的示例可以包括但不限于粘膜组织、生殖器组织、内脏器官组织和胃肠道组织的表面区域和亚表面区域。
图2是聚焦到皮肤组织中的真皮层的色素沉着性区域中的激光束的图示的示意图。皮肤组织包括皮肤表面100和上表皮层110或表皮,该上表皮层110或表皮在面部区域中的厚度可以为例如约60μm至120μm。真皮在身体的其他部位中可能稍厚。例如,一般而言,表皮的厚度的范围可以为约30μm(例如,眼睑上)至约1500μm(例如,手掌或脚底上)。在皮肤的某些状况(例如,牛皮癣)下,这种表皮可以比上文示例更薄或更厚。基底真皮层120或真皮从表皮110下方延伸至深层皮下脂肪层(未示出)。表现出深层黄褐斑或真皮黄褐斑的皮肤可以包括含有过量黑色素的色素沉着性细胞或区域130的群体。电磁辐射(EMR)150(例如,激光束)可以聚焦到可以位于真皮120或表皮110内的一个或多个聚焦区域160中。EMR 150可以以能够被黑色素吸收的一种或多种适当波长提供。一个或多个EMR波长可以基于下文所描述的一个或多个准则来选择。
治疗辐射特性
用于治疗诸如色素性状况和非色素性状况之类的某些皮肤状况的期望波长的确定可以取决于例如皮肤中存在的各种竞争发色团(例如,发色团、血红蛋白、纹身墨水等)的波长相关吸收系数等。图3A是黑色素的示例性吸收度光谱图。观察到黑色素对EMR的吸收在约350nm的波长处达到峰值,然后随着波长的增加而减小。尽管黑色素对EMR的吸收促进了对含黑色素区域130的加热和/或破坏,但是非常高的黑色素吸光度可能导致色素在表皮110中的大量吸收,并且降低EMR渗透到真皮120或表皮110中。如图3A所图示的,小于约500nm的EMR波长处的黑色素吸收相对较高,使得小于约500nm的波长可能不适合于充分渗透到真皮120中以加热和损坏或破坏其中的色素沉着性区域130。这种在较小波长下增强的吸收会导致对表皮110和真皮120的上部(表面)部分的不想要的破坏,其中相对较少的未吸收EMR穿过组织进入真皮120的更深层部分。
图3B是氧合血红蛋白或脱氧血红蛋白的示例性吸收度光谱图。血红蛋白存在于皮肤组织的血管中,并且可以被氧合(HbO
针对EMR选择适当波长还可以取决于与EMR相互作用的组织的波长相关散射分布。图4图示了黑色素和静脉血的吸收系数与波长的曲线图。图4还图示了皮肤中光的散射系数与波长的曲线图。黑色素的吸收随波长而单调减小。如果黑色素是色素性状况治疗的靶标,则期望黑色素中具有高吸收的波长。这可能表明光的波长越短,治疗就越有效。然而,血液的吸收在小于800nm的波长处增加,从而增加了对血管意外靶向的风险。另外,由于预期靶标可以位于皮肤表面下方,所以皮肤(例如,真皮层)的散射作用可能很重要。散射会减少到达预期靶标的光的量。散射系数随着波长的增加而单调减小。因此,虽然较短的波长可能有利于黑色素的吸收,但是较长的波长由于散射减少而有利于更深层渗透。同样,由于血液在较长波长下的吸收较低,所以较长的波长对于不伤害血管而言更好。
考虑到上述考量,波长的范围可以为约300nm至约3000nm,更特别地为约800nm至约1064nm,该波长可以用于靶向真皮中的某些结构(例如,黑色素)。特别地,约800nm和约1064nm的波长可以用于这样的治疗。800nm波长之所以有吸引力,是因为该波长的激光二极管成本更低且容易获得。然而,由于在该波长下的散射较低,所以1064nm对于靶向更深的病变尤其有用。1064nm的波长也可能更适合于存在大量表皮黑色素的深色皮肤类型。在这些个体中,表皮中黑色素对较低波长EMR(例如,约800nm)的较高吸收会增加热损伤皮肤的机会。因此,针对用于一些个体的某些治疗而言,1064nm可能为治疗辐射的更合适波长。
各种激光源可以用于生成EMR。例如,很容易获得含钕(Nd)激光源,其提供了1064nm EMR。这些激光源可以在脉冲模式下操作,其中重复率的范围为约1Hz至100kHz。调QNd激光源可以提供脉冲持续时间小于一纳秒的激光脉冲。其他Nd激光源可能会提供脉冲持续时间超过一毫秒的脉冲。提供1060nm波长EMR的示例性激光源是来自美国康涅狄格州East Granby的Nufern的20W NuQ光纤激光器。20W NuQ光纤激光器以范围为约20kHz至约100kHz之间的重复率提供脉冲持续时间为约100ns的脉冲。另一激光源为来自法国LesUlis的Quantel的Nd:YAG Q-smart 850。Q-smart 850以高达约10Hz的重复率提供脉冲能量高达850mJ并且脉冲持续时间为约6ns的脉冲。
可以期望用于治疗组织的光学治疗系统能够(例如,通过对色素、靶标组织中的真皮层和表皮层之间的界面进行成像)标识靶标组织中的治疗区。还可能期望监测/检测EMR与靶标组织之间的相互作用(例如,在组织中的等离子体生成)。附加地,基于检测,光学治疗系统可以修改治疗过程(例如,通过改变靶标组织中的聚焦区域的强度、大小/位置等)。下文对光学治疗系统的各种实施例进行了描述。
激光束可以与组织相互作用以在组织内生成等离子体,并且该等离子体可以用于治疗组织。等离子体可以通过多种机制生成。这样的机制可以包括激光诱导击穿,诸如激光诱导光学击穿(LIOB)和激光诱导热击穿(LITB)。
在LIOB中,高强度激光束被施加到组织。由于激光束的高强度,所以组织的原子/分子可以(例如,经由非线性吸收)吸收多个激光光子,其可以导致电子从原子/分子电离并且形成等离子体。
可替代地,可以经由激光诱导热击穿(LITB)生成等离子体。LITB为与LIOB不同的热物理过程。LITB可以通过由激光束加热靶标组织来引发。这可以导致对靶标组织的原子/分子进行电离以生成热电子。热电子可以迅速与它们所来自的电离分子重新组合。然而,在适当条件下,热电子还可以吸收而非重新组合来自激光束/EMR的传入光子,从而导致热离子等离子体的形成。
热离子等离子体引发可以取决于从靶标组织的原子/分子释放热电子的能力。与没有弱结合电子的分子相比较,具有弱结合电子的分子在加热时更可能生成热离子等离子体。通常,经由LIOB生成等离子体所需的激光强度高于经由LITB生成等离子体所需的激光强度(例如,高几个数量级)。
在靶标组织中存在掺杂剂的情况下,可以增强经由LIOB和LITB的等离子体生成。在一些实现方式中,掺杂剂(例如,金属纳米复合材料、树状物(dendrimer)、包含具有低电离能量的元素的任何材料(钠、钾)、以及具有低局部功函数的任何材料,其中低电离能量和低局部功函数相对于靶标组织中的那些特性等而言较低)可以修改激光束的电场(例如,在包围掺杂剂的区域中)。这可以降低经由LIOB生成等离子体所需的激光强度。在其他实现方式中,掺杂剂(例如,发色团)可以具有比周围靶标组织的离子/分子更高的线性吸收。这可以导致在较低激光强度下(例如,通过激光光子的线性吸收、通过加热等)引发热离子等离子体的形成。
加热掺杂剂以引发热离子等离子体的功效部分地取决于激光束的能量密度。激光束中激光脉冲的能量为激光功率的时间积分。因为脉冲的持续时间非常短,所以可以在很短的时间间隔内引发电介质击穿的飞秒激光脉冲和皮秒激光脉冲的能量密度往往低于热离子等离子体引发所需的能量密度。即使处于微秒域(为飞秒域的一百万倍长),较长的脉冲持续时间也会在存在合适掺杂剂并且局部功率密度足够高的条件下引发热离子等离子体的形成。脉冲能量可以聚焦到足以在组织中提供足够高的局部能量密度的程度。
本文中所描述的系统和方法的各个实施例可以被配置为将EMR聚焦在高度会聚束中。例如,该系统的一个实施例可以包括聚焦透镜布置或会聚透镜布置,该聚焦透镜布置或会聚透镜布置的数值孔径(NA)选自约0.3至0.9(例如,约0.5至0.9之间)。由NA产生的EMR的会聚角可以相对较大,并且它可以在透镜的聚焦区域中提供高通量和强度,该聚焦区域可以定位在靶标组织内部的区域。同时,靶标组织的位于聚焦区域上游的覆盖部分中可以存在较低通量。这样的聚焦几何形状可以帮助减少靶标组织的覆盖部分中的不想要的加热和热损伤。示例性光学布置还可以包括准直透镜布置,该准直透镜布置被配置为将EMR从发射布置引导到聚焦透镜布置上。准直透镜布置可以确保从激光布置发出的EMR光束在其传播(例如,传播通过光学系统)时具有均匀横截面。
在系统内采用的光学系统的实施例可以被配置为将EMR聚焦到大小预先确定的聚焦区域。作为示例,聚焦区域可以具有宽度或光斑大小,该宽度或光斑大小小于约200μm,例如,小于约100μm,或甚至小于约50μm,例如,小至约1μm。例如,光斑大小的范围可以为约1μm至约50μm、约50μm至约100μm、以及约100μm至约200μm。聚焦区域的光斑大小可以例如在空气中确定。可以选择这种光斑大小,作为足够小以在聚焦区域中提供EMR的高通量或强度(例如,有效照射皮肤组织的真皮中的色素沉着性结构、有效照射靶标组织的掺杂区域等)与足够大以便于在合理时间内照射靶标组织的大区域/体积之间的平衡。该示例性光学布置还可以被配置为将EMR的聚焦区域引导到靶标组织内的位置上,该位置处于靶标组织的表面(例如,皮肤组织的真皮层)下方的深度处,该深度诸如在约120μm至约1000μm的范围之内,例如,介于约150μm与约300μm之间。
这样的示例性深度范围可以与皮肤中表现出真皮黄褐斑的色素沉着性区域或其他感兴趣靶标的典型观察深度相对应。该聚焦深度可以与一定距离以及聚焦区域的位置相对应,该一定距离为距被配置为接触皮肤表面的装置的下表面的距离。附加地,一些实施例可以被配置为用于治疗表皮内的靶标。例如,光学布置可以被配置为将EMR的聚焦区域引导到表皮组织内的位置,例如,在皮肤表面下方约5μm至2000μm的范围内。又其他实施例可以被配置为用于治疗真皮深层的靶标。例如,纹身艺术家通常校准他的纹身枪以刺穿皮肤至与皮肤表面下面约1mm至约4mm的深度。因而,在一些实施例中,光学布置可以被配置为将EMR的聚焦区域引导到与皮肤组织下面约0.4mm至4mm的范围内的真皮组织内的位置。
在本公开的某些实施例中,一个或多个波长的EMR可以聚焦到靶标组织中,使得靶标组织的包含掺杂剂的区域选择性地吸收光学能量。在某些实施例中,EMR可以被脉冲化和/或扫描。光学能量的这种线性吸收可以引起电子的局部热离子发射。通过适当选择光学能量参数和光束几何形状,靶标组织的进一步照射可以引起由于所发射的电子所致的进一步能量吸收,接着局部形成等离子体,以及对能量的非线性吸收。由于靶标组织的含掺杂剂区域中的等离子体,所以这个过程可以产生强热、局部膨胀、诸如强声波或冲击波之类的应力波、和/或化学反应。
在本公开的示例性实施例中,可以部分地基于通过靶标组织中的掺杂剂对光学能量的选择性吸收来在靶标组织内的聚焦区域中生成激光诱导等离子体(例如,经由LIOB、LITB等)。形成热离子等离子体在存在掺杂剂的部位处需要阈值水平的功率和能量密度。根据一些实施例,可以扫描靶标组织内的聚焦区域以引发在激光焦点几何形状所限定的深度处的等离子体形成,并且可以仅在存在掺杂剂的部位处选择性地形成这种等离子体。以这种方式,聚焦扫描激光可以用于选择性地破坏靶标组织中含有掺杂剂的(例如,在一个或多个聚焦平面内的)良好限定区域。
聚焦区域大小/宽度、质量、以及沿着引导进入靶标组织中的聚焦激光束的光束轴线的长度可以通过诸如以下各项中的一项或多项之类的因子确定:激光束发散度、激光模式结构、光束聚焦光学器件的数值孔径、聚焦光学器件的像差、光束在组织表面处到组织中的耦合(例如,表面反射和折射效应)、以及组织的光学散射特性。
如本文中所讨论的,术语“瑞利范围”可以包括其由本领域技术人员所理解的普通含义,并且其可以用于描述沿着光学轴线的聚焦区域的程度或长度。例如,瑞利范围可以描述引导进入靶标组织中的光束的沿着深度或z轴的聚焦区域的大小。瑞利范围受诸如例如激光源发散度、光学能量的波长、一个或多个激光模式、通过光学元件会聚之前的光束的原始直径、以及聚焦系统的数值孔径等之类的因素的影响。例如,高度会聚光束可以表现出相对较小的瑞利长度,其中光束的外边界随着光束到达聚焦区域而以相对较大的角度会聚(并且以相似角度发散到聚焦区域之外)。较小的聚焦会聚角可以导致较大的瑞利范围,因为光束关于沿着光束轴线的距离缓慢会聚和发散。通常,瑞利范围是横向聚焦光斑直径的几倍大。
通过使聚焦光学设计和/或激光模式结构发生变化,可以产生广泛多种的激光聚焦光斑。这些聚焦光斑可以通过诸如光斑大小或宽度(例如,在聚焦区域中垂直于光束的轴线的特征尺寸)和瑞利范围(例如,聚焦区域的沿着光束的纵向轴线的尺寸)之类的几何参数来表征。用于(经由热离子发射)选择性地引发靶标组织中的等离子体的聚焦区域的适当尺寸可以基于诸如以下各项之类的因素来选择:被靶向的掺杂剂的大小、光学能量源的脉冲能量和功率(其与聚焦区域的大小一起将影响局部功率和能量密度)、瑞利范围(其将进一步影响可以在特定时间间隔内在靶标组织的体积内扫描的深度范围)等。
本公开的示例性实施例可以提供用于使用激光束在靶标组织(例如,真皮层)的期望(例如,预先确定的)部分中选择性地产生等离子体的设备和方法。这可以例如通过将掺杂剂添加到靶标组织的区域(“掺杂区域”)来完成。掺杂剂的添加可以降低在掺杂区域(例如,经由LIOB、LITB等)中生成等离子体所需的激光束的阈值强度。结果,与靶标组织的尚未掺杂的区域(例如,未掺杂区域)相比较,等离子体可以使用强度较低的激光束在掺杂区域中生成。这可以允许在靶标组织中选择性地生成等离子体。例如,强度低于阈值强度(例如,未掺杂区域的LIOB阈值强度、未掺杂区域的LITB阈值强度等)的激光束当与掺杂区域相互作用时生成等离子体,并且当与未掺杂区域相互作用时,不会生成等离子体(或生成很少的等离子体)。
图5是示例性光学系统500的示意图示,该光学系统500被配置为在靶标组织中(例如,在靶标组织的真皮层中)执行等离子体的选择性生成。光学系统500可以从激光源502接收激光束504。光学系统500包括物镜(未示出),该物镜可以聚焦激光束504并且将聚焦激光束506引导到靶标组织510中的聚焦区域508。靶标组织510可以包括掺杂区域512和非掺杂区域514。掺杂区域可以包括多个掺杂剂516。掺杂剂516可以通过从组织表面扩散,通过组织的经分级(fractionated)激光处理的表面、通过身体系统(例如,口服)和通过纹身的扩散而添加到靶标组织510。掺杂剂516可以包括例如硅、银纳米颗粒、金属纳米复合物、树枝状分子、金属纳米颗粒、染料、以及色素。
随着物镜移动(例如,相对于扫描系统500和/或由于整个扫描系统500的移动),聚焦区域可以追踪穿过/沿着靶标组织510的路径。例如,聚焦区域508可以从掺杂区域512行进到未掺杂区域514,或者反之。可以调整聚焦激光束506的强度,使得在掺杂区域中生成等离子体,而在未掺杂区域514中不生成等离子体(或与掺杂区域相比较,生成的程度小得多)。与未掺杂区域相比较,阈值LITB/LIOB强度在掺杂区域中可以更低。通过将聚焦激光束506的强度调整为未掺杂区514的阈值LITB强度与掺杂区域512的阈值LITB强度之间的值,可以在掺杂区域512中选择性地生成热离子等离子体。同样,通过将聚焦激光束506的强度调整为未掺杂区域514的阈值LIOB强度与掺杂区域512的阈值LIOB强度之间的值,可以在掺杂区域512中选择性地生成来自光学击穿的等离子体。在一些实现方式中,等离子体的选择性生成(例如,在掺杂区域中)可以通过使以下各项中的一项或多项发生变化来实现:聚焦激光束506的功率、脉冲能量、脉冲持续时间、以及波长。
聚焦激光束506与掺杂剂516之间的相互作用可能引起在掺杂剂516中和/或周围(例如,在包围掺杂剂516的体积中)生成等离子体。例如,聚焦激光束506可以通过电离来自掺杂剂516的电子来引发等离子体,这又可以使得靶标组织510的其他掺杂剂和/或原子(或分子)的电离。在一些实现方式中,通过LIOB可以在掺杂剂516中和/或周围生成等离子体。所生成的等离子体(例如,经由LIOB、经由LITB等)可以在靶标组织中传播(例如,沿着聚焦激光束506的传播方向)。传播等离子体可以(例如,通过电子碰撞解离)电离靶标组织的原子/分子。
掺杂剂可以添加到靶标组织以实现使用激光束进行选择性热解治疗。例如,将金纳米壳引入皮脂腺可以允许对痤疮进行选择性治疗。该过程已在美国专利号9,687,508中进行了描述,其全部内容通过引入并入本文。在一些实现方式中,掺杂不含色素毛囊可以允许具有白皙皮肤的个体进行激光脱毛。例如,当周围皮肤组织不吸收(或吸收很少)负责热分解治疗(例如,痤疮治疗、脱毛等)的激光束时,可以有效实现前述痤疮治疗和脱毛。对有色患者执行选择性热解治疗可能具有挑战性。这可能是由于包围组织靶标(例如,痤疮、毛囊等)的富含黑色素的皮肤组织(例如,皮肤组织的表皮)对EMR的吸收速率更高。根据一些实施例,由于富含黑色素的表皮内的激光强度小于靶标区域处的激光强度并且靶标区域处的吸收(或对激光诱导击穿的亲和性)通过掺杂剂增强,所以使用掺杂剂和会聚激光束会解决这一挑战。
图6是示例性光学系统600的示意图示。光学系统600包括光束组合器610,该光束组合器610被配置为接收准直激光束612。光束组合器610包括反射器614,该反射器614反射入射激光束612。反射器614被选择为反射具有预先确定的波长范围的光。在当前研究中,激光束612的波长为1060nm,反射器为Thorlabs NB1-K14,其在1047nm至1064nm的波长范围内反射率为99.5%。反射激光束612通过聚焦光学器件616成像并聚焦。本研究中使用的聚焦光学器件616为Thorlabs C240TME-C,其是一种衍射性能有限的非球面透镜,NA为0.5,并且有效焦距为8mm。激光束612在靶标组织618(皮肤样本)中聚焦至束腰(例如,聚焦体积)。在激光束612的束腰处,在靶标组织样本618内生成等离子体羽620。由等离子体羽620生成的辐射624通过聚焦光学器件616成像并且透射通过反射器614。在透射通过反射器614之后,辐射624通过光纤耦合器622成像到光纤(未示出)的第一端中。该研究中使用的光纤耦合器为Thorlabs PAF-SMA-7-A。光纤的第二端耦合到光谱仪(未示出),该光谱仪为OceanOptics HR2000+ES。在该研究的另一实现方式中,陷波滤光器(未示出)包括在反射器614与光纤耦合器622之间,以阻挡辐射624中具有与激光束612的波长类似的波长的部分进入光纤。靶标组织618安装在机动台630上。维持靶标组织618与聚焦光学器件616之间的工作距离,以控制激光束612的束腰在靶标组织618内的深度。
激光束612由激光源(具体地,10W Nufern光纤激光器)提供。激光器以20kHz、100nS脉冲持续时间和0.5mJ/脉冲操作。在激光照射期间以100mm/S的速率扫描组织。调整光谱仪以在5000mS的时段内捕获光,并且响应于激光辐照而触发捕获。
本申请中所描述的治疗系统和方法可以用于在皮肤样本的某些部分(例如,具有合成黑色素纹身、碳纹身等的猪皮肤)中选择性地生成等离子体。黑色素纹身可以位于皮肤样本的真皮中大约四分之一毫米至一毫米深之间。图7图示了治疗前的黑色素纹身的节段的示例性组织学。组织学的顶部处示出了皮肤表面710。表皮-真皮联结720界定了皮肤的表皮层和真皮层。真皮中存在的黑色素小球730构成黑色素纹身。从图7可以看出,表皮含有天然黑色素并且皮肤具有较深皮肤类型(Fitzgerald皮肤类型III)。
图8图示了具有黑色素纹身的皮肤样本的示例性光谱测量。皮肤样本光谱中存在可见光(波长为约400nm至约800nm)指示在样本(例如,皮肤样本618)中生成等离子体。沿着水平轴线810示出了以纳米为单位的波长。沿着垂直轴线812示出了相对强度。图8中图示了黑色素纹身光谱814和裸露皮肤光谱816。黑色素纹身光谱814示出了在照射包括黑色素纹身的皮肤样本的一部分期间进行的光谱测量,而裸露皮肤光谱816示出了在照射不包括黑色素纹身的皮肤样本(“裸露皮肤”)的一部分期间进行的光谱测量。黑色素纹身光谱814指示存在中心位于约600nm并且覆盖可见光谱的广谱光。裸露皮肤光谱816不包括可见光谱中的辐射。
碳纹身可以大致位于皮肤样本的真皮中的四分之一毫米至一毫米深之间。图9图示了治疗前的碳纹身的节段的示例性组织学。组织学的顶部处示出了皮肤表面910。表皮-真皮联结920界定皮肤的表皮层和真皮层。真皮中存在的碳小球930构成黑色素纹身。根据图9,可以看出,表皮包含天然黑色素并且皮肤具有较深色皮肤类型(Fitzgerald皮肤类型III)。
图10图示了具有碳纹身的皮肤样本的示例性光谱测量。皮肤样本光谱中存在可见光(波长为约400nm至约800nm)指示在样本(例如,皮肤样本618)中生成等离子体。沿着水平轴线1010示出了以纳米为单位的波长。沿着垂直轴线1012示出了相对强度。图10中图示了碳纹身光谱1014和裸露皮肤光谱1016。碳纹身光谱1014示出了在照射包括碳纹身的皮肤样本的一部分期间进行的光谱测量,而裸露皮肤光谱1016示出了在照射不包括碳纹身的皮肤样本的一部分(“裸露皮肤”)期间进行的光谱测量。碳纹身光谱1014指示存在中心位于约600nm并且覆盖可见光谱的广谱光。裸露皮肤光谱1016不包括可见光谱中的辐射。
图11中示出了治疗后的碳纹身的节段的组织学。组织学的顶部处示出了皮肤表面1110。表皮-真皮联结1120界定了皮肤的表皮层和真皮层。真皮中存在的碳小球1130构成了碳纹身。根据图11,可以看出,碳小球1130已经被破坏。皮肤表面1110与碳小球1130之间的距离1140如下所示。
如上述构思的证据所指示的,聚焦束可以用于在色素沉着性组织内的规定深度处的掺杂剂内选择性地引发等离子体。引导到富含碳的表皮下面的聚焦区域的激光束可以仅在真皮色素中选择性地引发等离子体,而在上述表皮中不引发等离子体。
图12是图示了用于在靶标组织中选择性地生成等离子体的方法的一个示例性实施例的流程图。在1202处,多个掺杂剂颗粒沉积在靶标组织的预先确定的区域中。预先确定的区域可以与需要治疗的靶标组织的部分相对应。在1204处,激光束(例如,聚焦激光束506)聚焦到聚焦区域(例如,聚焦区域508),该聚焦区域与预先确定的区域(例如,掺杂区域512)的至少一部分重叠。聚焦区域包括多个掺杂剂颗粒中的至少第一掺杂剂颗粒。例如,聚焦区域可以与掺杂剂颗粒(例如,掺杂剂颗粒516)重叠。激光束的聚焦区域可以与其中激光束的强度高于阈值(例如,激光束的在瑞利范围内的一部分)的区域相对应。在1206处,可以调整激光束的第一参数(例如,强度、波长、功率、脉冲能量),以在包括第一掺杂剂颗粒的等离子体体积内生成等离子体。等离子体体积可以为例如包围掺杂剂颗粒(例如,掺杂剂颗粒516)的体积。
示例1
根据一些实现方式的对组织的掺杂通过毛囊掺杂示例示出。为了对无色素毛囊进行掺杂,遵循了示例性毛囊掺杂过程。毛囊掺杂过程旨在打开毛囊并且移除多余脂质,以使含氢染料可以穿透毛囊,而不会穿透或弄脏皮肤的外层。毛囊比通常具有亲脂性的皮肤外层或角质层更具亲水性。以白色约克郡猪的皮肤为例。在准备掺杂时,通过打蜡移除皮肤上的毛发。所使用的蜡来自纽约州纽约Coty US LLC发行的Sally Hansen超强全身打蜡套件。还使用溶剂从打蜡套件中移除残留蜡。皮肤上的毛孔通过使用来自俄亥俄州辛辛那提市Kao USA Inc.发行的Bioré的深层清洁毛孔条进一步排空。然后,皮肤使用外用酒精去油。皮肤平分为两个样本。参考图13,示出了皮肤样本的图像1300。留下第一样本作为对照样本1310。并且,掺杂第二样本成为掺杂样本1320。制备用于掺杂的染料。该染料包括水以及在约1054nm处具有峰值吸收的水溶性近IR色素(来自佛罗里达州Port Lucie的QCR解决方案的零件号NIR1054B)。染料使用刷子施加到掺杂样本1320的皮肤的顶部表面。在顶部皮肤表面涂有染料的情况下,使用叩诊按摩器按摩掺杂样本。在按摩掺杂样本之后,把对照样本和掺杂样本擦拭干净。根据图13,可以看出,掺杂样本1320在掺杂毛囊1330中和周围含有可见色素,而对照样本中没有。在图14中,在放大下示出了来自对照样本的未掺杂毛囊的图像1400。在图15中,在放大下示出了来自掺杂样本的掺杂毛囊的图像1500。
示例2
已经执行了测试以示出:具有不同电离能量的透射材料可以用于降低阈值LIOB强度。已经选择了若干个光学窗口。不同的光学窗口由不同的材料制成:NaCl、KBr、蓝宝石、以及熔融石英。调Q的Nd:Yag激光器(Quantel Q-Smart 450)与光学链一起用于在每个窗口样本处递送聚焦激光脉冲。中性密度(ND)滤光器用于衰减激光,而调Q延迟用于使每个激光脉冲所递送的能量的量发生变化。激光使用累积OD为3.6的ND滤光器衰减。使用8mm EFL透镜(Thorlabs零件号C240TME-C)聚焦激光束。为了估计辐照度,假设所有材料的聚焦光斑尺寸均为10μm(1/e
可以看出,在每种材料中诱发击穿所需的最小能量并非恒定。包含电子供体(NaCl、KBr)的材料以较少能量击穿,并且因此为降低材料的LIOB阈值的合适掺杂剂。由于这些材料在激光波长(1064nm)下均可透射,所以认为击穿由光子诱发,并非由热离子诱发。
示例3
根据一些实施例,添加通常吸收材料作为掺杂剂以辅助LITB。参考图16,一系列图像1600示出了吸收色素及其对1060nm激光束的影响。直径为8mm的1060nm激光束递送到荧光盘1610,当施加近IR辐射时,该荧光盘发出绿色荧光。制备了三个载玻片,一个载玻片含有水1620,一个载玻片含有处于丙酮中的NIR1031M色素1630,并且一个载玻片含有处于水中的NIR1054B 1640。根据图像1600,可以看出,含有色素的载玻片仅仅稍微影响可见光的透射。当水1620放置在激光束路径中时,穿过水1650的激光束的强度(如荧光盘1610所指示的)通常不受影响。当NIR1031M载玻片1630放置在激光束路径中时,穿过NIR1031M 1660的激光束的强度降低。同样,当NIR1054B载玻片1640放置在激光束路径中时,穿过NIR1054B的激光束的强度几乎被完全衰减。因此表明,在激光波长附近具有峰值吸收的色素可以吸收激光束强度,并不会急剧地影响可见光(例如,材料的透明特性)。为了进一步总结,下文给出表,该表包括一些示例性实施例的参数范围。
附加地,氧气浓度和/或pH可以更改组织中的等离子体阈值。因此,根据一些实施例,更改组织内的pH和/或氧气浓度,以便改变组织内的激光诱导击穿阈值。可以使用更改pH和/或氧气浓度的掺杂剂。附加地,可以引发诱发pH和/或氧气浓度改变的生物学反应。例如,众所周知,炎症会更改组织内的pH值,运动也是如此(来自乳酸)。然后,可以在不同的激光诱导击穿阈值下照射该材料,以便实现选择性治疗。氧气浓度可能会因细胞而异。因此,根据一些实施例,可以选择性地治疗细胞(通过等离子体介导治疗)。
治疗各种皮肤状况(诸如用于美容目的)的方法可以使用本文中所描述的系统进行。应当理解,尽管这种方法可以由医师进行,但是诸如美容师和其他受过适当训练的人员之类的非医师可以在医师的监督下或在没有医师的监督下使用本文中所描述的系统来治疗各种皮肤状况。
附加实施例
在一些实施例中,输入激光束的重复率可以比靶标组织/靶标材料中的等离子体的衰减速率更快。这可以允许连续(例如,时间连续、空间连续等)生成等离子体。治疗区域/靶标区域(例如,生成等离子体的区域)的面积可以通过改变激光束的重复率来控制。
基于上文所描述的实施例,本领域技术人员应当领会本发明的其他特征和优点。因而,除了所附权利要求书所指示的以外,本发明不受已经具体示出和描述的内容的限制。本文中所引用的所有出版物和参考文献的全部内容均通过引用而明确并入本文。
如本文中在整个说明书和权利要求书中所使用的,近似语言可以用于修饰可容许发生变化的任何定量化表示,而不导致与其相关的基本功能的改变。“大约”、“基本上”或“约”可以包括沿任一方向落在1%范围内的数字,或在一些实施例中落在数字的5%的范围内的数字,或在一些实施例中落在数字的10%的范围内的数字(大于或小于该数字),除非另有陈述或从上下文中可以明显看出(除了该数字可能不容许超过100%的可能值)。因而,诸如“约”、“大约”或“基本上”之类的一个或多个术语所修饰的值不限于所指定的精确值。在至少一些实例中,近似语言可以与用于测量值的仪器的精度相对应。这里并且在整个说明书和权利要求书中,可以组合和/或互换范围限制,除非上下文或语言另有指示,否则这种范围被标识并且包括包含于其中的所有子范围。
除非明确相反指出,否则本文中在说明书和权利要求书中所使用的冠词“一”和“一个”应当被理解为包括复数参照对象。如果一组的一个或多个成员中的一个、多于一个或所有成员在给定产品或过程中存在、被采用或与之相关,则在这些组的成员之间包含“或”的权利要求或描述被认为是符合的,除非有相反指示或从上下文中明显看出。本公开内容包括其中该组的恰好一个成员在给定产品或过程中存在、被采用或与之相关的实施例。本公开还包括其中组成员中的多于一个或所有成员在给定产品或过程中存在、被采用或与之相关的实施例。更进一步地,应当理解,所公开的实施例提供了所有变化、组合和置换,其中除非另有指示或除非本领域普通技术人员可以明显看出可能出现矛盾或不一致,否则来自所列权利要求中的一个或多个所列权利要求的一个或多个限制、要素、从句、描述性术语等引入到从属于同一基础权利要求的另一权利要求(或与之相关,则引入到任何其他权利要求)中。应当设想,在适当的情况下,本文中所描述的所有实施例可适用于所公开的实施例的所有不同方面。还应当设想,在适当的情况下,实施例和方面中的任何实施例和方面都可以与一个或多个其他这样的实施例或方面自由组合。在元素例如以马库什(Markush)组或类似格式呈现为列表形式的情况下,应当理解,还公开了元素的每个子组,并且可以从该组中移除任一个或多个元素。应当理解,一般而言,在所公开的实施例或所公开的实施例的方面被称为包括特定元件、特征等的情况下,本公开的某些实施例或本公开的方面由这样的元素、特征等组成或基本上由其组成。为了简单起见,并没有在每一情况下都在本文中以如此多的单词对那些实施例进行具体阐述。还应当理解,可以从权利要求中明确排除本公开的任何实施例或方面,而不管说明书中是否记载了具体排除。例如,可以排除任一种或多种活性剂、添加剂、成分、可选剂、生物体类型、障碍、受试者或其组合。
在本文中给出范围的情况下,本公开的实施例包括其中端点包括在内的实施例、其中两个端点均被排除的实施例、以及其中一个端点被包括而另一端点被排除的实施例。除非另有指示,否则应当假设包括两个端点。更进一步地,应当理解,除非另外指示或根据上下文和本领域普通技术人员的理解可以明显看出,否则在本发明的不同实施例中,除非上下文另有明确指出,否则被表达为范围的值可以将所述范围内的任何特定值或子范围假设为该范围的下限的单位的十分之一。还应当理解,在本文中陈述一系列数值的情况下,本公开包括与该系列中的任何两个值所限定的任何中间值或范围类似相关的实施例,以及最低值可以视为最小值,而最大值可以视为最大值的实施例。如本文中所使用的,数值包括表达为百分比的值。
其中数值以“约”或“大约”开头的任何实施例都包括其中记载了精确值的实施例。对于其中数值不以“约”或“大约”开头的本公开的任何实施例,本公开包括其中值以“约”或“大约”开头的实施例。除非另有说明或根据上下文可以明显看出(除非该数字不容许超过可能值的100%),否则“大约”或“约”可以包括沿任一方向落在1%范围内的数字、或在某些实施例中落在数字的5%的范围内的数字、或在某些实施例中落在数字的10%的范围内的数字(大于或小于该数字)。
应当理解,除非另有明确相反指示,否则在本文中所要求保护的包括一个以上动作的任何方法中,该方法的动作的次序不必局限于其中叙述该方法的动作的次序,而是本公开包括其中次序如此被限制的实施例。还应当理解,除非另外指示或根据上下文明显看出,否则本文中所描述的任何产品或组合物可以被认为是“孤立的”。
如本文中所使用的,术语“包括(comprising或comprises)”用于涉及对所公开的实施例必不可少的组合物、方法、以及其一个或多个相应部件,但是仍然为开放式的,以包括未指定元素,无论其是否必不可少。
如本文中所使用的,术语“基本上由……组成”涉及给定实施例所需的那些元件。该术语容许存在实质上不影响本公开的该实施例的一个或多个基础和新颖或功能性特点的附加元件。
术语“由...组成”涉及本文中所描述的组合物、方法及其相应部件,其不包括未在该实施例的描述中叙述的任何要素。
尽管上文已经对一些变型进行了详细描述,但是其他修改或添加是可能的。
在上述描述和权利要求中,诸如“其中至少一个”或“其中一个或多个”的短语可能在元素或特征的连结性列表之后出现。术语“和/或”也可以出现在两个或更多个元件或特征的列表中。除非另外与短语所用于的上下文隐含地或明确地矛盾,否则该短语旨在意指单独所列元素或特征中的任何所列元素或特征、或任何叙述元素或特征与其他任何叙述元素或特征的组合。例如,短语“A和B中的至少一个”、“A和B中的一个或多个”、和“A和/或B”分别旨在意指“单独A、单独B、或A和B一起”。类似解释也旨在用于包括三个或更多个项的列表。例如,短语“A、B和C中的至少一个”、“A、B和C中的一个或多个”、以及“A、B和/或C”分别旨在意指“单独A、单独B、单独C、A和B一起、A和C一起、B和C一起、或A和B和C一起”。另外,在上文并且在权利要求中使用术语“基于”旨在意指“至少部分地基于”,使得也容许未叙述特征或元件。
依据期望配置,本文中所描述的主题可以在系统、装置、方法和/或物品中体现。前述描述中所阐述的实现方式并不代表与本文中所描述的主题一致的所有实现方式。相反,它们仅是和与所描述的主题有关的方面一致的一些示例。尽管上文已经对一些变型进行了详细描述,但是其他修改或添加也是可能的。特别地,除了本文中所阐述的那些特征和/或变化之外,还可以提供其他特征和/或变化。例如,上文所描述的实现方式可以是指所公开的特征的各种组合和子组合和/或上文所公开的若干其他特征的组合和子组合。另外,附图中所描绘的和/或本文中所描述的逻辑流程不一定需要所示的特定次序或顺序次序来实现期望结果。其他实现方式也可以在所附权利要求的范围内。
- 用于对组织进行选择性治疗的装置
- 用于非侵入性地对利用治疗射线进行治疗的生物组织进行温度测定的方法和装置
