基于机器学习的炎症性肠病精准用药方法及系统
文献发布时间:2023-06-19 11:26:00
技术领域
本发明涉及医学图像处理技术领域,具体地,涉及一种基于机器学习的炎症性肠病精准用药方法及系统。
背景技术
炎症性肠病(inflammatory bowel disease,IBD)是一种临床常见的慢性非特异性的肠道炎症性疾病。随着炎症性肠病情发展的严重程度会导致临床治疗方案的不同,因此炎症性肠病情的精准评估对药物疗效和个性化治疗具有重要意义。在临床上,内窥镜检查是估计和评估疾病、治疗结果的有效手段。然而,内窥镜操作复杂,患者耐受性差以及无法完整评估肠道损伤等缺点限制了内窥镜的使用。因此,寻找一种自动的炎症性肠病病情评估和无创疗效评估方法对炎症性肠病的临床诊断和精准治疗具有重要意义。
公开号为CN110880361A的中国发明专利,公开了一种个性化精准用药推荐方法及装置,包括:获取患同一疾病的多个病患的病历数据,包括结构化数据、文本数据及影像数据;从文本数据中得到病患的用药信息;从多个历史病患的用药信息中筛选得到目标病患的第一药品推荐结果;将病患的病历数据进行合并处理,得到病患的病情特征信息;从多个历史病患中筛选出与目标病患的当前病情特征信息相似的至少一个相似病患;根据相似病患的用药信息生成第二药品推荐结果;根据第一药品推荐结果及第二药品推荐结果得到目标病患的个性化药品推荐结果。本发明实施例提供的技术方案能够解决现有技术中病患用药精准度低的问题。
近几年,计算机技术的不断成熟为CT技术的完善和发展提供了条件。能谱CT的出现为炎症性肠病的无创疗效评估提供了新的机遇。能谱CT在普通CT的基础之上采用宝石探测器、高压瞬时变能发生器和动态变焦管,可以很好的克服常规CT密度分辨率低,硬化伪影、同物异影、异物同影等缺点,获取最优单能量图从而进行物质区分与定量。目前临床上对于炎症性肠病中克罗恩病(Crohn Disease,CD)的病情评估多采用CDAI评分。此评分涉及多种临床指标,收集复杂且得出结果可能与客观病情不符。如各种检查提示病变严重,但CDAI很低;CDAI很高但是患者客观病情轻微。目前最新评分系统包括MRE评分、CE-US评分和CE评分,这些评分系统虽然参数收集简单但还是无法提高评分的准确度。缺乏一种通过研究影像学特征进行更为精准的自动分类模型。
当前对于IBD的医疗模式多为通过一个治疗方案满足所有患者,虽然对部分患者有充分的疗效,但仍有大多数疗效不佳的患者。近年来精准医疗不断被接受和采纳,精准医疗可以根据每个患者的个性化特征定制治疗方法。在IBD的治疗方案选择中可以采用精准医学方法,考虑个体分子生物学和环境因素对治疗方案疗效的影响,促进更好的临床决策。但目前研究缺少统一的炎症性肠病病情严重程度与用药指导的映射,难以构建合适的炎症性肠病药物评估模型从而达到精准治疗的目的。
发明内容
针对现有技术中的缺陷,本发明的目的是提供一种基于机器学习的炎症性肠病精准用药方法及系统。
根据本发明提供的一种基于机器学习的炎症性肠病精准用药方法及系统,所述方案如下:
第一方面,提供了一种基于机器学习的炎症性肠病精准用药方法,所述方法包括:
步骤S1:获取炎症性肠病能谱CT数据并对能谱CT数据进行预处理,基于处理后的数据制作病情活动度-用药标签数据集;
步骤S2:对预处理后的能谱CT数据运用end to end卷积神经网络进行病灶区域分割,得到炎症性肠病病灶区域ROI
步骤S3:将炎症性肠病病灶区域ROI
构建迁移模型,将由176个特征进行目标任务T分类,迁移到由60个特征进行目标任务T分类的迁移模型,通过迭代优化获得60个与临床用药疗效最相关特征;
步骤S4:将选择出的60个最相关特征进行整合,通过影像组学方法训练多个分类器,并使用AdaBoost集成学习方法对这些分类器进行“加性模型”训练,获得炎症性肠病无创用药评估模型。
优选的,所述步骤S1具体如下:
通过CTE序列薄层扫描方式,能谱CT采用高140kV、低80kV能量瞬时切换,根据这两种能量下获得的采样数据确定体素在40~140keV能量范围内的衰减系数获取101个单能量图,扫描层厚及层间距5mm;
能谱CT采用自适应统计迭代重建算法(daptive statistical iterativereconstruction,ASIR)与滤波反投影算法(filtered back projection,FBP)将单能量图联合40%水平的ASiR进行重建,即图像由ASiR与FBP以4:6的权重混合而成,重建层厚及层间距1.25mm;
对获取的重建图像进行数据脱敏并剔除不规范的图像;
对训练数据进行预处理,采用去均值化操作,并将数据的幅度归一化到同一范围之内;
制定病情-用药规范,根据IBD病情严重程度不同采用不同的药物治疗。
优选的,所述步骤S2中对得到的能谱CT图像进行病灶区域分割,具体如下:
对CT图像进行下采样提取特征值,卷积核大小为3×3,步长为2,在每组卷积操作之后进行max-pooling操作,使得图片进一步缩小为原来的1/2;
在下采样过程中总共进行4次来获取特征,最后得到256幅16×16的下采样特征图,其中,各卷积层使用的卷积核个数分别是32、64、128、256;
上采样过程使用4组反卷积操作将图片扩展为原来的2倍,将对应层的特征图进行剪裁和复制,组成上卷积的结果;
上采样过程结束后,得到256×256大小的图,最后用一个1×1的卷积核将通道数减到2,用不同的标签进行标记,完成CT图片分割,得到ROI
在模型训练过程中采用损失函数对分割结果进行评估。
优选的,所述损失函数构建如下:
L
其中
优选的,所述步骤S3包括:
使用WORC工具包方法对步骤S2中获得的ROI
采用SVM和hinge loss函数构建迁移模型。
优选的,所述采用SVM和hinge loss函数构建迁移模型包括:
定义D为176个图像特征和病情程度标签的集合,源任务s为病情分类预测任务,将病情程度标签y
定义由176个特征进行目标任务T分类,迁移到由t个特征进行目标任务T分类的迁移模型
对于所有的(s,y
优选的,所述步骤S4包括:
通过影像特征进行IBD病情分类,将步骤S3选出的60个与临床用药疗效最相关的特征输入到多个基础分类器进行训练;
采用AdaBoost集成学习算法,输入定义为前一步选择出的各个特征x=[x
输出定义为一个多分类问题,即s
学习的组合分类器定义为4个基础分类器的线性组合
每次迭代利用下一轮基础分类器h
模型训练完成后输入测试集的数据,对每一个病例,模型都会自动输出列向量s
对应于病情程度标签y
第二方面,提供了一种基于机器学习的炎症性肠病精准用药系统,所述系统包括:
模型M1:获取炎症性肠病能谱CT数据并对能谱CT数据进行预处理,基于处理后的数据制作病情活动度-用药标签数据集;
模型M2:对预处理后的能谱CT数据运用end to end卷积神经网络进行病灶区域分割,得到炎症性肠病病灶区域ROI
模型M3:将炎症性肠病病灶区域ROI
构建迁移模型,将由176个特征进行目标任务T分类,迁移到由60个特征进行目标任务T分类的迁移模型,通过迭代优化获得60个与临床用药疗效最相关特征;
模型M4:将选择出的60个最相关特征进行整合,通过影像组学方法训练多个分类器,并使用AdaBoost集成学习方法对这些分类器进行“加性模型”训练,获得炎症性肠病无创用药评估模型。
优选的,所述模块M1具体如下:
模块M1.1:通过CTE序列薄层扫描方式,能谱CT采用高140kV、低80kV能量瞬时切换,根据这两种能量下获得的采样数据确定体素在40~140keV能量范围内的衰减系数获取101个单能量图,扫描层厚及层间距5mm;
模块M1.2:能谱CT采用自适应统计迭代重建算法(daptive statisticaliterative reconstruction,ASIR)与滤波反投影算法(filtered back projection,FBP)将单能量图联合40%水平的ASiR进行重建,即图像由ASiR与FBP以4:6的权重混合而成,重建层厚及层间距1.25mm;
模块M1.3:对获取的重建图像进行数据脱敏并剔除不规范的图像;
模块M1.4:对训练数据进行预处理,采用去均值化操作,并将数据的幅度归一化到同一范围之内;
模块M1.5:制定病情-用药规范,根据IBD病情严重程度不同采用不同的药物治疗。
优选的,所述模块M2中对得到的能谱CT图像进行病灶区域分割,具体如下:
模块M2.1:对CT图像进行下采样提取特征值,卷积核大小为3×3,步长为2,在每组卷积操作之后进行max-pooling操作,使得图片进一步缩小为原来的1/2;
在下采样过程中总共进行4次来获取特征,最后得到256幅16×16的下采样特征图,其中,各卷积层使用的卷积核个数分别是32、64、128、256;
模块M2.2:上采样过程使用4组反卷积操作将图片扩展为原来的2倍,将对应层的特征图进行剪裁和复制,组成上卷积的结果;
上采样过程结束后,得到256×256大小的图,最后用一个1×1的卷积核将通道数减到2,用不同的标签进行标记,完成CT图片分割,得到ROI
模块M2.3:在模型训练过程中采用损失函数对分割结果进行评估。
与现有技术相比,本发明具有如下的有益效果:
1、将卷积神经网络应用于IBD的病情分类,从而实现基于能谱CT影像的无创疗效人工智能评估,克服临床上采用的复杂评分带来的诸多局限;
2、本发明提供的IBD精准用药方法具有较高的灵敏度和准确性,可以帮助指导IBD患者的治疗方案选择,评估预后,进而缩短IBD患者的治疗时间,具有更好的临床实用性。
附图说明
通过阅读参照以下附图对非限制性实施例所作的详细描述,本发明的其它特征、目的和优点将会变得更明显:
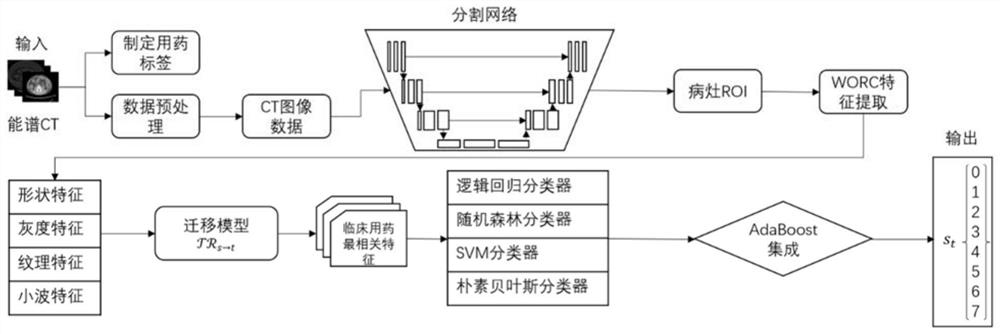
图1为本发明整体流程图。
具体实施方式
下面结合具体实施例对本发明进行详细说明。以下实施例将有助于本领域的技术人员进一步理解本发明,但不以任何形式限制本发明。应当指出的是,对本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变化和改进。这些都属于本发明的保护范围。
本发明实施例提供了一种基于机器学习的炎症性肠病精准用药方法,具体如下;
实施例1:
为了解决临床中对于炎症性肠病病情评估复杂,用药不规范的问题,本发明提出一种基于机器学习的炎症性肠病精准用药方法,包括:
步骤S1:获取炎症性肠病能谱CT数据并对能谱CT数据进行预处理,预处理包括采用40%ASiR重建出层厚1.25mm、层间距0.8cm的小肠静脉期CT图像,对CT数据进行脱敏、清洗、重采样等处理,获得分辨率统一、灰度分布相同的CT数据。基于处理后的数据制作病情活动度-用药标签数据集,具体地:
通过CTE序列薄层扫描方式,能谱CT采用高140kV、低80kV能量瞬时切换,根据这两种能量下获得的采样数据确定体素在40~140keV能量范围内的衰减系数获取101个单能量图,扫描层厚及层间距5mm。能谱CT采用自适应统计迭代重建算法(daptive statisticaliterative reconstruction,ASIR)与滤波反投影算法(filtered back projection,FBP)将单能量图联合40%水平的ASiR进行重建,即图像由ASiR与FBP以4:6的权重混合而成,重建层厚及层间距1.25mm,对比常规CT可以降低图像噪声,提高密度分辨率及降低辐射剂量。
对获取的重建图像进行数据脱敏并剔除不规范的图像,以提高数据的一致性。对训练数据进行预处理,采用去均值化操作,并将数据的幅度归一化到同一范围之内,减少各维度数据取值范围存在的差异而带来的干扰。
制定病情-用药规范,根据IBD病情严重程度不同采用不同的药物治疗。IBD分为溃疡性结肠炎(Ulcerative Colitis,UC)和克罗恩病(Crohn Disease,CD),其中溃疡性结肠炎和克罗恩病依据病情严重性分为缓解期、轻度、中度和重度。制定病情程度标签y
表1:IBD治疗方案
步骤S2:对预处理后的能谱CT数据运用end to end卷积神经网络进行病灶区域分割,得到炎症性肠病病灶区域ROI
对CT图像进行下采样提取特征值,卷积核大小为3×3,步长为2,在每组卷积操作之后进行max-pooling操作,使得图片进一步缩小为原来的1/2,在下采样过程中总共进行4次来获取特征,最后得到256幅16×16的下采样特征图,其中,各卷积层使用的卷积核个数分别是32、64、128、256。上采样过程使用4组反卷积操作将图片扩展为原来的2倍,将对应层的特征图进行剪裁和复制,组成上卷积的结果,上采样过程结束后,得到256×256大小的图,最后用一个1×1的卷积核将通道数减到2,用不同的标签进行标记,完成CT图片分割,得到ROI
在模型训练过程中采用损失函数对分割结果进行评估。其中,损失函数构建如下:
L
其中
步骤S3:将炎症性肠病病灶区域ROI
使用WORC工具包方法对步骤S2中获得的ROI
表2:特征选择
采用SVM和hinge loss函数构建迁移模型,具体地:
定义D为176个图像特征和病情程度标签的集合,源任务s为病情分类预测任务,将病情程度标签y
定义由176个特征进行目标任务T分类,迁移到由t个特征进行目标任务T分类的迁移模型
对于所有的(s,y
步骤S4:将选择出的60个最相关特征进行整合,通过影像组学方法训练多个分类器,并使用AdaBoost集成学习方法对这些分类器进行“加性模型”训练,获得炎症性肠病无创用药评估模型,该步骤具体如下:
通过影像特征进行IBD病情分类,将步骤S3选出的60个与临床用药疗效最相关的特征输入到四个基础分类器进行训练,四个分类器为:逻辑回归分类器、随机森林分类器、SVM分类器和朴素贝叶斯分类器。
采用AdaBoost集成学习算法,输入定义为前一步选择出的各个特征x=[x
每次迭代利用下一轮基础分类器h
实施例2:
实施例2是实施例1的变化例。
参照图1所示,本发明提出的一种基于机器学习的炎症性肠病精准用药方法,有以下步骤:
步骤(1):通过CTE序列薄层扫描方式获取CT图像,能谱CT采用高140kV、低80kV能量瞬时切换,根据这两种能量下获得的采样数据确定体素在40~140keV能量范围内的衰减系数,得到单能量图像。然后,通过数据脱敏、重采样等预处理方法获得分辨率统一、灰度分布大致相同的CT数据分,且数据大小均为256×256。并且制定病情-用药规范,根据IBD病情严重程度不同采用不同的药物治疗。
步骤(2):炎症性肠病CT图像病灶区域分割:利用步骤(1)获得的CT图像通过CNN网络分割出感兴趣区域(region of interest,ROI,大小为256×256)ROI
步骤(3):将炎症性肠病感兴趣区域ROI
步骤(4):将选择出的60个与临床用药疗效最相关特征进行整合,训练多个个体分类器,并使用AdaBoost集成学习方法对这些个体分类器进行“加性模型”训练从而构建炎症性肠病无创用药疗效评估模型,完成自动化精准用药的任务。
参照图1所示,步骤(1)中所述预处理方法具体包括:
数据脱敏和清洗;对医院采集到的原始能谱CT数据中的敏感信息按照脱敏规则进行数据的变形。数据重采样;本发明将全部数据集中以固定的同构分辨率重新采样,将所有样本重采样为256×256大小。
病情-用药规范,根据IBD病情严重程度不同采用不同的药物治疗。IBD分为溃疡性结肠炎(Ulcerative Colitis,UC)和克罗恩病(Crohn Disease,CD),其中溃疡性结肠炎和克罗恩病依据病情严重性分为轻度、中度和重度。
参照图1所示,步骤(2)中的病灶区域分割方法具体包括:
本发明采用CNN分割网络对步骤(1)获得的CT图像进行分割获得感兴趣区域(region of interest,ROI,大小为256×256×4)ROI
参照图1所示,步骤(3)中讲述的特征提取方法包括:
1、使用WORC工具包方法对ROI
2、采用SVM和合页损失函数构建关联迁移模型,将由176个特征进行目标任务T分类,迁移到由t(t=60)个特征进行目标任务T分类的迁移模型
参照图1所示,步骤(4)中讲述的无创用药疗效评估方法包括:
1、将选出的60个与临床用药疗效最相关的特征输入到四个个体分类器进行训练,四个个体分类器采用逻辑回归分类器、随机森林分类器、SVM分类器和朴素贝叶斯分类器。
2、用AdaBoost集成学习算法,输入定义为前一步选择出的各个特征x=[x
3、利用获得的下一轮基础分类器h
本发明实施例提供了一种基于机器学习的炎症性肠病精准用药方法,将卷积神经网络应用于IBD的病情分类,从而实现基于能谱CT影像的无创疗效人工智能评估,克服临床上采用的复杂评分带来的诸多局限;且本发明提供的IBD精准用药方法具有较高的灵敏度和准确性,可以帮助指导IBD患者的治疗方案选择,评估预后,进而缩短IBD患者的治疗时间,具有更好的临床实用性。
本领域技术人员知道,除了以纯计算机可读程序代码方式实现本发明提供的系统及其各个装置、模块、单元以外,完全可以通过将方法步骤进行逻辑编程来使得本发明提供的系统及其各个装置、模块、单元以逻辑门、开关、专用集成电路、可编程逻辑控制器以及嵌入式微控制器等的形式来实现相同功能。所以,本发明提供的系统及其各项装置、模块、单元可以被认为是一种硬件部件,而对其内包括的用于实现各种功能的装置、模块、单元也可以视为硬件部件内的结构;也可以将用于实现各种功能的装置、模块、单元视为既可以是实现方法的软件模块又可以是硬件部件内的结构。
以上对本发明的具体实施例进行了描述。需要理解的是,本发明并不局限于上述特定实施方式,本领域技术人员可以在权利要求的范围内做出各种变化或修改,这并不影响本发明的实质内容。在不冲突的情况下,本申请的实施例和实施例中的特征可以任意相互组合。
- 基于机器学习的炎症性肠病精准用药方法及系统
- 一种基于症状分析和机器学习的用药推荐系统和方法
