基于DNA纳米阶梯聚焦效应的尿嘧啶DNA糖基化酶双模式检测方法及应用
文献发布时间:2023-06-19 18:32:25
技术领域
本发明涉及电化学生物传感器的制备及双模式检测方法的构建,尤其是涉及基于DNA纳米阶梯聚焦效应的尿嘧啶DNA糖基化酶双模式检测方法及应用,属于功能生物材料和生物传感技术领域。
背景技术
基因组由形成特定碱基配对的DNA碱基组成,其准确性和稳定性对于细胞周期至关重要。尿嘧啶DNA糖基化酶(UDG)是一种重要的DNA修复酶,对于维持基因组完整性非常关键,UDG可以通过启动碱基切除修复(BER)从DNA中去除尿嘧啶碱基,从而产生无嘧啶(AP)位点。UDG活性异常常与许多病变有关,如高级别淋巴瘤、神经退行性疾病和布卢姆综合征等,且UDG水平异常通常先于病灶恶化,因此对于相关疾病的早期监测具有巨大潜力。目前,UDG检测方法包括电化学、化学发光、荧光法和比色法等,电化学方法因其简单、可靠和灵敏的内在优点而引起了极大关注。因此,基于电化学检测技术设计一种更灵敏更有效的策略来实现UDG活性检测具有较大的实际意义。
近年来对传染病和恶性肿瘤早期诊断的需求不断增加,因此用于疾病标志物检验的高灵敏度和高选择性生物传感方法受到极大关注。多种DNA信号扩大技术(如聚合酶链反应(PCR)、连接酶链反应(LCR)、滚环扩增(RCA)和杂交链反应(HCR)等)已经被用于该领域。其中,基于HCR的扩增技术以其无酶等温扩增的优势引起了研究者的兴趣,该方法的优势在于让引发剂快速触发自主复制反应以生成长的DNA链,从而作为负载大量信号标签的载体,如量子点、电化学氧化还原探针、荧光团和电化学发光探针等,以实现放大信号输出。本发明利用DNA的可寻址性引导的HCR反应构建了新型的DNA纳米阶梯,并用于UDG活性监测,具有较好的新颖性。
本发明专利首先合成了特殊的DNA纳米三棱柱,该三棱柱含有UDG的底物发卡DNA,因此将UDG滴到DNA纳米三棱柱修饰电极表面后,可以去除尿嘧啶使发卡DNA变成直链DNA,DNA U1由于能够被该直链DNA捕获,从而导致引发纳米阶梯(M1模块,M2模块)在电极表面组装,进而触发DNA纳米梯形的原位形成。随后本专利设计了双模态信号输出方式:(1)Ru(phen)
发明内容
本发明所要解决的技术问题是提供一种选择性好、灵敏度高、稳定性高、结果准确可靠、成本低的基于DNA纳米阶梯聚焦效应的尿嘧啶DNA糖基化酶双模式检测方法及应用。
本发明解决上述技术问题所采用的技术方案为:基于DNA纳米阶梯聚焦效应的尿嘧啶DNA糖基化酶双模式检测方法及应用,具体步骤如下:
(1)含UDG剪切位点的DNA三棱柱(prism)合成
①将L
L
10×TAE/Mg
prism合成步骤中退火条件为:95℃,5min;65℃,30min;50℃,30min;37℃,30min;22℃,30min;4℃,30min;hold,4℃。
(2)M1和M2的合成
鉴于本发明中需要DNA纳米阶梯来实现信号的放大,设计了三条特殊的DNA(U1,H1和H2),其序列如表中所述,且M1与M2的合成如下:
H1(终浓度:4μM)和H2(终浓度:4μM)分别在Tris-HCI-EDTA-Mg
Tris-HCI-EDTA-Mg
三条特殊的DNA(U1,H1和H2),序列如下:
(3)电化学发光传感器的制备
Electrode 1制备:金电极(Au)使用前分别用直径为0.3μm和0.05μm的Al
Electrode 2制备:将2.5~5μL合成的DNA三棱柱溶液滴到Electrode 1表面,置于冷藏冰箱中过夜。
Electrode 3制备:经DEPC水洗涤后,将2.5~5μL反应体系的1×UDG反应缓冲液以及不同浓度的UDG滴到三棱柱修饰电极表面,于37℃下孵育1~3小时,DEPC水缓缓冲洗电极,成功制备电极标记为Electrode 2,备用。
Electrode 4制备:
对于ECL检测方法:U1(2.5~5μL,100~200nM)滴于Electrode 3上,并在37℃下孵育1~2h。为了形成DNA纳米阶梯,将含有M1,M2(1~2μM)和Ru(phen)
对于EIS检测方法:U1(2.5~5μL,100~200nM)滴于Electrode 3上,并在37℃下孵育1~2h。为了形成DNA纳米阶梯,将含有M1,M2(1μM)和MnTMPyP(3μM)的混合物与电极一起温育16~20h。随后,为了在电极表面上获得沉淀,将改性的电极浸入含有5mM DAB和1mMH
在Electrode 3电极制备过程中,改变UDG浓度,探究其对电化学阻抗和电化学发光信号的影响。所采用的电化学发光参数条件如下:通过BPCL T15测量分析系统,设置高压为800V,扫描速率为100mV/s,扫描电压为0~1.35V。所采用的电化学阻抗参数条件如下:交流频率范围为10
发明原理:本发明专利首先在电极表面组装DNA三棱柱,再利用UDG去除尿嘧啶使发卡DNA变成直链DNA,可以捕获DNAU1,进而触发DNA纳米梯形(涉及M1和M2)的原位形成。随后我们设计了双模态信号输出方式:(1)Ru(phen)
(1)高灵敏度。实验得出传感器的电化学发光响应对UDG浓度对数值的线性相关方程为y=27181gC
(2)高特异性。常见其他相关酶对本检测体系均无干扰。原因在于:本发明是基于UDG去除尿嘧啶,最后促使DNA纳米梯形的原位形成。UDG的量会影响到Ru(phen)
(3)结果准确。回收率均在90%~110%之间。
(4)抑制剂。利用该生物传感器对插入Ru(phen)
(5)制备与检测方法试剂用量少、检测速度快、成本低。
综上所述,基于DNA纳米阶梯聚焦效应的尿嘧啶DNA糖基化酶双模式检测方法及应用,具有灵敏度高、选择性好、操作简单、分析快速、易于操作等优点,可以实现低浓度UDG的检测及其小分子抑制剂的筛选,具有良好的应用前景。
附图说明
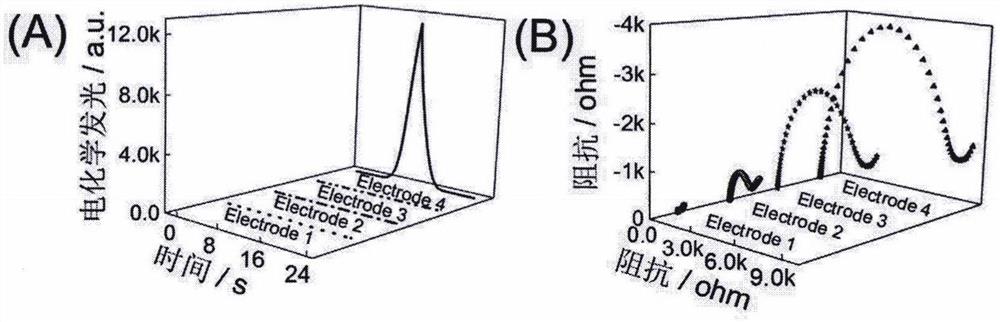
图1为本发明传感器的双模式检测方法可行性实验图;
图2为本发明传感器对有无UDG的电化学发光响应和电化学阻抗响应;
图3为本发明传感器对不同浓度UDG的电化学发光和电化学阻抗响应对UDG浓度
的对数校准曲线图;
图4为双模式检测下不同浓度UGI对UDG活性的抑制作用;
图5为双模式检测下本发明传感器的选择性实验图。
具体实施方式
以下结合附图实施例对本发明作进一步详细描述。
实施例1传感器的制备
(1)prism合成
①将L
10×TAE/Mg
prism合成步骤中退火条件为:95℃,5min;65℃,30min;50℃,30min;37℃,30min;22℃,30min;4℃,30min;hold,4℃。
(2)M1和M2的合成
鉴于本发明中需要DNA纳米阶梯来实现信号的放大,设计了三条特殊的DNA(U1,H1和H2),M1与M2的合成如下:
H1(终浓度:4μM)和H2(终浓度:4μM)分别在Tris-HCI-EDTA-Mg
Tris-HCI-EDTA-Mg
(3)电化学发光传感器的制备
Electrode 1的制备:金电极(Au)使用前分别用直径为0.3μm和0.05μm的Al
Electrode 2的制备:将5μL合成的DNA三棱柱溶液滴到Electrode 1表面,置于冷藏冰箱中过夜。
Electrode 3的制备:经DEPC水洗涤后,将5μL反应体系的1×UDG反应缓冲液以及不同浓度的UDG滴到三棱柱修饰电极表面,于37℃下孵育1小时,DEPC水缓缓冲洗电极,成功制备电极标记为Electrode 2,备用。
(4)电化学发光(ECL)和电化学阻抗(EIS)测试
对于ECL检测方法:U1(5μL,100nM)滴于Electrode 3上,并在37℃下孵育2h。为了形成DNA纳米阶梯,将含有M1,M2(1μM)和Ru(phen)
对于EIS检测方法:U1(5μL,100nM)滴于Electrode 3上,并在37℃下孵育2h。为了形成DNA纳米阶梯,将含有M1,M2(1μM)和MnTMPyP(3μM)的混合物与电极一起温育16h。随后,为了在电极表面上获得沉淀,将改性的电极浸入含有5mM DAB和1mM H
检测制备的四种电极的电化学阻抗和电化学发光响应,见图1。可看出制备的Electrode 4相比较于其他三种电极,电化学响应很明显,说明传感器已成功制备。
实施例2有无UDG的电化学发光和电化学阻抗响应
基于DNA纳米阶梯信号增强构建尿嘧啶DNA糖基化酶的电化学生物传感器,基于实施例1制备我们的生物传感器。见图2,UDG存在时,传感器在PB(0.1M,pH 7.0)中基本无电化学发光和电化学阻抗响应,而UDG存在时,存在明显的电化学发光和电化学阻抗响应,证明该传感器可用于UDG活性检测。
实施例3UDG活性检测
基于DNA纳米阶梯信号增强构建尿嘧啶DNA糖基化酶的电化学生物传感器,传感器的制备步骤同具体实施例1,Electrode 3构建过程中,依次改变UDG的浓度,UDG的浓度为:0,0.00001,0.00002,0.00005,0.0001,0.0002,0.0005,0.001,0.002,0.005,0.01,0.02,0.05,0.1,0.2,0.5U/mL。记录传感器在PB(0.1M,pH 7.0)中的电化学阻抗和电化学发光响应,根据实验结果,获得一系列不同浓度UDG对应的电化学响应曲线,建立电化学发光和电化学阻抗响应与UDG浓度之间的定量关系,根据两者之间的定量关系,确定待测样品中UDG的浓度。实验结果如图3所示,说明随着UDG浓度增大,传感器的电化学响应越明显,线性相关方程分别为y=2718lgC
实施例4 UDG抑制剂UGI的检测
基于DNA纳米阶梯信号增强构建尿嘧啶DNA糖基化酶的电化学生物传感器,传感器的制备步骤同具体实施例1,Electrode 3构建过程中,UDG的浓度为0.1U/mL,依次加入不同浓度的抑制剂UGI,UGI浓度为:0,0.001,0.002,0.003,0.005,0.008,0.01,0.02,0.03,0.05,0.08,0.1,0.2,0.3,0.5,0.8U/mL,随后用于制备传感器。记录传感器在PB(0.1M,pH7.0)中的电化学发光和电化学阻抗响应。根据实验结果得知(如图5),随着抑制剂UGI浓度的增大,相对应的电化学发光和电化学阻抗响应越弱,说明UGI对UDG活性的抑制作用越强,半抑制浓度分别为0.037U/mL、0.035U/mL。
实施例5选择性检测
选择性实验中UDG及其他酶的浓度均为0.1U/mL,所用到的其他酶的缩写如下:蛋白激酶(PKA)、末端转移酶(TdT)、组蛋白乙酰转移酶(HAT)、葡萄糖氧化酶(GOx)、辣根过氧化物酶(HRP)。按上述实施例1的传感器制备步骤,Electrode 3构建过程中,用其他相同浓度的酶代替UDG,制备得到传感器。结果如图5所示,与UDG对比,传感器对其他酶的电化学响应非常小,基本接近空白信号,说明传感器对于UDG的检测有很好的选择性。
当然,上述说明并非对本发明的限制,本发明也并不限于上述举例。本技术领域的普通技术人员在本发明的实质范围内做出的变化、改型、添加或替换,也应属于本发明保护范围。
- 热敏型尿嘧啶-DNA糖基化酶的制备方法
- 一种基于免标记无酶DNA机器荧光放大策略检测尿嘧啶-DNA糖基化酶活性的方法
- 检测尿嘧啶-DNA糖基化酶的、基于非酶纳米材料信号放大的无底物电化学生物传感器
