一种利用动态高压微射流技术制备枣多糖的方法
文献发布时间:2024-01-17 01:24:51
技术领域
本发明属于多糖提取技术领域,尤其涉及一种利用动态高压微射流技术制备枣多糖的方法。
背景技术
枣属于鼠李科,原产于中国。中国枣产量占全球产量的97%以上,世界上有枣树的国家约50多个,但均未形成规模化栽培。我国枣产区覆盖人口达2500万,种植面积约2200万亩,产量达到800余万吨,产值1000多亿元,种植地区以新疆、河南、河北、山东、陕西、山西等省份为主。据报道,枣含有多种生物活性化合物,如酚类、多糖、三萜类、核苷等,具有抗氧化、抗炎、降血脂、保护胃肠、防癌抗癌等作用,其中多糖是枣精深加工的产品之一。近年来,枣多糖作为一种天然大分子,因安全性高、副作用少等优点,受到了食品行业广泛关注。
目前枣多糖加工过程中存在的主要问题是分子量大、热稳定性差等。多糖改性是食品加工中的一种常见方法,与化学改性相比,物理改性更加安全高效,常见的物理改性方法有超声波、微波、超高压等。与之相比,动态高压微射流(Dynamic high pressuremicrofluidization,DHPM)技术是一种新兴的动态高压均质技术,它不仅结合高速冲击、高频振动、瞬时压降、强剪切、空化和超高压等技术优势,还可实现连续运行。前期研究聚焦在DHPM对蛋白质、淀粉、果胶等大分子的改性,多糖中的应用相对较少。因此,如何利用DHPM技术,降低枣多糖的分子量,提高其热稳定性是本领域亟需解决的关键问题。
发明内容
针对枣多糖分子量大、热稳定性差等技术问题,本发明提出一种利用DHPM技术制备枣多糖的方法。
为了达到上述目的,本发明的技术方案是这样实现的:
一种利用动态高压微射流技术制备枣多糖的方法,步骤如下:
(1)将枣去核烘干后,超微粉碎成枣粉,超声辅助热水法提取,提取液浓缩,醇沉,冷冻干燥得到枣粗多糖;
(2)将枣粗多糖溶液依次通过大孔树脂AB-8柱和DEAE纤维素DE-52柱纯化;
(3)纯化后的枣多糖溶液使用动态高压微射流处理,然后浓缩,冷冻干燥得到枣多糖。
所述步骤(1)中将枣粉与水按照料液质量比1:10~30混合后,在超声400~500 W,60~80 ℃的条件下提取30~40 min,提取液离心,离心条件为6000~7000 g,10~20 min,然后将上清液浓缩,浓缩液与3~5倍体积无水乙醇混合,在2~6 ℃下静置12~36 h,离心收集沉淀物,在-30~-40 ℃条件下冷冻干燥20~30 h后得到枣粗多糖。
所述步骤(3)中处理纯化后枣多糖溶液的动态高压微射流的压力为100~250 MPa,每个压力自动循环处理4~8次,处理温度20~30 ℃,将处理过后的多糖溶液浓缩,在-30~-40℃条件下冷冻干燥30~40 h得到枣多糖。
所述步骤(3)中处理纯化后枣多糖溶液的动态高压微射流处理压力优选为150MPa。
所述步骤(3)中每个压力自动循环处理优选为5次。
本发明的有益效果:DHPM是一种新兴高压处理技术,能够改善多糖结构及抗氧化活性。本研究比较了不同DHPM处理压力对枣多糖结构及抗氧化活性的影响。随着压力升高,枣多糖结构及抗氧化活性发生改变。当DHPM处理压力达150 MPa时,枣多糖溶液粒径从468.67 nm降至259.30 nm,降低44.7%,分子量从154.30KDa降至67.45 KDa,降低56.3%;枣多糖的峰值变性温度和焓变分别从159.4 ℃和25.7 J/g提高到173.5 ℃和110.4J/g,枣多糖结晶有序度增强,微观结构厚度更薄,热稳定性更高;同时,枣多糖溶液的DPPH和ABTS自由基清除能力的IC
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
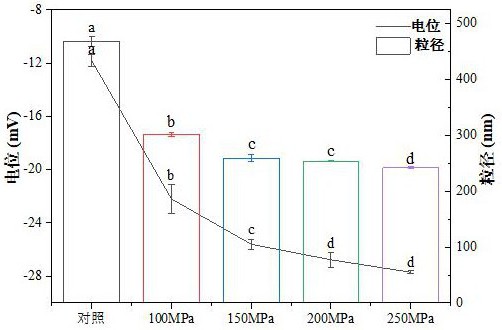
图1为不同DHPM处理压力对枣多糖溶液电位及粒径的影响图;
图2为不同DHPM处理压力对枣多糖分子量的影响图;
图3为不同DHPM处理压力下枣多糖红外光谱图;
图4为不同DHPM处理压力下枣多糖微观结构图;
图5为不同DHPM处理压力下枣多糖的DSC曲线图;
图6为不同DHPM处理压力下枣多糖溶液DPPH自由基清除率曲线图;
图7为不同DHPM处理压力下枣多糖溶液DPPH自由基清除IC
图8为不同DHPM处理压力下枣多糖溶液的ABTS自由基清除率曲线图;
图9为不同DHPM处理压力下枣多糖溶液ABTS自由基清除IC
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有付出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
实施例1
一种利用动态高压微射流技术制备枣多糖的方法,步骤如下:
(1)将枣去核烘干后,超微粉碎成枣粉,将枣粉与水按照料液质量比1:30混合后,在超声500 W,80 ℃的条件下提取40 min,提取液离心,离心条件为7000 g,20 min,然后将上清液浓缩,浓缩液与5倍体积无水乙醇混合,在6 ℃下静置36 h,离心收集沉淀物,在-40℃条件下冷冻干燥30 h后得到枣粗多糖;
(2)将枣粗多糖溶液依次通过大孔树脂AB-8柱和DEAE纤维素DE-52柱纯化;
(3)纯化后的枣多糖溶液使用动态高压微射流处理,动态高压微射流的压力为100MPa,每个压力自动循环处理5次,处理温度30 ℃,将处理过后的多糖溶液浓缩,在-40 ℃条件下冷冻干燥30 h得到枣多糖。
实施例2
一种利用动态高压微射流技术制备枣多糖的方法,与实施例1步骤不同的之处为动态高压微射流的压力为150 MPa,其余步骤相同。
实施例3
一种利用动态高压微射流技术制备枣多糖的方法,与实施例1步骤不同的之处为动态高压微射流的压力为200 MPa,其余步骤相同。
实施例4
一种利用动态高压微射流技术制备枣多糖的方法,与实施例1步骤不同的之处为动态高压微射流的压力为250 MPa,其余步骤相同。
实施例5
一种利用动态高压微射流技术制备枣多糖的方法,步骤如下:
(1)将枣去核烘干后,超微粉碎成枣粉,将枣粉与水按照料液质量比1:10~30混合后,在超声400~500 W,60~80 ℃的条件下提取30~40 min,提取液离心,离心条件为6000~7000 g,10~20 min,然后将上清液浓缩,浓缩液与3~5倍体积无水乙醇混合,在2~6 ℃下静置12~36 h,离心收集沉淀物,在-30~-40 ℃条件下冷冻干燥20~30 h后得到枣粗多糖;
(2)将枣粗多糖溶液依次通过大孔树脂AB-8柱和DEAE纤维素DE-52柱纯化;
(3)纯化后的枣多糖溶液使用动态高压微射流处理,动态高压微射流的压力为150MPa,每个压力自动循环处理4~8次,处理温度20~30 ℃,将处理过后的多糖溶液浓缩,在-30~-40 ℃条件下冷冻干燥30~40 h得到枣多糖。
实施例6
一种利用动态高压微射流技术制备枣多糖的方法,步骤如下:
(1)将枣去核烘干后,超微粉碎成枣粉,将枣粉与水按照料液质量比1:30混合后,在超声500 W,80 ℃的条件下提取40 min,提取液离心,离心条件为7000 g,20 min,然后将上清液浓缩,浓缩液与5倍体积无水乙醇混合,在6 ℃下静置36 h,离心收集沉淀物,在-40℃条件下冷冻干燥30 h后得到枣粗多糖;
(2)将枣粗多糖溶液依次通过大孔树脂AB-8柱和DEAE纤维素DE-52柱纯化;
(3)纯化后的枣多糖溶液使用动态高压微射流处理,动态高压微射流的压力为150MPa,每个压力自动循环处理8次,处理温度30 ℃,将处理过后的多糖溶液浓缩,在-40 ℃条件下冷冻干燥40 h得到枣多糖。
实施例7
一种利用动态高压微射流技术制备枣多糖的方法,步骤如下:
(1)将枣去核烘干后,超微粉碎成枣粉,将枣粉与水按照料液质量比1:10混合后,在超声400 W,60 ℃的条件下提取30 min,提取液离心,离心条件为6000 g,10 min,然后将上清液浓缩,浓缩液与3倍体积无水乙醇混合,在2 ℃下静置12h,离心收集沉淀物,在-30℃条件下冷冻干燥20 h后得到枣粗多糖;
(2)将枣粗多糖溶液依次通过大孔树脂AB-8柱和DEAE纤维素DE-52柱纯化;
(3)纯化后的枣多糖溶液使用动态高压微射流处理,动态高压微射流的压力为150MPa,每个压力自动循环处理6次,处理温度20 ℃,将处理过后的多糖溶液浓缩,在-30 ℃条件下冷冻干燥30 h得到枣多糖。
实施例8
一种利用动态高压微射流技术制备枣多糖的方法,步骤如下:
(1)将枣去核烘干后,超微粉碎成枣粉,将枣粉与水按照料液质量比1:20混合后,在超声450 W,70 ℃的条件下提取35 min,提取液离心,离心条件为6000 g,15 min,然后将上清液浓缩,浓缩液与4倍体积无水乙醇混合,在5 ℃下静置24 h,离心收集沉淀物,在-35℃条件下冷冻干燥25 h后得到枣粗多糖;
(2)将枣粗多糖溶液依次通过大孔树脂AB-8柱和DEAE纤维素DE-52柱纯化;
(3)纯化后的枣多糖溶液使用动态高压微射流处理,动态高压微射流的压力为200MPa,每个压力自动循环处理4次,处理温度30 ℃,将处理过后的多糖溶液浓缩,在-40 ℃条件下冷冻干燥40 h得到枣多糖。
实施例9
一种利用动态高压微射流技术制备枣多糖的方法,步骤如下:
(1)将枣去核烘干后,超微粉碎成枣粉,将枣粉与水按照料液质量比1:25混合后,在超声500 W,80 ℃的条件下提取30 min,提取液离心,离心条件为6000 g,20 min,然后将上清液浓缩,浓缩液与4倍体积无水乙醇混合,在5 ℃下静置24 h,离心收集沉淀物,在-40℃条件下冷冻干燥24 h后得到枣粗多糖;
(2)将枣粗多糖溶液依次通过大孔树脂AB-8柱和DEAE纤维素DE-52柱纯化;
(3)纯化后的枣多糖溶液使用动态高压微射流处理(FPG12800,英国SFP公司),动态高压微射流的压力为150 MPa,每个压力自动循环处理8次,处理温度25 ℃,将处理过后的多糖溶液浓缩,在-40 ℃条件下冷冻干燥36 h得到枣多糖。
上述实施例1-4得到的枣多糖性能测试
(1)电位粒径分析
使用纳米粒度电位仪(Zetasizer Nano ZS90,Malvern Instruments,UK),在25℃下测量1 mg/mL枣多糖溶液的平均粒径。
电位粒径分析结果如下:
随着DHPM压力升高,枣多糖溶液绝对Zeta电位显著增加,表明枣多糖溶液经DHPM处理后暴露出更多基团,颗粒表面电荷增加,颗粒间静电斥力增加,可以阻止颗粒进一步聚集。同时,与对照组枣多糖溶液粒径468.7 nm相比,随着处理压力上升,枣多糖溶液平均粒径逐渐下降。当处理压力达到150 MPa时,多糖溶液粒径为259.30 nm,降低44.7%,且与200Mpa多糖溶液粒径无显著差异。由此可知,DHPM处理可以降低枣多糖溶液的粒径,提高其稳定性(图1)。
(2)分子量分析
使用多角度激光散射凝胶色谱系统(Wyatt Technology Co.,USA)测定样品分子量分布。100 μL 1 mg/mL的枣多糖溶液通过0.45 μm滤膜后注入进样口,设备流动相为0.02% NaN
分子量分析结果如下:
DHPM处理后,枣多糖的分子量显著下降,从对照154.30 KDa下降到250 MPa的21.30 KDa,且200 MPa和250 MPa处理的枣多糖分子量没有显著变化。150 MPa处理压力时,枣多糖的分子量为67.45KDa,也远远低于对照(图2)。
(3)红外光谱分析
使用红外光谱仪(Vertex 70,Bruker Instruments,Germany)测定枣多糖的红外光谱。3 mg枣多糖样品和300 mg KBr固体粉末混合后,研磨均匀,用压片机压片,于4000~400 cm
红外光谱分析结果如下:
不同DHPM处理后的枣多糖样品具有相似的红外光谱。3420 cm
(4)多糖微观结构分析
使用场发射扫描电子显微镜(FE-SEM,Regulus 8100,Japan)观察样品的微观结构。枣多糖样品喷金,在高真空3 kV的加速电压下,观察500 ×倍数下样品微观结构。
微观结构分析结果如下:
对照组枣多糖样品结构较厚,且内部呈现多孔状态。DHPM处理后,枣多糖样品厚度变薄,内部基本无孔,结构更加均匀,且不同压力处理,微观结构变化不大(图4)。
(5)热稳定性分析
使用差示扫描热量热法(DSCQ20,TA Instruments,USA)分析DHPM处理对枣多糖热力学特性的影响。准确称取3 mg枣多糖样品放入铝坩埚中,设置测试温度范围为50-400℃,升温速率为10 ℃/min,氮气流速1 s/step。
热稳定性分析结果如下:
枣多糖在100-200 ℃范围内发生结晶吸热反应(图5)。对照组枣多糖的峰值变性温度和焓变分别为159.4 ℃和25.7 J/g,当压力达到150 MPa时,枣多糖的峰值变性温度达到173.5 ℃,ΔH为110.4J/g。ΔH与样品晶体的有序性有关,出现这种现象的原因是DHPM处理增强了枣多糖晶体的有序度,枣多糖产生更稳定的结构,需要更高的温度才能分解。然而,在200 MPa和250 MPa处理后,样品显示出两个吸热峰,这可能是由于高压破坏了枣多糖分子晶体的有序排列,导致多糖解聚和结构变化(表1)。
表1 不同DHPM处理压力对枣多样峰值变性温度和焓变的影响
(6)抗氧化活性分析
DPPH抗氧化活性:枣多糖溶解后得到浓度为0.5、1、1.5、2、2.5、3 mg/mL溶液。将100 μL枣多糖溶液与100 μL 0.1 mM DPPH溶液混合,37 ℃暗反应30 min,于517 nm处测量混合物的吸光度A
ABTS抗氧化活性:枣多糖溶解后得到浓度为0.5、1、1.5、2、2.5、3 mg/mL溶液。将7mmol/L ABTS溶液和2.45 mmol/L过硫酸钾溶液等体积混合均匀,避光放置12 h,制备ABTS储备溶液。将100 µL样品溶液和500 µL ABTS溶液混合均匀,避光反应5 min,734 nm处测吸光度。
抗氧化活性分析结果如下:
在0.5-3 mg/mL浓度范围内,枣多糖溶液对DPPH自由基表现出明显的清除作用,随着多糖浓度增加而升高,且呈现剂量依赖性。同时,DHPM处理压力越大,多糖溶液的DPPH自由基清除能力越强,IC
同样,在0.5-3 mg/mL浓度范围内,枣多糖溶液对ABTS自由基表现出明显的清除作用,随着多糖浓度增加而升高,且呈现剂量依赖性。ABTS处理压力越大,多糖溶液的ABTS自由基清除能力越强,IC
