贻贝仿生粘合剂、制备方法及其应用
文献发布时间:2024-04-18 20:01:55
技术领域
本发明涉及生物材料技术领域,具体而言涉及一种贻贝仿生粘合剂、制备方法及其应用。
背景技术
伤口闭合是影响外科手术疗效的重要环节,快速安全有效的伤口闭合技术能够减少病人的痛苦,粘合被认为是有效的伤口闭合技术,具有潜在的应用场景。
现有商用组织粘合剂主要有两种:一个是氰基丙烯酸酯粘合剂,但是其分解产物有着不可避免的生物毒性限制了它的应用;另外一个是纤维蛋白类粘合剂,但是其则受限于高昂价格和相对较弱的粘合性能而不能广泛应该。并且,大多数粘附性水凝胶在潮湿条件下无法实现有效粘合,这是因为水分子可以在潮湿条件下在目标基板表面形成薄水化层,这阻碍了水凝胶和目标基板之间的紧密接触;此外,水分子破坏了粘合剂水凝胶和目标基材之间的非共价相互作用。
为了开发具有优良性能的组织粘合剂,科学家从海洋粘附生物(贻贝和沙堡蠕虫等)汲取灵感,开发了一系列基于海洋生物的粘合剂。这种粘合剂虽然解决了上述两种粘合剂存在的问题,但普遍存在合成步骤繁琐、固化速度慢、所得粘合剂力学性能差的问题。
因此,我们有必要对伤口闭合技术进行革新,开发新一代具有临床意义的组织粘合剂。
发明内容
本发明目的在于针对现有得不足,提供一种贻贝仿生粘合剂、制备方法及其应用,该水凝胶粘合剂具有高生物相容性、高湿粘能力,且力学性能可调控,制备简单,固化快,成本低廉。
根据本发明目的的第一方面,提供一种贻贝仿生粘合剂的制备方法,包括以下步骤:
将多巴胺修饰的透明质酸溶解于蒸馏水中得到第一溶液;
向第一溶液中加入镓源溶液,混合均匀后得到第二溶液;
向第二溶液中加入聚多巴胺溶液,混匀后调节pH,即得所需粘合剂;
其中,通过调节pH调控所述粘合剂的力学性能。
作为可选的实施方式,pH的调节范围为1~10。
作为可选的实施方式,所述多巴胺修饰的透明质酸的多巴胺的修饰度为10~70%,透明质酸的分子量为10~1500KDa。
作为可选的实施方式,镓源为硝酸镓、硫酸镓、氯化镓、醋酸镓、溴化镓中的一种或几种。
作为可选的实施方式,所述聚多巴胺溶液的浓度为0.5~3.0mg/mL,聚多巴胺的粒径为20~5000nm。
作为可选的实施方式,多巴胺修饰透明质酸中的多巴胺与镓离子的摩尔比为(1:1)~(1:3)之间。
根据本发明目的的第二方面,提供一种采用前述方法制备的贻贝仿生粘合剂。
根据本发明目的的第三方面,提供一种前述贻贝仿生粘合剂在制备皮肤或组织器官的粘合与修复和/或密封止血和/或细胞封装的水凝胶上的应用。
根据本发明目的的第四方面,提供一种前述贻贝仿生粘合剂在材料水下粘合中的应用。
根据本发明目的的第四方面,提供一种前述贻贝仿生粘合剂在生物活性物质递送中的应用。
由以上本发明的技术方案可见,本发明的贻贝仿生粘合剂,通过多巴胺修饰透明质酸上的多酚基团以及聚多巴胺上的多酚羟基,皆与镓离子配位成胶获得;
其中,通过多巴胺修饰透明质酸上的多酚基团和镓离子配位,作为永久交联,增加聚合物网络的弹性;同时整个体系中存在大量的氢键和Π-Π键,这些弱的键可以可逆的断裂和重组,从而增加网络的能量耗散,这种强键和弱键的结合极大的增加了聚合物的内聚力,从而提高材料的力学性能。
本发明的贻贝仿生粘合剂,采用疏水性聚多巴胺破坏阻碍粘附的水层,再通过多巴胺修饰的透明质酸上的多酚基团与各种底物相互作用,从而产生强大的湿粘附性。
本发明制备的贻贝仿生粘合剂,有着广泛的粘合性能,在pH为1~10的溶液中都有着优良的水下粘合性能,且在不同的pH下有着不同的力学性能,可根据应用需求进行调节。
附图说明
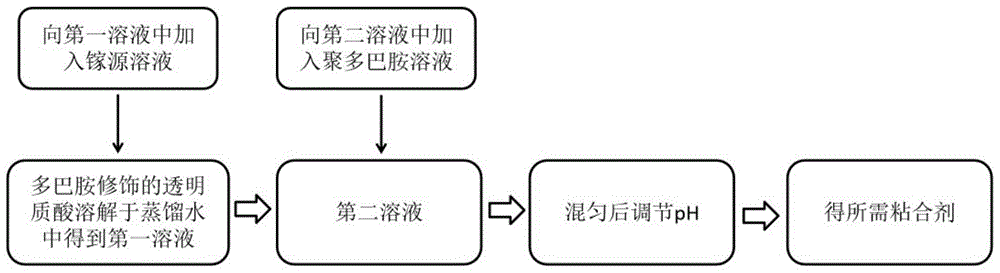
图1是本发明的贻贝仿生粘合剂的制备流程图。
图2A是本发明实施例3中的样品的实物图。
图2B是本发明实施例4中的样品的实物图。
图3是本发明实施例中样品4-2的粘附性能展示图。
图4是本发明实施例中样品4-2的水下粘附性能展示图。
图5是本发明实施例中样品4-2的自修复性能展示图。
图6是本发明实施例中样品4-2的可塑性性能展示图。
图7是本发明实施例中样品4-2的止血性能对比统计图。
图8是本发明实施例中样品4-2对姜黄素的包载能力测试图。
图9是本发明实施例中样品4-2对姜黄素得释放能力测试图。
具体实施方式
为了更了解本发明的技术内容,特举具体实施例并配合所附图式说明如下。
在本公开中参照附图来描述本发明的各方面,附图中示出了许多说明的实施例。本公开的实施例不必定意在包括本发明的所有方面。应当理解,上面介绍的多种构思和实施例,以及下面更加详细地描述的那些构思和实施方式可以以很多方式中任意一种来实施。
在自然界中,贻贝等海洋动物对海水中的各种基质表现出强大且可重复的水下附着力。贻贝的水下粘附是通过使用贻贝足蛋白(Mfps)中的阳离子赖氨酸和疏水残基破坏水化层来实现的,从而使儿茶酚基团与暴露的表面结合。
基于此,本发明通过精心设计复杂的水凝胶网络并仔细选择它们的成分,开发基于亲疏水平衡的湿粘附水凝胶。
本发明的技术方案是将多巴胺修饰的透明质酸、聚多巴胺、镓离子分散在水溶液中,混匀后发生凝胶化,并通过调节pH,获得具有不同力学性能的粘合剂。
结合图1所示,在本发明示例性的实施例中,提供一种贻贝仿生粘合剂的制备方法,包括以下步骤:
将多巴胺修饰的透明质酸溶解于蒸馏水中得到第一溶液;
向第一溶液中加入镓源溶液,混合均匀后得到第二溶液;
向第二溶液中加入聚多巴胺溶液,混匀后调节pH,即得所需粘合剂;
其中,通过调节pH调控所述粘合剂的力学性能。
作为可选的实施方式,pH的调节范围为1~10,pH值越高,金属-多酚的配位更加紧密,力学性能越好,使粘合剂在粘附过程中,尤其是在水下粘附的过程中增加保持凝胶形状的时间,从而延长凝胶粘附性的时间;但当pH超过10时会破坏聚合物网络,从而影响力学性能,减少了凝胶粘附性的时间,因此,pH的调节范围需在1~10。
力学性能差的水凝胶在水溶液中会快速溶胀,网络被破坏,凝胶解离,导致粘附性失效;而力学性能好的水凝胶,在溶胀后依旧能够保持凝胶的基本形态,保持其网络结构,保持凝胶的完整性,从而依旧具有粘附性;因此,可以根据需求通过调节pH值调节粘合剂的力学性能,以控制凝胶保持粘附性的时间。
作为可选的实施方式,所述多巴胺修饰的透明质酸的多巴胺的修饰度为10~70%,透明质酸的分子量为10~1500KDa。
可以理解的,多巴胺修饰的透明质酸得制备过程可采用现有技术,在此不做进一步限定。
作为可选的实施方式,镓源为硝酸镓、硫酸镓、氯化镓、醋酸镓、溴化镓中的一种或几种。
作为可选的实施方式,所述聚多巴胺溶液的浓度为0.5~3.0mg/mL,聚多巴胺的粒径为20~5000nm。
作为可选的实施方式,多巴胺修饰透明质酸中的多巴胺与镓离子的摩尔比为(1:1)~(1:3)之间。
在本发明另一个示例性的实施例中,提供一种采用前述方法制备的贻贝仿生粘合剂,该贻贝仿生粘合剂通过调节亲疏水平衡实现水下粘附,当粘合剂和一个表面湿润的物质接触时,粘合剂表面的聚多巴胺由于其疏水性会将物质表面的水膜破坏,从而使干燥的物质表面暴漏,进而让亲水的多巴胺修饰的透明质酸来跟干燥的物质表面直接接触,通过酚羟基连接从而使其具有湿粘附性。
在本发明另一个示例性的实施例中,提供一种前述贻贝仿生粘合剂在制备皮肤或组织器官的粘合与修复和/或密封止血和/或细胞封装的水凝胶上的应用,可应用于创伤伤口、尤其是动脉、内脏的湿粘附和快速止血。
在其他的实施例中,前述贻贝仿生粘合剂还可应用于玻璃、金属及其氧化物、塑料橡胶等多种材料的粘合。
在本发明另一个示例性的实施例中,提供一种前述贻贝仿生粘合剂在材料水下粘合中的应用,可在湿润的环境中进行材料的粘合。
在本发明另一个示例性的实施例中,提供一种前述贻贝仿生粘合剂在生物活性物质递送中的应用,生物活性物质包括药物、生物活性因子或细胞。
下面结合实施例来说明本发明的具体实施方式,但以下实施例只是用来详细说明本发明,并不以任何方式限制本发明的范围。
以下实施例中使用的试剂如无特别说明均采用市售试剂。
实施例1
[不同多巴胺修饰透明质酸衍生物的制备]
将2g透明质酸(HA)溶解在200mL 0.1M MES缓冲溶液中,并使用0.1M HCl将溶液的pH值调节至5.5,然后将1.4g EDC和0.2g NHS加入到透明质酸溶液中,反应活化约30分钟,后将多巴胺加入到上述反应混合液中并在室温下避光反应12小时,对所得反应溶液进行透析(透析袋截留分子量:3500Da),并在纯化过程中溶液的pH值保持在5.5。
透析过后,冷冻干燥,得到不同多巴胺修饰透明质酸衍生物,如表1所示。
表1不同多巴胺修饰透明质酸衍生物的制备
以下实施例中所用多巴胺修饰透明质酸:透明质酸分子量为400KDa,多巴胺修饰度为35.0%,即样品1-3。
实施例2
[不同类型镓离子下贻贝仿生粘合剂制备]
将4.00g多巴胺修饰的透明质酸溶解于100mL蒸馏水中,向其中加入0.75g镓源,然后像其中加入聚多巴胺,调节溶液pH=8,充分混合均匀,得到不同镓源下的粘合剂,如表2所示。
表2不同镓源粘合剂得制备
以下实施例采用硝酸镓作为镓源。
实施例3
[不同pH下贻贝仿生粘合剂的制备]
将4.00g多巴胺修饰的透明质酸溶解于100mL蒸馏水中,向其中加入0.75g硝酸镓,调节溶液pH,充分混合均匀,得到不同pH下的粘合剂,如表4所示。
表3不同pH下贻贝仿生粘合剂的制备
以下实施例采用溶液酸碱性为pH=8。
实施例4
[不同聚多巴胺尺寸和浓度下贻贝仿生粘合剂的制备]
将4.00g多巴胺修饰的透明质酸溶解于100mL蒸馏水中,向其中加入0.75g硝酸镓,然后像其中加入聚多巴胺,调节溶液pH=8,充分混合均匀,得到不同聚多巴胺尺寸和质量下的粘合剂,如表4所示。
表4不同尺寸和质量聚多巴胺下贻贝仿生粘合剂的制备
以下实施例中所用聚多巴胺:粒径200nm,质量1.0g。
实施例5
[贻贝仿生粘合剂的力学性能]
将样品3-1、3-2、3-3、3-5、3-6、3-7进行拍照,如图2A所示,随着pH的增加,凝胶的形状呈现出越来越立体的趋势,这是由于随着pH的增加,金属-多酚的配位由低pH下的单配位转变为高pH下的双配位或三配位,使得聚合物网络越来越紧密,凝胶的流变性能越来越好,从而使得水凝胶的形状呈现出越来越立体的趋势,对应的凝胶的力学性能也逐渐提高,使粘合剂在粘附过程中,尤其是在水下粘附的过程中能够增加保持凝胶基本形态的时间,保持凝胶的网络结构,保持凝胶的完整性,从而延长凝胶粘附性的时间;因此,可以根据需求通过调节pH值调节粘合剂的力学性能,以控制凝胶粘附性的时间。
将样品4-2、4-8、4-9进行拍照,如图2B所示,从图中可以看出,随着聚多巴胺量的增加,水凝胶的形状呈现出越来越立体的趋势,这与聚多巴胺加入后,聚多巴胺和游离的镓离子配位有关,聚多巴胺的加入也极大的增加了聚合物网络的内聚力使得力学性能增强。
实施例6
[贻贝仿生粘合剂的粘附性能]
将样品4-2制备的粘合剂进行粘附实验,从图中可以看到,本发明的粘合剂在干燥界面(图3)和湿界面(图4)上有着很好的粘附性能,且可以看出所制备的水凝胶可以实现多种材料的粘附。
实施例7
[贻贝仿生粘合剂的自修复性能和可塑性性能]
由于伤口的不规则性,这使得粘合剂应具有自修复性能和可塑性性能,在这里我们评估了样品4-2粘合剂的自修复性能(图5)和可塑性性能(图6)。
自修复性能通过先将水凝胶制备成直径为2cm,厚度为1cm的圆柱体,然后在中间将其破坏。不经任何处理的情况下,观察水凝胶圆柱体的变化,来证明其自修复性能。
可塑性实验通过将水凝胶塑造成各种不同的形状,且在它们之间进行变换,证明其具有可塑性性能。
从中可以看出,本发明的粘合剂具备一定的自修复能力和可塑性能力,可以适应各种不规则的伤口。
实施例8
[贻贝仿生粘合剂的止血性能评估]
将样品4-2与对比样品所制备的水凝胶进行大鼠断尾止血实验,评价该粘合剂的止血性能;采用8-10周的SD大鼠,实验前按体重随机分组(每组3只):a:空白组不做处理;b:对照组样品3-5;c:实验组样品4-2;将大鼠进行断尾实验,手术过程中,分别记录不同组的出血量。
从图7中可以看出,聚多巴胺的加入,引入了更多的酚羟基,使得可以粘附的位点增多,从而增加了水凝胶的粘合性能,使其具有更好的止血性能。
实施例9
[贻贝仿生粘合剂用于大鼠肝脏止血]
采用8-10周的SD大鼠,实验前按体重随机分组(每组10只):a:样品4-2贻贝仿生粘合剂水凝胶组;b:商品止血剂;c:模型空白组。手术过程中,分别记录不同组的出血量及出血时间。
结果显示,商品用的止血剂的止血效果比本发明的贻贝仿生粘合剂组效果差,这表明本发明制备的贻贝仿生粘合剂对于创伤有着更好的止血效果。
实施例10
[贻贝仿生粘合剂用于生物活性物质的包载与释放]
以样品4-2包载姜黄素为例,通过紫外测试分析溶液中药物的包载与释放。
药物的包载实验:
称取25.0mg Cur(姜黄素)加无水乙醇溶解,定容至25.00mL,作为1.000mg/mL的Cur储备液。精密量取储备液适量,用无水乙醇分别稀释成质量浓度为1.0、2.0、3.0、4.0、5.0、10、20μg/mL的系列对照品溶液。以无水乙醇为空白对照溶液,于430nm处测定吸光度(A)值。
以Cur的质量浓度(C)为横坐标,A值为纵坐标,绘制标准曲线,得线性回归方程。结果表明Cur在1.0~20.0μg/mL线性关系良好,并通过计算得出其包封率和载药量。
包封率=M1/M0
载药量=M1/(M0+M2)
式中:M0:投入的姜黄素质量;M1:计算得知实施例4-5样品中的姜黄素质量;M2:投入的样品4-5的质量。
每个样品平行测量三次,测试结果为平均值±标准偏差(SD)。
药物的释放实验:
将制备好的载药粘合剂分别放置于30mL的pH=6.0、6.8、7.2的PBS缓冲液中,将其放在37℃的恒温震荡摇床中(100rpm)进行药物释放实验,在预定的时间间隔,取出1mL的释放液,然后加入1mL的新鲜缓冲液以保持恒定的体积。
用紫外分光光度计来分析水凝胶释放的药物浓度,姜黄素的最大吸收峰在430nm,每个样品平行测量三次,测试结果为平均值±标准偏差(SD)。
如图8、9所示,本发明的粘合剂对姜黄素的载药量为4.0%;药物释放实验证明,本发明的粘合剂在pH=6.0的溶液中有更好的药物释放率,可达70%。
因此,本发明的粘合剂具有非常好的生物相容性,特别适用于生物活性物质的载体,包裹于本发明粘合剂中的生物活性物质通过分子的扩散作用和材料的降解作用实现药物持续释放的效果。
虽然本发明已以较佳实施例揭露如上,然其并非用以限定本发明。本发明所属技术领域中具有通常知识者,在不脱离本发明的精神和范围内,当可作各种的更动与润饰。因此,本发明的保护范围当视权利要求书所界定者为准。
