一种可降解金属-有机物复合骨修复材料的制备方法
文献发布时间:2023-06-19 10:11:51
技术领域
本发明涉生物医学工程技术领域,具体涉及一种可降解金属-有机物复合骨修复材料的制备方法。
背景技术
交通事故、外伤、肿瘤切除手术、先天性骨骼疾病、骨性关节炎等极易导致致残致畸率极高的大段骨缺损,据统计,骨缺损发病率为5-7%,目前全世界约3亿多人患有由各种原因导致骨缺损的疾病。大段骨缺损再生能力差,如何有效修复这类骨缺损始终是医学界和材料学界尚待解决的难题之一。
外界干预治疗是一种必要且有效的手段,临床上骨缺损治疗方法主要是自体骨移植术和异体骨移植术。自体骨具有良好的成骨能力和极小的免疫排斥反应,是骨缺损修复的“金标准”,但存在供骨量少,多次手术,增加手术及感染风险,创伤大,供骨部位易引起并发症等不足。异体骨移植存在免疫排斥反应、潜在宿主组织感染及组织坏死等明显不足。随着再生医学及生物材料的发展,仿生设计一种可以替代修复骨缺损的新型功能材料为治疗骨缺损提供了可行的方案。理想的骨修复材料应具备以下性能:1、具有良好的生物相容性及安全性;2、应具备一定的力学强度,为具有一定承力部位的骨缺损提供力学支撑;3、具有较好的成骨活性,诱导骨再生;4、具有可降解性且降解速率可调控;5、具有一定的仿生微纳多孔结构为新骨及血管长入提供空间。
当前,大量的骨修复材料被广泛报道,种类繁多,旨在提供成骨活性、力学强度或两者协同增强。如陶瓷类骨修复材料,陶瓷/高分子骨修复材料、陶瓷/水凝胶复合骨修复材料等;高分子类骨修复材料,如高分子/生物活性玻璃复合材料、含镁高分子骨修复材料等;水凝胶类材料、微纳纤维支架、3D打印支架、多孔金属支架等,这些材料均在一定程度上表现出良好的骨修复效果,并表现出良好的应用前景。其中,以天然多糖为基材制备的水凝胶具有良好的生物安全性,生物相容性、可降解性、仿细胞外基质结构等特性,使这类材料在骨缺损修复中优势明显,因而被广泛用于骨修复材料研究并成为近年来研究热点。但单一天然多糖水凝胶力学强度不足,难以用于具有一定承力部位骨缺损修复。
可降解金属,如镁基合金及锌基合金是潜在的骨修复材料,是近年来研究的热点。镁和锌元素是人体必需元素,参与人体多种重要的代谢过程。镁合金及锌合金具有与人体皮质骨相匹配的弹性模量,可为骨缺损部位提供力学支撑并避免其他不可降解金属由于应力过大导致的应力遮挡效应。镁合金及锌合金在人体内可降解,降解过程中产生的镁离子或锌离子在适宜浓度下具有良好的成骨及成血管活性。虽有以上优势,但块体可降解金属难以直接用于骨缺损修复,因为块体金属占据大量空间,影响新生骨及血管长入,且大量块体金属降解后将造成局部大量腐蚀产物堆积影响骨缺损修复。因此,具备多孔结构或网状的可降解金属相比块体金属在骨缺损修复中将更具优势。然而,虽多孔结构利于组织和血管长入,但多孔可降解金属比表面积大,在降解过程中将进一步加速其降解,特别是多孔镁合金。如何有效地减缓多孔可降解金属的降解速率是这类多孔可降解金属实际应用过程中应解决的关键问题。
现有技术可制备多孔或网状可降解金属,但制备成多孔或网状后,由于比表面积增加(与腐蚀介质接触面积增加)将进一步加速其降解,因而如何有效调控多孔或网状金属的降解速率是其实际临床应用的关键,然而有效的调控多孔或网状金属的降解并为骨细胞及血管长入提供良好的微环境(如与仿细胞外基质水凝胶复合)的报道极少。
发明内容
本发明针对现有多孔或网状可降解金属存在的上述问题,提供一种先对可降解金属进行表面改性处理,再使改性后金属与水凝胶预聚液发生聚合反应,从而制备得到可降解金属-有机复合骨修复材料的方法。
为实现上述目的,本发明采用以下技术方案。
一种可降解金属-有机物复合骨修复材料的制备方法,包括以下步骤:
S1、将可降解金属置于表面处理液中浸泡24h后取出,用水冲洗干净并干燥,得到改性可降解金属;
所述表面处理液是用1.0-1.5mg/mL的Tris水溶液配制多酚类化合物含量为0.5-5.0mg/mL的溶液后,再向该溶液中加入胺类化合物形成的溶液,所述胺类化合物的含量为1.0-2.0mg/mL。
优选的,所述多酚类化合物选自儿茶酚胺、儿茶酚、单宁酸、没食子酸、花青素、原花青素中的一种。更优选的,所述多酚类化合物为多巴胺。
优选的,所述胺类化合物为2-氨基乙基甲基丙烯酸酯或乙二胺。
更优选的,所述表面处理液是用1.2mg/mL的Tris水溶液配制多巴胺含量为2.0mg/mL的溶液后,再向该溶液中加入2-氨基乙基甲基丙烯酸酯形成的溶液,所述2-氨基乙基甲基丙烯酸酯的含量为2.0mg/mL。
更优选的,所述表面处理液是用1.2mg/mL的Tris水溶液配制多巴胺含量为5.0mg/mL的溶液后,再向该溶液中加入乙二胺形成的溶液,所述乙二胺的含量为1.0mg/mL。
优选的,所述可降解金属为镁、镁合金、锌、锌合金、铁或铁合金。
更优选的,所述可降解金属为多孔或网状的可降解金属。
优选的,将可降解金属浸泡于表面处理液前,先对可降解金属进行清洁处理;所述清洁处理为:先将可降解金属置于丙酮中进行超声清洗,再将可降解金属置于无水乙醇中进行超声清洗,然后对可降解金属进行干燥处理。
优选的,所述干燥处理是用干燥的氮气流吹干可降解金属,然后将可降解金属置于真空干燥箱中待用。
S2、将水凝胶预聚液倒入装有改性可降解金属的容器中,并将容器置于真空箱中抽真空0.5h以上;
所述水凝胶预聚液是5-40mg/mL的丙烯酸双键及磷酸修饰的天然多糖的水溶液中含有1mg/mL的紫外光引发剂的溶液;或水凝胶预聚液是18-22mg/mL的甲基丙烯酸修饰的天然多糖的水溶液中含1mg/mL的紫外光引发剂的溶液。
优选的,所述的天然多糖是壳聚糖、透明质酸、明胶或海藻酸钠。
优选的,所述紫外光引发剂为2-羟基-4’-(2-羟乙氧基)-2-甲基苯丙酮。
S3、用紫外光照射经步骤2处理的水凝胶预聚液和改性可降解金属,得到可降解金属-有机物复合骨修复材料。
与现有技术相比,本发明的有益效果是:
本发明首先在可降解金属上构建抗腐蚀及含丙烯酸功能团的涂层,改性后的可降解金属复合水凝胶预聚液后在紫外光下引发丙烯酸双键聚合,形成可降解金属-有机复合骨修复材料。本发明的骨修复材料中的可降解金属可为骨修复材料提供力学支撑,使其满足骨缺损修复的要求;经改性处理的可降解金属其表面涂层可提供腐蚀保护功能及为后续与水凝胶预聚液复合提供聚合位点;而水凝胶可为骨细胞及血管细胞的长入提供良好的微环境,利于骨长入及血管生成;同时,可降解金属中填充的水凝胶可起到一定的物理阻隔作用,减缓腐蚀介质与可降解金属的接触,从而进一步减缓可降解金属的腐蚀速率;此外,可降解金属在降解过程中释放的金属离子可与水凝胶中的官能团(如磷酸基)螯合,可缓释金属离子,具有缓释效果。
本发明通过优化表面处理液的组成及组分含量,使可降解金属表面形成的涂层牢固且具有良好的抗腐蚀性能;通过优化水凝胶预聚液中丙烯酸双键及磷酸修饰的天然多糖的浓度,不仅使水凝胶预聚液容易进入网状/多孔可降解金属的孔隙中,充分填充孔隙,且可避免交联反应后形成孔洞疏松的水凝胶。
经测试,本发明的骨修复材料具备一定的力学强度,可为骨缺损部位提供力学支撑,网状或多孔可降解金属中填充的水凝胶具有三维仿生结构可为骨细胞及血管细胞生长提供良好的微环境,可降解金属表面的涂层及填充的水凝胶可调控可降解金属降解速率及成骨活性金属离子释放速率以满足材料降解与骨长入速率匹配及金属离子成骨活性的目的。
附图说明
图1为实施例4制备的可降解金属-有机复合骨修复材料的宏观形貌图;
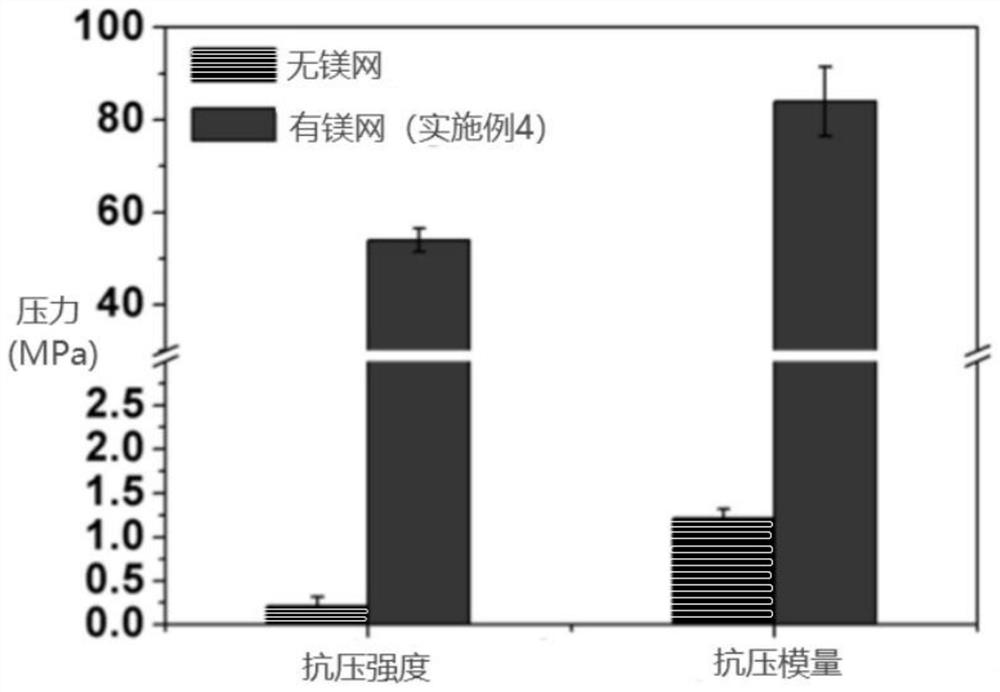
图2为实施例4制备的可降解金属-有机复合骨修复材料与不含镁网的水凝胶骨修复材料的抗压强度及抗压模量对比图。
具体实施方式
为了更充分的理解本发明的技术内容,下面结合具体实施例对本发明的技术方案作进一步介绍和说明。
磷酸修饰的甲基丙烯酸化天然多糖的制备方法如下:
(1)将天然多糖在溶剂中溶解后,加入甲基丙烯酸酐,室温下反应得到混合物A;
(2)取磷酸或膦酸改性原料溶解在去离子水中,依次加入MES,EDC及NHS,充分溶解后在室温下搅拌均匀得到混合物B;
(3)将混合物A加入到混合物B中,室温下反应,加入去离子水稀释,将稀释液置于透析袋中,室温下去离子水中透析,透析后冻干,得到磷酸修饰的甲基丙烯酸化天然多糖。
优选的,天然多糖为壳聚糖、透明质酸、海藻酸钠中的一种。
优选的,天然多糖、溶解天然多糖的溶剂和甲基丙烯酸酐的比例为1-5g:100mL:0-1mL。
更优选的,天然多糖、溶解天然多糖的溶剂和甲基丙烯酸酐的比例为1g:100mL:367μL。
优选的,当天然多糖为壳聚糖时,步骤(1)中,溶解壳聚糖的溶剂为乙酸水溶液,乙酸水溶液的体积分数为0.5-10%
优选的,当天然多糖为透明质酸或海藻酸钠时,溶解透明质酸或海藻酸钠的溶剂为去离子水,溶解后,加入氢氧化钠溶液将pH值调至7.3-8.5。
优选的,步骤(1)和步骤(2)中天然多糖和磷酸或膦酸改性原料的质量比为10:1-1:5。
更优选的,步骤(1)和步骤(2)中天然多糖和磷酸或膦酸改性原料的质量比为2:1。
优选的,步骤(2)中,磷酸或膦酸改性原料为3-膦酸基丙酸、磷酸肌酸、阿伦磷酸或磷酸乙醇胺中的一种;磷酸或膦酸改性原料、MES、EDC和NHS的质量比为0.1-10:50-80:3-9:1-3。
更优选的,磷酸或膦酸改性原料、MES、EDC和NHS的质量比为5:53.3:9:3。
优选的,步骤(3)中,使用过分子量为12-14kDa的透析袋透析。
以磷酸修饰甲基丙烯酸化壳聚糖为例,磷酸修饰甲基丙烯酸化壳聚糖的制备,包括以下步骤:
(1)将1g壳聚糖溶解在100mL体积分数为1%的乙酸水溶液中,溶解后逐滴加入367μL甲基丙烯酸酐(MA),室温下反应24h,得到甲基丙烯酸化壳聚糖(CSMA)。
(2)取0.5g3-膦酸基丙酸溶解在50mL去离子水中,加入5.33g2-(N-吗啉)乙磺酸一水合物(MESmonohydrate),加入0.9gEDC(1-Ethyl-3-(3'-dimethylaminopropyl)carbodiimide)及0.3gNHS(N-hydroxysuccinimide),充分溶解后在室温下搅拌30min。
(3)将步骤(1)中壳聚糖与甲基丙烯酸反应后的液体逐滴滴加到步骤(2)的3-膦酸基丙酸溶液中,一边滴加一边搅拌,全部滴加后在室温下反应24h后,加入100mL去离子水稀释,将稀释液置于12-14kDa透析袋中,在室温下去离子水中透析5天,每天早晚各换一次去离子水,并持续搅拌,透析后冻干,得到白色松散状磷酸修饰甲基丙烯酸化壳聚糖(CSMAP)。
上述的MES为2-(N-吗啉)乙磺酸一水物,EDC为1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐,NHS为N-羟基琥珀酰亚胺。
实施例1
本实施例提供一种可降解金属-有机复合骨修复材料的制备方法。本实施例中使用的可降解金属是网状的AZ31镁合金,中空网格为正方形形状,正方形边长为1.5mm,网格金属筋的宽度为0.25mm,镁网厚度为0.25mm。
具体步骤如下:
(1)将可降解金属在丙酮中超声清洗3次,每次5min,随后在无水乙醇中超声清洗3次,每次5min,取出后在干燥的氮气流下吹干,置于真空干燥箱中保存,待用。
(2)在敞口烧杯中用1.2mg/mL的Tris水溶液配制2mg/mL的多巴胺溶液,然后向该溶液中加入2mg/mL的2-氨基乙基甲基丙烯酸酯,在室温下敞口搅拌半小时,得到含多巴胺和2-氨基乙基甲基丙烯酸酯的混合溶液,即表面处理液。
(3)将步骤(1)中清洗干净的可降解金属浸泡在步骤(2)配制的表面处理液中,烧杯敞口室温下浸泡24h后,将可降解金属取出,并用去离子水冲洗干净,之后在干燥的氮气流下吹干,得到改性可降解金属。将改性可降解金属置于真空干燥箱中保存,待用。
(4)将磷酸修饰甲基丙烯酸化壳聚糖以20mg/mL的浓度溶解在去离子水中,溶解后在该溶液中加入1mg/mL的紫外光引发剂2-羟基-4’-(2-羟乙氧基)-2-甲基苯丙酮,得到水凝胶预聚液。
(5)取步骤(3)中得到的改性可降解金属置于烧杯中,将步骤(4)中得到的水凝胶预聚液倒入烧杯中以完全覆盖可降解金属,随后将烧杯置于真空箱中抽真空半小时。
(6)将步骤(5)的烧杯置于紫外光(波长为400nm-10nm)下,照射20min后得到网状的可降解金属-有机复合骨修复材料。
由本实施例步骤(3)制备得到的改性可降解金属的自腐蚀电流密度为26.8μA/cm
在其他实施方案中,还可以使用纯镁,以及AZ91、WE43等生物医用镁合金;并且还可以使用孔连通率在80%以上且孔径大小有利于水凝胶预聚液流入并使水凝胶预聚液在多孔结构中连通的多孔可降解金属。
实施例2
本实施例提供一种可降解金属-有机复合骨修复材料的制备方法。本实施例中使用的可降解金属与实施例1的相同,是网状的AZ31镁合金,中空网格为正方形形状,正方形边长为1.5mm,网格金属筋的宽度为0.25mm,镁网厚度为0.25mm。
具体步骤如下:
(1)将可降解金属在丙酮中超声清洗3次,每次5min,随后在无水乙醇中超声清洗3次,每次5min,取出后在干燥氮气流下吹干,置于真空干燥箱中待用。
(2)在敞口烧杯中用1.2mg/mL的Tris水溶液配制5mg/mL的多巴胺溶液,然后向该溶液中加入1mg/mL的2-氨基乙基甲基丙烯酸酯,在室温下敞口搅拌半小时,得到含多巴胺和2-氨基乙基甲基丙烯酸酯的混合溶液,即表面处理液。
(3)将步骤(1)中清洗干净的可降解金属浸泡在步骤(2)的混合溶液中,烧杯敞口室温下浸泡24h后,将可降解金属取出,并用去离子水轻轻冲洗,之后在干燥的氮气流下吹干,得到改性可降解金属。将改性可降解金属置于真空干燥箱中保存,待用。
(4)将磷酸修饰甲基丙烯酸化壳聚糖以20mg/mL的浓度溶解在去离子水中,溶解后在该溶液中加入1mg/mL的紫外光引发剂2-羟基-4’-(2-羟乙氧基)-2-甲基苯丙酮,得到水凝胶预聚液。
(5)取步骤(3)中得到的改性可降解金属置于烧杯中,将步骤(4)中得到的水凝胶预聚液倒入烧杯中以完全覆盖改性可降解金属,随后将烧杯置于真空箱中抽真空半小时。
(6)将步骤(5)的烧杯置于紫外光(波长为400nm-10nm)下,照射20min后得到网状的可降解金属-有机复合骨修复材料。
由本实施例步骤(3)制备得到的改性可降解金属的自腐蚀电流密度为28.2μA/cm
实施例3
本实施例提供一种可降解金属-有机复合骨修复材料的制备方法。本实施例中使用的可降解金属与实施例1的相同,是网状的AZ31镁合金,中空网格为正方形形状,正方形边长为1.5mm,网格金属筋的宽度为0.25mm,镁网厚度为0.25mm。
具体步骤如下:
(1)将可降解金属在丙酮中超声清洗3次,每次5min,随后在无水乙醇中超声清洗3次,每次5min,取出后在干燥氮气流下吹干,置于真空干燥箱中待用。
(2)在敞口烧杯中用1.2mg/mL的Tris水溶液配制5mg/mL的多巴胺溶液,然后向该溶液中加入1mg/mL的乙二胺,在室温下敞口搅拌半小时,得到含多巴胺和乙二胺的混合溶液,即表面处理液。
(3)将步骤(1)中清洗干净的可降解金属浸泡在步骤(2)的混合溶液中,烧杯敞口室温下浸泡24h后,将可降解金属取出,并用去离子水轻轻冲洗,之后在干燥的氮气流下吹干,得到改性可降解金属。将改性可降解金属置于真空干燥箱中保存,待用。
(4)将磷酸修饰甲基丙烯酸化壳聚糖以20mg/mL的浓度溶解在去离子水中,溶解后在该溶液中加入1mg/mL的紫外光引发剂2-羟基-4’-(2-羟乙氧基)-2-甲基苯丙酮,得到水凝胶预聚液。
(5)取步骤(3)中得到的改性可降解金属置于烧杯中,将步骤(4)中得到的水凝胶预聚液倒入烧杯中以完全覆盖改性可降解金属,随后将烧杯置于真空箱中抽真空半小时。
(6)将步骤(5)的烧杯置于紫外光(波长为400nm-10nm)下,照射20min后得到网状的可降解金属-有机复合骨修复材料。
由本实施例步骤(3)制备得到的改性可降解金属的自腐蚀电流密度为29.1μA/cm
实施例4
本实施例提供一种可降解金属-有机复合骨修复材料的制备方法。本实施例中使用的可降解金属与实施例1的相同,是网状的AZ31镁合金,中空网格为正方形形状,正方形边长为1.5mm,网格金属筋的宽度为0.25mm,镁网厚度为0.25mm。
具体步骤如下:
(1)将可降解金属在丙酮中超声清洗3次,每次5min,随后在无水乙醇中超声清洗3次,每次5min,取出后在干燥氮气流下吹干,置于真空干燥箱中待用。
(2)在敞口烧杯中用1.2mg/mL的Tris水溶液配制5mg/mL的多巴胺溶液,然后向该溶液中加入1mg/mL的乙二胺,在室温下敞口搅拌半小时,得到含多巴胺和乙二胺的混合溶液,即表面处理液。
(3)将步骤(1)中清洗干净的可降解金属浸泡在步骤(2)的混合溶液中,烧杯敞口室温下浸泡24h后,将可降解金属取出,并用去离子水轻轻冲洗,之后在干燥的氮气流下吹干,得到改性可降解金属。将改性可降解金属置于真空干燥箱中保存,待用。
(4)将甲基丙烯酸化壳聚糖以20mg/mL的浓度溶解在去离子水中,溶解后在该溶液中加入1mg/mL的紫外光引发剂2-羟基-4’-(2-羟乙氧基)-2-甲基苯丙酮,得到水凝胶预聚液。
(5)取步骤(3)中得到的改性可降解金属置于烧杯中,将步骤(4)中得到的水凝胶预聚液倒入烧杯中以完全覆盖改性可降解金属,随后将烧杯置于真空箱中抽真空半小时。
(6)将步骤(5)的烧杯置于紫外光(波长为400nm-10nm)下,照射20min后得到网状的可降解金属-有机复合骨修复材料。
由本实施例步骤(3)制备得到的改性可降解金属的自腐蚀电流密度为27.0μA/cm
实施例5
本实施例提供一种可降解金属-有机复合骨修复材料的制备方法。本实施例中使用的可降解金属与实施例1的相同,且本实施例的制备方法与实施例1的制备方法基本相同,不同之处在于使用的表面处理液的组分浓度不同,即步骤(2)制备表面处理液的方法如下:
在敞口烧杯中用1.2mg/mL的Tris水溶液配制6mg/mL的多巴胺溶液,然后向该溶液中加入2mg/mL的2-氨基乙基甲基丙烯酸酯,在室温下敞口搅拌半小时,得到含多巴胺和2-氨基乙基甲基丙烯酸酯的混合溶液,即表面处理液。
由本实施例步骤(3)制备得到的改性可降解金属的自腐蚀电流密度为45.5μA/cm
实施例6
本实施例提供一种可降解金属-有机复合骨修复材料的制备方法。本实施例中使用的可降解金属与实施例1的相同,且本实施例的制备方法与实施例1的制备方法基本相同,不同之处在于使用的表面处理液的组分浓度不同,即步骤(2)制备表面处理液的方法如下:
在敞口烧杯中用1.2mg/mL的Tris水溶液配制0.3mg/mL的多巴胺溶液,然后向该溶液中加入2mg/mL的2-氨基乙基甲基丙烯酸酯,在室温下敞口搅拌半小时,得到含多巴胺和2-氨基乙基甲基丙烯酸酯的混合溶液,即表面处理液。
由本实施例步骤(3)制备得到的改性可降解金属的自腐蚀电流密度为102.2μA/cm
实施例7
本实施例提供一种可降解金属-有机复合骨修复材料的制备方法。本实施例中使用的可降解金属与实施例4的相同,且本实施例的制备方法与实施例4的制备方法基本相同,不同之处在于使用的表面处理液的组分浓度不同,即步骤(2)制备表面处理液的方法如下:
在敞口烧杯中用1.2mg/mL的Tris水溶液配制6mg/mL的多巴胺溶液,然后向该溶液中加入1mg/mL的乙二胺,在室温下敞口搅拌半小时,得到含多巴胺和乙二胺的混合溶液,即表面处理液。
由本实施例步骤(3)制备得到的改性可降解金属的自腐蚀电流密度为80.5μA/cm
实施例8
本实施例提供一种可降解金属-有机复合骨修复材料的制备方法。本实施例中使用的可降解金属与实施例4的相同,且本实施例的制备方法与实施例4的制备方法基本相同,不同之处在于使用的表面处理液的组分浓度不同,即步骤(2)制备表面处理液的方法如下:
在敞口烧杯中用1.2mg/mL的Tris水溶液配制0.3mg/mL的多巴胺溶液,然后向该溶液中加入1mg/mL的乙二胺,在室温下敞口搅拌半小时,得到含多巴胺和乙二胺的混合溶液,即表面处理液。
由本实施例步骤(3)制备得到的改性可降解金属的自腐蚀电流密度为75.5μA/cm
实施例9
本实施例提供一种可降解金属-有机复合骨修复材料的制备方法。本实施例中使用的可降解金属与实施例1的相同,且本实施例的制备方法与实施例1的制备方法基本相同,不同之处在于使用的水凝胶预聚液的组分浓度不同,即步骤(4)制备水凝胶预聚液的方法如下:
使用与实施例1相同的磷酸修饰甲基丙烯酸化壳聚糖,将磷酸修饰甲基丙烯酸化壳聚糖以3mg/mL的浓度溶解在去离子水中,溶解后在该溶液中加入1mg/mL的紫外光引发剂2-羟基-4’-(2-羟乙氧基)-2-甲基苯丙酮,得到水凝胶预聚液。
本实施例制备的可降解金属-有机复合骨修复材料,由于水凝胶预聚液的浓度太小,其粘度太小,水凝胶不能成型。
实施例10
本实施例提供一种可降解金属-有机复合骨修复材料的制备方法。本实施例中使用的可降解金属与实施例1的相同,且本实施例的制备方法与实施例1的制备方法基本相同,不同之处在于使用的水凝胶预聚液的组分浓度不同,即步骤(4)制备水凝胶预聚液的方法如下:
使用与实施例1相同的磷酸修饰甲基丙烯酸化壳聚糖,将磷酸修饰甲基丙烯酸化壳聚糖以5mg/mL的浓度溶解在去离子水中,溶解后在该溶液中加入1mg/mL的紫外光引发剂2-羟基-4’-(2-羟乙氧基)-2-甲基苯丙酮,得到水凝胶预聚液。
本实施例制备的可降解金属-有机复合骨修复材料,水凝胶可充分地进入改性可降解金属的孔洞内部,填充效果佳,水凝胶中未出现疏松的孔洞。
实施例11
本实施例提供一种可降解金属-有机复合骨修复材料的制备方法。本实施例中使用的可降解金属与实施例1的相同,且本实施例的制备方法与实施例1的制备方法基本相同,不同之处在于使用的水凝胶预聚液的组分浓度不同,即步骤(4)制备水凝胶预聚液的方法如下:
使用与实施例1相同的磷酸修饰甲基丙烯酸化壳聚糖,将磷酸修饰甲基丙烯酸化壳聚糖以40mg/mL的浓度溶解在去离子水中,溶解后在该溶液中加入1mg/mL的紫外光引发剂2-羟基-4’-(2-羟乙氧基)-2-甲基苯丙酮,得到水凝胶预聚液。
本实施例制备的可降解金属-有机复合骨修复材料,水凝胶可充分地进入改性可降解金属的孔洞内部,填充效果佳,水凝胶中未出现疏松的孔洞。
实施例12
本实施例提供一种可降解金属-有机复合骨修复材料的制备方法。本实施例中使用的可降解金属与实施例1的相同,且本实施例的制备方法与实施例1的制备方法基本相同,不同之处在于使用的水凝胶预聚液的组分浓度不同,即步骤(4)制备水凝胶预聚液的方法如下:
使用与实施例1相同的磷酸修饰甲基丙烯酸化壳聚糖,将磷酸修饰甲基丙烯酸化壳聚糖以45mg/mL的浓度溶解在去离子水中,溶解后在该溶液中加入1mg/mL的紫外光引发剂2-羟基-4’-(2-羟乙氧基)-2-甲基苯丙酮,得到水凝胶预聚液。
本实施例制备的可降解金属-有机复合骨修复材料,由于水凝胶预聚液的浓度太大,其粘度太大,水凝胶预聚液难以进入改性可降解金属的孔洞内部,难以充分填充,复合材料的均匀性差。
实施例13
本实施例提供一种可降解金属-有机复合骨修复材料的制备方法。本实施例中使用的可降解金属与实施例4的相同,且本实施例的制备方法与实施例1的制备方法基本相同,不同之处在于使用的水凝胶预聚液的组分浓度不同,即步骤(4)制备水凝胶预聚液的方法如下:
将甲基丙烯酸化壳聚糖以3mg/mL的浓度溶解在去离子水中,溶解后在该溶液中加入2mg/mL的多巴胺Tris水溶液及1mg/mL的紫外光引发剂2-羟基-4’-(2-羟乙氧基)-2-甲基苯丙酮,得到水凝胶预聚液。(多巴胺Tris水溶液与实施例4的相同。)
本实施例制备的可降解金属-有机复合骨修复材料,由于水凝胶预聚液的浓度太小,其粘度太小,水凝胶不能成型。
实施例14
本实施例提供一种可降解金属-有机复合骨修复材料的制备方法。本实施例中使用的可降解金属与实施例4的相同,且本实施例的制备方法与实施例1的制备方法基本相同,不同之处在于使用的水凝胶预聚液的组分浓度不同,即步骤(4)制备水凝胶预聚液的方法如下:
将甲基丙烯酸化壳聚糖以45mg/mL的浓度溶解在去离子水中,溶解后在该溶液中加入2mg/mL的多巴胺Tris水溶液及1mg/mL的紫外光引发剂2-羟基-4’-(2-羟乙氧基)-2-甲基苯丙酮,得到水凝胶预聚液。(多巴胺Tris水溶液与实施例4的相同。)
本实施例制备的可降解金属-有机复合骨修复材料,由于水凝胶预聚液的浓度太大,其粘度太大,水凝胶预聚液难以进入改性可降解金属的孔洞内部,难以充分填充,复合材料的均匀性差。
实施例15
本实施例提供一种可降解金属-有机复合骨修复材料的制备方法。本实施例中使用的可降解金属是网状的锌金属,中空网格为正方形形状,正方形边长为1.5mm,网格金属筋的宽度为0.25mm,锌网厚度为0.25mm。
本实施例的制备方法,除所用可降解金属与实施例4的不同外,其余与实施例4的相同。由本实施例步骤(3)制备得到的改性可降解金属的自腐蚀电流密度为12.4μA/cm
实施例16
本实施例提供一种可降解金属-有机复合骨修复材料的制备方法。本实施例中使用的可降解金属是网状的铁合金,中空网格为正方形形状,正方形边长为1.5mm,网格金属筋的宽度为0.25mm,铁网厚度为0.25mm。
本实施例的制备方法,除所用可降解金属与实施例4的不同外,其余与实施例4的相同。由本实施例步骤(3)制备得到的改性可降解金属的自腐蚀电流密度为5.3μA/cm
在其他实施方案中,使用的表面处理液中的多巴胺还可以用儿茶酚、单宁酸、没食子酸、花青素、原花青素等代替;水凝胶预聚液中的磷酸修饰甲基丙烯酸化壳聚糖或甲基丙烯酸化壳聚糖,其中的壳聚糖还可以用透明质酸、明胶或海藻酸钠等替代,如磷酸修饰甲基丙烯酸化壳聚糖可用磷酸修饰甲基丙烯酸化明胶、磷酸修饰甲基丙烯酸化透明质酸、磷酸修饰甲基丙烯酸化海藻酸钠等替代。
以上所述仅以实施例来进一步说明本发明的技术内容,以便于读者更容易理解,但不代表本发明的实施方式仅限于此,任何依本发明所做的技术延伸或再创造,均受本发明的保护。
- 一种可降解金属-有机物复合骨修复材料的制备方法
- 一种可降解金属丝定向增强聚乳酸多孔骨修复材料及其制备方法
