胰高血糖素类似物及其医药用途
文献发布时间:2024-04-18 19:58:30
本申请要求2021年06月18日提交的申请号为202110676681.3的中国专利申请的优先权。
本公开涉及胰高血糖素类似物及其医药用途。本公开的胰高血糖素类似物可用于治疗低血糖、肥胖症、糖尿病等代谢性疾病或缓解病症。
控制体内血糖的平衡对机体代谢极其重要。正常情况下,人体血糖水平在多种不同多肽类激素(以胰岛素和胰高血糖素为主)调节下保持动态平衡。血糖失衡可能导致并发症。当血糖浓度低于正常水平,就会出现低血糖(Hypoglycemia)现象。胰岛中胰腺产生胰高血糖素,使血糖水平增加到正常范围。非严重的低血糖通常产生自主性的或神经性的低血糖症状,患者能够识别低血糖的发病,因此无需他人辅助治疗。而当血液中葡萄糖浓度因其它药物、或疾病、或者激素或酶的缺陷而下降(如治疗糖尿病、肾功能衰竭、特定肿瘤、肝疾病、甲状腺机能低下症、遗传性代谢缺陷、败血症与反应性低血糖所引起的一系列临床的严重低血糖症状),体内的胰高血糖素就不足以使血糖恢复,甚至可危及到生命,通常表现为认知或身体功能受损,自我治疗能力受限,所以需要他人的帮助治疗才能恢复正常血糖。
目前,在低血糖防治中,完全清醒的低血糖患者的治疗方法首选口服糖类食物;对于意识障碍者,需要在非医护人员或医护人员的帮助下接受静脉注射50%葡萄糖液或肌肉注射0.5至2mg胰高血糖素的治疗。非医护人员较难开展50%葡萄糖液的静脉注射。注射剂量过高则会引起反弹性高血糖,如果葡萄糖液渗漏出血管,会造成局部组织损伤。因此,在非医院环境下,意识障碍的严重低血糖患者的最佳治疗策略是通过皮下或肌肉注射胰高血糖素。胰高血糖素作为严重低血糖的急救药物也已应用于临床;并且基于胰高血糖素的降脂及促进能量消耗作用,其与肠促胰素的双重受体激动剂也使肥胖的糖尿病患者进一步获益。
胰高血糖素为由胰腺α-细胞分泌的29个氨基酸组成的直链多肽,控制肝脏生产葡萄糖和酮体。胰高血糖素在夜间及两餐之间分泌,通过增加源自氨基酸前体的葡萄糖生成(糖异生)和促进糖原降解成葡萄糖(糖酵解),导致肝脏的葡萄糖外流增加,从而提高血糖浓度。胰高血糖素与胰腺β细胞分泌的胰岛素共同精确控制体内血糖的平衡。胰高血糖素除了有低血糖的治疗效果,还抑制食欲、 并活化脂肪细胞的激素敏感性脂肪酶以促进脂肪分解,从而显示出抗肥胖效果。
胰高血糖素是抵抗低血糖防御机制的重要组成部分,低剂量的胰高血糖素可防止胰岛素诱导性的低血糖,并改善从低血糖恢复的能力。低剂量的胰高血糖素还可引起饱腹感抑制食欲,同时可活化脂肪细胞的激素敏感性脂肪酶,促进脂肪分解,从而有潜在的抗肥胖效果,可用于治疗许多患有II型糖尿病患者的体重超重或者肥胖。
然而,天然胰高血糖素在中性pH的水相溶液中溶解度极低。此外,胰高血糖素含有可产生氨基酸残基侧链脱酰氨基化、氧化、环状亚胺中间物形成的氨基酸或氨基酸序列,以及含有可发生异构化、肽链切割等的氨基酸或氨基酸序列,无法保持长时间稳定,并且在几小时至几天内就会形成凝胶或者原纤维(fibril),化学及物理稳定性极差。因此,需要开发溶解度优异,物理/化学稳定性良好的新型胰高血糖素类似物以满足注射制剂开发的要求。
第一代胰高血糖素注射制剂,如胰高血糖素应急试剂盒(
第二代胰高血糖素注射制剂,如人胰高血糖素鼻喷粉末(
本领域仍然亟需高活性、溶解度优异、物理/化学稳定性良好的胰高血糖素类似物。本公开提供了一类高活性(相比天然胰高血糖素,活性提高)、水性溶液中溶解度高(尤其在生理pH下)和稳定性(包含物理稳定性和化学稳定性)改善的胰高血糖素类似物。与本领域内的胰高血糖素类似物相比,本公开的胰高血糖素类似物具有更强的体外胰高血糖素受体激动剂活性,对降低皮下给药的体积和次数、提高低血糖患者的使用便利性、减轻患者经济负担都有很大帮助。本公开的胰高血糖素类似物可单独或与其它治疗性药物联合用于治疗低血糖、肥胖症、糖尿病等代谢性疾病或病症方法中。
发明内容
本公开提供胰高血糖素类似物或其可药用盐和/或溶剂化物,包含其的药物组合物,编码所述胰高血糖素类似物的多核苷酸、含有所述多核苷酸的载体、含有所述多核苷酸或载体的宿主细胞。以及,所述胰高血糖素类似物或其可药用盐和/或溶剂化物或包含其的药物组合物用于治疗疾病、缓解病症(例如低血糖、肥胖症、糖尿病等代谢性疾病或病症)的方法和相关制药用途。
胰高血糖素类似物或其可药用盐和/或溶剂化物
本公开提供了如式(I)所示结构的胰高血糖素类似物或其可药用盐和/或溶剂化物:
R
(I)
本公开还提供了包含式(I)所示结构的胰高血糖素类似物或其可药用盐和/或溶剂化物,其中,R
其中:
R
R
X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,R
本公开的可药用盐和/或溶剂化物选自:无机盐或有机盐。
本公开的胰高血糖素类似物可与酸性化合物或碱性化合物反应而生成相应的盐。
“与酸性化合物反应而生成相应的盐”是指能够保留游离碱的生物有效性而无其它副作用的,与无机酸或有机酸所形成的盐。无机酸盐包括但不限于:盐酸盐、氢溴酸盐、硫酸盐、硝酸盐、磷酸盐等;有机酸盐包括但不限于:甲酸盐、乙酸盐、2,2-二氯乙酸盐、三氟乙酸盐、丙酸盐、己酸盐、辛酸盐、癸酸盐、十一碳烯酸盐、乙醇酸盐、葡糖酸盐、乳酸盐、癸二酸盐、己二酸盐、戊二酸盐、丙二酸盐、草酸盐、马来酸盐、琥珀酸盐、富马酸盐、酒石酸盐、柠檬酸盐、棕榈酸盐、硬脂酸盐、油酸盐、肉桂酸盐、月桂酸盐、苹果酸盐、谷氨酸盐、焦谷氨酸盐、天冬氨酸盐、苯甲酸盐、甲磺酸盐、苯磺酸盐、对甲苯磺酸盐、海藻酸盐、抗坏血酸盐、水杨酸盐、4-氨基水杨酸盐、萘二磺酸盐等。可通过本领域已知的方法制备这些盐。
“与碱性化合物反应而生成相应的盐”是指能够保持游离酸的生物有效性而无其它副作用的、与无机碱或有机碱所形成的盐。衍生自无机碱的盐包括但不限于:钠盐、钾盐、锂盐、铵盐、钙盐、镁盐、铁盐、锌盐、铜盐、锰盐、铝盐等。衍生自有机碱的盐包括但不限于:伯胺、仲胺、叔胺、取代的胺、环状胺;例如氨、异丙胺、三甲胺、二乙胺、三乙胺、三丙胺、乙醇胺、乙二胺、二乙醇胺、三乙醇胺、二甲基乙醇胺、2-二甲氨基乙醇、2-二乙氨基乙醇、二环己胺、赖氨酸、精氨酸、组氨酸、咖啡因、普鲁卡因、胆碱、甜菜碱、葡萄糖胺、甲基葡萄糖胺、可可碱、嘌呤、哌嗪、哌啶、N-乙基哌啶、聚胺树脂等。优选的有机碱包括异丙胺、二乙胺、乙醇胺、三甲胺、二环己基胺、胆碱及咖啡因。可通过本领域已知的方法制备这些盐。
术语“溶剂化物”表示本公开的胰高血糖素类似物或其可药用盐与适宜的溶剂形成的复合物。溶剂的非限制性实例包括:水、乙醇、乙腈、异丙醇、DMSO、乙酸乙酯。在具体的实施方案中,所述溶剂化物为水合物。
在一些实施方案中,本公开提供胰高血糖素类似物或其可药用盐和/或溶剂化物,所述胰高血糖素类似物是选自SEQ ID NO:1-49中任一所示的化合物。
在一些具体的实施方案中,本公开提供胰高血糖素类似物或其可药用盐和/或溶剂化物,所述胰高血糖素类似物是选自以下的化合物:
H-HSQGTFTSDYSKYLDTAibRAQEFVQWLEST-OH(SEQ ID NO:39);
H-HSQGTFTSDYSKYLDLAibRAQEFVQWLEST-OH(SEQ ID NO:40);
H-HSQGTFTSDYSKYLDVAibRAQEFVQWLEST-OH(SEQ ID NO:41);
H-HSQGTFTSDYSKYLDIAibRAQEFVQWLEST-OH(SEQ ID NO:42);
H-HSHGTFTSDYSKYLDLAibRAQEFVQWLEST-OH(SEQ ID NO:43);
H-HSHGTFTSDYSKYLDLAibRAQEFVEWLEST-OH(SEQ ID NO:47)。
在本公开的每一个胰高血糖素类似物的序列中,C端“-OH”部分(moiety)可以替换成C端的“-NH
在一些具体的实施方案中,本公开提供胰高血糖素类似物或其可药用盐和/或溶剂化物,所述胰高血糖素类似物包含选自SEQ ID NO:39、40、41、42、43、47任一的结构,其中,所述SEQ ID NO:39、40、41、42、43、47的N端的H和/或C端的OH是不存在的。
本公开提供了如式(I)所示结构的胰高血糖素类似物或其可药用盐和/或溶剂化物:
R
(I)
本公开还提供了包含式(I)所示结构的胰高血糖素类似物或其可药用盐和/或溶剂化物,其中,R
其中:
R
R
X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,R
本公开提供了一种胰高血糖素类似物或其可药用盐和/或溶剂化物,所述胰高血糖素类似物包含如式(I)所示的结构:
R
(I)
本公开还提供了包含式(I)所示结构的胰高血糖素类似物或其可药用盐和/或溶剂化物,其中,R
其中:
R
R
X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,R
本公开提供式(I)所示结构的胰高血糖素类似物或其可药用盐和/或溶剂化物:
R
(I)
本公开还提供了包含式(I)所示结构的胰高血糖素类似物或其可药用盐和/或溶剂化物,其中,R
其中:
R
R
X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,X
在一些实施方案中,R
本公开的胰高血糖素类似物或其可药用盐和/或溶剂化物具有胰高血糖素受 体(GCGR)激动剂活性,其与GCGR的结合可用作激动剂活性的指示。在一些可选实施方案中,也可测量由化合物与受体结合时引起的细胞内信号转导。例如,胰高血糖素受体激动剂对GCGR的活化,将刺激细胞环磷酸腺苷(cAMP)的形成。因此,可使用合适的表达受体的细胞中cAMP的产生来监测受体活性。例如,可使用实施例2中给出的材料(例如CHO-K1/GCGR/CRE-Luc稳转细胞株和Cisbio-cAMP-Gs Dynamic kit)并且在所述条件下进行测定。可使用EC
在一些实施方案中,胰高血糖素受体是哺乳动物的胰高血糖素受体,例如人胰高血糖素受体。
在一些实施方案中,本公开的胰高血糖素类似物或其可药用盐和/或溶剂化物对人GCGR的激动剂活性是天然胰高血糖素的至少1.5倍、至少1.6倍、至少1.7倍、至少1.8倍、至少1.9倍、至少2.0倍、至少2.1倍、至少2.2倍、至少2.3倍、至少2.4倍、至少2.5倍、至少2.6倍、至少2.7倍、至少2.8倍、至少2.9倍、至少3.0倍、或至少3.1倍。
在一些实施方案中,本公开的胰高血糖素类似物或其可药用盐和/或溶剂化物对人GLP-1R和/或GIPR无激动剂活性或可以忽略不计。
在一些实施方案中,与天然胰高血糖素相比,本公开的胰高血糖素类似物或其可药用盐和/或溶剂化物具有提高的溶解度和/或稳定性。
在一些实施方案中,提高的溶解度可以包括或者是指:在pH 4(例如,在pH 4的醋酸盐缓冲液中)、pH 5(例如,在pH 5的醋酸盐缓冲液中)、pH 6(例如,在pH 6的磷酸盐缓冲液中)、pH 7(例如,在pH7的磷酸盐缓冲液中)和/或pH 7.5(例如,在pH 7.5的磷酸盐缓冲液中)下,与天然胰高血糖素相比,具有提高的溶解度。作为一个示例,可以在实施例5中给出的条件下进行测定。可以期望溶解度≥1mg/mL。
在一些实施方案中,例如通过测量在280nm的吸光度,并依据比尔定律计算的,本公开的胰高血糖素类似物在pH7.4的磷酸盐缓冲液中的溶解度为≥1.00mg/mL、≥1.10mg/mL、≥1.20mg/mL、≥1.30mg/mL、≥1.40mg/mL、≥1.50mg/mL、≥1.60mg/mL、≥1.70mg/mL、≥1.80mg/mL、≥1.90mg/mL、≥2.00mg/mL、≥2.10mg/mL、≥2.20mg/mL、≥2.30mg/mL、≥2.40mg/mL、≥2.50mg/mL、≥2.60mg/mL、≥2.70mg/mL、≥2.80mg/mL、≥2.90mg/mL、≥3.00mg/mL、≥3.10mg/mL、≥3.20mg/mL、≥3.30mg/mL、≥3.40mg/mL、≥3.50mg/mL、≥3.60mg/mL、≥3.70mg/mL、≥3.80mg/mL、≥3.90mg/mL、≥4.00mg/mL、≥4.10mg/mL、≥4.20mg/mL、≥4.30mg/mL、≥4.40mg/mL、≥4.50mg/mL、≥4.60mg/mL、≥4.70mg/mL、≥4.80mg/mL、≥4.90mg/mL、或≥5.00mg/mL。
在一些实施方案中,提高的稳定性可以包括或者是指:与天然人胰高血糖素相比提高的物理稳定性和/或提高的化学稳定性。
在一些实施方案中,提高的物理稳定性可以包括或者是指:聚集(例如形成可溶性或不溶性聚集体(例如,原纤维))的趋势降低。可以以0.1N HCl溶解胰高血糖素类似物,以1mg/mL的浓度37℃下测定聚集(例如,原纤维形成)。可使用任何合适的时间段,例如,24小时、48小时、96小时或120小时。可以适用ThT荧光测试测定聚集。可以在实施例4给出的条件下测定聚集。
在一些实施方案中,提高的化学稳定性可以包括或者是指:在水性缓冲液(通常不存在污染性蛋白酶或肽酶活性)中肽被切割或降解的趋势降低。可以以例如pH 7.4的磷酸盐缓冲液,溶解胰高血糖素类似物,以1mg/mL的浓度4℃、25℃或40℃下测定稳定性。评估可包括在孵育合适的时间段例如1天、7天、14天、21天、或28天后测定稳定性。这可包括按照实施例4中所限定,来测定化合物纯度,即各色谱图中主峰相对于所有整合峰的总面积的面积百分比。可以在实施例4给出的条件下测定稳定性。
多核苷酸
本公开提供编码本公开胰高血糖素类似物前体肽的多核苷酸,可以为RNA、DNA或cDNA。根据本公开的一些实施方案,本公开的多核苷酸是基本上分离的多核苷酸。
所述前体肽是经修饰后能够获得本公开胰高血糖素类似物的肽。例如,前体肽的X
本公开的多核苷酸也可呈载体形式,可存在于载体中和/或可为载体的一部分,该载体例如质粒、粘端质粒、YAC或病毒载体。载体可尤其为表达载体,即可提供胰高血糖素类似物在体外和/或体内(即在适合宿主细胞、宿主有机体和/或表达系统中)表达的载体。该表达载体通常包含至少一种本公开的多核苷酸,其可操作地连接至一个或多个适合的表达调控元件(例如启动子、增强子、终止子等)。针对在特定宿主中的表达,对所述元件及其序列进行选择为本领域技术人员的常识。
在一些实施方案中,载体包含5’→3’方向上的且可操作地连接的以下元件(element):用于驱动核酸片段表达的启动子,编码使得能够进行分泌(分泌至胞外相或适当时分泌到周质(periplasma)中)的前导肽的任选的多核苷酸,编码前体肽的多核苷酸,以及编码终止子的任选的多核苷酸。
本公开的多核苷酸可基于本公开胰高血糖素类似物前体肽的氨基酸序列的信息通过已知的方式(例如通过自动DNA合成和/或重组DNA技术)制备或获得。
宿主细胞
本公开提供表达本公开的胰高血糖素类似物前体肽或含有本公开的多核苷酸或载体的重组宿主细胞。一些实施方案中,宿主细胞为细菌细胞、真菌细胞或哺乳动物细胞。
细菌细胞例如包括革兰氏阴性细菌菌株(例如大肠杆菌(Escherichia coli)菌株、变形杆菌属(Proteus)菌株及假单胞菌属(Pseudomonas)菌株)及革兰氏阳性细菌菌株(例如芽孢杆菌属(Bacillus)菌株、链霉菌属(Streptomyces)菌株、葡萄球菌属(Staphylococcus)菌株及乳球菌属(Lactococcus)菌株)的细胞。
真菌细胞例如包括木霉属(Trichoderma)、脉孢菌属(Neurospora)及曲菌属(Aspergillus)的物种的细胞;或者包括酵母属(Saccharomyces)(例如酿酒酵母(Saccharomyces cerevisiae))、裂殖酵母属(Schizosaccharomyces)(例如粟酒裂殖酵母(Schizosaccharomyces pombe))、毕赤酵母属(Pichia)(例如巴斯德毕赤酵母(Pichia pastoris)及嗜甲醇毕赤酵母(Pichia methanolica))及汉森酵母属(Hansenula)的物种的细胞。
哺乳动物细胞例如包括例如HEK293细胞、CHO细胞、BHK细胞、HeLa细胞、COS细胞等。
然而,本公开也可使用两栖类细胞、昆虫细胞、植物细胞及本领域中用于表达异源蛋白的任何其他细胞。
本公开的细胞不能发育成完成的植株或动物个体。
生产或制备方法
本公开提供制备本公开的胰高血糖素类似物的方法,包括例如以下的方法:
(a)通过化学合成(例如,固相或液相合成)方法合成胰高血糖素类似物,并回收由此获得的所合成的胰高血糖素类似物;或者
(b)由编码前体肽的多核苷酸或载体表达前体肽,回收表达产物,以及修饰所述前体肽,以产生本公开的胰高血糖素类似物,例如,可通过引入一种或多种非天然氨基酸(例如Aib)来修饰前体肽。
在一个实施方案中,包含以下步骤:
-在允许表达前体肽的条件下,培养本公开的宿主细胞;及
-从培养物中回收前体肽;及
-修饰所述前体肽,获得本公开的胰高血糖素类似物。可选地,包含纯化前体肽的步骤。
用于重组产生多肽的方法及试剂,例如特定适合表达载体、转化或转染方法、选择标记物、诱导蛋白表达的方法、培养条件等在本领域中是已知的。类似地,适用于制造前体肽的方法中的多肽分离及纯化技术为本领域技术人员所公知。固 相或液相合的方法在本领域中是已知的,例如,可参考WO98/11125,尤其是Fields,GB et al.,2002,“Principles and practice of solid-phase peptide synthesis”.In:Synthetic Peptides(第二版),以及本公开中的实施例。
在一些实施方案中,还提供胰高血糖素类似物形成其可药用盐和/或溶剂化物的方法。例如,本公开胰高血糖素类似物可以与药学上可接受的酸性或碱性化合物反应成盐。
在一些实施方案中,本公开的胰高血糖素类似物可以采用微生物重组表达的方法来制备,也可以采用Fmoc固相合成的方法来制备(例如SPPS方法,包括氨基酸脱保护的方法、从树脂上切割肽的方法及其纯化的方法)。
在一些实施方案中,采用Fmoc固相合成的方法时,合成载体为Fmoc-L-Thr(tBu)-Wang树脂(吉尔生化,载量0.533mmol/g)。在一些实施方案中,合成过程中使用的氨基酸衍生物包括:Fmoc-L-Ala-OH,Fmoc-L-Arg(Pbf)-OH,Fmoc-L-Asn(Trt)-OH,Fmoc-L-Asp(OtBu)-OH,Fmoc-L-Gln(Trt)-OH,Fmoc-L-Glu(OtBu)-OH,Fmoc-Gly-OH,Fmoc-L-His(Trt)-OH,Fmoc-L-Ile-OH,Fmoc-L-Leu-OH,Fmoc-L-Lys(Boc)-OH,Fmoc-L-Met-OH,Fmoc-L-Phe-OH,Fmoc-L-Pro-OH,Fmoc-L-Ser(tBu)-OH,Fmoc-L-Thr(tBu)-OH,Fmoc-L-Trp(Boc)-OH,Fmoc-L-Tyr(tBu)-OH,Fmoc-L-Val-OH,Fmoc-Aib-OH,Fmoc-L-Nle-OH等。在一些实施方案中,合成过程包括:洗涤固相合成载体后,首先用含20%4-甲基哌啶的氮,氮-二甲基甲酰胺(DMF)溶液脱去固相合成载体α-氨基上的Fmoc保护基团,接着该固相载体与序列中下一个氨基酸衍生物在过量情况下使用HCTU/4-甲基吗啉活化后进行缩合形成酰胺键以延长肽链;重复缩合→洗涤→去保护→洗涤→下一轮氨基酸缩合的操作以达到所要合成的多肽链长度,最后用三氟乙酸:水:三异丙基硅烷(90:5:5,v:v:v)的混合溶液与树脂反应将多肽从固相载体上裂解下来,再由冷冻甲基叔丁基醚沉降后得到多肽衍生物的固体粗品;多肽固体粗品由含0.1%三氟乙酸的乙腈/水的混合溶液溶解后由C-18反相制备色谱柱纯化分离后得到多肽及其衍生物的纯品。
药物组合物
本公开提供药物组合物,其含有预防、治疗或缓解有效量的本公开的胰高血糖素类似物或可药用盐和/或溶剂化物,以及一种或多种药学上可接受的载体、稀释剂、缓冲剂或赋形剂。
在一些实施方案中,所述药物组合物单位剂量中可含有0.01至99重量%的本公开的胰高血糖素类似物或可药用盐和/或溶剂化物。在另一些实施方案中,药物组合物单位剂量中含本公开的胰高血糖素类似物或可药用盐和/或溶剂化物的量为0.1-2000mg;一些具体实施方案中为1-1000mg。
在一些实施方案中,药物组合物进一步包括至少一种具有代谢性疾病治疗活性的化合物或物质。
在一些实施方案中,所述具有代谢性疾病治疗活性的化合物或物质选自以下中的一种或多种:葡萄糖依赖性促胰岛素肽(GIP)、胰高血糖素样肽-1(GLP-1)受体激动剂、胰岛素、肠高血糖素、神经肽Y5受体拮抗剂、乙酰辅酶A羧化酶抑制剂、Leptin受体激动剂、格列奈、α-葡萄糖苷酶抑制剂(AGi)、噻唑烷二酮(TZD)、二肽基肽酶-4抑制剂类(DPP-IV)、钠葡萄糖协同转运蛋白2抑制剂(SGLT-2)、法尼醇X受体(FXR)激动剂和肥胖抑制素(Obestatin)。
本公开的药物组合物可以通过胃肠外给药,用注射器(任选笔型注射器),通过皮下、肌内、腹膜内或静脉内注射进行。或者,胃肠外给药可以用输注泵进行。另外的选择是组合物可以是经鼻或肺喷雾的形式给予胰高血糖素肽的溶液剂或混悬剂;或者,其可以是透皮给药例,如通过无针注射或由贴剂、任选离子导入贴剂;或者,其可以是经粘膜(例如口腔)给药。
试剂盒(或药盒)
本公开还提供了一种药盒,所述药盒包括本公开的胰高血糖素类似物或其可药用盐和/或溶剂化物或包含其的药物组合物和施用装置。
在一些实施方案中,所述装置包含注射器和针。在一些具体实施方案中,所述装置是预充针。
在一些实施方案中,本公开的胰高血糖素类似物或其可药用盐和/或溶剂化物或包含其的药物组合物于预充针中。
预防、治疗疾病或病症的方法和制药用途
本公开还提供了上述胰高血糖素类似物或其可药用盐和/或溶剂化物,和/或上述药物组合物在制备用于预防、治疗疾病或病症的药物中的用途。
本公开还提供上述胰高血糖素类似物或其可药用盐和/或溶剂化物,和/或上述药物组合物,其用于预防、治疗疾病或病症。
本公开还提供了预防、治疗疾病或病症方法,其包括向有其需要的对象施用治疗有效量的本公开的胰高血糖素类似物或其可药用盐和/或溶剂化物,和/或施用治疗有效量的本公开的药物组合物。
在一些实施方案中,所述疾病或病症选自低血糖、高血糖症、2型糖尿病、1型糖尿病、冠心病、动脉粥样硬化、β-受体阻滞剂中毒、胰岛素瘤和冯吉尔克病;所述病症或病症选自葡萄糖耐量减低、血脂异常、高血压、体重超重、暴食症、肝脂肪变性、肥胖。
在一些实施方案中,所述低血糖选自病理性低血糖或非病理性低血糖。
在一些实施方案中,所述低血糖选自糖尿病性低血糖、非糖尿病性低血糖、 空腹低血糖、药物诱发性低血糖、急性胰岛素诱发低血糖、胃旁路术诱发性低血糖、酒精诱发性低血糖、反应性低血糖和妊娠期低血糖。
在一些实施方案中,提供了一种迅速增加葡萄糖水平、使血糖水平正常、使血糖水平稳定、或者预防或治疗低血糖的方法,其包括向有需要的对象施用有效量的本公开的胰高血糖素类似物或其可药用盐和/或溶剂化物或包含其的药物组合物。
在一些实施方案中,提供了一种减少体重增加或引起体重下降的方法,其包括向有需要的对象施用有效量的本公开的胰高血糖素类似物或其可药用盐和/或溶剂化物或包含其的药物组合物。减少体重增加或引起体重下降的方法预期可用于治疗各种起因的肥胖,包括药物诱导的肥胖,并减少与肥胖相关的并发症,包括血管疾病(例如冠状动脉疾病、中风、周围血管疾病、缺血性再灌注等)、高血压、II型糖尿病、高脂血症和骨骼肌疾病。本公开提供相应胰高血糖素类似物或其可药用盐和/或溶剂化物或包含其的药物组合物用于制备预防、治疗、缓解肥胖的药物的制药用途。
在一些实施方案中,提供了一种治疗高血糖症或糖尿病的方法,其包括联合施用胰岛素与本公开的胰高血糖素类似物或其可药用盐和/或溶剂化物或包含其的药物组合物。联合施用胰岛素(例如基础、速效或长效胰岛素)和本公开的胰高血糖素类似物或其可药用盐和/或溶剂化物或包含其的药物组合物,能够减少夜间低血糖和/或缓冲胰岛素的使血糖过低的效应。本公开提供相应胰高血糖素类似物或其可药用盐和/或溶剂化物或包含其的药物组合物用于制备预防、治疗、缓解高血糖症或糖尿病的制药用途。
在一些实施方案中,上述方法是用于人受试者的,上述制药用途是用于人受试者的药物的制备用途。
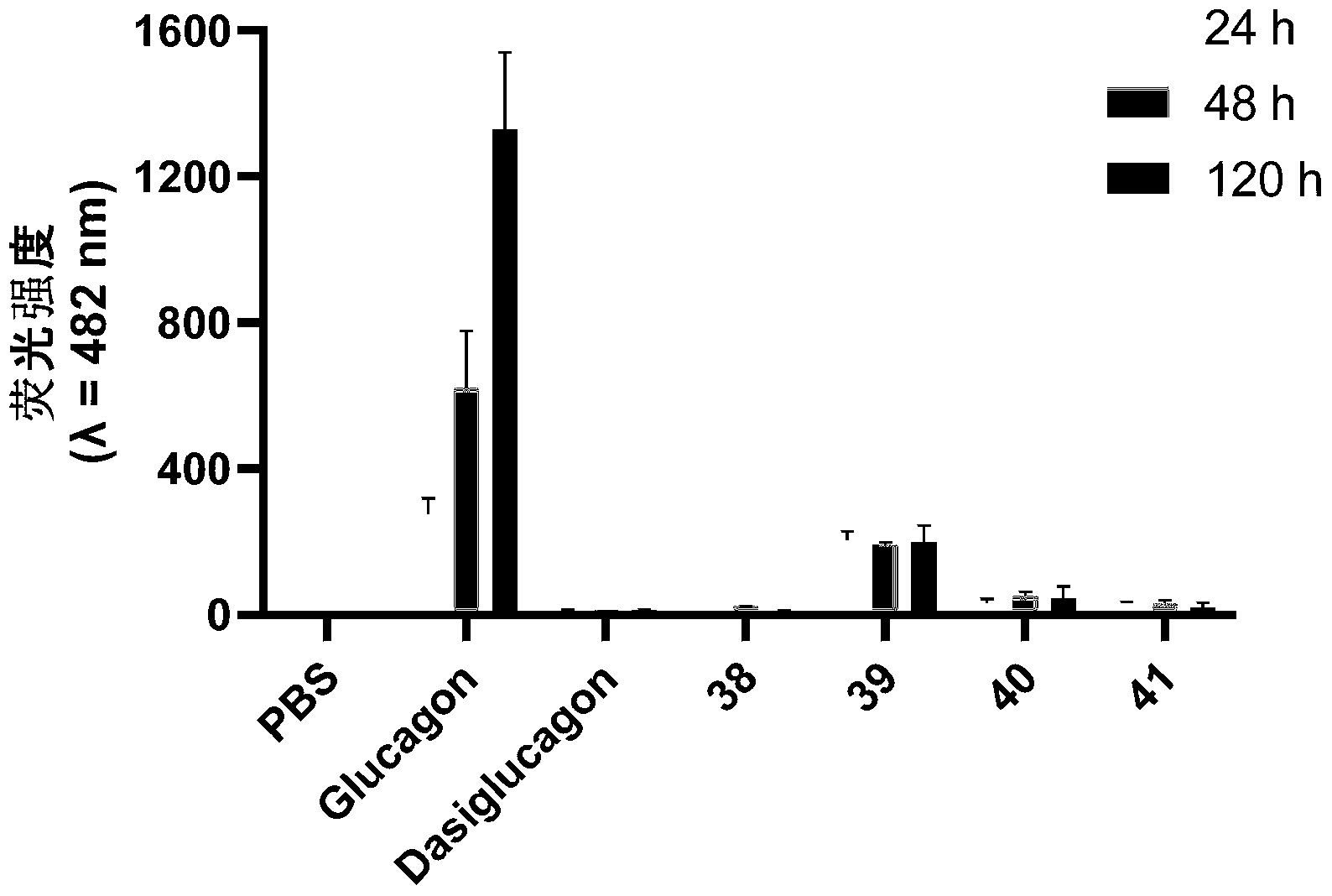
图1为通过ThT原纤维形成测定法评价胰高血糖素类似物的物理稳定性的结果。
图2为正常血糖大鼠模型中胰高血糖素类似物40和Dasiglucagon的药效结果。
图3为低血糖大鼠模型中胰高血糖素类似物40和Dasiglucagon的药效结果。
图4A为Dasiglucagon的溶血性检查结果;图4B为胰高血糖素类似物40的溶血性检查结果。
图5A和图5B分别为胰高血糖素类似物40和Dasiglucagon在人肝微粒体中、人肾微粒体中的稳定性结果。
图6为胰高血糖素类似物40和Dasiglucagon经皮下或静脉注射给药后的药时曲线结果。
定义
为了更容易理解本公开,以下具体定义了某些技术和科学术语。除显而易见在本公开中的它处另有明确定义,否则本公开使用的所有其它技术和科学术语都具有本公开所属领域的一般技术人员通常理解的含义。
术语“胰高血糖素类似物”是指具有天然胰高血糖素对胰高血糖素受体的至少一部分、全部、或更高的激动剂活性的化合物。例如胰高血糖素类似物包括但不限于:在SEQ ID NO:51所示的氨基酸序列基础上包含任意氨基酸替换、添加或删除,或包含翻译后修饰或其他化学修饰的多肽,前提是所述类似物具有刺激胰高血糖素受体的活性,例如使用实施例2描述的测定法通过cAMP的产生来测定的。
本公开中,胰高血糖素类似物也包括具有修饰的氨基末端和/或羧基末端的肽。例如,包含以酰胺基团取代末端羧酸的肽。例如,本公开的胰高血糖素类似物可以在序列的氨基端(N-端)引入“H-”部分,在序列的羧基端(C-端)引入“-OH”部分或“-NH
“天然胰高血糖素”是指具有以下序列的天然人胰高血糖素:
H-His-Ser-Gln-Gly-Thr-Phe-Thr-Ser-Asp-Tyr-Ser-Lys-Tyr-Leu-Asp-Ser-Arg-Arg-Ala-Gln-Asp-Phe-Val-Gln-Trp-Leu-Met-Asn-Thr-OH(SEQ ID NO:51)。
“Dasiglucagon”特指由西兰制药公司(Zealand Pharma)开发的胰高血糖素类似物,其氨基酸序列为:H-HSQGTFTSDYSKYLDAibARAEEFVKWLEST-OH(SEQ ID NO:52)。
本公开中,如果没有进一步解释,术语“GLP-1”是指人GLP-1(7-36或7-37);术语“GIP”是指人GIP(1-42)。
本公开所用氨基酸三字母代码和单字母代码如J.biol.chem,243,p3558(1968)中所述。除非明确说明,否则本公开中所有氨基酸残基的构型为L-型。另外,Aib是2-氨基异丁酸(又称α-氨基异丁酸),α-甲基-Ser(α-甲基丝氨酸)是α位 H被甲基取代的丝氨酸,pGlu是焦谷氨酸。
“天然氨基酸”是指20种常规氨基酸(即丙氨酸(A),半胱氨酸(C),天冬氨酸(D),谷氨酸(E),苯丙氨酸(F),甘氨酸(G),组氨酸(H),异亮氨酸(I),赖氨酸(K),亮氨酸(L),甲硫氨酸(M),天冬酰胺(N),脯氨酸(P),谷氨酰胺(Q),精氨酸(R),丝氨酸(S),苏氨酸(T),缬氨酸(V),色氨酸(W)和酪氨酸(Y)。
“非天然氨基酸”是指不是天然编码的或不在任何生物体的遗传密码中发现的氨基酸。它们可以是例如纯化学合成的化合物。非天然氨基酸的实例包括但不限于:羟基脯氨酸,γ-羧基谷氨酸,O-磷酸丝氨酸,氮杂环丁烷羧酸,2-氨基己二酸,3-氨基己二酸,β-丙氨酸,氨基丙酸,2-氨基丁酸,4-氨基丁酸,6-氨基己酸,2-氨基庚酸,2-氨基异丁酸(Aib),3-氨基异丁酸,2-氨基庚二酸,叔丁基甘氨酸,2,4-二氨基异丁酸(Dap),锁链素(desmosine),2,2′-二氨基庚二酸,2,3-二氨基丙酸(Dab),N-乙基甘氨酸,N-甲基甘氨酸,N-乙基天冬酰胺,高脯氨酸,羟基赖氨酸,别羟基赖氨酸(allo-hydroxylysine),3-羟基脯氨酸,4-羟基脯氨酸,异锁链素(isodesmosine),别异亮氨酸,N-甲基丙氨酸,N-甲基甘氨酸,N-甲基异亮氨酸,N-甲基戊基甘氨酸,N-甲基缬氨酸,萘基丙氨酸(naphthalanine),正缬氨酸,正亮氨酸(Nle),鸟氨酸(Orn),D-鸟氨酸,D-精氨酸,对氨基苯丙氨酸,戊基甘氨酸,呱啶酸(pipecolic acid)和硫代脯氨酸。此外,“非天然氨基酸”还包括在天然氨基酸或非天然氨基酸的C-末端羧基,N-末端氨基和/或其侧链官能团上经化学修饰所得的化合物。
术语“激动剂”定义为激活所讨论的受体类型的物质或配体。例如,本公开上下文中使用的术语GLP-1或GIP或胰高血糖素(受体)激动剂指可以激活GLP-1受体或GIP受体或胰高血糖素受体的物质或配体。
术语“可药用盐”是指对待治疗的患者或对象无害的盐。这样的盐通常是酸加成盐或碱式盐。
术语“溶剂化物”是指由限定化学计量的溶质(在这种情况下为本公开的胰高血糖素类似物或者其可药用盐)和溶剂形成的复合物。
术语“药物组合物”表示含有一种或多种本公开的胰高血糖素类似物或其生理学上/可药用的盐或前体药物与其他化学组分的混合物,以及其他组分例如生理学/可药用的载体和赋形剂。
术语“可药用载体”包括任何标准药用载体或稀释剂,例如用于适于经口、肺、直肠、鼻、局部、皮下、肌内、静脉内、腹膜内、皮内、透皮或阴道内施用的组合物或制剂中使用的那些。
术语“治疗”是指用于获得有益的或期望的临床结果的方法。就本公开目的 而言,有益的或期望的临床结果包括但不限于缓解病症、减轻疾病程度、稳定(即,不恶化)疾病状态、延迟或减缓疾病发展、改善或缓和疾病状态以及(部分或全部地)消除(remission),无论是可检出的还是不可检出的。“治疗”还可以指与未接受治疗时的预期存活相比延长存活期。“治疗”是以防止疾病发生或改变疾病病理状况为目的而进行的介入。因此,“治疗”是指治疗性处理和预防性或防护性手段二者。如在预防性或防护性手段的上下文中使用的,化合物未必完全防止疾病或病症发生。需要治疗的对象包括已经患病或需要预防疾病发生的对象。“治疗”也指与不进行治疗的情况相比抑制或减少病理状况或症状(例如,体重增加或低血糖)的增加,并且不暗示相关病症的完全终止。
术语“有效量”或“治疗有效量”是指足以治愈、缓解、或部分阻止、或者以其他方式促进给定病症(紊乱、疾病)或损伤以及优选地由它们引起的并发症的治愈或康复的量或剂量。对于特定目的有效的量或剂量取决于疾病或病症的严重程度以及待治疗对象或患者的体重和总体状况。合适的量或剂量的确定在经过训练的一般技术的医生(或兽医)的能力范围之内。
术语“对象”可与“患者”、“个体”、“受试者”等互换使用,并且均指人或非人动物,包括但不限于哺乳动物,例如人、灵长类动物、家畜动物(例如,牛、猪)、宠物(例如,狗、猫)和啮齿类动物(例如,小鼠和大鼠)。
实施例
以下结合实施例进一步描述本公开,但这些实施例并非限制着本公开的范围。本公开实施例中未注明具体条件的实验方法,通常按照常规条件,如常规多肽Fmoc固相合成法手册,冷泉港的抗体技术实验手册,分子克隆手册;或按照原料或商品制造厂商所建议的条件。未注明具体来源的试剂,为市场购买的常规试剂。
本公开主要实验试剂(来源):Fmoc-Thr(tBu)-Wang树脂(吉尔生化),HCTU(昊帆生物),Fmoc-Aib-OH(吉尔生化),氮,氮-二甲基甲酰胺(国药),二氯甲烷(国药),三氟乙酸(TCI Chemicals),三异丙基硅烷(TCI Chemicals),乙腈(Merck-Millipore),二异丙基乙胺(Sigma),4-甲基哌啶(TCI Chemicals),甲基叔丁基醚(TCI Chemicals),4-甲基吗啉(TCI Chemicals),Fmoc-Nle-OH(吉尔生化)。DMEM/F12(Gibco 11330032),酪蛋白(Casein),3-异丁基-1-甲基黄嘌呤(Sigma I7018-250MG),cAMP-Gs Dynamic kit(Cisbio 62AM4PEC,20000个测试),384孔板(Sigma CLS4514-50EA),96V型底板(PS)(Axygen WIPP02280),96孔板(Cisbio 66PL96100),
本公开主要实验仪器(来源):H-CLASS分析型超高效液相色谱(WATERS),Agilent 1290-6530超高效液相色谱-质谱仪(Agilent Technologies),Prep-150制备型高效液相色谱(WATERS),Prelude-X多通道多肽固相合成仪(Protein Technologies),酶标仪(BioTek H1MFD;Tecan-Infinite F Plex)。
实施例1.胰高血糖素类似物的合成
本实施例设计并按照以下方法合成了表1的化合物。
表1.胰高血糖素类似物(又称化合物或本公开化合物)
1.化合物1的化学合成
1.1多肽骨架的合成
称取0.1mmol固相合成载体Fmoc-Thr(tBu)-Wang树脂置于一次性聚丙烯多肽合成固相反应管中,加入DMF(10mL)溶胀树脂10分钟,真空抽掉DMF,加入DMF(10mL)洗涤树脂,重复洗涤2次。使用Prelude-X全自动多肽合成仪完成多肽骨架的合成,其中酰胺键缩合使用10倍过量,相应的Fmoc-保护氨基酸,用HCTU/4-甲基吗啉活化后在室温下反应30分钟进行氨基酸的缩合。Fmoc基团脱保护使用含20%4-甲基哌啶的氮,氮-二甲基甲酰胺溶液在室温下反应2次,每次10分钟。此外,对于Aib旁N-端氨基酸的缩合,需要在室温下进行二次乃至三次缩合,缩合时间每次30-60分钟,这对改善粗品肽的纯度至关重要。
1.2树脂肽的裂解
上述步骤得到的树脂肽依次用DMF,DCM洗涤3次后进行真空干燥,后加入新鲜配制的裂解液10mL(三氟乙酸:三异丙基硅烷:水=90:5:5,v:v:v)在室温下振荡反应3小时。反应结束后过滤,用三氟乙酸洗涤树脂2次,合并滤液后加入大量冷冻甲基叔丁基醚析出固体,离心后除去上清液并得到化合物1的多肽粗品。
1.3粗品肽的反相液相色谱纯化
将粗品肽溶于含有0.1%(v/v)三氟乙酸,20%(v/v)乙腈/水的混合溶剂中, 经过0.22μm膜过滤后用WATERS Prep150 LC反相高效液相色谱系统进行分离,流动相为A(0.1%三氟乙酸,10%乙腈,水溶液,v/v)和B(0.1%三氟乙酸,90%乙腈,水溶液,v/v)。其中,色谱柱为X-SELECT OBD C-18(WATERS)反相色谱柱,纯化过程中色谱仪检测波长设定为220nm,流速为20mL/min。收集产物相关馏分冻干后得到化合物编号1的多肽纯品,收率20%。多肽纯品通过分析性高效液相色谱和液相色谱/质谱联用确定纯度及化合物身份,其中纯度=96.09%,且分子量正确。
2.化合物2-49的化学合成
采用化合物1的实验方案合成本公开化合物2-49的多肽化合物,并用分析型超高效液相色谱和液相色谱/质谱联用确定纯度和化合物分子量,其中化合物分子量正确,纯度如表2。
表2.化合物纯度
以下实施例对实施例1合成的胰高血糖素类似物进行了生物学测试评价。
实施例2.胰高血糖素类似物对胰高血糖素受体(GCGR)、胰高血糖素样肽-1受体(GLP-1R)和葡萄糖依赖性促胰岛素分泌多肽受体(GIPR)的激动剂活性评估
1.实验目的
测定本公开的胰高血糖素类似物对人胰高血糖素受体(GCGR)、胰高血糖素样肽-1受体(GLP-1R)和葡萄糖依赖性促胰岛素分泌多肽受体(GIPR)的激动剂活性。相关化合物对GCGR的活化将刺激细胞环磷酸腺苷(cAMP)的形成。因此,可使用合适的表达受体的细胞中cAMP的产生来监测受体活性。
2.实验方法
对GCGR的激动剂活性检测:从液氮罐中取出冻存的CHO-K1/GCGR/CRE-Luc稳转细胞株,放于37℃水浴锅中快速融化,用DMEM/F12培养基(Sigma Cat#D8437)重悬,离心后将细胞接种至T75培养瓶中,细胞至少传代一次之后,再用于后续测试。测试前,胰酶消化细胞,离心后清洗一遍细胞,使用不含血清DMEM/F12培养基重悬细胞,调整细胞密度,以2,500个细胞/5μL/孔的密度铺于96孔板;配制Cisbio-cAMP-Gs Dynamic试剂盒中的1×缓冲液,添加IBMX至终浓度为0.5mM;每孔加入5μL缓冲液梯度稀释的多肽,轻震混匀,37℃静置孵育30分钟;将cAMP-d2和Anti-cAMP-Eu
对GLP-1R的激动剂活性检测:与上述对GCGR的激动剂活性检测方法不同在于,使用的是CHO-GLP-1R稳转细胞株。
对GIPR的激动剂活性检测:与上述对GCGR的激动剂活性检测方法不同在于,使用的是CHO-K1/GIPR稳转细胞株,细胞密度是3,000个细胞/5μL/孔。
3.实验结果
使用Tecan-Infinite F Plex酶标仪读取HTRF的信号,激发波长为320nm,发射波长为620nm和665nm。计算信号比值(665nm/620nm*10,000),将其与样品浓度使用四参数方程非线性拟合,得出EC
表3.化合物对人GCGR的激动剂活性
(相对活性是以天然胰高血糖素的活性为100%,进行归一化。)
表4.化合物对人GLP-1R和GIPR的激动剂活性
(n.d.表示未检出。)
表3结果显示,本公开的胰高血糖素类似物对人GCGR的激动剂活性显著优于Dasiglucagon。表4结果显示,与天然胰高血糖素相比,本公开的胰高血糖素类似物对GLP-1R和GIPR的激动剂活性极低,可以忽略,即本公开的胰高血糖素类似物对GCGR有良好的特异性。
实施例3.胰高血糖素类似物在生理条件缓冲液中的溶解度评估
1.实验目的
天然胰高血糖素直接作为治疗剂的使用受到限制,是因为其在中性pH 7.4条件下溶解度远低于1mg/mL。本实施例的目的是评估本公开胰高血糖素类似物在中性pH缓冲液中的溶解度,期望与天然胰高血糖素相比具有更高的溶解度。
2.实验方法
在pH 7.4的磷酸盐缓冲液中制备部分本公开胰高血糖素类似物的饱和溶液,室温超声5min后,离心(10000g,5min),吸取上清液并确保无可见沉淀。测量溶液在280nm的吸光度(Abs
3.实验结果
本公开的多种胰高血糖素类似物相比天然的胰高血糖素具有显著提升的溶解度,见表5。比较化合物2至化合物5发现,在第17位包含Aib的化合物3比在18位包含Aib的化合物4具有提升的溶解度;在第17位包含Aib的化合物3比在16或19位包含α-甲基-Ser的化合物2和化合物4具有提升的溶解度。可见胰高血糖素类似物在第17位包含Aib对提升多肽溶解度有重要作用。
表5.化合物的溶解度数据
实施例4.胰高血糖素类似物的物理稳定性和化学稳定性评估
天然的胰高血糖素在溶液中的物理和化学稳定性极差。天然胰高血糖素水溶液会在数小时至数天内形成凝胶或者纤维状沉淀,并且在多肽浓度较高、外界扰动及含盐情况下更容易凝胶化。此外,天然胰高血糖素的化学不稳定性主要是由于其序列发生异构化(天冬氨酸残基)、脱酰胺化(天冬酰胺、谷氨酰胺残基)及氧化(甲硫氨酸残基)等导致。
1.实验目的
本实施例的目的是评估本公开胰高血糖素类似物在溶液中的物理稳定性和化学稳定性。
2.物理稳定性评估实验方法
本实验通过Thioflavin-T(ThT)荧光测试方法监测原纤维形成。将冻干后的胰高血糖素类似物溶解于0.1N HCl水溶液,浓度1mg/mL。多肽溶液在恒温振荡器上孵育120h(37℃,300rmp)并分别于24h、48h及120h检测溶液原纤维含量。ThT荧光测试中,准确称取8mg ThT粉末溶于50mL PBS缓冲液(1×),经过0.22μm滤膜过滤后避光保存于4℃备用。使用时用PBS缓冲液(1×)进行1:500的比例稀释配制成工作溶液,在96孔板中每个孔中分别加入100μL工作溶液及5μL待测多肽溶液,混匀后室温孵育20-30min,使用Tecan-Infinite F Plex酶标仪读取ThT荧光信号,激发波长为450nm,发射波长为482nm,每个多肽的测试包含四次生物学重复。
3.化学稳定性评估实验方法
将胰高血糖素类似物冻干粉末溶于磷酸盐缓冲液(10mM磷酸二氢钠,15 mg/mL丙二醇,0.01%吐温-80,pH 7.4)至终浓度1mg/mL(通过测量溶液在280nm的吸光度确定),将样品置于玻璃瓶中并在4℃和25℃下孵育30天。在第0天、7天、14天、21天和28天取样后利用超高效液相色谱检测样品纯度和降解产物,色谱使用C-18反相色谱柱,UV=214nm。化合物纯度定义为各色谱图中主峰相对于所有整合峰的总面积的面积百分比,以给定多肽不同时间的纯度参照第0天样品的纯度进行归一化。
4.实验结果
通过以上实验方法,部分本公开胰高血糖素类似物在水溶液中的物理稳定性如图1所示,在磷酸盐缓冲液中的化学稳定性如表6所示。
表6.化合物在磷酸盐缓冲液中的化学稳定性
(n.d.表示多肽沉淀,纯度未测出。)
通过研究发现,本公开的胰高血糖素类似物与天然胰高血糖素(Glucagon)相比展现出优异的物理稳定性和化学稳定性;其中化合物40在磷酸盐缓冲液中的化学稳定性比Dasiglucagon更优。
实施例5.胰高血糖素类似物在正常血糖大鼠模型体内的药效评估
1.实验目的
本实施例是为对比评估本公开中的胰高血糖素类似物40、天然胰高血糖素(Glucagon)和Dasiglucagon在正常大鼠模型体内的升血糖药效。
2.实验方法
7-8周龄的雄性SD大鼠(Sprague-Dawley rats)适应性饲养一周。根据体重分组,分组后确保每组大鼠的平均体重和标准差相似。实验前4小时及实验过程中禁食,正常给水。完成禁食4小时后,实验组大鼠分别单次皮下给予0.5nmol/kg、 2nmol/kg、6nmol/kg的胰高血糖素类似物40或2nmol/kg的天然胰高血糖素或2nmol/kg的Dasiglucagon,对照组大鼠皮下给予与配置胰高血糖素类似物相同的磷酸盐缓冲液。给药前尾部采血测定T0点血糖,之后分别在15min,30min,45min,60min,75min,90min,105min,120min测定大鼠血糖。
3.实验结果
胰高血糖素类似物40提升大鼠血糖水平呈现剂量依赖性,与天然胰高血糖素、Dasiglucagon都呈现短时起效的特点,但相同剂量下的胰高血糖素类似物40升糖水平更高,具体结果见图2和表7。
表7.化合物在正常大鼠中的升糖数据
4.实验结论
结果显示,经皮下注射给药后,胰高血糖素类似物40、天然胰高血糖素(Glucagon)和Dasiglucagon均能快速地提高大鼠的血糖水平。0.5nmol/kg剂量的胰高血糖素类似物40与2nmol/kg剂量的Dasiglucagon对血糖提升的效果相近,且同等剂量下(2nmol/kg),胰高血糖素类似物40的药效明显好于Dasiglucagon。
在正常血糖大鼠模型中,与Dasiglucagon相比,同等剂量条件下本公开中的胰高血糖素类似物40升糖水平更高,药效更好。
实施例6.胰高血糖素类似物在低血糖大鼠模型体内的药效评估
通过皮下注射胰岛素诱导大鼠出现低血糖症状,模拟人发生低血糖场景,再皮下给予胰高血糖素类似物治疗,使血糖快速恢复至正常水平。
1.实验目的
对比Dasiglucagon,评估本公开中的胰高血糖素类似物40在低血糖大鼠模型体内的药效。
2.实验方法
7-8周龄的雄性SD大鼠(Sprague-Dawley rats)适应性饲养一周。根据血糖分组,分组后确保每组大鼠的平均血糖和标准差相似。实验前4小时及实验过程中禁食,正常给水。完成禁食4小时后,尾部采血测定T0点血糖,造模组大鼠立即皮下注射0.65IU/kg胰岛素,非造模组大鼠皮下注射相同体积的生理盐水。 之后在15min,30min,45min测定血糖。在45min时,造模组大鼠分别单次皮下给予6nmol/kg、12nmol/kg、20nmol/kg的胰高血糖素类似物40或12nmol/kg的Dasiglucagon,对照组大鼠和非造模组大鼠皮下给予与配置胰高血糖素类似物40相同的磷酸盐缓冲液。之后继续在60min,75min,90min,105min,120min,150min,180min测定大鼠血糖。
3.实验结果
胰岛素处理后,在大鼠血糖最低点给予本公开中的胰高血糖素类似物40治疗,能迅速恢复大鼠血糖且呈现剂量依赖性,虽然本公开的胰高血糖素类似物40与Dasiglucagon都呈现短时起效的特点,但在相同剂量下本公开中的胰高血糖素类似物40升糖水平更高,具体结果见图3和表8。
表8.化合物在低血糖大鼠模型中的升糖结果
4.实验结论
结果显示,在胰岛素诱导低血糖大鼠模型中,经皮下注射给药后,胰高血糖素类似物40、天然胰高血糖素(Glucagon)和Dasiglucagon均能在15分钟内快速地恢复并提高大鼠的血糖水平。同等剂量下(12nmol/kg),胰高血糖素类似物40对血糖的提升效果明显优于Dasiglucagon,并且持续时间更长。
在胰岛素诱导低血糖大鼠模型中,同等剂量条件下,胰高血糖素类似物40相比Dasiglucagon药效更好。
实施例7.胰高血糖素类似物的溶血性实验评估
溶血指红细胞膜被破坏,并且透明度增加呈深红色的现象;某些药物成分,辅料等含有溶血成分,可导致人体的溶血反应,引起局部肿胀,血液循环功能障碍等不良反应。根据红细胞破裂释放出来的血红蛋白在可见光波段具有吸收的原理,将供试化合物溶液加入大鼠的红细胞混悬液,孵育后用酶标仪测定吸光度值,评价溶血程度。
1.实验目的
观察胰高血糖素类似物40是否会引起溶血反应。
2.溶血性实验方法
红细胞混悬液的制备:取100μL新鲜大鼠全血,然后加入900μL 1×PBS溶液,置于平板摇床上,30rpm震摇5min,然后1000g离心5min,弃去上清液;重复以上清洗步骤,直到上清液不显红色为止,供测试用。
供试品溶液的制备:向供试品固体中加入适量1×PBS溶液,溶解得到标准储备液,然后用1×PBS稀释,得到浓度为1μg/mL,3μg/mL,10μg/mL,30μg/mL,100μg/mL和300μg/mL的供试品溶液。同时将空白1×PBS作为阴性对照,将含有0.1%Triton X-100(1μg/mL)的1×PBS溶液作为阳性对照。
孵育过程:加入500μL供试品溶液到红细胞混悬液,平板摇床上,30rpm震摇5min,使其充分混匀,然后将混悬液在37℃下温育1小时,然后1000g速度离心5min,取上清液100μL至酶标板单孔中,测定540nm处的吸光度。
3.实验结果
溶血率(%)计算公式为(供试品吸光度-阴性对照吸光度)/(阳性对照吸光度-阴性对照吸光度)×100%。当结果小于5%,判断无溶血性;当结果大于5%,判断待测物有溶血性。
本公开的胰高血糖素类似物的溶血性检查结果如图4A、图4B和表9所示。结果显示本公开的胰高血糖素类似物40与Dasiglucagon,在1至300μg/mL浓度范围内,溶血性检查均符合规定要求,未发现显著溶血副作用风险。
表9.化合物在人全血中的溶血率%
实施例8.胰高血糖素类似物的人体肝、肾微粒体稳定性评估
肝脏和肾脏是人体最主要的代谢器官,富含一相和二相代谢酶,会影响药物的代谢速度,对药物的降解清除起重要作用,影响血药浓度和半衰期。肝肾代谢常用的模型包括肝肾微粒体,S9组分,肝细胞,组织匀浆等。体外肝肾代谢稳定性是预测体内药动和药效学性质的主要指标之一。就肝肾微粒体模型而言,其采用从肝脏或肾脏提取的微粒体,加入还原型辅酶(NADPH)再生系统,模拟生理环境下代谢反应,评价测试化合物的体外代谢稳定性,可用于预测药物的体内降解和清除速度。理想条件下,胰高血糖素类似物需要快速吸收和清除,在体内有相对快的降解速度,解救低血糖的同时,避免高血糖的毒副反应。
1.实验目的
比较和评价胰高血糖素类似物在人的肝微粒体和肾微粒体体外代谢系统中的代谢稳定性。
2.人肝微粒、肾微粒体检测实验方法
溶液配置:称取适量化合物纯品,加入适量DMSO溶解分别得到Dasiglucagon和40的1mM供试溶液。
MgCl
稳定性实验过程:样本分别按照以下方式进行处理,
(1)孵育系统准备
a)加入NADPH:取10μL 20mg/mL的肝微粒体和40μL 10mM NADPH溶液加入到孵育系统中,肝微粒体和NADPH的终浓度分别为0.5mg/mL和1mM;
b)不加NADPH:取10μL 20mg/mL的肝微粒体和40μL H
(2)孵育反应系统中加入4μL 100μM的测试化合物溶液和阳性对照化合物(人肝微粒体采用维拉帕米(Verapamil),人肾微粒体采用盐酸苄达明),孵育体系终浓度为1μM,孵育温度为37℃;其中,维拉帕米和盐酸苄达明分别为已知的肝代谢酶和肾代谢酶的底物(参见Pauli-Magnus C等,J Pharmacol Exp Ther.2000May;293(2):376-82.),用于确证微粒体孵育系统的酶反应活性;
(3)分别在0min,15min,30min,60min和120min取样50μL,加入4倍体积的含有内标和3%甲酸的乙腈溶液终止反应。样本进一步经过3220g速度离心40min,取100μL上清液,加入等体积的H
3.实验结果:
本公开中的胰高血糖素类似物人肝微粒体和肾微粒体的稳定性结果如图5A、图5B和表10、表11所示。
表10.人肝微粒体孵育体系的稳定性结果
表11.人肾微粒体孵育体系的稳定性结果
4.实验结论
肝代谢方面,其一,Dasiglucagon和胰高血糖素类似物40在肝微粒体中代谢速度比肾微粒体中慢,代谢与NADPH无关。其二,胰高血糖素类似物40降解比Dasiglucagon稍快(体外T1/2:40为68.76min,Dasiglucagon为161.74min)。
肾代谢方面,其一,Dasiglucagon和胰高血糖素类似物40在肾微粒体中被代谢,但代谢与NADPH无关;其二,胰高血糖素类似物40降解比Dasiglucagon更快(体外T1/2:40为35.73min,Dasiglucagon为51.27min)。
总之,在肝肾微粒体孵育过程中,本公开中的胰高血糖素类似物40比Dasiglucagon的代谢速度更快,因此体内更容易被清除,高血糖副反应的发生风险更低,更有利于糖尿病患者的血糖控制。
实施例9.胰高血糖素类似物的大鼠体内药代动力学评估
动物药代动力学研究一般方法是采用临床拟用的给药途径,给予动物一定剂量的测试化合物,然后采用HPLC,GC,HPLC-MS等分析仪器方法测定血液,尿液等生物基质中药物浓度随着时间的变化情况,从而了解该化合物在体内的动态变化规律,获得血药浓度-时间曲线测定,进而得到药物的药代动力学参数,阐明化合物的吸收,分布,代谢和排泄过程和特点。
1.实验目的
以雄性SD大鼠为受试动物,单次皮下注射给予Dasiglucagon和胰高血糖素类似物40,研究Dasiglucagon和胰高血糖素类似物40在SD大鼠体内(血浆)的药代动力学特征。
2.实验方法
(1)按照表12对动物分组,给药前大鼠自由饮水和进食。
表12.动物实验分组
(2)采血
采样时间:给药前0min(predose),给药后2min,4min,7min,10min,20min,40min,1h和2h。从大鼠颈静脉插管采血。
(3)样本采集
1)每个时间点取0.2mL全血,转移至含有EDTA-K2抗凝的离心管中;
2)血样本在4℃下4000g速度离心5min,分离获得血浆;
3)血浆样本储存在-80℃冷冻保存。
(4)生物样本分析
样本前处理方法:取100μL血浆样本,加入300μL含有1ng/mL内标(维拉帕米)甲醇溶液,涡旋5min,低温离心10min,取上清液100μL,加入100μL0.1%甲酸水溶液,混合均匀,进仪器分析;
液相色谱和质谱分析:使用LC-30A液相色谱系统(日本岛津公司);API 5500型液相色谱-三重四级杆质谱联用仪(Analyst Software数据处理系统,美国AB公司)。色谱柱为nanomicro Unisil C18aq(4.6mm×150mm,5μm)色谱柱;柱温40℃;流动相A为0.1%甲酸水溶液,流动相B为0.1%甲酸乙腈溶液;流速0.5mL/min;进样量20μL;梯度条件如下表13所示。质谱采用电喷雾离子源(ESI),正离子分析模式,多反应监测(MRM)扫描方式。
表13.液相梯度程序
3.实验结果
采用以上HPLC-MS/MS方法测定血浆中各待测物的血药浓度,绘制血药浓度时间曲线,并用PKSolver软件计算药动学参数。通过以上实验方法,本公开的胰高血糖素类似物的药代动力学(PK)参数如表14和图6所示。
表14.皮下注射(SC)给药后Dasiglucagon和40的药动学参数比较
4.实验结论
结果显示,经皮下注射给药后,胰高血糖素类似物40的T1/2明显短于Dasiglucagon(40的T
总之,与Dasiglucagon相比,胰高血糖素类似物40能够更快地吸收起效和更迅速的清除,具有更优的药代动力学特性。
- 含有胰高血糖素样肽-1和胰高血糖素的片段类似物的嵌合多肽及其用途
- 长效胰高血糖素样肽-1类似物二聚体及其医药应用
