一种自模板调控的C/CoS2纳米管结构制备方法
文献发布时间:2023-06-19 09:29:07
技术领域
本发明涉及结构可控的C/CoS
背景技术
全球能源危机已成为严重的世界性问题。石油、煤炭、天然气等传统能源是一次能源,不可再生,寻求可持续、可再生、清洁能源显得尤为重要。在过去的几十年里,人们致力于开发氢燃料、太阳能电池、锂硫电池、金属空气电池、二氧化碳电化学还原、钙钛矿太阳能电池、传感器等新能源,其中氢能源则成为科研学者最为关注的研究对象。众所周知,氢一直被认为是一种清洁、地球资源丰富、环境友好的能源。但是,若要开发出足够的氢能,则需要提供较大偏压,这对设备功率提出很高的要求。那么,能否提出一种改进方式,以降低电耗为出发点,实现高效催化的目的。迄今为止,众多科研人员都在极力寻找高效制氢的催化剂,如贵金属Pt和Pd则成为研究电催化性能的首选材料。然而,这些贵金属含量少,价格昂贵,从长远角度考虑,它并不是一种合适的催化剂,因此,找到一种高效,无污染且成本低的催化剂来代替贵金属显得尤为重要。
近年来,过渡金属硫属化合物MX
发明内容
本发明是为避免上述现有技术所存在的不足之处,提出一种简便自模板调控的C/CoS
本发明解决技术问题采用如下技术方案:
一种自模板调控的C/CoS
a、称取0.58g Co(NO
b、待反应冷却后,取出初始产物Co(OH)Cl-urea,进而对初始产物Co(OH)Cl-urea进行超声以保证其纯度,超声时间20分钟,再使用酒精和去离子水多次洗涤初始产物Co(OH)Cl-urea,最后将初始产物Co(OH)Cl-urea置于真空干燥箱里烘干12-24小时,烘箱温度为60℃;
c、称量0.01g初始产物Co(OH)Cl-urea置于化学气相沉积系统中的高温区,温度设定为 400℃;将0.1g S粉置于化学气相沉积系统中的低温区,温度设定为240℃;初始产物Co(OH)Cl-urea与S粉之间的位置保持在15-20cm;整个化学气相反应在Ar/H
作为本发明的进一步改进,所述步骤a中反应温度为140℃,所述步骤c中Ar/H
作为本发明的进一步改进,所述步骤a中反应温度为140℃,所述步骤c中Ar/H
作为本发明的进一步改进,所述步骤a中反应温度为140℃,所述步骤c中Ar/H
作为本发明的进一步改进,所述步骤a中反应温度为140℃,所述步骤c中Ar/H
与现有技术相比,本发明的有益效果体现在:
1.制备方法简单,产物纯度高;
2.产物形貌可控。通过控制反应Ar/H
3.制备的产物活性位点多。纳米管的比表面积大,催化活性位点多,有利于催化性能提高;
4.本发明方法具有普适性。同样适用于其他硫属纳米材料在电存储及电催化等方面的应用。
附图说明
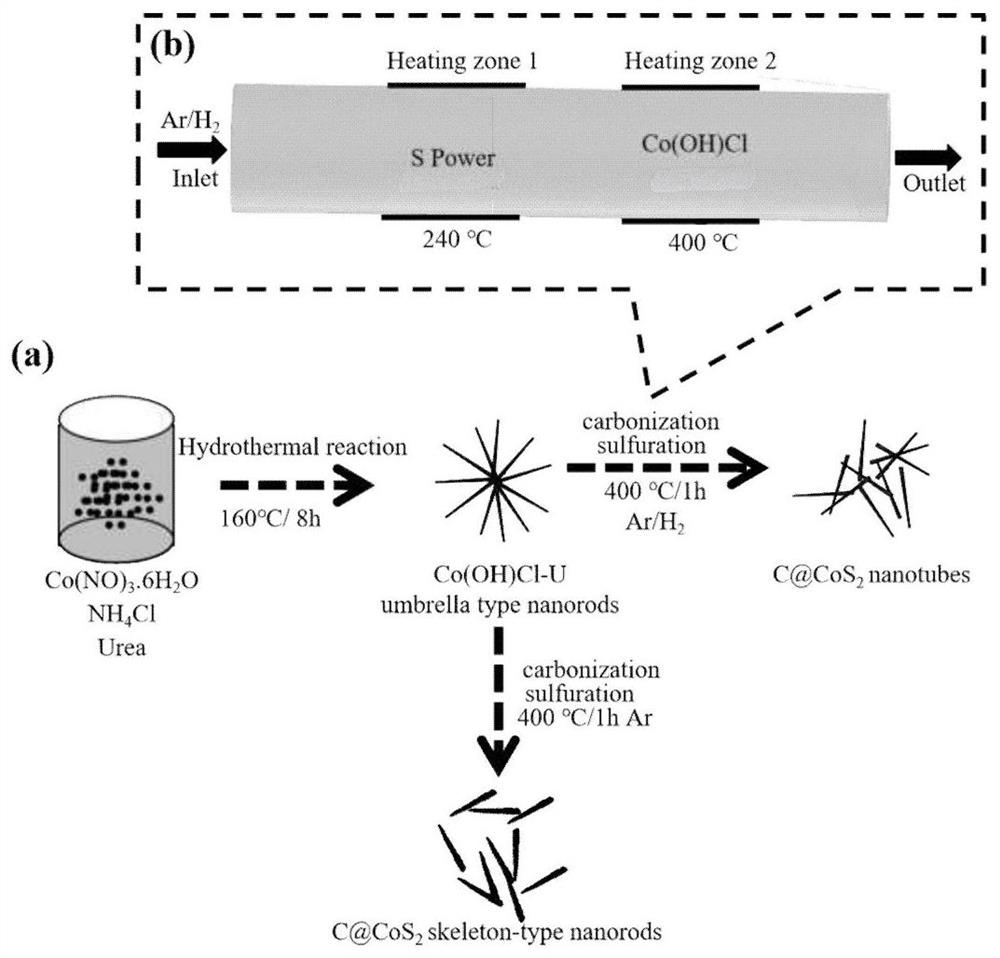
图1a为实施例1、2、3和4中的工艺流程图;
图1b为实施例1、2、3和4中的化学气相工艺流程图;
图2为不同温度下前驱物Co(OH)Cl-urea的扫描电子显微镜图;
图2a-b为80℃下的前驱物Co(OH)Cl-urea的形貌图;
图2c-d为100℃下的前驱物Co(OH)Cl-urea的形貌图;
图2e-f为140℃下的前驱物Co(OH)Cl-urea的形貌图;
图2g-h为140℃下的前驱物Co(OH)Cl-urea的形貌图;
图2i-j为180℃下的前驱物Co(OH)Cl-urea的形貌图;
图3为实施例1、2、3和4样品的形成机理图和不同Ar/H
图4为实施例1、2、3和4不同温度下的硫化产物的扫描电子显微镜图;
图4a-c为300℃下硫化产物的扫描电子显微镜图;
图4d-f为350℃下硫化产物的扫描电子显微镜图;
图4g-i为400℃下硫化产物的扫描电子显微镜图;
图4j-l为600℃下硫化产物的扫描电子显微镜图;
图4m-o为800℃下硫化产物的扫描电子显微镜图;
图5a-b为实施例3样品的扫描电子显微镜;
图5c-d为实施例3样品的透射电子显微镜;
图5e-f为实施例3样品的电子能谱图;
图6a-c为本发明在实施例3样品的光电子能谱图;
图6d为本发明在实施例3样品的热重分析图。
具体实施方式
下面结合具体实施例和附图对本发明做进一步说明,而不限制于本发明的范围。
a、称取0.58g Co(NO
b、待反应冷却后,取出初始产物Co(OH)Cl-urea,进而对初始产物Co(OH)Cl-urea进行超声以保证其纯度,超声时间20分钟,再使用酒精和去离子水多次洗涤初始产物Co(OH)Cl-urea,最后将初始产物Co(OH)Cl-urea置于真空干燥箱里烘干12-24小时,烘箱温度为60℃;
c、称量0.01g初始产物Co(OH)Cl-urea置于化学气相沉积系统中的高温区,温度设定为 400℃;将0.1g S粉置于化学气相沉积系统中的低温区,温度设定为240℃;初始产物Co(OH)Cl-urea与S粉之间的位置保持在15-20cm;整个化学气相反应在Ar/H
作为本发明的进一步改进,所述步骤a中反应温度为140℃,所述步骤c中Ar/H
作为本发明的进一步改进,所述步骤a中反应温度为140℃,所述步骤c中Ar/H
作为本发明的进一步改进,所述步骤a中反应温度为140℃,所述步骤c中Ar/H
作为本发明的进一步改进,所述步骤a中反应温度为140℃,所述步骤c中Ar/H
实施例1
本实施例按如下步骤制备C/CoS
a、称取0.58g Co(NO
b、待反应冷却后,取出初始产物Co(OH)Cl-urea,进而对初始产物Co(OH)Cl-urea进行超声以保证其纯度,超声时间20分钟,再使用酒精和去离子水多次洗涤初始产物Co(OH)Cl-urea,最后将初始产物Co(OH)Cl-urea置于真空干燥箱里烘干12-24小时,烘箱温度为60℃;
c、称量0.01g初始产物Co(OH)Cl-urea置于化学气相沉积系统中的高温区,温度设定为 400℃;将0.1g S粉置于化学气相沉积系统中的低温区,温度设定为240℃;初始产物Co(OH)Cl-urea与S粉之间的位置保持在15-20cm;整个化学气相反应在Ar/H
实施例2
本实施例按如下步骤制备C/CoS
a、称取0.58g Co(NO
b、待反应冷却后,取出初始产物Co(OH)Cl-urea,进而对初始产物Co(OH)Cl-urea进行超声以保证其纯度,超声时间20分钟,再使用酒精和去离子水多次洗涤初始产物Co(OH)Cl-urea,最后将初始产物Co(OH)Cl-urea置于真空干燥箱里烘干12-24小时,烘箱温度为60℃;
c、称量0.01g初始产物Co(OH)Cl-urea置于化学气相沉积系统中的高温区,温度设定为 400℃;将0.1g S粉置于化学气相沉积系统中的低温区,温度设定为240℃;初始产物Co(OH)Cl-urea与S粉之间的位置保持在15-20cm;整个化学气相反应在Ar/H
实施例3
本实施例按如下步骤制备C/CoS
a、称取0.58g Co(NO
b、待反应冷却后,取出初始产物Co(OH)Cl-urea,进而对初始产物Co(OH)Cl-urea进行超声以保证其纯度,超声时间20分钟,再使用酒精和去离子水多次洗涤初始产物Co(OH)Cl-urea,最后将初始产物Co(OH)Cl-urea置于真空干燥箱里烘干12-24小时,烘箱温度为60℃;
c、称量0.01g初始产物Co(OH)Cl-urea置于化学气相沉积系统中的高温区,温度设定为 400℃;将0.1g S粉置于化学气相沉积系统中的低温区,温度设定为240℃;初始产物Co(OH)Cl-urea与S粉之间的位置保持在15-20cm;整个化学气相反应在Ar/H
实施例4
本实施例按如下步骤制备C/CoS
a、称取0.58g Co(NO
b、待反应冷却后,取出初始产物Co(OH)Cl-urea,进而对初始产物Co(OH)Cl-urea进行超声以保证其纯度,超声时间20分钟,再使用酒精和去离子水多次洗涤初始产物Co(OH)Cl-urea,最后将初始产物Co(OH)Cl-urea置于真空干燥箱里烘干12-24小时,烘箱温度为60℃;
c、称量0.01g初始产物Co(OH)Cl-urea置于化学气相沉积系统中的高温区,温度设定为 400℃;将0.1g S粉置于化学气相沉积系统中的低温区,温度设定为240℃;初始产物Co(OH)Cl-urea与S粉之间的位置保持在15-20cm;整个化学气相反应在Ar/H
图1是实施例1、2、3和4产物的工艺流程图。其中图1a为实施例1、2、3和4中的工艺流程图;图1b为实施例1、2、3和4中的化学气相工艺流程图。图中明显可以看出,第一步采用低温溶剂热法制备前驱体Co(OH)Cl-urea;第二步采用化学气相沉积法制备出C@CoS
图2为不同温度下前驱物Co(OH)Cl-urea的扫描电子显微镜图。从图2a-b中可以看出,溶剂热反应温度设定80℃,产物出现少量纳米棒;当温度升高至100℃时,如图2c-d所示,产物出现部分无序纳米棒,且有聚集现象;进一步升高温度至140℃,如图2e-f,此刻产物形貌发生较大改变,形成伞型纳米棒结构;当反应温度达到160℃,如图2g-h,产物形貌呈现伞状纳米棒结构;继续升温至180℃,如图2i-j所示,产物形貌不再发生变化。
图3为实施例1、2、3和4样品的形成机理图和不同Ar/H
图4为实施例1、2、3和4不同温度下硫化产物的扫描电子显微镜图;图4a-c为300℃下硫化产物扫描电子显微镜图;图4d-f为400℃下硫化产物扫描电子显微镜图;图4g-i为500℃下硫化产物的扫描电子显微镜图;图4j-l为600℃下硫化产物的扫描电子显微镜图;图4m-o为800℃下硫化产物的扫描电子显微镜图;从图中可以看出,反应温度在400℃时的产物,纳米管结构最为明显,由此得出,反应最优温度为400℃。
图5a-b为实施例3样品的扫描电子显微镜;从图中可以看出产物呈现中空结构。图5c-d为实施例3样品的透射电子显微镜。如图5c是产物TEM图,从图中可以看出,该结构呈管状,从高分辨率TEM(HRTEM)图像可以看出,晶体的晶格条纹明显,其晶格间距也与文献报道的 CoS
图6a-c为本发明在实施例3样品的光电子能谱图;图6d为本发明在实施例3样品的热重分析图。图中分析可知,位于778.3eV和780.5eV处的峰分别对应于Co 2p
