一种亲水性氧化锌量子点及其制备方法和用途
文献发布时间:2023-06-19 09:58:59
技术领域
本发明涉及纳米氧化锌,具体涉及一种亲水性氧化锌量子点及其制备方法和用途,属于纳米材料和功能高分子材料技术领域。
背景技术
由于纳米材料具有独特的理化性质,近年来引起了人们的广泛关注。其中,纳米氧化锌作为一种重要的纳米材料和功能高分子材料,具有良好的光电、荧光和抗菌等特性,在传感、催化、包装、生物医药、日用化妆品等领域具有广泛的应用前景,引起人们的极大关注。
大量研究表明,纳米氧化锌的大小、形貌及晶型等形态结构,会对其性能造成极大影响。为满足各种条件下的使用需要,人们对纳米氧化锌的制备进行了一系列研究,主要为通过使用湿法化学法、溶剂热、静电纺丝和溶胶凝胶等不同方法制备不同形貌、不同性能的纳米氧化锌。目前,工业上以湿法化学法应用较多,其反应温度要求低,无需添加催化剂,实验原料价格低廉且毒性低,同时易于大规模工业化生产。然而,湿法化学法生产的纳米氧化锌多属于醇溶性的氧化锌,其水溶不完全、抗菌力不强、以及对衬底的选择有局限性,因而不利于生物医药及日用化妆品领域的应用。
发明内容
为了解决现有技术中的问题,根据本发明的第一方面,本发明的目的在于提供一种亲水性氧化锌量子点。
除特殊说明外,本发明所述份数均为重量份,所述百分比均为质量百分比。
本发明的目的是这样实现的:
一种亲水性纳米氧化锌量子点,其特征在于:在3425cm
上述亲水性纳米氧化锌量子点颗粒呈球状,平均粒径小于5nm。
上述亲水性纳米氧化锌量子点在深紫外区有吸收,范围为250nm-380nm,其最佳激发波长为365nm。在最佳激发波长下,上述亲水性纳米氧化锌量子点呈现黄色荧光发射,最强发射峰位于530nm。
根据本发明的第二方面,本发明的目的在于提供上述亲水性氧化锌量子点的制备方法。
本发明亲水性氧化锌量子点的制备方法,采用如下步骤:将乙酸锌,二水用无水乙醇溶解,然后置于冰浴中,滴加溶解有氢氧化钾的乙醇溶液,并不断搅拌以充分反应20~30min,然后将反应液从冰浴中取出置于室温环境,滴加3-氨丙基三乙氧基硅烷(APTES)水溶液,并不断搅拌3~5h,然后在5800~6200rmp离心乳白色浑浊溶液8~12min,弃去上层清液,加入无水乙醇分散并清洗沉淀物,再按照上述离心步骤操作两次,沉淀物置于鼓风干燥箱中于50~70℃下干燥1.5~2.5h,即得本发明亲水性氧化锌量子点。
上述将乙酸锌,二水用无水乙醇溶解为将乙酸锌,二水加入盛有无水乙醇的单口烧瓶中,80℃下搅拌回流直至乙酸锌完全溶解。
具体的说,本发明亲水性氧化锌量子点的制备方法,采用如下步骤:取35mM氢氧化钾至于50mL烧杯中,加入20mL无水乙醇搅拌15min直至氢氧化钾完全溶解,放置于4℃下的冰箱中冷藏;将25mM乙酸锌,二水加入盛有150mL无水乙醇的单口烧瓶中,80℃下搅拌回流直至乙酸锌完全溶解,随后将混合液置于冰浴中;将溶解有氢氧化钾的乙醇溶液滴加到盛有乙酸锌乙醇溶液的单口烧瓶,并不断搅拌以充分反应30min;将反应混合液取出冰浴待其温度回温至室温时,滴加1.5mL去离子水和500uL3-氨丙基三乙氧基硅烷(APTES)混合溶液,并不断搅拌5h;在6000rmp下离心乳白色浑浊溶液10min,移去上层清液,加入35mL无水乙醇分散并清洗沉淀物,再反复上述离心操作两次,然后将沉淀物置于鼓风干燥箱中60℃下干燥2h,即得本发明亲水性氧化锌量子点。
根据本发明的第三方面,本发明的目的在于提供上述亲水性氧化锌量子点在抗菌性化妆品中的应用。本发明所述抗菌性化妆品为具有抗菌功能的化妆品。本发明所述抗菌为杀灭细菌或抑制细菌生长繁殖及其活性的过程。本发明亲水性氧化锌量子点在抗革兰氏阳性菌或革兰氏阴性菌中的应用。本发明所述细菌为革兰氏阳性菌(例如:葡萄球菌(Staphylococcus)、金黄色葡萄球菌、屎肠球菌、蜡样芽孢杆菌、巨大芽孢杆菌、藤黄微球菌、链球菌(Streptococcus)、肺炎双球菌、炭疽杆菌、白喉杆菌、破伤风杆菌等)或革兰氏阴性菌(痢疾杆菌、伤寒杆菌、变形杆菌、大肠杆菌、霍乱弧菌等)。
有益效果:
本发明提供的亲水性氧化锌量子点,在透射电镜下观察到亲水性氧化锌量子点呈球状,大小均匀,分散良好,无团聚现象,平均颗粒粒径小于5nm。本发明亲水性纳米氧化锌量子点高分辨透射电子显微镜图谱,可观察到量子点清晰地晶格衍射条纹,晶格间距为0.281nm。XRD衍射实验显示本发明亲水性氧化锌量子点为纯六方纤锌矿结构。本发明亲水性氧化锌量子点(ZnO QDs)在深紫外区有宽的吸收,其范围由250nm至380nm,其最佳激发波长为365nm;在最佳激发波长下,样品呈现强的宽范围的黄色荧光发射,最强发射峰位于530nm。在日光和365nm的紫外灯辐照下,本发明亲水性氧化锌量子点水分散体澄清透明,表明制备的ZnO QDs具有良好的水溶性,并且在UV光照射下,ZnO QDs表现出强的黄色荧光,同时ZnO QDs的水溶液放置一个月之后其荧光强度并没有发生明显下降,表明ZnO QDs在水溶液中具有良好的胶体性和光学稳定性,未有光漂白和光闪烁现象。由透过率实验及三种溶液肉眼观察可得,亲水性氧化锌量子点比商业纳米氧化锌颗粒水溶性更好,既便于清洗,也更容易后续与其他材料复合。本发明亲水性氧化锌量子点对革兰氏阳性菌和革兰氏阴性菌均有明显的膜破坏性,经0.5g/L的亲水性氧化锌量子点处理后的细胞组有大量红色荧光的死细胞。本发明亲水性氧化锌量子点对金黄色葡萄球菌和大肠杆菌均有明显的破坏性,处理后的细菌细胞壁皱缩,受损严重。本发明亲水性氧化锌量子点对一些食源性病菌体如屎肠球菌、蜡样芽孢杆菌,巨大芽孢杆菌及藤黄微球菌也有明显的抑制作用,抗菌范围较广。本发明亲水性氧化锌量子点的抑菌能力远远强于商业化纳米氧化锌,用0.5g/L的本发明亲水性氧化锌量子点可以抑制细菌生长1.5个滴度,而商业纳米氧化锌抑制细菌生长远不到0.5个滴度,可见本发明亲水性氧化锌量子点的抑菌能力远远强于商业化纳米氧化锌。本发明使用乙酸锌二水、氢氧化钾以及APTES制备具有水溶性的荧光发射的氧化锌量子点,相对于传统制备纳米氧化锌的方法而言,制备过程略去了沉淀ZnO量子点步骤,工艺更简便,适合大规模生产。
附图说明
图1亲水性氧化锌量子点透射电镜图;
图2亲水性氧化锌量子点结构XRD图;
图3亲水性氧化锌量子点动态光散射图;
图4亲水性氧化锌量子点的紫外-可见光吸收光谱图;
图5亲水性氧化锌量子点的激发和发射光谱图;
图6亲水性氧化锌量子点的形貌图;
图7商业纳米氧化锌(棒状)形貌图;
图8商业纳米氧化锌(花状)形貌图;
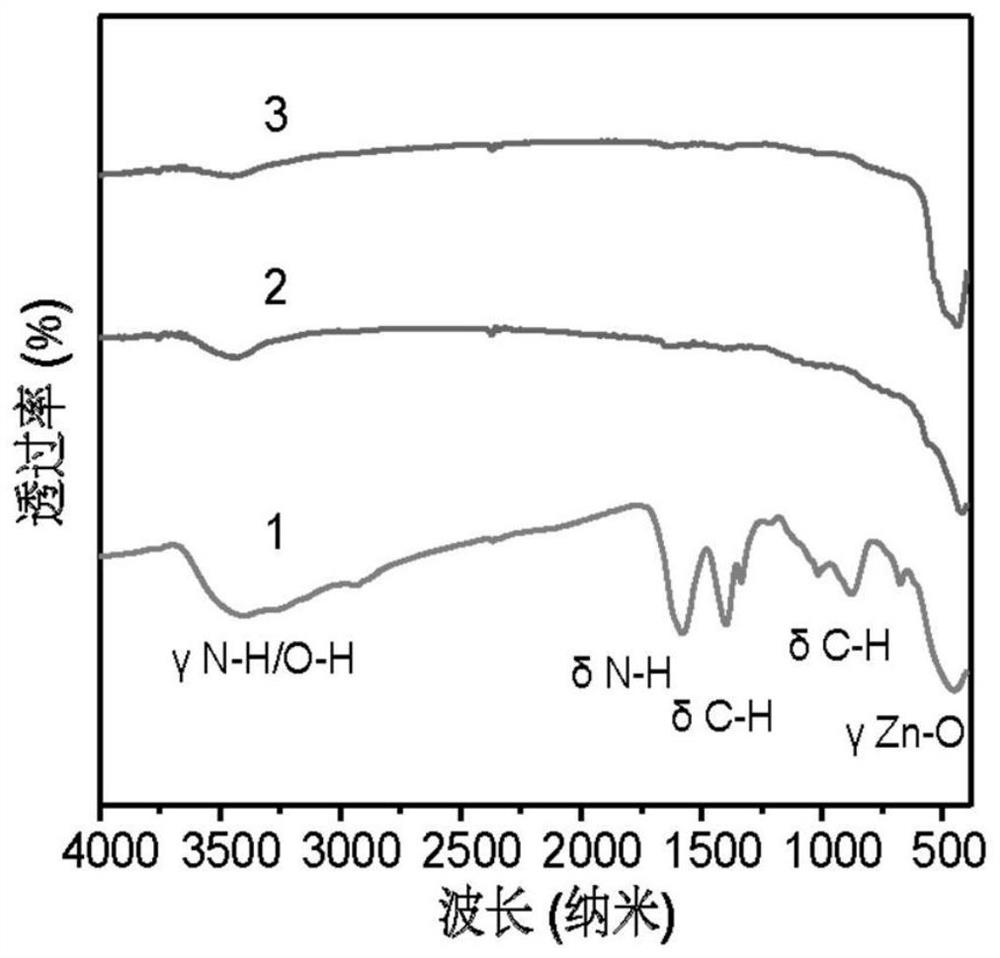
图9亲水性氧化锌量子点与商业纳米氧化锌的傅里叶红外图谱对比图,其中1号样品为本发明所制备的亲水性氧化锌量子点,2号样品为对比所使用的一种商业纳米氧化锌(棒状),3号样为对比所使用的另一种商业纳米氧化锌(花状);
图10亲水性氧化锌量子点与商业纳米氧化锌的透过率对比图,其中1号样品为本发明所制备的亲水性氧化锌量子点,2号样品为对比所使用的一种商业纳米氧化锌(棒状),3号样为对比所使用的另一种商业纳米氧化锌(花状);
图11亲水性氧化锌量子点与商业纳米氧化锌的水溶液图像对比图,1号样品为本发明所制备的亲水性氧化锌量子点,2号样品为对比所使用的一种商业纳米氧化锌(棒状),3号样为对比所使用的另一种商业纳米氧化锌(花状);
图12亲水性氧化锌量子点对金黄色葡萄球菌的杀菌统计结果图;
图13亲水性氧化锌量子点对大肠杆菌的杀菌统计结果图;
图14未经亲水性氧化锌量子点处理的金黄色葡萄球菌的表面形貌图;
图15经过亲水性氧化锌量子点处理30分钟后的金黄色葡萄球菌形貌图;
图16未经亲水性氧化锌量子点处理的大肠杆菌的形貌图;
图17经亲水性氧化锌量子点处理30分钟后的大肠杆菌的形貌图;
图18亲水性氧化锌量子点处理细菌后的红绿死活染色结果图;
图19亲水性氧化锌量子点对屎肠球菌、蜡样芽孢杆菌、巨大芽孢杆菌和藤黄球菌的抑菌效果评价结果图;
图20亲水性氧化锌量子点与另外两种商业纳米氧化锌的抗菌性能对比结果图,其中1号样品为本发明所制备的亲水性氧化锌量子点,2号样品为对比所使用的一种商业纳米氧化锌(棒状),3号样为对比所使用的另一种商业纳米氧化锌(花状);
图21亲水性氧化锌量子点与另外两种商业纳米氧化锌的抗菌性能对比结果图;其中1号样品为本发明所制备的亲水性氧化锌量子点,2号样品为对比所使用的一种商业纳米氧化锌(棒状),3号样为对比所使用的另一种商业纳米氧化锌(花状);
图22屎肠球菌、蜡样芽孢杆菌、巨大芽孢杆菌、藤黄球菌和亲水性氧化锌量子点的表面电位图;
图23亲水性氧化锌量子点水溶液的活性物质以及处理细菌后内源性活性物质的含量测试结果图,其中a为不同浓度氧化锌量子点水溶液中H
具体实施方式
下面通过具体实施例对本发明进行具体描述,在此指出以下实施例只用于对本发明进行进一步说明,不能理解为对本发明保护范围的限制,本领域的技术熟练人员可以根据上述发明内容对本发明作出一些非本质的改进和调整。
原料与试剂
乙酸锌,二水(Zinc aetate dehydrate,Zn(OAc)2·2H2O),3-氨丙基三乙氧基硅烷((3-aminopropyl)triethoxysilane,APTES),氢氧化钾(Europium oxide andpotassiumhydroxide,KOH)购自阿拉丁。对比所使用的商业氧化锌(纳米氧化锌90±10nm,99.8%metals basis)购买自上海麦克林生化科技有限公司。活/死细胞活力试剂盒(L13152)购自美国Invitrogen公司。活性物质检测试剂盒:过氧化氢检测试剂盒(S0038)、二氢乙锭(S0063)、超氧化物检测试剂盒(S0060)购自碧云天生物技术(上海)有限公司。其余实验中所设计到的原料和试剂均购买自麦克林生化科技有限公司。无水乙醇(Absolute ethanol)购自天津永达化学试剂厂。所有试剂均为分析级及以上,未经进一步纯化直接使用。实验室所用水为超纯水(二次蒸馏水经由四川沃特普超纯水机公司生产的超纯水机进行纯化)。实验过程中所用到的常规培养基,试剂缓冲液等参照《分子克隆实验指南第三版译》以及《TaKaRa商品目录》中实验室常规试剂配制方法章节进行配置。
实施例
(一)亲水性氧化锌量子点制备
亲水性氧化锌量子点的合成:取35mM氢氧化钾至于50mL烧杯中,加入20mL无水乙醇搅拌15min直至氢氧化钾完全溶解,放置于4℃下的冰箱中冷藏。将25mM乙酸锌,二水加入盛有150mL无水乙醇的单口烧瓶中,80℃下搅拌回流直至乙酸锌完全溶解(2h左右),随后将混合液置于冰浴中。将氢氧化钾的乙醇溶液逐滴滴加到盛有乙酸锌乙醇溶液的单口烧瓶,并不断搅拌以充分反应30min。此时可观察反应液由澄清变浑浊又逐渐澄清的现象。将反应混合液取出冰浴待其温度回温至室温时,逐滴滴加1.5mL去离子水和500uL3-氨丙基三乙氧基硅烷(APTES)混合溶液,并不断搅拌5h,此时观察溶液由澄清变为乳白色。在6000rmp下离心乳白色浑浊溶液10min,移去上层清液,加入35mL无水乙醇分散并清洗沉淀物,反复上操作两次。将沉淀物置于鼓风干燥箱中60℃下干燥2h,最终得到本发明亲水性氧化锌量子点(ZnO QDs)颗粒(粉末)。
(二)亲水性氧化锌量子点的性质表征
将上述实施例制备的亲水性氧化锌量子点进行性质表征
表征方法
透射电镜(TEM)
透射电子显微镜用来观察亲水性ZnO QDs的形貌大小,将亲水性氧化锌的水溶液,滴在超薄碳膜上,然后烘干,置仪器中观察。仪器型号为JEM-21100(日本),加速电压:200kV,放大倍数:X1000-X100万。
扫描电子显微镜(SEM)
(a)扫描电子显微镜用来观察商业纳米氧化锌的形貌。将商业纳米氧化锌的粉末均匀涂抹在导电胶上,然后置于铜台上,表面喷金60秒,然后置于扫描电子显微镜中观察。仪器型号为JSM-6700F,加速电压:0.5-30kV,放大倍数:X100-X65万。
(b)0SEM用来观察细菌受损前后的表面状态。将氧化锌-细菌溶液培养30min后,5000rpm离心5min,用2.5%戊二醛在4℃/8h。PBS缓冲液洗涤3次后,分别用20%、40%、60%、80%、100%乙醇依次处理30min,脱水,然后按照(a)中同样操作,制备样品,进行观察。
X射线衍射仪
样品的晶体结构采用日本Rigaku D/MAX-3B型X射线衍射仪(XRD)来表征,工作时所用X射线为铜的Kα射线,其波长是
马尔文激光粒度仪
样品测试在水溶液中的分散粒径由ZetasizerNano系列ZEN5600型激光粒度仪进行测试,其原理为动态光散射。
傅里叶红外光谱仪(FTIR)
傅里叶红外光谱用来分析两种氧化锌的表面基团,仪器型号为:Nicolet iSl0型(美国赛默飞世尔科技公司),测试范围为4000-400cm
紫外可见吸收光谱
吸收光谱用来分析两种氧化锌水溶液的透过率以及相应的吸收特性。以去离子水作为背景基线,测透过时,纯水透过率为100%;测吸收时,纯水吸收系数为0。将两种氧化锌配置成等同浓度的水溶液,每次取2ml置于1cm厚的石英槽中测试即可。仪器型号为:UH-450,透过率范围400-800nm,吸收范围设置为340nm-800nm。
表征结果
如图1所示,在透射电镜下观察到本发明亲水性氧化锌量子点呈球状,大小均匀,分散良好,无团聚现象,平均颗粒粒径小于5nm。图1的插图处为单个ZnO QDs的高倍透射电子显微镜图谱,可观察到ZnO QDs清晰地晶格衍射条纹,晶格间距为0.281nm。本发明亲水性氧化锌量子点XRD图谱如图2所示,XRD衍射实验显示其为纯六方纤锌矿结构,同时XRD图谱显示所有衍射峰无明显偏移且没有出现其他结晶杂质衍射峰,表明实验过程未有其他副产物的生成。本发明亲水性氧化锌量子点动态光散射图谱(图3)中展示10nm粒径处出现一个峰,进一步验证了ZnO QDs在水中分散良好未发生团聚现象,该结果与透射电镜结果符合良好。
图4为ZnO QDs的紫外-可见光吸收光谱,由图4可知ZnO QDs在深紫外区有宽的吸收,其范围由250nm至380nm,其最佳激发波长为365nm。图5为ZnO QDs的激发和发射光谱,图5中虚线展示ZnO QDs具有宽的激发带,其范围由250nm至380nm,其最佳激发波长为365nm。此实验结果与ZnO QDs的紫外-可见光吸收光谱相吻合。在最佳激发波长下,该样品呈现强的宽范围的黄色荧光发射,最强发射峰位于530nm(实线)其可归因于氧化锌量子点的表面缺陷引起的荧光发射。
本发明亲水性氧化锌量子点与商业纳米氧化锌颗粒的性质对比
如图6所示,在透射电镜下观察到亲水性氧化锌量子点呈球状,大小均匀,分散良好,无团聚现象。而商业纳米氧化锌颗粒呈现出棒状或者花状(图7及8),分布不均匀,团聚现象随处可见。亲水性氧化锌量子点的XRD衍射结果显示其为纯六方纤锌矿结构,此结构最为稳定,属于六方晶系,为六方最紧密堆积。这种纯六方纤锌结构就决定了纳米氧化锌的稳定性及安全性。
图9为ZnO QDs的FTIR光谱,由图9可知在3425cm
图10是本发明亲水性氧化锌量子点与商业纳米氧化锌的透过率对比图,图11是本发明亲水性氧化锌量子点与商业纳米氧化锌的水溶液图像对比图。从图10和图11来看,本发明ZnO QDs的水溶液分别在日光(左)和365nm的紫外灯(右)辐照下的数码照片,日光下ZnO QDs的水分散体是澄清透明的,此结果表明制备的ZnO QDs具有良好的水溶性,并且在UV光照射下,ZnO QDs表现出强的黄色荧光;同时ZnO QDs的水溶液放置一个月之后其荧光强度并没有发生明显下降(实线),表明ZnO QDs在水溶液中具有良好的胶体性和光学稳定性,未有光漂白和光闪烁现象。从图10透过率实验和图11三种溶液肉眼观察可得,亲水性氧化锌量子点比商业纳米氧化锌颗粒水溶性更好,既便于清洗,也更容易后续与其他材料复合。在最佳激发波长365nm下,亲水性氧化锌量子点溶液呈现强的宽范围的黄色荧光发射,而商业化纳米氧化锌溶液呈现蓝紫色荧光发射。
(三)亲水性氧化锌量子点的抗菌实验
将上述实施例制备的亲水性氧化锌量子点进行抗菌实验,包括革兰氏阳性菌和革兰氏阴性菌的抗菌实验。
细菌培养
培养金黄色葡萄球菌S.aureus(CGMCC 1.2465)和大肠杆菌E.coil(CVCC216)时,分别取S.aureus和E.coil的单菌落于20ml的LB培养基中,金葡菌条件为37℃/12h,然后转接1次(1ml于20ml LB培养基之中),继续培养3h,得到浓度为10
氧化锌对细菌的灭活操作
本发明亲水性氧化锌量子点和商业纳米氧化锌对细菌灭活的操作相同,具体细节如下:
(a)分别配制不同浓度的氧化锌水溶液,体积为10ml,浓度依次为0.001、0.01、0.1、0.5和1mg/ml。
(b)同时将上述两种浓度为10
(c)去除上清液,收集沉淀,依次与10ml的不同的浓度的氧化锌溶液互相混合,此时细菌浓度为10
(d)将(c)中的最后的悬浮液,依次取100ul加入到900ul的去离子水中,梯度稀释,然后采用稀释平板法,均匀涂板,置于鼓风干燥箱,在条件37℃下培养12h后计数。
红绿死活染色法检测亲水性氧化锌量子点对细菌的作用
(a)采用BestBio细胞染色试剂盒,用0.5g/L亲水性ZnO分别处理革兰氏阳性菌和阴性菌30min,根据样品数按说明书比例配置染色工作液。
(b)收集样本细胞,细胞数量在1X106以内。用PBS洗涤细胞两次。
(c)用200ul染色工作液将细胞重悬。
(d)4℃避光孵育15-30分钟后,PBS洗涤。
(e)用PBS洗涤细胞后重悬后用荧光显微镜观察。
氧化锌量子点的活性氧检测
配置不同浓度的亲水性氧化锌量子点溶液(0.4mg/mL,0.8mg/mL,1.2mg/mL,1.6mg/mL,2.0mg/mL),分别作用于蜡样芽孢杆菌、大地懒杆菌和屎肠球细杆菌,然后收集细菌悬液,设定空白对照孔,约按5-10万个细胞/毫升的比例加入96孔板之后用超氧化物检测工作液悬浮细胞,37℃孵育3分钟。接着依次加入过氧化氢检测试剂(S0038)、二氢乙锭(S0063)和超氧化物检测试剂(S0060),在450nm测定吸光度得到检测数值。
数据分析
数据表示为平均标准差(n=3、6或8)。统计分析采用GraphPad Prism 5.0软件。p<0.05被认为具有统计学意义。
抗菌结果
将亲水性氧化锌量子点分别配制不同浓度的氧化锌水溶液,体积为10ml,浓度依次为0.001、0.01、0.1、0.5和1mg/ml。分别作用于细菌浓度为10
未经氧化锌量子点处理的金黄色葡萄球菌的表面形貌照片如图14所示;经过氧化锌量子点处理30分钟后的金黄色葡萄球菌形貌照片如图15所示;未经氧化锌量子点处理的大肠杆菌的形貌照片如图16所示;经氧化锌量子点处理30分钟后的大肠杆菌的形貌照片如图17所示。对比图14-17,在电镜下可明显观察到亲水性氧化锌量子点对金黄色葡萄球菌和大肠杆菌均有明显的破坏性,处理后的细菌细胞壁皱缩,受损严重。
图18为亲水性氧化锌量子点处理细菌后的红绿死活染色结果。红绿死活染色法也显示亲水性氧化锌量子点处理之前的对照组有大量绿色荧光的活细胞,而经0.5g/L的亲水性氧化锌量子点处理后的细胞组有大量红色荧光的死细胞。证明亲水性氧化锌量子点对革兰氏阳性菌和阴性菌均有明显的膜破坏性。
分别用0.1g/L、0.3g/L、0.5g/L、1.0.g/L及2.0g/L的亲水性氧化锌量子点作用于屎肠球菌、蜡样芽孢杆菌,巨大芽孢杆菌及藤黄微球菌,在48h后检测细菌相对数量,检测结果如图19所示,说明ZnO QDs对一些食源性病菌体也有明显的抑制作用,表现出较广的抗菌范围和较长的抗菌时间。
亲水性氧化锌量子点与商业纳米氧化锌的抗菌对比
将亲水性氧化锌量子点分别配制不同浓度的氧化锌水溶液,体积为10ml,浓度依次为0.001、0.01、0.1、0.5和1mg/ml。分别作用于细菌浓度为10
亲水性氧化锌量子点的抗菌机理
屎肠球菌、蜡样芽孢杆菌、巨大芽孢杆菌、藤黄球菌和亲水性氧化锌量子点的表面电位如图22所示,亲水性ZnO QDs带正电荷,而细菌带负电荷。将亲水性ZnO QDs作用于蜡样芽孢杆菌、巨大芽孢杆菌和屎肠球细杆菌后,通过活性氧检测试剂检测内源性活性氧的含量,结果如图23所示,发现三种细菌中超氧化物的量几乎全部有两倍甚至两倍以上的增长。因此ZnO QDs对各种细菌的抗菌机理可总结如下:一方面,亲水性ZnO QDs表面带有的基团(正电荷),增加了与细菌的粘附能力,量子点长时间粘附在细菌表面,会对细胞膜造成一定程度的损坏;另一方面可诱导细菌产生过度的氧化应激反应,大量活性物质(包括内源性ROS和外源性ROS)产生造成细菌死亡。
- 一种亲水性氧化锌量子点及其制备方法和用途
- 氧化锌量子点-铌酸钾光催化剂的制备方法及该催化剂的用途
