体外生命支持系统
文献发布时间:2023-06-19 11:00:24
本申请是国家知识产权局专利局给出的国家申请号为201780030051.0,申请日为2017年7月12日,发明名称为“体外生命支持系统”的专利申请的分案申请。
技术领域
本发明涉及体外生命支持系统,其主要是在静脉-静脉型体外膜氧合(VenovenousExtra-Corporeal Membrane Oxygenation,VV ECMO)系统中使用主动控制的流量调节方法,防止含氧血经由引流导管再循环回到ECMO回路之中。具体地说,本发明是使用心电讯号(ECG)作为主动控制流量调节系统的作动控制时间之参考,经由迟滞或加速导管内流量,来进一步改善再循环现象。目的是要在心脏舒张,三尖瓣打开时让最大量的高含氧血流入右心室;而心脏收缩,三尖瓣关闭时降低ECMO回路中的高含氧血灌注到右心房和腔静脉,但同时能大量地让人体低含氧静脉回血流回到ECMO回路之中。
背景技术
自1992年禽流感大流行后,全世界使用体外膜氧合(ECMO)系统来抢救严重的呼吸系统疾病,如急性呼吸窘迫症候群(Acute Respiratory Distress Symdrome,ARDS),其使用量是逐步地升高。目前,约有40%的ECMO年使用量是与治疗急性呼吸窘迫症候群或其他严重的呼吸道疾病相关,其中插管方法和设计对于如何有效地治疗肺部疾病至关重要。
ECMO通常分为静脉-动脉型ECMO(VA ECMO)和静脉-静脉型ECMO(VV ECMO)两类的插管型式。临床上VA ECMO多用于治疗心衰竭患者,而VV ECMO则用于治疗呼吸衰竭患者。VVECMO的体外肺循环回路源自于使用单腔室导管于双部位进行插管的方式,其中最常见为分别于下腔静脉(Inferior Vena Cava,IVC)中插入引流导管,上腔静脉(Superior VenaCava,SVC)中插入灌流导管。这种最常见的VV ECMO型式,其引流导管由鼠蹊处插入再向前推入到下腔静脉,而灌流导管则是由颈静脉插入后再向前推入到上腔静脉,最后这两处的导管会在右心房(Right Atrium,RA)区域附近相汇聚。由于引流导管和灌流导管两者的尖端相距的位置很接近,因此会有相当一部份的灌流导管内的高含氧血会被吸入到引流导管内而不是进入右心房,产生一种称为“再循环”(Recirculation)的现象,而损及VV ECMO的救治功效。通常随着ECMO流量增加,再循环率也会增加,尤其是当严重损伤的肺需要较大的ECMO灌流量辅助时。当再循环发生时,VV ECMO的功效不仅会受到影响,也会使得血液于ECMO回路中停留时间延长,引起更多因血球细胞损伤所产生的并发症,这是临床上非常不乐见的情况。例如,当血球细胞在ECMO回路中再循环更长的时间,就会造成更多的血球细胞被裂解,特别是发生在氧合器(Oxygenator)的狭窄纤维通道中,引发出血或血栓栓塞的并发症,导致需要使用更高剂量的肝素抗凝血剂。
目前已有一些降低VV ECMO再循环率的解决方案被提出,实际执行上着重于改进导管设计和相关插管方法。结合不同型式的导管设计和插管方法,VV ECMO临床上有四种插管型式:1)使用单腔室导管于双部位进行插管,2)使用双腔室导管于单一部位进行插管,3)使用双腔室导管于双部位进行插管,4)使用单腔室导管于三部位进行插管。近年来,双腔室导管于单一部位进行插管的型式可经由核准市售的Avalon导管而得以实现,并且因为此导管可以降低再循环率,以及能够提供患者更好的活动能力来帮助肺脏能更快复原的优点,而逐渐在欧美地区获得普及。
上述的所有插管型式都是采用被动式而无主动式调控组件的设计概念来降低再循环率。值得注意的是,右心室仅在心脏舒张且三尖瓣打开时,才能接受含氧血的灌注。当在心脏收缩而三尖瓣关闭时,无论灌流导管的尖端是如何放置在靠近三尖瓣的入口附近,所灌注的含氧血也无法进入到右心室,这是限制所有被动式导管的性能上限的根本原因。在发明人的实验室中,已发展出特别设计的肺循环仿生生理测试平台,可测定VV ECMO的再循环率。实验发现当ECMO流量为每分钟3.5升的情况下,传统上使用单腔室导管于双部位插管的型式,再循环率可高至40~50%范围,而使用Avalon双腔室导管于单一部位插管的型式,再循环率则约为20~25%。因此,设计上仍然有相当大的空间可以来进一步改善,使患者可以获得更佳的肺部VV ECMO治疗。
装置ECMO的患者通常是被镇静和卧床在加护病房(ICU)中,虽然使用双腔室导管于单一部位插管的型式的优点是病患可以走动而加快复元的时间,但在实际临床应用中却是难以实现此优点。事实上,全世界绝大多数的加护病房中,加护病房内的护理人员和工作人员的人力,无法允许ECMO患者下床并常规且安全地在加护病房周围的走廊走动。
通常ECMO导管的管径大多会有所限制,因为管径过大的导管难以插入血管之中,也可能在血管内的操作而造成血管的损伤,以及导管移除后发生血管腔室会变狭窄的并发症。灌流通道和引流通道同时存在的双腔室导管在本质上其流道管径会小于单腔室导管的流道管径,不可避免地会有更高的流阻和壁面剪应力会存在于双腔室导管之中,因此当血流由双腔室导管较狭窄的引流通道流出再流入到较狭窄的灌流通道中会造成更多血球细胞的伤害。事实上,ECMO流量在双腔室导管中会因高流阻而受到限制,这对于迫切需要较大ECMO流量辅助的严重呼吸衰竭患者来说是不理想的。
发明内容
本发明采用特别设计的双腔室导管双部位插管的型式,使用心电讯号作为改善再循环之控制系统依据来进一步减少再循环率,并将在后续作说明。首先须特别注意到本发明与前述定义导管腔室的分类有所不同,在本发明中的双腔室是定义为由空气流道和血液流道组成的管状整体,其中血液流道的横截面远比空气流道的横截面为大。实际上来说,本发明的双腔室导管的血流阻抗与前述的单腔式导管相当,因此,就血流动力学上来说可以得到较高的血流量辅助及较小流动阻力的双重优点。由于导管中采用较大的血流通道,大大地减少管状流动的剪应力,造成较少的血球细胞损伤,以及需要更少的肝素和抗凝血的临床管理优点。
依据三尖瓣的开关来调整引流和灌流的流速分布,理论上而言VV ECMO的再循环率可以最小化到现有技术无法实现的程度。本发明人认为,若能进一步降低目前双腔室导管在单一部份插管型式的再循环率,同时又能够在较低血球细胞损伤下扩大ECMO流量的辅助范围,将会是更为理想的治疗方案。若能考虑到与三尖瓣瓣膜运动相关的时间和血液流动特性,VV ECMO辅助功效则可经由安装在导管上的主动控制的致动器作动而进一步改善,让罹病的肺脏可以更充分地休息而获得更快的恢复,大大地减少患者使用ECMO和待在加护病房房的时间,这将会使患者真正地受益。而帮助患者加速肺部恢复的复健治疗,则可以在患者脱离ECMO辅助并移出加护病房后才进行。
本发明涉及一种可以强化静脉-静脉体外膜氧合(VV ECMO)效率的创新设计血流调节系统。这种主动控制的ECMO系统包括引流导管、灌流导管、血泵、氧合器和依心电讯号作控制的气动式驱动器。由腔静脉中将低含氧血引流至ECMO系统的引流导管组件包括有:引流导管(Drainage Cannula)、顺容储血器(Compliant Reservoir)、引流端的闭塞器(Occluder)和第一球囊(First Balloon)。将ECMO的高含氧血灌注到腔静脉或右心房的灌流导管组件包括有:灌流导管(Infusion Cannula)、顺容储血器、灌流端闭塞器和第二气囊(Second Balloon)。这些主动性组件:球囊、闭塞器和被动性组件:顺容储血器,可以全部或部分采用于控制系统设计中,并使用心电讯号作为系统控制逻辑的触发参考,构成具流量调节组件的导管组件。依据三尖瓣的开启和关闭来间歇性地调控闭塞器控制静脉回血和ECMO驱动的引流和灌流,可以达到让最大量的高氧合血灌注到右心室中并随后再流入肺循环中。使用此依心电讯号作调控的VV ECMO可以显着地减少高含氧血回流到ECMO回路中的再循环现象,减轻病患肺脏的氧合负载。再者,降低血液的再循环现象也会缩短血液在ECMO回路中的滞留时间,有助于减少血球细胞损伤如溶血、血栓,和脑中风的风险。
本发明的引流导管或灌流导管包含有可膨胀的球囊,此球囊可以包覆在导管外表面的一部分,或另外由球囊导管与所述之引流导管或灌流导管相互结合而达成设计的功能需求。球囊材料必须是具耐用性和生物兼容性,并且是由可变形或可延展的弹性体材料制成。当球囊泄气时,球囊收缩成小的轮廓外形,以便减少流动阻抗。当球囊充气时,球囊膨胀而抵住在血管壁或紧邻血管壁,从而阻塞血流通道。此血管内的导管和球囊组件被放置在大的静脉血管内来负责血液的引流或灌流。经由控制导管上球囊的膨胀和收缩,就可调控上腔静脉或下腔静脉的回血回到右心房时被阻塞住的时间区间和回流量。
本发明的导管还可以进一步在导管上加装可调控的阻塞器,而此阻塞器是位于病患的身体之外。阻塞器是用于压缩管流的管道截面积来降低流量的机构,换句话说,它是经由增加流动的阻抗来减缓内部管流的流动。或者,可利用内部球囊或可挠性薄膜来提供内部流动的阻抗亦可以视为是广泛型的阻塞器。透过挤压阻塞器来达成不同的阻塞程度、时间点和时间区间,将可以调控导管内的血流通道在整个时间序列中具有全开、部分打开或关闭的时态。因此可以调控将静脉回血被吸入到ECMO入流端的时间区间和流量,以及高含氧血从ECMO出流端流出的时间区间和流量。
顺容储血器的功能类似电路上的电容,是用于储存或送回血液,并且与ECMO的流道路径相互结合和连通,这是为了当回路中的球囊或阻塞器作动时能提供ECMO血泵能稳定且连续地运转。被动式顺容储血器可以使用弹性材料来制造,其功能类似于人体血管的顺容弹性。设计上也可以建构类似容积式泵(Displacement Pump)的主动式顺容储血器,由外部驱动系统来控制顺容储血器的体积变化。顺容储血器可以和流道串联或并联。被动式顺容储血器的优点在于具有简单和流线的流道设计,然而在某些情况下,装置主动式顺容储血器来主动控制流体进出顺容储血器的流体体积则更有助于调节ECMO回路内的流动。
球囊和阻塞器皆是使用心电讯号作为控制触发的参考讯号以激活气囊和闭塞器作动。只要能在操控时间上正确地配合三尖瓣打开和关闭的时间点,则球囊的膨胀和收缩以及阻塞器的打开和闭合,可以分开操控或合并进行操控。这样的操控目的是要在三尖瓣打开之前能在右心房内储存最大量的高含氧血(准备随后在心脏舒张期间填充到右心室),然而在心脏收缩三尖瓣关闭时能让已消耗掉氧气的静脉回血大量地进入到ECMO回路中。此外,顺容储血器是和阻塞器一起作动,其目的是要补偿当阻塞器关闭时ECMO回路内的流动受到阻塞,在下一阶段当阻塞器打开时顺容储血器就像助推器一样可以将储血器内储存且升压的血液再加速推回到ECMO回路之中。本发明使用以心电讯号作为控制参考的VV ECMO主动流控系统,可以在不需要减少ECMO的流量前提下将传统ECMO回路中的再循环率大大降低。
附图说明
本发明的简要说明可以透过附图中所示的实施例来更具体地描述。这些附图仅描绘了本发明的典型实施例,但不被视为限制其使用范围。目前本发明所提及的实施例和最佳模式将使用附图来作描述,其中:
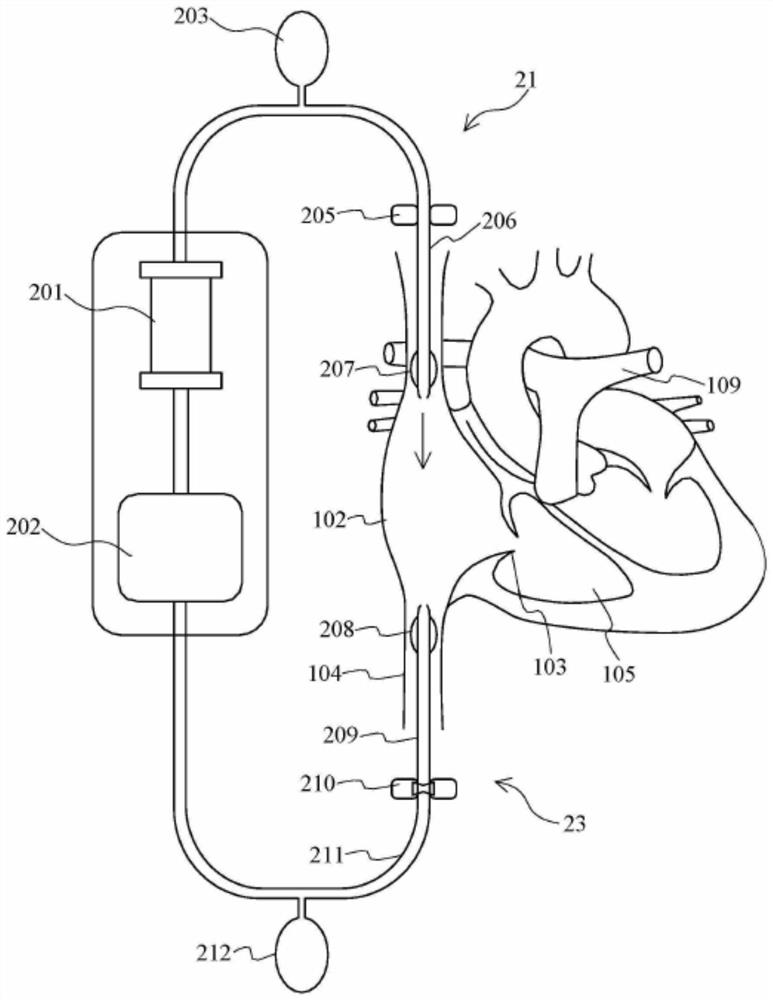
图1是描绘VV ECMO回路和肺循环的示意图。图中呈现出当心脏舒张期三尖瓣打开时六个流量调节器中每一个组件的控制动作特性。
图2是描绘VV ECMO回路和肺循环的示意图。图中呈现出当心脏收缩期三尖瓣闭合时六个流量调节器中每一个组件的控制动作特性。
图3A是本发明的控制流程方块图。
图3B描绘了与每个流量调节器触发的时间点(制动或不制动)。
图4A和4B是根据本发明的实施例1的引流导管组件的侧视图。
图5A和5B是根据本发明的实施例1的引流导管组件纵向剖面视图。
图5C是根据实施例1的引流导管组件的截面视图。
图6是根据本发明的实施例1的引流导管球囊的纵向剖面视图。
图7是描绘实施例1的引流导管放置在下腔静脉和右心房接合处的位置示意图。
图8A和8B是根据本发明的实施例2的引流导管组件的侧视图。
图9A和9B是根据本发明的实施例2的引流导管组件的纵向剖面视图。
图10是根据本发明的实施例2的引流导管球囊的纵向剖面视图。
图11是根据本发明的实施例1的引流导管的引流Y型接头的纵向剖面视图。
图12A是根据本发明的实施例2的引流导管的引流Y型接头的详细图示。
图12B是根据本发明的实施方式2的引流导管的引流Y型接头的分解图。
图13是描绘实施例2引流导管放置在下腔静脉和右心房接合处的位置示意图。
图14A和14B是根据本发明的实施例3的灌流导管组件的侧视图。
图15A和15B是根据本发明的实施例3的灌流导管组件的截面视图。
图16和图17是根据本发明的实施例3的灌流导管阻塞器的剖面视图。
附图标记
21:灌流导管组;23:引流导管组;30:引流导管组;40:引流导管组;50:灌流导管组;101:上腔静脉;102:右心房;103:三尖瓣;104:下腔静脉;105:右心室;109:肺动脉;201:氧合器;202:血泵;203:灌流端储血器;205:灌流端阻塞器;206:灌流导管;207:灌流端球囊;208:引流端球囊;209:引流端球囊;210:引流端阻塞器;211:ECMO引流导管;212:引流端储血器;301:引流导管;302:强化的引流导管管壁;303:引流孔;304:入流斜面;305:密封导管末端;310:空气导管;311:球囊;312:球囊体;313:侧孔;314:辐射线无法穿透的指示物;315:辐射线无法穿透的指示物;316:密封的导管端部;317:锥形延伸部;401:引流导管;402:ECMO管;403:引流孔;404:强化的引流导管管壁;411:内管;412:外管;414:空气导管;415:球囊;416:导管末端;417:球囊体;418:黏着剂;421:辐射线无法穿透的指示物;422:辐射线无法穿透的指示物;423:顶端开孔;424:内管空腔;430:Y型接头;431:Y形接头主体;432:塞子;433:Y狭缝锥形物;434:锁固盖;501:灌流导管;503:侧孔;504:尖端开口;511:ECMO管;520:阻塞器模块;521:转接器;522:储血器;523:阻塞器腔室;524:气体管线;525:阻塞器;526:转接头;527:气体腔室。
具体实施方式
本控制方法的重点是要根据三尖瓣的运动来调控静脉回流和ECMO导管的流量,目的是降低VV ECMO的再循环的缺点。图1和图2分别显示出每个控制组件的位置,及为了降低再循环率而当心脏收缩和舒张时每个控制组件的操作模式。图1和图2是根据本发明的实施例所描绘的VV ECMO回路和肺循环的示意图。体外生命支持系统20是由氧合器201、血泵202、灌流导管组件21和引流导管组件22所组成。氧合器201和血泵202是设置在病患体外。此外,灌流导管组件21是放置在与引流导管组件22相对的位置上。在本发明的一个实施例中,引流导管组件22可以包含有引流端球囊208,或可以加装引流端阻塞器210或引流端顺容储血器212,或者两者都加装。在本发明的其它实施例中,灌流管组件21可以包含有灌流端球囊207,或可以加装灌流端阻塞器205或有灌流端顺容储血器203,或者两者都加装。
在这两张图中,引流导管209被放置在下腔静脉104中,引流端球囊208则被装置在引流导管209上。引流端阻塞器210和顺容储血器212是设置在病患的身体之外,并且连接到ECMO引流导管211。同样地,灌流导管206、灌流端球囊207,亦以类似的方式被放置在上腔静脉中,而灌流端阻塞器205和顺容储血器203则设置在病患的身体之外。须注意到在手术设置中,灌流导管206和引流导管209可以相互交换插管的位置,而与图1和图2中所揭示的插管方式相反。在实际应用中,导管组件21、22可以同样使用本文提供的控制方法和硬件系统来作主动控制。
关于上述流量调节系统的控制动作将在下面作说明:
心脏舒张期:
1.在心脏舒张期间,位在右心房102和右心室105之间的三尖瓣103是开启的。在三尖瓣103打开之前,右心房102应尽可能地多填充含氧血以准备进入右心室105。在三尖瓣103打开时,已经储存在右心房102的含氧血即可大量地流入右心室105并将它填满。依此安排,右心室105可以被灌注最大量的含氧血,并且在随后的心脏收缩时,将含氧血射出到肺动脉109和肺脏之中以完成肺循环。
2.在三尖瓣103打开之前的心脏收缩后期和三尖瓣103打开的下一个心脏舒张期间,球囊207和球囊208充气膨胀以阻止分别从上腔静脉和下腔静脉104回来的静脉回血,从而防止低氧血进入右心房102,同时制动灌流导管206将氧合血灌流到右心房102的空间。
3.将灌流导管组件21的灌流阻塞器205打开以允许来自ECMO流出端的含氧血进入到右心房102。由于血流流动和混合需要时间,因此可提早在三尖瓣103打开之前的一小段时间先将含氧血“灌洗”右心房102。在这个短暂的灌洗期间,两个球囊207和208都是充气膨胀,两个阻塞器205、210都是打开的状态。因此,存储在右心房102中的血液和先前在心脏收缩期被储存在灌流端储血器203中的氧合血会混合并被强制排出,致使含氧血能大量地填充到右心房102中并准备进入到右心室105。
4.将引流导管209上的阻塞器210关闭,防止右心房102中的氧合血被抽进到ECMO的入流路径中。位在ECMO的引流端的阻塞器210在右心房102完成“灌洗”程序后开始关闭,并且在大部分的舒张期都保持关闭,因此可以进一步地减少再循环的氧合血回流到ECMO回路中。
5.当引流端阻塞器210关闭时,此时在上一次心脏收缩期已被动地充满低含氧血或混合血的引流端储血器212会将储存的血液供应到ECMO回路,以维持ECMO血泵可以稳定地连续运转。
心脏收缩期:
1.在心脏收缩期间,位在右心房102和右心室105之间的三尖瓣103是闭合的。在此期间,静脉回血应最大程度地被吸入到ECMO引流回路中,再经由血泵推送通过氧合器来产生含氧血。由于静脉回血在之前的舒张末期受到阻碍而升高下腔静脉的预负荷(Preload,即压力),此预负荷会加速血泵的流量,从而加强了对下腔静脉回血的抽吸,并且在下一个舒张期的初始期间帮助氧合血流入右心房102。
2.在心脏收缩时,两个导管组件21、22的球囊208、207都被泄气收缩起来,因此会产生低压的抽吸力量,有助于静脉回血从上腔静脉和上腔静脉104回流和填充右心房105。
3.灌流导管组件21的阻塞器205关闭以防止ECMO的氧合血进入右心房102。在此ECMO灌流受阻塞的期间,ECMO的氧合血将被分流到灌流端的储血器203中。随着储血器内血液体积的增加,储血器203中的压力将升高而建立相对于灌流导管的压力梯度,当在下一个心脏舒张期阻塞器205打开时,此压力梯度将有助于排出储血器203内储存的血液。
4.将引流导管组件22的阻塞器210打开以接收右心房102中收集的静脉回流血。在血泵202的运转帮助下,吸入到引流导管209的血液将被推送流过氧合器201而产生含氧血液。同时,引流导管组件22的储血器212可在此心脏收缩期再扩张并填充额外的低氧血,随后于下一次心脏舒张期当引流端的阻塞器210关闭时,排出所储存的血液以保持稳定的ECMO流量。
5.为了维持血泵202的连续运转,当在心脏收缩期灌流端阻塞器205关闭时,由ECMO送出的含氧血将被推送到灌流导管组件21中的储血器203中储存并且逐渐升高压力。灌流端储血器203内储存的高压血液将在下一个心脏舒张期当灌流端阻塞器205打开时会以加压的方式被排出。
本发明包括分布在引流导管组件22和灌流导管组件21上的六个流量调节器,以及使用心电讯号作为控制参考的VV ECMO控制系统,其设计目的是要降低再循环率,同时亦能维持血泵稳定地连续运转。例如,流量调节器可以包括两个球囊207、208,两个阻塞器205、210和两个储血器203、212。球囊207、208的使用目的在于调节人体的静脉回流血量,而阻塞器210、205则分别用于阻止ECMO导管内的血液流过引流端和灌流端。储血器212、203分别放置在血泵202之前和氧合器201之后。存储器212、203的控制方式可以是主动的或是被动的,取决于要维持ECMO血泵连续流动的流量设定要求。球囊207、208被放置在上腔静脉或下腔静脉104中,所以是会和血液接触的,设计上应考虑适合血流动力学(Hemodynamics)的构型设计以避免产生血流停滞(Hemostasis)区。阻塞器205、210可以安装在导管206、209的内部或外部,通常偏好采用体外且不会与血液接触的阻塞器设计。本发明须开发使用心电信号作为控制参考讯号的开回路控制器的控制逻辑设计。理论上,目前的主动控制流量调节系统为单输入多输出的控制器,控制目标是要降低VV ECMO系统的再循环率。在实际的设计实现上,前述的六个致动器(流量调节器)可以全部都选用、或部分被选用、或以不同的方式作组合。对于每个流量调节器要相对于心电讯号上的那些时间点来进行制动是须经过调适而设定的。总体而言,对于所选择的流量调节器的所有控制参数须同时进行优化以达成让再循环率降至最低的设计目标。
图3A是本发明的控制流程方块图。心律(通常为心电讯号波形)可以经由数据撷取系统连续撷取得到并经过算法将讯号放大,据以侦测心脏开始收缩的时间点(即R波)。图3B示意性地描绘了每个流量调节器制动的触发时间点(制动或不制动)。在图3B所示时间序列上方波的陡升和陡降分别是代表调节器的制动和关闭。对于每个流量调节器的制动或关闭的时间点都是相对于R波来作触发定时。相对于R波的时间延迟大小则是预先决定的控制输入参数。在这个主动控制系统中最多可有12个控制变量,但要依选用装置在ECMO系统引流和灌流导管组件上的球囊、阻塞器和储血器来作控制组合,才能决定相应于这些流量调节器制动和关闭的控制变量是全部被采用或只部份采用。设计时可以使用仿生循环测试台实验或动物实验的方来进行再循环的测定,经过反复的实验来找出降低再循环率的最佳控制时间点作为控制输入参数,而在本VV ECMO发明中予以实现。
在本发明的一个实施例中,体外流量调节器系统包括气动式泵、可以接收表征心律讯号的感测系统、可以依据所设定的控制逻辑和所感测到的心律讯号产生控制命令的控制器。控制逻辑是经过优化后,可以使心脏舒张期灌注最大量的氧合血以进入右心室中,以及在心脏收缩期抽入最大量的静脉回流缺氧血到ECMO回路中。
实施例1:装配有球囊的引流导管:
图4A和4B是根据本发明的实施例1的引流导管组件的侧视图。图4A是引流导管组件的1:1比例绘图,图4B是图4A的放大图。图4A实施例1,绘出了引流导管组件上装置的球囊和引流侧孔。图5A和5B是根据本发明的实施例1的引流导管组件的纵向剖面视图。图5C是根据实施例1的引流导管组件的截面视图,图中显示出分配给控制用空气通道较小的管腔而分配给血流通道较大的管腔。图6是本发明的实施例1的引流导管的球囊的纵向剖面视图,图中显示出附有球囊、空气孔、血液引流侧孔和辐射无法穿透的显像标记。出现在不同视图中的类似组件在整个说明中都使用相似标注。
引流导管组件30通常包括两个流体通道,一个流体通道能够传送或抽出血液,另一个流体通道连接到引流端球囊311来驱动引流端球囊311膨胀或收缩,例如这两个流体通道可以是引流导管301和引流端空气导管310。引流导管301形成第一管腔,引流端空气导管310形成第二管腔,例如引流空气导管310可以设置在引流导管301内。在至少一个实施例中,引流导管组件30中的引流套管301和引流端空气导管310都有一部分的侧壁会合并成共同侧壁,并由隔膜分隔两者的管腔。引流导管301的下端(或近端)可以方便地使用例如有倒钩的快速接头与ECMO管连接。引流套管301的另一侧的上端(或远程)终止于密封的导管端部316。引流导管301在靠近密封的导管端部316附近在锥形延伸部317的侧壁上安装引流端球囊311。球囊体312与其指定的体外控制器的气体连通是透过引流端空气导管310再进一步地通过锥形延伸部317上钻的侧孔313来达成。引流端空气导管310在远离密封导管端部316的位置处和引流导管组件30分隔开,例如引流导管301和引流端空气导管310设置在有密封导管端部316的引流导管组件30的一端。引流端球囊311和侧孔303设置分布在引流导管组件30的尖端区域。对于引流端空气导管310,其侧孔313是设置在引流端球囊311内部,并且靠近密封导管端部316。引流端空气导管310的分隔接合部会与引流导管组件30穿出患者身体外部的皮肤切口位置分开适当的距离。在本实施例中,合并过渡区被具有较大壁厚的引流导管组件30的分叉结构体加强和保护。
多个开孔或引流孔303沿着引流导管301的长度作配置。引流孔303分布在球囊311下方的区段上。引流孔303数组最好以交错方式来排列,以便能最大量地吸入静脉回流血液。在引流孔数组和分隔转换区之间的导管壁302使用聚合物或金属线进行加强。由于导管端部316被密封,所以引流套管301侧壁上的引流孔303应具有平滑的内部入流斜面304来以密封导管末端305,从而避免在引流孔303周围出现局部血流迟滞区域。
如图6所示,引流端球囊311被安装在连接到引流导管组件30的密封导管端部316的锥形延伸部317外部上。引流端球囊311两侧的指示物314、315与引流导管301相连,是由辐射线无法穿透的材料所制成,并且与引流导管301结合在一起或包埋成一体。球囊可以使用聚合材料来制造,例如硅胶(Silicon)或聚氨酯(Polyurethane),但不限于此。球囊体积312约为3~15毫升,这取决于要插入的血管的尺寸和球囊311被充气以阻止静脉回流血时要达到血管阻塞比。球囊311与指定的控制器的气动连通是经由空气导管310完成,导管一端终止于流量调节器,另一端连接到锥形延伸部317,并根据控制命令而造成减压或压缩空气来回移动使球囊311泄气收缩或充气膨胀。
血液从放置在上腔静脉或下腔静脉中的引流导管301引流而出。如图7所示为目前引流套管放置在下腔静脉104和右心房102的接合处的相对插入位置示意图。
本实施例是图1和图2所示的工作原理的转化应用。须注意到在图1和图2中,血液仅经由球囊311的末梢端部进入到ECMO回路中,而储血器212需要与阻塞器210一起连动地作动来调节ECMO回路内的流动。本实施例中导管具有密封的导管端部316和分布在球囊311附近的引流孔数组303,并且可以省略储血器212、203或省略阻塞器210、205或者两者都省略掉,以简化硬件的设置和控制逻辑的设计。
当引流端球囊311膨胀以阻止从右心房102流出的氧合血或混合血时,密封的导管端316有助于防止氧合血或混合血液被吸入到ECMO回路中,因此可以减少不期望发生的再循环。尽管引流端球囊311膨胀,但在心脏舒张期的静脉回流低含氧血仍可以从多个引流孔303连续地被抽入。因此不存在会中断抽入静脉回流血的时刻,免除需使用储血器的运作来维持不间断的ECMO血泵连续运转。事实上,在本实施例中控制导管来阻塞流动和调节静脉回流是被融合为有密封端的球囊导管的一个机构来控制。当引流端球囊311膨胀时,根据放置引流导管209的位置而将上腔静脉或下腔静脉的静脉回流血经由引流孔303将血引流出来。当引流端球囊311收缩时,上腔静脉和下腔静脉的静脉回流上都可以被抽出到引流导管209中。引流端球囊311还可作为流动的阻流器用来阻止右心房内流动的再循环。伴随引流端球囊311的膨胀,来自于引流端球囊311阻塞产生的流动减速和堵塞所导致的局部高压会将灌入的氧合血流转向到三尖瓣103,若假定球囊扩张时间点是配合右心室肌肉的放松和三尖瓣的开启而适当地控制,该流动方向的改变可造成右心室灌入最大量的氧合血,共同为右心室产生推拉的驱动力以接收来自右心房加速的灌注流。
可以使用普通市售的单腔室灌流导管(没有可动部件或安装流量调节器)与目前的引流导管实施例一起运作,由此组成低再循环率的VV ECMO回路。实际上这种装配就是最简单的主动控制VV ECMO装置。
实施例2:装配非紧密耦合球囊的引流导管:
图8A和8B是根据本发明的实施例2的引流导管组件的侧视图,以显示球囊导管与所插入的单腔室引流导管之间的关系。图8A是引流导管组件的1:1比例绘图,图8B是图8A的放大图。引流导管组件40包括引流导管401、引流端空气导管414和引流端Y型接头430。图9A和9B是根据本发明实施例2的引流导管组件纵向剖面视图,显示出当引流导管组件内部插入引流端空气导管时的内部关系。图9A是引流导管组件的1:1比例绘图,图9B是图9A的放大图。引流导管401与空气导管414及Y型接头430相互结合在一起,在图9A和9B中显示出提供调节静脉回流血的主动控制流量阻塞器是利用球囊415和空气导管414来达成。图10是实施例2的引流导管的气囊纵向剖面视图,图中显示出了球囊、气流孔、血液引流侧孔和辐射线无法穿透的标记。图11是实施例2的引流导管的Y型接头的纵向剖面视图,显示出由Y型接头提供空气导管插入的通路和控制血流停滞区的设计。在图11、12A和12B中详细Y型接头430的构造包含有提供空气导管插入的转接器,让空气导管被送入引流导管中时不会有血液渗漏和空气进入。
引流导管组件40是由生物兼容性的聚合物材料(例如聚氨酯或硅胶,但不限于此)所制成的薄壁管。在本实施例中,导管尖端416是开口的,并且紧邻此导管尖端开口416附近沿着引流导管401的管壁钻有多个引流孔403。这些引流孔403被设计成无论球囊415是否膨胀或收缩都可以最大量地抽入静脉回流血。为了达到手术插入时较少的创伤,因此导管为薄壁且增加埋线加强单元404,让导管插入时可以平滑且无弯折。引流导管组件40的下半部逐渐扩大,目的是要降低流动阻力并且提供结构上的过渡来和Y型接头430作对接。
图9A和9B描绘出引流导管组件40中插入空气导管的情况。空气导管414在插入引流导管之前通常是直的,但是空气导管414可弯曲的特性使空气导管414可顺着插入的路径作弯曲。空气导管414通常可以包括内管411(感测压力)和外管412(输送空气),内管411纵向设置在外管412内。围绕在空气导管414的上端是由诸如聚氨酯或硅胶的聚合物制成的球囊415。球囊415可以由体外的致动器系统来控制其膨胀或收缩。图8A、8B、9A、9B和10所示是完全膨胀的球囊415,其形状是与浸制成形的轴心外形或吹制成形的模具形状一致的。球囊415是无缝地结合或连接到空气导管414上。图10显示了一种较佳的球囊接合方式,管状球囊远侧端部与内管411作无缝黏合,管状球囊近侧端部与外管412作无缝黏合。内管411通常具有大约1mm的外径尺寸。可以注入生理食盐水来填充内管空腔424以形成水压感测通道并延伸到顶端开孔423,以便于在ECMO运作期间测量腔静脉血压。球囊体417和体外控制器之间的气体连通是经由内管411和外管412之间的管腔空间来达成。为了在插入过程中帮助球囊415放置在适当位置,辐射线无法穿透的标记设置在球囊415的近端422和远程421。导管末端416以衬套封装在内管411的远程部位形成平滑轮廓以保护血管不会在推送导管时受到伤害。
如图12A和12B所示,Y型接头430通常包括Y形主体431、Y狭缝的止血锥形物433、塞子432和锁固盖434。Y型接头430的主臂的双侧分别与引流导管401和ECMO管402相互对接在一起,形成抽取下腔静脉或上腔静脉的静脉回流血的引流通道。塞子432设置在Y型接头430的侧臂中与Y狭缝锥形物433一起使用,形成在空气导管414推送和安装时的密封机构。塞子432和Y狭缝锥形物433通常是由诸如硅胶或橡胶这类具弹性可变形的聚合物制成。塞子432的一侧平整安装在引流导管的内壁。通常在空气导管414进入引流导管401并且与血液接触的塞子表面需要构建一个平滑、连续的流动界面,使引流导管和空气导管接口周围的表面不连续处形成血块的可能性降至最低。在塞子432的另一端容纳有Y狭缝锥形物作为止血阀。
要安装空气导管414时,首先将空气导管414插入穿过Y狭缝锥形物433,然后再将空气导管414推过塞子432的通道壁。空气导管414的外壁和塞子432的通道应设计适当的间隙,使得在往前推送空气导管的过程中能保持平滑且不泄漏。如图11所示,锁固盖434是透过螺纹与Y型接头主体431作结合,利用旋转螺纹的圈数,控制锁固盖434施加在Y狭缝锥形物433止血阀上的挤压力量,来提供不同程度的密封效果。在插入空气导管414时,先松开锁固盖434放松空气导管414和球囊415与塞子间的啮合,然后锁上锁固盖来压缩Y狭缝锥形物433来防止从引流导管和空气导管接口边缘间逆流的血液来达成止血的目的。当ECMO血泵运转时,沿着导管会产生负的压力梯度来抽出血液,所以Y型接头430周围的血压通常低于大气压力,因此Y狭缝锥形物433止血阀须提供紧密的密封防止外界空气被吸入血流之中。紧密的密封失败的话会产生危及患者生命的气栓(Air Embolism)。
在本实施例2的实际应用中,插管过程分两步骤完成。第一步是使用针头、导丝、和导引器的工具组来植入引流导管401。该程序与常见的外科医生在临床上执行从上腔静脉或下腔静脉部位插入ECMO系统的单腔室导管做法相同。第二步是要导入空气导管414。空气导管414上的球囊415先泄气收缩成更小的轮廓准备插入通过Y狭缝锥形物433止血阀的入口。首先松开锁固盖434以便接收空气导管414,然后在空气导管414穿过塞子432后再沿着引流导管401往前进,最后球囊415正确放置在导管尖端开口416的外部到达所需位置之后锁紧。可以使用影像系统来进行精确的导引以便完成步骤1和2的放置。图13显示出了本实施例2插入和放置在下腔静脉和右心房接合处的情况。
实施例3:装配有阻塞器的灌流导管:
本实施例3的灌流导管组件50如图14A和14B所示。图14A为灌流导管组件的1:1比例图,图14B是图14A的放大图。图15A和15B是实施例3的灌流导管组件的剖面视图,图中显示出阻塞器、储血器和灌流导管和ECMO管作的结合之间的关系细节。图15A是灌流导管组件的1:1比例绘图,图15B是图15A的放大图。灌流套管组件50包括灌流导管501、阻塞器模块520、气体管线524和ECMO管511,其中阻塞器模块520分别串联接在灌流导管501和ECMO管511之间。阻塞器模块520包括配置在阻塞器腔室523和储血器522中的阻塞器525。在本发明的一个实施例中,阻塞器525连接到灌流导管501,而储血器522连接到ECMO管511。灌流套管501是常见的单腔室导管,如同实施例2中公开的导管。阻塞器(灌流阻塞器)525、205、210和(灌流)储血器522、202、212串联排列以降低流动阻力,其中灌流流量的调控可以经由压缩或扩大阻塞器(灌流阻塞器)525、205、210横截面大小,或以被动式储血器522、203、212随着阻塞器(灌流阻塞器)525、205、210的作动以控制体积来达成,并维持生命支持系统中血泵的连续运转。灌流导管上的尖端开口504和侧孔503用于提供血液的灌注。例如,尖端开口504配置在灌流导管501的一端,侧孔503配置在灌流导管501的侧壁上。目前设计用于阻止灌流导管501中血液流动的阻塞器525是具有分布式壁厚的可挠性导管。当该导管受到空气压缩时,装在阻塞器腔室523中的灌流阻塞器525将被挤压造成横截面面积变小而阻止或减缓灌流血液的流动,同时灌流储血器522将跟着反应而扩张来接收受到阻滞的流量,使ECMO回路内的流动能连续地运行。实际上,本实施例结合阻塞器和储血器功能的操作方式已在图1和图2作了显示和说明。储血器容积是被动地与由体外流量调节系统提供主动的阻塞流量控制一起作反应。
图16和图17显示阻塞器模块的详细结构。图16描绘出在心脏舒张期的阻塞器和储血器操作,其中闭塞器处于完全打开状态而储血器则保持在未扩张拉伸的状态。图17描绘出在心脏收缩期的阻塞器和储血器操作,其中阻塞器处于完全关闭状态,同时储血器被弹性扩张以接收ECMO回路的流量。目前的阻塞堵器次系统通常包括具倒钩的转接头521、阻塞器模块525、气体腔室527以及在具倒钩的转接头526处连接到气体腔室527的气体管线524。阻塞器模块525是经由和体外的流量调节系统作气动连通来进行控制。ECMO管511是经由具倒钩的转接器521连接到阻塞器模块520上。阻塞器模块520的阻塞器525密封结合到气体腔室527的两端。气体腔室结构相对于可挠性管道来说是为刚性的或半刚性的,因此可以随着气体腔室的压力的调节来控制阻塞器525的横截面面积。灌流套管501使用具倒钩的转接头快速地连接到阻塞器的远程523。
本发明上述实施例的体外生命支持系统可以只有包括一个球囊207、208、311、415,一个阻塞器(模块)205、210、525或一个储血器203、212、522。球囊207、208、311、415,或者有阻塞器(模块)205、210、525或者有储血器203、212、522或者两者都有,这些都可以根据患者的心律来致动,使得在心脏舒张期让最多的氧合血进入到右心室内和最多的静脉回流缺氧血在心脏收缩期被抽到生命支持的回路上。
在不脱离本文所公开和解释的基本控制原理的情况下,本发明可以用其他具体形式来实施。在此所描述的实施例是就所有方面上被认为仅是说明性的而不是限制性的。所有与宣告权利具同等的含义和范围的所有变化都被包括在其范围内。
- 用于体外生命支持设备的运送装置和体外生命支持系统
- 用于静脉血引流端封堵的导管组件、能有效减少再循环的引流导管装置及体外生命支持系统
