一类1,3,4-噻二唑类化合物的制备与应用
文献发布时间:2023-06-19 19:30:30
技术领域
本发明涉及有机化学药物合成技术领域,尤其涉及一类1,3,4-噻二唑类化合物的制备与应用。
背景技术
癌症是人类第二大死亡原因,严重威胁人类健康。在2020年全球范围内有1930万癌症新发病例,以及1000万癌症死亡病例,我国癌症现状同样令人担忧。据国家癌症中心在2019年1月发布的最新一期全国癌症统计数据显示,2015年我国癌症发病人数约392.9万,死亡约233.8万人,每年癌症所致的医疗花费超过2200亿。癌症已经成为威胁人类健康的主要公共卫生问题之一,因此,寻找新的抗癌靶标,开发新型抗癌药物成为当务之急,传统的放、化疗方法并不能降低死亡率,延续患者生存时间,而分子靶向治疗将小分子药物定位于肿瘤细胞的靶分子,特异性阻碍肿瘤细胞恶性生物学活动,具有显著的优势和良好的前景,研究发现蛋白酪氨酸磷酸酶SHP2与肿瘤细胞恶性生物学活动密切相关。
SHP2是蛋白酪氨酸磷酸酶(PTP)家族的重要成员之一,参与了发育、新陈代谢、免疫反应以及肿瘤发生等重要的生理病理过程,大量的临床和基础研究显示,在努南综合征、黑色素瘤、白血病和实体瘤等多种疾病中存在SHP2的过表达或激活突变。SHP2是由PTPN11基因编码的蛋白酪氨酸磷酸酶,它的结构由两个SH2结构域(N-SH2和C-SH2)、一个PTP催化活性区域和一个具有至少两个磷酸化位点的C-末端尾部组成,SHP2广泛表达于各组织、细胞的胞浆蛋白,不仅在受体或胞浆酪氨酸蛋白激酶介导的信号途径中起促进作用,还具有磷酸酶非依赖性接头蛋白功能,是第一个被定义为原癌基因的酪氨酸磷酸酶。
目前,虽然SHP2作为抗肿瘤靶点已被广泛报道,但是目前并没有SHP2抑制剂小分子药物上市。而且报道的SHP2抑制剂多带有磺酸、磷酸、羧酸等,在生理条件下以负离子形式存在的极性基团,导致膜通透性差,最终出现生物利用度差的现象,此外,SHP2与其它PTPs家族在催化位点内的高蛋白质序列同源性(尤其是SHP2和SHP1在催化结构域具有75%的序列相似性),对实现磷酸酶之间的选择性提出巨大挑战。
因此,开发对蛋白酪氨酸磷酸酶SHP2有较高的选择性抑制作用,并表现出良好的抗肿瘤效果,成为一个需要突破的技术难题。
综上可知,现有技术在实际使用上显然存在不便与缺陷,所以有必要加以改进。
发明内容
针对上述的缺陷,本发明的目的在于提供一类1,3,4-噻二唑类化合物的制备与应用,其对蛋白酪氨酸磷酸酶SHP2有较好的抑制作用,可以抑制MV4-11白血病细胞的增殖,具有良好的抗肿瘤效果。
为了实现上述目的,本发明提供一类1,3,4-噻二唑类化合物,所述1,3,4-噻二唑类化合物的结构通式如下所示:
根据本发明的1,3,4-噻二唑类化合物,所述NR
根据本发明的1,3,4-噻二唑类化合物,所述基团NR
本发明还提供一种1,3,4-噻二唑类化合物的制备方法,包括如下步骤:
A、将噻二唑类化合物与胺类化合物通过亲核取代,得到中间体。
B、将所述中间体与硫醇类化合物进行亲核取代反应,得到目标化合物。
根据本发明的1,3,4-噻二唑类化合物的制备方法,所述目标化合物为以下化合物中的任意一种:
本发明还提供一种1,3,4-噻二唑类化合物在抑制蛋白酪氨酸磷酸酶SHP2的活性以及抑制癌细胞的增殖的应用。
本发明的目的在于提供一类1,3,4-噻二唑类化合物的制备与应用,利用噻二唑类化合物与胺类化合物通过亲核取代得到中间体,将中间体与硫醇类化合物通过亲核取代反应即可得到目标化合物;一类1,3,4-噻二唑类化合物对蛋白酪氨酸磷酸酶SHP2有较好的抑制作用,可以抑制MV4-11白血病细胞的增殖。综上所述,本发明的有益效果是:对蛋白酪氨酸磷酸酶SHP2有较好的抑制作用,可以抑制MV4-11白血病细胞的增殖,具有良好的抗肿瘤效果。
附图说明
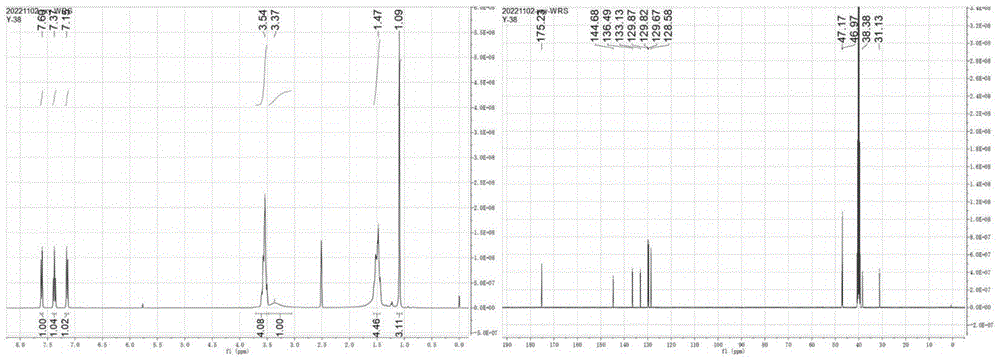
图1为化合物SHP2-01的核磁共振氢谱图和碳谱图;
图2为化合物SHP2-02的核磁共振氢谱图和碳谱图;
图3为化合物SHP2-03的核磁共振氢谱图和碳谱图;
图4为化合物SHP2-04的核磁共振氢谱图和碳谱图;
图5为化合物SHP2-05的核磁共振氢谱图和碳谱图;
图6为化合物SHP2-06的核磁共振氢谱图和碳谱图;
图7为化合物SHP2-07的核磁共振氢谱图和碳谱图;
图8为化合物SHP2-08的核磁共振氢谱图和碳谱图;
图9为化合物SHP2-09的核磁共振氢谱图和碳谱图;
图10为化合物SHP2-10的核磁共振氢谱图和碳谱图;
图11为化合物SHP2-11的核磁共振氢谱图和碳谱图;
图12为化合物SHP2-12的核磁共振氢谱图和碳谱图;
图13为化合物SHP2-13的核磁共振氢谱图和碳谱图;
图14为化合物SHP2-14的核磁共振氢谱图和碳谱图;
图15为化合物SHP2-15的核磁共振氢谱图和碳谱图;
图16为化合物SHP2-16的核磁共振氢谱图和碳谱图;
图17为化合物SHP2-17的核磁共振氢谱图和碳谱图;
图18为化合物SHP2-18的核磁共振氢谱图和碳谱图;
图19为化合物SHP2-19的核磁共振氢谱图和碳谱图;
图20为化合物SHP2-20的核磁共振氢谱图和碳谱图;
图21为化合物SHP2-21的核磁共振氢谱图和碳谱图;
图22为化合物SHP2-22的核磁共振氢谱图和碳谱图;
图23为化合物SHP2-23的核磁共振氢谱图和碳谱图。
具体实施方式
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合附图,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
参见图1,本发明提供了一类1,3,4-噻二唑类化合物,其结构通式(记为结构通式Ⅰ)如下:
其中,NR
上述结构通式Ⅰ化合物或其药学上可接受的盐(结构通式Ⅰ化合物与无机酸或有机酸生成的药学上可接受的盐)所代表的化合物如下:
本发明还提供一种制备上述一类1,3,4-噻二唑类化合物的方法,包括如下合成路线:
2,5-二溴-1,3,4-噻二唑与胺类化合物通过亲核取代得到中间体A-2;中间体A-2与硫醇类化合物通过亲核取代反应得到目标化合物A-3。
基于上述合成路线,化合物SHP2-01的制备方法:
/>
步骤一化合物A-2-1的制备
在500mL圆底烧瓶中加入化合物2,5-二溴-1,3,4-噻二唑(A-1,5~7g,24~25mmol),(4-甲基哌啶-4-基)氨基甲酸叔丁酯(8~9g,39~40mmol),碳酸钾(10~11g,74~75mmol),加入200mL 1,4-二氧六环,加热回流2小时,TLC显示反应完毕时,得到第一混合物。
将在真空条件下除去第一混合物中的溶剂,再用二氯甲烷(50mL×3)萃取,用饱和食盐水(50mL×3)进行洗涤,合并有机相,得到第二混合物;将第二混合物用无水硫酸钠干燥,干燥后的有机相通过旋转蒸发仪除去溶剂,得到的第三混合物;将第三混合物通过甲醇重结晶,得到产物A-2-1,8~9g,产率92~93%。
步骤二化合物A-3-1的制备
在250mL圆底烧瓶中加入化合物A-2-1(0.2~0.4g,0.7~0.9mmol),2,3-二氯硫醇(0.2~0.3g,1~2mmol),碘化亚铜(0.02~0.04g,0.1~0.2mmol),1,10-邻菲罗啉(0.02~0.03g,0.1~0.2mmol),碳酸钾(0.3~0.4g,2~3mmol),加入28~32mL1.4-二氧六环,加热回流3小时,TLC监测反应完毕时,得到第一反应物,将第一反应物通过旋转蒸发仪除去反应瓶中的有机溶剂,用二氯甲烷(20mL×3)萃取,用5%食盐水(20mL×3)洗涤,合并有机相,得到第二反应物,将第二反应物用无水硫酸钠干燥,将干燥后的有机相通过旋转蒸发仪除去溶剂,第三反应物,通过柱层析纯化,得到产物A-3-1,0.3~0.4g,产率90~91%。
步骤三化合物SHP2-01的制备
在50mL圆底烧瓶中加入化合物A-3-1(0.2~0.4g),加入11~13mL二氯甲烷,3~5mL三氟乙酸,常温搅拌0.5小时,TLC监测反应完毕,在真空条件下减压除去溶剂,得到第一产物,在第一产物中加入10mL乙酸乙酯和10mL水,进行稀释,分离各相后,在水相中加入乙酸乙酯(5mL×2),并通过碳酸钠碱化至pH 8~10,最后用乙酸乙酯(20mL×3)进行萃取,合并有机相记为第二产物,将第二产物用无水硫酸钠干燥,干燥后的有机相通过旋转蒸发仪除去溶剂,得到第三产物,将第三产物通过柱层析纯化,得到化合物SHP2-01,0.2~0.3g,产率88~89%。
因为化合物SHP2-02~SHP2-23的合成路线与化合物1相同,所以化合物SHP2-02~SHP2-23的制备方法参照化合物SHP2-01的制备方法即可。
参见图1~图23,得出表1中的化合物的核磁共振氢谱和碳谱数据:
表1化合物SHP2-01~SHP2-23的核磁共振氢谱和碳谱数据
/>
/>
/>
/>
通过表1的核磁共振氢谱和碳谱数据可确定化合物SHP2-01~SHP2-23的结构。
为了验证本发明制备的一类1,3,4-噻二唑母核类化合物的药用价值,本发明将制备的一类1,3,4-噻二唑母核类化合物进行活性研究,并测定酶抑制活性、细胞增殖活性等指标。
一类2,5-二取代-1,3,4-噻二唑类化合物的活性研究
酶抑制活性:蛋白酪氨酸磷酸酶SHP2的活性测定。将0.5nM全长SHP2磷酸酶和0.5μM的激活肽IRS1稀释在100μL测试缓冲液(60mM HEPES、pH 7.2、75mM NaCl、75mM KCl、1mMEDTA、0.05%P-20、5mM DTT)中,加入测试化合物,使其终浓度为50、10、2、0.4、0.08、0.016、0.0032μM,室温静置40min,加入替代底物DiFMUP(终浓度为50μM),并在25℃下孵育30分钟。荧光信号使用微孔板读取器监测,激发和发射波长分别为355和460nm。活性结果如表2所示。
表2化合物SHP2-01~SHP2-23的对SHP2的酶抑制活性
注:“
细胞增殖活性:将MV4-11白血病细胞系接种于96孔板中,并培养过夜。将不同梯度浓度的待测化合物加入96孔板中孵育48h,化合物终浓度为50、10、2、0.4、0.08、0.016、0.0032μM,每100μL培养基加10μLCCK8溶液,混匀后孵育培养1-4h,读取OD
表3化合物SHP2-01~SHP-23的对MV4-11白血病细胞增殖活性
注:“
由上述化合物SHP01-23的结构和应用可知,一类1,3,4-噻二唑类化合物对蛋白酪氨酸磷酸酶SHP2有较好的抑制作用,可以抑制MV4-11白血病细胞的增殖,具有良好的抗肿瘤效果。
本发明提供了一类1,3,4-噻二唑类化合物的制备与应用,利用噻二唑类化合物与胺类化合物通过亲核取代得到中间体,将中间体与硫醇类化合物通过亲核取代反应即可得到目标化合物;一类1,3,4-噻二唑类化合物对蛋白酪氨酸磷酸酶SHP2有较好的抑制作用,可以抑制MV4-11白血病细胞的增殖。综上所述,本发明的有益效果是:对蛋白酪氨酸磷酸酶SHP2有较好的抑制作用,可以抑制MV4-11白血病细胞的增殖,具有良好的抗肿瘤效果。
当然,本发明还可有其它多种实施例,在不背离本发明精神及其实质的情况下,熟悉本领域的技术人员当可根据本发明作出各种相应的改变和变形,但这些相应的改变和变形都应属于本发明所附的权利要求的保护范围。
