一种用于去除锑(III)的纳米Fe3O4-Cu2O@壳聚糖微球的制备方法
文献发布时间:2023-06-19 19:30:30
技术领域
本发明属于水处理技术领域,尤其涉及一种用于去除锑(III)的纳米Fe
背景技术
水环境中日益严重的锑污染引起人们的广泛重视,尤其是聚酯纤维(涤纶)的印染废水中。含锑化合物作为催化剂在聚酯纤维的生产过程中被封存在纤维中,在后续的生产过程中,如碱减量、染色、印花等工段排放到废水中。吸附法具有适用范围广,成本低,处理效果好,以及吸附剂可以重复使用等优点,是一种良好的锑去除手段。但值得注意的是,锑(III)的毒性是锑(V)的10倍,单纯的吸附无法达到降低毒性的效果。因此,十分有必要开发一类同步吸附-氧化的除锑技术,使得高毒性的锑(III)转化为低毒性的锑(V),并从水中分离去除。
铁氧化物具有优异的锑污染物吸附性能,同时具有价格低廉,环境友好等优点,被认为是一类良好的锑吸附材料。当锑(III)污染物成功被铁氧化物吸附后,可以借助不同的手段,如添加氧化剂、外加电场或者利用光催化等手段,实现锑(III)的氧化脱毒。然而,随着人们对温室效应以及碳排放观念的愈加关注,上述常用的锑(III)氧化手段都伴随着较高的试剂和能量的消耗。另一个关键的问题是,在锑(III)被氧化的过程中所传递的电子并没有被很好的利用,通常需要额外添加电子来加速Fe(III)/Fe(II)循环的效率。
因此,如何提供一种高效吸附-原位氧化的绿色去除锑(III)的方法,在响应低碳经济的同时,实现锑(III)的氧化脱毒和高效去除,并将锑(III)氧化过程中所传递电子的有效利用起来,是本领域亟待解决的问题。
发明内容
有鉴于此,本发明提供了一种用于去除锑(III)的纳米Fe
一种用于去除锑(III)的纳米Fe
优选的是,本发明制备纳米Fe
优选的是,本发明乙酸铜和氯化亚铁的摩尔比为1:(1.5~2.25)。
优选的是,本发明溶解壳聚糖,铁盐和铜盐的溶液为体积比为1%的乙酸-柠檬酸混合溶液,其中柠檬酸的质量百分比为0.2~1%。
优选的是,本发明氢氧化钠-十二烷基硫酸钠的混合溶液中十二烷基硫酸钠的浓度为0.2~0.8mol/L。
优选的是,本发明孵化时间为3~24h。
优选的是,本发明反应条件为室温,磁力搅拌的转速为350r/min,反应时间为180min。
将纳米Fe
本发明所述的纳米Fe
本发明针对同步吸附-氧化去除锑(III)的原理为:溶液中的锑(III)被Fe
有益效果
1、本发明的纳米Fe
2、本发明无需添加氧化剂或其他辅助手段即可实现锑(III)的氧化。本发明中锑(III)的氧化不涉及氧化剂的添加,氧化后的锑(V)依旧可以被Fe
3、本发明制备的的纳米Fe
附图说明
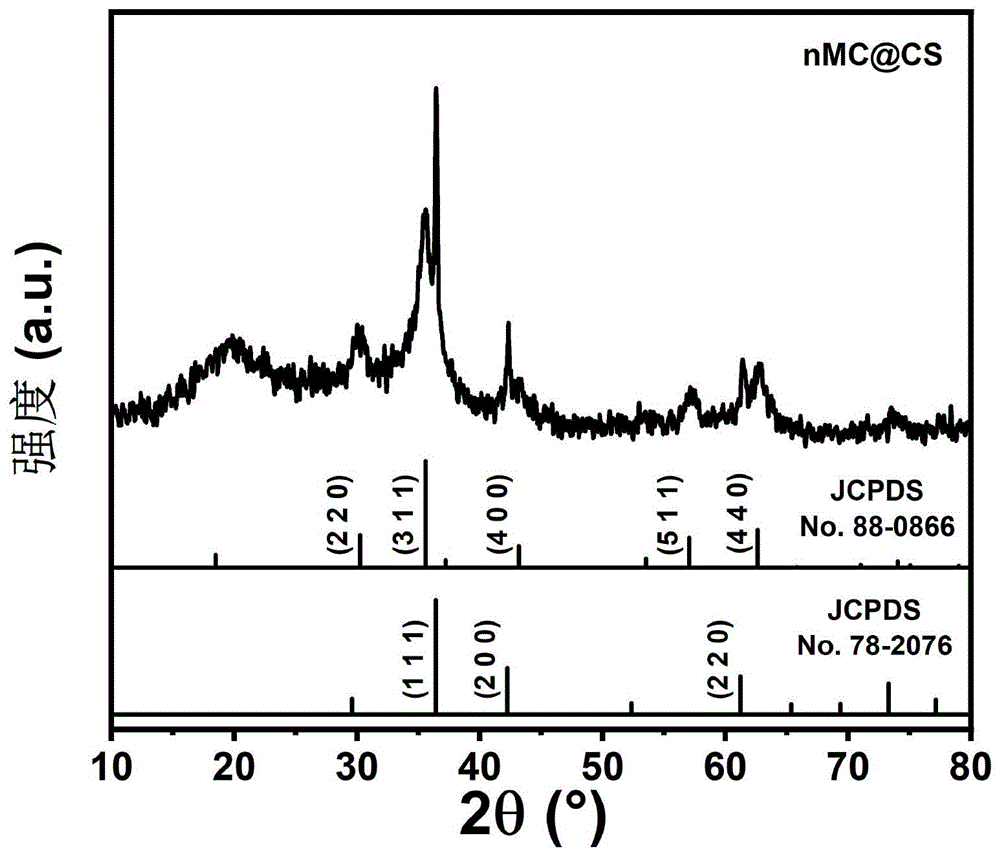
图1为实施例1中所制备纳米Fe
图2为实施例1中所制备纳米Fe
具体实施方式
下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。此外应理解,在阅读了本发明讲授的内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。实施例所用试剂均为分析纯,购买后不经纯化直接使用。
实施例1
在本发明中,所述纳米Fe
图1为制备纳米Fe3O4-Cu2O@壳聚糖微球的XRD图,图2为制备纳米Fe3O4-Cu2O@壳聚糖微球的横截面SEM图。根据数据库比对结果可知,主要成分为四氧化三铁(Fe
实施例2
将实施例1中的壳聚糖改为分子量为1.2×10kDa的壳聚糖,其余均与实施例1相同。
对比例1
将实施例1中的壳聚糖改为分子量为7.6×10
实验以:将实施例1-2,对比例1制备的材料0.1g,加入到50mL、锑(III)浓度为50mg/L的酒石酸锑钾溶液中,在室温下搅拌(350r/min),反应180min,用ICP-AES测定溶液中总锑含量,XAFS分析被吸附锑的价态。
表1
如表1所示,壳聚糖的分子量对总锑去除影响不大,但对被吸附锑(III)的氧化效率影响较大。这可能是因为低分子量的壳聚糖结构中具有更多的还原端羰基、伯、仲-OH和-NH
实施例3
将实施例1中FeCl
实施例4
将实施例1中FeCl
实施例5
将实施例1中FeCl
对比例2
将实施例1中溶解壳聚糖的乙酸-柠檬酸混合液体积改为160mL,其余均与实施例1相同。
对比例3
将实施例1中溶解FeCl
对比例4
将实施例1中溶解乙酸铜的乙酸-柠檬酸混合液体积改为60mL,取消FeCl
将实施例1和实施例3-5,对比例2-4制得的材料进行性能实验。
实验以:将实施例1和实施例3-5,对比例2-4制备的材料0.1g,加入到50mL、锑(III)浓度为50mg/L的酒石酸锑钾溶液中,在室温下搅拌(350r/min),反应180min,用ICP-AES测定溶液中总锑含量,XAFS分析被吸附锑的价态。
表2
如表2所示,前驱体中铜铁的含量是影响总锑去除和被吸附锑(III)氧化效果的主要因素。锑(III)的吸附主要依靠Fe
实施例6
将实施例1中乙酸(1%v/v)-柠檬酸(0.5%w/t)混合溶液改为乙酸(1%v/v)-柠檬酸(1%w/t)混合溶液,其余均与实施例1相同。
对比例5
将实施例1中乙酸(1%v/v)-柠檬酸(0.5%w/t)混合溶液改为乙酸(1%v/v)溶液,其余均与实施例1相同。
实验以:取实施例1和实施例6,对比例5制备的材料0.1g,加入到50mL、锑(III)浓度为50mg/L的酒石酸锑钾溶液中,在室温下搅拌(350r/min),反应180min,用ICP-AES测定溶液中总锑含量,XAFS分析被吸附锑的价态。
表3
如表3所示,前驱体制备时柠檬酸的添加是影响总锑去除和被吸附锑(III)氧化效果的主要因素。当柠檬酸的浓度较高时,前驱体溶液较稀,以此所制备的材料机械强度不高,不利于锑的吸附和氧化。柠檬酸具备一定的还原性,适当的添加有助于保证Fe
实施例7
将实施例1孵化液中十二烷基硫酸钠的浓度改为0.5mol/L,其余均与实施例1相同。
对比例6
将实施例1孵化液中十二烷基硫酸钠的浓度改为1mol/L,其余均与实施例1相同。
对比例7
将实施例1孵化液改为1mol/L的氢氧化钠,其余均与实施例1相同。
实验以:取实施例1和实施例7,对比例6-7制备的材料0.1g,加入到50mL、锑(III)浓度为50mg/L的酒石酸锑钾溶液中,在室温下搅拌(350r/min),反应180min,用ICP-AES测定溶液中总锑含量,XAFS分析被吸附锑的价态。
表4
孵化液中十二烷基硫酸钠的浓度是影响总锑去除和被吸附锑(III)氧化效果的主要因素。当十二烷基硫酸钠浓度过度时,不利于总锑的吸附。十二烷基硫酸钠浓度过高时,对总锑的去除率和被吸附锑的氧化效率都有负面影响。
实施例8
将实施例1中孵化时间改为3h,其余均与实施例1相同。
实施例9
将实施例1中孵化时间改为12h,其余均与实施例1相同。
实施例10
将实施例1中孵化时间改为24h,其余均与实施例1相同。
对比例8
将实施例1中孵化时间改为1h,其余均与实施例1相同。
实验以:取实施例1和实施例8-10,对比例8制备的材料0.1g,加入到50mL、锑(III)浓度为50mg/L的酒石酸锑钾溶液中,在室温下搅拌(350r/min),反应180min,用ICP-AES测定溶液中总锑含量,XAFS分析被吸附锑的价态。
表5
/>
如表5所示,孵化液时间是影响总锑去除和被吸附锑(III)氧化效果的主要因素。孵化时间过短,材料的机械强度较低,可能导致吸附过程中材料发生了解体,影响了锑(III)的吸附和氧化过程。当孵化时间持续增加时,总锑的去除效率和被吸附锑(III)的氧化率并没有持续上升。从环保节能的角度出发,选择合适的孵化时间有助于降低成本,节约能耗。
实施例11
将实施例1中nMC@CS的投加量改为0.15g,其余均与实施例1相同。
实施例12
将实施例1中nMC@CS的投加量改为0.2g,其余均与实施例1相同。
对比例9
将实施例1中nMC@CS的投加量改为0.02g,其余均与实施例1相同。
实验以:将实施例1制备的材料按照不同的投加量加入到50mL、锑(III)浓度为50mg/L的酒石酸锑钾溶液中,在室温下搅拌(350r/min),反应180min,用ICP-AES测定溶液中总锑含量,XAFS分析被吸附锑的价态。
表6
如表6所示,nMC@CS的投加量会影响总锑的去除效率和被吸附锑(III)的氧化率。当nMC@CS投加量过低时,无法有效吸附溶液中的锑(III),导致锑(III)的去除率和氧化率都较低。但当nMC@CS投加量过高时,总锑去除率和被吸附锑(III)的氧化率并没有很明显的提升,从经济和能耗的角度并不合适。
实施例13
将实施例1中初始锑(III)浓度改为1mg/L,其余均与实施例1相同。
实施例14
将实施例1中初始锑(III)浓度改为20mg/L,其余均与实施例1相同。
实施例15
将实施例1中初始锑(III)浓度改为100mg/L,其余均与实施例1相同。
实验以:将实施例1制备的材料0.1g加入到50mL不同锑(III)浓度的酒石酸锑钾溶液中,在室温下搅拌(350r/min),反应180min,用ICP-AES测定溶液中总锑含量,XAFS分析被吸附锑的价态。
表7
如表7所示,所制备材料适用于不同浓度含锑(III)废水的应用,呈现出优异的总锑去除率和被吸附锑(III)的氧化率。
实施例16
将实施例1中模拟含锑废水的初始pH值调为3,其余均与实施例1相同。
实施例17
将实施例1中模拟含锑废水的初始pH值调为7,其余均与实施例1相同。
实施例18
将实施例1中模拟含锑废水的初始pH值调为9,其余均与实施例1相同。
实施例19
将实施例1中模拟含锑废水的初始pH值调为11,其余均与实施例1相同。
实验以:取实施例1制备的材料0.1g,加入到50mL、不同初始pH值、锑(III)浓度为50mg/L的酒石酸锑钾溶液中,在室温下搅拌(350r/min),反应180min,用ICP-AES测定溶液中总锑含量,XAFS分析被吸附锑的价态。根据初始pH值,以0.1mol/L的HCl或0.1mol/L的NaOH调节pH值。
表8
如表8所示,初始pH对nMC@CS对总锑的去除率以及被吸附锑(III)的氧化率影响并不大,这可能归因于铁铜双金属材料具有较宽的pH适用范围。
实施例20
将实施例1中酒石酸锑钾改为三氯化锑配置模拟含锑(III)废水,其余均与实施例1相同。
对比例10
将实施例1中酒石酸锑钾改为焦锑(V)酸钾配置模拟含锑(V)废水,其余均与实施例1相同。
实验以:取实施例1制备的材料0.1g,分别加入到50mL实施例1、实施例20和对比例8配置的模拟含锑废水中,在室温下搅拌(350r/min),反应180min,用ICP-AES测定溶液中总锑含量,XAFS分析被吸附锑的价态。
表9
如表9所示,无论是酒石酸锑钾还是三氯化锑,nMC@CS对总锑的去除率都保持在一个较高的水平,但酒石酸锑钾还有有机配体酒石酸,可能会消耗一部分的活性氧去氧化有机配体,导致三氯化锑的氧化率相较于酒石酸锑钾会稍高一点。可以发现,nMC@CS对锑(V)的去除率明显低于锑(III),使得nMC@CS同步吸附-氧化锑(III)的优点更加突出,吸附耦合氧化除锑(III)技术具有良好的应用前景。
