一种高效二联检测口蹄疫和小反刍兽疫的引物以及试剂盒
文献发布时间:2023-06-19 11:34:14
技术领域
本发明属于基因检测技术领域,具体涉及一种高效二联检测口蹄疫和小反刍兽疫的引物以及试剂盒。
背景技术
口蹄疫(foot-and-mouth disease,FMD),俗名“口疮”、“辟癀”,是由口蹄疫病毒所引起的偶蹄动物的一种急性、热性、高度接触性传染病。主要侵害偶蹄兽,偶见于人和其他动物。症状主要是二至三天后快速下降的高烧;口中的水疱导致粘性或泡沫状唾液的过度分泌并流淌出口外;足部的水泡有可能破裂并导致残废。成年动物感染后可能会伴有数月无法恢复的体重减轻,以及成年雄性动物的睾丸肿胀,对于母牛,牛奶产量会明显减少。虽然大部分动物得病后可自行恢复,但该疾病严重时亦可能导致心肌炎或死亡。
小反刍兽疫(peste des petits ruminants,PPR)俗称羊瘟,是由小反刍兽疫病毒引起的一种急性病毒性传染病。感染动物临诊症状与牛瘟病牛相似。急性型体温可上升至41℃,并持续3~5天。感染动物烦躁不安,背毛无光,口鼻干燥,食欲减退。流黏液脓性鼻漏,呼出恶臭气体。在发热的前4天,口腔黏膜充血,颊黏膜进行性广泛性损害、导致多涎,随后出现坏死性病灶,开始口腔黏膜出现小的粗糙的红色浅表坏死病灶,以后变成粉红色,感染部位包括下唇、下齿龈等处。严重病例可见坏死病灶波及齿垫、腭、颊部及其乳头、舌头等处。后期出现带血水样腹泻,严重脱水,消瘦,随之体温下降。出现咳嗽、呼吸异常。发病率高达100%,在严重暴发时,死亡率为100%。
目前的对上述两种疾病的诊断方法是RT-PCR法。采用现有的PCR技术,由于其反应要在2个不同的温度区循环,对仪器要求高,成本也相对高昂,并且PCR技术仅仅1对扩增引物,易受干扰,特异性相对不足,且出结果时间较久,操作专业要求高,微量加量步骤多。而LAMP技术共有4条不同的特异性引物,故而检测结果准确度更高,但是由于是恒温反应,缺少类似PCR的热启动酶,在设备升温阶段容易产生非特异性扩增从而影响检测结果。
发明内容
本发明所要解决的技术问题是针对现有技术的缺陷提供一种高效二联检测口蹄疫和小反刍兽疫的引物及试剂盒。
本发明解决上述技术问题所采用的技术方案为:一种高效二联检测口蹄疫和小反刍兽疫的引物,具体为:
FMDV-F3:AGGTTTCCACAACTGACACA;
FMDV-B3:GTTAGGACGTGGCTTTCGG;
FMDV-FIP:CGAGCGTGGAGTCAAACACAGT-GTGCAATTTGAAACTCCGCC;
FMDV-BIP:AGCGAGTGCTAGTAGCAGCAC-CGGGTCCTTGTCACCAAG。
PPRV-F3:GGTCTCCTTCCTCCAGCA;
PPRV-B3:GCCTCACGAGGGTTTTGAC;
PPRV-FIP:TCCCTTCCTTCGGACCCATTTG-GGAGAGTCGCCTACACCA;PPRV-BIP:AACACGCTCAGGAAAGCCCAG-TCTCGCGAGAGTTCATCCTC。
本发明还提供一种高效二联检测口蹄疫和小反刍兽疫的试剂盒,所述试剂盒包括上述引物以及反应液,所述反应液的组成为:
所述口蹄疫引物的浓度和体积为:90μM的FMDV-F3引物0.5μL、90μM的FMDV-B3引物0.5μL、180μM的FMDV-FIP引物2μL、180μM的FMDV-BIP引物2μL。所述小反刍兽疫引物的浓度和体积为:90μM的PPRV-F3引物0.5μL、90μM的PPRV-B3引物0.5μL、180μM的PPRV-FIP引物2μL、180μM的PPRV-BIP引物2μL。其中,该试剂盒选用8样本芯片,即1个加样孔对应4个检测孔,第1检测孔位包埋扩增FMDV序列的引物和第2检测孔包埋扩增PPRV序列的引物,第3检测孔是空白,第4检测孔包埋内参引物和内参质粒,如图1,冻干。
所述口蹄疫病毒的核酸序列为M29409.1,小反刍兽疫病毒的核酸序列为HQ197753.1。
与现有技术相比,本发明具有如下优点:本发明以改良后的LAMP技术为基因扩增反应原理,在反应体系里加入金纳米颗粒,吸附ssDNA和蛋白酶,抑制升温过程中的非特异性反应,达到热启动的目的,避免在升温过程中的非特异性反应;结合改良后的LAMP技术与微流控芯片技术,既可以快速、准确的检测区分口蹄疫与小反刍兽疫,同时,反应试剂预埋于微流控芯片上,实现一样双指标检测,又使用户操作简便。
附图说明
图1是8样本芯片测试孔位图。
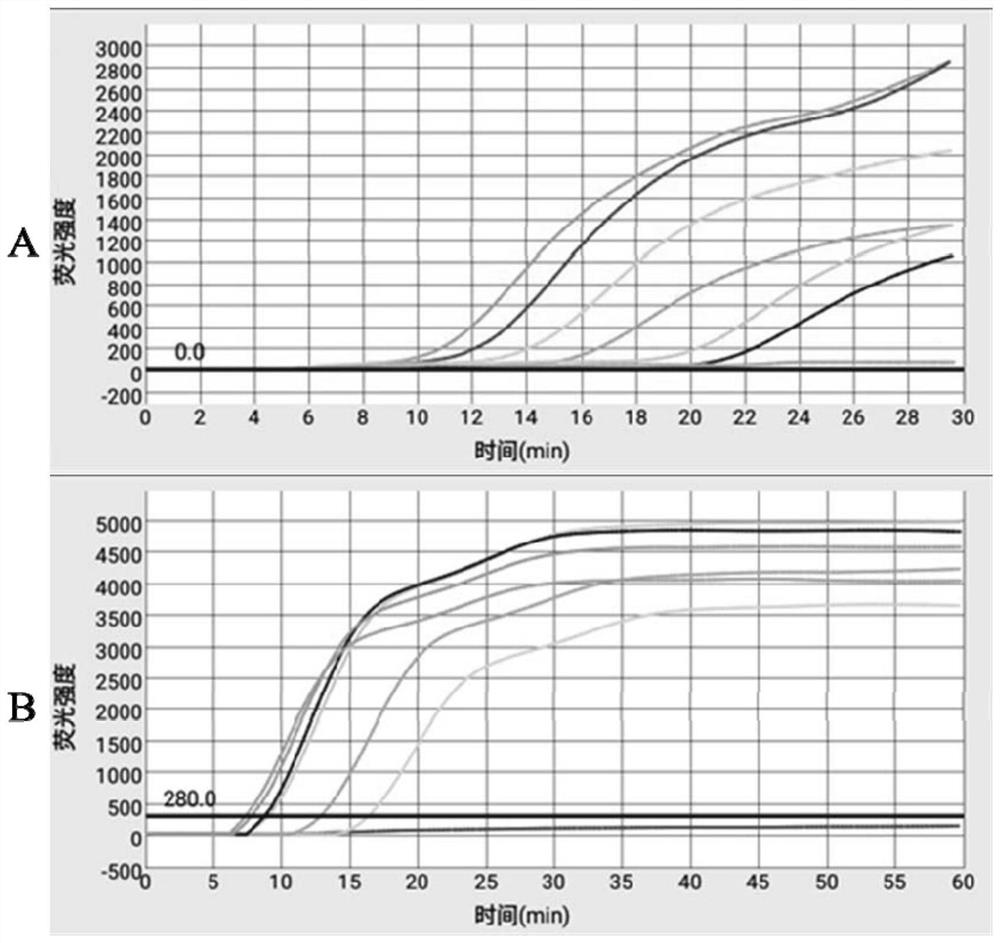
图2是FMDV和PPRV引物敏感性扩增结果图;图中A为FMDV敏感性扩增结果,B为PPRV敏感性扩增结果。
图3是FMDV和PPRV引物重复性扩增图;图中A为FMDV重复性扩增结果,B为PPRV重复性扩增结果。
图4是FMDV和PPRV引物特异性扩增图;图中A为FMDV引物特异性扩增结果;B为PPRV引物特异性扩增结果。
具体实施方式
实施例1
先通过NCBI GenBank寻找目标序列,并针对目标序列设计引物,并将其分别固定在微流控芯片相应位置后对微流控芯片进行封装,与从鼻拭子及其各种脏器、血液、排泄物、环境样本和细胞培养物中提取的核酸模板混合反应后,加入到封装好的微流控芯片中,之后放入到带有离心功能、恒温功能及实时荧光检测的微流控芯片检测仪中,上述仪器和芯片均为市售产品,宁波爱基因科技有限公司也有相应公开产品,利用离心力驱动样品进入微流控芯片反应孔,进行恒温扩增。若样本中含有目的片段而得到恒温扩增,扩增产物与荧光物质进行有效的结合,通过荧光检测仪实时捕获荧光信号,直观的反应扩增产物的产生,根据实时荧光信号的出现时间、强度和位置,判断样本中是否含有口蹄疫和小反刍兽疫病毒。
具体的操作步骤如下:
1、微流控芯片检测体系中18μL反应液的组成如下:
所述引物的浓度和体积为:90μM的FMDV-F3引物0.5μL、90μM的FMDV-B3引物0.5μL、180μM的FMDV-FIP引物2μL、180μM的FMDV-BIP引物2μL。所述小反刍兽疫引物的浓度和体积为:90μM的PPRV-F3引物0.5μL、90μM的PPRV-B3引物0.5μL、180μM的PPRV-FIP引物2μL、180μM的PPRV-BIP引物2μL。其中,该试剂盒选用8样本芯片,即1个加样孔对应4个检测孔,第1检测孔位包埋扩增FMDV序列的引物和第2检测孔包埋扩增PPRV序列的引物,第3检测孔是空白,第4检测孔包埋内参引物(如图1),冻干。
所述口蹄疫病毒的核酸序列为M29409.1,小反刍兽疫病毒的核酸序列为HQ197753.1。
取16μL的FMDV的核酸,该核酸序列为M29409.1;取16μL的PPRV的核酸,该核酸序列为HQ197753.1,两核酸充分混匀,然后将反应液18μL与FMDV和PPRV模板核酸32μL混合,加入到芯片的加样孔,再将加样孔用封口膜封住,上机;
2、微流控芯片上机扩增:
由于本方法采用的是恒温扩增,不需要经过PCR扩增的变性、退火和延伸等变温过程,整个反应过程在恒温条件下完成,扩增程序:温度设定为63.5℃,反应时间设定为30min。运行程序:低速离心转速为1600r/min,低速离心时间为10sec,高速离心转速为4600r/min,高速离心时间为30sec。
3、微流控芯片结果判断:
3.1微流控芯片检测仪阈值线设置
阈值线一般情况设置为800(可根据实际情况进行调整,设定原则以阈值线刚好超过非典型S型扩增曲线的最高点,且Ct值显示为30),仪器配套软件自动分析结果。
3.2质量控制
内参出现扩增曲线,且Ct值<30时,实验结果有效。
3.3结果判定
3.3.1实验成立条件
阳性对照:Ct<30,阳性对照的反应孔(1、2)和内标反应孔(4)有明显的典型S型扩增曲线。
阴性对照:阴性对照的反应孔(1、2)均无扩增曲线,内标反应孔(4)有明显的典型S型扩增曲线。
3.3.2判定标准
阳性:反应时间30分钟内,项目检测孔位出现明显扩增曲线,且Ct值<30,判定该孔对应的检测项目为阳性。
阴性:反应时间30分钟内,项目检测孔位未出现明显扩增曲线,判定该孔对应的检测项目为阴性。
在微流控芯片检测仪上进行微流控芯片的恒温扩增,仪器会进行实时荧光检测,根据荧光检测的有效扩增曲线进行判读,任意一检测孔中有标准的S型的扩增曲线,则该孔判断为阳性,即该样本中含有对应检测孔的病毒核酸;没有扩增曲线的检测孔判断为阴性,即该样本不含有对应检测孔的病毒核酸。
4、敏感性及检测限的验证
4.1实验材料
试剂:反应液;1×10
仪器:恒温扩增仪;掌上离心机;移液器。
4.2检测体系
参照上述的检测体系进行实验操作,然后把上好样的芯片放进恒温扩增仪进行试验检测,扩增结果可如图2检测限的结果看,FMDV(3A)和PPRV(3B)引物的最低检测限都是1×10
5、重复性的验证
5.1实验材料
试剂:反应液;FMDV和PPRV引物1×10
仪器:恒温扩增仪;掌上离心机;移液器。
5.2检测体系
参照上述检测体系进行实验操作,然后把芯片放进恒温扩增仪进行试验检测。
5.3扩增结果
图3是FMDV和PPRV重复性实验扩增结果图。下表是FMDV和PPRV的Ct值的变异系数(CV,%)。
经计算,引物FMDV的Ct值的变异系数(CV,%)为2.05%,重复性好,小于5%,符合要求;引物PPRV的Ct值的变异系数(CV,%)为2.93%,重复性好,小于5%,符合要求。
6、特异性的验证
6.1实验材料
试剂:反应液;核酸(分别提取自猪伪狂犬阳性实际样本、猪流行性腹泻实际样本、口蹄疫阳性实际样本、猪细小病毒病实际样本、猪圆环病毒病实际样本、小反刍兽疫实际样本、猪瘟实际样本、山羊痘实际样本);阴性对照。
仪器:恒温扩增仪;掌上离心机;移液器。
6.2检测体系
参照上述1中的检测体系进行实验操作,然后把芯片放进恒温扩增仪进行试验检测。
6.3扩增结果
FMDV和PPRV特异性实验扩增结果可参考图4,从FMDV的扩增结果可知,除口蹄疫样本所提核酸扩增结果为阳性,猪伪狂犬阳性实际样本、猪流行性腹泻实际样本、猪细小病毒病实际样本、猪圆环病毒病实际样本、小反刍兽疫实际样本、猪瘟实际样本、山羊痘实际样本核酸和阴性对照均无扩增曲线,说明FMDV引物只能特异性地扩增检测出口蹄疫核酸,特异性好,一般不会与其它病毒产生交叉反应。从PPRV的扩增结果可知,除小反刍兽疫样本所提核酸扩增结果为阳性,猪伪狂犬阳性实际样本、猪流行性腹泻实际样本、口蹄疫阳性实际样本、猪细小病毒病实际样本、猪圆环病毒病实际样本、猪瘟实际样本、山羊痘实际样本核酸和阴性对照均无扩增曲线,说明PPRV引物只能特异性地扩增检测出小反刍兽疫样本核酸,特异性好,一般不会与其它病毒产生交叉反应。
以上仅是本发明的特征实施范例,对本发明保护范围不构成任何限制。凡采用同等交换或者等效替换而形成的技术方案,均落在本发明权利保护范围之内。
- 一种高效二联检测口蹄疫和小反刍兽疫的引物以及试剂盒
- 一种高效二联检测兔瘟和兔瘟2型的引物以及试剂盒
