微流控人工肺及其制造方法
文献发布时间:2023-06-19 19:27:02
技术领域
本发明涉及人工肺技术领域,特别地,有关于一种微流控人工肺及其制造方法。
背景技术
机械通气是一种机械辅助或替代自主呼吸的方法,但这类治疗方法常会产生一些副作用,如通气相关的肺损伤等。机械通气的一些不良后果可通过体外循环系统解决。体外循环和氧合系统以体外循环血液氧合(Extracorporeal Membrane Oxygenation,ECMO)和体外循环二氧化碳去除(Extracorporeal Carbon Dioxide Removal,ECCO2R)为目标。
现有技术的体外循环和氧合系统,主要分为两大类。
第一类是以使用中空纤维膜为代表的膜式氧合器,它们通常依赖于气体交换膜的使用。具体为,气体交换膜将体外循环血液与气室分开,在气体交换膜的两侧构建血(液)-气交换界面,体外循环血液中的二氧化碳穿过气体交换膜并弥散到气室中,同时气室中的氧气穿过气体交换膜弥散到体外循环血液中。这类氧合器的特点是体积较大、流量较高,但是它们在对液-气交换界面的使用时,很容易在界面处发生凝血,膜血栓情况严重,同时必须防止气体进入体外循环血液而造成气栓。
第二类是以新兴的微流控技术为核心的微流控人工肺氧合器。微流控是一种起源于微机电系统(MEMS,Micro-Electro-Mechanical System)的对微纳尺度流体进行操控的技术,其拥有体积小、速度快、精度高等诸多优点,已被广泛应用于各领域不同的微型器件内,并逐渐向临床技术开发领域延伸。现有技术公开的微流控扩散装置和系统便是一种人工肺的模型。这些微流控人工肺,即包含微米级流动通道和扩散膜的人工肺,可以克服传统人工肺系统的缺点,主要是由于微流控人工肺的扩散距离小,从而拥有优异的气体交换效率以便进行小型化和便携化;血液接触表面积进一步减小以降低血栓风险;得益于微流控技术的精细,微流控人工肺还可包含血液流动路径,其更接近地模拟天然肺中的那些血液流动路径,从而潜在地提高生物相容性并增加寿命。然而,目前所设计的微流控人工肺的气体交换必须通过扩散膜和器件壁面进行,其气体交换效率的进一步提升受到了根本的制约,而进一步减薄扩散膜和壁面则会带来较高的不稳定性。
发明内容
本发明的目的是提供一种微流控人工肺及其制造方法,以解决目前微流控人工肺必须通过扩散膜和器件壁面进行气体交换,气体交换效率难以得到进一步提升的技术问题。
本发明的上述目的可采用下列技术方案来实现:
本发明提供一种微流控人工肺,包括:基体,设有至少一血流通道、至少一第一气流通道以及至少一所述第一气流通道与所述血流通道的交汇区域;至少一仿生密封微结构阵列,包括多个微结构,多个所述微结构阵列排布在所述交汇区域而使所述血流通道内的血液和所述第一气流通道内的气体之间形成分界面。
本发明的实施方式中,所述血流通道的数量、所述第一气流通道的数量以及所述仿生密封微结构阵列的数量均为多个,所述基体还设有入血通道和出血通道,所述入血通道通过多个所述血流通道与所述出血通道相连通,多个所述第一气流通道和多个所述血流通道交替排布设置,多个所述仿生密封微结构间隔排布并位于多个所述第一气流通道和多个所述血流通道之间。
本发明的实施方式中,所述基体还设有至少一第二气流通道,所述第二气流通道与所述血流通道之间通过换氧膜进行分隔。
本发明的实施方式中,所述基体包括第一基体以及第二基体,所述第一基体的第一表面开设有至少一血流沟槽、至少一第一气流沟槽以及至少一中间沟槽,所述仿生密封微结构阵列位于所述中间沟槽内,所述第二基体的第一表面开设有至少一第二气流沟槽,所述第一基体的第一表面与所述第二基体的第一表面通过所述换氧膜相贴合,所述血流沟槽形成所述血流通道,所述第一气流沟槽形成所述第一气流通道,所述中间沟槽形成所述交汇区域,所述第二气流沟槽形成所述第二气流通道。
本发明的实施方式中,多个所述微结构沿所述血液的输送方向排布在所述交汇区域。
本发明的实施方式中,相邻两所述微结构之间的间距为5μm~500μm。
本发明的实施方式中,所述微结构包括中间结构、连接结构以及两端部结构,两所述端部结构通过所述连接结构与所述中间结构相连接并相对于所述中间结构对称设置,两个所述端部结构配合所述连接结构形成与所述血液接触的第一接触部,两个所述端部结构配合所述中间结构形成与所述气体接触的第二接触部。
本发明的实施方式中,所述第一接触部包括第一侧面以及两第二侧面,两所述第二侧面通过所述第一侧面相连接;所述第二接触部包括第三侧面、两第四侧面以及两第五侧面,两所述第五侧面通过两所述第四侧面与所述第三侧面相连接;所述第一侧面、所述第三侧面以及所述第五侧面沿所述输送方向延伸并相互平行设置,所述第四侧面沿所述输送方向的垂直方向延伸设置,所述第二侧面的一端与所述第一侧面相连接,所述第二侧面的另一端朝所述第五侧面倾斜延伸并与所述第五侧面相连接。
本发明的实施方式中,所述中间结构在所述输送方向上的宽度为10μm~300μm。
本发明的实施方式中,所述连接结构在所述输送方向上的宽度为5μm~500μm。
本发明的实施方式中,所述端部结构与所述中间结构之间具有夹角,所述夹角的角度为0°-180°。
本发明的实施方式中,所述端部结构在所述输送方向上的宽度为0.5μm-20μm,所述端部结构在所述输送方向的垂直方向上的宽度为0.5μm-50μm。
本发明还提供一种微流控人工肺的制造方法,包括以下步骤:制备第一模板;将成型材料注入所述第一模板的成型腔内固化形成第一基体;其中,所述第一基体的第一表面形成至少一血流沟槽、至少一第一气流沟槽以及至少一连通所述血流沟槽和所述第一气流沟槽的中间沟槽,且所述中间沟槽内成型有仿生密封微结构阵列;将所述第一基体的第一表面与第二基体相贴合,使所述血流沟槽形成血流通道,所述第一气流沟槽形成第一气流通道,所述中间沟槽形成交汇区域。
本发明的实施方式中,所述第一基体的第一表面通过换氧膜与所述第二基体的第一表面相贴合;所述制造方法还包括制备所述第二基体,包括以下步骤:制备第二模板;将成型材料注入所述第二模板的成型腔内固化形成所述第二基体;其中,所述第二基体的第一表面上形成至少一第二气流沟槽;将所述换氧膜铺设在所述第二基体的第一表面上并覆盖所述第二气流沟槽,使所述第二气流沟槽形成第二气流通道。
本发明的实施方式中,还包括以下步骤:在所述第一基体的与其第一表面相对的第二表面上开设与所述血流通道连通的血流输入口和血流输出口,以及与所述第一气流通道连通的第一气流输入口以及第一气流输出口;在所述第二基体的与其第一表面相对的第二表面上开设与所述第二气流通道连通的第二气流输入口以及第二气流输出口。
本发明的特点及优点是:
本发明的微流控人工肺,通过血流通道输送氧气含量较低的血液,通过第一气流通道输送纯氧或者氧气含量较高的气体,通过将多个微结构阵列排布在交汇区域形成仿生密封微结构阵列,使得血流通道内的血液和第一气流通道内的气体在流经交汇区域时会填充于多个微结构之间的间隙中而形成稳定的分界面,使得血液和气体之间不会掺混,从而实现密封功能,并且实现密封功能时无需进行额外的控制与输入,同时血液和气体又能在该分界面处进行气体交换,即血液中的二氧化碳从该分界面扩散到气体中,而气体中的氧气则从该分界面扩散到血液中。
本发明的微流控人工肺的制造方法,通过将仿生密封微结构阵列与第一基体一体固化成型,进而通过与第二基体贴合便能将仿生密封微结构阵列制造在微流控人工肺的内部,从而实现仿生密封微结构阵列在微流控人工肺内的应用,且操作简单。
附图说明
为了更清楚地说明本发明实施例中的技术方案,下面将对实施例描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
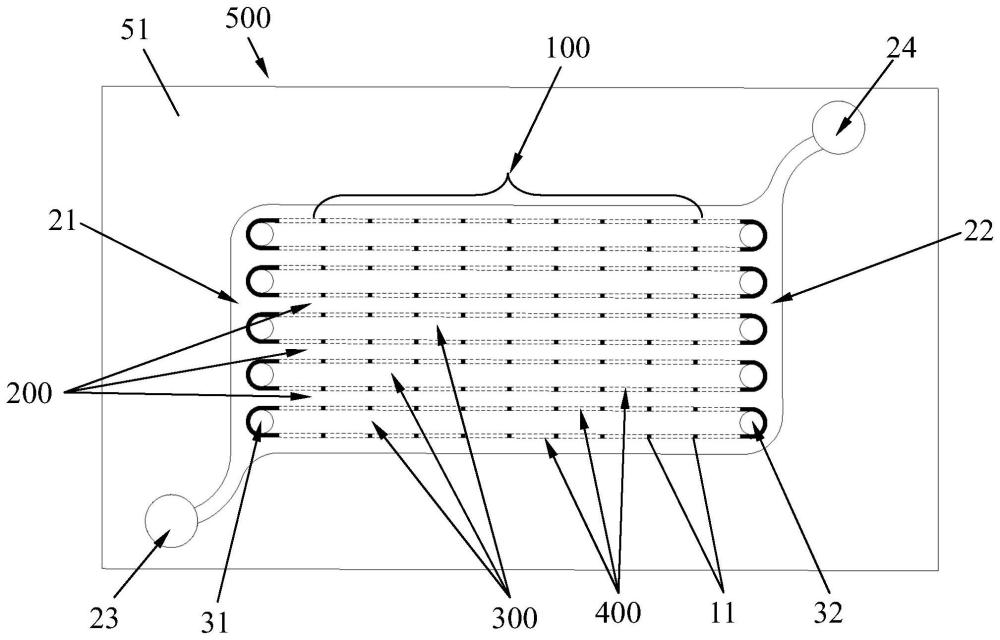
图1为本发明中微流控人工肺的结构示意图。
图2为本发明中仿生密封微结构阵列的结构示意图。
图3为本发明中微结构的结构示意图。
图4为本发明中微流控人工肺的第一基体的俯视图。
图5为本发明的微流控人工肺的第二基体的俯视图。
图6为本发明的微流控人工肺的局部剖面图。
图中:
100、仿生密封微结构阵列;11、微结构;12、第一接触部;13、第二接触部;14、第一侧面;15、第二侧面;16、第三侧面;17、第四侧面;18、第五侧面;19、中间结构;110、端部结构;111、连接结构;
200、血流通道;21、进血通道;22、出血通道;23、血液输入口;24、血液输出口;300、第一气流通道;31、第一气流输入口;32、第一气流输出口;400、交汇区域;41、分界面;500、基体;51、第一基体;52、第二基体;53、换氧膜;600、第二气流通道;61、第二气流输入口;62、第二气流输出口;B、血液;G、气体。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
实施方式一
如图1和图2所示,本发明提供一种微流控人工肺,包括:基体500,设有至少一血流通道200、至少一第一气流通道300以及至少一第一气流通道300与血流通道200的交汇区域400;至少一仿生密封微结构阵列100,包括多个微结构11,多个微结构11阵列排布在交汇区域400而使血流通道200内的血液B和第一气流通道300内的气体G之间形成分界面41。
本发明的微流控人工肺,通过血流通道200输送氧气含量较低的血液B,通过第一气流通道300输送纯氧或者氧气含量较高的气体G,通过将多个微结构11阵列排布在交汇区域400形成仿生密封微结构阵列100,使得血流通道200内的血液B和第一气流通道300内的气体G在流经交汇区域400时会填充于多个微结构11之间的间隙中而形成稳定的分界面41,使得血液B和气体G之间不会掺混,从而实现密封功能,并且实现密封功能时无需进行额外的控制与输入,同时血液B和气体G又能在该分界面41处进行气体交换,即血液B中的二氧化碳从该分界面41扩散到气体G中,而气体G中的氧气则从该分界面41扩散到血液B中。
本发明中微结构11的设计灵感和参数设计来自于仿生学原理,选取的具有特殊润湿性能的自然界微结构11原型包括槐叶萍叶面的“灯笼状”微结构、水蜘蛛和跳虫体毛的“T”型结构等,从这些结构提取归纳出微结构11,使得微结构11大体可呈“T”型、伞形、梯形、三角形或“灯笼”型,进而通过阵列排布于交汇区域400,使多个微结构11的第一接触部12与血液B接触,多个微结构11的第二接触部13与气体G接触,从而在血液B和气体G之间形成分界面41。
具体的,通入的血液B在流经交汇区域400时会在仿生密封微结构阵列100处扩张而与气体G之间形成血-气分界面41。分界面41的形貌与仿生密封微结构阵列100中多个微结构11的阵列形状、间距以及微结构11的具体形状有关,分界面41的形貌和大小会影响分界面41收缩变小的表面张力,而通入的血液B具有一定的工作压力,当这两个力相互平衡时,分界面41则能稳定存在,从而使仿生密封微结构阵列100具备较佳的密封效果。
由此可知,本发明中仿生密封微结构阵列100的密封效果与分界面41的稳定性相关,而分界面41的稳定性与血液B和气体G在分界面41处的表面张力以及血液B和气体G的工作压力有关。
其中,血液B和气体G在分界面41处的表面张力与微结构11的形状、间距以及阵列形状相关,因此,本发明中微结构11的形状、间距以及阵列形状可以不具体限定,根据表面张力的要求进行调整即可。但为了更好地实施,本发明通过相关理论计算和仿真、实验验证,提供各个参数较佳地调整范围如下。
如图1所示,对于阵列形状,交汇区域400的两侧设置有用于输送血液B的血流通道200以及用于输送气体G的第一气流通道300,且血液B和气体G的输送方向相同,多个微结构11可以是沿输送方向X直线形并排排布;也可以是沿输送方向X波浪线形交错排布;还可以是多个微结构11沿垂直于输送方向X排成多列微结构11,多列微结构11沿输送方向X排布;当然还可以是其他排列形式,只要确保多个微结构11能够在交汇区域400像“护栏”一样对两侧的流体继续拦截,从而实现密封即可。
如图2所示,对于多个微结构11之间的间距L,提供一较佳的范围为5μm~500μm。
如图2所示,对于微结构11形状,为了使微结构11的形状更具体化,本发明进一步地提取归纳出微结构11包括中间结构19、连接结构111以及两端部结构110,两端部结构110通过连接结构111与中间结构19相连接并相对于中间结构19对称,两个端部结构110配合连接结构111形成有第一接触部12,两个端部结构110配合中间结构19形成有第二接触部13。下面将提供中间结构19、连接结构111、端部结构110的较佳的形状和尺寸,使得仿生密封微结构阵列100处能提供足够的表面张力,从而实现较佳地密封效果。
如图3所示,具体的,中间结构19沿水平方向的截面形状为矩形,连接结构111沿水平方向的截面形状为矩形,端部结构110靠近相邻微结构11的一端呈任意角度的尖角状,端部结构110与中间结构19之间具有夹角,夹角的角度为0°~180°。中间结构19在输送方向上的宽度W1为10μm~300μm。连接结构111在输送方向上的宽度W2为5μm~500μm。端部结构110在输送方向X上的宽度W3为0.5μm-20μm,端部结构110在输送方向X的垂直方向上的宽度W4为0.5μm-50μm。本实施例中,端部结构110与中间结构19之间夹角的角度为90度,端部结构110沿水平方向的截面形状为直角梯形,第一接触部12包括第一侧面14以及两第二侧面15,两第二侧面15通过第一侧面14相连接;第二接触部13包括第三侧面16、两第四侧面17以及两第五侧面18,两第五侧面18通过两第四侧面17与第三侧面16相连接;第一侧面14、第三侧面16以及第五侧面18沿输送方向X延伸并相互平行设置,第四侧面17沿输送方向X的垂直方向延伸设置,第二侧面15的一端与第一侧面14相连接,第二侧面15的另一端朝第五侧面18倾斜延伸并与第五侧面18相连接。
可选的,中间结构的截面形状还可以为梯形、三角形、椭圆形或其他不规则形状。连接结构的截面形状还可以为梯形、圆形、椭圆形或其他不规则形状。端部结构近相邻微结构的一端还可以呈圆角状或直角状。
如图1所示,对于血液B和气体G的工作压力可以在0-100kPa(表压)的范围内进行调控,使仿生密封微结构阵列100处形成的分界面41所能提供的表面张力与血液B和气体G的工作压力相平衡。
如图2所示,微结构11采用PDMS(聚二甲基硅氧烷)、玻璃或亚克力等材料制造而成。本发明的实施方式中,为使仿生密封微结构阵列100更好地实现对血液B和气体G的分隔和密封作用,第一接触部12铺设有亲水处理剂形成的亲水层。进一步地,第二接触部13铺设有疏水处理剂形成的疏水层。
如图4所示,本发明的实施方式中,血流通道200的数量、第一气流通道300的数量以及仿生密封微结构阵列100的数量均为多个,基体500还设有入血通道21和出血通道22,入血通道21通过多个血流通道200与出血通道22相连通,多个第一气流通道300和多个血流通道200交替排布设置,多个仿生密封微结构阵列100间隔排布并位于多个第一气流通道300和多个血流通道200之间。血液B从入血通道21进入多个血流通道200内,气体G则分别流入多个第一气流通道300内,进而使血液B和气体G在多个仿生密封微结构阵列100处形成稳定的分界面41并进行气体交换,进一步地提高了气体交换的效率,增加了血液B和氧气的接触面积。
具体的,基体500上设有与入血通道21连通的血液输入口23、与出血通道22连通的血液输出口24、与多个第一气流通道300的一端连通的多个第一气流输入口31、与多个第一气流通道300的另一端连通的多个第一气流输出口32。
如图5和图6所示,为了进一步增加血液B在微流控人工肺中与氧气的接触面积,本发明的实施方式中,基体500还设有至少一第二气流通道600,第二气流通道600与血流通道200之间通过换氧膜53进行分隔。血流通道200内的血液B在水平方向上能在两侧的仿生密封微结构阵列100处与两侧的第一气流通道300内的气体G进行气体交换,在竖直方向上则能通过换氧膜53与第二气流通道600内的气体G进行气体交换。本实施例中,第二气流通道600大体呈格栅形,铺设于多个血流通道200的下方,从而能与多个血流通道200内的血液B同时进行气体交换。
可选的,基体还设有第三气流通道,第三气流通道与血流通道之间也通过一换氧膜进行分隔,第三气流通道大体呈格栅形,铺设于多个血流通道的上方,使得血流通道内的血液能与其上下左右的气体进行气体交换。
由于血流通道200、第一气流通道300、仿生密封微结构阵列100以及第二气流通道600均需要制造在微流控人工肺的内部,为了降低制造难度,本发明的实施方式中,基体500包括第一基体51以及第二基体52,第一基体51的第一表面开设有至少一血流沟槽、至少一第一气流沟槽以及至少一中间沟槽,仿生密封微结构阵列100位于中间沟槽内,第二基体52的第一表面开设有至少一第二气流沟槽,第一基体51的第一表面与第二基体52的第一表面通过换氧膜53相贴合,血流沟槽形成血流通道200,第一气流沟槽形成第一气流通道300,中间沟槽形成交汇区域400,第二气流沟槽形成第二气流通道600。微流控人工肺的具体制造步骤在实施方式二中进行详细的说明,在此先不详述。
实施方式二
如图4、图5以及图6所示,本发明还提供一种微流控人工肺的制造方法,包括以下步骤:制备第一模板;将成型材料注入第一模板的成型腔内固化形成第一基体51;其中,第一基体51的第一表面形成至少一血流沟槽、至少一第一气流沟槽以及至少一连通血流沟槽和第一气流沟槽的中间沟槽,且中间沟槽内成型有仿生密封微结构阵列100;将第一基体51的第一表面与第二基体52相贴合,使血流沟槽形成血流通道200,第一气流沟槽形成第一气流通道300,中间沟槽形成交汇区域400。本实施方式中微流控人工肺与实施方式一中微流控人工肺的具体结构、工作原理以及有益效果均相同,在此不再赘述。
本发明的微流控人工肺的制造方法,通过将仿生密封微结构阵列100与第一基体51一体固化成型,进而通过与第二基体52贴合,从而使仿生密封微结构阵列100制造在微流控人工肺的内部,且微流控人工肺的内部形成血流通道200和第一气流通道300,操作简单。
如图5和图6所示,本发明的实施方式中,第一基体51的第一表面通过换氧膜53与第二基体52的第一表面相贴合;制造方法还包括制备第二基体52,包括以下步骤:制备第二模板;将成型材料注入第二模板的成型腔内固化形成第二基体52;其中,第二基体52的第一表面上形成至少一第二气流沟槽;将换氧膜53铺设在第二基体52的第一表面上并覆盖第二气流沟槽,使第二气流沟槽形成第二气流通道600。
具体的,第一模板和第二模板均可以采用硅片通过软光蚀刻制造而成。成型材料为PDMS(聚二甲基硅氧烷)、玻璃或亚克力。第一基体51、换氧膜53以及第二基体52之间可以利用等离子体键合的方式相连接。
如图4和图5所示,本发明的实施方式中,还包括以下步骤:在第一基体51的与其第一表面(即第一基体51的底面)相对的第二表面(即第一基体51的顶面)上开设与血流通道200连通的血液输入口23和血液输出口24,以及与第一气流通道300连通的第一气流输入口31以及第一气流输出口32;在第二基体52的与其第一表面(即第二基体52的顶面)相对的第二表面(即第二基体52的底面)上开设与第二气流通道600连通的第二气流输入口61以及第二气流输出口62。
以上所述仅为本发明的几个实施例,本领域的技术人员依据申请文件公开的内容可以对本发明实施例进行各种改动或变型而不脱离本发明的精神和范围。
- 一种微流控芯片、微流控检测装置及微流控检测方法
- 微流控芯片、干细胞分离方法及微流控芯片的制备方法
- 芯片上阀门的制造方法、微流控芯片与液体流动控制方法
- 微流控装置和微流控方法
- 一种微流控组件、微流控芯片及其制备方法
- 微流控结构、微流控系统、微流控方法和制造微流控结构的方法
- 含有试剂的筒、包括该筒的微流控装置、制造该微流控装置的方法以及利用该微流控装置的生物化学分析方法
