一种用于检测MYBPC3突变基因的试剂及其应用
文献发布时间:2023-06-19 19:28:50
技术领域
本发明涉及基因检测技术领域,尤其涉及一种用于检测MYBPC3突变基因的试剂及其应用。
背景技术
肥厚型心肌病(hypertrophic cardiomyopathy,HCM)的我国患病率约1/500,是最为常见的单基因遗传性心血管疾病,是青少年和运动员心脏性猝死的主要原因之一,主要表现为左心室壁增厚。心脏性猝死(sudden cardiac death,SCD)常见于10~35岁的年轻患者,心力衰竭(心衰)死亡多发生于中年患者,HCM相关的心房颤动(房颤)导致的卒中则以老年患者多见。SCD的危险性随年龄增长而逐渐下降,但不会消失。在三级医疗中心就诊的HCM患者年死亡率为2~4%,SCD是最常见的死因之一。
绝大部分HCM呈常染色体显性遗传,约60%的家族性和30%的散发性HCM患者可检测到明确的致病基因突变。目前,已发现27个致病基因与HCM相关,其中,MYBPC3是心脏型肌球蛋白结合蛋白C编码基因,MYBPC3突变基因会导致显著的肌节紊乱和发育不良,从而引发心肌病。《中国成人肥厚型心肌病诊断与治疗指南》建议:推荐所有临床诊断为HCM的患者进行基因筛查。通过基因筛查发现患者致病基因突变,结合临床表型,帮助确诊和鉴别诊断。
虽然目前已发现许多MYBPC3突变基因的突变位点,但是在前人的研究基础上,进一步发现新的MYBPC3突变基因将有助于进一步研究肥厚型心肌病,对肥厚型心肌病的早期诊断,或者辅助临床判断具有重要意义。
发明内容
本发明的目的在于针对上述缺陷,提供一种用于检测MYBPC3突变基因的试剂及其应用。
本发明目的之一在于提供:一种用于检测MYBPC3突变基因的试剂,所述MYBPC3突变基因具有c.2996delG杂合错义变异,核苷酸序列为SEQ ID NO:1,编码蛋白的氨基酸序列为SEQ ID NO:2;或所述MYBPC3突变基因具有c.1441G>A杂合错义变异,核苷酸序列为SEQID NO:3,编码蛋白的氨基酸序列为SEQ ID NO:4。
本发明经过大量试验、研究和分析成功地筛选出MYBPC3突变基因,并利用MYBPC3突变基因开发出能够用于快速、灵敏、有效的检测MYBPC3突变基因的试剂盒。
基因突变信息见下表:
本发明目的之二在于提供上述MYBPC3突变基因在制备肥厚型心肌病检测试剂盒中的应用。优选地,所述肥厚型心肌病检测试剂盒包括PCR预混液、阴性对照试剂和阳性对照试剂。
本发明有益效果在于:本发明公开的MYBPC3突变基因可以作为临床辅助诊断肥厚型心肌病的生物标志物,对肥厚型心肌病的早期诊断,或者辅助临床判断具有重要意义;基于用于检测MYBPC3突变基因的试剂开发的检测试剂盒,可以将具有MYBPC3 c.2996delG或c.1441G>A杂合错义突变的患者和正常人群区分开,为受试者提供优生优育指导和遗传咨询,减少患儿出生。
附图说明
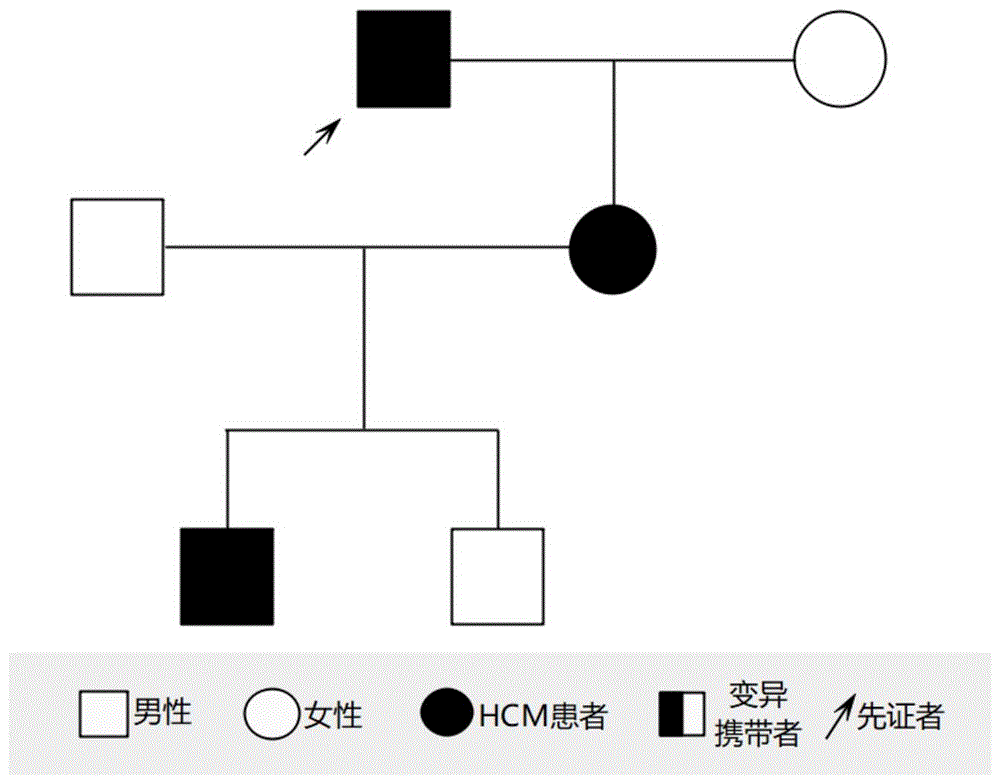
图1为实施例1中的肥厚型心肌病家系图;
图2为实施例1先证者及其家系中患病成员Sanger测序图;
图3为实施例2中的肥厚型心肌病家系图;
图4为实施例2先证者及其家系中患病成员Sanger测序图。
具体实施方式
下面通过具体实施方式进一步详细说明:
试剂来源:PCR预混液:2×Taq MasterMix(Dye),购自江苏康为世纪生物科技有限公司,货号:l01037/70335;包含如下成分:Taq DNA Polymerase、PCR Buffer、Mg
实施例1:MYBPC3 c.2996delG验证实验
在临床诊断为肥厚型心肌病先证者(男,51岁)及其家属自愿签署知情同意书的前提下,寄送5-10mL全血样本(加入EDTA抗凝,-80℃保存),建立病历资料库,详细记录先证者病情、家系情况等资料(家系图如图1所示)。本研究已得到本单位伦理委员会批准。随机收集412名与该肥厚型心肌病先证者家系无关的健康样本作为验证样本,每位采集2-4mLEDTA抗凝血,-80℃保存。
S1、提取基因组DNA:对先证者和验证样本的人类全血EDTA抗凝样本进行全基因组DNA的提取,采用江苏百世诺医疗科技有限公司磁珠法全血基因组DNA提取试剂盒,操作步骤按照产品说明书进行。对DNA的浓度和纯度进行检测,作为PCR扩增的模板DNA。
S2、准备PCR反应体系,该PCR反应体系用于扩增包含目的基因位点在内的一段DNA序列,其组成为:PCR预混液25μL、正向引物(10μM)2μL、反向引物(10μM)2μL、模板DNA<1000ng,加RNase-Free H
S3、将反应体系混合,在PCR仪上进行目的基因片段的扩增反应,扩增程序为:95℃预变性2min;94℃变性30s,57℃退火30s,72℃延伸30s,共30循环。72℃终延伸2min。
S4、PCR产物的检测:取2μL的PCR产物,使用1.5%的琼脂糖凝胶电泳检测PCR产物,选用1000bp Marker作为参考,检测验证扩增产物为预期的大小。
S5、PCR产物检测后,使用Agencourt AMPure XP磁珠对PCR产物进行纯化,纯化步骤按照产品说明书进行,具体步骤如下:(1)振荡磁珠30s,使其彻底混匀为均一溶液。(2)向1.5mL的离心管中加入待纯化的PCR产物,然后加入2倍样品体积的磁珠溶液。涡旋振荡混匀后,室温下在1400rpm的Thermomixer上振荡5min。(3)将上一步的离心管放于磁力架上,直至磁珠完全吸附(约需1min)。(4)保持离心管固定于磁力架上,弃去溶液,期间避免接触磁珠。(5)向上一步的离心管中加入500μL Buffer PW后,将离心管从磁力架上取下,涡旋振荡10s钟后将离心管重新放回磁力架,静置1min,待磁珠完全吸附于离心管侧壁后彻底弃去漂洗液。(6)重复步骤(5)。(7)保持离心管固定于磁力架上静置10min,使乙醇完全挥发干净。(8)将离心管从磁力架上取下,加入20-100μL Buffer EB,涡旋振荡将磁珠重悬于洗脱液中后将离心管放于65℃、1400rpm的Thermomixer上振荡洗脱5min。(9)将离心管放于磁力架上直至磁珠完全吸附(约需1min)。(10)将洗脱液转移至一个新的1.5mL离心管中,此时,可弃去磁珠。
S6、使用AppliedBiosystems 3500Dx系列基因分析仪对扩增产物进行Sanger测序。
S7、将测序结果和在NCBI(https://www.ncbi.nlm.nih.gov/)中获取的野生型MYBPC3基因序列在软件Chromas中进行序列比对,确定检测位点是否发生变异。
S8、基因变异论证:412名表型健康人群及家系中未患肥厚型心肌病成员均未检测到MYBPC3c.2996delG杂合错义突变;肥厚型心肌病先证者及家系中患肥厚型心肌病成员均检测到MYBPC3c.2996delG杂合错义变异。具有c.2996delG杂合错义突变的MYBPC3基因的编码核苷酸序列为SEQ ID NO:1,编码蛋白的氨基酸序列为SEQ ID NO:2。
千人基因组(https://www.ncbi.nlm.nih.gov/variation/tools/1000genomes/):无。ClinVar(https://www.snpedia.com/index.php/ClinVar):无。ESP6500(https://esp.gs.washington.edu/drupal/):无。ExAC(http://exac.hms.harvard.edu/):无。HGMD(http://www.hgmd.c.ac.uk/ac/index.php):无。
根据现有证据:该变异为罕见变异、该变异可能会使蛋白截短表达、附近及下游的移码或无义变异多次被报导为致病突变、移码或无义变异为该基因主要致病类型,所以该变异为肥厚型心肌病的高度可疑致病突变。
实施例2:MYBPC3 c.1441G>A验证
在临床诊断为肥厚型心肌病先证者(男,19岁)及其家属自愿签署知情同意书的前提下,寄送5-10mL全血样本(加入EDTA抗凝,-80℃保存),建立病历资料库,详细记录先证者病情、家系情况等资料。家系图如图3所示。随机收集500名与该肥厚型心肌病先证者家系无关的健康样本作为验证样本,每位采集2-4mL EDTA抗凝血,-80℃保存。采用实施例1的S1-S7的方法,确定检测位点是否发生MYBPC3 c.1441G>A杂合错义突变,所用到的引物信息如下:正向引物(Seq_7,SEQ ID NO:7):5'CATCGGTGCCAAGCGTACCC 3';反向引物(Seq_8,SEQID NO:8):5'TGATGCTCACCAGGCCCGTA 3'。长度:772bp。扩增程序为:95℃预变性2min;94℃变性30s,60℃退火30s,72℃延伸30s,共35循环。72℃终延伸2min。
S8、基因变异论证:500名表型健康人群及家系中未患肥厚型心肌病成员均未检测到MYBPC3c.1441G>A杂合错义突变;肥厚型心肌病先证者及家系中患肥厚型心肌病成员均检测到MYBPC3c.1441G>A杂合错义变异。具有c.1441G>A杂合错义突变的MYBPC3基因的编码核苷酸序列为SEQ ID NO:3,编码蛋白的氨基酸序列为SEQ ID NO:4。
检索千人基因组(https://www.ncbi.nlm.nih.gov/variation/tools/1000genomes/):无。ClinVar(https://www.snpedia.com/index.php/ClinVar):无。ESP6500(https://esp.gs.washington.edu/drupal/):无。ExAC(http://exac.hms.harvard.edu/):无。HGMD(http://www.hgmd.c.ac.uk/ac/index.php):无。
根据现有证据:该变异为罕见变异、该变异可能会使蛋白截短表达、附近及下游的移码或无义变异多次被报导为致病突变、移码或无义变异为该基因主要致病类型,该变异为肥厚型心肌病的高度可疑致病突变。
实施例3:无关样本验证实验
在中国范围内,采用实施例1的方法检测1800例无关样本MYBPC3 c.2996delG、MYBPC3c.1441G>A杂合错义突变,1800例无关样本包括健康人群,以及临床诊断为扩张型心肌病、致心律失常性右心室心肌病、代谢性心肌病、心脏离子通道病(包括长QT综合征、Brugada综合征)等单基因遗传性心血管疾病的患者,每种疾病的患病人数不等。
结果显示,仅在临床诊断患有肥厚型心肌病的患者中检测到突变MYBPC3c.2996delG和MYBPC3 c.1441G>A,支持临床诊断。
实施例4:体外检测肥厚型心肌病患者的MYBPC3基因试剂盒
1.组成:
表2组成
2.使用方法:(1)基因组DNA提取:使用DNA提取试剂盒提取外周血液样本基因组DNA。(2)PCR扩增:采用上述的试剂盒进行PCR扩增,反应体系和反应条件参照实施例1。(3)对PCR扩增产物进行纯化。(4)对纯化的PCR扩增产物进行Sanger测序。(5)分析测序结果,比对是否有MYBPC3 c.2996delG或MYBPC3 c.1441G>A杂合突变。
以上详细描述了本发明的较佳具体实施例。应当理解,本领域的普通技术人员无需创造性劳动就可以根据本发明的构思作出诸多修改和变化。因此,凡本技术领域中技术人员依本发明的构思在现有技术的基础上通过逻辑分析、推理或者有限的实验可以得到的技术方案,皆应在由权利要求书所确定的保护范围内。
