一种多肽的绿色合成方法
文献发布时间:2023-06-19 09:24:30
技术领域
本发明属于多肽药物合成领域,具体涉及一种多肽的合成工艺。
背景技术
多肽的生产制造主要有三种方法,分别是液相合成、固相合成、重组发酵三大类。固相合成方法快捷灵活,适合中长肽的修饰,主要缺点是放大生产时成本会比较高。液相合成适用于一些短肽,不适合制备具有药用价值的中长肽。基因重组法制备多肽,研发周期很长,生产成本高,适合生产像胰岛素这样的大型品种,对于合成大多数药用肽没有竞争优势。由于多肽药物活性高、靶点明确,实际临床剂量较小,固相合成方法目前可以满足大部分的多肽药物品种的生产制备。目前行业中流行的固相多肽合成法存在如下问题:
每步多肽酰胺键形成不完全,造成大量片段杂质,链越长,产品的含量越低;在树脂上形成的多肽不溶解,造成反应无法进行;在树脂上形成的多肽发生折叠,导致反应中心被屏蔽,造成反应无法进行;反应速度慢导致副反应增多;大大过量使用氨基酸,成本高;长链多肽合成的难度特别大;产生杂溶剂,不易回收,对环境影响大。
微波固相多肽合成仪的利用提高了多肽合成效率,但是其依然存在产量低、个别氨基酸消旋严重以及没有解决溶剂消耗量大的问题(Org.Lett.2014,16,940-943)。
最近几年的连续流多肽合成工艺大幅提高了固相多肽合成的效能(Continuous-Flow Solid-Phase Peptide Synthesis:A Revolutionary Reduction of the AminoAcid Excess,ChemSus Chem 2014,7,3172–3176)。连续流多肽合成通过将反应液循环通过反应柱,反应结束后用有机溶剂冲走未反应的原料和杂质,然后再进行下一步操作。连续流多肽合成工艺的氨基酸、溶剂消耗低于现有其它工艺。但是其依然没有达到实现大幅降低溶剂消耗的问题。
1kg分子量700Da左右的6肽,采用不同固相多肽合成工艺的物料消耗统计见下表:
表1不同固相多肽合成工艺的物料消耗统计
从表1可以看出,如果多肽含氨基酸个数越多,生产量越大,溶剂消耗非常巨大。溶剂消耗量大是目前的固相合成多肽方法的主要弊端之一。因此需要开发一套可以大幅降低溶剂消耗的多肽生产工艺,而不是从溶剂如何回收的问题上着手。
发明内容
本发明针对现有技术中存在的不足,提供了一种多肽的绿色合成方法,以解决现有技术中存在的问题。
通过连续流固相多肽合成工艺完成多肽的偶联或脱保护,然后利用超临界二氧碳流体或含有改性溶剂的超临界二氧碳混合流体替代原来的有机溶剂来冲洗多肽树脂。
本工艺通过如下步骤来实现:
步骤1.多肽偶联前的脱保护:多肽树脂脱保护
按照通用的多肽脱保护方法,将脱保护溶液循环地输入装有Boc或Fmoc保护氨基酸-多肽合成树脂的反应柱中,待脱保护完成后,用泵把多肽合成柱里的反应溶液排干,然后通入超临界二氧碳流体或含有改性溶剂的超临界二氧碳混合流体冲洗被脱除的保护基、保护基脱除试剂及杂质,直到检测显示被脱除的保护基、保护基脱除试剂及杂质被完全冲走。
改性超临界二氧化碳为改性溶剂与超临界二氧化碳的混合流体,改性溶剂与超临界二氧化碳混合流体的体积比为1-50:50-99。
所述改性溶剂选自N,N’-二甲基甲酰胺、N,N’-二甲基乙酰胺、二甲亚砜、乙腈、四氢呋喃、2-甲基四氢呋喃、1,4-二氧六环、丙酮、甲醇、乙醇、丙醇、异丙醇、二氯甲烷、氯仿、四氯化碳、苯、甲苯、N-甲基吡咯烷酮、二硫化碳中一种或两种以上任意比例的混合物。
采用超临界二氧化碳流体或改性超临界二氧化碳来冲洗多肽树脂时,反应温度为3-60℃。步骤2.脱保护后进行多肽偶联:通过常见Boc或Fmoc固相多肽偶联方法将Boc或Fmoc保护氨基酸偶联到多肽树脂上。
将Boc或Fmoc保护氨基酸、多肽缩合试剂、有机碱分别溶于有机溶液,同时将三种溶剂通过泵循环地输入步骤1得到的反应柱中,待偶联完成后,用泵把多肽合成柱里的反应溶液排干,然后通入超临界二氧碳流体或含有改性溶剂的超临界二氧碳混合流体冲洗未反应的原料及杂质,直到检测显示原料及杂质被完全冲走。
改性超临界二氧化碳为改性溶剂与超临界二氧化碳的混合流体;改性溶剂与超临界二氧化碳的体积比为1-50:50-99。
所述改性溶剂包括N,N’-二甲基甲酰胺、N,N’-二甲基乙酰胺、二甲亚砜、乙腈、四氢呋喃、2-甲基四氢呋喃、1,4-二氧六环、丙酮、甲醇、乙醇、丙醇、异丙醇、二氯甲烷、氯仿、四氯化碳、苯、甲苯、N-甲基吡咯烷酮、二硫化碳中一种或两种以上任意比例的混合物。
采用超临界二氧化碳流体或改性超临界二氧化碳来冲洗多肽树脂时,温度为3-60℃。
反应体系里面的二氧化碳经过减压收集再冷凝为液态二氧化碳,实现二氧化碳重复利用。
本发明使用的缩写及英文所对应的含义
与现有技术相比,本实用发明的有益效果是:
1、多肽合成当中大幅减少了有机溶剂的使用。连续流固相多肽合成在循环反应阶段,有机溶剂的使用量是固定的,主要消耗发生在洗涤阶段,通常洗涤溶剂量是合成所需溶剂的8-10倍。显而易见,本发明将反应所需的溶剂量减少了80%左右。
2、二氧化碳成本低廉,从大气中提取利用再返回大气当中,完全没有环境污染问题。
附图说明
图1为连续流固相多肽合成结合超临界二氧化碳制备多肽的生产装置的结构示意图;
图2为实施例1制备所得的索马鲁肽粗品的高效液相色谱图;
图3为实施例1制备所得的索马鲁肽粗品的质谱图;
图4为对比实施例1制备所得的索马鲁肽粗品的高效液相色谱图;
图5为对比实施例1制备所得的索马鲁肽粗品的质谱图;
图6为实施例2制备所得的Ac-Ser-Val-Val-Val-Arg-Thr-OH粗品的高效液相色谱图;
图7为实施例2制备所得的Ac-Ser-Val-Val-Val-Arg-Thr-OH粗品的质谱图;
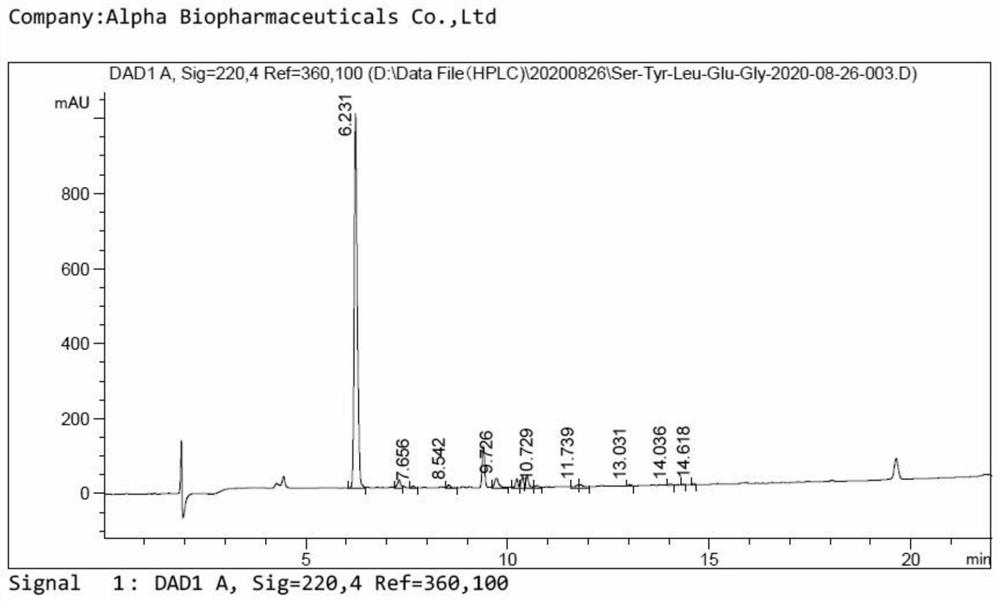
图8为实施例3制备所得的Ser-Tyr-Leu-Glu-Gly的高效液相色谱图;
图9为实施例3制备所得的Ser-Tyr-Leu-Glu-Gly粗品的质谱图;
图中:1、泵,2、溶剂瓶,3、试剂瓶,4、混合器,5、紫外检测器,6、三通阀门一,7、改性溶剂容器,8、超临界二氧化碳生产装置,9、二氧化碳钢瓶,10、多肽合成柱,11、三通阀门二。
具体实施方式
本发明公布了一种多肽的制备方法,实施例仅仅是本发明一部分实施例,而不是全部实施例。实施例只为说明本发明的技术构思及特点,其目的在于让熟悉此项技术的人士能够了解本发明的内容并据以实施,并不能以此限制本发明的保护范围。凡根据本发明精神实质所作的等效变化或修饰,都应涵盖在本发明的保护范围之内。
下面结合实施例进一步阐明本发明。
为了方便描述连续流固相多肽合成结合超临界二氧化碳制备多肽的过程,实施例按照图1进行操作。
实施例1:索马鲁肽的制备
索马鲁肽多肽序列:
H-His-Aib-Glu-Gly-Thr-Phe-Thr-Ser-Asp-Val-Ser-Ser-Tyr-Leu-Glu-Gly-Gln-Ala-Ala-Lys(AEEAc-AEEAc-γ-Glu-17-carboxyheptadecanoyl)-Glu-Phe-Ile-Ala-Trp-Leu-Val-Arg-Gly-Arg-Gly-OH
步骤1、Fmoc-Gly-HMPA-PEG-AM-PS树脂脱除Fmoc
Fmoc-Gly-HMPA-PEG-AM-PS树脂结构图
称取80g取代度为0.36mmol/g的Fmoc-Gly-HMPA-PEG-AM-PS树脂装进多肽合成柱10,将树脂恰好填满柱子,然后拧紧盖子。
将DMF以90mL/min的速度经由混合器4和三通阀门一6泵入多肽合成柱10,从多肽合成柱10顶部流回混合器4,循环5分钟使树脂溶胀,排空混合器4和多肽合成柱10里面的溶液。切换试剂瓶3,把200mL 1%DBU/2%1-辛硫醇DMF溶液以90mL/min经由混合器4和三通阀门一6泵入多肽合成柱10,从多肽合成柱10顶部三通流回混合器4,循环8分钟。排空混合器4和多肽合成柱10里面的溶液,将31.5℃超临界二氧化碳流体以40mL/min的速度泵入多肽合成柱10,经由三通阀门二11、UV12进入废液收集室,直到在线紫外监测器显示Fmoc被冲洗干净。
步骤2:
H-Ser(tBu)-Tyr(tBu)-Leu-Glu(OtBu)-Gly-Gln(Trt)-Ala-Ala-Lys(AEEA-AEEA-(γ-Glu-(OtBu))-monoButyl Octadecanate)-Glu(OtBu)-Phe-Ile-Ala-Trp(Boc)-Leu-Val-Arg(Pbf)-Gly-Arg(Pbf)-Gly-HMPB-PEG-AM-PS树脂合成
42.6g(65.6mmol)Fmoc-Arg(Pbf)-OH和32.6mL(196.8mmol)DIEA溶于120mL DMF,24.9(65.6mmol)HBTU和8.9g(65.6mmol)HOBt溶解于120mLDMF,将2种溶液分别以30mL/min的速度泵入混合器4,经由混合器4和三通阀门一6泵入多肽合成柱10,从多肽合成柱10顶部三通流回混合器4,循环10分钟。排空混合器4和多肽合成柱10里面的溶液,将31.5℃含5%甲醇的超临界二氧化碳流体以40mL/min的速度泵入多肽合成柱10,经由三通阀门二11、UV12进入废液收集室,直到在线紫外监测器显示未反应的Fmoc-Arg(Pbf)-OH被冲洗干净。
采用步骤1和步骤2的多肽制备方法,余下氨基酸及多肽片段Fmoc-Ser(tBu)-Tyr(tBu)-Leu-Glu(OtBu)-Gly-OH和Fmoc-Lys(AEEA-AEEA-(γ-Glu-(OtBu))-monoButylOctadecanate)-OH片段按照氨基酸序列依次偶联。
所述多肽片段、缩合试剂、有机碱、多肽合成树脂(HMPB-PEG-AM-PS树脂)的摩尔比为2:2:6:1;多肽片段、缩合试剂、有机碱、多肽合成树脂(HMPB-PEG-AM-PS树脂)的摩尔比为2:2:6:1;所述保护氨基酸、缩合试剂、有机碱、多肽合成树脂(HMPB-PEG-AM-PS树脂)的摩尔比为1.5:2:6:1;
多肽合成溶剂为DMF,因保护氨基酸不同,多肽合成溶剂与多肽合成树脂的质量比为10~20:1;有机碱为DIEA,缩合剂为HBTU/HOBt。保护氨基酸的液体流速控制在50mL/min~100mL/min。超临界二氧化碳流体洗涤的温度控制在33℃左右,流速范围为40mL/min~60mL/min。其中偶联Fmoc-Trp(Boc)-OH和Fmoc-Ser(tBu)-Tyr(tBu)-Leu-Glu(OtBu)-Gly-OH,采用含有7%2-甲基四氢呋喃的超临界二氧化碳流体洗涤树脂,偶联其它氨基酸或片段采用含有9%甲醇的超临界二氧化碳流体洗涤树脂。
Fmoc被脱除条件:每次200mL1%DBU/2%1-辛硫醇DMF溶液,流速控制在90mL/min,脱Fmoc后洗涤树脂的超临界二氧化碳流体的温度控制在33℃左右,流速范围为40mL/min~60mL/min。除偶联Fmoc-Gln(Trt)-OH时采用9%乙腈作为改性溶剂,偶联其它保护氨基酸和片段采用超临界二氧化碳流体洗涤树脂。
步骤3:
Boc-His(Boc)-Aib-Glu(OtBu)-Gly-Thr(tBu)-Phe-Thr(tBu)-Ser(tBu)-Asp(OtBu)-Val-Ser(Psi(me.me)Pro)-Ser(tBu)-Tyr(tBu)-Leu-Glu(OtBu)-Gly-Gln(Trt)-Ala-Ala-Lys(AEEA-AEEA-(γ-Glu-(OtBu))-monoButylOctadecanate)-Glu(OtBu)-Phe-Ile-Ala-Trp(Boc)-Leu-Val-Arg(Pbf)-Gly-Arg(Pbf)-Gly-HMPB-PEG-AM-PS树脂片段
参照步骤2的数据及操作方法。将24.9g(65.6mmol)HBTU,8.9g(65.6mmol)HOBt溶于120mLDMF,DIEA21.6mL(131.2mmol)和82.4g(65.6mmol)Fmoc-Thr(tBu)-Phe-Thr(tBu)-Ser(tBu)-Asp(OtBu)-Val-Ser(Psi(me.me)Pro)-OH溶于240mLDMF,将2种溶液分别以50mL/min和100mL/min的速度泵入混合器4,经由混合器4和三通阀门一6泵入多肽合成柱10,从多肽合成柱10顶部三通流回混合器4,循环10分钟。排空混合器4和多肽合成柱10里面的溶液,将32℃含9%二氯甲烷的超临界二氧化碳流体以40mL/min的速度经由多肽合成柱10和三通阀门二11,从UV12进入废液收集室,直到在线紫外监测器显示未反应的Fmoc-Thr(tBu)-Phe-Thr(tBu)-Ser(tBu)-Asp(OtBu)-Val-Ser(Psi(me.me)Pro)-OH被冲洗干净。Fmoc脱除条件参照步骤1进行。
将Boc-His(Boc)-Aib-Glu(OtBu)-Gly-OH偶联到多肽树脂上,操作步骤为:将24.9g(65.6mmol)HBTU,8.9g(65.6mmol)HOBt溶于120mLDMF,Boc-His(Boc)-Aib-Glu(OtBu)-Gly-OH 46g(65.6mmol)和DIEA 21.6mL(131.2mmol)溶于240mLDMF,将2种溶液分别以50mL/min和100mL/min的速度泵入混合器4,经由混合器4和三通阀门一6泵入多肽合成柱10,从多肽合成柱10顶部三通流回混合器4,循环10分钟。排空混合器4和多肽合成柱10里面的溶液,将31.5℃含10%乙腈的超临界二氧化碳流体以40mL/min的速度经由多肽合成柱10和三通阀门二11,从UV12进入废液收集室,直到在线紫外监测器显示未反应的Boc-His(Boc)-Aib-Glu(OtBu)-Gly-OH被冲洗干净。经洗涤和真空干燥后得到多肽树脂256g。
索马鲁肽多肽树脂经过三氟乙酸切割溶液处理得到索马鲁肽粗品81g,纯度45.43%,粗品总收率:69.6%。制备出来的索马鲁肽粗品HPLC谱图如图2所示,质谱如图3所示。
实施例1脱保护及偶联一共使用溶剂的量为6.2升,洗涤树脂所用溶剂的量为1.6升。
实施例2:合成Ac-Ser-Val-Val-Val-Arg-Thr-OH
步骤1、Fmoc-Thr(tBu)-HMPA-PEG-SO
Fmoc-Thr(tBu)-HMPA-PEG-SO2-Carboxyl-PS树脂的结构
称取12g取代度为0.34mmol/g的Fmoc-Gly-HMPA-PEG-SO
将DMF以30mL/min的速度经由混合器4和三通阀门一6泵入多肽合成柱10,从多肽合成柱10顶部流回混合器4,循环5分钟使树脂溶胀,排空混合器4和多肽合成柱10里面的溶液。切换试剂瓶3,把40mL 5%哌啶/DMF溶液以30mL/min经由混合器4和三通阀门一6泵入多肽合成柱10,从多肽合成柱10顶部三通流回混合器4,循环6分钟。排空混合器4和多肽合成柱10里面的溶液,将32℃含11%1,4-二氧六环的超临界二氧化碳流体以20mL/min的速度经由多肽合成柱10和三通阀门二11,从UV12进入废液收集室,直到在线紫外监测器显示Fmoc被冲洗干净。
步骤2、合成Fmoc-Arg(pbf)-Thr(tBu)-HMPA-PEG-SO
5.3g(8.16mmol)Fmoc-Arg(Pbf)-OH和2.7mL(16.32mmol)DIEA溶于20mL DMF,3.1(8.16mmol)HBTU和1.1g(8.16mmol)HOBt溶解于20mL DMF,将2种溶液分别以30mL/min的速度泵入混合器4,经由混合器4和三通阀门一6泵入多肽合成柱10,从多肽合成柱10顶部三通流回混合器4,循环10分钟。排空混合器4和多肽合成柱10里面的溶液,将32℃含6%丙酮的超临界二氧化碳流体以20mL/min的速度经由多肽合成柱10和三通阀门二11,从UV12进入废液收集室,直到在线紫外监测器显示未反应的Fmoc-Arg(Pbf)-OH被冲洗干净。
采用步骤1和步骤2的多肽制备方法按照氨基酸序列完成3个Fmoc-Val-OH和Fmoc-Ser(tBu)-OH的偶联及脱保护,得到的H-Ser-Val-Val-Val-Thr(tBu)-HMPA-PEG-SO
保护氨基酸、缩合试剂、有机碱、多肽合成树脂(HMPB-PEG-AM-PS树脂)的摩尔比为2:2:4:1;多肽合成溶剂为DMF,多肽合成溶剂与多肽合成树脂的质量比为10~20:1;有机碱为DIEA,缩合剂为HBTU/HOBt。保护氨基酸的液体流速控制在20mL/min~30mL/min。偶联其它氨基酸所用的洗脱溶剂为采用含6%丙酮的改性溶剂的超临界二氧化碳流体,流体的温度控制在33℃左右,流速范围为20mL/min~30mL/min。
Fmoc被脱除条件:每次用40mL 5%哌啶/DMF溶液,循环流速控制在30mL/min,脱Fmoc后洗涤树脂的洗脱溶剂采用超临界二氧化碳流体,流体的温度控制在32℃,流速范围为20mL/min~30mL/min。
多肽树脂经过三氟乙酸切割溶液处理得到Ac-Ser-Val-Val-Val-Arg-Thr-OH粗品2.37g,纯度81.9%,粗品总收率:82.9%。粗品HPLC见图6,粗品质谱见图7。
实施例2脱保护及偶联一共使用溶剂的量为560毫升,洗涤树脂所用溶剂的总量为210毫升。
实施例3:合成Ser-Tyr-Leu-Glu-Gly
步骤1、Boc-Gly-Merrifield树脂脱Boc
称取20g取代度为0.72mmol/g的Boc-Gly-Merrifield树脂装进多肽合成柱10,将树脂恰好填满柱子,然后拧紧盖子。
将DCM以30mL/min的速度经由混合器4和三通阀门一6泵入多肽合成柱10,从多肽合成柱10顶部流回混合器4,循环3分钟使树脂溶胀,排空混合器4和多肽合成柱10里面的溶液。切换试剂瓶3,把50%TFA/DCM溶液以30mL/min经由混合器4和三通阀门一6泵入多肽合成柱10,从多肽合成柱10顶部三通流回混合器4,循环5分钟。排空混合器4和多肽合成柱10里面的溶液,将32.5℃含7%二硫化碳的超临界二氧化碳流体以20mL/min的速度经由多肽合成柱10和三通阀门二11,从UV12进入废液收集室,一共冲洗10分钟。
步骤2、合成Boc-Glu(OBzl)-Gly-Merrifield树脂
9.7g(28.8mmol)Boc-Glu(OBzl)-OH和9.5mL(57.6mmol)DIEA溶于70mL DMF,18.4mL(28.8mmol)50%T
采用步骤1和步骤2的多肽制备方法按照氨基酸序列,采用Boc-Leu-OH、Boc-Tyr(tBu)-OH和Boc-Ser(Bzl)-OH Boc保护氨基酸把余下氨基酸偶联到多肽树脂上。
Boc保护氨基酸、T
Boc被脱除条件:每次用50%TFA/DCM溶液,循环流速控制在30mL/min,脱Boc后洗涤树脂的洗脱溶剂采用含7%二硫化碳的超临界二氧化碳流体,流体的温度控制在33℃左右,流速范围为20mL/min~30mL/min。
多肽树脂经过氟化氢切割溶液处理得到Ser-Tyr-Leu-Glu-Gly粗品5.76g,纯度84.6%,粗品总收率:70.5%。粗品HPLC见图8,粗品质谱见图9。
实施例3脱保护及偶联一共使用溶剂的量为400毫升,洗涤树脂所用溶剂的总量为110毫升。
对比实施例1:
本实施例与实施例1的不同之处在于每次洗涤部分采用有机溶剂洗涤,即DMF洗3次,甲醇洗3次,二氯甲烷洗3次,其他步骤与实施例1相同,最终得到的索马鲁肽粗品80.7g,纯度46.13%.,粗品总收率:69.5%,制备出来的索马鲁肽粗品HPLC谱图如图4所示,质谱如图5所示。合成脱保护及偶联所用有机溶剂的量为6.2升,洗涤树脂所用的有机溶剂的量为93升。
对比实施例2:
本实施例与实施例2的不同之处在于每次洗涤部分采用有机溶剂洗涤,即DMF洗3次,甲醇洗3次,二氯甲烷洗3次,其他步骤与实施例2相同,最终得到Ac-Ser-Val-Val-Val-Arg-Thr-OH粗品2.28g,纯度46.17%,粗品总收率:66.4%。脱保护及偶联所用有机溶剂的总量为560毫升,洗涤树脂所用的有机溶剂的总量为7570毫升。
对比实施例3:
本实施例与实施例3的不同之处在于每次洗涤部分采用有机溶剂洗涤,即DMF洗3次,甲醇洗3次,二氯甲烷洗3次,其他步骤与实施例2相同,最终得到Ac-Ser-Val-Val-Val-Arg-Thr-OH粗品5.37g,纯度46.58%.,粗品总收率:64.1%。脱保护及偶联所用有机溶剂的总量为400毫升,洗涤树脂所用的有机溶剂的总量为6860毫升。
上述实施例仅为本发明的优选技术方案,而不应视为对于本发明的限制,本发明的保护范围应以权利要求记载的技术方案,包括权利要求记载的技术方案中技术特征的等同替换方案为保护范围,即在此范围内的等同替换改进,也在本发明的保护范围之内。
