抗CCT5结合分子及其使用方法
文献发布时间:2023-06-19 09:29:07
本申请要求2017年12月15日提交的标题为“抗CCT5结合分子及其使用方法(ANTI-CCT5 BINDING MOLECULES AND METHODS OF USE THEREOF)”的美国临时申请62/599,682的优先权,出于所有目的将其内容通过引用以其整体并入。
本申请是与电子格式的序列表一起提交的。序列表以2018年12月14日创建、大小为96千字节的名为735042014640SeqList.txt的文件提供。将在电子格式的序列表中的信息通过引用以其整体并入。
技术领域
在一些方面,本公开文本涉及结合含TCP1伴侣蛋白亚基5(CCT5)的结合分子,特别是涉及抗CCT5抗体(包括抗体片段)。本公开文本进一步涉及抗体缀合物,包括抗体-药物缀合物;双特异性抗体;和重组受体,如含有此类抗体的嵌合抗原受体(CAR)。本公开文本进一步涉及表达此类受体和抗体的基因工程化细胞、以及其在过继细胞疗法中的用途。
背景技术
各种针对肿瘤抗原的结合分子(包括抗体或抗原结合片段)是可得的。在一些情况下,此类结合分子、特别是抗体的抗原结合片段(例如scFv)已被用作嵌合抗原受体(CAR)中的抗原结合结构域,并且在工程化细胞(例如CAR-T细胞)的表面上表达。需要改善的结合分子和工程化肿瘤靶向细胞(如CAR-T细胞)。例如,需要用于在过继细胞疗法中使用的分子和细胞(包括特异性地结合实体瘤靶抗原的抗体片段)、和表达此类人抗体的嵌合受体。本文提供了满足此类需求的实施方案。
发明内容
本文提供了抗体或其抗原结合片段,其中所述抗体或抗原结合片段特异性地结合SEQ ID NO:68(X
在任何所提供的抗体或抗原结合片段的某些实施方案中,X
在任何所提供的抗体或抗原结合片段的一些实施方案中,所述抗体或抗原结合片段包含:重链可变(V
在任何所提供的抗体或抗原结合片段的某些实施方案中,所述抗体或抗原结合片段包含:重链可变(V
在任何所提供的抗体或抗原结合片段的特定实施方案中:所述V
本文提供了抗体或其抗原结合片段,所述抗体或其抗原结合片段包含:重链可变(V
在任何所提供的抗体或抗原结合片段的某些实施方案中:所述V
本文提供了抗体或其抗原结合片段,其中所述抗体或抗原结合片段包含:重链可变(V
在任何所提供的抗体或抗原结合片段的特定实施方案中,所述抗体或抗原结合片段包含V
在任何所提供的抗体或抗原结合片段的一些实施方案中,所述V
在一些实施方案中,任何所提供的抗体或抗原结合片段是抗CCT5抗体或抗原结合片段。
在任何所提供的抗体或抗原结合片段的一些实施方案中,所述抗体或抗原结合片段特异性地结合与由任何所提供的抗体或抗原结合片段特异性地结合的表位相同或重叠的表位。在任何所提供的抗体或抗原结合片段的某些实施方案中,所述抗体或抗原结合片段与任何所提供的抗体或抗原结合片段竞争结合CCT5;竞争结合SEQ ID NO:68(X
在任何所提供的抗体或抗原结合片段的特定实施方案中,所述抗体或抗原结合片段特异性地结合含TCP1伴侣蛋白亚基5(CCT5)蛋白。在任何所提供的抗体或抗原结合片段的一些实施方案中,所述CCT5蛋白是人CCT5蛋白、小鼠CCT5蛋白、或非人灵长类CCT5蛋白。在任何所提供的抗体或抗原结合片段的某些实施方案中,所述CCT5蛋白是人CCT5蛋白。
在任何所提供的抗体或抗原结合片段的特定实施方案中,所述CCT5包含SEQ IDNO:45或46中所示的序列或展现出与SEQ ID NO:45或46至少或约至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高序列同一性的氨基酸序列。在任何所提供的抗体或抗原结合片段的一些实施方案中,所述CCT5蛋白包含SEQ ID NO:45或46中所示的氨基酸序列。在任何所提供的抗体或抗原结合片段的一些实施方案中,所述CCT5蛋白在细胞、任选地肿瘤或癌细胞的表面上表达。
在任何所提供的抗体或抗原结合片段的某些实施方案中,所述抗体或抗原结合片段特异性地结合SEQ ID NO:68(X
在任何所提供的抗体或抗原结合片段的一些实施方案中:所述抗体或抗原结合片段包含重链可变(V
在任何所提供的抗体或抗原结合片段的某些实施方案中:所述CDR-H1和/或CDR-H2包含分别与由种系核苷酸人重链V区段编码的序列内的CDR-H1和/或CDR-H2的氨基酸序列相比为100%相同或具有不多于一个氨基酸差异的序列;和/或所述CDR-L1和/或CDR-L2包含分别与由种系核苷酸人κ或λ链v区段编码的序列内的CDR-L1和/或CDR-L2的氨基酸序列相比100%相同或具有不多于一个氨基酸差异的序列。
在任何所提供的抗体或抗原结合片段的特定实施方案中,所述抗体或抗原结合片段是重组的。在任何所提供的抗体或抗原结合片段的一些实施方案中,所述抗体或抗原结合片段是单克隆的。在任何所提供的抗体或抗原结合片段的某些实施方案中,所述抗体或其抗原结合片段是抗原结合片段。在任何所提供的抗体或抗原结合片段的特定实施方案中,所述抗体或其抗原结合片段是单链片段。在任何所提供的抗体或抗原结合片段的一些实施方案中,所述抗原结合片段包括scFv。在任何所提供的抗体或抗原结合片段的某些实施方案中,所述V
在任何所提供的抗体或抗原结合片段的一些实施方案中,所述抗体或抗原结合片段是包含通过柔性接头连接的抗体V
在任何所提供的抗体或抗原结合片段的特定实施方案中,所述scFv包含SEQ IDNO:52中所示的氨基酸序列,或与SEQ ID NO:52中所示的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在任何所提供的抗体或抗原结合片段的一些实施方案中,所述抗体或其抗原结合片段进一步包含免疫球蛋白恒定区的至少一部分。
在任何所提供的抗体或抗原结合片段的某些实施方案中,所述抗体或其抗原结合片段是全抗体或完整抗体。在任何所提供的抗体或抗原结合片段的特定实施方案中,所述抗体或其抗原结合片段是双特异性抗体。在任何所提供的抗体或抗原结合片段的一些实施方案中,所述抗体或其抗原结合片段进一步特异性地结合第二抗原。在任何所提供的抗体或抗原结合片段的一些实施方案中,所述第二抗原在肿瘤细胞或T细胞上表达。
在任何所提供的抗体或抗原结合片段的某些实施方案中,所述抗体或其抗原结合片段所述第二抗原表达于肿瘤细胞上、任选地表达或异常表达CCT5的肿瘤细胞上,或T细胞上。在任何所提供的抗体或抗原结合片段的特定实施方案中,所述抗体或其抗原结合片段所述第二抗原在肿瘤细胞上表达,并且所述肿瘤细胞是上皮细胞癌的肿瘤细胞。在任何所提供的抗体或抗原结合片段的一些实施方案中,所述第二抗原在T细胞上表达,并且所述T细胞抗原是CD2或CD3。
本文提供了单链细胞表面蛋白,其包含任何所提供的抗体或抗原结合片段、和任选的跨膜结构域。本文提供了单链细胞表面蛋白,其包含特异性地结合CCT5的抗体或抗原结合片段、和任选的跨膜结构域。在任何所提供的单链细胞表面蛋白的某些实施方案中,所述单链细胞表面蛋白是抗原结合片段、任选地scFv。在任何所提供的单链细胞表面蛋白的特定实施方案中,所述抗原结合片段是scFv,并且所述scFv包含SEQ ID NO:52中所示的氨基酸序列或者展现出与SEQ ID NO:52至少85%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性并且结合CCT5或结合包含SEQ ID NO:68所示序列的肽、任选地SEQ ID NO:70-72中任一个所示的肽的氨基酸序列。
本文提供了缀合物,其包含任何所提供的抗体或抗原结合片段以及异源分子或异源部分。本文提供了缀合物,其包含特异性地结合CCT5的抗体或抗原结合片段以及异源分子或异源部分。在任何所提供的缀合物的一些实施方案中,所述异源分子或异源部分是蛋白质、肽、核酸或小分子。在任何所提供的缀合物的某些实施方案中,所述异源分子或异源部分是细胞毒性剂、毒素、放射性同位素、化学治疗剂、裂解肽或细胞因子。在任何所提供的缀合物的特定实施方案中,所述抗体或抗原结合片段和部分直接连接或经由接头间接连接。在任何所提供的缀合物的一些实施方案中,所述抗体或抗原结合片段和所述部分共价或化学连接。在任何所提供的缀合物的某些实施方案中,所述部分是蛋白质或肽,并且所述缀合物是融合蛋白。
本文提供了嵌合抗原受体(CAR),其包含含有任何所提供的抗体或抗原结合片段的细胞外部分和细胞内信号传导区。本文提供了嵌合抗原受体(CAR),其包含细胞外部分和细胞内信号传导区,所述细胞外部分含有特异性地结合CCT5的抗体或抗原结合片段。在任何所提供的嵌合抗原受体的特定实施方案中,所述细胞外部分包含抗原结合片段,并且所述抗原结合片段是scFv。在任何所提供的嵌合抗原受体的一些实施方案中,所述scFv包含SEQ ID NO:52中所示的氨基酸序列或者展现出与SEQ ID NO:52至少85%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性并且结合CCT5或结合包含SEQID NO:68所示序列的肽、任选地SEQ ID NO:70-72中任一个所示的肽的氨基酸序列。
在任何所提供的嵌合抗原受体的某些实施方案中,其中所述细胞内信号传导区是或包含初级信号传导结构域、能够在T细胞中诱导初级激活信号的信号传导结构域、T细胞受体(TCR)组分的信号传导结构域和/或包含基于免疫受体酪氨酸的激活基序(ITAM)的信号传导结构域。在任何所提供的嵌合抗原受体的特定实施方案中,所述细胞内信号传导区是或包含CD3链、任选地CD3-zeta(CD3ζ)链的细胞内信号传导结构域或其信号传导部分。
在任何所提供的嵌合抗原受体的一些实施方案中,所述CAR进一步包含设置在所述细胞外结构域与所述细胞内信号传导区之间的跨膜结构域。在任何所提供的嵌合抗原受体的某些实施方案中,所述跨膜结构域包含CD28的跨膜部分。在任何所提供的嵌合抗原受体的特定实施方案中,所述细胞内信号传导区进一步包括共刺激信号传导结构域。在任何所提供的嵌合抗原受体的一些实施方案中,所述共刺激信号传导结构域包含T细胞共刺激分子的细胞内信号传导结构域或其信号传导部分。在任何所提供的嵌合抗原受体的某些实施方案中,所述共刺激信号传导结构域包含CD28、4-1BB或ICOS的细胞内信号传导结构域或其信号传导部分。在任何所提供的嵌合抗原受体的特定实施方案中,所述共刺激信号传导结构域包含4-1BB的细胞内信号传导结构域或其信号传导部分。在任何所提供的嵌合抗原受体的一些实施方案中,所述共刺激信号传导结构域位于所述跨膜结构域与所述细胞内信号传导结构域之间。
本文提供了多核苷酸,其编码任何所提供的抗体或其抗原结合片段、任何所提供的单链细胞表面蛋白、任何所提供的缀合物或任何所提供的嵌合抗原受体。在某些实施方案中,所提供的多核苷酸进一步编码信号序列,任选地其中所述信号序列是GM-CSF信号序列、CD8信号序列、Igκ信号序列或CD33信号序列。
本文提供了载体,其包含任何所提供的多核苷酸。在任何所提供的载体的特定实施方案中,所述载体是表达载体。在任何所提供的载体的一些实施方案中,所述载体是病毒载体。在任何所提供的载体的某些实施方案中,所述病毒载体是逆转录病毒载体。在任何所提供的载体的特定实施方案中,所述病毒载体是慢病毒载体。在任何所提供的载体的一些实施方案中,所述慢病毒载体源自HIV-1。
本文提供了工程化细胞,其包含任何所提供的载体。本文提供了表达受体的工程化细胞,其包含任何所提供的抗体或抗原结合片段、任何所提供的单链细胞表面蛋白、任何所提供的缀合物或任何所提供的嵌合抗原受体。在任何所提供的工程化细胞的某些实施方案中,所述细胞是免疫细胞。在任何所提供的工程化细胞的特定实施方案中,所述免疫细胞是T细胞。在任何所提供的工程化细胞的一些实施方案中,所述T细胞是CD4+ T细胞或CD8+T细胞。在任何所提供的工程化细胞的某些实施方案中,所述细胞是诱导多能干细胞(iPS细胞)。任何所提供的工程化细胞的特定实施方案进一步包含为嵌合共刺激受体的另一基因工程化抗原受体,所述嵌合共刺激受体特异性地结合另一抗原并且能够将共刺激信号诱导至所述细胞,任选地其中所述另一抗原在与CCT5所在的相同的细胞上表达或是肿瘤抗原。
任何所提供的工程化细胞的一些实施方案进一步包含为抑制性嵌合抗原受体的另一基因工程化抗原受体,所述抑制性嵌合抗原受体特异性地结合另一抗原并且在识别所述第二抗原后能够将抑制性或免疫抑制性或阻遏信号诱导至所述细胞,任选地其中所述第二抗原在正常细胞上表达或在前列腺或乳腺上皮细胞上表达。
本文提供了组合物,其包含任何所提供的抗体或其抗原结合片段、任何所提供的单链细胞表面蛋白、任何所提供的缀合物、任何所提供的嵌合抗原受体或任何所提供的工程化细胞。
任何所提供的组合物的某些实施方案进一步包含药学上可接受的赋形剂。本文提供了治疗方法,其包括将任何所提供的抗体或其抗原结合片段、任何所提供的单链细胞表面蛋白、任何所提供的缀合物、任何所提供的嵌合抗原受体、任何所提供的工程化细胞或任何所提供的组合物给予至患有疾病或障碍的受试者。
本文提供了治疗方法,所述方法包括向受试者给予特异性地结合CCT5的包含抗体或抗原结合片段的结合分子以用于治疗疾病或障碍。在任何所提供的方法的特定实施方案中,所述结合分子是缀合物、任选地抗体-药物缀合物(ADC)。在任何所提供的方法的一些实施方案中,结合分子是嵌合抗原受体,并且向所述受试者给予表达所述嵌合抗原受体的工程化细胞。
在任何所提供的方法的某些实施方案中,所述疾病或障碍与CCT5、任选地异常表达的CCT5、任选地表面CCT5或膜定位的CCT5相关。
在任何所提供的方法的特定实施方案中,所述疾病或障碍是肿瘤或癌症。在任何所提供的方法的一些实施方案中,所述疾病或障碍是白血病、淋巴瘤或实体瘤,任选地肉瘤或上皮恶性肿瘤(carcinoma)。在任何所提供的方法的某些实施方案中,所述疾病或病症是胰腺癌、膀胱癌、结直肠癌、乳腺癌、前列腺癌、肾癌、肝细胞癌、肺癌、卵巢癌、宫颈癌、胰腺癌、直肠癌、甲状腺癌、子宫癌、胃癌、食道癌、头颈癌、黑色素瘤、神经内分泌癌、CNS癌症、脑肿瘤、骨癌或软组织肉瘤。在任何所提供的方法的特定实施方案中,所述疾病或障碍是上皮恶性肿瘤(carcinoma)或上皮细胞癌。在任何所提供的方法的一些实施方案中,所述上皮恶性肿瘤或上皮细胞癌选自鳞状细胞癌(皮肤)、基底细胞癌、胃癌、腺癌、腺鳞癌、间变性癌、移行细胞癌、大细胞癌、小细胞癌、肝细胞癌、肾细胞癌、子宫内膜癌、浸润性乳腺癌、或癌转移。在任何所提供的方法的某些实施方案中,所述疾病或病症是结肠癌、乳腺癌、卵巢癌、前列腺癌、胰腺癌、膀胱癌、或肺癌。
附图说明
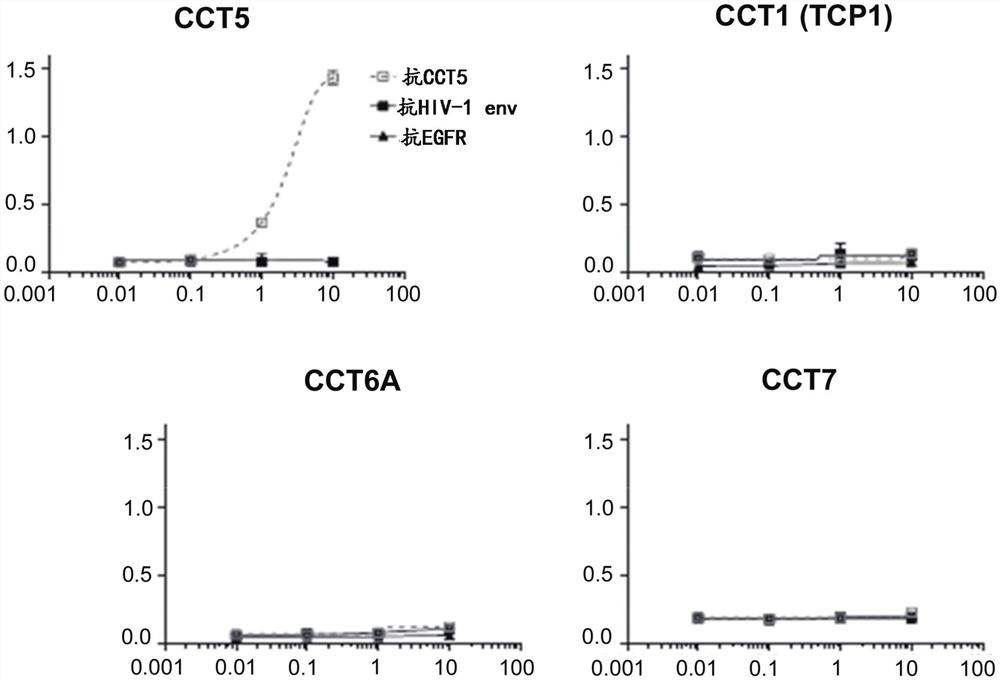
图1A和图1B描绘了抗CCT5抗体与来自TRiC环复合物的重组蛋白的结合。
图2描绘了通过免疫沉淀对细胞表面上的TRiC蛋白的检测。
图3A描绘了各种抗CCT5 CAR的表达,如通过GFP表达和IgG4铰链检测指示的。图3B描述了所指定的CAR构建体的转导效率。
具体实施方式
提供了针对含TCP1伴侣蛋白亚基5(CCT5)的结合分子,包括抗体或抗原结合抗体片段,如单链片段(包括scFv)。在一些方面,CCT5也称为T复合蛋白1(TCP1)亚基ε或TCP1亚基5。还提供了编码此类抗体和抗原结合片段的核酸分子,和用于表达和产生这些抗体或其抗原结合片段的细胞,如重组细胞。还提供了含有此类抗体和抗原结合片段的抗体缀合物,和含有此类抗体和抗原结合片段的重组受体(包括嵌合抗原受体(CAR))。还提供了制备和使用抗体和抗原结合片段以及表达或含有抗体、抗原结合片段、和/或重组受体的细胞(例如,工程化细胞)的方法。在一些实施方案中,此类分子和工程化细胞可以在用于治疗癌症、特别是实体瘤的方法中使用。
在一些方面,由于缺乏合适的靶抗原,用于治疗包括实体瘤的癌症的治疗策略并不完全令人满意。在许多情况下,靶抗原在非靶组织的表面上有一定程度的表达,这在某些方面可导致脱靶活性,包括脱靶毒性。另外,许多肿瘤抗原仅在一种或几种肿瘤类型中表达,从而使许多患者对靶向许多肿瘤抗原的治疗产生抗性和/或无应答。需要包括靶向在肿瘤细胞或组织上表达或在其中差异表达但在非肿瘤细胞或组织上不表达的抗原的策略,如以避免或最小化脱靶毒性。另外,需要在多种肿瘤类型或组织上丰富和/或相对广泛表达的靶抗原。
所提供的实施方案基于在包括实体瘤的广泛多种肿瘤中将CCT5鉴定为肿瘤靶抗原。具体地,CCT5在本文中被鉴定为患者来源的肿瘤浸润淋巴细胞(TIL)、特别是B细胞浸润淋巴细胞的靶抗原,这表明它是相关的肿瘤抗原。TIL的存在牵涉杀伤肿瘤细胞,并且它们在肿瘤中的存在常常与更佳的临床结果相关,包括与针对许多癌症的患者的存活率相关(Nelson(2010)J.Immunol.185(9):4977-82)。在一些情况下,B细胞可占TIL的40%或更多,在其中它们常常富含自身反应性和肿瘤反应性抗体。CCT5是此类TIL的靶标这一发现将其验证为合适的肿瘤抗原,以便靶向以作为用于治疗癌症的治疗性干预。
CCT5是t-复合多肽(tailless complex polypeptide)1(TCP1)环复合物(TRiC)(也称为含TCP1伴侣蛋白[CCT])的一部分,所述复合物是杂合-寡聚复合物,其在一些方面有助于许多细胞蛋白(如肌动蛋白和微管蛋白)的正确折叠。至少有八(8)个亚基组装形成TRiC,它们共享大约30%的同一性。每个亚基被认为具有共同的和特定的功能。CCT5中的突变在一些方面与遗传性感觉和自主神经病伴痉挛性截瘫(HSNSP)相关。
本文的观察结果表明CCT5展现用作靶抗原的所需特征。作为TRiC的一部分的CCT5表达定位于胞浆和核仁中。在正常细胞中,CCT5在细胞表面上通常不表达或以低水平表达,并且因此通常不会被识别为靶抗原。然而,CCT5在多种肿瘤细胞的表面上调或过表达,或在多种肿瘤细胞中异常表达,包括在多种侵袭性癌症适应症中,如乳腺癌(包括p53突变肿瘤)、非小细胞肺癌、宫颈癌、尿道癌、非霍奇金淋巴瘤(NHL)、头颈癌、卵巢癌、睾丸癌等。在一些方面,预期其在多种癌症中而不在正常组织和细胞中的广泛的表面和/或异常表达降低或最小化了脱靶活性和/或毒性。
在一些实施方案中,所提供的结合分子(包括抗体或其抗原结合片段)、含有此类结合分子(例如ADC)的缀合物或表达此类结合分子的工程化细胞(例如CAR表达T细胞)特异性地结合CCT5(例如SEQ ID NO:45或SEQ ID NO:46中所示;UniProt号P4883)。在一些方面,所提供的结合分子展现跨物种反应性,使得它们特异性地结合人CCT5和一种或多种其他物种CCT5,如一种或多种灵长类或啮齿动物物种的CCT5。CCT5在不同的哺乳动物物种之间展现高序列同源性,其中在人与小鼠或大鼠CCT5之间有大约96%同源性,并且在人类与灵长类物种之间有甚至更高的同一性。在一些方面,物种之间的高序列同源性是有利的,因为它允许在体内动物模型中使用抗体来评估功效(包括抗肿瘤活性)、和/或对毒性的影响。
所提供的实施方案包括表达重组受体(例如CAR)的工程化细胞,用于与过继细胞疗法结合使用。细胞疗法(如基于T细胞的疗法,例如过继T细胞疗法(包括涉及给予表达对目的疾病或障碍具有特异性的嵌合受体(如嵌合抗原受体(CAR)和/或其他重组抗原受体)的细胞的那些,以及其他过继免疫细胞和过继T细胞疗法))可以在癌症以及其他疾病和障碍的治疗方面有效。T细胞表面上重组受体(如嵌合抗原受体(CAR))的工程化表达使得能够重定向T细胞特异性。然而,在某些情况下,过继细胞疗法的可行方法可能并不总是完全令人满意。在一些情况下,最佳功效可能取决于所给予细胞识别并结合靶标(例如,靶抗原)的能力,所述能力常常是未充分实现的。在一些方面,所提供的实施方案是基于以下发现:将所提供的抗CCT5抗体,如抗原结合片段(例如scFv)重组为用于在工程化细胞的表面上表达的CAR是特别有效的,从而产生CAR+ T细胞的靶特异性活性。观察到这种活性针对广泛多种的癌细胞系。
本申请中提及的所有出版物(包括专利文献、科学文章和数据库)出于所有目的通过引用以其整体并入,在程度上如同每个单独的出版物通过引用单独并入。如果本文所述的定义与通过引用并入本文的专利、申请、公开申请和其他出版物中阐述的定义相反或在其他方面不一致,则本文所述的定义优先于通过引用并入本文的定义。
本文使用的章节标题仅用于组织目的,而不应解释为限制所描述的主题。
I.CCT5结合分子
在一些方面提供了结合分子(包括抗体或其抗原结合片段),所述结合分子特异性地结合CCT5蛋白或特异性地结合SEQ ID NO:68(X
A.抗CCT5抗体
提供了抗CCT5抗体,包括功能抗原结合片段。在一些实施方案中,抗体包括重链可变区和/或轻链可变区。在一些实施方案中,抗体包括重链可变区和轻链可变区。抗体包括特异性地结合CCT5(例如人CCT5)的抗体。所提供的抗CCT5抗体包括人抗体。CCT5结合分子包括分离的或重组的分子。
本文中的术语“抗体”在最广泛的意义上使用,并且包括多克隆和单克隆抗体,包括完整抗体和功能性(抗原结合)抗体片段,包括片段抗原结合(Fab)片段、F(ab')2片段、Fab'片段、Fv片段、重组IgG(rIgG)片段、能够特异性地结合抗原的重链可变(V
术语“互补决定区”和“CDR”(与“高变区”或“HVR”同义)已知是指抗体可变区内的氨基酸的非连续序列,其赋予抗原特异性和/或结合亲和力。通常,在每个重链可变区中有三个CDR(CDR-H1、CDR-H2、CDR-H3),并且在每个轻链可变区中有三个CDR(CDR-L1、CDR-L2、CDR-L3)。“框架区”和“FR”已知是指重链和轻链的可变区的非CDR部分。通常,在每个全长重链可变区中有四个FR(FR-H1、FR-H2、FR-H3和FR-H4),并且在每个全长轻链可变区中有四个FR(FR-L1、FR-L2、FR-L3和FR-L4)。
给定CDR或FR的精确氨基酸序列边界可以使用许多熟知的方案中的任一种容易地确定,包括以下文献中所述的那些:Kabat等人(1991),“Sequences of Proteins ofImmunological Interest,”第5版Public Health Service,National Institutes ofHealth,贝塞斯达,马里兰州D(“Kabat”编号方案);Al-Lazikani等人,(1997)JMB 273,927-948(“Chothia”编号方案);MacCallum等人,J.Mol.Biol.262:732-745(1996),“Antibody-antigen interactions:Contact analysis and binding site topography,”J.Mol.Biol.262,732-745”。(“Contact”编号方案);Lefranc MP等人,“IMGT uniquenumbering for immunoglobulin and T cell receptor variable domains and Igsuperfamily V-like domains,”Dev Comp Immunol,2003年1月;27(1):55-77(“IMGT”编号方案);Honegger A和Plückthun A,“Yet another numbering scheme forimmunoglobulin variable domains:an automatic modeling and analysis tool,”JMol Biol,2001年6月8日;309(3):657-70(“Aho”编号方案);以及Martin等人,“Modelingantibody hypervariable loops:a combined algorithm,”PNAS,1989,86(23):9268-9272(“AbM”编号方案)。
给定CDR或FR的边界可能根据用于鉴定的方案而变化。例如,Kabat方案是基于结构比对,而Chothia方案是基于结构信息。Kabat和Chothia方案的编号都是基于最常见的抗体区域序列长度,其中通过插入字母(例如“30a”)提供插入,并且在一些抗体中出现缺失。这两种方案将某些插入和缺失(“插入缺失(indel)”)放置在不同的位置,从而产生不同的编号。Contact方案是基于对复杂晶体结构的分析,并且在许多方面与Chothia编号方案相似。AbM方案是Kabat与Chothia定义之间的折衷,是基于Oxford Molecular's AbM抗体建模软件使用的方案。
下表1列出了分别通过Kabat、Chothia、AbM和Contact方案鉴定的CDR-L1、CDR-L2、CDR-L3以及CDR-H1、CDR-H2、CDR-H3的示例性位置边界。对于CDR-H1,使用Kabat和Chothia两种编号方案列出残基编号。FR位于CDR之间,例如,FR-L1位于CDR-L1之前,FR-L2位于CDR-L1与CDR-L2之间,FR-L3位于CDR-L2与CDR-L3之间,等等。应注意,因为所示的Kabat编号方案在H35A和H35B处放置插入,所以当使用所示的Kabat编号惯例进行编号时,Chothia CDR-H1环的末端根据环的长度在H32与H34之间变化。
表1.根据各种编号方案的CDR边界。
因此,除非另有规定,否则应当理解给定抗体或其区域(如其可变区)的“CDR”或“互补决定区”或单个指定的CDR(例如,CDR-H1、CDR-H2、CDR-H3)涵盖如由任何上述方案所定义的一个(或特定)互补决定区。例如,在声明特定的CDR(例如,CDR-H3)含有给定V
同样,除非另有规定,否则给定抗体或其区域如其可变区的FR或单独指定的一个或多个FR(例如,FR-H1、FR-H2、FR-H3、FR-H4)应理解为涵盖如任何已知方案所定义的一个(或特定)框架区。在一些情形中,规定了用于鉴定特定的CDR、FR或者多个特定的FR或CDR的方案,如通过Kabat、Chothia、AbM或Contact方法定义的CDR。在其他情况下,给出了CDR或FR的具体氨基酸序列。
术语“可变区”或“可变结构域”是指抗体重链或轻链的参与抗体与抗原的结合的结构域。天然抗体的重链和轻链的可变区(分别为V
所提供的抗体包括抗体片段。“抗体片段”或“抗原结合片段”是指除了完整抗体以外的分子,其包含完整抗体的结合完整抗体所结合的抗原的一部分。抗体片段的例子包括但不限于Fv、Fab、Fab'、Fab'-SH、F(ab')2;双抗体;线性抗体;重链可变(V
单结构域抗体(sdAb)是包含抗体的全部或部分重链可变区或者全部或部分轻链可变区的抗体片段。在某些实施方案中,单结构域抗体是人单结构域抗体。在一些实施方案中,所提供的抗体包括含有重链可变(V
抗体片段可以通过各种技术制备,包括但不限于完整抗体的蛋白水解消化以及通过重组宿主细胞产生。在一些实施方案中,抗体是重组产生的片段,如包含天然不存在的排列的片段(如具有通过合成接头(例如,肽接头)连接的两个或更多个抗体区或链的那些),和/或可以不通过酶消化天然存在的完整抗体产生的片段。在一些方面,抗体片段是scFv。
“人源化”抗体是这样的抗体,其中全部或基本上全部CDR氨基酸残基源自非人CDR并且全部或基本上全部FR氨基酸残基源自人FR。人源化抗体任选地可以包括源自人抗体的抗体恒定区的至少一部分。非人抗体的“人源化形式”是指非人抗体的变体,其已经经历人源化以通常降低对人的免疫原性,同时保留亲本非人抗体的特异性和亲和力。在一些实施方案中,人源化抗体中的一些FR残基被来自非人抗体(例如,衍生出CDR残基的抗体)的相应残基取代,例如以恢复或改善抗体特异性或亲和力。(参见,例如Queen,美国专利号5,585,089和Winter,美国专利号5,225,539。)此类嵌合单克隆抗体和人源化单克隆抗体可以通过重组DNA技术产生。
所提供的抗体或抗原结合片段(包括抗CCT5抗体或片段)包括人抗体。“人抗体”是具有与人或人细胞或者利用人抗体库或其他人抗体编码序列(包括人抗体文库)的非人来源产生的抗体的氨基酸序列对应的氨基酸序列的抗体。所述术语不包括包含非人抗原结合区的非人抗体的人源化形式,如所有或基本上所有CDR都是非人的那些。所述术语包括人抗体的抗原结合片段。
人抗体可以通过将免疫原给予至转基因动物来制备,所述转基因动物已经被修饰以响应于抗原激发产生完整人抗体或具有人可变区的完整抗体。此类动物通常含有人免疫球蛋白基因座的全部或一部分,其替代内源免疫球蛋白基因座,或者其存在于染色体外或随机整合至动物染色体中。在此类转基因动物中,通常已经使内源免疫球蛋白基因座失活。人抗体也可以源自含有源自人库的抗体编码序列的人抗体文库,包括噬菌体展示和无细胞文库。
所提供的抗体包括单克隆抗体,包括单克隆抗体片段。如本文所用的术语“单克隆抗体”是指从基本上同质抗体的群体(即,构成所述群体的单独抗体是相同的,但含有天然存在的突变或在单克隆抗体制剂的产生期间产生的可能变体除外,此类变体通常以少量存在)获得或在所述群体内的抗体。与通常包括针对不同表位的不同抗体的多克隆抗体制剂相反,单克隆抗体制剂的每种单克隆抗体针对抗原上的单个表位。所述术语不应解释为需要通过任何特定方法产生抗体。单克隆抗体可以通过多种技术制备,包括但不限于从杂交瘤产生、重组DNA方法、噬菌体展示和其他抗体展示方法。
在一些实施方案中,抗体(例如,抗CCT5抗体或其抗原结合片段)含有如所述的重链可变(V
在一些实施方案中,抗体(例如其抗原结合片段)具有重链可变(V
在一些实施方案中,所提供的抗体或其抗原结合片段的V
提供了抗体或其抗原结合片段,所述抗体或其抗原结合片段包括包含重链互补决定区1(CDR-H1)、CDR-H2和CDR-H3的重链可变(V
在一些实施方案中,所提供的抗体或其抗原结合片段的V
在一些实施方案中,所提供的抗体或其抗原结合片段的VH区含有在SEQ ID NO:1中所示的V
在一些实施方案中,所提供的抗体或其抗原结合片段的V
在一些实施方案中,所提供的抗体或其抗原结合片段包含CDR-H1、CDR-H2和CDR-H3,所述CDR-H1、CDR-H2和CDR-H3分别包含在SEQ ID NO:1中所示的V
在本文所提供的抗体或其抗原结合片段的一些实施方案中,V
在一些实施方案中,所提供的抗体或其抗原结合片段包含含有在SEQ ID NO:1中所示的氨基酸序列的V
还提供具有与此类序列至少或至少约90%、91%、92%、93%、94%、95%、96%、97%、98%或99%相同的序列的抗体及其抗原结合片段。
在一些任何此类实施方案中,抗体或抗原结合片段是仅重链、仅V
在一些实施方案中,包含V
在一些实施方案中,抗体(例如其抗原结合片段)具有轻链可变(V
在一些实施方案中,所提供的抗体或其抗原结合片段的V
在一些实施方案中,所提供的抗体或其抗原结合片段包括包含轻链互补决定区1(CDR-L1)、CDR-L2和CDR-L3的轻链可变(V
在一些实施方案中,所提供的抗体或其抗原结合片段的V
在一些实施方案中,所提供的抗体或其抗原结合片段的V
在一些实施方案中,所提供的抗体或其抗原结合片段的V
在一些实施方案中,所提供的抗体或其抗原结合片段包含CDR-L1、CDR-L2和CDR-L3,所述CDR-L1、CDR-L2和CDR-L3分别包含在SEQ ID NO:2中所示的V
在本文所提供的抗体或其抗原结合片段的一些实施方案中,V
在一些实施方案中,所提供的抗体或其抗原结合片段包含含有在SEQ ID NO:2中所示的氨基酸序列的V
还提供具有与此类序列至少或至少约90%、91%、92%、93%、94%、95%、96%、97%、98%或99%相同的序列的抗体。
在一些实施方案中,抗体或其抗原结合片段的V
在一些实施方案中,抗体或抗原结合片段以任何顺序或取向包含一个或多个重链可变(V
在一些实施方案中,抗CCT5抗体是抗原结合片段。在一些实施方案中,抗原结合片段选自抗原结合的片段(Fab)片段、F(ab')
在一些实施方案中,抗体或其抗原结合片段是单链抗体片段,如包含重链可变(V
在一些方面,富含甘氨酸和丝氨酸(和/或苏氨酸)的接头包括至少80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的此类氨基酸。在一些实施方案中,它们包括至少或至少约50%、55%、60%、70%或75%的甘氨酸、丝氨酸和/或苏氨酸。在一些实施方案中,接头基本上完全由甘氨酸、丝氨酸和/或苏氨酸组成。接头的长度通常在约5个与约50个氨基酸之间,通常在为或约10个与为或约30个之间,例如10个、11个、12个、13个、14个、15个、16个、17个、18个、19个、20个、21个、22个、23个、24个、25个、26个、27个、28个、29个或30个,并且在一些例子中长度在10个与25个氨基酸之间。示例性接头包括具有序列GGGGS(4GS;SEQ ID NO:47)或GGGS(3GS;SEQ ID NO:48)的不同数量的重复,如在这种序列的2、3、4和5个重复之间的接头。示例性接头包括具有SEQ ID NO:49(GGGGSGGGGSGGGGS)所示序列或由其组成的那些接头。示例性接头进一步包括具有SEQ ID NO:50(GSTSGSGKPGSGEGSTKG)所示序列或由其组成的那些接头。
在一些方面,本文所提供的scFv包含SEQ ID NO:52中所示的氨基酸序列,或者具有与SEQ ID NO:52中所示的氨基酸序列具有至少或至少约90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。在一些实施方案中,scFv具有SEQID NO:52中所示的序列。
在一些实施方案中,抗体或抗原结合片段含有V
所提供的抗体(例如抗原结合片段)包括人抗体。在所提供的人抗CCT5抗体(例如,抗原结合片段)的一些实施方案中,人抗体含有V
在一些实施方案中,人抗体或其抗原结合片段含有CDR-H1,所述CDR-H1与由种系核苷酸人重链V区段编码的序列内的相应CDR-H1区的氨基酸序列具有至少95%、96%、97%、98%、99%或100%序列同一性。例如,在一些实施方案中,人抗体含有具有如下序列的CDR-H1,所述序列与由种系核苷酸人重链V区段编码的序列内的相应CDR-H1区相比为100%相同或具有不多于一个、两个或三个氨基酸差异。
在一些实施方案中,人抗体或其抗原结合片段含有CDR-H2,所述CDR-H2与由种系核苷酸人重链V区段编码的序列内的相应CDR-H2区的氨基酸序列具有至少95%、96%、97%、98%、99%或100%序列同一性。例如,在一些实施方案中,人抗体含有具有如下序列的CDR-H2,所述序列与由种系核苷酸人重链V区段编码的序列内的相应CDR-H2区相比为100%相同或具有不多于一个、两个或三个氨基酸差异。
在一些实施方案中,人抗体或其抗原结合片段含有CDR-H3,所述CDR-H3与由种系核苷酸人重链V区段、D区段和J区段编码的序列内的相应CDR-H3区的氨基酸序列具有至少95%、96%、97%、98%、99%或100%序列同一性。例如,在一些实施方案中,人抗体含有具有如下序列的CDR-H3,所述序列与由种系核苷酸人重链V区段、D区段和J区段编码的序列内的相应CDR-H3区相比为100%相同或具有不多于一个、两个或三个氨基酸差异。
在一些实施方案中,人抗体或其抗原结合片段含有CDR-L1,所述CDR-L1与由种系核苷酸人轻链V区段编码的序列内的相应CDR-L1区的氨基酸序列具有至少95%、96%、97%、98%、99%或100%序列同一性。例如,在一些实施方案中,人抗体含有具有如下序列的CDR-L1,所述序列与由种系核苷酸人轻链V区段编码的序列内的相应CDR-L1区相比为100%相同或具有不多于一个、两个或三个氨基酸差异。
在一些实施方案中,人抗体或其抗原结合片段含有CDR-L2,所述CDR-L2与由种系核苷酸人轻链V区段编码的序列内的相应CDR-L2区的氨基酸序列具有至少95%、96%、97%、98%、99%或100%序列同一性。例如,在一些实施方案中,人抗体含有具有如下序列的CDR-L2,所述序列与由种系核苷酸人轻链V区段编码的序列内的相应CDR-L2区相比为100%相同或具有不多于一个、两个或三个氨基酸差异。
在一些实施方案中,人抗体或其抗原结合片段含有CDR-L3,所述CDR-L3与由种系核苷酸人轻链V区段和J区段编码的序列内的相应CDR-L3区的氨基酸序列具有至少95%、96%、97%、98%、99%或100%序列同一性。例如,在一些实施方案中,人抗体含有具有如下序列的CDR-L3,所述序列与由种系核苷酸人轻链V区段和J区段编码的序列内的相应CDR-L3区相比为100%相同或具有不多于一个、两个或三个氨基酸差异。
在一些实施方案中,人抗体或其抗原结合片段包含含有人种系基因区段序列的框架区。例如,在一些实施方案中,人抗体含有V
还提供编码抗体和/或其部分(例如链)的核酸,例如多核苷酸。所提供的核酸包括编码本文所述的任何所提供的抗体或抗原结合片段(例如抗CCT5抗体或抗原结合片段)的那些。还提供了编码一种或多种抗体和/或其部分的核酸(例如多核苷酸),例如编码本文所述的抗CCT5抗体(例如抗原结合片段)和/或另一抗体和/或其部分(例如,结合其他靶抗原的抗体和/或其部分)中的一种或多种的那些核酸。核酸可以包括包含天然和/或非天然存在的核苷酸和碱基的那些,例如包括具有骨架修饰的那些。术语“核酸分子”、“核酸”和“多核苷酸”可以互换使用,并且是指核苷酸的聚合物。核苷酸的此类聚合物可以含有天然和/或非天然核苷酸,并且包括但不限于DNA、RNA和PNA。“核酸序列”是指构成核酸分子或多核苷酸的核苷酸的线性序列。
所提供的实施方案进一步包括用于表达和产生抗体和其他抗原结合蛋白的载体和宿主细胞以及其他表达系统(包括真核和原核宿主细胞(包括细菌、丝状真菌和酵母)以及哺乳动物细胞(如人细胞))以及无细胞表达系统。
还提供例如用于产生抗体或其抗原结合片段的含有核酸(例如多核苷酸)的载体以及含有所述载体的宿主细胞。还提供用于产生抗体或其抗原结合片段的方法。核酸可以编码包含抗体的V
在进一步的实施方案中,提供包含此类核酸的一种或多种载体(例如,表达载体)。在进一步的实施方案中,提供包含此类核酸的宿主细胞。在一个这样的实施方案中,宿主细胞包含载体(例如,已经用载体转化),所述载体包含编码含有抗体的V
还提供了制备所提供抗体(包括抗原结合片段)的方法。对于重组产生,可以将编码例如如上所述的抗体或片段的核酸序列或多核苷酸分离并插入一种或多种载体中,以在宿主细胞中进一步克隆和/或表达。使用常规程序(例如,通过使用能够与编码抗体重链和轻链的基因特异性地结合的寡核苷酸探针)可以容易地分离和测序此类核酸序列。在一些实施方案中,提供了制备抗体的方法,其中所述方法包括在适用于表达抗体的条件下培养包含编码如以上所提供的抗体的核酸序列的宿主细胞,并且任选地从宿主细胞(或宿主细胞培养基)回收所述抗体。
除原核生物之外,真核微生物(如丝状真菌或酵母)也是编码抗体的载体的合适的克隆或表达宿主,包括其糖基化途径已经被修饰为模拟或接近人细胞中的那些糖基化途径从而产生具有部分或完全人糖基化模式的抗体的真菌和酵母菌株。参见Gerngross,Nat.Biotech.22:1409-1414(2004)和Li等人,Nat.Biotech.24:210-215(2006)。
可用于表达多肽的示例性真核细胞包括但不限于COS细胞,包括COS 7细胞;293细胞,包括293-6E细胞;CHO细胞,包括CHO-S、DG44.Lec13 CHO细胞和FUT8 CHO细胞;
在一些实施方案中,本文所提供的抗体或抗原结合片段是在无细胞系统中产生的。示例性无细胞系统描述于例如Sitaraman等人,Methods Mol.Biol.498:229-44(2009);Spirin,Trends Biotechnol.22:538-45(2004);Endo等人,Biotechnol.Adv.21:695-713(2003)中。
1.变体和修饰
在某些实施方案中,与本文所述的抗体的序列相比,抗体(例如抗原结合片段)包含一个或多个氨基酸变异,例如取代、缺失、插入和/或突变。示例性变体包括被设计为改善抗体的结合亲和力和/或其他生物学特性的那些。可以通过在编码所述抗体的核苷酸序列中引入适当的修饰或通过肽合成来制备抗体的氨基酸序列变体。此类修饰包括例如抗体氨基酸序列内的残基缺失和/或插入和/或取代。可以进行缺失、插入和取代的任何组合以获得最终的构建体,条件是最终的构建体具有所需的特征(例如抗原结合)。
在某些实施方案中,例如与本文所述的抗体序列相比和/或与天然库(例如人类库)的序列相比,抗体(例如抗原结合片段)包含一个或多个氨基酸取代。用于取代诱变的目的位点包括CDR和FR。可以将氨基酸取代引入目的抗体中,并针对如下所需活性筛选产物:例如,保留/改善的抗原结合、降低的免疫原性、改善的半衰期和/或改善的效应子功能,例如促进抗体依赖性细胞毒性(ADCC)或补体依赖性细胞毒性(CDC)的能力。
在一些实施方案中,亲本抗体(例如人源化或人抗体)的CDR内的一个或多个残基被取代。在一些实施方案中,进行取代以将序列或序列中的位置恢复为种系序列(例如在种系(例如人种系)中发现的抗体序列),例如以降低例如在向人受试者给予后免疫原性的可能性。
在一些实施方案中,在CDR“热点”(即,由在体细胞成熟过程中经历高频率突变的密码子编码的残基(参见例如Chowdhury,Methods Mol.Biol.207:179-196(2008))和/或接触抗原的残基)中进行改变,并对所得的变体V
在某些实施方案中,取代、插入或缺失可以在一个或多个CDR内发生,只要此类改变基本上不降低抗体结合抗原的能力。例如,可以在CDR中进行基本上不降低结合亲和力的保守改变(例如,如本文所提供的保守取代)。例如,此类改变可以在CDR中的抗原接触残基之外。在上文提供的变体V
氨基酸序列插入包括长度范围从一个残基到含有一百个或更多个残基的多肽的氨基末端和/或羧基末端融合,以及单个或多个氨基酸残基的序列内插入。末端插入的例子包括具有N末端甲硫酰基残基的抗体。抗体分子的其他插入变体包括抗体的N末端或C末端与增加抗体的血清半衰期的酶或多肽的融合物。
在某些实施方案中,通过例如以下方式改变抗体以增加或降低抗体被糖基化的程度:通过去除或插入一个或多个糖基化位点、通过改变氨基酸序列和/或通过修饰附接至糖基化位点的一个或多个寡糖(例如,使用特定细胞系)。在一些实施方案中,去除或插入N连接的糖基化,其是在共有序列-Asn-Xaa-Ser/Thr中的天冬酰胺处出现的糖基化位点。
示例性修饰、变体和细胞系描述于例如,专利公开号US 2003/0157108、US 2004/0093621、US 2003/0157108;WO 2000/61739;WO 2001/29246;US 2003/0115614;US 2002/0164328;US 2004/0093621;US 2004/0132140;US 2004/0110704;US 2004/0110282;US2004/0109865;WO 2003/085119;WO 2003/084570;WO 2005/035586;WO 2005/035778;WO2005/053742;WO 2002/031140;Okazaki等人J.Mol.Biol.336:1239-1249(2004);Yamane-Ohnuki等人Biotech.Bioeng.87:614(2004);Ripka等人Arch.Biochem.Biophys.249:533-545(1986);美国专利申请号US 2003/0157108 A1,Presta,L;和WO 2004/056312 A1,Yamane-Ohnuki等人Biotech.Bioeng.87:614(2004);Kanda,Y.等人,Biotechnol.Bioeng.,94(4):680-688(2006);和WO 2003/085107;WO 2003/011878(Jean-Mairet等人);美国专利号6,602,684(Umana等人);和US 2005/0123546(Umana等人);WO 1997/30087(Patel等人);WO 1998/58964(Raju,S.);和WO 1999/22764(Raju,S.)中。
经修饰的抗体包括在Fc区中具有一个或多个氨基酸修饰的那些,例如具有在一个或多个氨基酸位置处包含氨基酸修饰(例如取代)的人Fc区序列或恒定区的其他部分(例如人IgG1、IgG2、IgG3或IgG4Fc区)的那些。
可以进行此类修饰,例如以改善半衰期,改变与一种或多种类型的Fc受体的结合和/或改变效应子功能。
变体还包括半胱氨酸工程化抗体,如“thioMAb”和其他半胱氨酸工程化变体,其中抗体的一个或多个残基被半胱氨酸残基取代,以便在可接近位点产生反应性硫醇基团,例如用于药剂和接头-药剂的缀合,从而产生免疫缀合物。半胱氨酸工程化抗体描述于例如美国专利号7,855,275和7,521,541中。
在一些实施方案中,将抗体(例如,抗原结合片段)修饰为含有另外的非蛋白质部分,包括水溶性聚合物。示例性聚合物包括但不限于聚乙二醇(PEG)、乙二醇/丙二醇的共聚物、羧甲基纤维素、葡聚糖、聚乙烯醇、聚乙烯吡咯烷酮、聚1,3-二氧戊环、聚1,3,6-三噁烷、乙烯/马来酸酐共聚物、聚氨基酸(均聚物或随机共聚物)、和葡聚糖或聚(n-乙烯基吡咯烷酮)聚乙二醇、聚丙二醇均聚物、聚氧化丙烯/氧化乙烯共聚物、聚氧乙基化多元醇(例如,甘油)、聚乙烯醇及其混合物。聚乙二醇丙醛由于其在水中的稳定性而可以在制备中具有优势。所述聚合物可以具有任何分子量,并且可以有支链或无支链。附接至抗体的聚合物的数量可以变化,并且如果附接超过一种聚合物,则它们可以是相同或不同的分子。通常,用于衍生化的聚合物的数量和/或类型可以基于包括但不限于以下的考虑因素来确定:要改善的抗体的特定特性或功能、抗体衍生物是否将要用于在确定条件下的疗法等。
2.示例性特征
在一些方面,所提供的结合分子(包括抗体或其抗原结合片段或含有此类抗体或抗原结合片段的缀合物或嵌合抗原受体)具有一个或多个指定的功能特征,如结合特性,包括与特定表位的结合。
在一些实施方案中,结合分子(包括抗体或其抗原结合片段或含有此类抗体或抗原结合片段的缀合物或嵌合抗原受体)特异性地结合CCT5蛋白。在一些实施方案中,CCT5蛋白是哺乳动物CCT5,如或包括人CCT5、非人灵长类(例如食蟹猴)CCT5蛋白或啮齿动物(例如小鼠或大鼠)CCT5蛋白。在一些实施方案中,抗体或抗原结合片段与哺乳动物CCT5蛋白(包括与天然存在的CCT5变体,如某些剪接变体或等位基因变体)结合。
在一些实施方案中,所提供的结合分子(包括抗体或其抗原结合片段或含有此类抗体或抗原结合片段的缀合物或嵌合抗原受体)特异性地结合人CCT5蛋白,如人CCT5蛋白的表位或区域,如包含SEQ ID NO:45或SEQ ID NO:46的氨基酸序列的人CCT5蛋白(例如UniProt号P48643)、其等位基因变体或剪接变体、这种人CCT5的物种变体或表位或区域。在一些实施方案中,抗体特异性地结合展现出与SEQ ID NO:45或SEQ ID NO:46至少或约至少或为75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高序列同一性的CCT5蛋白。在一些实施方案中,所提供的结合分子(包括抗体或其抗原结合片段或含有此类抗体或抗原结合片段的缀合物或嵌合抗原受体)特异性地结合SEQ ID NO:45或SEQ ID NO:46中所示的CCT5蛋白。
在一些实施方案中,所提供的结合分子(包括抗体或其抗原结合片段或含有此类抗体或抗原结合片段的缀合物或嵌合抗原受体)结合人CCT5(例如SEQ ID NO:45或SEQ IDNO:46中所示的),并且在一些方面还结合一种或多种其他物种的CCT5。CCT5在哺乳动物物种之间展现出高序列同一性。灵长类(包括食蟹猴)CCT5的各种序列展现出与人CCT5的100%序列同一性,并且啮齿动物物种的CCT5(如大鼠或小鼠CCT5)展现出与人CCT5的大于96%序列同一性。在一些实施方案中,所提供的结合分子(包括抗体或其抗原结合片段或含有此类抗体或抗原结合片段的缀合物或嵌合抗原受体)结合灵长类CCT5(如食蟹猴CCT5)(例如UniProt Q4R6V2;SEQ ID NO:45或SEQ ID NO:46中所示的)。在一些实施方案中,所提供的结合分子(包括抗体或其抗原结合片段或含有此类抗体或抗原结合片段的缀合物或嵌合抗原受体)结合大鼠CCT5(例如UniProt P80316;SEQ ID NO:58或SEQ ID NO:59中所示的)。在一些实施方案中,所提供的结合分子(包括抗体或其抗原结合片段或含有此类抗体或抗原结合片段的缀合物或嵌合抗原受体)结合小鼠CCT5(例如UniProt P80316;SEQ IDNO:83或SEQ ID NO:84中所示的)。
抗体或其他结合分子结合CCT5蛋白或特异性地结合CCT5蛋白的观察结果并不一定意味着其结合每种物种的CCT5蛋白或与不同物种的CCT5蛋白具有相同亲和力。在一些实施方案中,与CCT5蛋白结合的特征(如与其特异性地结合和/或在某种程度上以特定亲和力结合的能力)在一些实施方案中是指对于人CCT5蛋白的能力,并且抗体对于另一物种(如小鼠)的CCT5蛋白可能不具有此特征、或可能未展现出相同的结合程度。
在一个实施方案中,抗CCT5抗体与不相关的非CCT5蛋白(如非人CCT5蛋白或其他非CCT5蛋白)的结合程度为抗体与人CCT5蛋白的结合的小于或小于约10%,如例如通过放射免疫测定(RIA)所测量。在一些实施方案中,所提供的抗体包括这样的抗体,其中与小鼠CCT5蛋白的结合为抗体与人CCT5蛋白的结合的小于或等于或约10%。在一些实施方案中,所提供的抗体包括这样的抗体,其中与小鼠CCT5蛋白的结合与抗体与人CCT5蛋白的结合相似或大致相同。
在一些实施方案中,抗体特异性地结合和/或在某种程度上以特定亲和力结合CCT5蛋白(例如人CCT5或小鼠CCT5蛋白)。
在一些实施方案中,所提供的抗体能够以至少一定的亲和力结合CCT5蛋白(如人CCT5蛋白),如通过多种已知方法中的任一种所测量。在一些实施方案中,亲和力由平衡解离常数(K
已知多种测定用于评估结合亲和力和/或确定结合分子(例如,抗体或其片段)是否特异性地结合特定配体(例如,抗原,如CCT5蛋白)。确定结合分子(例如,抗体)对抗原(例如CCT5,如人CCT5或小鼠CCT5)的结合亲和力的方法是已知的。例如,若干种结合测定是熟知的。例如,在一些实施方案中,使用表面等离子体共振(SPR)分析,可以将
在分子结合至表面或从表面解离时,SPR测量传感器表面处分子浓度的变化。SPR信号的变化与靠近表面的质量浓度变化成正比,从而允许测量两个分子之间的结合动力学。可以通过监测当缓冲液经过芯片时折射率关于时间的变化来确定与复合物的解离常数。用于测量一种蛋白质与另一种蛋白质的结合的其他合适的测定包括例如免疫测定(如酶联免疫吸附测定(ELISA)和放射免疫测定(RIA)),或通过借助荧光、紫外吸收、圆二色性或核磁共振(NMR)监测蛋白质的光谱或光学特性的变化来确定结合。其他示例性测定包括但不限于蛋白质印迹、ELISA、分析型超速离心、光谱学、流式细胞术、测序和用于检测表达的核酸或蛋白质结合的其他方法。
在一些实施方案中,结合分子(例如抗体或其片段)与抗原(例如,CCT5蛋白或其中的表位)结合(如特异性地结合),其中亲和力或K
在一些实施方案中,抗体(例如抗原结合片段)与CCT5蛋白(如人CCT5蛋白)的结合亲和力(EC
在一些实施方案中,可以将结合亲和力分类为高亲和力或低亲和力。在一些情况下,展现出低至中等亲和力结合的结合分子(例如抗体或其片段)展现出高达10
在一些实施方案中,可以比较结合分子(如抗CCT5抗体)对不同抗原(例如来自不同物种的CCT5蛋白)的结合亲和力以确定物种交叉反应性。例如,可以将物种交叉反应性分类为高交叉反应性或低交叉反应性。在一些实施方案中,可以比较对于不同抗原(例如来自不同物种(如人或小鼠)的CCT5蛋白)的平衡解离常数K
在一些实施方案中,所提供的抗体或其抗原结合片段与人CCT5蛋白和非人CCT5蛋白以相似的程度结合。例如,在一些实施方案中,所提供的抗体或其抗原结合片段与人CCT5蛋白(如包含SEQ ID NO:45或SEQ ID NO:46的氨基酸序列的人CCT5蛋白(UniProt号P48643)或其等位基因变体或剪接变体)以特定平衡解离常数(K
例如,在一些实施方案中,所提供的抗体或其抗原结合片段与人CCT5以约或小于或小于约1μM、500nM、100nM、50nM、40nM、30nM、25nM、20nM、19nM、18nM、17nM、16nM、15nM、14nM、13nM、12nM、11nM、10nM、9nM、8nM、7nM、6nM、5nM、4nM、3nM、2nM、或1nM或更小的K
在一些实施方案中,将如使用特定的表面等离子体共振(SPR)条件所测量的总结合容量(R
在一些实施方案中,抗体或其抗原结合片段结合(例如特异性地结合)和/或识别CCT5(例如人CCT5)中的一个或多个表位。在一些实施方案中,表位包括肽表位。在一些实施方案中,表位包括线性表位和/或构象表位或其组合。在一些实施方案中,例如本文所提供的抗CCT5抗体或其抗原结合片段结合的在CCT5上的一个或多个表位包括构象表位(例如,包括来自CCT5的若干个肽段(peptide stretch)的表位)。
在一些实施方案中,所提供的抗体或其抗原结合片段特异性地结合如下肽序列,或为如下肽序列或在如下肽序列内含有的表位,所述肽序列具有序列XSVEXXKX(SEQ IDNO:68),其中X可以是任何氨基酸。在一些实施方案中,肽序列是序列X
在一些实施方案中,抗体(例如抗原结合片段)显示出如与CCT5阴性细胞相比对表达CCT5的细胞(如本文已知和/或描述的表达CCT5和已知不表达CCT5的特定细胞)的结合偏好。在一些实施方案中,抗体(例如抗原结合片段)显示出如与在表面上不CCT5的细胞相比对在表面上表达CCT5的细胞(如本文已知和/或描述的表达表面CCT5和已知不表达表面CCT5的特定细胞)的结合偏好。在一些实施方案中,抗体显示出对展现出TRiC复合物的一个或多个亚基的增加表达的细胞的结合偏好。在一些实施方案中,所提供的抗体显示出对癌细胞或肿瘤细胞的结合偏好。在一些实施方案中,观察到结合偏好,其中与不表面表达的细胞相比,测量出与表面表达CCT5的细胞的结合程度显著更高。在一些实施方案中,如与不表达CCT5的细胞相比,针对表达CCT5的细胞检测到的结合程度(例如,如通过在基于流式细胞术的测定中的平均荧光强度和/或解离常数或EC
在一些实施方案中,所提供的结合分子(包括抗体或其抗原结合片段或含有此类抗体或抗原结合片段的缀合物或嵌合抗原受体)结合异常表达CCT5(如过表达CCT5、表达错误折叠的CCT5)的细胞、表面表达的CCT5或与膜相关或定位于膜的CCT5。在一些实施方案中,结合是针对某些癌细胞系,如上皮细胞。在一些实施方案中,癌细胞系是来自以下的肿瘤细胞系:乳腺癌(SK-BR-3、MCF7、HCC 1806、HCC 2218、BT549和MDA-MB-231)、胰腺癌(MIAPaCa-2、PANC-1、BxPC-3、SU86.86和Panc10.05)、卵巢癌(OVCAR-8、Caov-3、ES-2、NIH:OVCAR-3和OVCAR-4)、肺癌(A549、NCI-H1975、NCI H1299、NCI H1573和NCI H1915)、头颈部鳞状细胞癌(HNSCC;UPCI:SCC152)、宫颈癌(CaSki)、皮肤癌(SV-80)、急性髓性白血病(AML;Kasumi-1、SH-2、HT-93、HL60、ML-2、BDCM、KG-1、SKM-1、THP-1和OCI-M1)或慢性髓性白血病(CML;K-562)。
在一些方面,可以通过各种已知测定对所提供的抗体或抗原结合片段,如抗CCT5抗体(例如抗原结合片段)鉴定、筛选或表征其物理/化学特性和/或生物学活性。在一方面,对抗体测试其抗原结合活性,例如通过已知方法,如ELISA、蛋白质印迹和/或流式细胞术测定,包括基于细胞的结合测定,例如评估(例如与荧光标记缀合或标记的)抗体与在其表面上表达靶抗原(例如表面CCT5)的细胞的结合,在一些情况下与使用不在其表面上表达靶抗原的细胞的结果进行比较。可以将结合亲和力测量为K
竞争测定可以用于鉴定与本文所述的任何抗体(例如抗原结合片段)竞争的抗体。也可以使用用于定位被抗体和参考抗体所结合的表位的测定,并且所述测定是已知的。
B.免疫缀合物
本文还提供了抗体缀合物或免疫缀合物。在一些实施方案中,抗体(例如,抗原结合片段)是免疫缀合物或是免疫缀合物的一部分,其中抗体直接或间接地(如经由接头)缀合至一个或多个异源分子或异源部分。所提供的缀合物可用于靶向递送细胞毒性剂或细胞抑制剂(即药物),以杀伤或抑制表达CCT5,如异常表达CCT5和/或含有SEQ ID NO:68或69中所示的序列(例如,SEQ ID NO:70-72中任一个中所示的序列)的多肽的靶细胞。在一些实施方案中,此类缀合物可用于如在癌症的治疗中杀伤或抑制肿瘤靶细胞。在一些实施方案中,所提供的缀合物被称为抗体-药物缀合物或ADC。此类缀合物展现出与未患病的细胞相比对希望被消除的肿瘤细胞的选择性,并且从而不会对正常细胞产生不可接受的毒性水平。因此,此类化合物可用于本文所述的诊断或治疗癌症和其他疾病或障碍的方法中。
在一些实施方案中,异源分子或异源部分是靶向剂。示例性异源分子或异源部分包括但不限于一种或多种细胞毒性剂或显像剂。在一些方面,此类缀合物含有以下组分:抗体(Ab)、(接头(L))
在一些实施方案中,靶向剂的数目由变量m标明,其中m是1或更大的整数。在一些实施方案中,靶向剂与本文所提供的抗体通过由变量q标明的数目的接头缀合,其中q为0或任何整数。选择变量q和m,以使所得的缀合物与如在靶细胞、特别是肿瘤细胞的表面上的靶抗原相互作用,所述靶抗原例如CCT5(如异常表达的CCT5)和/或含有SEQ ID NO:68或69中所示的序列基序(例如,SEQ ID NO:70-72中的任一个中所示的序列)的多肽。在一些方面,这种相互作用将靶向剂递送至靶细胞和/或致使或引起靶向剂被靶细胞内化。在一些实施方案中,内化后,全部或部分的内化蛋白质运输至此类细胞的细胞质。
在一些实施方案中,m在1与8之间。在一些实施方案中,q为0或更大,这取决于连接的靶向和靶向剂的数目和/或接头的功能;q通常为0至4。当缀合物中存在超过一种的靶向剂时,靶向剂可以相同或不同。
靶向剂可以直接或通过一个或多个接头共价连接至抗体。设想了缀合物的元件中的任何合适的缔合,只要所得的缀合物与靶抗原相互作用,所述靶抗原例如CCT5(如异常表达的CCT5)、和/或含有SEQ ID NO:68或69中所示的序列基序(例如,SEQ ID NO:70-72中的任一个中所示的序列)的多肽。本文所提供的缀合物可以产生为融合蛋白,可以化学偶联,或可以包括融合蛋白部分和化学连接的部分或其任何组合。
还可以修饰靶向剂以使其更适合与接头和/或所提供的抗体缀合或增加其细胞内活性。例如,在多肽靶向剂的情况下,此类修饰包括但不限于在N端或C端处或附近引入Cys残基、衍生化以引入反应性基团(如硫醇基)、和/或添加分选信号,如(Xaa-Asp-Glu-Leu)
在一些实施方案中,可以修饰靶向剂以消除一个或多个半胱氨酸残基,例如以在优选位置处提供更可预测的硫醇缀合。在一些情况下,除非需要这种改变,否则必须小心避免改变所得修饰的靶向剂的特异性。在所有情况下,可以根据经验确定特定的修饰。
在一些实施方案中,接头L通过一个或多个共价键将抗体附接至靶向剂。接头可以是肽或非肽。在一些实施方案中,可以选择接头以减轻或减少由靶向剂与抗体的接近引起的空间位阻和/或增加或改变缀合物的其他特性,如靶向部分的特异性、毒性、溶解度、血清稳定性和/或细胞内可用性,和/或增加抗体与靶向剂之间连接的灵活性。
当设想融合蛋白时,选择接头,以使得所得的核酸分子编码融合蛋白,所述融合蛋白结合表达或过表达靶抗原的细胞,并且在一些情况下被所述细胞内化,所述靶抗原例如CCT5(如异常表达的CCT5)、和/或含有SEQ ID NO:68或69中所示的序列基序(例如,SEQ IDNO:70-72中的任一个中所示的序列)的多肽。还可以设想可以连接若干个接头,以使用每个接头的有利特性。在此类情况下,缀合物的接头部分可含有超过50个氨基酸残基。残基的数量并不重要,只要所得的融合蛋白结合在细胞的表面上的靶抗原(例如CCT5(如异常表达的CCT5)、和/或含有SEQ ID NO:68或69中所示的序列基序(例如,SEQ ID NO:70-72中的任一个中所示的序列)的多肽)并经由将靶向剂运输至细胞质和/或细胞核的途径内化连接的靶向剂。
靶向剂可以是蛋白质、肽、核酸、小分子、治疗性部分或其他希望向所选择的肿瘤细胞群进行靶向递送的药剂。此类靶向剂包括但不限于细胞毒性剂、DNA和RNA核酸酶、毒素、药物或其他药剂。治疗性部分包括但不限于细胞毒性部分、放射性同位素、化学治疗剂、裂解肽和细胞因子。
示例性治疗性部分包括但不限于紫杉醇、细胞松弛素B、短杆菌肽D、溴化乙锭、依米丁、丝裂霉素、依托泊苷、替尼泊苷、长春新碱、长春碱、秋水仙碱、多柔比星、道诺霉素、二羟基炭疽菌素二酮、美登素及其类似物或衍生物、澳瑞司他汀(auristatin)或其功能肽类似物或其衍生物、多拉司他汀10或15或其类似物、伊立替康或其类似物、米托蒽醌、光神霉素、放线菌素D、1-脱氢睾酮、糖皮质激素、普鲁卡因、丁卡因、利多卡因、普萘洛尔、嘌呤霉素、卡奇霉素或其类似物或衍生物、抗代谢物、烷化剂、铂衍生物、倍癌霉素A、倍癌霉素SA、雷查霉素(CC-1065)或其类似物或衍生物、抗生素、吡咯[2,1-c][1,4]-苯并二氮杂卓(PDB)、毒素、核糖核酸酶(RNA酶)、DNA酶I、葡萄球菌肠毒素A、及美洲商陆抗病毒蛋白。
药物也可以在所提供的缀合物中用作靶向剂。此类药物包括5-氟尿嘧啶、长春花生物碱和抗生素如更生霉素、博来霉素、道诺霉素、多柔比星、伊达比星、甲氨蝶呤、光神霉素、丝裂霉素、米托蒽醌、普卡霉素和安曲霉素(AMC)、新制癌菌素和长春地辛。
用于抗体-毒素缀合物中的毒素包括细菌毒素如白喉毒素及其活性片段以及杂交分子,植物毒素如蓖麻毒素,小分子毒素如格尔德霉素(geldanamycin),美登木素生物碱如DM1、DM3和DM4,以及卡奇霉素(calicheamicin)。最后,可以使用澳瑞司他汀肽、澳瑞司他汀E(AE)、单甲基澳瑞司他汀E(MMAE)和单甲基澳瑞司他汀F(MMAF)、多拉司他汀的合成类似物。其他毒素包括霍乱毒素、志贺样毒素、LT毒素、C3毒素、志贺毒素、百日咳毒素、破伤风毒素、大豆Bowman-Birk蛋白酶抑制剂、假单胞菌素外毒素、alorin、皂草素、蒴莲根毒素、甘丙肽、相思豆毒素A链、蒴莲根毒素A链、α-帚曲毒蛋白、油桐蛋白、石竹素蛋白、美洲商陆蛋白、苦瓜抑制剂、麻疯树毒蛋白、巴豆毒素、白树毒素、丝林霉素、局限曲菌素、酚霉素、和依诺霉素毒素。毒素可通过包括微管蛋白结合、DNA结合或拓扑异构酶抑制的机制产生其细胞毒性和细胞抑制活性。
1.靶向剂
在一些实施方案中,靶向剂可以是蛋白质、肽、核酸、小分子、治疗性部分、放射性同位素或其他希望向所选择的肿瘤细胞群进行靶向递送的药剂。此类靶向剂包括但不限于细胞毒性剂、DNA和RNA核酸酶、毒素、药物或其他药剂。
a.放射性部分
在一些实施方案中,放射性同位素可用作所提供的缀合物中的靶向剂,其中抗体(例如,抗原结合片段)与放射性原子缀合以形成放射性缀合物。示例性放射性同位素包括At
b.美登木素生物碱药物部分
在一些实施方案中,在缀合物中作为靶向剂的细胞毒性部分包括美登木素生物碱药物部分,包括美国专利号8,142,784中描述的那些。在一些实施方案中,美登素化合物通过抑制微管蛋白质(微管蛋白)的聚合来抑制有丝分裂期间微管蛋白质的形成来抑制细胞增殖(Remillard等人(1975)Science 189:1002-1005;美国专利号5,208,020)。美登素和美登木素生物碱是高度细胞毒性的,但是其在癌症疗法中的临床应用已由于其全身性副作用而受限,所述全身性副作用在一些方面归因于其不佳的肿瘤选择性。由于对中枢神经系统和胃肠道系统有严重的不良影响,因此已停止使用美登素的临床试验(Issell等人(1978)Can.Treatment.Rev.5:199-207)。
在一些方面,美登木素生物碱药物部分在抗体-药物缀合物中是引人注目的药物部分,这是因为它们:(i)通过发酵或化学修饰、衍生化发酵产物相对容易制备,(ii)能用适于通过非二硫键接头与抗体缀合的官能团衍生化,(iii)在血浆中稳定,和(iv)针对多种肿瘤细胞系有效。
适合用作美登木素生物碱药物部分的美登素化合物是可根据已知方法自天然来源分离、使用基因工程化技术产生(参见Yu等人(2002)PNAS 99:7968-7973)的那些,或者根据已知方法合成制备的美登醇和美登醇类似物。
示例性美登木素生物碱药物部分包括具有修饰的芳香环的那些,如:C-19-脱氯(美国专利号4,256,746)(通过安丝菌素P2的氢化铝锂还原而制备);C-20-羟基(或C-20-去甲基)+/¨C-19-脱氯(美国专利号4,361,650和4,307,0.16)(通过使用链霉菌属或放线菌属去甲基化或使用LAH脱氯而制备);及C-20-去甲氧基、C-20-酰氧基(-000R)、+/¨脱氯(美国专利号4,294,757)(通过使用酰基氯酰化而制备);以及具有在其他位置的修饰的那些。
示例性美登木素生物碱药物部分还包括具有修饰的那些,如:C-9-SH,通过美登醇与H2S或P2S5反应而制备(美国专利号4,424,219);C-14-烷氧甲基(去甲氧基/CH2OR)(美国专利号4,331,598);从诺卡氏菌属(Nocardia)中制备的C-14-羟甲基或酰氧基甲基(CH2OH或CH20Ac)(美国专利号4,450,234);通过链霉菌属对美登醇转化而制备的C-15-羟基/酰氧基(美国专利号4,364,866);从滑桃树(Trewia nudijlora)中分离的C-15-甲氧基(美国专利号4,313,946和美国专利号4,315,929);通过链霉菌属对美登醇去甲基化而制备的C-18-N-去甲基(美国专利号4,362,663和美国专利号4,322,348);通过美登醇的三氯化钛/LAH还原而制备的4,5-脱氧基(美国专利号4,371,533)。
已知美登素化合物上的许多位置根据连接类型可用作连接--位置。例如,对于形成酯连接,具有羟基的C-3位置、用羟甲基修饰的C-14位置、用羟基修饰的C-15位置以及具有羟基的C-20位置均是合适的。
在一些实施方案中,美登木素生物碱药物部分可以通过直接缀合或者使用接头(如本文所述的任一种)与所提供的抗体或片段连接。在特定的例子中,细胞毒性剂或药剂是mertansine,也称作DM1(N2t-去乙酰基-N2'-(3-巯基-1-氧基丙基)-美登素)。Mertansine可以经由4-巯基戊酸连接。
在一些实施方案中,恩星(emtansine)缀合物也可以用本发明的抗体,使用接头4-(3-巯基-2,5-二氧-1-吡咯烷基甲基)-环己基羧酸(MCC)形成。
c.澳瑞司他汀和多拉司他汀药物部分
在一些实施方案中,在缀合物中作为靶向剂的细胞毒性部分包括澳瑞司他汀和多拉司他汀,包括美国公开号US2011/0217321中描述的那些。澳瑞司他汀和多拉司他汀已经显示出干扰微管动力学、GTP水解及核与细胞分裂(Woyke等人(2001)Antimicrob.Agentsand Chemother.45(12):3580-3584)并具有抗癌(美国专利号5,663,149)和/或抗真菌活性(Pettit等人(1998)Antimicrob.Agents Chemother.42:2961-2965)。此外,澳瑞司他汀是高效的、合成的、稳定的及耐受化学修饰,以允许接头附接(Senter(2009)CUPT Opin ChemBiol 13:235-244)。
由于澳瑞司他汀是合成的,因此可以进行整体结构修饰以显著改变母体药物的特性。例如,单甲基澳瑞司他汀F(MMAF)末端是氨基酸残基苯丙氨酸,这样削弱了细胞膜通透性(Doronina等人,(2006)Bioconjug Chem.17:114-124)。在一些实施方案中,MMAF与ADC的缀合可促进抗原阳性细胞的选择性药物摄取(Doronina等人,(2006)Bioconjug Chem.17:114-124;Doronina等人,(2003)Nat Biotechnol.21:778-784)。
在一些实施方案中,多拉司他汀或澳瑞司他汀药物部分可以通过肽药物部分的N(氨基)末端或C(羧基)末端附接至抗体(WO 2002/088172)。示例性澳瑞司他汀实施方案包括N末端和C末端连接的单甲基澳瑞司他汀药物部分MMAE和MMAF(Senter等人(2004)“Proceedings of the American Association for Cancer Research,”第45卷,文摘号623,且2004年3月28号呈递;美国公开号2011/0020343)。
多拉司他汀或澳瑞司他汀可以通过直接缀合或者使用接头(如所述的任何接头)与抗体或片段连接。在特定的实例中,多拉司他汀或澳瑞司他汀可以用肽接头如缬氨酸-瓜氨酸(Val-Cit)接头与抗体或片段连接。
d.吡咯苯并二氮杂卓(PBD)
在一些实施方案中,作为缀合物中的靶向剂的细胞毒性部分包括吡咯苯并二氮杂卓(PBD)(或吡咯并[2,1-c][1,4]-苯并二氮杂卓),其是具有抗肿瘤特性的序列选择性DNA烷基化抗生素。PBD具有识别和结合DNA特定序列的能力。在一些实施方案中,PBD的DNA序列是或包含PuGPu(嘌呤-鸟嘌呤-嘌呤)。PBD通常也可以结合PuGPy(嘌呤-鸟嘌呤-嘧啶)或通常相对于PyGPy序列结合PyGPu序列。
PBDS可以是天然存在的或合成的。天然存在的PBD包括阿比霉素(abbeymycin)(Hochlowski等人,J.Antibiotics,40,145-148(1987))、安曲霉素=(Leimgruber等人,J.Am.Chem.Soc,87,5793-5795(1965);Leimgruber等人,J.Am.Chem.Soc,87,5791-5793(1965))、契卡霉素(chicamycin)(Konishi等人,J.Antibiotics,37,200-206(1984))、DC-81(Thurston等人,Chem.Brit.,26,767-772(1990);Bose等人,Tetrahedron,48,751-758(1992))、甲基氨茴霉素(Kunimoto等人,J.Antibiotics,33,665-667(1980))、新茴霉素A和B(Takeuchi等人,J.Antibiotics,29,93-96(197.6))、泊罗霉素(porothramycin)(Tsunakawa等人,J.Antibiotics,41,1366-1373(1988))、普拉卡素(prothracarcin)(Shimizu等人,J.Antibiotics,29,2492-2503(1982);Langley和Thurston,J.Org.Chem.,52,91-91(1987))、西班米星(sibanomicin)(DC-102)(Hara等人,J.Antibiotics,41,702-704(1988);hob等人,J.Antibiotics,41,1281-1284(1988))、西伯利亚霉素(sibiromycin)(Leber等人,J.Am.Chem.Soc,110,2992-2993(1988))、以及托马霉素(tomamycin)(Arima等人,J.Antibiotics,25,437-444(1972))。也已经描述了PBD的合成和合成类似物的产生(参见,例如美国专利号6,562,806、6,608,192 6,747,144和7,049,311、7,528,126)。
PBD的不同之处在于其芳香族A环和吡咯并C环两者中的取代基的数目、类型和位置以及C环的饱和度。在B环中,在N10-C11位置处存在亚胺(N=C)、甲醇胺(NH-CH(OH))或甲醇胺甲基醚(NH-5 CH(Olvle)),所述N10-C11位置为负责烷基化DNA的亲电中心。所有已知的天然产物在手性C11a位置处具有(S)-构型,当从C环朝向A环观察时,所述位置为其提供右手扭转。这给予它们适当的三维形状以实现具有B型DNA的小沟的等螺旋性(Kohn,InAntibiotics III.Springer-Verlag,纽约,第10页3-11(1975);Hurley和Needham-VanDevanter,Acc.Chem.Res.,19,230-237(1986))。
在一些实施方案中,PBD与PuGPu共有序列中鸟嘌呤的环外N2形成共价的氨基连接,形成PBD/DNA加合物,其干扰DNA加工并导致细胞周期停滞和细胞凋亡。因此,PBD是有效的抗肿瘤剂。
在一些实施方案中,PBD的二聚体可以是有效的抗肿瘤剂。在一些方面,PBD二聚体覆盖六个碱基对而不是被PBD单体覆盖的三个碱基对。此外,二聚体中的PBD可以结合DNA的互补链中的序列(即,链间鸟嘌呤-鸟嘌呤交联),从而导致序列选择性DNA交联。PBD二聚体诱导的交联防止链分离,从而防止DNA复制。在一些方面,这导致G2/M交接处的细胞周期停滞和细胞凋亡。在一些实施方案中,除了DNA交联之外,PBD-二聚体与PBD单体相比的覆盖率增加可以导致作为抗癌剂的功效大幅增加。
在一些实施方案中,PBD二聚体可以是同二聚体或异二聚体,并且通过以下方式合成:经由柔性接头通过其C8位置将两个单体PBD单元连接在一起。常用的接头包括丙基二氧基(PBD-C8-0-(C1-12)3-0-C8'-PBD)和戊基二氧基(PBD-C8-0-(CH2)5-0-C8'-PBD’)。可以选择接头的特性(如接头的长度),以将二聚体靶向特定的DNA序列(Rahman等人,(2011)Nucleic Acids Res.39(13):5800-5812和Gregson等人,(2004)J Med Chem 47:1161-1174)。
示例性PBD间接头描述于以下文献中:Bose等人,(1992)J Am Chem Soc.114:4939-4941;Bose等人,(1992)J Chem Soc Chem Commun.14:1518-1520;Thurston等人,(1996)J Org Chem.61:8141-8147;Gregson等人,(2001).1Med Chem.44:737-748;和Gregson等人,J Med Chem 2004;47:1161-1174。已描述了示例性PBD二聚体(参见,例如美国专利号6,562,806、6,608,192 6,747,144、7,049,311、7,528,126、7,741,319、8,592,576)并且包括但不限于命名为以下的化合物:DSB-120(US 7,049,311)、DRH-165(US 7,049,311)、ELB21(Rahman等人,(2011)Nucleic Acids Res.39(13):5800-5812)、5G2000/5JG136(Rahman等人,(2011)Nucleic Acids Res.39(13):5800-5812;US 7,049,311)、5G2057/DRG16(Rahman等人,(2011)Nucleic Acids Res.39(13):5800-5812)、5G2202(US7,741,319;Hartley等人,(2010)Cancer Res.70(17):6849-6858)、5G2285(Hartley等人,(2010)Cancer Res.70(17):6849-6858)、5G3132(US 20130028919)。
在一些实施方案中,PBD和PBD二聚体可以通过任何方法与本文所提供的任何抗体缀合,所述方法包括但不限于硫醇、胺和苯酚缀合。通常,使用在体内循环中稳定的可切割接头将PBD或PBD二聚体与抗体缀合,以使得在靶细胞内在切割接头后,PBD或PBD二聚体从抗体释放。在一些例子中,PBD或PBD二聚体可以与链间半胱氨酸缀合。在一些例子中,可以修饰抗体以替代一个或多个氨基酸以插入或去除链间半胱氨酸,从而促进PBD或PBD二聚体的定向硫醇连接。
e.细胞毒素部分
在一些实施方案中,所提供的缀合物中的毒素包括小分子,如DNA切割剂,及蛋白质样细胞毒素,包括但不限于细菌、真菌、植物、昆虫、蛇和蜘蛛毒素。设想掺入本文所提供的缀合物中的示例性的细胞毒素包括异株泻根毒蛋白(Bryodin)(SEQ ID NO:73)、皂草素-6(SEQ ID NO:75)、抗病毒蛋白MAP(SEQ ID NO:77)、志贺毒素A链(SEQ ID NO:79)、志贺样毒素亚基A(Vero毒素2)(SEQ ID NO:80)、天花粉蛋白(SEQ ID NO:86)。
(i)DNA切割剂
适于作为毒素包含于所提供的缀合物中的DNA切割剂的例子包括但不限于蒽醌-寡吡咯-甲酰胺、苯并咪唑、雷拉霉素(leinamycin)、dynemycin A、烯二炔,以及其生物学活性类似物或衍生物(即具有基本等同的生物学活性的那些)。已知的类似物和衍生物公开于例如以下文献中:Islam等人,J.Med.Chem.342954-61,1991;Skibo等人,J.Med.Chem.37:78-92,1994;Behroozi等人,Biochemistry 35:1768-74,1996;Helissey等人,AnticancerDrug Des.11:527-551,1996;Unno等人,Chem.Pharm.Bull.45:125-133,1997;Unno等人,Bioorg.Med.Chem.,5:903-919,1997;Unno等人,Bioorg.Med.Chem.,5:883-901,1997;以及Xu等人,Biochemistry 37:1890-1897,1998)。其他例子包括但不限于endiyne醌亚胺(美国专利号5,622,958);2,2r-双(2-氨基乙基)-4-4'-双氮唑(Lee等人,Biochem.Mot.Biol.Int.40:151-7,1996);epilliticine-萨伦铜缀合物(Routier等人,Bioconjug.Chem.,8:789-92,1997)。
(ii)抗代谢物
可用作细胞毒素包含于所提供的缀合物中的抗代谢物的例子包括但不限于5-氟尿嘧啶、甲氨蝶呤、美法仑、道诺霉素、多柔比星、氮芥和丝裂霉素c。
(iii)蛋白质性细胞毒素
所提供的缀合物中的蛋白质性毒素的例子包括但不限于1型和2型核糖体失活蛋白质(RIP)。有用的1型植物RIP包括但不限于石竹素30、石竹素32、剪秋罗甙、皂草素1-9、美洲商陆激活的蛋白质(PAP)、PAP II、PAP-R、PAP-S、PAP-C、mapalmin、商陆毒蛋白、异株泻根毒蛋白-L、异株泻根毒蛋白、大肠菌素1和2、丝瓜素-A、丝瓜素-B、丝瓜素-S、19K-蛋白质合成抑制蛋白(PSI)、15K-PSI、9K-PSI、、α-kirilowin、β-kirilowin、白树毒素、地肤子皂苷、地肤子皂苷-II、地肤子皂苷-Ic、MAP-30、α-苦瓜素、β-苦瓜素、天花粉蛋白、TAP-29、栝楼素(trichokirin)、大麦RIP、亚麻RIP、麦芽凝集素、玉米RIP、Asparin 1和2。有用的2型RIP包括但不限于沃氏藤黄辛(volkensin)、蓖麻毒素、nigrin-b、CIP-29、相思豆毒素、蒴莲根毒素、ebulitin-a、ebulitin-13、vircumin、黄樟毒蛋白(porrectin),以及其生物学活性酶亚基(Stirpe等人,Bio/Technology 10:405-12,1992;Pastan等人,Annu.Rev.Biochem.61:331-54;Brinkmann和Pastan,Biochim.et Biophys.Acta 1198:27-45,1994;以及Sandvig和Van Deurs,PhysioL Rev.76:949-66,1996)。
(iv)细菌毒素
所提供的缀合物中的细菌毒素的例子包括但不限于志贺毒素和志贺样毒素(即具有相同活性或结构的毒素),以及其催化亚基及其生物功能片段。这些细菌毒素也是2型RIP(Sandvig和Van Deurs,PhysioL Rev.76:949-66,1996;Armstrong,J.Infect.Dis.,171:1042-5,1995;Kim等人,Microbiol.Immunol.41:805-8,1997;和Skinner等人,Microb.Pathog.24:117-22,1998)。有用的细菌毒素的另外例子包括但不限于假单胞菌外毒素和白喉毒素(Pastan等人,Annu.Rev.Biochem.61:331-54;以及Brinkmann和Pastan,Biochim.et Biophys.Acta 1198:27-45,1994)。毒素酶亚基的截短形式和突变体也可用作细胞毒素部分(Pastan等人,Annu.Rev.Biochem.61:331-54;Brinkmann和Pastan,Biochim.et Biophys.Acta 1198:27-45,1994;Mesri等人,J.Biol.Chem.268:4853-62,1993;Skinner等人,Microb.Pathog.24:117-22,1998;和美国专利号5,082,927)。其他靶向剂包括但不限于RNA酶毒素的大肠杆菌素家族的毒素(包括大肠菌素A、B、D、E1-9)、阴沟肠杆菌素DF13和真菌RNA酶、a-帚曲毒蛋白(Ogawa等人Science 283:2097-100,1999;Smarda等人,Folia Microbiol(Praha)43:563-82,1998;Wool等人,Trends Biochem.Sci.,17:266-69,1992)。
(v)卟啉和其他光激活毒素
在一些实施方案中,所提供的缀合物中的毒素是卟啉,其是可以容易地与蛋白质进行交联的可光激活毒素(参见,例如美国专利号5,257,970;5,252,720;5,238,940;5,192,788;5,171,749;5,149,708;5,202,317;5,217,966;5,053,423;5,109,016;5,087,636;5,028,594;5,093,349;4,968,715;4,920,143和国际公开号WO 93/02192)。
f.用于靶向递送的核酸
在一些实施方案中,本文所提供的缀合物也可用于将核酸递送至靶细胞。在一些实施方案中,核酸包括用于修饰细胞基因组并且从而实现基因疗法的DNA,以及用作反义剂的DNA和RNA。核酸包括反义RNA、DNA、核酶和旨在用作反义剂的其他寡核苷酸。所述核酸也可包括RNA运输信号,如病毒包装序列(参见,例如Sullenger等人(1994)Science 262:1566-1569)。在一些情况下,核酸也包括DNA分子,其编码完整基因或编码旨在用于基因疗法中的蛋白质。
在一些实施方案中,可以递送至细胞以实现基因疗法的DNA(或RNA)包括编码肿瘤特异性细胞毒性分子如肿瘤坏死因子、病毒抗原和使细胞易感于抗癌剂的其他蛋白质的DNA,以及编码用于以替代缺陷基因的基因的DNA。
如本文所述使用的核酸和寡核苷酸可以通过任何已知方法合成(参见,例如WO93/01286和美国专利号5,218,088;5,175,269;和5,109,124)。用作反义剂的寡核苷酸和核酶的鉴定是已知的。编码靶向递送以进行基因疗法的DNA可以通过已知方法选择。例如,此类寡核苷酸的所需特性、长度及其他特性是熟知的。反义寡核苷酸被设计以抵抗内源性溶核酶的降解并且包括但不限于:硫代磷酸酯、甲基磷酸酯、砜、硫酸盐、羰游离基、二硫代磷酸酯、氨基磷酸酯、磷酸酯及其他这种连接(参见,例如Agrawal等人(1987)TetrahedronLett.28:3539-3542;Miller等人(1971)J.Am.Chem.Soc.93:6657-6665;Stec等人(1985)Tetrahedron Lett.26:2191-2194;Moody等人(1989)NucL Acids Res.17:4769-4782;Letsinger等人(1984)Tetrahedron 40:137-143;Eckstein(1985)Annu.Rev.Biochem.54:367-402;Eckstein(1989)Trends Biochem.Sci.14:97-100;Stein(1989)In:Oligodeoxynucleotides.Antisense Inhibitors of Gene Expression,Cohen编,Macmillan Press,London,第97-117页;Jager等人(1988)Biochemistry 27:7237-7246)。
在一些实施方案中,为了实现本文的化学缀合,将靶向剂直接或经由一个或多个接头与核酸连接。已知在5'端、3'端和其他地方将核酸缀合至蛋白质中的氨基和羧基末端以及其他位点的方法是已知的(对于综述,参见例如Goodchild,(1993)In:Perspectivesin Bioconjugate Chemistry,Mears编,American Chemical Society,Washington,D.C.第77-99页)。例如,已经使用以下方式将蛋白质连接至核酸:紫外线照射(Sperling等人(1978)Nucleic Acids Res.5:2755-2773;Fiser等人(1975)FEBS Lett.52:281.283)、双官能化学物质(Baumert等人(1978)Eur.J.Biochem.89:353-359;和Oste等人(1979)Mol.Gen.Genet.168:81-86)、和光化学交联(Vanin等人(1981)FEBS Lett.124:89-92;Rinke等人(1980)1Mol.Biol./37:301-304;Millon等人(1980)Eur.J.Biochetn.110:485-492)。在一些实施方案中,可以将各种反应性基团引入核酸中以进行连接,如巯基、胺基、溴乙酰基或硫醇基。
(i)反义核苷酸,包括:反义寡核苷酸、三链(triplex)分子、哑铃状寡核苷酸、DNA、胞外蛋白质结合寡核苷酸及小核苷酸分子
在一些实施方案中,核酸是反义核苷酸,包括特异性地结合具有互补序列的mRNA的寡核苷酸,所述特异性地结合在一些方面可以阻止所述mRNA的翻译(参见,例如授予Altman等人的美国专利号5,168,053;授予Inouye的美国专利号5,190,931;授予Burch的美国专利号5,135,917;授予Smith的美国专利号5,087,617和Clusel等人(1993)NucL AcidsRes.21:3405-3411,其描述了哑铃状反义寡核苷酸)。三链分子是指单链DNA,其靶向双链DNA,从而阻止转录(参见,例如美国专利号5,176,996,其描述了用于制备结合双链DNA上靶位点的合成的寡核苷酸的方法)。
(ii)核酶
在一些实施方案中,核酸包括核酶,如特异性切割信使RNA的RNA构建体。此类核酶可以包括已知的参与RNA链的切割和/或连接的至少五类核酶中的任一种。核酶可以靶向任何RNA转录物,并且可以催化性切割这种转录物(参见,例如美国专利号5,272,262;5,144,019 5,168,053;5,180,818;5,116,742和5,093,246,其描述了核酶及其产生方法)。任何这种核糖体均可以与所提供的抗体或片段连接以递送至靶细胞。
在一些实施方案中,核酶可以作为与真核启动子(如真核病毒启动子,通常为晚期启动子)连接的编码核酶的DNA被递送至靶细胞,以使得在引入核中时,核酶将被直接转录。在此类情况下,构建体还包括核易位序列,通常作为靶向剂的一部分或者作为接头的一部分,以使其适于递送连接的核酸至核。
(iii)编码用于靶向递送的治疗性产物的核酸
在一些实施方案中,编码设想使用的治疗性产物的DNA包括编码正确拷贝抗癌剂的DNA,所述治疗性产物如细胞因子(例如肿瘤坏死因子)和细胞毒性剂(例如志贺毒素A1或皂草素)或其他治疗剂。在一些实施方案中,此类缀合物包括核易位序列(NTS)。在一些方面,如果设计缀合物以使得靶向剂和连接的DNA在细胞质中被切割,则NTS应包含在接头的保持结合DNA的部分中,以使得当内化时,缀合物将被输送至细胞核。在一些方面,核易位序列(NTS)可以是异源序列或者可以源自所选择的趋化因子受体靶向剂。典型的共有NTS序列含有氨基末端脯氨酸或甘氨酸,随后是在7至9个氨基酸阵列中的至少三个碱性残基(参见,例如Dang等人(1989)1Biol.Chem.264:18019-18023)。
2.接头
在一些实施方案中,抗体或抗原结合片段与部分,例如靶向剂(如毒素)间接地经由接头间接连接。在一些实施方案中,接头L通过一个或多个共价键将抗体或片段附接至靶向剂。在一些实施方案中,接头是一种双功能或多功能部分,其可用于将一种或多种靶向剂与抗体或片段连接以形成抗体-药物缀合物(ADC)。
在一些实施方案中,ADC可使用具有反应功能性的接头来与靶向剂和抗体或片段结合而容易地制备。抗体的半胱氨酸硫醇基团或胺基团(例如N末端或赖氨酸侧链)可以与接头试剂、靶向剂或靶向剂-接头试剂的官能团形成键。
在一些实施方案中,接头在胞外环境中是稳定的,以使得抗体-药物缀合物(ADC)是稳定的并保持完整,即在转运或递送至靶细胞之前抗体保持与靶向剂连接。在一些情况下,接头在靶细胞外部是稳定的,并且一旦在细胞内部时可以被切割或使得抗体和靶向剂以某个有效速率解离。设想的接头包括以下的接头:(i)不干扰或总体上不干扰抗体的特异性结合特性;(ii)允许细胞内递送缀合物或靶向剂;(iii)保持稳定及完整,即不被切割,直至缀合物已经递送或转运至其靶向部位;以及(iv)不干扰或总体上不干扰靶向剂的细胞毒性、细胞杀伤作用或细胞抑制作用。ADC的稳定性可以通过标准分析技术如质谱和/或HPLC测量。
在一些实施方案中,接头具有两个反应性官能团,以允许抗体与靶向剂的共价附接,并因此在反应性意义上展现出二价。可用于附接两个或更多个功能或生物学活性部分(如肽、核酸、药物、毒素、抗体、半抗原及报道基团)的此类化学交联试剂是已知的,并且已经描述了所述化学交联试剂用于产生缀合物的方法(Hermanson,G.T.(1996)BioconjugateTechniques;Academic Press:纽约,第234-242页)。
在一些实施方案中,接头具有反应性官能团,所述反应性官能团具有对存在于抗体上的亲电子基团有反应性的亲核基团。抗体上可用的亲电子基团包括但不限于醛及酮羰基。接头的亲核基团的杂原子可与抗体上的亲电子基团反应且与抗体单元形成共价键。接头上的可用亲核基团包括但不限于酰肼、肟、氨基、肼、缩氨基硫脲、肼羧酸酯及芳基酰肼。抗体上的亲电子基团为附接至接头提供了便利位点。
a.肽接头
在一些实施方案中,接头可以是包含一或多个氨基酸单元的肽的接头。肽接头试剂可以通过固相或液相合成方法(E.Schroder和K.Lubke,The Peptides,第1卷,第76-136页(1965)Academic Press)制备,所述方法为肽化学领域熟知,包括t-BOC化学(Geiser等人“Automation of solid-phase peptide synthesis”in Macromolecular Sequencing andSynthesis,Alan R.Liss,Inc.,1988,第199-218页)和Fmoc/HBTU化学(Fields,G.和Noble,R.(1990)“Solid phase peptide synthesis utilizing 9-fluorenylmethoxycarbonylamino acids”,Int.J.Peptide Protein Res.35:161-214),在自动合成仪如RaininSymphony肽合成仪(Protein Technologies,Inc.)或型号433(Applied Biosystems)上进行。在一些情况下,基于肽的接头与水解或还原剂不稳定的接头相比提供更多优势,因为蛋白酶解是酶促的,并且所述酶可以针对在肿瘤细胞内的优先表达而被选择。组织蛋白酶B-可切割的肽接头缬氨酸-瓜氨酸(Val-Cit)及其修饰如马来酰亚胺己酰基-缬氨酸-瓜氨酸(mc-vc)、苯丙氨酸-赖氨酸、Ala-Leu-Ala-Ala(SEQ ID NO:64)、其他三/四肽是示例性的肽接头,它们已经用于ADC中(Dosio等人,(2010)Toxins 3:848-883;Doronina等人,(2006)Bioconjug Chem.17:114-124;Doronina等人,(2003)Nat Biotechnot.21:778-784;Sanderson等人,(2005)Clin Cancer Res 11:843-852;Ducry and Stump(2010)BioconjugChem.21:5-13)。示例性的不可切割的肽接头包括N-甲基-缬氨酸-瓜氨酸。其他肽接头描述于美国公开号2011/0020343中。
在一些实施方案中,肽接头包括可以掺入融合蛋白中并且在宿主细胞如大肠杆菌中表达的那些接头。此类接头包括:酶底物,如组织蛋白酶B底物、组织蛋白酶D底物、胰蛋白酶底物、凝血酶底物、枯草杆菌蛋白酶底物、因子Xa底物及肠激酶底物;增加溶解度、灵活性和/或细胞内可切割性的接头包括如以下的接头:(glymser)ii和(sermgly)ii,其中m是1至6,优选1至4,更优选2至4,并且n是1至6,优选1至4,更优选2至4(参见,例如国际PCT申请号WO 96/06641,其提供了示例性的用于缀合物中的接头)。在一些实施方案中,可包含若干个接头以利用每个接头的希望特性。
b.化学接头
在一些实施方案中,缀合物(如ADC)也可以使用作为不可切割部分或化学交联试剂的接头制备。示例性不可切割接头包括酰胺接头以及具有琥珀酸盐间隔物的酰胺和酯连接(Dosio等人,(2010)Toxins 3:848-883)。示例性化学交联接头包括但不限于SMCC(琥珀酰亚胺-4-(N-马来酰亚胺甲基)环己烷-1-羧酸酯)和SIAB(琥珀酰亚胺(4-碘乙酰)氨基苯甲酸酯)。SMCC是一种氨-巯基交联接头,其在中等长度的环己烷稳定的间隔子臂的相对端含有NHS-酯和马来酰亚胺反应基团。SIAB是短的NHS-酯和碘乙酰交联剂,以用于氨-巯基缀合。其他示例性的交联试剂包括但不限于硫醚接头、化学不稳定的腙接头、4-巯基戊酸、BMPEO、BMPS、EMCS、GMBS、HBVS、LC-SMCC、MBS、MPBH、SBAP、SIA、SMPB、SMPH、磺基-EMCS、磺基-GMBS、磺基-KMUS、磺基-MBS、磺基-SIAB、磺基-SMCC和磺基-SMPB及SVSB(琥珀酰亚胺-(4-乙烯基砜)苯甲酸酯),以及双马来酰亚胺试剂如DTME、BMB、BMDB、BMH、BMOE、BM(PEO)3、和BM(PEO)4,这些是可商购的(Pierce Biotechnology、Inc.)。双马来酰亚胺试剂使得抗体的半胱氨酸残基的游离硫醇基团以相继的或同时的方式附接至含有硫醇的靶向剂或接头中间物。除了马来酰亚胺之外的其他硫醇反应性官能团包括碘乙酰胺、溴乙酰胺、乙烯基吡啶、二硫化物、吡啶二硫化物、异氰酸酯和异硫氰酸酯。其他示例性的接头及其使用方法描述于美国公开号2005/0276812和在Ducry和Stump(2010)Bioconjug Chem.21:5-13中。
接头任选地可以由调节溶解度或反应性的基团取代。例如,磺酸盐取代基可增加试剂的水溶解度和促进接头试剂与抗体或药物部分的偶联反应,或者促进抗体-接头(Ab-L)与靶向剂或者靶向剂-L与抗体的偶联反应,这取决于用于制备缀合物(例如ADC)的合成途径。
在一些情况下,接头试剂也可以经由商业来源(如Molecular Biosciences Inc.(Boulder,Colo.))获得,或者根据以下文献中所示的程序合成:Toki等人(2002)J.Org.Chem.67:1866-1872;美国专利号6,214,345;WO 02/088172;U.S.2003130189;U.S.2003096743;WO 03/026577;WO 03/043583;和WO 04/032828。例如,接头试剂如DOTA-马来酰亚胺(4-马来酰亚胺丁酰氨基苄基-DOTA)可以通过根据Axworthy等人(2000)Proc.Natl.Acad.Sci.USA 97(4):1802-1807的程序,使氨基苄基-DOTA与用异丙基氯甲酸酯(Aldrich)激活的4-马来酰亚胺丁酸(Fluka)反应来制备。DOTA-马来酰亚胺与半胱氨酸工程化的抗体的游离半胱氨酸氨基酸反应,并且在抗体上提供金属络合配体(Lewis等人(1998)Bioconj.Chem.9:72-86)。螯合接头标记试剂如DOTA-NHS(1,4,7,10-四氮杂环十二烷-1,4,7,10-四乙酸单(N-羟基琥珀酰亚胺酯)是可商购的(Macrocyclics,Dallas,Tex.)。
在一些实施方案中,接头可以是树枝状类型接头,用于通过分支的多功能接头部分使多于一个的药物部分与抗体共价附接(Sun等人(2002)Bioorganic&MedicinalChemistry Letters 12:2213-2215;Sun等人(2003)Bioorganic&Medicinal Chemistry11:1761-1768;King等人(2002)Tetrahedron Letters 43:1987-1990)。在一些情况下,树枝状接头可增加靶向剂与抗体的摩尔比率,即荷载(loading),这可增加ADC的效力。因此,在抗体仅携带一个反应性半胱氨酸硫醇基团时,大量药物部分可以通过树枝状接头附接。示例性树枝状接头试剂描述于美国专利公开号2005/0276812中。
C.多特异性抗体
在某些实施方案中,所提供的结合分子(例如抗体或多肽,如含有抗体或多肽的嵌合受体)是多特异性的。多特异性结合分子包括多特异性抗体,所述多特异性抗体包括例如双特异性或三特异性抗体。多特异性结合配偶体(例如抗体)对至少两个不同的位点具有结合特异性,所述至少两个不同的位点可以在相同或不同的抗原中。
在一些实施方案中,结合特异性之一是针对CCT5(如异常表达的CCT5),或含有SEQID NO:68或69中所示的序列的多肽(例如,SEQ ID NO:70-72中的任一个)的,而另一个是针对另一种抗原。在一些实施方案中,另外的结合分子结合和/或识别第三种或更多种抗原。在某些实施方案中,双特异性抗体可以结合CCT5的两个不同表位,如异常表达的CCT5的两个或更多个表位,或含有SEQ ID NO:68或69中所示的序列的多肽(如SEQ ID NO:70-72中的任一个中所示的)的两个或更多个表位。在一些实施方案中,至少一个表位含有SEQ ID NO:68或69中所示的序列,如SEQ ID NO:70-72中任一个中所示的。双特异性抗体也可用于将细胞毒性剂定位至表达CCT5(如异常表达的CCT5,例如在表面上表达或定位至细胞膜的CCT5)的细胞,或含有SEQ ID NO:68中所示的序列的多肽。
可以将双特异性抗体制备成全长抗体或抗体片段。多特异性抗体包括多特异性单链抗体(例如双抗体、三抗体和四抗体)、串联双scFv和串联三scFv。还提供含有抗体(例如抗原结合片段)的多特异性嵌合受体,如多特异性CAR。在某些实施方案中,多特异性结合分子(例如多特异性嵌合受体,如多特异性CAR)可以含有任何多特异性抗体,包括例如双特异性抗体、多特异性单链抗体,例如双抗体、三抗体和四抗体、串联双scFv和串联三scFv,如上文章节I.A中所述的任何一种。
由所提供的多特异性(如双特异性)抗体靶向的其他抗原包括与由CCT5靶向的相同的疾病或病症相关的抗原,例如肿瘤抗原。示例性抗原包括为通用肿瘤抗原的抗原或其家族成员。在一些实施方案中,第二或另外的抗原是在肿瘤上表达的抗原。在一些实施方案中,所述第二或另外的抗原靶向与由所提供的结合分子靶向的相同的肿瘤类型上的抗原,例如CCT5(如异常表达的CCT5),和/或含有SEQ ID NO:68或69中所示的序列的多肽(例如,SEQ ID NO:70-72中的任一个)。在一些实施方案中,所述第二或另外的抗原可以是通用肿瘤抗原或可以是为肿瘤类型所特有的肿瘤抗原。
示例性抗原包括CD4、CD5、CD8、CD14、CD15、CD19、CD20、CD21、CD22、CD23、CD25、CD33、CD37、CD38、CD40、CD40L、CD46、CD52、CD54、CD74、CD80、CD126、CD138、B7、MUC-1、Ia、HM1.24、HLA-DR、腱生蛋白、血管生成因子、VEGF、PIGF、ED-B纤连蛋白、致癌基因、致癌基因产物、CD66a-d、坏死抗原、Ii、IL-2、T101、TAC、IL-6、ROR1、TRAIL-R1(DR4)、TRAIL-R2(DR5)、B细胞成熟抗原(BCMA)、tEGFR、Her2、L1-CAM、间皮素、CEA、乙型肝炎表面抗原、抗叶酸受体、CD24、CD30、CD44、EGFR、EGP-2、EGP-4、EPHa2、ErbB2、ErbB3、ErbB4、erbB二聚体、EGFR vIII、FBP、FCRL5、FCRH5、胎儿乙酰胆碱受体、GD2、GD3、HMW-MAA、IL-22R-α、IL-13R-α2、kdr、κ轻链、Lewis Y、L1-细胞粘附分子(L1-CAM)、黑色素瘤相关抗原(MAGE)-A1、MAGE-A3、MAGE-A6、黑色素瘤优先表达抗原(PRAME)、存活蛋白、EGP2、EGP40、TAG72、B7-H6、IL-13受体a2(IL-13Ra2)、CA9、CD171、G250/CAIX、HLA-AI MAGE Al、HLA-A2NY-ESO-1、PSCA、叶酸受体-a、CD44v6、CD44v7/8、avb6整合素、8H9、NCAM、VEGF受体、5T4、胎儿AchR、NKG2D配体、双抗原、与通用标签相关的抗原、癌症-睾丸抗原、MUC1、MUC16、NY-ESO-1、MART-1、gp100、癌胚胎抗原、VEGF-R2、癌胚抗原(CEA)、前列腺特异性抗原、PSMA、Her2/neu、雌激素受体、孕酮受体、肝配蛋白B2、CD123、c-Met、GD-2、O-乙酰化GD2(OGD2)、CE7、Wilms肿瘤1(WT-1)、细胞周期蛋白、细胞周期蛋白A2、CCL-1、hTERT、MDM2、CYP1B、WT1、活素、AFP、p53、细胞周期蛋白(D1)、CS-1、BCMA、BAFF-R、TACI、CD56、TIM-3、CD123、L1-细胞粘附分子、MAGE-A1、MAGE A3、细胞周期蛋白(如细胞周期蛋白A1(CCNA1))和/或病原体特异性抗原、生物素化分子、由HIV、HCV、HBV和/或其他病原体表达的分子;和/或在一些方面,其新表位或新抗原。在一些实施方案中,抗原与通用标签相关或者是通用标签。
在一些实施方案中,第二或另外的抗原是为上皮细胞癌症所特有的抗原。在一些实施方案中,抗原是为上皮恶性肿瘤所特有或在上皮恶性肿瘤上表达的抗原。示例性第二或另外的抗原包括但不限于Ca-1、TA-4、SQM1、3H-1、鳞状细胞癌抗原(SCC-ag)、和癌症抗原(CA)125。
在一些实施方案中,第二或另外的抗原是在T细胞上表达的分子。在一些实施方案中,表面分子是T细胞的激活组分,如T细胞受体复合物的组分。在一些实施方案中,表面分子是CD3或者是CD2。在一些实施方案中,多特异性,如双特异性抗体含有结合在T细胞上表达的分子如T细胞的激活组分(例如T细胞表面分子,例如CD3或CD2)的至少一个抗原结合结构域和结合CCT5(如异常表达的CCT5)、和/或如本文所述的含有SEQ ID NO:68或69中所示的序列(例如,含有SEQ ID NO:70-72中的任一个中所示的序列)的多肽的至少一个抗原结合结构域。在一些实施方案中,这种抗体与其两种靶标同时或几乎同时结合可以导致靶细胞和T细胞之间的暂时相互作用,从而导致T细胞的激活(例如细胞毒活性)和随后的靶细胞裂解。
D.重组受体和基因工程化细胞
结合分子还包括含有此类抗体的多肽,包括含有此类抗体的单链细胞表面蛋白(例如,重组受体,如嵌合抗原受体)。还提供了表达此类重组受体(包括CAR)的工程化细胞,如免疫细胞,如T细胞。
1.重组受体
所提供的结合分子包括包含所提供的抗体(例如抗原结合片段)中的一种的单链细胞表面蛋白,如重组受体(例如抗原受体)。重组受体包括特异性地结合CCT5(如异常表达的CCT5)、和/或含有SEQ ID NO:68或69中所示的序列(例如,含有SEQ ID NO:70-72中的任一个中所示的序列)的多肽,包括含有任何所提供的抗体(例如,抗原结合片段)的抗原受体。抗原受体包括功能性非TCR抗原受体,如嵌合抗原受体(CAR)。还提供了表达重组受体的细胞及其在过继细胞疗法(如与CCT5表达相关的疾病和障碍的治疗)中的用途。
示例性抗原受体(包括CAR)、和用于将此类抗原受体工程化和引入到细胞中的方法包括例如在以下文献中所述的那些:国际专利申请公开号WO 200014257、WO2013126726、WO 2012/129514、WO 2014031687、WO 2013/166321、WO 2013/071154、WO2013/123061,美国专利申请公开号US 2002131960、US 2013287748、US 20130149337,美国专利号6,451,995、7,446,190、8,252,592、8,339,645、8,398,282、7,446,179、6,410,319、7,070,995、7,265,209、7,354,762、7,446,191、8,324,353、和8,479,118,以及欧洲专利申请号EP 2537416;和/或以下文献中所述的那些:Sadelain等人,Cancer Discov.2013年4月;3(4):388-398;Davila等人(2013)PLoS ONE 8(4):e61338;Turtle等人,Curr.Opin.Immunol.,2012年10月;24(5):633-39;Wu等人,Cancer,2012年3月18(2):160-75。在一些方面,抗原受体包括如美国专利号7,446,190中描述的CAR,以及国际专利申请公开号WO/2014055668 A1中描述的那些。示例性CAR包括任何上述出版物(如WO 2014031687、US 8,339,645、US 7,446,179、US 2013/0149337、美国专利号7,446,190、美国专利号8,389,282)中披露的CAR,例如并且其中抗原结合部分(例如scFv)被抗体或其抗原结合片段(例如,如本文所提供的)替代。
嵌合受体包括嵌合抗原受体(CAR)。在一些实施方案中,嵌合抗原受体包括含有本文所述的抗体或片段的细胞外部分(例如scFv)、含有细胞内信号传导结构域的细胞内信号传导区(如含有ITAM的细胞内信号传导结构域(例如CD3ζ信号传导结构域))、和连接细胞外结构域和细胞内信号传导区的跨膜结构域。在一些实施方案中,嵌合抗原受体含有共刺激分子(例如T细胞共刺激分子)的细胞内结构域,如在跨膜结构域与细胞内信号传导结构域之间。
嵌合受体(如CAR)通常在其细胞外部分中包含所提供的结合分子的细胞外抗原结合结构域,如一个或多个抗原结合片段、结构域或部分,或一个或多个抗体可变区和/或抗体分子(如本文所述的那些)。在一些实施方案中,CAR包含抗体分子的一个或多个结合部分,如抗体的重链可变(V
在一些实施方案中,包含本文所提供的抗体(例如抗原结合片段)的重组受体(如CAR)进一步包括间隔子,所述间隔子可以是或包括免疫球蛋白恒定区的至少一部分或其变体或经修饰的形式,如铰链区(例如,IgG4铰链区)和/或CH1/CL和/或Fc区。在一些实施方案中,恒定区或部分是人IgG(如IgG4或IgG1)的。在一些方面,恒定区的所述部分用作抗原识别组分(例如,scFv)与跨膜结构域之间的间隔子区。与不存在间隔子的情况相比,间隔子的长度可以提供在抗原结合后增加的细胞应答性。示例性间隔子包括具有以下的那些:至少约10至250个氨基酸,如10至229个氨基酸、约10至200个氨基酸、约10至175个氨基酸、约10至150个氨基酸、约10至125个氨基酸、约10至100个氨基酸、约10至75个氨基酸、约10至50个氨基酸、约10至40个氨基酸、约10至30个氨基酸、约10至20个氨基酸、约10至15个氨基酸、约40至229个氨基酸、约40至200个氨基酸、约40至175个氨基酸、约40至150个氨基酸、约40至100个氨基酸、约40至75个氨基酸、约75至250个氨基酸、约75至200个氨基酸、约75至175个氨基酸、约75至150个氨基酸、约75至100个氨基酸、约100至250个氨基酸、约100至200个氨基酸、约100至150个氨基酸、约150至250个氨基酸,并且包括任何所列范围的端值之间的任何整数。在一些实施方案中,间隔子区具有约12个氨基酸或更少,如长度为或为约12个氨基酸或长度不超过12个氨基酸。示例性间隔子包括至少或至少约或为或为约10、12、14、16、18、20、25、30、40、50、60、70、80、90、100、110、115、120、130、140、150、160、170、180、190、200、210、220、230或更多个的那些。在一些实施方案中,间隔子区具有约119个氨基酸或更少,如长度为或为约119个氨基酸或长度不超过119个氨基酸。在一些实施方案中,间隔子区具有约229个氨基酸或更少,如长度为或为约229个氨基酸或长度不超过229个氨基酸。示例性间隔子包括单独的IgG4铰链、与CH2和CH3结构域连接的IgG4铰链或与CH3结构域连接的IgG4铰链。示例性间隔子包括但不限于以下文献中所述的那些:Hudecek等人(2013)Clin.Cancer Res.,19:3153;Hudecek等人(2015)Cancer Immunol.Res.,3(2):125-135或国际专利申请公开号WO 2014031687。
在一些实施方案中,间隔子具有SEQ ID NO:6中所示的序列。在一些实施方案中,间隔子具有SEQ ID NO:81中所示的序列。在一些实施方案中,间隔子具有SEQ ID NO:5中所示的序列。在一些实施方案中,间隔子具有SEQ ID NO:74中所示的序列。
抗原识别组分通常与一种或多种细胞内信号传导组分(例如模拟通过抗原受体复合物(在CAR的情况下,如TCR复合物)进行激活和/或经由另一种细胞表面受体传导信号的信号传导组分)连接。因此,在一些实施方案中,结合分子(例如抗体或其抗原结合片段)与一个或多个跨膜结构域(如本文所述的那些)和包含一种或多种细胞内组分(如本文所述的那些)的细胞内信号传导结构域连接。在一些实施方案中,跨膜结构域与细胞外结构域融合。在一个实施方案中,使用天然地与受体(例如CAR)中的一个结构域缔合的跨膜结构域。在一些情形中,通过氨基酸取代选择或修饰跨膜结构域,以避免此类结构域与相同或不同表面膜蛋白的跨膜结构域结合,以使与受体复合物的其他成员的相互作用最小化。
在一些实施方案中,跨膜结构域源自天然来源或源自合成来源。在来源是天然的情况下,在一些方面,结构域源自任何膜结合蛋白或跨膜蛋白。跨膜结构域包括源自以下各项的那些(即,包含以下各项的至少一个或多个跨膜结构域):T细胞受体的α、β或ζ链、CD3ε、CD4、CD5、CD8、CD9、CD16、CD22、CD28、CD33、CD37、CD45、CD64、CD80、CD86、CD134、CD137和/或CD154。可替代地,在一些实施方案中,跨膜结构域是合成的。在一些方面,合成跨膜结构域主要包含疏水性残基,如亮氨酸和缬氨酸。在一些方面,将在合成跨膜结构域的每个末端处发现苯丙氨酸、色氨酸和缬氨酸的三联体。在一些实施方案中,通过接头、间隔子和/或一个或多个跨膜结构域进行连接。
所述细胞内信号传导结构域包括模拟或接近通过天然抗原受体的信号、通过这种受体与共刺激受体的组合的信号、和/或仅通过共刺激受体的信号的那些。在一些实施方案中,短的寡肽或多肽接头(例如,长度在2与10个之间的氨基酸的接头,如含有甘氨酸和丝氨酸的接头,例如甘氨酸-丝氨酸双联体)存在并形成CAR的跨膜结构域与细胞内信号传导结构域之间的连接。
受体(例如CAR)通常包括含有至少一种或多种细胞内信号传导组分的细胞内信号传导结构域。在一些实施方案中,受体包括TCR复合物的细胞内组分,如介导T细胞激活和细胞毒性的TCR CD3链,例如CD3ζ链。因此,在一些方面,CCT5结合抗体与一个或多个细胞信号传导模块连接。在一些实施方案中,细胞信号传导模块包括CD3跨膜结构域、CD3细胞内信号传导结构域和/或其他CD跨膜结构域。在一些实施方案中,受体(例如,CAR)进一步包括一种或多种另外的分子(如Fc受体γ、CD8、CD4、CD25或CD16)的一部分。例如,在一些方面,CAR包括CD3-zeta(CD3-ζ)或Fc受体γ与CD8、CD4、CD25或CD16之间的嵌合分子。
在一些实施方案中,在连接所述CAR后,所述CAR的胞质结构域或细胞内信号传导结构域激活免疫细胞(例如,被工程化以表达所述CAR的T细胞)的正常效应子功能或应答中的至少一种。例如,在一些情境下,CAR诱导T细胞的功能,如细胞溶解活性或T辅助活性,如细胞因子或其他因子的分泌。在一些实施方案中,使用抗原受体组分或共刺激分子的细胞内信号传导结构域的截短部分代替完整的免疫刺激链,例如如果所述截短部分转导效应子功能信号的话。在一些实施方案中,所述一个或多个细胞内信号传导结构域包括T细胞受体(TCR)的胞质序列,并且在一些方面还包括共受体(其在天然背景下与这种受体一齐作用以在抗原受体接合后启动信号转导)和/或此类分子的任何衍生物或变体的那些,和/或具有相同功能能力的任何合成序列。
在天然TCR的情境下,完全激活通常不仅需要通过TCR进行信号传导,还需要共刺激信号。因此,在一些实施方案中,为了促进完全激活,用于产生次级或共刺激信号的组分也被包括在CAR中。在其他实施方案中,CAR不包括用于产生共刺激信号的组分。在一些方面,在同一细胞中表达另一CAR,并且提供用于产生次级或共刺激信号的组分。
在一些方面,将T细胞激活描述为由两个类别的胞质信号传导序列来介导:通过TCR启动抗原依赖性初级激活的那些(初级胞质信号传导序列)以及以抗原非依赖性方式作用以提供次级或共刺激信号的那些(次级胞质信号传导序列)。在一些方面,CAR包括此类胞质信号传导组分中的一种或两种。
在一些方面,CAR包括调节TCR复合物的初级激活的初级胞质信号传导序列。以刺激方式起作用的初级胞质信号传导序列可以含有信号传导基序(其称为基于免疫受体酪氨酸的激活基序或ITAM)。含有ITAM的初级胞质信号传导序列的例子包括源自TCR或CD3ζ、FcRγ、CD3γ、CD3δ和CD3ε的那些。在一些实施方案中,CAR中的细胞内信号传导结构域含有源自CD3ζ的胞质信号传导结构域、其部分或序列。
在一些实施方案中,CAR包括共刺激分子(如T细胞共刺激分子)的信号传导区(例如细胞内信号传导结构域)和/或跨膜部分。示例性共刺激分子包括CD28、4-1BB、OX40、DAP10和ICOS。在一些方面,同一CAR包括激活或刺激组分(例如胞质信号传导序列)和共刺激组分二者。在一些实施方案中,共刺激区域源自4-1BB的细胞内信号传导结构域。
在某些实施方案中,细胞内信号传导结构域包含连接至CD3(例如,CD3-ζ)细胞内结构域的CD28跨膜和信号传导结构域。在一些实施方案中,细胞内信号传导结构域包含与CD3ζ细胞内结构域连接的嵌合CD28和CD137(4-1BB,TNFRSF9)共刺激结构域。
在一些实施方案中,CAR涵盖在胞质部分中的一个或多个(例如,两个或更多个)共刺激结构域和激活结构域(例如初级激活结构域)。示例性CAR包括CD3ζ、CD28和4-1BB的细胞内组分。
在一些情况下,CAR称为第一代、第二代和/或第三代CAR。在一些方面,第一代CAR是在抗原结合后仅提供CD3链诱导的信号的CAR;在一些方面,第二代CAR是提供这种信号和共刺激信号的CAR,如包括来自共刺激受体(如CD28或CD137)的细胞内信号传导结构域的CAR;在一些方面,第三代CAR是在一些方面包括不同共刺激受体的多个共刺激结构域的CAR。
在一些实施方案中,嵌合抗原受体包括含有本文所述的抗体(例如抗CCT5抗体)或片段的细胞外部分。在一些方面,嵌合抗原受体包括含有本文所述的抗体或片段的细胞外部分和细胞内信号传导区或结构域。在一些实施方案中,抗体或片段包括scFv或仅包含V
在一些实施方案中,CAR含有抗体(例如,如本文所述的抗体片段(例如抗CCT5抗体))、跨膜结构域(其是或含有CD28的跨膜部分或其功能变体)以及含有CD28的信号传导部分或其功能变体和CD3ζ的信号传导部分或其功能变体的细胞内信号传导结构域。在一些实施方案中,CAR含有抗体(例如,如本文所述的抗体片段(例如抗CCT5抗体))、跨膜结构域(其是或含有CD28的跨膜部分或其功能变体)以及含有4-1BB的信号传导部分或其功能变体和CD3ζ的信号传导部分或其功能变体的细胞内信号传导结构域。在一些此类实施方案中,受体进一步包括间隔子,所述间隔子含有Ig分子(如人Ig分子)的一部分,如Ig铰链,例如IgG4铰链、与CH2和CH3结构域连接的IgG4铰链、或与CH3结构域连接的IgG4铰链。
在一些实施方案中,CAR包括特异性于或特异性地结合CCT5(如异常表达的CCT5)、和/或含有SEQ ID NO:68或69中所示的序列(例如,含有SEQ ID NO:70-72中的任一个中所示的序列)的多肽的抗体或片段,包括任何所提供的抗体或抗原结合片段(例如scFv);间隔子,如含有任何Ig铰链的间隔子;CD28跨膜结构域;CD28细胞内信号传导结构域;和CD3ζ信号传导结构域。在一些实施方案中,CAR包括特异性于或特异性地结合CCT5(如异常表达的CCT5)、和/或含有SEQ ID NO:68或69中所示的序列(例如,含有SEQ ID NO:70-72中的任一个中所示的序列)的多肽的抗体或片段,包括任何所提供的抗体或抗原结合片段(例如scFv);间隔子,如含有任何Ig铰链的间隔子;CD28跨膜结构域;4-1BB细胞内信号传导结构域;和CD3ζ信号传导结构域。
在一些实施方案中,受体(例如CAR)的跨膜结构域是人CD28的跨膜结构域或其变体,例如人CD28(GenBank登录号:P10747.1)的27个氨基酸的跨膜结构域,或者是包含SEQID NO:7中所示的氨基酸序列或展现出与SEQ ID NO:7至少或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高序列同一性的氨基酸序列的跨膜结构域;在一些实施方案中,含有重组受体的部分的跨膜结构域包含SEQID NO:78中所示的氨基酸序列或与SEQ ID NO:78具有至少或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高序列同一性的氨基酸序列。
在一些实施方案中,嵌合抗原受体含有T细胞共刺激分子的细胞内结构域。在一些方面,T细胞共刺激分子是CD28或4-1BB。
在一些实施方案中,细胞内信号传导区包含人CD28的细胞内共刺激信号传导结构域或其功能变体或部分,如其41个氨基酸的结构域,和/或在天然CD28蛋白的位置186-187处具有LL至GG取代的这种结构域。在一些实施方案中,细胞内信号传导区和/或结构域可以包含SEQ ID NO:61或63中所示的氨基酸序列,或展现出与SEQ ID NO:61或63至少或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高序列同一性的氨基酸序列。在一些实施方案中,细胞内区域包含4-1BB的细胞内共刺激信号传导结构域或其功能变体或部分,如人4-1BB(登录号Q07011.1)的42个氨基酸的胞质结构域或其功能变体或部分,如SEQ ID NO:8中所示的氨基酸序列或展现出与SEQ ID NO:8至少或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高序列同一性的氨基酸序列。
在一些实施方案中,细胞内信号传导区包含人CD3链、任选地CD3ζ刺激信号传导结构域或其功能变体,如人CD3ζ(登录号:P20963.2)的亚型3的112个AA的胞质结构域或如美国专利号7,446,190或美国专利号8,911,993中所述的CD3ζ信号传导结构域。在一些实施方案中,细胞内信号传导区包含SEQ ID NO:9、60、62或67中所示的氨基酸序列或展现出与SEQID NO:9、60、62或67至少或至少约85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高序列同一性的氨基酸序列。
在一些方面,间隔子仅含有IgG的铰链区,如仅IgG4或IgG1的铰链,如SEQ ID NO:6中所示的仅铰链间隔子。在其他实施方案中,间隔子是与C
2.多靶向
还提供了多特异性细胞,其含有本文所提供的抗体或抗原结合片段或包括本文所提供的抗体或抗原结合片段的多肽,包括特异性地结合CCT5(如异常表达的CCT5)、或含有SEQ ID NO:68或69中所示的序列(例如,含有SEQ ID NO:70-72中的任一个中所示的序列)的多肽的此类结合分子。在一些实施方案中,此类细胞含有包含如提供的抗体或抗原结合片段的细胞表面蛋白(包括受体(例如CAR)),和与不同抗原或CCT5的不同表位结合的另外的细胞表面蛋白(如另外的嵌合抗体)。
在一些实施方案中,所述细胞和方法包括多靶向策略,如在细胞上表达两种或更多种基因工程化受体,每种受体识别相同或不同的抗原,并且通常各自包括不同的细胞内信号传导组分。此类多靶向策略描述于例如以下文献中:国际专利申请公开号WO2014055668A1(描述激活和共刺激CAR的组合,例如,靶向单独存在于脱靶(例如正常细胞)上,但仅一起存在于待治疗疾病或病症的细胞上的两种不同抗原)和Fedorov等人,Sci.Transl.Medicine,5(215)(2013年12月)(描述表达激活和抑制性CAR的细胞,例如这样的细胞,其中激活CAR与同时在正常或非患病细胞和待治疗疾病或病症的细胞上表达的一种抗原结合,并且抑制性CAR与仅在正常细胞或不希望治疗的细胞上表达的另一种抗原结合)。
在一些实施方案中,CAR包括在同一细胞上表达的激活或刺激CAR和共刺激CAR(参见WO 2014/055668)。在一些实施方案中,细胞包括表达第一基因工程化抗原受体(例如,CAR或TCR)的受体,所述受体通常在特异性结合由第一受体识别的抗原(例如第一抗原)后,能够将激活或刺激信号诱导至所述细胞。在一些实施方案中,细胞进一步包括第二基因工程化抗原受体(例如,CAR或TCR),例如嵌合共刺激受体,所述受体通常在特异性结合由第二受体识别的第二抗原后,能够将共刺激信号诱导至免疫细胞。在一些实施方案中,第一抗原与第二抗原是相同的。
在一些实施方案中,第一抗原与第二抗原是不同的。在一些方面,靶向或特异性地结合CCT5(如异常表达的CCT5)、和/或含有SEQ ID NO:68或69中所示的序列(例如,含有SEQID NO:70-72中的任一个中所示的序列)的多肽的CAR是刺激或激活CAR;在其他方面,它是共刺激CAR。在一些实施方案中,第二基因工程化抗原受体包括刺激CAR或共刺激CAR中的另一者,并且对第二或不同抗原具有特异性。在一些实施方案中,第二或另外的抗原是在肿瘤上表达的抗原,如与由所提供的结合分子靶向的相同的肿瘤类型上的抗原,例如与CCT5(如异常表达的CCT5),和/或含有SEQ ID NO:68或69中所示的序列的多肽(例如含有SEQ IDNO:70-72中的任一个中所示的序列)所在的相同的肿瘤上的抗原。在一些实施方案中,第二或不同的抗原是如上文结合多靶向策略,例如章节I.D.2所述的任何抗原。在一些实施方案中,第二或不同的抗原是对上皮细胞癌具有特异性的抗原,所述上皮细胞癌如上皮恶性肿瘤,例如结肠癌、乳腺癌、卵巢癌、前列腺癌、胰腺癌、膀胱癌或肺癌的上皮恶性肿瘤。在一些实施方案中,第二或不同的抗原是通用肿瘤抗原。
在一些实施方案中,第一和/或第二基因工程化抗原受体(例如CAR或TCR)能够诱导激活或刺激信号至所述细胞。在一些实施方案中,受体包括含有ITAM或ITAM样基序的细胞内信号传导组分。在一些实施方案中,由第一受体诱导的激活涉及信号转导或细胞中蛋白质表达的变化,从而导致免疫应答(如ITAM磷酸化)的起始和/或ITAM介导的信号转导级联的起始、免疫突触的形成和/或所结合受体(例如CD4或CD8等)附近的分子的聚簇、一种或多种转录因子(如NF-κB和/或AP-1)的激活和/或对诸如细胞因子等因子的基因表达的诱导、增殖和/或存活。
在一些实施方案中,第一和/或第二受体包括共刺激受体如CD28、CD137(4-1BB)、OX40和/或ICOS的细胞内信号传导结构域。在一些实施方案中,第一受体和第二受体包括不同的共刺激受体的细胞内信号传导结构域。在一个实施方案中,第一受体含有CD28共刺激信号传导区,并且第二受体含有4-1BB共刺激信号传导区,或反之亦然。
在一些实施方案中,第一和/或第二受体包括含有ITAM或ITAM样基序的细胞内信号传导结构域和共刺激受体的细胞内信号传导结构域。
在一些实施方案中,第一受体含有包含ITAM或ITAM样基序的细胞内信号传导结构域,并且第二受体含有共刺激受体的细胞内信号传导结构域。与在相同细胞中诱导的激活或刺激信号组合的共刺激信号是导致免疫应答的共刺激信号,所述免疫应答例如为稳健且持续的免疫应答,例如增加的基因表达,细胞因子和其他因子的分泌,以及T细胞介导的效应子功能(如细胞杀伤)。
在一些实施方案中,单独的第一受体的连接和单独的第二受体的连接都不会诱导稳健的免疫应答。在一些方面,如果仅连接一种受体,则细胞变得耐受抗原或对抗原无反应,或被抑制,和/或不被诱导增殖或分泌因子或实现效应子功能。然而,在一些此类实施方案中,在连接所述多种受体时,如在遇到表达第一和第二抗原的细胞时,实现所需反应,如完全免疫激活或刺激,例如如通过一种或多种细胞因子的分泌、增殖、持久性和/或实施免疫效应子功能(如对靶细胞的细胞毒性杀伤)所指示。
在一些实施方案中,基因工程化细胞表达两种受体,所述两种受体分别将激活和抑制性信号诱导至细胞,使得一种受体与其抗原的结合激活细胞或诱导应答,但是第二抑制性受体与其抗原的结合诱导了抑制或减弱所述应答的信号。例子是激活CAR与抑制性CAR或iCAR的组合。例如,可以使用这种策略,其中激活CAR结合在疾病或病症中表达但也在正常细胞上表达的抗原,并且抑制性受体结合在正常细胞上表达但不在疾病或病症的细胞上表达的单独抗原。
在一些实施方案中,多靶向策略用于以下情况:其中与特定疾病或病症相关的抗原在未患病细胞上表达和/或在工程化细胞本身上表达,所述表达为瞬时表达(例如,在与基因工程化相关的刺激后)或永久表达。在此类情况下,通过需要连接两种分开且单独特异性的抗原受体,可以改善特异性、选择性和/或功效。在一些实施方案中,多种抗原(例如第一并且在一些情况下第二抗原)在所靶向的细胞、组织或疾病或病症上(如在癌细胞上)表达。在一些实施方案中,多种抗原中的一种或多种通常也在不需要用细胞疗法靶向的细胞(如正常或未患病细胞或组织,和/或工程化细胞本身)上表达。在此类实施方案中,因为需要连接多种受体以实现细胞的应答,实现特异性和/或功效。
在一些实施方案中,基因工程化细胞包括靶向或特异性地结合CCT5(如异常表达的CCT5)、和/或含有SEQ ID NO:68或69中所示的序列(例如,含有SEQ ID NO:70-72中的任一个中所示的序列)的多肽的CAR,所述CAR是刺激或激活CAR,并且还表达抑制性CAR(iCARs,参见Fedorov等人,Sci.Transl.Medicine,5(215)(2013年12月),如识别除CCT5之外、如除异常表达的CCT5之外、和/或除含有SEQ ID NO:68或69中所示的序列(例如,含有SEQ ID NO:70-72中的任一个中所示的序列)的多肽之外的抗原的CAR。在一些此类实施方案中,通过靶向CCT5(如异常表达的CCT5)、和/或含有SEQ ID NO:68或69中所示的序列(例如,含有SEQ ID NO:70-72中的任一个中所示的序列)的多肽的CAR递送的激活或刺激信号通过抑制性CAR与其配体的结合而有所减小或被抑制,例如以减小脱靶效应。在一些实施方案中,iCAR对不在上皮细胞癌上表达的第二或不同抗原具有特异性。在一些实施方案中,iCAR对为前列腺或哺乳动物上皮抗原的第二或不同抗原具有特异性。
3.工程化细胞和产生工程化细胞的方法
还提供了含有重组受体(例如嵌合抗原受体)的细胞(如工程化细胞),所述重组受体如为含有细胞外结构域(包括如本文所述的抗CCT5抗体或片段)的重组受体。还提供了此类细胞的群体、含有此类细胞和/或富含此类细胞的组合物,如其中表达CCT5结合分子的细胞构成组合物中总细胞或某种类型的细胞(如T细胞或CD8+或CD4+细胞)的至少50、60、70、80、90、91、92、93、94、95、96、97、98、99或更高百分比。组合物包括用于给予(如用于过继细胞疗法)的药物组合物和配制品。还提供了用于向受试者(例如,患者)给予所述细胞和组合物的治疗方法。
因此,还提供表达含有抗体的重组受体的基因工程化细胞,例如含有CAR的细胞。细胞通常是真核细胞,如哺乳动物细胞,并且通常是人细胞。在一些实施方案中,细胞源自血液、骨髓、淋巴或淋巴器官,是免疫系统的细胞,如先天免疫或适应性免疫的细胞,例如骨髓或淋巴样细胞(包括淋巴细胞,通常是T细胞和/或NK细胞)。其他示例性细胞包括干细胞,如多潜能干细胞和多能干细胞,包括诱导多能干细胞(iPSC)。细胞通常是原代细胞,如直接从受试者分离和/或从受试者分离并冷冻的那些。在一些实施方案中,细胞包括T细胞或其他细胞类型的一个或多个子集,如整个T细胞群、CD4+细胞、CD8+细胞及其亚群,如由以下所定义的那些亚群:功能、激活状态、成熟度、分化的可能性、扩增、再循环、定位和/或持久能力、抗原特异性、抗原受体类型、在特定器官或区室中的存在、标记或细胞因子分泌特征和/或分化程度。关于待治疗的受试者,细胞可以是同种异体的和/或自体的。方法包括现成的方法。在一些方面,如对于现成的技术,细胞是多能的和/或多潜能的,如干细胞,如诱导多能干细胞(iPSC)。在一些实施方案中,所述方法包括从受试者中分离细胞,如本文所述制备、加工、培养和/或工程化它们,并且在冷冻保存之前或之后将它们重新引入同一患者体内。
T细胞和/或CD4+和/或CD8+ T细胞的亚型和亚群包括幼稚T(T
在一些实施方案中,细胞是自然杀伤(NK)细胞。在一些实施方案中,细胞是单核细胞或粒细胞,例如骨髓细胞、巨噬细胞、嗜中性粒细胞、树突细胞、肥大细胞、嗜酸性粒细胞和/或嗜碱性粒细胞。
在一些实施方案中,细胞包括经由基因工程化引入的一个或多个核酸,从而表达此类核酸的重组或基因工程化产物。在一些实施方案中,核酸是异源的,即通常不存在于细胞或从细胞获得的样品中,如从另一种生物或细胞获得的核酸,例如,所述核酸通常不在被工程化的细胞和/或这种细胞所来源的生物中被发现。在一些实施方案中,核酸不是天然存在的,如在自然界中未发现的核酸,包括包含编码来自多种不同细胞类型的各种结构域的核酸的嵌合组合的核酸。在一些实施方案中,细胞(例如工程化细胞)包含如本文所述的载体(例如病毒载体、表达载体等),如包含编码本文所述的重组受体的核酸的载体。
a.用于基因工程化的载体和方法
还提供了用于表达结合分子(例如抗CCT5结合分子或抗体)(包括包含结合分子的重组受体(例如CAR))以及用于产生表达此类结合分子的基因工程化细胞的方法、核酸、组合物和试剂盒。在一些实施方案中,可以将包括重组受体(例如CAR)的一种或多种结合分子基因工程化至细胞或多种细胞中。基因工程化通常涉及将编码重组或工程化组分的核酸引入细胞中,例如通过逆转录病毒转导、转染或转化。还提供了编码重组受体的多核苷酸,以及含有此类核酸和/或多核苷酸的载体或构建体。
在一些情况下,编码重组受体的核酸序列含有编码信号肽的信号序列。在一些方面,信号序列可以编码源自天然多肽的信号肽。在其他方面,信号序列可以编码异源或非天然信号肽。
在一些实施方案中,载体骨架含有编码一种或多种标记的核酸序列。在一些实施方案中,所述一种或多种标记是转导标记、替代标记和/或选择标记。
在一些实施方案中,标记是转导标记或替代标记。可以将转导标记或替代标记用于检测已经引入多核苷酸(例如,编码重组受体的多核苷酸)的细胞。在一些实施方案中,转导标记可以指示或确认细胞的修饰。在一些实施方案中,替代标记是制备以在细胞表面上与重组受体(例如CAR)共表达的蛋白质。在特定实施方案中,这样的替代标记是已经被修饰以具有极少活性或无活性的表面蛋白。在某些实施方案中,替代标记由编码重组受体的同一多核苷酸编码。在一些实施方案中,编码所述重组受体的核酸序列与编码标记的核酸序列可操作地连接,任选地通过内部核糖体进入位点(IRES)或编码自切割肽或导致核糖体跳跃的肽(如2A序列,如T2A、P2A、E2A或F2A)的核酸分开。在一些情况下,外在标记基因可以结合工程化细胞以允许检测或选择细胞,并且在一些情况下还允许促进细胞自杀。
示例性替代标记可以包括细胞表面多肽的截短形式,如无功能并且不转导或不能转导信号或通常被细胞表面多肽的全长形式转导的信号、和/或不内化或不能内化的截短形式。示例性截短的细胞表面多肽包括生长因子或其他受体的截短形式,如截短的人表皮生长因子受体2(tHER2)、截短的表皮生长因子受体(tEGFR,SEQ ID NO:65或66中所示的示例性tEGFR序列)或前列腺特异性膜抗原(PSMA)或其修饰形式。tEGFR可以含有由抗体西妥昔单抗
在一些实施方案中,标记是或包含荧光蛋白,如绿色荧光蛋白(GFP)、增强型绿色荧光蛋白(EGFP)(如超折叠GFP(sfGFP))、红色荧光蛋白(RFP)(如tdTomato、mCherry、mStrawberry、AsRed2、DsRed或DsRed2)、青色荧光蛋白(CFP)、蓝绿色荧光蛋白(BFP)、增强型蓝色荧光蛋白(EBFP)和黄色荧光蛋白(YFP)及其变体,包括荧光蛋白的物种变体、单体变体和密码子优化的和/或增强的变体。在一些实施方案中,标记是或包含酶(如萤光素酶)、来自大肠杆菌的lacZ基因、碱性磷酸酶、分泌的胚胎碱性磷酸酶(SEAP)、氯霉素乙酰转移酶(CAT)。示例性发光报告基因包括萤光素酶(luc)、β-半乳糖苷酶、氯霉素乙酰转移酶(CAT)、β-葡糖醛酸糖苷酶(GUS)或其变体。
在一些实施方案中,标记是选择标记。在一些实施方案中,选择标记是或包含赋予对外源药剂或药物的抗性的多肽。在一些实施方案中,选择标记是抗生素抗性基因。在一些实施方案中,选择标记是向哺乳动物细胞赋予抗生素抗性的抗生素抗性基因。在一些实施方案中,选择标记是或包含嘌呤霉素抗性基因、潮霉素抗性基因、杀稻瘟菌素抗性基因、新霉素抗性基因、遗传霉素抗性基因或博莱霉素抗性基因或其经修饰形式。
在一些实施方案中,可以对包括抗体和/或重组受体(例如CAR)的一种或多种结合分子进行基因工程化,以在细胞或多种细胞中表达。在一些实施方案中,第一重组受体和第二结合分子(例如重组受体)由同一或单独的核酸分子编码。在一些实施方案中,将另外的结合分子工程化为在细胞或多种细胞中表达。
在一些实施方案中,载体或构建体可以含有驱动一种或多种核酸分子的表达的单个启动子。在一些实施方案中,此类核酸分子(例如转录物)可以是多顺反子的(双顺反子的或三顺反子的,参见例如美国专利号6,060,273)。例如,在一些实施方案中,可以将转录单元工程化为含有IRES(内部核糖体进入位点)的双顺反子单元,其允许通过来自单一启动子的信息共表达基因产物(例如其编码第一和第二嵌合受体)。可替代地,在一些情况下,单一启动子可以指导RNA的表达,所述RNA在单个开放阅读框(ORF)中含有两个或三个基因(例如,编码参与调节代谢途径的分子和编码重组受体),所述两个或三个基因由编码自切割肽(例如2A序列)或蛋白酶识别位点(例如弗林蛋白酶(furin))的序列彼此分开。因此,ORF编码单一多肽,其在翻译期间(在2A的情况下)或在翻译之后被加工成单一蛋白质。在一些情况下,肽(如T2A)可导致核糖体跳过2A元件C末端处肽键的合成(核糖体跳跃),导致2A序列末端与下游的下一个肽之间分开(参见例如de Felipe.Genetic Vaccines and Ther.2:13(2004)和deFelipe等人Traffic 5:616-626(2004))。已知许多2A元件。可以用于本文公开的方法和核酸中的2A序列的例子包括但不限于来自以下的2A序列:口蹄疫病毒(F2A,例如,SEQ ID NO:39或40)、马鼻炎A病毒(E2A,例如,SEQ ID NO:37或38)、明脉扁刺蛾β四体病毒(Thosea asigna virus)(T2A,例如,SEQ ID NO:31-34)和猪捷申病毒(porcineteschovirus)-1(P2A,例如,SEQ ID NO:35或36),如美国专利公开号20070116690中所述。在一些实施方案中,所述一种或多种不同或单独的启动子驱动编码所述一种或多种结合分子(例如重组受体)的一种或多种核酸分子的表达。
本文所提供的任何结合分子(例如抗体和/或重组受体,例如CCT5结合分子和/或另外的重组受体)可以由含有编码受体的一种或多种核酸分子的多核苷酸以任何组合或排列进行编码。例如,一种、两种、三种或更多种多核苷酸可以编码一种、两种、三种或更多种不同的受体或结构域。在一些实施方案中,一种载体或构建体含有编码一种或多种结合分子(例如抗体和/或重组受体)的核酸分子,并且单独的载体或构建体含有编码另外的结合分子(例如抗体和/或重组受体)的核酸分子。核酸分子中的每一种还可以编码一种或多种标记,如表面标记,例如截短的EGFR(tEGFR)。
还提供含有一种或多种核酸分子、载体或构建体(如上文所述的任何核酸分子、载体或构建体)的组合物。在一些实施方案中,核酸分子、载体、构建体或组合物可以用于将细胞(如T细胞)工程化以表达任何结合分子,例如抗体或重组受体和/或另外的结合分子。
在一些实施方案中,通过以下方式完成基因转移:首先刺激细胞,如通过将其与诱导反应(如增殖、存活和/或激活)的刺激物进行组合,例如如通过细胞因子或激活标记的表达测量的,然后转导激活的细胞,并且在培养中扩增至足以用于临床应用的数量。
在一些情境下,刺激因子(例如淋巴因子或细胞因子)的过表达可能对受试者有毒性。因此,在一些情境下,工程化细胞包括例如在过继免疫疗法中给予后导致细胞在体内对阴性选择易感的基因区段。例如,在一些方面,将细胞工程化,使得它们可以由于给予过它们的患者的体内状况的改变而被消除。阴性选择性表型可以由赋予对所给予的药剂(例如化合物)的敏感性的基因的插入而产生。阴性选择性基因包括单纯疱疹病毒I型胸苷激酶(HSV-I TK)基因(Wigler等人,Cell 2:223,1977),其赋予更昔洛韦敏感性;细胞次黄嘌呤磷酸核糖基转移酶(HPRT)基因;细胞腺嘌呤磷酸核糖基转移酶(APRT)基因;细菌胞嘧啶脱氨酶(Mullen等人,Proc.Natl.Acad.Sci.USA.89:33(1992))。
在一些方面,对细胞进一步工程化以促进细胞因子或其他因子的表达。用于引入基因工程化组分(例如,抗原受体,例如CAR)的各种方法是熟知的,并且可以与所提供的方法和组合物一起使用。示例性方法包括用于转移编码受体的核酸的那些,包括通过病毒(如逆转录病毒或慢病毒)、转导、转座子和电穿孔。
在一些实施方案中,使用重组感染性病毒颗粒(例如源自猿猴病毒40(SV40)、腺病毒、腺相关病毒(AAV)的载体)将重组核酸转移到细胞中。在一些实施方案中,使用重组慢病毒载体或逆转录病毒载体(如γ-逆转录病毒载体)将重组核酸转移到T细胞中(参见例如Koste等人(2014)Gene Therapy 2014年4月3日.doi:10.1038/gt.2014.25;Carlens等人(2000)Exp Hematol 28(10):1137-46;Alonso-Camino等人(2013)Mol Ther Nucl Acids2,e93;Park等人,Trends Biotechnol.2011年11月29日(11):550-557)。
在一些实施方案中,逆转录病毒载体具有长末端重复序列(LTR),例如,源自莫洛尼鼠白血病病毒(MoMLV)、骨髓增生性肉瘤病毒(MPSV)、鼠胚胎干细胞病毒(MESV)、鼠干细胞病毒(MSCV)、脾病灶形成病毒(SFFV)、人免疫缺陷病毒1型(HIV-1)或腺相关病毒(AAV)的逆转录病毒载体。大多数逆转录病毒载体源自鼠逆转录病毒。在一些实施方案中,逆转录病毒包括源自任何禽类或哺乳动物细胞来源的那些。逆转录病毒通常是双嗜性的,这意味着它们能够感染包括人在内的若干种物种的宿主细胞。在一个实施方案中,待表达的基因替代逆转录病毒gag、pol和/或env序列。已经描述了许多例示性逆转录病毒系统(例如,美国专利号5,219,740;6,207,453;5,219,740;Miller和Rosman(1989)BioTechniques 7:980-990;Miller,A.D.(1990)Human Gene Therapy 1:5-14;Scarpa等人(1991)Virology 180:849-852;Burns等人(1993)Proc.Natl.Acad.Sci.USA 90:8033-8037;以及Boris-Lawrie和Temin(1993)Cur.Opin.Genet.Develop.3:102-109。
慢病毒转导的方法是已知的。示例性方法描述于例如Wang等人(2012)J.Immunother.35(9):689-701;Cooper等人(2003)Blood.101:1637-1644;Verhoeyen等人(2009)Methods Mol Biol.506:97-114;以及Cavalieri等人(2003)Blood.102(2):497-505。
在一些实施方案中,通过电穿孔将重组核酸转移到T细胞中(参见例如Chicaybam等人,(2013)PLoS ONE 8(3):e60298;和Van Tedeloo等人(2000)Gene Therapy 7(16):1431-1437)。在一些实施方案中,通过转座将重组核酸转移到T细胞中(参见例如Manuri等人(2010)Hum Gene Ther 21(4):427-437;Sharma等人(2013)Molec Ther Nucl Acids 2,e74;以及Huang等人(2009)Methods Mol Biol 506:115-126)。在免疫细胞中引入和表达遗传物质的其他方法包括磷酸钙转染(例如,如在Current Protocols in MolecularBiology,John Wiley&Sons,New York.N.Y.中所述)、原生质体融合、阳离子脂质体介导的转染;钨粒子促进的微粒轰击(Johnston,Nature,346:776-777(1990));以及磷酸锶DNA共沉淀(Brash等人,Mol.Cell Biol.,7:2031-2034(1987))。
用于转移编码重组产物的核酸的其他方法和载体是例如国际专利申请公开号WO2014055668和美国专利号7,446,190中所述的那些。
另外的核酸(例如,用于引入的基因)包括用于改善治疗功效的那些,例如通过促进转移细胞的活力和/或功能;提供用于选择和/或评价细胞的遗传标记的基因,例如以评估体内存活或定位;改善安全性的基因,例如通过使细胞在体内对阴性选择易感,如LuptonS.D.等人,Mol.and Cell Biol.,11:6(1991);和Riddell等人,Human Gene Therapy 3:319-338(1992)所述;还参见Lupton等人的PCT/US91/08442和PCT/US94/05601的公开,其描述了使用源自将显性阳性选择性标记与阴性选择性标记融合的双功能选择性融合基因。参见例如Riddell等人,美国专利号6,040,177,第14-17栏。
b.制备用于工程化的细胞
在一些实施方案中,工程化细胞的制备包括一个或多个培养和/或制备步骤。用于引入重组受体(例如CAR)的细胞可以从样品(如生物样品,例如获自或源自受试者的样品)中分离。在一些实施方案中,分离出所述细胞的受试者是患有疾病或病症或需要细胞疗法或将给予细胞疗法的受试者。在一些实施方案中,受试者是需要特定治疗性干预(如所分离、加工和/或工程化的细胞所用于的过继细胞疗法)的人。
因此,在一些实施方案中,细胞是原代细胞,例如原代人细胞。样品包括直接取自受试者的组织、流体和其他样品,以及从一个或多个加工步骤(如分离、离心、基因工程化(例如用病毒载体转导)、洗涤和/或孵育)得到的样品。生物样品可以是直接从生物来源获得的样品或经过加工的样品。生物样品包括但不限于体液(如血液、血浆、血清、脑脊液、滑液、尿液和汗液)、组织和器官样品,包括源自它们的加工样品。
在一些方面,细胞从其中来源或分离的样品是血液或血液来源的样品,或者是或源自单采术或白细胞单采术产物。示例性样品包括全血、外周血单核细胞(PBMC)、白细胞、骨髓、胸腺、组织活检、肿瘤、白血病、淋巴瘤、淋巴结、肠相关淋巴组织、粘膜相关淋巴组织、脾、其他淋巴组织、肝、肺、胃、肠、结肠、肾、胰腺、乳房、骨、前列腺、子宫颈、睾丸、卵巢、扁桃体或其他器官和/或源自它们的细胞。在细胞疗法(例如,过继细胞疗法)的情境下,样品包括来自自体和同种异体来源的样品。
在一些实施方案中,细胞源自细胞系,例如T细胞系。在一些实施方案中,细胞获自异种来源,例如获自小鼠、大鼠、非人灵长类动物或猪。
在一些实施方案中,细胞的分离包括一个或多个制备和/或基于非亲和力的细胞分离步骤。在一些例子中,将细胞在存在一种或多种试剂的情况下进行洗涤、离心和/或孵育,例如以去除不需要的组分,针对所需组分进行富集,裂解或去除对特定试剂敏感的细胞。在一些例子中,基于一种或多种特性(如密度、粘附特性、大小、对特定组分的敏感性和/或抗性)分离细胞。
在一些例子中,例如通过单采术或白细胞单采术获得来自受试者的循环血液的细胞。在一些方面,样品含有淋巴细胞(包括T细胞、单核细胞、粒细胞、B细胞)、其他有核白细胞、红细胞和/或血小板,并且在一些方面含有除红细胞和血小板之外的细胞。
在一些实施方案中,洗涤从受试者收集的血细胞,例如以去除血浆级分,并将细胞置于适当的缓冲液或介质中以用于随后的加工步骤。在一些实施方案中,用磷酸盐缓冲盐水(PBS)洗涤细胞。在一些实施方案中,洗涤溶液缺乏钙和/或镁和/或许多或全部二价阳离子。在一些方面,洗涤步骤是根据制造商的说明书在半自动化“流通式”离心机(例如,Cobe2991细胞加工器,Baxter)中完成的。在一些方面,根据制造商的说明书,通过切向流过滤(TFF)完成洗涤步骤。在一些实施方案中,洗涤后将细胞重悬于多种生物相容性缓冲液(例如不含Ca
在一些实施方案中,所述方法包括基于密度的细胞分离方法,如通过裂解红细胞并通过Percoll或Ficoll梯度离心而从外周血制备白细胞。
在一些实施方案中,分离方法包括基于细胞中一种或多种特定分子(如表面标记(例如,表面蛋白)、细胞内标记或核酸)的表达或存在来分离不同细胞类型。在一些实施方案中,可以使用任何已知的基于此类标记的分离方法。在一些实施方案中,分离是基于亲和力或基于免疫亲和力的分离。例如,在一些方面,分离包括基于一种或多种标记(通常是细胞表面标记)在细胞中的表达或表达水平来分离细胞和细胞群,例如通过与和此类标记特异性地结合的抗体或结合配偶体一起孵育,之后通常进行洗涤步骤并将已结合所述抗体或结合配偶体的细胞与尚未结合至所述抗体或结合配偶体的那些细胞分离。
此类分离步骤可以基于阳性选择(其中保留已结合试剂的细胞以供进一步使用)和/或阴性选择(其中保留尚未结合至所述抗体或结合配偶体的细胞)。在一些例子中,保留两种级分以供进一步使用。在一些方面,在无法获得专门鉴定异质性群体中的细胞类型的抗体,使得最好基于除所需群体之外的细胞表达的标记来进行分离的情况下,阴性选择可以特别有用。
分离不需要导致100%富集或去除特定细胞群或表达特定标记的细胞。例如,针对特定类型的细胞(如表达标记的那些)的阳性选择或富集是指增加此类细胞的数量或百分比,但不需要导致不表达所述标记的细胞的完全不存在。同样地,特定类型的细胞(如表达标记的那些)的阴性选择、去除或耗尽是指减少此类细胞的数量或百分比,但不需要导致所有此类细胞的完全去除。
在一些例子中,进行多轮分离步骤,其中来自一个步骤的阳性或阴性选择的级分经受另一个分离步骤,如随后的阳性或阴性选择。在一些例子中,单个分离步骤可以同时耗尽表达多种标记的细胞,如通过将细胞与多种抗体或结合配偶体(每种抗体或结合配偶体对被靶向用于阴性选择的标记具有特异性)一起孵育。同样,可以通过将细胞与在各种细胞类型上表达的多种抗体或结合配偶体一起孵育,对多种细胞类型同时进行阳性选择。
例如,在一些方面,T细胞的特定亚群,如对一种或多种表面标记呈阳性或高水平表达的细胞(例如CD28+、CD62L+、CCR7+、CD27+、CD127+、CD4+、CD8+、CD45RA+和/或CD45RO+T细胞)通过阳性或阴性选择技术来分离。
例如,可以使用抗CD3/抗CD28缀合的磁珠(例如,
在一些实施方案中,通过阳性选择富集特定细胞群,或通过阴性选择耗尽特定细胞群来进行分离。在一些实施方案中,阳性或阴性选择是通过将细胞与一种或多种抗体或其他结合剂一起孵育完成的,所述一种或多种抗体或其他结合剂与分别在阳性或阴性选择的细胞上表达(标记
在一些实施方案中,通过对非T细胞(如B细胞、单核细胞或其他白细胞)上表达的标记(如CD14)进行阴性选择,将T细胞从PBMC样品分离。在一些方面,CD4+或CD8+选择步骤用于分离CD4+辅助T细胞和CD8+细胞毒性T细胞。通过对在一种或多种幼稚、记忆和/或效应T细胞亚群上表达或以相对较高程度表达的标记的阳性或阴性选择,可以将此类CD4+和CD8+群体进一步分类成亚群。
在一些实施方案中,如通过基于与相应亚群相关的表面抗原进行阳性或阴性选择,将CD8+细胞针对幼稚、中枢记忆、效应记忆和/或中枢记忆干细胞进一步富集或耗尽。在一些实施方案中,针对中枢记忆T(T
在实施方案中,记忆T细胞存在于CD8+外周血淋巴细胞的CD62L+和CD62L-两个子集中。可以例如使用抗CD8和抗CD62L抗体将PBMC针对CD62L-CD8+和/或CD62L+CD8+级分进行富集或耗尽。
在一些实施方案中,中枢记忆T(T
在特定例子中,使PBMC样品或其他白细胞样品经历CD4+细胞的选择,其中保留了阴性和阳性两种级分。然后使阴性级分经历基于CD14和CD45RA的表达的阴性选择和基于中枢记忆T细胞所特有的标记(如CD62L或CCR7)的阳性选择,其中阳性和阴性选择是以任何顺序进行的。
通过鉴定具有细胞表面抗原的细胞群,将CD4+ T辅助细胞分类为幼稚、中枢记忆和效应细胞。CD4+淋巴细胞可以通过标准方法获得。在一些实施方案中,幼稚CD4+ T淋巴细胞是CD45RO-、CD45RA+、CD62L+、CD4+ T细胞。在一些实施方案中,中枢记忆CD4+细胞是CD62L+和CD45RO+。在一些实施方案中,效应CD4+细胞是CD62L-和CD45RO-。
在一个例子中,为了通过阴性选择富集CD4+细胞,单克隆抗体混合剂通常包括针对CD14、CD20、CD11b、CD16、HLA-DR和CD8的抗体。在一些实施方案中,抗体或结合配偶体与固体支持物或基质(如磁珠或顺磁珠)结合,以允许细胞分离以用于阳性和/或阴性选择。例如,在一些实施方案中,使用免疫磁性(或亲和磁性)分离技术来分离或分离开细胞和细胞群(综述于以下文献中:Methods in Molecular Medicine,第58卷:Metastasis ResearchProtocols,第2卷:Cell Behavior In vitro and In vivo,第17-25页S.A.Brooks和U.Schumacher编辑
在一些方面,将待分离的细胞的样品或组合物与小的可磁化或磁响应材料(如磁响应粒子或微粒,如顺磁珠(例如像Dynabeads
在一些实施方案中,磁性颗粒或磁珠包含与特异性结合成员(如抗体或其他结合配偶体)结合的磁响应材料。存在许多熟知的用于磁分离方法的磁响应材料。合适的磁性颗粒包括在Molday,美国专利号4,452,773和欧洲专利说明书EP 452342 B中所述的那些,将所述专利通过引用特此并入。胶体大小的颗粒(例如在Owen美国专利号4,795,698和Liberti等人,美国专利号5,200,084中所述的那些)是其他的例子。
孵育通常在这样的条件下进行,由此抗体或结合配偶体或者与附接至磁性颗粒或磁珠的此类抗体或结合配偶体特异性地结合的分子(如二抗或其他试剂)与细胞表面分子(如果存在于样品内的细胞上的话)特异性地结合。
在一些方面,将样品置于磁场中,并且附接有磁响应或可磁化颗粒的那些细胞将被吸引至磁体并与未标记的细胞分离。对于阳性选择,保留被吸引至磁体的细胞;对于阴性选择,保留未被吸引的细胞(未标记的细胞)。在一些方面,在同一选择步骤期间进行阳性与阴性选择的组合,其中保留阳性和阴性级分并进一步处理或进行进一步的分离步骤。
在某些实施方案中,磁响应颗粒被包被在一抗或其他结合配偶体、二抗、凝集素、酶或链霉亲和素中。在某些实施方案中,磁性颗粒通过对一种或多种标记具有特异性的一抗的包衣而附接至细胞。在某些实施方案中,用一抗或结合配偶体标记细胞而不是珠,然后添加细胞类型特异性二抗或其他结合配偶体(例如,链霉亲和素)包被的磁性颗粒。在某些实施方案中,链霉亲和素包被的磁性颗粒是与生物素化的一抗或二抗结合使用的。
在一些实施方案中,磁响应颗粒保持附接至细胞,所述细胞随后被孵育、培养和/或工程化;在一些方面,颗粒保持附接至细胞以用于给予患者。在一些实施方案中,从细胞去除可磁化或磁响应颗粒。用于从细胞中去除可磁化颗粒的方法是已知的,并且包括例如使用竞争性非标记抗体、可磁化颗粒或与可切割接头缀合的抗体等。在一些实施方案中,所述可磁化颗粒是可生物降解的。
在一些实施方案中,基于亲和力的选择是通过磁激活细胞分选
在某些实施方案中,使用进行所述方法的分离、细胞制备、分开、处理、孵育、培养和/或配制步骤中的一个或多个的系统、装置或设备进行分离或分开。在一些方面,将所述系统用于在封闭或无菌环境中进行这些步骤中的每一个,例如以使错误、用户操作和/或污染降至最低。在一个例子中,系统是如国际专利申请公开号WO 2009/072003、或US20110003380 A1中所述的系统。
在一些实施方案中,所述系统或设备在集成或独立系统中和/或以自动化或可编程方式进行分离、处理、工程化和配制步骤中的一个或多个(例如,全部)。在一些方面,所述系统或设备包括与所述系统或设备通信的计算机和/或计算机程序,其允许用户对处理、分离、工程化和配制步骤的各个方面进行编程、控制、评估其结果和/或调整。
在一些方面,使用
在一些方面,
在某些实施方案中,使用CliniMACS
在一些实施方案中,经由流式细胞术收集并富集(或耗尽)本文所述的细胞群,其中针对多种细胞表面标记染色的细胞携载于流体流中。在一些实施方案中,经由制备规模(FACS)分选来收集并富集(或耗尽)本文所述的细胞群。在某些实施方案中,通过使用微机电系统(MEMS)芯片结合基于FACS的检测系统来收集和富集(或耗尽)本文所述的细胞群(参见例如WO 2010/033140,Cho等人(2010)Lab Chip 10,1567-1573;和Godin等人(2008)JBiophoton.1(5):355-376。在两种情况下,可以用多种标记来标记细胞,从而允许以高纯度分离明确限定的T细胞子集。
在一些实施方案中,用一种或多种可检测标记来标记抗体或结合配偶体,以促进用于阳性和/或阴性选择的分离。例如,分离可以基于与荧光标记的抗体的结合。在一些例子中,基于对一种或多种细胞表面标记具特异性的抗体或其他结合配偶体的结合来分离细胞携载于流体流中,如通过荧光激活细胞分选(FACS)(包括制备规模(FACS))和/或微机电系统(MEMS)芯片,例如与流式细胞检测系统组合。此类方法允许基于多种标记来同时进行阳性和阴性选择。
在一些实施方案中,制备方法包括在分离、孵育和/或工程化之前或之后冷冻(例如,冷冻保存)细胞的步骤。在一些实施方案中,冷冻和后续解冻步骤去除细胞群中的粒细胞,并且在一定程度上去除单核细胞。在一些实施方案中,例如在洗涤步骤之后将细胞悬浮在冷冻溶液中以去除血浆和血小板。在一些方面,可以使用多种已知的冷冻溶液和参数中的任何一种。一个例子涉及使用含有20%DMSO和8%人血清白蛋白(HSA)的PBS或其他合适的细胞冷冻培养基。然后用培养基将其1:1稀释,使得DMSO和HSA的最终浓度分别为10%和4%。然后将细胞以1°/分钟的速率冷冻至-80℃并储存在液氮储罐的气相中。
在一些实施方案中,所提供的方法包括培育、孵育、培养和/或基因工程化步骤。例如,在一些实施方案中,提供了用于孵育耗尽的细胞群和培养起始组合物和/或将它们工程化的方法。
因此,在一些实施方案中,在培养起始组合物中孵育所述细胞群。孵育和/或工程化可以在培养器皿中进行,所述培养容器是例如单元、室、孔、柱、管、管组、阀、小瓶、培养皿、袋或其他用于培养或培育细胞的容器。
在一些实施方案中,在基因工程化之前或与基因工程化结合孵育和/或培养细胞。孵育步骤可以包括培养、培育、刺激、激活和/或繁殖。在一些实施方案中,在刺激条件或刺激剂的存在下孵育组合物或细胞。此类条件包括针对以下而设计的那些条件:诱导群体中的细胞的增殖、扩增、激活和/或存活,模拟抗原暴露,和/或引发细胞用于基因工程化(如用于引入重组抗原受体)。
条件可以包括以下中的一种或多种:特定培养基、温度、氧含量、二氧化碳含量、时间、药剂(例如,营养素、氨基酸、抗生素、离子和/或刺激因子(如细胞因子、趋化因子、抗原、结合配偶体、融合蛋白、重组可溶性受体和任何其他旨在激活细胞的药剂))。
在一些实施方案中,刺激条件或刺激剂包括能够激活TCR复合物的细胞内信号传导结构域的一种或多种药剂(例如,配体)。在一些方面,药剂在T细胞中开启或启动TCR/CD3细胞内信号传导级联。此类药剂可以包括抗体,如对TCR具特异性的那些,例如抗CD3。在一些实施方案中,刺激条件包括能够刺激共刺激受体的一种或多种药剂(例如配体),例如抗CD28。在一些实施方案中,此类药剂和/或配体可以与固体支持物(如珠)和/或一种或多种细胞因子结合。任选地,扩增方法还可以包括向培养基中(例如,以至少约0.5ng/ml的浓度)添加抗CD3和/或抗CD28抗体的步骤。在一些实施方案中,刺激剂包括IL-2、IL-15和/或IL-7。在一些方面,IL-2浓度为至少约10单位/mL。
在一些方面,孵育是根据多种技术来进行,例如以下文献中所述的那些技术:授予Riddell等人的美国专利号6,040,177;Klebanoff等人(2012)J Immunother.35(9):651-660,Terakura等人(2012)Blood.1:72-82,和/或Wang等人(2012)J Immunother.35(9):689-701。
在一些实施方案中,通过以下方式扩增T细胞:向培养起始组合物中添加饲养细胞(如非分裂外周血单核细胞(PBMC))(例如,使得所得细胞群含有至少约5、10、20或40种或更多种PBMC饲养细胞,以使初始群体中的每种T淋巴细胞进行扩增);以及孵育培养物(例如,持续足以扩增T细胞数的时间)。在一些方面,非分裂饲养细胞可以包含γ辐照的PBMC饲养细胞。在一些实施方案中,用约3000至3600拉德范围内的γ射线辐照PBMC以防止细胞分裂。在一些方面,在添加T细胞群之前将饲养细胞添加至培养基中。
在一些实施方案中,刺激条件包括适合于人T淋巴细胞生长的温度,例如至少约25摄氏度,通常为至少约30摄氏度,并且通常为或为约37摄氏度。任选地,孵育还可以包括添加非分裂EBV转化的类淋巴母细胞(LCL)作为饲养细胞。可以用约6000至10,000拉德范围内的γ射线辐照LCL。在一些方面,以任何合适的量提供LCL饲养细胞,如LCL饲养细胞与初始T淋巴细胞的比率为至少约10:1。
在实施方案中,通过用抗原刺激幼稚或抗原特异性T淋巴细胞获得抗原特异性T细胞,如抗原特异性CD4+和/或CD8+ T细胞。例如,可以通过从被感染的受试者分离T细胞并在体外用相同抗原刺激所述细胞,针对巨细胞病毒抗原来产生抗原特异性T细胞系或克隆。
c.用于多靶向的工程化细胞、载体和组合物
还提供可以结合和/或靶向多种抗原的细胞,如工程化细胞。在一些实施方案中,通过靶向多种抗原的策略实现改善的选择性和特异性。此类策略通常涉及多个抗原结合结构域,其通常存在于不同的基因工程化抗原受体上并特异性地结合不同的抗原。在一些实施方案中,将细胞工程化为具有结合多于一种抗原的能力。例如,在一些实施方案中,将细胞工程化以表达多特异性结合分子。在一些实施方案中,细胞表达多种结合分子(例如重组受体),其每一种都可以靶向一种抗原或多种抗原,例如一种受体(如本文所述的任何一种)靶向CCT5且另一种受体靶向另一种抗原(例如肿瘤抗原)。在一些方面,将与不同抗原特异地结合的多种基因工程化抗原受体引入细胞中,所述不同抗原中的每一种在将被细胞或组织或其细胞靶向的疾病或病症之中或之上表达。在一些方面,此类特征可以解决脱靶效应或减少脱靶效应的可能性或增加功效。例如,在疾病或病症中表达的单个抗原也在非患病或正常细胞之上或之中表达的情况下,此类多靶向方法可以通过要求经由多种抗原受体结合来激活细胞或诱导特定效应子功能,从而提供对所需细胞类型的选择性。在一些实施方案中,可以将多种细胞工程化以表达一种或多种不同的结合分子(例如重组受体),其每一种都可以靶向一种抗原或多种抗原。
还提供了含有本文所述的任何结合分子的多特异性细胞,如含有细胞表面蛋白(包括抗CCT5抗体)和与不同抗原或CCT5上的不同表位结合的另外的细胞表面蛋白(如另外的嵌合受体)的细胞。在一些实施方案中,提供了表达重组受体的细胞的组合物,其中结合分子、多特异性结合分子和/或重组受体中的一种或多种结合和/或靶向CCT5。还提供了含有多种细胞的细胞组合物,所述多种细胞表达可以靶向一种或多种抗原的一种或多种不同的结合分子,例如重组受体。在一些实施方案中,多特异性结合分子和/或重组受体靶向CCT5上的一个或多个不同的表位。
在一些实施方案中,提供细胞的组合物,其中每种类型的细胞表达一种或多种结合分子,例如重组受体。在一些实施方案中,细胞包含(例如,已经用以下项转化)一种或多种载体,所述一种或多种载体包含编码一种或多种氨基酸序列的一种或多种核酸,所述一种或多种氨基酸序列包含一种或多种抗体和/或其部分(例如其抗原结合片段)。在一些实施方案中,提供一种或多种此类细胞。在一些实施方案中,提供含有一种或多种此类细胞的组合物。在一些实施方案中,所述一种或多种细胞可以表达不同的抗体或相同的抗体。在一些实施方案中,每种细胞表达一种或多种抗体,如多于一种抗体。在一些实施方案中,每种细胞表达多特异性结合分子,例如多特异性受体,例如CAR。
在一些实施方案中,细胞包括靶向CCT5和与特定疾病或病症相关的第二或另外的抗原的多靶向策略。在一些实施方案中,第二或另外的抗原被多特异性结合分子和/或多种结合分子和/或多种细胞(例如,一种或多种细胞)靶向,每种细胞被工程化以表达一种或多种重组受体。在一些实施方案中,靶向第二或另外的抗原的重组受体在与CCT5结合分子相同的细胞上或在不同的细胞上表达。
在一些实施方案中,用于多靶向策略的第二或另外的抗原包括其中至少一种抗原是通用肿瘤抗原或其家族成员的那些抗原。在一些实施方案中,第二或另外的抗原是在肿瘤上表达的抗原。在一些实施方案中,本文所提供的CCT5结合分子靶向与第二或另外的抗原相同的肿瘤类型上的抗原。在一些实施方案中,第二或另外的抗原可以是通用肿瘤抗原或可以是为肿瘤类型所特有的肿瘤抗原。在一些实施方案中,细胞进一步包含识别在待治疗的疾病或病症上表达的第二或另外的抗原并诱导刺激或激活信号的另外的基因工程化抗原受体。
示例性抗原包括CD4、CD5、CD8、CD14、CD15、CD19、CD20、CD21、CD22、CD23、CD25、CD33、CD37、CD38、CD40、CD40L、CD46、CD52、CD54、CD74、CD80、CD126、CD138、B7、MUC-1、Ia、HM1.24、HLA-DR、腱生蛋白、血管生成因子、VEGF、PIGF、ED-B纤连蛋白、致癌基因、致癌基因产物、CD66a-d、坏死抗原、Ii、IL-2、T101、TAC、IL-6、ROR1、TRAIL-R1(DR4)、TRAIL-R2(DR5)、B细胞成熟抗原(CCT5)、tEGFR、Her2、L1-CAM、间皮素、CEA、乙型肝炎表面抗原、抗叶酸受体、CD24、CD30、CD44、EGFR、EGP-2、EGP-4、EPHa2、ErbB2、ErbB3、ErbB4、erbB二聚体、EGFR vIII、FBP、FCRL5、FCRH5、胎儿乙酰胆碱受体、GD2、GD3、HMW-MAA、IL-22R-α、IL-13R-α2、kdr、κ轻链、Lewis Y、L1-细胞粘附分子(L1-CAM)、黑色素瘤相关抗原(MAGE)-A1、MAGE-A3、MAGE-A6、黑色素瘤优先表达抗原(PRAME)、存活蛋白、EGP2、EGP40、TAG72、B7-H6、IL-13受体a2(IL-13Ra2)、CA9、CD171、G250/CAIX、HLA-AI MAGE Al、HLA-A2 NY-ESO-1、PSCA、叶酸受体-a、CD44v6、CD44v7/8、avb6整合素、8H9、NCAM、VEGF受体、5T4、胎儿AchR、NKG2D配体、双抗原、与通用标签相关的抗原、癌症-睾丸抗原、MUC1、MUC16、NY-ESO-1、MART-1、gp100、癌胚胎抗原、VEGF-R2、癌胚抗原(CEA)、前列腺特异性抗原、PSMA、Her2/neu、雌激素受体、孕酮受体、肝配蛋白B2、CD123、c-Met、GD-2、O-乙酰化GD2(OGD2)、CE7、Wilms肿瘤1(WT-1)、细胞周期蛋白、细胞周期蛋白A2、CCL-1、hTERT、MDM2、CYP1B、WT1、活素、AFP、p53、细胞周期蛋白(D1)、CS-1、CCT5、BAFF-R、TACI、CD56、TIM-3、CD123、L1-细胞粘附分子、MAGE-A1、MAGE A3、细胞周期蛋白(如细胞周期蛋白A1(CCNA1))和/或病原体特异性抗原、生物素化分子、由HIV、HCV、HBV和/或其他病原体表达的分子;和/或在一些方面,其新表位或新抗原。在一些实施方案中,抗原与通用标签相关或者是通用标签。
在一些实施方案中,多种抗原(例如,第一抗原(例如CCT5)和第二或另外的抗原)在所靶向的细胞、组织或者疾病或病症上(例如在癌细胞上)表达。在一些方面,细胞、组织、疾病或病症是多发性骨髓瘤或多发性骨髓瘤细胞。所述多种抗原中的一种或多种通常也在不需要用细胞疗法靶向的细胞(如正常或未患病细胞或组织)和/或工程化细胞本身上表达。在此类实施方案中,通过需要连接多种受体以实现细胞的反应,实现了特异性和/或功效。
在一些实施方案中,所述细胞和方法包括多靶向策略,如例在细胞上表达两种或更多种基因工程化受体,每种受体识别不同的抗原并且通常各自包括不同的细胞内信号传导组分。此类多靶向策略描述于例如以下文献中:国际专利申请公开号WO 2014055668 A1(描述激活和共刺激CAR的组合,例如,靶向单独存在于脱靶(例如正常细胞)上,但仅一起存在于待治疗疾病或病症的细胞上的两种不同抗原)和Fedorov等人,Sci.Transl.Medicine,5(215)(2013年12月)(描述表达激活和抑制性CAR的细胞,例如这样的细胞,其中激活CAR与同时在正常或非患病细胞和待治疗疾病或病症的细胞上表达的一种抗原结合,并且抑制性CAR与仅在正常细胞或不希望治疗的细胞上表达的另一种抗原结合)。
在一些实施方案中,提供多种细胞,每种细胞被工程化以表达一种或多种重组受体。例如,在一些实施方案中,将一种细胞工程化以表达结合和/或靶向CCT5的结合分子,并且将另一种细胞工程化以表达结合和/或靶向另外或第二抗原的结合分子。在一些实施方案中,细胞可以各自表达多特异性结合分子,例如多特异性重组受体,其中靶抗原中的一种或多种是CCT5。在一些此类实施方案中,所述多种细胞可以一起或单独给予。在一些实施方案中,所述多种细胞中的一些与其他细胞同时或并行地给予,例如与所述多种细胞中的另一种工程化细胞在同一天和/或以任何顺序依次或间歇地给予。例如,在一些实施方案中,将表达CCT5结合分子(例如CAR)的工程化细胞与表达结合不同靶抗原或CCT5上的不同表位的结合分子的另一种工程化细胞同时或以任何顺序依次给予。在一些实施方案中,所述多种细胞可以在同一组合物中或在不同组合物中。细胞的示例性组合物包括以下章节II中所描述的组合物。
II.药物组合物
还提供了包含CCT5结合分子(例如抗体)、免疫缀合物、重组受体和工程化细胞的组合物,包括药物组合物和配制品。
提供了药物配制品,其包含CCT5结合分子(例如抗体)、免疫缀合物、重组受体(例如嵌合抗原受体)、表达所述分子(例如重组受体)的工程化细胞、表达所述分子(例如重组受体)的多种工程化细胞和/或用于组合治疗或疗法的另外的药剂。药物组合物和配制品通常包含一种或多种任选的药学上可接受的载体或赋形剂。在一些实施方案中,所述组合物包含至少一种另外的治疗剂。
术语“药物配制品”是指这样的制剂,其处于使得其中所含活性成分的生物活性有效的形式,并且不含对给予配制品的受试者具有不可接受的毒性的另外的组分。
“药学上可接受的载体”是指药物配制品中除活性成分之外对受试者无毒的成分。药学上可接受的载体包括但不限于缓冲液、赋形剂、稳定剂或防腐剂。
在一些方面中,载体的选择部分地由特定细胞、结合分子和/或抗体和/或由给予方法决定。因此,存在多种合适的配制品。例如,药物组合物可以含有防腐剂。合适的防腐剂可以包括例如对羟基苯甲酸甲酯、对羟基苯甲酸丙酯、苯甲酸钠和苯扎氯铵。在一些方面,使用两种或更多种防腐剂的混合物。防腐剂或其混合物通常以按总组合物的重量计约0.0001%至约2%的量存在。载体描述于例如Remington’s Pharmaceutical Sciences第16版,Osol,A.编辑(1980)。药学上可接受的载体在所用的剂量和浓度下通常对接受者无毒,并且包括但不限于:缓冲液,如磷酸盐、柠檬酸盐和其他有机酸;抗氧化剂,包括抗坏血酸和甲硫氨酸;防腐剂(如十八烷基二甲基苄基氯化铵;六甲氯铵;苯扎氯铵;苄索氯铵;苯酚、丁醇或苄醇;烷基对羟基苯甲酸酯,如对羟基苯甲酸甲酯或对羟基苯甲酸丙酯;儿茶酚;间苯二酚;环己醇;3-戊醇;和间甲酚);低分子量(少于约10个残基)多肽;蛋白质,如血清白蛋白、明胶或免疫球蛋白;亲水性聚合物,如聚乙烯吡咯烷酮;氨基酸,如甘氨酸、谷氨酰胺、天冬酰胺、组氨酸、精氨酸或赖氨酸;单糖、二糖和其他碳水化合物,包括葡萄糖、甘露糖或糊精;螯合剂,如EDTA;糖类,如蔗糖、甘露醇、海藻糖或山梨糖醇;成盐抗衡离子,如钠;金属络合物(例如锌-蛋白质络合物);和/或非离子表面活性剂,如聚乙二醇(PEG)。
在一些方面,在所述组合物中包含缓冲剂。合适的缓冲剂包括例如柠檬酸、柠檬酸钠、磷酸、磷酸钾以及各种其他酸和盐。在一些方面,使用两种或更多种缓冲剂的混合物。所述缓冲剂或其混合物通常以按总组合物的重量计约0.001%至约4%的量存在。用于制备可给予的药物组合物的方法是已知的。示例性方法更详细地描述于例如Remington:TheScience and Practice of Pharmacy,Lippincott Williams&Wilkins;第21版(2005年5月1日)中。
本文所述的抗体配制品可以包括冻干配制品和水性溶液。
配制品或组合物还可以含有可用于用结合分子或细胞治疗的特定适应症、疾病或病症的多于一种的活性成分,优选地具有与结合分子或细胞互补的活性的那些,其中各活性不会相互产生不利影响。此类活性成分以有效用于既定目的的量合适地组合存在。因此,在一些实施方案中,药物组合物还包含其他药物活性剂或药物如化学治疗剂,例如天冬酰胺酶、白消安、卡铂、顺铂、道诺霉素、多柔比星、氟尿嘧啶、吉西他滨、羟基脲、甲氨蝶呤、紫杉醇、利妥昔单抗、长春碱、长春新碱等。在一些实施方案中,所述细胞或抗体以盐(例如药学上可接受的盐)的形式给予。合适的药学上可接受的酸加成盐包括源自以下的那些:无机酸,如盐酸、氢溴酸、磷酸、偏磷酸,硝酸和硫酸;以及有机酸,如酒石酸、乙酸、柠檬酸、苹果酸、乳酸、富马酸、苯甲酸、乙醇酸、葡萄糖酸、琥珀酸和芳基磺酸,例如对甲苯磺酸。
可以将活性成分包埋在微胶囊、胶体药物递送系统(例如,脂质体、白蛋白微球、微乳液、纳米颗粒和纳米胶囊)或粗乳液中。在某些实施方案中,将药物组合物配制为包合物(如环糊精包合物)或配制成脂质体。脂质体可以用于将宿主细胞(例如,T细胞或NK细胞)靶向特定组织。许多方法可用于制备脂质体,例如在例如以下参考文献中所述的那些方法:Szoka等人,Ann.Rev.Biophys.Bioeng.,9:467(1980);以及美国专利4,235,871、4,501,728、4,837,028和5,019,369。
在一些方面,药物组合物可以利用定时释放、延迟释放和持续释放递送系统,使得所述组合物的递送发生在待治疗部位的致敏之前并且有足够的时间引起致敏。许多类型的释放递送系统是可用的且已知的。此类系统可以避免重复给予所述组合物,从而增加对受试者和医师的便利性。
在一些实施方案中,药物组合物含有有效治疗或预防疾病或病症的量(如治疗有效量或预防有效量)的结合分子和/或细胞。在一些实施方案中,通过定期评估所治疗的受试者来监测治疗或预防功效。对于数天或更长时间的重复给予,根据病症,重复所述治疗直至出现疾病症状的所需抑制为止。然而,其他剂量方案可能有用并且可以被确定。所需剂量可以通过单次推注给予组合物、通过多次推注给予组合物、或通过连续输注给予组合物来递送。
在某些实施方案中,在含有结合分子的基因工程化细胞的情境下,向受试者给予以下范围的细胞:约一百万至约1000亿个细胞(例如100万至约500亿个细胞(例如,约500万个细胞、约2500万个细胞、约5亿个细胞、约10亿个细胞、约50亿个细胞、约200亿个细胞、约300亿个细胞、约400亿个细胞或由任两个前述值限定的范围),如约1000万至约1000亿个细胞(例如,约2000万个细胞、约3000万个细胞、约4000万个细胞、约6000万个细胞、约7000万个细胞、约8000万个细胞、约9000万个细胞、约100亿个细胞、约250亿个细胞、约500亿个细胞、约750亿个细胞、约900亿个细胞或由任两个前述值限定的范围),并且在一些情况下约1亿个细胞至约500亿个细胞(例如,约1.2亿个细胞、约2.5亿个细胞、约3.5亿个细胞、约4.5亿个细胞、约6.5亿个细胞、约8亿个细胞、约9亿个细胞、约30亿个细胞、约300亿个细胞、约450亿个细胞)或在这些范围之间的任何值和/或每千克受试者体重的这种数量的细胞。
可以使用标准给予技术、配制品和/或装置来给予细胞。提供用于储存和给予组合物的配制品和装置,如注射器和小瓶。细胞的给予可以是自体的或异源的。例如,免疫反应性细胞或祖细胞可以从一名受试者获得,并给予至同一受试者或不同的相容受试者。外周血衍生的免疫应答细胞或其后代(例如,体内、离体或体外衍生的)可以通过局部注射给予,包括导管给予、全身注射、局部注射、静脉内注射或肠胃外给予。在给予治疗组合物(例如,含有经基因修饰的免疫应答细胞的药物组合物)时,通常将其配制成单位剂量可注射形式(溶液、悬浮液、乳液)。
配制品包括用于口服、静脉内、腹膜内、皮下、经肺、透皮、肌内、鼻内、经颊、舌下或栓剂给予的那些。在一些实施方案中,肠胃外地给予细胞群。如本文所用,术语“肠胃外”包括静脉内、肌内、皮下、直肠、阴道、颅内、胸腔内和腹膜内给予。在一些实施方案中,通过静脉内、腹膜内或皮下注射使用外周全身递送向受试者给予细胞群。
在一些实施方案中,组合物作为无菌液体制剂(例如,等渗水溶液、悬浮液、乳液、分散体或粘性组合物,其在一些方面可以缓冲至所选pH)提供。液体制剂通常比凝胶、其他粘性组合物和固体组合物更容易制备。另外地,液体组合物稍微更便于给予,尤其是通过注射给予。另一方面,粘性组合物可以配制在适当的粘度范围内,以提供与特定组织的更长的接触时间段。液体或粘性组合物可以包含载体,所述载体可以是溶剂或分散介质,所述溶剂或分散介质含有例如水、盐水、磷酸盐缓冲盐水、多元醇(例如,甘油、丙二醇、液体聚乙二醇)及其合适的混合物。
无菌可注射溶液可以通过将结合分子掺入溶剂中来制备,如与合适的载体、稀释剂或赋形剂(如无菌水、生理盐水、葡萄糖、右旋糖等)掺合。组合物也可以是冻干的。组合物可以含有辅助物质,如润湿剂、分散剂或乳化剂(例如,甲基纤维素)、pH缓冲剂、胶凝或粘度增强添加剂、防腐剂、调味剂、着色剂等,这取决于给予途径和所需的制剂。在一些方面,可以查阅标准文本来制备合适的制剂。
可以添加各种增强所述组合物的稳定性和无菌性的添加剂,包括抗微生物防腐剂、抗氧化剂、螯合剂和缓冲液。可以通过各种抗细菌剂和抗真菌剂(例如,对羟基苯甲酸酯、氯丁醇、苯酚、抗坏血酸等)来确保防止微生物的作用。可以通过使用延迟吸收的药剂(例如,单硬脂酸铝和明胶)来实现可注射药物形式的延长吸收。
可以制备持续释放制剂。持续释放制剂的合适例子包括含有抗体的固体疏水聚合物的半透性基质,所述基质呈成型制品(例如薄膜)或微胶囊的形式。
用于体内给予的配制品通常是无菌的。可以例如通过经无菌滤膜过滤容易地实现无菌性。
还提供用于组合疗法的药物组合物。可以制备本文所述的用于组合疗法的任何另外的药剂(如章节III.B中所述的药剂),并将其与本文所述的CCT5结合分子(例如抗体)、免疫缀合物、重组受体(例如嵌合抗原受体)和/或表达所述分子(例如重组受体)的工程化细胞一起作为一种或多种药物组合物来给予。可以将组合疗法在一种或多种药物组合物中给予,例如,其中结合分子、重组受体和/或细胞与另外的药剂在同一药物组合物中或在单独的药物组合物中。例如,在一些实施方案中,另外的药剂是另外的工程化细胞(例如被工程化以表达靶向不同抗原或CCT5上的不同表位的不同重组受体的细胞)并在同一组合物或在单独的组合物中式给予。在一些实施方案中,根据特定的结合分子、重组受体、细胞(例如工程化细胞)和/或另外的药剂、以及特定的剂量方案和/或递送方法,将每种药物组合物配制成合适的配制品。
III.方法和用途
还提供了使用CCT5结合分子(例如抗体)、免疫缀合物、重组受体、工程化细胞及其药物组合物和配制品的方法,以及CCT5结合分子、免疫缀合物、重组受体、工程化细胞及其药物组合物和配制品如在治疗其中表达CCT5的疾病、病症和障碍中、和/或在检测、诊断和预后方法中的用途。还提供了组合疗法和/或治疗的方法。
A.治疗性和预防性方法和用途
还提供了CCT5结合分子(包括抗CCT5抗体(例如抗体片段)和含有所述CCT5结合分子的蛋白质如重组受体(例如CAR))、表达重组受体(例如CAR)的工程化细胞、表达受体的多种工程化细胞和/或包含上述各项的组合物的给予方法和用途(如治疗性和预防性用途)。此类方法和用途包括例如涉及向受试者给予分子(例如,CCT5结合分子、缀合物和重组受体)、细胞(例如,工程化细胞)或含有所述分子、所述细胞的组合物的治疗方法和用途,所述受试者患有与CCT5相关的疾病、病症或障碍,如与CCT5表达相关和/或其中细胞或组织表达(例如特异性表达)CCT5的疾病、病症或障碍。在一些实施方案中,以实现所述疾病或障碍的治疗的有效量给予所述分子、细胞和/或组合物。本文提供了结合分子(例如抗CCT5抗体或其抗原结合片段)、重组受体(例如CAR)和细胞(例如工程化细胞)在此类方法和治疗中以及在制备药物以便进行此类治疗方法中的用途。在一些实施方案中,通过向患有、已经患有或怀疑患有疾病或病症的受试者给予结合分子或细胞或包含所述结合分子或所述细胞的组合物来进行所述方法。在一些实施方案中,所述方法从而治疗受试者的疾病或病症或障碍。
如本文所用,“治疗”(“treatment”)(及其语法变体如“治疗”(“treat”或“treating”))是指疾病或病症或障碍、或者与之相关的症状、不良影响或结果、或表型的完全或部分改善或减轻。所希望的治疗效果包括但不限于预防疾病的发生或复发、缓和症状、减少疾病的任何直接或间接病理后果、预防转移、降低疾病进展的速度、改善或减缓疾病状态以及缓解或改善预后。所述术语并不暗示完全治愈疾病或完全消除任何症状或对所有症状或结果的一种或多种影响。
如本文所用,“延迟疾病的发生”意指推迟、阻碍、减缓、延缓、稳定、抑制和/或延期疾病(如癌症)的发生。这种延迟可以具有不同的时间长度,这取决于病史和/或所治疗的受试者。已知足够或显著的延迟实际上可以涵盖预防,因为个体不会患上疾病。例如,可能延迟晚期癌症,如转移的发展。
如本文所用,“预防”包括提供关于受试者的疾病的发生或复发的预防,所述受试者可能易患上所述疾病但尚未被诊断患有所述疾病。在一些实施方案中,将所提供的分子和组合物用于延迟疾病的发生或减缓疾病的进展。
如本文所用,“抑制”功能或活性是当与除了目的条件或参数以外其他都相同的条件相比时,或者可替代地与另一种条件相比时,降低功能或活性。例如,与不存在抗体或组合物或细胞的情况下的肿瘤生长速率相比,抑制肿瘤生长的抗体或组合物或细胞降低肿瘤的生长速率。
在给予的情境下,药剂(例如,药物配制品、结合分子、抗体、细胞或组合物)的“有效量”是指在必要的剂量/量下和必要的时间段内有效实现所需结果(如治疗或预防结果)的量。
药剂(例如药物配制品、结合分子、抗体、细胞或组合物)的“治疗有效量”是指在必要的剂量下和必要的时间段内有效实现所需治疗结果(如针对治疗疾病、病症或障碍)和/或治疗的药代动力学或药效动力学作用的量。治疗有效量可以根据诸如以下的因素而变化:疾病状态、受试者的年龄、性别和体重、和所给予的细胞群。在一些实施方案中,所提供的方法涉及以有效量(例如,治疗有效量)给予分子、抗体、细胞和/或组合物。
“预防有效量”是指在所需剂量下和所需时间段内有效实现所需预防结果的量。通常但不一定,因为预防剂量是在疾病之前或在疾病较早期用于受试者,所以预防有效量将小于治疗有效量。
如本文所用,“受试者”或“个体”是哺乳动物。在一些实施方案中,“哺乳动物”包括人、非人灵长类动物、家畜和农场动物,以及动物园、运动或宠物动物,如狗、马、兔、牛、猪、仓鼠、沙鼠、小鼠、雪貂、大鼠、猫、猴等。在一些实施方案中,受试者是人。
在某些疾病和病症中,CCT5在恶性细胞和癌症上表达。在一些实施方案中,癌症(例如,表达CCT5的癌症)是实体瘤。在一些实施方案中,癌症(例如,表达CCT5的癌症)是弥漫型或循环性癌症或肿瘤。在一些实施方案中,癌症是肾上腺癌、膀胱癌、脑癌、乳腺癌、宫颈癌、结肠癌、结直肠癌、上皮鳞状细胞癌、头颈癌、白血病、肝癌、肺癌、淋巴瘤、黑色素瘤、骨髓瘤(例如、多发性骨髓瘤)、神经母细胞瘤、卵巢癌、胰腺癌、前列腺癌、肾癌、肾细胞癌、皮肤癌、胃癌、睾丸癌、甲状腺癌、尿路上皮癌、子宫癌等。
在一些实施方案中,癌症是上皮细胞癌,如起源于源自内胚层、中胚层或外胚层的细胞的上皮恶性肿瘤。在一些实施方案中,上皮恶性肿瘤是鳞状细胞癌(皮肤)、基底细胞癌、胃癌(例如,肠型胃癌或弥漫型(粘液样)胃癌)、腺癌、腺鳞癌、间变性癌、移行细胞癌、大细胞癌、小细胞癌、肝细胞癌、肾细胞癌、子宫内膜癌、浸润性乳腺癌、或癌转移(例如,淋巴结)。在一些实施方案中,上皮细胞癌是结肠癌、乳腺癌、卵巢癌、前列腺癌、胰腺癌、膀胱癌或肺癌。
在一些实施方案中,与CCT5相关的疾病或障碍是自身免疫性疾病或障碍。自身免疫性疾病或障碍包括但不限于系统性红斑狼疮(SLE)、狼疮性肾炎、炎性肠病、类风湿性关节炎(例如青少年类风湿性关节炎)、ANCA相关性血管炎、特发性血小板减少性紫癜(ITP)、血栓性血小板减少性紫癜(TTP)、自身免疫性血小板减少症、查加斯病(Chagas’disease)、格雷夫斯病(Grave’s disease)、韦格纳氏肉芽肿病(Wegener’s granulomatosis)、结节性多动脉炎、舍格伦综合征(Sjogren’s syndrome)、寻常型天疱疮、硬皮病、多发性硬化症、牛皮癣、IgA肾病、IgM多发性神经病变、血管炎、糖尿病、雷诺综合征(Reynaud’s syndrome)、抗磷脂综合征、古德帕斯丘病(Goodpasture’s disease)、川崎病、自身免疫性溶血性贫血、重症肌无力或进行性肾小球肾炎。
在一些实施方案中,所述方法可以鉴定患有、怀疑患有或有风险患上与CCT5相关的疾病或障碍的受试者。因此,提供了用于鉴定患有与CCT5表达升高相关的疾病或障碍的受试者并选择他们来用所提供的CCT5结合分子(包括任何抗CCT5抗体(例如抗体片段)和含有所述CCT5结合分子的蛋白质(如重组受体(例如CAR))和/或表达重组受体的工程化细胞进行治疗的方法。
例如,可以对受试者筛选与CCT5表达升高相关的疾病或障碍(如表达CCT5的癌症)的存在。在一些实施方案中,所述方法包括筛选或检测CCT5相关疾病(例如肿瘤)的存在。因此,在一些方面,可以从怀疑患有与CCT5表达升高相关的疾病或障碍的患者获得样品,并对其测定CCT5的表达水平。在一些方面,可以选择测试为对于CCT5相关的疾病或障碍呈阳性的受试者进行通过本发明方法的治疗,并且可以向其给予治疗有效量的如本文所述的CCT5结合分子(例如抗CCT5抗体或其抗原结合片段)、包含CCT5结合分子的重组受体(例如CAR)、含有重组受体的细胞或其药物组合物。在一些实施方案中,可以将所述方法用于监测表达CCT5的组织(例如肿瘤)随时间推移(例如在通过所述方法治疗之前、期间或之后)的大小或密度。
在一些实施方案中,例如在用另一种CCT5特异性抗体和/或表达靶向CCT5的嵌合受体的细胞和/或其他疗法(包括化学疗法、辐射和/或造血干细胞移植(HSCT)(例如同种异体HSCT))治疗之后,受试者患有顽固性或复发性疾病。在一些实施方案中,尽管受试者已经对另一种CCT5靶向疗法产生抗性,但给予仍有效地治疗所述受试者。在一些实施方案中,受试者尚未复发,但是被确定为具有复发风险(例如具有高复发风险),因此预防性地给予化合物或组合物,例如以降低复发的可能性或防止复发。
在一些实施方案中,治疗不诱导受试者对疗法的免疫应答,和/或诱导这样的应答没有达到阻止疾病或病症的有效治疗的程度。在一些方面,免疫原性和/或移植物抗宿主应答的程度小于用不同但可比较的治疗所观察到的程度。例如,与包含结合与所提供抗体(如小鼠或猴或兔或人源化抗体)相似的(例如重叠的)表位和/或竞争结合CCT5的不同抗体的CAR相比,在使用表达包含所提供的抗CCT5抗体的CAR的细胞的过继细胞疗法的情况下,在一些实施方案中免疫原性的程度降低。
在一些实施方案中,所述方法包括过继细胞疗法,由此将表达包含CCT5结合分子的所提供的重组受体(例如,包含抗CCT5抗体或其抗原结合片段的CAR)的基因工程化细胞给予至受试者。这种给予能以CCT5靶向的方式促进细胞激活(例如,T细胞激活),使得疾病或障碍的细胞被靶向进行破坏。
因此,所提供的方法和用途包括用于过继细胞疗法的方法和用途。在一些实施方案中,所述方法包括将细胞、多种细胞、含有所述细胞或所述多种细胞的组合物给予至受试者、组织或细胞,例如患有、有风险患上或怀疑患有疾病、病症或障碍的受试者、组织或细胞。在一些实施方案中,将细胞、群体和组合物给予至患有将要例如通过过继细胞疗法(如过继T细胞疗法)治疗的特定疾病或病症的受试者。在一些实施方案中,将细胞或组合物给予至受试者,例如患有或有风险患上疾病或病症的受试者。在一些方面,所述方法由此治疗疾病或病症(例如,改善其一种或多种症状),例如通过减轻表达CCT5的癌症中的肿瘤负荷来治疗。
用于过继细胞疗法的细胞的给予方法是已知的,并且可以与所提供的方法和组合物一起使用。例如,过继T细胞治疗方法描述于例如授予Gruenberg等人的美国专利申请公开号2003/0170238;授予Rosenberg的美国专利号4,690,915;Rosenberg(2011)Nat RevClin Oncol.8(10):577-85)。参见例如Themeli等人(2013)Nat Biotechnol.31(10):928-933;Tsukahara等人(2013)Biochem Biophys Res Commun 438(1):84-9;Davila等人(2013)PLoS ONE 8(4):e61338。
在一些实施方案中,细胞疗法(例如过继细胞疗法,例如过继T细胞疗法)通过自体转移进行,其中从接受所述细胞疗法的受试者或从源自这种受试者的样品中分离和/或以其他方式制备细胞。因此,在一些方面,细胞源自需要治疗的受试者(例如患者),并且在分离和加工后将所述细胞给予至同一受试者。
在一些实施方案中,细胞疗法(例如过继细胞疗法,例如过继T细胞疗法)通过同种异体转移进行,其中从除了将要接受或最终接受所述细胞疗法的受试者以外的受试者(例如第一受试者)分离和/或以其他方式制备细胞。在此类实施方案中,然后将细胞给予至相同物种的不同受试者,例如第二受试者。在一些实施方案中,第一和第二受试者在遗传上是相同的。在一些实施方案中,第一和第二受试者在遗传上是相似的。在一些实施方案中,第二受试者与第一受试者表达相同的HLA类别或超类型。
在一些实施方案中,给予细胞、细胞群或组合物的受试者是灵长类动物,如人。在一些实施方案中,给予细胞、细胞群或组合物的受试者是非人灵长类动物。在一些实施方案中,非人灵长类动物是猴(例如食蟹猴)或猿。受试者可以是雄性或雌性,并且可以是任何合适的年龄,包括婴儿、幼年、青春期、成年和老年受试者。在一些实施方案中,受试者是非灵长类哺乳动物,如啮齿动物(例如小鼠、大鼠等)。在一些例子中,患者或受试者是用于疾病、过继细胞疗法和/或用于评估毒性结果(如细胞因子释放综合征(CRS))的经验证的动物模型。
在一些实施方案中,肿瘤细胞的RNA表达谱可用于预测抗CCT5 CAR表达T细胞对肿瘤细胞的应答。在一些方面,可以挖掘RNA-seq数据(例如定量癌细胞系百科全书(CCLE)RNA-seq数据)中的可预测抗CCT5 CAR T细胞激活的上调转录物。例如,包括针对已知能够激活抗CCT5 CAR T细胞的细胞系和已知不能激活抗CCT5 CAR T细胞的细胞系的RNA-seq数据库可用于鉴定与预测的抗CCT5 CAR T细胞激活相关联的因子。在一些实施方案中,基于RNA-seq数据,CCT5 RNA表达可能与抗CCT5 CAR T细胞激活不相关联。在一些实施方案中,T复合物蛋白1(TCP1),TCP1复合物的成员(CCT)的表达可以与预测的抗CCT5 CAR T细胞激活相关联。在一些方面,通过myc途径上调了CCT5和TCP复合物的其他成员,并且TCP复合物可能与myc依赖性癌症相关。在一些实施方案中,与抗CCT5 CAR T细胞激活相关的途径或基因包括MYC、雌激素受体、INSR、miR-124-3p、ESRRA、miR-199a-5p、MYCN、mir-210和TFAP2C途径。在一些实施方案中,这些途径可用于预测包括乳腺癌、卵巢癌和肺癌细胞系的肿瘤细胞系中的抗CCT5 CAR激活。
CCT5结合分子(如抗体、含有所述抗体的重组受体(例如CAR))和表达所述CCT5结合分子的细胞可以通过任何合适的手段给予,例如通过注射,例如静脉内或皮下注射、眼内注射、眼周注射、视网膜下注射、玻璃体内注射、经中隔注射、巩膜下注射、脉络膜内注射、前房内注射、结膜下注射(subconjunctival injection,subconjunctival injection)、眼球筋膜下(sub-Tenon)注射、眼球后注射、眼球周注射或后近巩膜(posterior juxtascleral)递送。在一些实施方案中,它们通过肠胃外、肺内和鼻内给予以及(如果需要用于局部治疗的话)病灶内给予。肠胃外输注包括肌内、静脉内、动脉内、腹膜内、颅内、胸腔内或皮下给予。给药和给予可以部分取决于给予是短暂的还是长期的。各种给药时间表包括但不限于在不同时间点的单次或多次给予、推注给予和脉冲输注。
为了预防或治疗疾病,结合分子、重组受体或细胞的适当剂量可以取决于待治疗的疾病类型、结合分子或重组受体的类型、疾病的严重程度和病程、给予结合分子或重组受体是出于预防目的还是治疗目的、先前的疗法、患者的临床病史和对结合分子、重组受体或细胞的反应以及主治医师的决断。在一些实施方案中,组合物和分子和细胞合适地一次或在一系列治疗中给予至患者。
根据疾病的类型和严重程度,结合分子(例如抗CCT5抗体或其抗原结合片段)或重组受体的剂量可以包括约1μg/kg至约15mg/kg(例如0.1mg/kg-10mg/kg)、约1μg/kg至约100mg/kg、约0.05mg/kg至约10mg/kg、约0.5mg/kg、约2.0mg/kg、约4.0mg/kg或约10mg/kg。可以间歇地(例如每周一次或每三周一次)给予多个剂量。可以给予初始较高负荷剂量,接着给予一个或多个较低剂量。
在某些实施方案中,在含有结合分子或重组受体的基因工程化细胞的情境下,向受试者给予以下范围的细胞:约一百万至约1000亿个细胞和/或每千克体重的该细胞量,例如100万至约500亿个细胞(例如,约500万个细胞、约2500万个细胞、约5亿个细胞、约10亿个细胞、约50亿个细胞、约200亿个细胞、约300亿个细胞、约400亿个细胞或由任两个前述值限定的范围),如约1000万至约1000亿个细胞(例如,约2000万个细胞、约3000万个细胞、约4000万个细胞、约6000万个细胞、约7000万个细胞、约8000万个细胞、约9000万个细胞、约100亿个细胞、约250亿个细胞、约500亿个细胞、约750亿个细胞、约900亿个细胞或由任两个前述值限定的范围),并且在一些情况下约1亿个细胞至约500亿个细胞(例如,约1.2亿个细胞、约2.5亿个细胞、约3.5亿个细胞、约4.5亿个细胞、约6.5亿个细胞、约8亿个细胞、约9亿个细胞、约30亿个细胞、约300亿个细胞、约450亿个细胞)或在这些范围和/或每公斤体重的这些范围之间的任何值。同样,剂量可以根据疾病或障碍和/或患者和/或其他治疗特定的属性而变化。
在一些实施方案中,例如,在所述受试者是人的情况下,所述剂量包括少于约1x10
在一些方面,所述剂量的大小基于一个或多个标准来确定,如受试者对先前治疗(例如化学疗法)的反应、受试者的疾病负荷(如肿瘤负担、体积、尺寸或程度)、转移的程度或类型、分期和/或受试者发生毒性结果(例如,CRS、巨噬细胞活化综合征、肿瘤溶解综合征、神经毒性和/或针对所给予的细胞和/或重组受体的宿主免疫应答)的可能性或发生率。
在一些方面,剂量的大小由受试者的疾病或病症的负荷决定。例如,在一些方面,在剂量中给予的细胞数量是基于就在所述细胞剂量开始给予之前在受试者中存在的肿瘤负荷来确定。在一些实施方案中,第一剂量和/或随后剂量的大小与疾病负荷呈逆相关。在一些方面,如在疾病负荷大的情境下,向受试者给予少量的细胞。在其他实施方案中,如在疾病负荷较低的情境下,向受试者给予较大量的细胞。
在一些实施方案中,将细胞、结合分子或重组受体作为组合治疗的一部分与另一种治疗性干预(如另一种抗体或工程化细胞或受体或药剂,如细胞毒性剂或治疗剂,如章节I.E或III.B中所述的任何一种)如同时或以任何顺序依次给予。
在一些实施方案中,细胞、结合分子和/或重组受体是与一种或多种另外的治疗剂或结合另一种治疗性干预同时或以任何顺序依次共给予。在一些情境下,细胞是与另一种疗法共给予,其时间足够接近,使得细胞群增强一种或多种另外的治疗剂的作用,或反之亦然。在一些实施方案中,在所述一种或多种另外的治疗剂之前给予细胞、结合分子和/或重组受体。在一些实施方案中,在所述一种或多种另外的治疗剂之后给予细胞、结合分子和/或重组受体。
在将细胞给予至哺乳动物(例如人)后,工程化细胞群和/或抗体的生物活性在一些方面通过许多已知方法中的任何一种来测量。待评估的参数包括工程化或天然T细胞或其他免疫细胞与抗原的特异性结合,其在体内例如通过成像进行评估,或离体例如通过ELISA或流式细胞术进行评估。在某些实施方案中,工程化细胞破坏靶细胞的能力可以使用任何合适的方法来测量,所述方法例如描述于例如以下文献中的细胞毒性测定:Kochenderfer等人,J.Immunotherapy,32(7):689-702(2009),和Herman等人J.Immunological Methods,285(1):25-40(2004)。在某些实施方案中,还可以通过测定某些细胞因子(如CD 107a、IFNγ、IL-2和TNF)的表达和/或分泌来测量所述细胞的生物活性。在一些方面,通过评估临床结果(如肿瘤负荷或负担的减少)来测量生物活性。
在某些实施方案中,工程化的细胞以任何数量的方式进行修饰,使得其治疗或预防功效增加。例如,在一些实施方案中,将由群体表达的工程化CAR或TCR直接或通过接头间接与靶向部分缀合。将化合物(例如,CAR或TCR)与靶向部分缀合的实践在本领域是已知的。参见例如Wadwa等人,J.Drug Targeting,3(2):111(1995)和美国专利5,087,616。
B.组合疗法
还提供了组合疗法的方法,所述组合疗法包括CCT5结合分子(包括抗CCT5抗体(例如抗体片段)和含有所述CCT5结合分子的蛋白质如重组受体(例如CAR))、表达重组受体(例如CAR)的工程化细胞、表达受体的多种工程化细胞和/或包含上述各项的组合物的给予方法和用途(如治疗性和预防性用途)。
在一些实施方案中,将本文所述的CCT5结合分子(例如抗体)、免疫缀合物、重组受体(例如嵌合抗原受体)和/或表达所述分子(例如重组受体)的工程化细胞作为组合治疗或组合疗法的一部分例如与一种或多种另外的治疗性干预同时、以任何顺序依次或间歇地给予。在一些实施方案中,所述一种或多种另外的治疗性干预包括例如抗体、工程化细胞、受体和/或药剂(如表达重组受体的细胞和/或细胞毒性剂或治疗剂(例如化学治疗剂))。在一些实施方案中,组合疗法包括给予一种或多种另外的药剂、疗法和/或治疗,例如本文所述的另外的药剂、疗法和/或治疗中的任何一种。在一些实施方案中,组合疗法包括给予用于治疗或疗法的一种或多种另外的药剂,如免疫调节剂、免疫检查点抑制剂、腺苷途径或腺苷受体拮抗剂或激动剂和激酶抑制剂。在一些实施方案中,组合治疗或组合疗法包括另外的治疗,如手术治疗、移植和/或放射疗法。还提供了组合治疗或组合疗法的方法,所述组合治疗或组合疗法包括给予本文所述的结合分子(例如CCT5结合分子)、重组受体、细胞和/或组合物、以及一种或多种另外的治疗性干预。
在一些实施方案中,用于组合治疗或组合疗法的另外的药剂增强、加强和/或促进结合分子、重组受体、细胞和/或组合物的治疗作用的功效和/或安全性。在一些实施方案中,另外的药剂增强或改善所给予的细胞(例如表达结合分子或重组受体的细胞)的功效、存活或持久性。在一些实施方案中,另外的药剂选自蛋白磷酸酶抑制剂、激酶抑制剂、细胞因子、免疫调节剂或降低调节性T(Treg)细胞的水平或活性的药剂。在一些实施方案中,另外的药剂通过减少或改善所给予的结合分子、重组受体、细胞和/或组合物的不良反应而增强安全性。在一些实施方案中,另外的药剂可以治疗同一疾病、病症或共病(comorbidity)。在一些实施方案中,另外的药剂可以改善、减少或消除与结合分子、重组受体、细胞和/或组合物(例如CAR表达细胞)的给予相关的一种或多种毒性、不良反应或副作用。
在一些实施方案中,所述另外的疗法、治疗或药剂包括化学疗法、放射疗法、手术、移植、过继细胞疗法、抗体、细胞毒性剂、化学治疗剂、细胞因子、生长抑制剂、抗激素剂、激酶抑制剂、抗血管生成剂、保心药、免疫刺激剂、免疫抑制剂、免疫检查点抑制剂、抗生素、血管发生抑制剂、代谢调节剂或其他治疗剂或其任何组合。在一些实施方案中,所述另外的药剂是蛋白质、肽、核酸、小分子药剂、细胞、毒素、脂质、碳水化合物或其组合,或任何其他类型的治疗剂,例如辐射。在一些实施方案中,另外的疗法、药剂或治疗包括手术、化学疗法、放射疗法、移植、给予表达重组受体(例如CAR)的细胞、激酶抑制剂、免疫检查点抑制剂、mTOR途径抑制剂、免疫抑制剂、免疫调节剂、抗体、免疫清除剂、抗体和/或其抗原结合片段、抗体缀合物、其他抗体疗法、细胞毒素、类固醇、细胞因子、肽疫苗、激素疗法、抗代谢物、代谢调节剂、抑制钙依赖性磷酸酶钙调磷酸酶或p70S6激酶FK506或抑制p70S6激酶的药物、烷化剂、蒽环类、长春花生物碱、蛋白酶体抑制剂、GITR激动剂、蛋白质酪氨酸磷酸酶抑制剂、蛋白质激酶抑制剂、溶瘤病毒和/或其他类型的免疫疗法。在一些实施方案中,另外的药剂或治疗是骨髓移植、使用化学治疗剂(如氟达拉滨)的T细胞清除疗法、外线束放射疗法(XRT)、环磷酰胺和/或抗体疗法。
在一些实施方案中,将细胞、结合分子(例如,CCT5结合分子)、缀合物、重组受体和/或组合物(例如CAR表达细胞)与其他结合分子,如抗体、缀合物、重组受体、和/或工程化细胞(例如其他CAR表达细胞)组合给予。在一些实施方案中,另外的药剂是另一CCT5结合分子,如抗CCT5抗体、缀合物、重组受体、和/或抗CCT5 CAR表达细胞。在一些实施方案中,另外的CCT5结合分子或含有CCT5结合分子的药剂结合与本文所提供的CCT5结合分子(例如抗体或CAR)不同或重叠的表位。
在一些实施方案中,所述另外的药剂是激酶抑制剂,例如,布鲁顿酪氨酸激酶(Btk)抑制剂,例如,依鲁替尼。在一些实施方案中,所述另外的药剂是腺苷途径或腺苷受体拮抗剂或激动剂。在一些实施方案中,所述另外的药剂是免疫调节剂,如沙利度胺或沙利度胺衍生物(例如,来那度胺)。在一些实施方案中,所述另外的疗法、药剂或治疗是细胞毒性剂或化学治疗剂、生物疗法(例如,抗体,例如,单克隆抗体,或细胞疗法)或抑制剂(例如,激酶抑制剂)。
在一些实施方案中,向受试者给予化学治疗剂(有时称为细胞毒性剂)以破坏病灶。在某些实施方案中,病灶是肿瘤。在特定实施方案中,病灶是癌性的。在特定实施方案中,化学治疗剂是已知对于治疗、预防或改善过度增殖性障碍(如癌症)有效的任何药剂。化学治疗剂包括但不限于小分子、合成药物、肽、多肽、蛋白质、核酸(例如,DNA和RNA多核苷酸,其包括但不限于编码生物活性蛋白质、多肽或肽的反义核苷酸序列、三螺旋和核苷酸序列)、抗体、合成或天然无机分子、模拟剂和合成或天然有机分子。在特定实施方案中,化学治疗药物包括烷化剂、蒽环类、细胞骨架破坏剂(紫杉烷类)、埃博霉素、组蛋白脱乙酰化酶抑制剂、拓扑异构酶抑制剂、拓扑异构酶II抑制剂、激酶抑制剂、核苷酸类似物和前体类似物、肽抗生素、基于铂的药剂以及长春花生物碱和衍生物。
在某些实施方案中,通过给予化学治疗剂破坏病灶以在体内调节基因工程化细胞。化学治疗剂可以包括但不限于阿巴瑞克、阿地白介素、阿仑单抗、阿利维A酸、别嘌呤醇、六甲蜜胺、氨磷汀、阿那曲唑、三氧化二砷、天冬酰胺酶、活性BCG、贝伐单抗、贝沙罗汀、博来霉素、硼替佐米、白消安、卡鲁睾酮、喜树碱、卡培他滨、卡铂、卡莫司汀、塞来昔布、西妥昔单抗、苯丁酸氮芥、西那卡塞、顺铂、克拉屈滨、环磷酰胺、阿糖胞苷、达卡巴嗪、更生霉素、阿法达贝泊汀、道诺霉素、地尼白介素、右雷佐生、多西紫杉醇、多柔比星、屈他雄酮、Elliott'sB溶液、表柔比星、阿法依泊汀、雌莫司汀、依托泊苷、依西美坦、非格司亭、氟尿嘧啶、氟达拉滨、氟尿嘧啶、氟维司群、吉西他滨、吉妥珠单抗奥佐米星、吉非替尼、戈舍瑞林、羟基脲、替伊莫单抗、伊达比星、异环磷酰胺、伊马替尼、干扰素α-2a、干扰素α-2b、伊立替康、来曲唑、甲酰四氢叶酸、左旋咪唑、洛莫司汀、氯硝胺(meclorethamine)、甲地孕酮、美法仑、巯嘌呤、美司钠、甲氨蝶呤、甲氧沙林、甲基泼尼松龙、丝裂霉素C、米托坦、米托蒽醌、诺龙、诺菲单抗、奥利美生、奥普瑞白介素、奥沙利铂、紫杉醇、帕米膦酸二钠、培加酶、培门冬酶、培非格司亭、培美曲塞、喷司他丁、哌泊溴烷、普卡霉素、聚苯丙生、卟菲尔钠、丙卡巴肼、奎纳克林、拉布立酶、利妥昔单抗、沙格司亭、链脲佐菌素、滑石、他莫昔芬、特罗凯、替莫唑胺、替尼泊苷、睾内酯、硫鸟嘌呤、噻替哌、拓扑替康、托瑞米芬、托西莫单抗、曲妥珠单抗、维A酸、尿嘧啶氮芥、戊柔比星、长春碱、长春新碱、长春瑞滨和唑来膦酸盐。
在一些实施方案中,示例性化学治疗剂包括蒽环类(例如多柔比星,如脂质体多柔比星);长春花生物碱(例如长春碱、长春新碱、长春地辛、长春瑞滨);烷化剂(例如环磷酰胺、达卡巴嗪、美法仑、异环磷酰胺、替莫唑胺);免疫细胞抗体(例如阿仑单抗、吉妥珠单抗、利妥昔单抗、托西莫单抗);抗代谢物(包括例如叶酸拮抗剂、嘧啶类似物、嘌呤类似物和腺苷脱氨酶抑制剂如氟达拉滨);TNFR糖皮质激素诱导的TNFR相关蛋白(GITR)激动剂;蛋白酶体抑制剂(例如阿克拉霉素A、胶霉毒素或硼替佐米);免疫调节剂,如沙利度胺或沙利度胺衍生物(例如来那度胺)。
在一些实施方案中,另外的疗法或治疗是细胞疗法,例如过继细胞疗法。在一些实施方案中,另外的疗法包括给予工程化细胞,例如另外的CAR表达细胞。在一些实施方案中,另外的工程化细胞是CAR表达细胞,所述CAR表达细胞表达与本文所提供的工程化细胞(例如抗CCT5 CAR表达细胞)相同或不同的重组受体。在一些实施方案中,在另外的工程化细胞上表达的重组受体(例如CAR)识别不同的抗原和/或表位。在一些实施方案中,在另外的工程化细胞上表达的重组受体(例如CAR)与本文所述的重组受体识别相同抗原(例如CCT5)的不同表位。在一些实施方案中,在另外的工程化细胞上表达的重组受体(例如CAR)识别不同的抗原,例如不同的肿瘤抗原或抗原的组合。例如,在一些实施方案中,在另外的工程化细胞上表达的重组受体(例如CAR)靶向表达早期谱系标记的癌细胞(例如癌干细胞),而其他CAR表达细胞靶向表达晚期谱系标记的癌细胞。在此类实施方案中,在给予(例如输注)本文所述的CAR表达细胞之前、与其并行或之后给予另外的工程化细胞。在一些实施方案中,另外的工程化细胞表达同种异体CAR。
在一些实施方案中,一种或多种CAR分子的构型包含一个初级细胞内信号传导结构域和两个或更多个(例如2、3、4或5或更多个)共刺激信号传导结构域。在一些实施方案中,所述一种或多种CAR分子可以具有相同或不同的初级细胞内信号传导结构域、相同或不同的共刺激信号传导结构域、或相同数量或不同数量的共刺激信号传导结构域。在一些实施方案中,所述一种或多种CAR分子可以被配置为分离的CAR,其中一种CAR分子包含抗原结合结构域和共刺激结构域(例如4-1BB),而另一种CAR分子包含抗原结合结构域和初级细胞内信号传导结构域(例如CD3ζ)。
在一些实施方案中,另外的药剂是多特异性结合分子和/或被工程化以表达本文所述的一种或多种结合分子的细胞和/或被工程化以表达靶向不同抗原的另外的结合分子(例如重组受体(例如CAR))的细胞中的任何一种。在一些实施方案中,另外的药剂包括本文(例如在章节I.E中)所述的细胞中的任何一种或多种细胞。在一些实施方案中,另外的药剂是被工程化以表达靶向不同表位和/或抗原(例如与疾病或病症相关的不同抗原)的重组受体(例如CAR)的细胞。
在一些实施方案中,另外的药剂是免疫调节剂。在一些实施方案中,组合疗法包括可以刺激、放大和/或以其他方式增强抗肿瘤免疫应答(例如,来自所给予工程化细胞的抗肿瘤免疫应答)的免疫调节剂,如通过抑制免疫抑制信号传导或增强免疫刺激信号传导。在一些实施方案中,免疫调节剂是肽、蛋白质或是小分子。在一些实施方案中,所述蛋白质可以是融合蛋白或重组蛋白。在一些实施方案中,所述免疫调节剂结合至免疫靶标,如在免疫细胞(如T细胞、B细胞或抗原呈递细胞)上表达的细胞表面受体。例如,在一些实施方案中,所述免疫调节剂是抗体或抗原结合抗体片段、融合蛋白、小分子或多肽。在一些实施方案中,所述结合分子、重组受体、细胞和/或组合物是与作为抗体或其抗原结合片段(如单克隆抗体)的另外的药剂组合给予。
在一些实施方案中,免疫调节剂阻断、抑制或抵消免疫检查点途径的组分。免疫系统具有参与维持自身耐受性和用于调节免疫应答的多个抑制途径。肿瘤可以使用某些免疫检查点途径作为免疫抗性的主要机制,特别是针对对肿瘤抗原具有特异性的T细胞(Pardoll(2012)Nature Reviews Cancer 12:252-264),例如工程化细胞,如CAR表达细胞。因为许多此类免疫检查点是通过配体-受体相互作用开始的,所以它们可以容易地被针对配体和/或其受体的抗体阻断。
因此,用阻断免疫检查点途径的拮抗性分子(如小分子、核酸抑制剂(例如RNAi)或抗体分子)的疗法正在成为针对癌症和其他疾病的免疫疗法的有前途的途径。与大多数抗癌剂相反,检查点抑制剂不一定直接靶向肿瘤细胞,而是靶向淋巴细胞受体或其配体,以增强免疫系统的内源性抗肿瘤活性。
如本文所用,术语“免疫检查点抑制剂”是指完全或部分降低、抑制、干扰或调节一种或多种检查点蛋白的分子。检查点蛋白调节T细胞激活或功能。这些蛋白质负责T细胞应答的共刺激或抑制性相互作用。免疫检查点蛋白调节并维持自身耐受性和生理免疫应答的持续时间和幅度。在一些实施方案中,可以向受试者给予另外的药剂,所述另外的药剂可以增强或加强针对疾病或病症(例如癌症,如本文所述的任何一种)的免疫应答,例如由本文所提供的结合分子(例如CCT5结合分子)、重组受体、细胞和/或组合物所产生的免疫应答。
免疫检查点抑制剂包括以统计学上显著的方式阻断或抑制免疫系统的抑制途径的任何药剂。此类抑制剂可以包括小分子抑制剂或者可以包括与免疫检查点受体、配体结合并阻断或抑制免疫检查点受体、配体和/或受体-配体相互作用的抗体或其抗原结合片段。在一些实施方案中,特定受体的调节、增强和/或刺激可以胜过免疫检查点途径组分。可以被靶向用于阻断、抑制、调节、增强和/或刺激的示例性免疫检查点分子包括但不限于PD-1(CD279)、PD-L1(CD274、B7-H1)、PDL2(CD273、B7-DC)、CTLA-4、LAG-3(CD223)、TIM-3、4-1BB(CD137)、4-1BBL(CD137L)、GITR(TNFRSF18、AITR)、CD40、OX40(CD134、TNFRSF4)、CXCR2、肿瘤相关抗原(TAA)、B7-H3、B7-H4、BTLA、HVEM、GAL9、B7H3、B7H4、VISTA、KIR、2B4(属于分子的CD2家族并且在所有NK、γδ和记忆CD8+(αβ)T细胞上表达)、CD160(也称为BY55)、CGEN-15049、CEACAM(例如,CEACAM-1、CEACAM-3和/或CEACAM-5)、TIGIT、LAIR1、CD160、2B4、CD80、CD86、B7-H3(CD276)、B7-H4(VTCN1)、HVEM(TNFRSF14或CD270)、KIR、A2aR、MHC I类、MHC II类、GAL9、腺苷和转化生长因子受体(TGFR;例如,TGFRβ)。免疫检查点抑制剂包括抗体或其抗原结合片段或其他结合蛋白,其与一种或多种任何所述分子结合并阻断或抑制和/或增强或刺激一种或多种任何所述分子的活性。
示例性免疫检查点抑制剂包括曲美目单抗(CTLA-4阻断抗体,也称为替西木单抗、CP-675,206)、抗OX40、PD-L1单克隆抗体(抗B7-H1;MEDI4736)、MK-3475(PD-1阻断剂)、纳武单抗(抗PD-1抗体)、CT-011(抗PD-1抗体)、BY55单克隆抗体、AMP224(抗PD-L1抗体)、BMS-936559(抗PD-L1抗体)、MPLDL3280A(抗PD-L1抗体)、MSB0010718C(抗PD-L1抗体)和伊匹单抗(抗CTLA-4抗体,也称为
程序性细胞死亡1(PD-1)是在B细胞、NK细胞和T细胞中表达的免疫检查点蛋白(Shinohara等人,1995,Genomics 23:704-6;Blank等人,2007,Cancer ImmunolImmunother 56:739-45;Finger等人,1997,Gene 197:177-87;Pardoll(2012)NatureReviews Cancer 12:252-264)。PD-1的主要作用是在响应感染的炎症过程中限制外周组织中T细胞的活性,以及限制自身免疫。在激活的T细胞中诱导PD-1表达,并且PD-1与其内源性配体之一的结合通过抑制刺激性激酶起到抑制T细胞激活的作用。PD-1还起到抑制TCR“停止信号”的作用。PD-1在Treg细胞上高度表达,并且可以在配体存在下增加所述Treg细胞的增殖(Pardoll(2012)Nature Reviews Cancer 12:252-264)。抗PD 1抗体已被用于治疗黑色素瘤、非小细胞肺癌、膀胱癌、前列腺癌、结直肠癌、头颈癌、三阴性乳腺癌、白血病、淋巴瘤和肾细胞癌(Topalian等人,2012,N Engl J Med 366:2443-54;Lipson等人,2013,ClinCancer Res 19:462-8;Berger等人,2008,Clin Cancer Res 14:3044-51;Gildener-Leapman等人,2013,Oral Oncol 49:1089-96;Menzies和Long,2013,Ther Adv Med Oncol5:278-85)。示例性抗PD-1抗体包括纳武单抗(BMS的Opdivo)、派姆单抗(Merck的Keytruda)、匹地利珠单抗(Cure Tech的CT-011)、兰姆利珠单抗(lambrolizumab)(Merck的MK-3475)和AMP-224(Merck),纳武单抗(也称为Opdivo、BMS-936558或MDX1106;Bristol-Myers Squibb)是特异性阻断PD-1的完全人IgG4单克隆抗体。纳武单抗(克隆5C4)和特异性地结合PD-1的其他人单克隆抗体描述于US 8,008,449和WO 2006/121168。匹地利珠单抗(CT-011;Cure Tech)是与PD-1结合的人源化IgG1k单克隆抗体。匹地利珠单抗和其他人源化抗PD-1单克隆抗体描述于WO 2009/101611中。派姆单抗(先前称为兰姆利珠单抗,也称为Keytruda,MK03475;Merck)是与PD-1结合的人源化IgG4单克隆抗体。派姆单抗和其他人源化抗PD-1抗体描述于US 8,354,509和WO 2009/114335中。其他抗PD-1抗体尤其包括AMP514(Amplimmune),例如,US 8,609,089、US 2010028330、US 20120114649和/或US20150210769中描述的抗PD-1抗体。AMP-224(B7-DCIg;Amplimmune;例如,描述于WO 2010/027827和WO2011/066342中)是阻断PD-1与B7-H1之间的相互作用的PD-L2Fc融合可溶性受体。
PD-L1(也称为CD274和B7-H1)和PD-L2(也称为CD273和B7-DC)是PD-1的配体,发现于激活的T细胞、B细胞、骨髓细胞、巨噬细胞和一些类型的肿瘤细胞上。抗肿瘤疗法已集中于抗PD-L1抗体。PD-1与PD-L1的复合物抑制CD8+ T细胞的增殖并降低免疫应答(Topalian等人,2012,N Engl J Med 366:2443-54;Brahmer等人,2012,N Eng J Med 366:2455-65)。抗PD-L1抗体已被用于治疗非小细胞肺癌、黑色素瘤、结直肠癌、肾细胞癌、胰腺癌、胃癌、卵巢癌、乳腺癌和血液恶性肿瘤(Brahmer等人,2012,N Eng J Med 366:2455-65;Ott等人,2013,Clin Cancer Res 19:5300-9;Radvanyi等人,2013,Clin Cancer Res 19:5541;Menzies&Long,2013,Ther Adv Med Oncol 5:278-85;Berger等人,2008,Clin Cancer Res14:13044-51)。示例性抗PD-L1抗体包括MDX-1105(Medarex)、MEDI4736(Medimmune)、MPDL3280A(Genentech)、BMS-935559(Bristol-Myers Squibb)和MSB0010718C。MEDI4736(Medimmune)是结合至PD-L1并抑制所述配体与PD-1的相互作用的人单克隆抗体。MDPL3280A(Genentech/Roche)是结合至PD-L1的人Fc优化的IgG1单克隆抗体。MDPL3280A和针对PD-L1的其他人单克隆抗体描述于美国专利号7,943,743和美国公开号20120039906中。其他抗PD-L1结合剂包括YW243.55.S70(参见WO 2010/077634)和MDX-1105(也称为BMS-936559,以及例如描述于WO 2007/005874中的抗PD-L1结合剂)。
细胞毒性T淋巴细胞相关抗原(CTLA-4)也称为CD152,是功能为调节T细胞激活的一种共抑制分子。CTLA-4是仅在T细胞上表达的免疫球蛋白超家族的成员。CTLA-4起到抑制T细胞激活的作用,并且据报道其抑制辅助T细胞活性并增强调节性T细胞免疫抑制活性。尽管CTLA-4的准确作用机制仍在研究之中,但已经提出其通过在与CD80和CD86结合中与CD28竞争而胜出以及将抑制剂信号主动递送至T细胞来抑制T细胞激活(Pardoll(2012)NatureReviews Cancer 12:252-264)。抗CTLA-4抗体已在临床试验中用于治疗黑色素瘤、前列腺癌、小细胞肺癌、非小细胞肺癌(Robert&Ghiringhelli,2009,Oncologist 14:848-61;Ott等人,2013,Clin Cancer Res 19:5300;Weber,2007,Oncologist 12:864-72;Wada等人,2013,J Transl Med 11:89)。抗CTLA-4的重要特征是抗肿瘤作用的动力学,其中在生理反应所需的初始治疗后迟滞期长达6个月。在一些情况下,在治疗开始后,在观察到缩小之前,肿瘤的大小可能实际上增加(Pardoll(2012)Nature Reviews Cancer 12:252-264)。示例性抗CTLA-4抗体包括伊匹单抗(Bristol-Myers Squibb)和曲美目单抗(Pfizer)。伊匹单抗最近已经被FDA批准用于治疗转移性黑色素瘤(Wada等人,2013,J Transl Med 11:89)。
淋巴细胞激活基因-3(LAG-3)也称为CD223,是另一种免疫检查点蛋白。LAG-3与对淋巴细胞活性的抑制相关,并且在一些情况下与淋巴细胞无反应性的诱导相关。LAG-3在免疫系统中的各种细胞上表达,包括B细胞、NK细胞和树突细胞。LAG-3是MHC II类受体的天然配体,所述MHC II类受体在黑色素瘤浸润的T细胞(包括被赋予有效免疫抑制活性的那些T细胞)上大量表达。示例性抗LAG-3抗体包括BMS-986016(Bristol-Myers Squib),其是靶向LAG-3的单克隆抗体。IMP701(Immutep)是拮抗剂LAG-3抗体,并且IMP731(Immutep和GlaxoSmithKline)是耗尽的LAG-3抗体。其他LAG-3抑制剂包括IMP321(Immutep),其是LAG-3的可溶部分和结合MHC II类分子并激活抗原呈递细胞(APC)的Ig的重组融合蛋白。其他抗体描述于例如WO 2010/019570和US 2015/0259420中。
最初在激活的Th1细胞上鉴定的T细胞免疫球蛋白结构域和粘蛋白结构域-3(TIM-3)已被证明是免疫应答的负调节物。TIM-3的阻断促进T细胞介导的抗肿瘤免疫,并且在一系列小鼠肿瘤模型中具有抗肿瘤活性。TIM-3阻断与其他免疫治疗剂(如TSR-042、抗CD137抗体和其他)的组合在增加抗肿瘤作用方面可以是加和的或协同的。TIM-3表达与许多不同的肿瘤类型(包括黑色素瘤、NSCLC和肾癌)相关,另外,肿瘤内TIM-3的表达已经被证明与跨越一系列肿瘤类型(包括NSCLC、宫颈癌和胃癌)的不良预后相关。TIM-3的阻断也有利于提高对许多慢性病毒性疾病的免疫。TIM-3也已被证明与许多配体(包括半乳糖凝集素-9、磷脂酰丝氨酸和HMGB1)相互作用,尽管目前尚不清楚这些配体中有哪些(如果有的话)是与抗肿瘤反应的调节有关。在一些实施方案中,靶向TIM-3的抗体、抗体片段、小分子或肽抑制剂可以与TIM-3的IgV结构域结合以抑制与其配体的相互作用。抑制TIM-3的示例性抗体和肽描述于US 2015/0218274、WO 2013/006490和US 2010/0247521中。其他抗TIM-3抗体包括RMT3-23的人源化形式(Ngiow等人,2011,Cancer Res,71:3540-3551)和克隆8B.2C12(Monney等人,2002,Nature,415:536-541)。抑制TIM-3和PD-1的双特异性抗体描述于US2013/0156774中。
在一些实施方案中,另外的药剂是CEACAM抑制剂(例如,CEACAM-1、CEACAM-3和/或CEACAM-5抑制剂)。在一些实施方案中,CEACAM抑制剂是抗CEACAM抗体分子。示例性抗CEACAM-1抗体描述于WO 2010/125571、WO 2013/082366、WO 2014/059251和WO 2014/022332中,例如,单克隆抗体34B1、26H7和5F4;或其重组形式,如在例如US 2004/0047858、US 7,132,255和WO 99/052552中所述。在一些实施方案中,抗CEACAM抗体与CEACAM-5结合,如在例如Zheng等人PLoS One.(2011)6(6):e21146中所述;或与CEACAM-1和CEACAM-5交叉反应,如在例如WO 2013/054331和US 2014/0271618中所述。
4-1BB也称为CD137,是属于TNFR超家族的跨膜糖蛋白。4-1BB受体存在于激活的T细胞和B细胞和单核细胞上。示例性抗4-1BB抗体是乌瑞鲁单抗(BMS-663513),其具有潜在的免疫刺激和抗肿瘤活性。
肿瘤坏死因子受体超家族成员4(TNFRSF4)也称为OX40和CD134,是TNFR超家族的另一个成员。OX40在静止幼稚T细胞上并非组成型表达,并且起次级共刺激免疫检查点分子的作用。示例性抗OX40抗体是MEDI6469和MOXR0916(RG7888,Genentech)。
在一些实施方案中,另外的药剂包括减少调节性T细胞(Treg)群体的分子。减少Treg细胞的数量(例如,耗尽)的方法是已知的,并且包括例如CD25耗尽、环磷酰胺给予和调节糖皮质激素诱导的TNFR家族相关基因(GITR)功能。GITR是TNFR超家族的成员,其在激活的T细胞上被上调,从而增强免疫系统。在单采术之前或在给予工程化细胞(例如,CAR表达细胞)之前减小受试者中Treg细胞的数量可以减小肿瘤微环境中不需要的免疫细胞(例如,Treg)的数量并降低所述受试者的复发风险。在一些实施方案中,另外的药剂包括靶向GITR和/或调节GITR功能的分子,如耗尽调节性T细胞(Treg)的GITR激动剂和/或GITR抗体。在一些实施方案中,另外的药剂包括环磷酰胺。在一些实施方案中,GITR结合分子和/或调节GITR功能的分子(例如GITR激动剂和/或耗尽Treg的GITR抗体)是在工程化细胞(例如CAR表达细胞)之前给予。例如,在一些实施方案中,GITR激动剂可以在细胞的单采术之前给予。在一些实施方案中,在给予(例如,输注或再输注)工程化细胞(例如,CAR表达细胞)之前或在细胞的单采术之前,将环磷酰胺给予受试者。在一些实施方案中,在给予(例如,输注或再输注)工程化细胞(例如,CAR表达细胞)之前或在细胞的单采术之前,将环磷酰胺和抗GITR抗体给予受试者。
在一些实施方案中,另外的药剂是GITR激动剂。示例性GITR激动剂包括例如GITR融合蛋白和抗GITR抗体(例如,二价抗GITR抗体),如例如美国专利号6,111,090、欧洲专利号090505B 1、美国专利号8,586,023、PCT公开号WO 2010/003118和2011/090754中描述的GITR融合蛋白;或例如美国专利号7,025,962、欧洲专利号1947183B 1、美国专利号7,812,135、美国专利号8,388,967、美国专利号8,591,886、欧洲专利号EP 1866339、PCT公开号WO2011/028683、PCT公开号WO 2013/039954、PCT公开号WO 2005/007190、PCT公开号WO 2007/133822、PCT公开号WO2005/055808、PCT公开号WO 99/40196、PCT公开号WO 2001/03720、PCT公开号WO99/20758、PCT公开号WO2006/083289、PCT公开号WO 2005/115451、美国专利号7,618,632和PCT公开号WO 2011/051726中描述的抗GITR抗体。示例性抗GITR抗体是TRX518。
在一些实施方案中,另外的药剂增强所给予细胞(例如CAR表达细胞)的肿瘤浸润或迁移。例如,在一些实施方案中,另外的药剂刺激CD40,如CD40L,例如,重组人CD40L。分化簇40(CD40)也是TNFR超家族的成员。CD40是在抗原呈递细胞上发现的共刺激蛋白,并且介导众多种免疫应答和炎性应答。CD40还在一些恶性肿瘤上表达,其中CD40促进增殖。示例性抗CD40抗体是达西珠单抗(SGN-40)、鲁卡木单抗(Novartis,拮抗剂)、SEA-CD40(SeattleGenetics)和CP-870,893。在一些实施方案中,增强肿瘤浸润的另外的药剂包括酪氨酸激酶抑制剂舒尼替尼、乙酰肝素酶和/或趋化因子受体(如CCR2、CCR4和CCR7)。
在一些实施方案中,另外的药剂是沙利度胺的结构或功能类似物或衍生物和/或E3泛素连接酶的抑制剂。在一些实施方案中,免疫调节剂与赛拉隆蛋白(cereblon)(CRBN)结合。在一些实施方案中,免疫调节剂与CRBN E3泛素连接酶复合物结合。在一些实施方案中,免疫调节剂与CRBN和CRBN E3泛素连接酶复合物结合。在一些实施方案中,免疫调节剂上调CRBN的蛋白质或基因表达。在一些方面,CRBN是CRL4
在一些实施方案中,另外的药剂是Ikaros(IKZF1)转录因子的抑制剂。在一些实施方案中,另外的药剂增强Ikaros的泛素化。在一些实施方案中,另外的药剂增强Ikaros的降解。在一些实施方案中,另外的药剂下调Ikaros的蛋白质或基因表达。在某些实施方案中,另外的药剂的给予导致Ikaros蛋白水平降低。
在一些实施方案中,另外的药剂是Aiolos(IKZF3)转录因子的抑制剂。在一些实施方案中,另外的药剂增强Aiolos的泛素化。在一些实施方案中,另外的药剂增强Aiolos的降解。在一些实施方案中,另外的药剂下调Aiolos的蛋白质或基因表达。在某些实施方案中,另外的药剂的给予导致Aiolos蛋白水平降低。
在一些实施方案中,另外的药剂是Ikaros(IKZF1)和Aiolos(IKZF3)转录因子二者的抑制剂。在一些实施方案中,另外的药剂增强Ikaros和Aiolos二者的泛素化。在某些实施方案中,另外的药剂增强Ikaros和Aiolos二者的降解。在一些实施方案中,另外的药剂增强Ikaros和Aiolos二者的泛素化和降解。在一些实施方案中,另外的药剂的给予引起Aiolos蛋白水平和Ikaros蛋白水平同时下降。
在一些实施方案中,另外的药剂是选择性细胞因子抑制药物(SelCID)。在一些实施方案中,另外的药剂抑制磷酸二酯酶-4(PDE4)的活性。在一些实施方案中,另外的药剂抑制CDC25磷酸酶的酶活性。在一些实施方案中,另外的药剂改变CDC25磷酸酶的细胞内运输。
在一些实施方案中,另外的药剂是沙利度胺(2-(2,6-二氧代哌啶-3-基)-lH-异吲哚-l,3(2H)-二酮)或沙利度胺的类似物或衍生物。在某些实施方案中,沙利度胺衍生物包括具有相似生物学活性的沙利度胺结构变体。示例性沙利度胺衍生物包括但不限于来那度胺(REVLIMMUNOMODULATORY COMPOUND
在一些实施方案中,另外的药剂是被苯并环中的氨基取代的1-氧代-和1,3二氧代-2-(2,6-二氧代哌啶-3-基)异吲哚啉,如美国专利号5,635,517中所述,将所述专利通过引用并入本文。
在一些实施方案中,另外的药剂是下式的化合物:
其中X和Y中的一个是-C(O)-,并且X和Y中的另一个是-C(O)-或-CH
在一些实施方案中,另外的药剂是属于一类经取代的2-(2,6-二氧代哌啶-3-基)邻苯二甲酸酯免疫调节化合物和经取代的2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚,例如在美国专利号6,281,230、6,316,471、6,335,349和6,476,052以及国际专利申请号PCT/US97/13375(国际公开号WO 98/03502)中所述的那些,将所述专利中的每一篇通过引用并入本文。
在一些实施方案中,另外的药剂是下式的化合物:
其中X和Y中的一个是-C(O)-并且X和Y中的另一个是-C(O)-或-CH
在一些实施方案中,另外的药剂是属于以下专利中所披露的一类异吲哚免疫调节化合物的化合物:美国专利号7,091,353、美国专利公开号2003/0045552和国际申请号PCT/USOI/50401(国际公开号WO02/059106),将所述专利中的每一篇通过引用并入本文。例如,在一些实施方案中,另外的药剂是[2-(2,6-二氧代-哌啶-3-基)-1,3-二氧代-2,3-二氢-1H-异吲哚-4-基甲基]-酰胺;(2-(2,6-二氧代-哌啶-3-基)-1,3-二氧代-2,3-二氢-1H-异吲哚-4-基甲基)-氨基甲酸叔丁酯;4-(氨基甲基)-2-(2,6-二氧代(3-哌啶基))-异吲哚啉-1,3-二酮;N-(2-(2,6-二氧代-哌啶-3-基)-1,3-二氧代-2,3-二氢-1H-异吲哚-4-基甲基)-乙酰胺;N-{(2-(2,6-二氧代(3-哌啶基)-1,3-二氧代异吲哚啉-4-基)甲基}环丙基-甲酰胺;2-氯-N-{(2-(2,6-二氧代)(3-哌啶基))-1,3-二氧代异吲哚啉-4-基)甲基}乙酰胺;N-(2-(2,6-二氧代(3-哌啶基))-1,3-二氧代异吲哚-4-基)-3-吡啶基甲酰胺;3-{1-氧代-4-(苄基氨基)异吲哚啉-2-基}哌啶-2,6-二酮;2-(2,6-二氧代(3-哌啶基))-4-(苄氨基)异吲哚啉-1,3-二酮;N-{(2-(2,6-二氧代(3-哌啶基))-1,3-二氧代异吲哚啉-4-基)甲基}丙酰胺;N-{(2-(2,6-二氧代(3-哌啶基))-1,3-二氧代异吲哚-4-基)甲基}-3-吡啶基甲酰胺;N-{(2-(2,6-二氧代(3-哌啶基))-1,3-二异吲哚啉-4-基)甲基}庚酰胺;N-{(2-(2,6-二氧代(3-哌啶基))-1,3-二氧代异吲哚-4-基)甲基}-2-呋喃甲酰胺;{N-(2-(2,6-二氧代(3-哌啶基))-1,3-二氧代异吲哚-4-基)氨基甲酰基}乙酸甲酯;N-(2-(2,6-二氧代(3-哌啶基))-1,3-二氧代异吲哚啉-4-基)戊酰胺;N-(2-(2,6-二氧代(3-哌啶基))-1,3-二氧代异吲哚啉-4-基)-2-噻吩基甲酰胺;N-{[2-(2,6-二氧代(3-哌啶基))-1,3-二氧代异吲哚啉-4-基]甲基}(丁基氨基)甲酰胺;N-{[2-(2,6-二氧代(3-哌啶基))-1,3-二氧代异吲哚啉-4-基]甲基}(辛基氨基)甲酰胺;或N-{[2-(2,6-二氧代(3-哌啶基))-1,3-二氧代异吲哚-4-基]甲基}(苄氨基)甲酰胺。
在一些实施方案中,另外的药剂是属于以下专利中所披露的一类异吲哚免疫调节化合物的化合物:美国专利申请公开号2002/0045643、国际公开号WO 98/54170和美国专利号6,395,754,将所述专利中的每一篇通过引用并入本文。在一些实施方案中,另外的药剂是以下专利中所述的四取代的2-(2,6-二氧代哌啶-3-基)-1-氧代异吲哚啉:美国专利号5,798,368,将其通过引用并入本文。在一些实施方案中,另外的药剂是通过引用并入本文的美国专利号6,403,613中所披露的1-氧代和1,3-二氧代-2-(2,6-二氧代哌啶-3-基)异吲哚啉。在一些实施方案中,另外的药剂是美国专利号6,380,239和美国专利号7,244,759中所述的在吲哚啉环的4-或5-位取代的1-氧代或1,3-二氧代异吲哚啉,所述两篇专利均通过引用并入本文。
在一些实施方案中,另外的药剂是2-(4-氨基-1-氧代-1,3-二氢-异吲哚-2-基)-4-氨基甲酰基-丁酸或4-(4-氨基-1-氧代-1,3-二氢-异吲哚-2-基)-4-氨基甲酰基-丁酸。在一些实施方案中,免疫调节化合物是4-氨基甲酰基-4-{4-[(呋喃-2-基-甲基)-氨基]-1,3-二氧代-1,3-二氢-异吲哚-2-基}-丁酸、4-氨基甲酰基-2-{4-[(呋喃-2-基-甲基)-氨基]-1,3-二氧代-1,3-二氢-异吲哚-2-基}-丁酸、2-{4-[(呋喃-2-基-甲基)-氨基]-1,3-二氧代-1,3-二氢-异吲哚-2-基}-4-苯基氨基甲酰基-丁酸或2-{4-[(呋喃-2-基-甲基)-氨基]-1,3-二氧代-1,3-二氢-异吲哚-2-基}-戊二酸。
在一些实施方案中,另外的药剂是如通过引用并入本文的美国专利号6,458,810中所述的在2-位被2,6-二氧代-3-羟基哌啶-5-基取代的异吲哚啉-1-酮或异吲哚啉-1,3-二酮。在一些实施方案中,免疫调节化合物是3-(5-氨基-2-甲基-4-氧代-4H-喹唑啉-3-基)-哌啶-2,6-二酮,或其对映异构体或对映异构体的混合物;或它们的药学上可接受的盐、溶剂化物、水合物、共晶、包合物或多晶型物。在一些实施方案中,免疫调节化合物是3-[4-(4-吗啉-4-基甲基-苄氧基)-1-氧代-1,3-二氢-异吲哚-2-基]-哌啶-2,6-二酮。
在一些实施方案中,另外的药剂是如以下文献中所述:Oshima,K.等人,NihonRinsho.,72(6):1130-5(2014);Millrine,D.等人,Trends Mol Med.,23(4):348-364(2017);和Collins等人,Biochem J.,474(7):1127-1147(2017)。
在一些实施方案中,另外的药剂是来那度胺、泊马度胺、阿伐度胺,来那度胺、泊马度胺、阿伐度胺的立体异构体,或其药学上可接受的盐、溶剂化物、水合物、共晶、包合物或多晶型物。在一些实施方案中,免疫调节化合物是来那度胺、来那度胺的立体异构体、或其药学上可接受的盐、溶剂化物、水合物、共晶、包合物或多晶型物。在一些实施方案中,免疫调节化合物是来那度胺或((RS)-3-(4-氨基-1-氧代-1,3-二氢-2H-异吲哚-2-基)哌啶-2,6-二酮)。
在某些实施方案中,通过向受试者给予沙利度胺衍生物来那度胺((RS)-3-(4-氨基-1-氧代-1,3-二氢-2H-异吲哚-2-基)哌啶-2,6-二酮)来破坏病灶。来那度胺被FDA批准用于治疗多发性骨髓瘤、与缺失5q相关的骨髓增生异常综合征以及最近用于治疗复发/难治性套细胞淋巴瘤(MCL)。来那度胺通常是沙利度胺的合成衍生物,并且目前被理解为具有多种免疫调节作用,包括在T细胞与抗原呈递细胞(APC)之间使得免疫突触形成。例如,在一些情况下,来那度胺调节T细胞应答并导致增加CD4
在一些实施方案中,另外的药剂包括沙利度胺药物或其类似物和/或其衍生物,如来那度胺、泊马度胺或阿普斯特。参见例如Bertilaccio等人,Blood(2013)122:4171;Otahal等人,Oncoimmunology(2016)5(4):e1115940;Fecteau等人,Blood(2014)124(10):1637-1644;和Kuramitsu等人,Cancer Gene Therapy(2015)22:487-495。来那度胺((RS)-3-(4-氨基-1-氧代-1,3-二氢-2H-异吲哚-2-基)哌啶-2,6-二酮;也称为Revlimid)是沙利度胺的合成衍生物,并且具有多种免疫调节作用,包括加强T细胞与抗原呈递细胞(APC)之间的免疫突触形成。例如,在一些情况下,来那度胺调节T细胞应答并导致增加CD4+和CD8+T细胞中白细胞介素(IL)-2的产生,诱导T辅助(Th)应答从Th2转变为Th1,抑制调节性T细胞子集(Treg)的扩增,以及改进滤泡性淋巴瘤和慢性淋巴细胞白血病(CLL)中免疫突触的功能(Otahal等人,Oncoimmunology(2016)5(4):e1115940)。来那度胺在患有多发性骨髓瘤(MM)的患者中也具有直接的肿瘤杀伤活性,并且通过影响支持细胞(如在淋巴组织的微环境中发现的呵护样细胞(nurse-like cell))直接和间接地调节CLL肿瘤细胞的存活。来那度胺还可以响应于通过CD3连接激活T细胞或树突细胞介导的激活而增强T细胞增殖和干扰素-γ产生。来那度胺还可以诱导恶性B细胞表达更高水平的免疫刺激分子,如CD80、CD86、HLA-DR、CD95和CD40(Fecteau等人,Blood(2014)124(10):1637-1644)。
在一些实施方案中,另外的药剂是B细胞抑制剂。在一些实施方案中,另外的药剂是一种或多种B细胞抑制剂,所述一种或多种B细胞抑制剂选自CD10、CD19、CD20、CD22、CD34、CD123、CD79a、CD79b、CD179b、FLT-3或ROR1或其组合的抑制剂。在一些实施方案中,B细胞抑制剂是抗体(例如,单特异性或双特异性抗体)或其抗原结合片段。在一些实施方案中,另外的药剂是表达靶向B细胞靶标(例如,CD10、CD19、CD20、CD22、CD34、CD123、CD79a、CD79b、CD179b、FLT-3或ROR1)的重组受体的工程化细胞。
在一些实施方案中,另外的药剂是CD20抑制剂,例如,抗CD20抗体(例如,抗CD20单特异性或双特异性抗体)或其片段。示例性抗CD20抗体包括但不限于利妥昔单抗、奥法木单抗、奥瑞珠单抗(也称为GA101或RO5072759)、维妥珠单抗、奥比妥珠单抗、TRU-015(TrubionPharmaceuticals)、奥卡妥珠单抗(也称为AME-133v或奥卡妥珠单抗)和Pro131921(Genentech)。参见例如Lim等人Haematologica.(2010)95(1):135-43。在一些实施方案中,抗CD20抗体包含利妥昔单抗。利妥昔单抗是嵌合小鼠/人单克隆抗体IgG1κ,其与CD20结合并引起CD20表达细胞的细胞溶解。在一些实施方案中,另外的药剂包括利妥昔单抗。在一些实施方案中,CD20抑制剂是小分子。
在一些实施方案中,另外的药剂是CD22抑制剂,例如,抗CD22抗体(例如,抗CD22单特异性或双特异性抗体)或其片段。示例性抗CD22抗体包括依帕珠单抗和RFB4。在一些实施方案中,CD22抑制剂是小分子。在一些实施方案中,抗体是单特异性抗体,任选地与诸如化学治疗剂的第二药剂缀合。例如,在一些实施方案中,抗体是抗CD22单克隆抗体-MMAE缀合物(例如,DCDT2980S)。在一些实施方案中,抗体是抗CD22抗体的scFv,例如,抗体RFB4的scFv。在一些实施方案中,scFv与假单胞菌属(Pseudomonas)外毒素-A(例如,BL22)的全部或片段融合。在一些实施方案中,scFv与假单胞菌属外毒素-A(例如,moxetumomabpasudotox)的全部或片段(例如,38kDa片段)融合。在一些实施方案中,抗CD22抗体是抗CD19/CD22双特异性抗体,任选地与毒素缀合。例如,在一些实施方案中,抗CD22抗体包含抗CD19/CD22双特异性部分(例如,两个scFv配体,识别人CD19和CD22),其任选地连接至白喉毒素(DT)的全部或一部分,例如白喉毒素(DT)的前389个氨基酸(DT 390),例如配体引导的毒素如DT2219ARL。在一些实施方案中,双特异性部分(例如抗CD19/抗CD22)连接至毒素如脱糖基化蓖麻毒素A链(例如,Combotox)。
在一些实施方案中,免疫调节剂是细胞因子。在一些实施方案中,免疫调节剂是细胞因子或者是诱导肿瘤微环境中的细胞因子表达增加的药剂。细胞因子具有与T细胞扩增、分化、存活和稳态有关的重要功能。可以向接受本文所提供的结合分子(例如CCT5结合分子)、重组受体、细胞和/或组合物的受试者给予的细胞因子包括以下中的一种或多种:IL-2、IL-4、IL-7、IL-9、IL-15、IL-18和IL-21。在一些实施方案中,所给予的细胞因子是IL-7、IL-15或IL-21或其组合。在一些实施方案中,将细胞因子给予至对工程化细胞(例如,CAR表达细胞)的给予具有次最佳反应的受试者,改善所给予细胞(例如CAR表达细胞)的功效和/或抗肿瘤活性。
“细胞因子”意指由一个细胞群释放的作为细胞间介体作用于另一种细胞的蛋白质的通用术语。此类细胞因子的例子是淋巴因子、单核因子和传统的多肽激素。细胞因子包括生长激素,如人生长激素、N-甲硫氨酰基人生长激素和牛生长激素;甲状旁腺激素;甲状腺素;胰岛素;胰岛素原;松弛素;松弛素原;糖蛋白激素,如卵泡刺激素(FSH)、甲状腺刺激素(TSH)和黄体化激素(LH);肝生长因子;成纤维细胞生长因子;泌乳素;胎盘催乳素;肿瘤坏死因子-α和-β;缪勒抑制物质;小鼠促性腺激素相关肽;抑制素;激活素;血管内皮生长因子;整合素;血小板生成素(TPO);神经生长因子,如NGF-β;血小板生长因子;转化生长因子(TGF),如TGF-α和TGF-β;胰岛素样生长因子-I和-II;促红细胞生成素(EPO);骨诱导因子;干扰素,如干扰素-α、-β和-γ;集落刺激因子(CSF),如巨噬细胞-CSF(M-CSF);粒细胞-巨噬细胞-CSF(GM-CSF);和粒细胞-CSF(G-CSF);白细胞介素(IL),如IL-1、IL-1α、IL-2、IL-3、IL-4、IL-5、IL-6、IL-7、IL-8、IL-9、IL-10、IL-11、IL-12、IL-15;肿瘤坏死因子,如TNF-α或TNF-β;以及其他多肽因子,包括LIF和kit配体(KL)。如本文所用,术语细胞因子包括来自天然来源或来自重组细胞培养物的蛋白质,以及天然序列细胞因子的生物活性等同物。例如,免疫调节剂是细胞因子,并且细胞因子是IL-4、TNF-α、GM-CSF或IL-2。
在一些实施方案中,另外的药剂包括白细胞介素-15(IL-15)多肽、白细胞介素-15受体α(IL-15Rα)多肽、或其组合(例如hetIL-15(Admune Therapeutics,LLC))。hetIL-15是IL-15与IL-15Rα的异二聚体非共价复合物。hetIL-15描述于例如以下文献中:U.S.8,124,084、U.S.2012/0177598、U.S.2009/0082299、U.S.2012/0141413和U.S.2011/0081311。在一些实施方案中,免疫调节剂可以含有一种或多种细胞因子。例如,白细胞介素可以包括白细胞-白细胞介素注射剂(Multikine),其是天然细胞因子的组合。在一些实施方案中,免疫调节剂是Toll样受体(TLR)激动剂、佐剂或细胞因子。
在一些实施方案中,另外的药剂是改善或中和与细胞疗法相关的一种或多种毒性或副作用的药剂。在一些实施方案中,另外的药剂选自类固醇(例如皮质类固醇)、TNFα抑制剂和IL-6抑制剂。TNFα抑制剂的例子是抗TNFα抗体分子,如英利昔单抗、阿达木单抗、培赛利珠单抗单抗(certolizumab pegol)和戈利木单抗。TNFα抑制剂的另一个例子是融合蛋白,如依那西普。TNFα的小分子抑制剂包括但不限于黄嘌呤衍生物(例如己酮可可碱)和安非他酮。IL-6抑制剂的例子是抗IL-6抗体分子,如托珠单抗、萨瑞鲁单抗、伊西莫单抗(elsilimomab)、CNTO 328、ALD518/BMS-945429、CNTO 136、CPSI-2364、CDP6038、VX30、ARGX-109、FE301和FM101。在一些实施方案中,抗IL-6抗体分子是托珠单抗(tocilizumab)。在一些实施方案中,另外的药剂是IL-1R抑制剂,如阿那白滞素。
在一些实施方案中,另外的药剂是腺苷水平和/或腺苷途径组分的调节剂。腺苷可以在体内起免疫调节剂的功能。例如,腺苷和非选择性地激活腺苷受体亚型的一些腺苷类似物降低炎性氧化产物的嗜中性粒细胞产生(Cronstein等人,Ann.N.Y.Acad.Sci.451:291,1985;Roberts等人,Biochem.J.,227:669,1985;Schrier等人,J.Immunol.137:3284,1986;Cronstein等人,Clinical Immunol.Immunopath.42:76,1987)。在一些情况下,细胞外腺苷或腺苷类似物的浓度在特定环境(例如肿瘤微环境(TME))中可能增加。在一些情况下,腺苷或腺苷类似物信号传导取决于缺氧或在缺氧或其调节中所涉及的因子,例如缺氧诱导因子(HIF)。在一些实施方案中,腺苷信号传导的增加可以增加细胞内cAMP和cAMP依赖性蛋白激酶,从而导致抑制促炎性细胞因子产生,并且可以导致免疫抑制分子的合成和Treg的发展(Sitkovsky等人,Cancer Immunol Res(2014)2(7):598-605)。在一些实施方案中,另外的药剂可以降低或逆转腺苷、腺苷类似物和/或腺苷信号传导的免疫抑制效应。在一些实施方案中,另外的药剂可以减少或逆转缺氧驱动的A2-腺苷酸能T细胞免疫抑制。在一些实施方案中,另外的药剂选自腺苷受体的拮抗剂、细胞外腺苷降解剂、CD39/CD73胞外酶的腺苷产生的抑制剂、和缺氧-HIF-1α信号传导的抑制剂。在一些实施方案中,所述另外的药剂是腺苷受体拮抗剂或激动剂。
通过细胞外腺苷的抑制剂(例如防止细胞外腺苷形成、降解细胞外腺苷、使细胞外腺苷失活和/或减少细胞外腺苷的药剂)和/或腺苷受体抑制剂(例如腺苷受体拮抗剂)可以增强免疫应答,如巨噬细胞、嗜中性粒细胞、粒细胞、树突细胞、T细胞和/或B细胞介导的应答。此外,Gs蛋白介导的cAMP依赖性细胞内途径的抑制剂和腺苷受体触发的Gi蛋白介导的细胞内途径的抑制剂也可以增加急性和慢性炎症。
在一些实施方案中,另外的药剂是腺苷受体拮抗剂或激动剂,例如腺苷受体A2a、A2b、A1和A3中的一种或多种的拮抗剂或激动剂。分别地,A1和A3抑制腺苷酸环化酶活性,并且A2a和A2b刺激腺苷酸环化酶活性。某些腺苷受体(如A2a、A2b和A3)可以在炎症期间抑制或降低免疫应答。因此,拮抗免疫抑制性腺苷受体可以扩大、加强或增强免疫应答,例如来自所给予细胞(例如,CAR表达T细胞)的免疫应答。在一些实施方案中,所述另外的药剂抑制细胞外腺苷的产生和腺苷通过腺苷受体触发的信号传导。例如,通过抑制或减少产生腺苷的局部组织缺氧;通过降解积累的细胞外腺苷(或使其失活);通过阻止或减少免疫细胞上腺苷受体的表达;和/或通过抑制/拮抗腺苷配体通过腺苷受体进行的信号传导,可以增强免疫应答、局部组织炎症和所靶向组织破坏的增强。
拮抗剂是作为与细胞受体结合而不引发生物学反应的药剂,倾向于消除另一种物质的作用的任何物质。在一些实施方案中,拮抗剂是化学化合物,其是腺苷受体(如A2a、A2b或A3受体)的拮抗剂。在一些实施方案中,拮抗剂是结合腺苷受体但是不触发Gi蛋白依赖性细胞内途径的肽或拟肽。示例性拮抗剂描述于以下文献中:美国专利号5,565,566、5,545,627、5,981,524、5,861,405、6,066,642、6,326,390、5,670,501、6,117,998、6,232,297、5,786,360、5,424,297、6,313,131、5,504,090和6,322,771。
在一些实施方案中,另外的药剂是A2受体(A2R)拮抗剂,如A2a拮抗剂。示例性A2R拮抗剂包括KW6002(伊曲茶碱(istradefyline))、SCH58261、咖啡因、副黄嘌呤、3,7-二甲基-1-炔丙基黄嘌呤(DMPX)、8-(间氯苯乙烯基)咖啡因(CSC)、MSX-2、MSX-3、MSX-4、CGS-15943、ZM-241385、SCH-442416、瑞德南特(preladenant)、韦帕南特(vipadenant)(BII014)、V2006、ST-1535、SYN-115、PSB-1115、ZM241365、FSPTP和靶向A2R表达的抑制性核酸(例如,siRNA或shRNA)或靶向A2R的任何抗体或其抗原结合片段。在一些实施方案中,另外的药剂是描述于例如以下文献中的A2R拮抗剂:Ohta等人,Proc Natl Acad Sci U S A(2006)103:13132-13137;Jin等人,Cancer Res.(2010)70(6):2245-2255;Leone等人,Computational and Structural Biotechnology Journal(2015)13:265-272;Beavis等人,Proc Natl Acad Sci U S A(2013)110:14711-14716;和Pinna,A.,Expert OpinInvestig Drugs(2009)18:1619-1631;Sitkovsky等人,Cancer Immunol Res(2014)2(7):598-605;US 8,080,554;US 8,716,301;US 20140056922;WO 2008/147482;US 8,883,500;US 20140377240;WO 02/055083;US 7,141,575;US 7,405,219;US 8,883,500;US 8,450,329和US 8,987,279。
在一些实施方案中,拮抗剂是特异性地结合编码腺苷受体的mRNA的反义分子、抑制性核酸分子(例如,小抑制性RNA(siRNA))或催化性核酸分子(例如,核酶)。在一些实施方案中,反义分子、抑制性核酸分子或催化性核酸分子结合编码A2a、A2b或A3的核酸。在一些实施方案中,反义分子、抑制性核酸分子或催化核酸靶向腺苷受体下游的生化途径。例如,所述反义分子或催化核酸可以抑制Gs蛋白或Gi蛋白依赖性细胞内途径中涉及的酶。在一些实施方案中,另外的药剂包括腺苷受体(如A2a、A2b或A3)的显性阴性突变形式。
在一些实施方案中,抑制细胞外腺苷的另外的药剂包括使细胞外腺苷无功能(或降低这种功能)的药剂,例如修饰腺苷结构以抑制腺苷通过腺苷受体进行信号传导的能力的物质。在一些实施方案中,另外的药剂是细胞外产生腺苷或腺苷降解的酶,其修饰形式或其调节剂。例如,在一些实施方案中,另外的药剂是酶(例如,腺苷脱氨酶)或另一种催化分子,所述酶或另一种催化分子选择性地结合并破坏腺苷,从而消除或显著降低内源形成的腺苷通过腺苷受体进行信号传导并终止炎症的能力。
在一些实施方案中,另外的药剂是腺苷脱氨酶(ADA)或其修饰形式,例如,重组ADA和/或聚乙二醇修饰的ADA(ADA-PEG),其可以抑制细胞外腺苷的局部组织积累。ADA-PEG已用于治疗患有ADA SCID的患者(Hershfield(1995)Hum Mutat.5:107)。在一些实施方案中,抑制细胞外腺苷的药剂包括阻止或减少细胞外腺苷形成,和/或阻止或减少细胞外腺苷积累,从而消除或显著降低腺苷的免疫抑制作用的药剂。在一些实施方案中,另外的药剂特异性地抑制参与对促炎性分子的合成和/或分泌进行调节的酶和蛋白质,所述另外的药剂包括核转录因子的调节剂。对腺苷受体表达、或Gs蛋白或Gi蛋白依赖性细胞内途径、或cAMP依赖性细胞内途径的抑制可以导致免疫应答的增加/增强。
在一些实施方案中,另外的药剂可以靶向生成或产生细胞外腺苷的胞外酶。在一些实施方案中,另外的药剂靶向共同作用于产生细胞外腺苷的CD39和CD73胞外酶。CD39(也称为外核苷三磷酸二磷酸水解酶)将细胞外ATP(或ADP)转化为5'AMP。随后,CD73(也称为5'核苷酸酶)将5'AMP转化为腺苷。CD39的活性可通过NDP激酶和腺苷酸激酶的作用逆转,而CD73的活性是不可逆的。CD39和CD73在肿瘤基质细胞(包括内皮细胞和Treg)上表达,并且也在许多癌细胞上表达。例如,在肿瘤微环境的低氧条件下,CD39和CD73在内皮细胞上的表达增加。肿瘤缺氧可能源于血液供应不足和肿瘤血管杂乱,从而削弱氧气的递送(Carroll和Ashcroft(2005),Expert.Rev.Mol.Med.7(6):1-16)。缺氧也抑制将腺苷转化为AMP的腺苷酸激酶(AK),从而导致非常高的细胞外腺苷浓度。因此,响应缺氧以高浓度释放腺苷,缺氧是在实体瘤中或实体瘤周围的肿瘤微环境(TME)中频繁出现的条件。在一些实施方案中,另外的药剂是抗CD39抗体或其抗原结合片段、抗CD73抗体或其抗原结合片段(例如MEDI9447或TY/23)、α-β-亚甲基-腺苷二磷酸(ADP)、ARL 67156、POM-3、IPH52中的一种或多种(参见例如Allard等人Clin Cancer Res(2013)19(20):5626-5635;Hausler等人,Am JTransl Res(2014)6(2):129-139;Zhang,B.,Cancer Res.(2010)70(16):6407-6411)。
在一些实施方案中,另外的药剂是缺氧诱导因子1α(HIF-1α)信号传导的抑制剂。示例性HIF-1α抑制剂包括地高辛、吖啶黄素、瑟土因-7(sirtuin-7)和加特司匹(ganetespib)。
在一些实施方案中,另外的药剂包括蛋白质酪氨酸磷酸酶抑制剂,例如,本文所述的蛋白质酪氨酸磷酸酶抑制剂。在一些实施方案中,蛋白质酪氨酸磷酸酶抑制剂是SHP-1抑制剂,例如本文所述的SHP-1抑制剂,例如,葡萄糖酸锑钠。在一些实施方案中,蛋白质酪氨酸磷酸酶抑制剂是SHP-2抑制剂,例如本文所述的SHP-2抑制剂。
在一些实施方案中,另外的药剂是激酶抑制剂。激酶抑制剂(如CDK4激酶抑制剂、BTK激酶抑制剂、MNK激酶抑制剂或DGK激酶抑制剂)可以调节肿瘤细胞中存在的组成型活性的存活途径和/或调节免疫细胞的功能。在一些实施方案中,激酶抑制剂是布鲁顿酪氨酸激酶(BTK)抑制剂,例如依鲁替尼(ibrutinib)。在一些实施方案中,激酶抑制剂是磷脂酰肌醇-4,5-二磷酸酯3-激酶(PI3K)抑制剂。在一些实施方案中,激酶抑制剂是CDK4抑制剂,例如,CDK4/6抑制剂。在一些实施方案中,激酶抑制剂是mTOR抑制剂,例如雷帕霉素、雷帕霉素类似物、OSI-027。mTOR抑制剂可以是例如mTORC1抑制剂和/或mTORC2抑制剂,例如mTORC1抑制剂和/或mTORC2抑制剂。在一些实施方案中,激酶抑制剂是MNK抑制剂或双重PI3K/mTOR抑制剂。在一些实施方案中,其他示例性激酶抑制剂包括AKT抑制剂哌立福辛(perifosine)、mTOR抑制剂坦罗莫司(temsirolimus)、Src激酶抑制剂达沙替尼(dasatinib)和福他替尼(fostamatinib)、JAK2抑制剂帕克替尼和鲁索替尼、PKCβ抑制剂恩扎妥林(enzastaurin)和苔藓抑素,以及AAK抑制剂阿立塞替(alisertib)。
在一些实施方案中,所述激酶抑制剂是选自以下的BTK抑制剂:依鲁替尼(PCI-32765);GDC-0834;RN-486;CGI-560;CGI-1764;HM-71224;CC-292;ONO-4059;CNX-774;和LFM-A13。在一些实施方案中,所述BTK抑制剂不会降低或抑制白细胞介素-2诱导型激酶(ITK)的激酶活性,并且选自GDC-0834;RN-486;CGI-560;CGI-1764;HM-71224;CC-292;ONO-4059;CNX-774;和LFM-A13。
在一些实施方案中,激酶抑制剂是BTK抑制剂,例如,依鲁替尼(1-[(3R)-3-[4-氨基-3-(4-苯氧基苯基)-1H-吡唑并[3,4-d]嘧啶-1-基]哌啶-1-基]丙-2-烯-1-酮;也称为PCI-32765)。在一些实施方案中,激酶抑制剂是BTK抑制剂,例如依鲁替尼(PCI-32765)。在一些实施方案中,给予1、2、3、4、5、6、7、8、9、10、11、12或更多个周期的依鲁替尼。在一些实施方案中,BTK抑制剂是国际申请WO 2015/079417中描述的BTK抑制剂。
在一些实施方案中,所述激酶抑制剂是PI3K抑制剂。PI3K是参与细胞周期调节和淋巴瘤存活的PI3K/Akt/mTOR途径的核心。示例性PI3K抑制剂包括艾代拉里司(idelalisib)(PI3Kδ抑制剂)。在一些实施方案中,另外的药剂是艾代拉利司和利妥昔单抗。
在一些实施方案中,另外的药剂是雷帕霉素的哺乳动物靶标(mTOR)的抑制剂。在一些实施方案中,激酶抑制剂是选自以下的mTOR抑制剂:坦罗莫司;利罗莫司(ridaforolimus)(也称为AP23573和MK8669);依维莫司(RAD001);雷帕霉素(AY22989);simapimod;AZD8055;PF04691502;SF1126;和XL765。在一些实施方案中,另外的药剂是丝裂原激活蛋白激酶(MAPK)抑制剂,如威罗菲尼(vemurafenib)、达拉非尼(dabrafenib)和曲美替尼(trametinib)。
在一些实施方案中,另外的药剂是调节促细胞凋亡或抗细胞凋亡蛋白的药剂。在一些实施方案中,另外的药剂包括B细胞淋巴瘤2(BCL-2)抑制剂(例如,维奈妥拉(venetoclax),也称为ABT-199或GDC-0199;或ABT-737)。维奈托克是抑制抗细胞凋亡蛋白BCL-2的小分子(4-(4-{[2-(4-氯苯基)-4,4-二甲基-1-环己烯-1-基]甲基}-1-哌嗪基)-N-({3-硝基-4-[(四氢-2H-吡喃-4-基甲基)氨基]苯基}磺酰基)-2-(1H-吡咯并[2,3-b]吡啶-5-基氧基)苯甲酰胺)。调节促细胞凋亡或抗细胞凋亡蛋白的其他药剂包括BCL-2抑制剂ABT-737、那维妥拉(navitoclax)(ABT-263);用于最大功效的Mcl-1siRNA或Mcl-1抑制剂类视色素N-(4-羟苯基)维甲酰胺(4-HPR)。在一些实施方案中,另外的药剂提供促细胞凋亡刺激,如重组肿瘤坏死因子相关细胞凋亡诱导配体(TRAIL),其可以通过与肿瘤细胞表面上的TRAIL死亡受体DR-4和DR-5结合激活细胞凋亡途径;或TRAIL-R2激动抗体。
在一些实施方案中,另外的药剂包括吲哚胺2,3-双加氧酶(IDO)抑制剂。IDO是一种催化氨基酸L-色氨酸降解为犬尿氨酸的酶。许多癌症过表达IDO,例如前列腺癌、结直肠癌、胰腺癌、宫颈癌、胃癌、卵巢癌、头癌和肺癌。浆细胞样树突细胞(pDC)、巨噬细胞和树突细胞(DC)可以表达IDO。在一些方面,L-色氨酸的减少(例如由IDO催化)通过诱导T细胞无反应性和凋亡而导致免疫抑制环境。因此,在一些方面,例如通过减少所给予的CAR表达细胞的抑制或死亡,IDO抑制剂可以增强本文所述的结合分子(例如CCT5结合分子)、重组受体、细胞和/或组合物的功效。IDO的示例性抑制剂包括但不限于1-甲基-色氨酸、吲哚莫德和INCB024360(艾卡哚司他(epacadostat))。
在一些实施方案中,另外的药剂包括细胞毒性剂,例如,CPX-351(CelatorPharmaceuticals)、阿糖胞苷、道诺霉素、沃沙隆沙星(vosaroxin)(SunesisPharmaceuticals)、沙帕他滨(Cyclacel Pharmaceuticals)、伊达比星或米托蒽醌。在一些实施方案中,另外的药剂包括低甲基化剂,例如,DNA甲基转移酶抑制剂,例如,阿扎胞苷或地西他滨。
在另一个实施方案中,另外的疗法是移植,例如,同种异体干细胞移植。
在一些实施方案中,另外的疗法是淋巴细胞清除疗法。在一些实施方案中,在例如给予工程化细胞(例如,CAR表达细胞)之前对受试者进行淋巴细胞清除。在一些实施方案中,淋巴细胞清除包括给予以下中的一种或多种:美法仑、环磷酰胺(Cytoxan)、环磷酰胺(cyclophosphamide)和氟达拉滨。在一些实施方案中,在工程化细胞(例如,CAR表达细胞)的给予(例如,输注)之前、与其并行或之后,向受试者给予淋巴细胞清除化学疗法。在一个例子中,在工程化细胞(例如,CAR表达细胞)的给予之前向受试者给予淋巴细胞清除化学疗法。
在一些实施方案中,另外的药剂是溶瘤病毒。在一些实施方案中,溶瘤病毒能够在癌细胞中选择性地复制并触发所述癌细胞的死亡或减慢所述癌细胞的生长。在一些情况下,溶瘤病毒对非癌细胞无影响或影响极小。溶瘤病毒包括但不限于溶瘤腺病毒、溶瘤单纯疱疹病毒、溶瘤逆转录病毒、溶瘤细小病毒、溶瘤痘苗病毒、溶瘤辛德毕斯病毒(oncolyticSinbis virus)、溶瘤流感病毒或溶瘤RNA病毒(例如,溶瘤呼吸弧病毒、溶瘤新城疫病毒(NDV)、溶瘤麻疹病毒或溶瘤水疱性口炎病毒(VSV))。
其他示例性组合疗法、治疗和/或药剂包括抗过敏剂、止吐药、镇痛药和辅助疗法。在一些实施方案中,另外的药剂包括细胞保护剂,如神经保护剂、自由基清除剂、心脏保护剂、蒽环类外渗中和剂和营养素。
在一些实施方案中,用作另外的药剂的抗体与本文所述的治疗剂缀合或以其他方式结合,所述治疗剂是例如化学治疗剂(例如,环磷酰胺、氟达拉滨、组蛋白脱乙酰化酶抑制剂、脱甲基剂、肽疫苗、抗肿瘤抗生素、酪氨酸激酶抑制剂、烷化剂、抗微管剂或抗有丝分裂剂)、抗过敏剂、止吐剂(anti-nausea agent)(或止吐药(anti-emetic))、止痛药或细胞保护剂。在一些实施方案中,所述另外的药剂是抗体-药物缀合物。
在一些实施方案中,另外的药剂可以在DNA、RNA或蛋白质水平上调节、抑制或刺激特定因子,以增强或加强本文所提供的结合分子(例如CCT5结合分子)、重组受体、细胞和/或组合物的功效。在一些实施方案中,另外的药剂可以在所给予的细胞(例如被工程化以表达重组受体(例如CAR)的细胞)内在核酸(例如DNA或RNA)水平上调节因子。在一些实施方案中,抑制性核酸(例如抑制性核酸,例如dsRNA,例如siRNA或shRNA)或成簇的规律间隔短回文重复序列(CRISPR)、转录激活因子样效应核酸酶(TALEN)或锌指核酸内切酶(ZFN)可以用于抑制工程化细胞(例如CAR表达细胞)中抑制性分子的表达。在一些实施方案中,抑制剂是shRNA。在一些实施方案中,抑制性分子在工程化细胞(例如CAR表达细胞)内被抑制。在一些实施方案中,编码抑制调节或调控(例如抑制)T细胞功能的分子的表达的dsRNA分子的核酸分子可操作地连接至启动子(例如源自HI或U6的启动子),使得抑制所述抑制性分子的表达的dsRNA分子在工程化细胞(例如CAR表达细胞)内表达。参见例如Brummelkamp TR,等人(2002)Science 296:550-553;Miyagishi M,等人(2002)Nat.Biotechnol.19:497-500。
在一些实施方案中,另外的药剂(如本文所述的任何免疫检查点抑制剂)能够破坏编码抑制性分子的基因。在一些实施方案中,破坏是通过缺失(例如整个基因、外显子或区域的缺失),和/或用外源序列替代,和/或通过在基因内通常在基因的外显子内的突变(例如移码或错义突变)。在一些实施方案中,破坏导致提前终止密码子并入基因中,使得抑制性分子不表达或不以能够在细胞表面上表达和/或能够介导细胞信号传导的形式表达。破坏通常在DNA水平上进行。破坏通常是永久性的、不可逆的或非暂时性的。
在一些方面,破坏通过基因编辑如使用在被靶向进行破坏的区域处与基因特异性地结合或杂交的DNA结合蛋白或DNA结合核酸进行。在一些方面,所述蛋白质或核酸与核酸酶偶联或复合,例如以嵌合或融合蛋白的形式。例如,在一些实施方案中,使用对所破坏的基因具有特异性的、包含DNA靶向蛋白质和核酸酶的融合物(如锌指核酸酶(ZFN)或TAL效应子核酸酶(TALEN)或RNA指导的核酸酶(如成簇的规律间隔短回文重复序列(CRISPR)-Cas系统,如CRISPR-Cas9系统))来实现破坏。在一些实施方案中,产生或生成基因工程化细胞(例如CAR表达细胞)的方法包括向细胞群中引入编码基因工程化抗原受体(例如CAR)的核酸分子和编码靶向抑制性分子的药剂的核酸分子,所述药剂是对抑制分子具有特异性的基因编辑核酸酶,例如DNA靶向蛋白质和核酸酶的融合物(如ZFN或TALEN或RNA指导的核酸酶(如CRISPR-Cas9系统))。
可以制备任何本文所述的另外的药剂,并将其与本文所述的CCT5结合分子(例如抗体)、免疫缀合物、重组受体(例如嵌合抗原受体)和/或表达所述分子(例如重组受体)的工程化细胞一起作为组合疗法来给予,如以包含组合疗法的一种或多种药剂和药学上可接受的载体(如本文所述的任何一种)的药物组合物来给予。在一些实施方案中,可以将CCT5结合分子(例如抗体)、免疫缀合物、重组受体(例如嵌合抗原受体)、表达所述分子(例如重组受体)的工程化细胞、表达所述分子(例如重组受体)的多种工程化细胞与另外的药剂、疗法或治疗同时、并行或以任何顺序依次给予,其中这种给予在受试者体内提供每种药剂的治疗有效水平。可以将药剂与本文所述的结合分子(例如CCT5结合分子)、重组受体、细胞和/或组合物共给予,例如作为同一药物组合物的一部分或使用相同的递送方法来共给予。在一些实施方案中,在给予细胞之前,将另外的药剂与所述工程化细胞(例如,CAR表达细胞)一起孵育。
在一些例子中,在给予本文所述的结合分子(例如CCT5结合分子)、重组受体、细胞和/或组合物之后或之前(相隔所选时间段),给予所述一种或多种另外的药剂。在一些例子中,所述时间段是1天、2天、3天、4天、5天、6天、1周、2周、3周、1个月、2个月或3个月。在一些例子中,多次给予所述一种或多种另外的药剂和/或多次给予本文所述的结合分子(例如CCT5结合分子)、重组受体、细胞和/或组合物。例如,在一些实施方案中,在本文所述的结合分子(例如CCT5结合分子)、重组受体、细胞和/或组合物之前,例如在给予前两周、12天、10天、8天、1周、6天、5天、4天、3天、2天或1天,给予另外的药剂。例如,在一些实施方案中,在本文所述的结合分子(例如CCT5结合分子)、重组受体、细胞和/或组合物之后,例如在给予后两周、12天、10天、8天、1周、6天、5天、4天、3天、2天或1天,给予另外的药剂。
另外的药剂的剂量可以是任何治疗有效量,例如本文所述的任何剂量的量,并且另外的药剂的适当剂量可以取决于待治疗疾病的类型,所给予的结合分子、重组受体、细胞和/或组合物的类型、剂量和/或频率,疾病的严重程度和病程,给予结合分子、重组受体、细胞和/或组合物是出于预防目的还是治疗目的,先前疗法,患者的临床病史和对结合分子、重组受体、细胞和/或组合物的反应,以及主治医师的决断。可以将结合分子、重组受体、细胞和/或组合物和/或另外的药剂和/或疗法一次给予至患者、重复地给予或经一系列治疗来给予。
C.诊断和检测方法
还提供了涉及在检测CCT5中,例如在与表达CCT5的疾病或病症相关的诊断和/或预后方法中使用所提供的结合分子(例如抗体或其抗原结合片段)的方法。在一些实施方案中,所述方法包括将生物样品与抗体或其抗原结合片段一起孵育和/或将抗体或其抗原结合片段给予至受试者。在某些实施方案中,生物样品包括细胞或组织,如肿瘤或癌症组织。在某些实施方案中,接触是在允许抗CCT5抗体与CCT5结合并检测在抗CCT5抗体与CCT5之间是否形成复合物的条件下进行。这样的方法可以是体外或体内方法。在一个实施方案中,将抗CCT5抗体(例如抗原结合片段)用于选择有资格进行用抗CCT5抗体(例如抗原结合片段)或重组受体的疗法的受试者,例如其中CCT5是用于选择患者的生物标记。
在一些实施方案中,使样品(如细胞、组织样品、裂解物、组合物或源自其的其他样品)与抗CCT5抗体(例如抗原结合片段)接触,并且确定或检测在抗体与样品(例如样品中的CCT5)之间的结合或复合物的形成。当与相同组织类型的参考细胞相比证明或检测到测试样品中的结合时,这可能指示存在相关疾病或病症。在一些实施方案中,样品来自人组织。
可以使用已知用于检测特异性抗体-抗原结合的各种方法。示例性免疫测定包括荧光偏振免疫测定(FPIA)、荧光免疫测定(FIA)、酶免疫测定(EIA)、比浊法抑制免疫测定(NIA)、酶联免疫吸附测定(ELISA)和放射免疫测定(RIA)。可以将指示剂部分或标记基团附接到所述主题抗体上并进行选择以满足所述方法的各种应用的需要,所述各种应用通常由测定设备的可用性和相容的免疫测定程序决定。示例性标签包括放射性核素(例如
出于诊断目的,可以用可检测部分标记抗体(例如抗原结合片段),所述可检测部分包括但不限于放射性同位素、荧光标签和各种其他酶-底物标签。将标记与抗体缀合的方法是已知的。
在一些实施方案中,不需要对抗体(例如抗原结合片段)进行标记,并且可以使用与抗体结合的经标记的抗体来检测所述抗体的存在。
在一些实施方案中,所提供的抗体(例如抗原结合片段)可以用于任何已知的测定方法,如竞争性结合测定、直接和间接夹心测定和免疫沉淀测定。Zola,MonoclonalAntibodies:A Manual of Techniques,第147-158页(CRC Press,Inc.1987)。
抗体(例如抗原结合片段)和多肽也可以用于体内诊断测定(如体内成像)。通常,将抗体用放射性核素(如
抗体(例如抗原结合片段)也可以在例如使用已知技术的病理学中用作染色试剂。
IV.制品或试剂盒
还提供制品或试剂盒,所述制品或试剂盒含有所提供的结合分子(例如抗体)、重组受体(例如CAR)、基因工程化细胞和/或包含上述各项的组合物。所述制品可以包括容器和在所述容器上或与所述容器相关的标签或包装插页。合适的容器包括例如瓶子、小瓶、注射器、试管、IV输液袋等。容器可以由多种材料(如玻璃或塑料)形成。在一些实施方案中,容器具有无菌入口。示例性容器包括静脉输液袋、小瓶,包括具有可被注射针刺穿的塞子的那些。所述制品或试剂盒可以进一步包括包装插页,其指示所述组合物可以用于治疗特定病症如本文所述的病症(例如多发性骨髓瘤)。可替代地或另外地,所述制品或试剂盒可以进一步包括另一个或相同的包含药学上可接受的缓冲液的容器。它可以进一步包括其他材料,如其他缓冲液、稀释剂、过滤器、针和/或注射器。
标签或包装插页可以指示所述组合物用于治疗个体中表达CCT5的或CCT5相关的疾病、障碍或病症。在容器上或与容器相关的标签或包装插页可以指示关于重构和/或使用配制品的指导说明。标签或包装插页可以进一步指示所述配制品可用于或旨在用于皮下、静脉内或其他方式的给予以治疗或预防个体中表达CCT5的或CCT5相关的疾病、障碍或病症。
在一些实施方案中,容器容纳组合物本身或组合物与可有效治疗、预防和/或诊断病症的另一种组合物的组合。所述制品或试剂盒可以包括(a)在其中含有组合物(即第一药物)的第一容器,其中所述组合物包含抗体(例如抗CCT5抗体)或其抗原结合片段或重组受体(例如CAR);和(b)在其中含有组合物(即第二药物)的第二容器,其中所述组合物包含另外的药剂(如细胞毒性剂或其他治疗剂),并且所述制品或试剂盒进一步包含在标签或包装插页上的用于采用有效量的所述第二药物治疗受试者的说明书。
V.定义
除非另有定义,否则本文使用的所有技术术语、符号和其他技术和科学术语或用辞旨在具有与所要求保护的主题所属领域的普通技术人员通常理解的含义相同的含义。在一些情况下,为了清楚和/或为了便于引用而在本文中定义具有通常理解的含义的术语,并且本文中包含此类定义不一定应当被解释为代表与本领域通常所理解的含义有实质性差异。
如本文所用,提及抗体的“相应形式”意指当比较两种抗体的特性或活性时,使用相同形式的抗体来比较特性。例如,如果声明抗体与第一抗体的对应形式的活性相比具有更高的活性,则意味着特定形式(如所述抗体的scFv)与第一抗体的scFv形式相比具有更高的活性。
“效应子功能”是指可归因于抗体Fc区的那些生物活性,其随抗体同种型的变化而变化。抗体效应子功能的例子包括:C1q结合和补体依赖性细胞毒性(CDC);Fc受体结合;抗体依赖性细胞介导的细胞毒性(ADCC);吞噬作用;细胞表面受体(例如,B细胞受体)的下调;和B细胞激活。
本文中的术语“Fc区”用于定义免疫球蛋白重链的含有恒定区的至少一部分的C末端区。所述术语包括天然序列Fc区和变体Fc区。在一个实施方案中,人IgG重链Fc区从Cys226或从Pro230延伸至重链的羧基末端。然而,Fc区的C末端赖氨酸(Lys447)可以存在或可以不存在。除非本文另有说明,否则Fc区或恒定区中氨基酸残基的编号是根据EU编号系统(也称为EU索引),如Kabat等人,Sequences of Proteins of Immunological Interest,第5版Public Health Service,National Institutes of Health,B贝塞斯达,马里兰州,1991中所述。
术语“全长抗体”、“完整抗体”和“全抗体”在本文中可互换地使用以指代具有与天然抗体结构基本上相似的结构或具有含有如本文所定义的Fc区的重链的抗体。
“分离的”抗体是已经与其天然环境的组分分开的抗体。在一些实施方案中,如通过例如电泳(例如,SDS-PAGE、等电聚焦(IEF)、毛细管电泳)或色谱(例如,离子交换或反相HPLC)确定的,将抗体纯化至大于95%或99%的纯度。关于评估抗体纯度的方法的综述,参见例如Flatman等人,J.Chromatogr.B 848:79-87(2007)。
“分离的”核酸是指已经与其天然环境的组分分开的核酸分子。分离的核酸包括细胞中含有的核酸分子,所述细胞通常含有所述核酸分子,但所述核酸分子存在于染色体外或存在于不同于其天然染色体位置的染色体位置。
“编码抗CCT5抗体的分离的核酸”是指编码抗体重链和轻链(或其片段)的一种或多种核酸分子,包括在单个载体或单独载体中这样的一种或多种核酸分子、以及在宿主细胞中的一个或多个位置存在的这样的一种或多种核酸分子。
术语“宿主细胞”、“宿主细胞系”和“宿主细胞培养物”可互换使用,并且是指已引入外源核酸的细胞,包括此类细胞的后代。宿主细胞包括“转化体”和“转化细胞”,其包括原代转化细胞和源自其的后代,不考虑传代次数。后代在核酸含量上可能与亲代细胞不完全相同,但可能含有突变。本文包括如在初始转化细胞中所筛选或选择的,具有相同功能或生物活性的突变体后代。
术语“多肽”和“蛋白质”可互换使用以指代氨基酸残基的聚合物,并且不限于最小长度。多肽(包括所提供的抗体和抗体链以及其他肽(例如,接头和CCT5结合肽))可以包括含有天然和/或非天然氨基酸残基的氨基酸残基。所述术语还包括多肽的表达后修饰,例如糖基化、唾液酸化、乙酰化、磷酸化等。在一些方面,多肽可以含有关于原生或天然序列的修饰,只要蛋白质保持所需活性即可。这些修饰可能是故意的(如通过定点诱变),或者可能是偶然的(如通过产生蛋白质的宿主的突变或由于PCR扩增引起的错误)。
如本文所用,在关于氨基酸序列(参考多肽序列)使用时,“氨基酸序列同一性百分比(%)”和“同一性百分比”和“序列同一性”被定义为,在比对序列并在必要时引入空位以实现最大序列同一性百分比并且不将任何保守取代视作序列同一性的一部分之后,候选序列(例如,主题抗体或片段)中与参考多肽序列中的氨基酸残基相同的氨基酸残基的百分比。用于确定氨基酸序列同一性百分比的比对可以以多种方式来实现,如使用公众可获得的计算机软件,如BLAST、BLAST-2、ALIGN或Megalign(DNASTAR)软件。可以确定用于比对序列的适当参数,包括在所比较序列的全长上实现最大比对所需的任何算法。
氨基酸取代可以包括用另一种氨基酸替代多肽中的一个氨基酸。可以将氨基酸取代引入目的结合分子(例如抗体)和针对所需活性(例如,保留/改善的抗原结合、降低的免疫原性或改善的ADCC或CDC)筛选的产物中。
通常可以根据以下常见的侧链特性将氨基酸进行分组:
(1)疏水性的:正亮氨酸、Met、Ala、Val、Leu、Ile;
(2)中性亲水性的:Cys、Ser、Thr、Asn、Gln;
(3)酸性的:Asp、Glu;
(4)碱性的:His、Lys、Arg;
(5)影响链取向的残基:Gly、Pro;
(6)芳香族的:Trp、Tyr、Phe。
非保守氨基酸取代将涉及将这些类别之一的成员与另一个类别交换。
如本文所用,术语“载体”是指能传播其所连接的另一核酸分子的核酸分子。所述术语包括作为自我复制核酸结构的载体以及掺入已引入其的宿主细胞的基因组中的载体。某些载体能够引导它们可操作地连接的核酸的表达。此类载体在本文中称为“表达载体”。
术语“包装插页”用于指通常包括在治疗产品的商业包装中的说明书,所述说明书包含关于使用此类治疗产品的适应症、用法、剂量、给予、组合疗法、禁忌症和/或警告的信息。
除非上下文另有明确规定,否则如本文所用,单数形式“一种/一个”(“a”)、“一种/一个”(“an”)和“所述”(“the”)包括复数指示物。例如,“一种/一个”(“a”)或“一种/一个”(“an”)意指“至少一种/至少一个”或“一种或多种/一个或多个”。应理解,本文所述的方面、实施方案和变化包括“包含”方面、实施方案和变化、“由方面、实施方案和变化组成”和/或“本质上由方面、实施方案和变化组成”。
在整个本公开文本中,所要求保护的主题的各个方面以范围形式呈现。应当理解,范围形式的描述仅仅是为了方便和简洁,并且不应被解释为对所要求保护的主题的范围的僵硬限制。因此,应当将范围的描述视为已明确公开所有可能的子范围以及该范围内的单独数值。例如,在提供值的范围的情况下,应理解,该范围的上限与下限之间的每个中间值以及该所陈述范围中的任何其他所陈述值或中间值涵盖在所要求保护的主题内。这些较小范围的上限和下限可以独立地被包括在所述较小范围内,并且也涵盖在所要求保护的主题内,受制于在所陈述范围内任何明确排除的限值。在所陈述范围包括所述限值中的一个或两个的情况下,排除那些所包括限值中的任何一个或两个的范围也被包括在所要求保护的主题内。无论范围的广度如何,这都适用。
如本文所用的术语“约”是指本技术领域的技术人员容易知道的相应值的常用误差范围。本文提及“约”某一值或参数时包括(并描述)涉及该值或参数本身的实施方案。例如,提及“约X”的描述包括“X”的描述。
如本文所用,“组合物”是指两种或更多种产物、物质或化合物(包括细胞)的任何混合物。其可以是溶液、悬浮液、液体、粉末、糊剂、水性、非水性或其任何组合。
如本文所用,细胞或细胞群针对特定标记呈“阳性”的陈述是指,特定标记(通常是表面标记)在细胞上或细胞中的可检测存在。当提及表面标记时,所述术语是指如通过流式细胞术检测到的,表面表达的存在,例如通过用与所述标记特异性地结合的抗体进行染色并检测所述抗体,其中所述染色通过流式细胞术以如下水平是可检测的,所述水平基本上高于在其他方面相同的条件下用同种型匹配对照进行相同程序检测到的染色,和/或所述水平基本上与已知呈所述标记阳性的细胞的水平相似,和/或所述水平基本上高于已知呈所述标记阴性的细胞的水平。
如本文所用,细胞或细胞群对特定标记呈“阴性”的陈述是指,特定标记(通常是表面标记)在细胞上或细胞中不存在基本上可检测的存在。当提及表面标记时,所述术语是指如通过流式细胞术检测到的,表面表达的不存在,例如通过用与所述标记特异性地结合的抗体进行染色并检测所述抗体,其中所述染色通过流式细胞术以如下水平没有检测到,所述水平基本上高于在其他方面相同的条件下用同种型匹配对照进行相同程序检测到的染色,和/或所述水平基本上低于已知呈所述标记阳性的细胞的水平,和/或所述水平与已知呈所述标记阴性的细胞的水平相比是基本上相似的。
VI.示例性实施方案
所提供的实施方案包括:
1.1.一种抗体或其抗原结合片段,其中所述抗体或抗原结合片段特异性地结合包含SEQ ID NO:68(X
2.一种抗体或其抗原结合片段,其中所述抗体或抗原结合片段特异性地结合为如下肽序列或在如下肽序列内含有的表位,所述肽序列在SEQ ID NO:68(X
3.根据实施方案1或实施方案2所述的抗体或抗原结合片段,其中X
4.根据实施方案1-3中任一项所述的抗体或抗原结合片段,其中所述肽序列由序列TSVEDYKA(SEQ ID NO:70)、SSVEAFKR(SEQ ID NO:71)或DSVEAIKA(SEQ ID NO:72)组成。
5.根据实施方案1-4中任一项所述的抗体或抗原结合片段,其中所述抗体或抗原结合片段包含:
重链可变(V
轻链可变(V
6.一种抗体或其抗原结合片段,其中所述抗体或抗原结合片段包含:
重链可变(V
轻链可变(V
7.根据实施方案1-6中任一项所述的抗体或抗原结合片段,其中:
所述V
所述V
8.根据实施方案1-7中任一项所述的抗体或抗原结合片段,其中:
所述V
所述V
9.一种抗体或其抗原结合片段,其包含:
重链可变(V
轻链可变(V
10.根据实施方案1-9中任一项所述的抗体或其抗原结合片段,其中:
所述V
所述V
11.一种抗体或其抗原结合片段,其中所述抗体或抗原结合片段包含:
重链可变(V
轻链可变(V
12.根据实施方案1-11中任一项所述的抗体或其抗原结合片段,所述抗体或其抗原结合片段包含V
13.根据实施方案1-12中任一项所述的抗体或抗原结合片段,其中所述V
14.根据实施方案1-13中任一项所述的抗体或抗原结合片段,其中所述V
15.根据实施方案1-14中任一项所述的抗体或抗原结合片段,其中所述抗体或其抗原结合片段的V
16.一种抗体或抗原结合片段,其中所述抗体或抗原结合片段特异性地结合与由根据实施方案6-15中任一项所述的抗体或抗原结合片段特异性地结合的表位相同或重叠的表位。
17.一种抗体或抗原结合片段,其中所述抗体或抗原结合片段竞争结合CCT5或SEQID NO:68(X
18.根据实施方案1-17中任一项所述的抗体或抗原结合片段,其中所述抗体或抗原结合片段特异性地结合含TCP1伴侣蛋白亚基5(CCT5)蛋白。
19.根据实施方案17或实施方案18所述的抗体或抗原结合片段,其中所述CCT5蛋白是人CCT5蛋白、小鼠CCT5蛋白或非人灵长类CCT5蛋白。
20.根据实施方案17-19中任一项所述的抗体或抗原结合片段,其中所述CCT5蛋白是人CCT5蛋白。
21.根据实施方案17-20中任一项所述的抗体或抗原结合片段,其中所述CCT5包含SEQ ID NO:45或46中所示的序列或展现出与SEQ ID NO:45或46至少或约至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或更高序列同一性的氨基酸序列。
22.根据实施方案17-22中任一项所述的抗体或抗原结合片段,其中所述CCT5蛋白包含SEQ ID NO:45或46中所示的氨基酸序列。
23.根据实施方案6-22中任一项所述的抗体或抗原结合片段,其中所述抗体或抗原结合片段特异性地结合SEQ ID NO:68(X
24.根据实施方案17或实施方案23所述的抗体或抗原结合片段,其中X
25.根据实施方案17、实施方案23或实施方案24所述的抗体或抗原结合片段,其中所述肽序列由序列TSVEDYKA(SEQ ID NO:70)、SSVEAFKR(SEQ ID NO:71)或DSVEAIKA(SEQID NO:72)组成。
26.根据实施方案1-25中任一项所述的抗体或抗原结合片段,其中所述抗体或抗原结合片段是人的。
27.根据实施方案1-26中任一项所述的抗体或其抗原结合片段,其中所述抗体是人抗体。
28.根据实施方案26或实施方案27所述的抗体或抗原结合片段,其中:
所述抗体或抗原结合片段包含重链可变(V
所述抗体或抗原结合片段包含轻链可变(V
29.根据实施方案26-28中任一项所述的抗体或抗原结合片段,其中:
所述CDR-H1和/或CDR-H2包含分别与由种系核苷酸人重链V区段编码的序列内的CDR-H1和/或CDR-H2的氨基酸序列相比为100%相同或具有不多于一个氨基酸差异的序列;和/或
所述CDR-L1和/或CDR-L2包含分别与由种系核苷酸人κ或λv区段编码的序列内的CDR-L1和/或CDR-L2的氨基酸序列相比为100%相同或具有不多于一个氨基酸差异的序列。
30.根据实施方案1-29中任一项所述的抗体或抗原结合片段,其中所述抗体或抗原结合片段是重组的。
31.根据实施方案1-30中任一项所述的抗体或抗原结合片段,其中所述抗体或抗原结合片段是单克隆的。
32.根据实施方案1-31中任一项所述的抗体或抗原结合片段,所述抗体或抗原结合片段是抗原结合片段。
33.根据实施方案1-32中任一项所述的抗体或抗原结合片段,所述抗体或抗原结合片段是单链片段。
34.根据实施方案32或实施方案33所述的抗体或抗原结合片段,其中所述片段包含scFv。
35.根据实施方案32-34中任一项所述的抗体或抗原结合片段,其中所述V
36.根据实施方案32-34中任一项所述的抗体或抗原结合片段,其中所述V
37.根据实施方案32-36中任一项所述的抗体或抗原结合片段,所述抗体或抗原结合片段是包含通过柔性接头连接的抗体V
38.根据实施方案34-37中任一项所述的抗体或抗原结合片段,其中所述scFv包含含有氨基酸序列GGGGSGGGGSGGGGS(SEQ ID NO:49)的接头。
39.根据实施方案34-38中任一项所述的抗体或抗原结合片段,其中所述scFv包含SEQ ID NO:52中所示的氨基酸序列,或与SEQ ID NO:52中所示的氨基酸序列具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性的氨基酸序列。
40.根据实施方案1-39中任一项所述的抗体或抗原结合片段,所述抗体或抗原结合片段进一步包含免疫球蛋白恒定区的至少一部分。
41.根据实施方案1-31和40中任一项所述的抗体或抗原结合片段,所述抗体或抗原结合片段是全抗体或完整抗体。
42.根据实施方案1-41中任一项所述的抗体或抗原结合片段,所述抗体或抗原结合片段是双特异性抗体。
43.根据实施方案42所述的抗体或抗原结合片段,所述抗体或抗原结合片段进一步特异性地结合第二抗原。
44.根据实施方案43所述的抗体或抗原结合片段,其中所述第二抗原表达于肿瘤细胞上、任选地表达或异常表达CCT5的肿瘤细胞上,或T细胞上。
45.根据实施方案43或实施方案44所述的抗体或抗原结合片段,其中所述第二抗原在肿瘤细胞上表达,并且所述肿瘤细胞是上皮细胞癌的肿瘤细胞。
46.根据实施方案43或实施方案44所述的抗体或抗原结合片段,其中所述第二抗原在T细胞抗原上表达,并且所述T细胞抗原是CD2或CD3。
47.一种单链细胞表面蛋白,其包含根据实施方案1-46中任一项所述的抗体或抗原结合片段、和任选的跨膜结构域。
48.一种单链细胞表面蛋白,其包含特异性地结合CCT5的抗体或抗原结合片段、和任选的跨膜结构域。
49.根据实施方案47或实施方案48所述的单链细胞表面蛋白,所述单链细胞表面蛋白是抗原结合片段,任选地scFv。
50.根据实施方案49所述的单链细胞表面蛋白,其中所述抗原结合片段是scFv,并且所述scFv包含SEQ ID NO:52中所示的氨基酸序列或者展现出与SEQ ID NO:52至少85%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性并且结合CCT5或结合包含SEQ ID NO:68所示序列的肽、任选地SEQ ID NO:70-72中任一个所示的肽的氨基酸序列。
51.一种缀合物,其包含根据实施方案1-46中任一项所述的抗体或抗原结合片段以及异源分子或异源部分。
52.一种缀合物,其包含特异性地结合CCT5的抗体或抗原结合片段以及异源分子或异源部分。
53.根据实施方案51或实施方案52所述的缀合物,其中所述异源分子或异源部分是蛋白质、肽、核酸或小分子。
54.根据实施方案51-53中任一项所述的缀合物,其中所述异源分子或异源部分是细胞毒性剂、毒素、放射性同位素、化学治疗剂、裂解肽或细胞因子。
55.根据实施方案51-54中任一项所述的缀合物,其中所述抗体或抗原结合片段和部分直接连接或经由接头间接连接。
56.根据实施方案51-55中任一项所述的缀合物,其中所述抗体或抗原结合片段和所述部分共价或化学连接。
57.根据实施方案51-55中任一项所述的缀合物,其中所述部分是蛋白质或肽,并且所述缀合物是融合蛋白。
58.一种嵌合抗原受体(CAR),其包含细胞外部分和细胞内信号传导区,所述细胞外部分含有根据实施方案1-46中任一项所述的抗体或抗原结合片段。
59.一种嵌合抗原受体(CAR),其包含细胞外部分和细胞内信号传导区,所述细胞外部分含有特异性地结合CCT5的抗体或抗原结合片段。
60.根据实施方案58或实施方案59所述的嵌合抗原受体,其中所述细胞外部分包含抗原结合片段,并且所述抗原结合片段是scFv。
61.根据实施方案60所述的嵌合抗原受体,其中所述scFv包含SEQ ID NO:52中所示的氨基酸序列或者展现出与SEQ ID NO:52至少85%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性并且结合CCT5或结合包含SEQ ID NO:68所示序列的肽、任选地SEQ ID NO:70-72中任一个所示的肽的氨基酸序列。
62.根据实施方案58-61中任一项所述的嵌合抗原受体,其中所述细胞内信号传导区是或包含初级信号传导结构域、能够在T细胞中诱导初级激活信号的信号传导结构域、T细胞受体(TCR)组分的信号传导结构域、和/或包含基于免疫受体酪氨酸的激活基序(ITAM)的信号传导结构域。
63.根据实施方案62所述的嵌合抗原受体,其中所述细胞内信号传导区是或包含CD3链任选地CD3-zeta(CD3ζ)链的细胞内信号传导结构域或其信号传导部分。
64.根据实施方案58-63中任一项所述的嵌合抗原受体,其中所述CAR进一步包含设置在所述细胞外结构域与所述细胞内信号传导区之间的跨膜结构域。
65.根据实施方案64所述的嵌合抗原受体,其中所述跨膜结构域包含CD28的跨膜部分。
66.根据实施方案58-65中任一项所述的嵌合抗原受体,其中所述细胞内信号传导区进一步包含共刺激信号传导结构域。
67.根据实施方案66所述的嵌合抗原受体,其中所述共刺激信号传导结构域包含T细胞共刺激分子的细胞内信号传导结构域或其信号传导部分。
68.根据实施方案66或实施方案67所述的嵌合抗原受体,其中所述共刺激信号传导结构域包含CD28、4-1BB或ICOS的细胞内信号传导结构域或其信号传导部分。
69.根据实施方案66-68中任一项所述的嵌合抗原受体,其中所述共刺激信号传导结构域包含4-1BB的细胞内信号传导结构域或其信号传导部分。
70.根据实施方案66-69中任一项所述的嵌合抗原受体,其中所述共刺激信号传导结构域位于所述跨膜结构域与所述细胞内信号传导结构域之间。
71.一种多核苷酸,其编码根据实施方案1-46中任一项所述的抗体或其抗原结合片段、根据实施方案47-50中任一项所述的单链细胞表面蛋白、根据实施方案51-57中任一项所述的缀合物或根据实施方案58-70中任一项所述的嵌合抗原受体。
72.根据实施方案71所述的多核苷酸,所述多核苷酸进一步编码信号序列,任选地其中所述信号序列是GM-CSF信号序列、CD8信号序列、Igκ信号序列或CD33信号序列。
73.一种载体,其包含根据实施方案71或实施方案72所述的多核苷酸。
74.根据实施方案73所述的载体,其中所述载体是表达载体。
75.根据实施方案73或实施方案74所述的载体,其中所述载体是病毒载体。
76.根据实施方案75所述的载体,其中所述病毒载体是逆转录病毒载体。
77.根据实施方案75或实施方案76所述的载体,其中所述病毒载体是慢病毒载体。
78.根据实施方案77所述的载体,其中所述慢病毒载体源自HIV-1。
79.一种工程化细胞,其包含根据实施方案73-78中任一项所述的载体。
80.一种工程化细胞,其表达包含根据实施方案1-46中任一项所述的抗体或抗原结合片段的受体、根据实施方案47-50中任一项所述的单链细胞表面蛋白、根据实施方案51-57中任一项所述的缀合物或根据实施方案58-70中任一项所述的嵌合抗原受体。
81.根据实施方案79或实施方案80所述的工程化细胞,其中所述细胞是免疫细胞。
82.根据实施方案81所述的工程化细胞,其中所述免疫细胞是T细胞。
83.根据实施方案82所述的工程化细胞,其中所述T细胞是CD4+ T细胞或CD8+ T细胞。
84.根据实施方案79或实施方案80所述的工程化细胞,其中所述细胞是诱导多能干细胞(iPS细胞)。
85.根据实施方案79-84中任一项所述的工程化细胞,其进一步包含为嵌合共刺激受体的另一基因工程化抗原受体,所述嵌合共刺激受体特异性地结合另一抗原并且能够将共刺激信号诱导至所述细胞,任选地其中所述另一抗原在与CCT5所在的相同的细胞上表达或是肿瘤抗原。
86.根据实施方案79-85中任一项所述的工程化细胞,其进一步包含为抑制性嵌合抗原受体的另一基因工程化抗原受体,所述抑制性嵌合抗原受体特异性地结合另一抗原并且在识别所述第二抗原后能够将抑制性或免疫抑制性或阻遏信号诱导至所述细胞,任选地其中所述第二抗原在正常细胞上表达或在前列腺或乳腺上皮细胞上表达。
87.一种组合物,其包含根据实施方案1-46中任一项所述的抗体或其抗原结合片段、根据实施方案47-50中任一项所述的单链细胞表面蛋白、根据实施方案51-57中任一项所述的缀合物、根据实施方案58-70中任一项所述的嵌合抗原受体或根据实施方案71-86中任一项所述的工程化细胞。
88.根据实施方案87所述的组合物,其进一步包含药学上可接受的赋形剂。
89.一种治疗方法,其包括将根据实施方案1-46中任一项所述的抗体或其抗原结合片段、根据实施方案47-50中任一项所述的单链细胞表面蛋白、根据实施方案51-57中任一项所述的缀合物、根据实施方案58-70中任一项所述的嵌合抗原受体、根据实施方案71-86中任一项所述的工程化细胞或根据实施方案87或实施方案88所述的组合物给予至患有疾病或障碍的受试者。
90.一种治疗方法,所述方法包括向受试者给予特异性地结合CCT5的包含抗体或抗原结合片段的结合分子以用于治疗疾病或障碍。
91.根据实施方案90所述的方法,其中所述结合分子是缀合物、任选地抗体-药物缀合物(ADC)。
92.根据实施方案90所述的方法,其中所述结合分子是嵌合抗原受体,并且向所述受试者给予表达所述嵌合抗原受体的工程化细胞。
93.根据实施方案89-92中任一项所述的治疗方法,其中所述疾病或障碍与CCT5、任选地异常表达的CCT5、任选地表面CCT5或膜定位的CCT5相关。
94.根据实施方案89-93中任一项所述的治疗方法,其中所述疾病或障碍是肿瘤或癌症。
95.根据实施方案89-94中任一项所述的治疗方法,其中所述疾病或障碍是白血病、淋巴瘤、或实体瘤,任选地肉瘤或上皮恶性肿瘤。
96.根据实施方案89-95中任一项所述的治疗方法,其中所述疾病或病症是胰腺癌、膀胱癌、结直肠癌、乳腺癌、前列腺癌、肾癌、肝细胞癌、肺癌、卵巢癌、宫颈癌、胰腺癌、直肠癌、甲状腺癌、子宫癌、胃癌、食道癌、头颈癌、黑色素瘤、神经内分泌癌、CNS癌症、脑肿瘤、骨癌或软组织肉瘤。
97.根据实施方案89-96中任一项所述的治疗方法,其中所述疾病或障碍是上皮恶性肿瘤或上皮细胞癌。
98.根据实施方案96所述的治疗方法,其中所述上皮恶性肿瘤或上皮细胞癌选自鳞状细胞癌(皮肤)、基底细胞癌、胃癌、腺癌、腺鳞癌、间变性癌、移行细胞癌、大细胞癌、小细胞癌、肝细胞癌、肾细胞癌、子宫内膜癌、浸润性乳腺癌、或癌转移。
99.根据实施方案89-98中任一项所述的治疗方法,其中所述疾病或病症是结肠癌、乳腺癌、卵巢癌、前列腺癌、胰腺癌、膀胱癌、或肺癌。
VII.实施例
以下实施例被包括在内仅用于说明目的,并不旨在限制本发明的范围。
肿瘤浸润淋巴细胞(TIL)收获自胰腺癌患者,并且使用基于阴性选择的人B细胞富集试剂盒(Stem Cell Technologies)分离B细胞。然后使用IgG特异性引物使所选择的B细胞经历单细胞IgG测序,总体上如WO2016044227、WO 2016176322和WO 2012048340中所述,以确定从肿瘤分离的B细胞中IgG分子的配对可变重(VH)链和可变轻(VL)链的序列。
然后将所测序的抗体克隆、表达,并且使用表面和细胞内流式细胞术测试其与六种不同的癌症来源的细胞系(SK-BR-3、MiaPaCa2、Panc1、Panc10.05、SU8686、和BxPC3)的结合反应性。对癌细胞系展现出阳性反应性的示例性抗体含有SEQ ID NO:1中所示的可变重(VH)链(由SEQ ID NO:3中所示的核苷酸序列编码)和SEQ ID NO:2中所示的可变轻(VL)链(由SEQ ID NO:4中所示的核苷酸序列编码)。选择示例性抗体用于进一步研究。
实施例2:靶抗原的鉴定
A.进行免疫沉淀和质谱以鉴定候选靶蛋白
将示例性卵巢或白血病细胞系的全细胞裂解物与实施例1中鉴定出的抗体一起用于免疫沉淀实验。将所鉴定出的抗体与环氧树脂磁珠共价缀合,并且将10μg珠结合的抗体与卵巢癌细胞系(OvCar8)或急性髓性白血病细胞系(SKM1)的1-2mL全细胞裂解液(以1mg蛋白/mL裂解液)一起孵育。还将细胞裂解物与已知结合细胞系的对照抗体、或单独的珠一起孵育。然后洗涤免疫沉淀物,并且首先在低pH的情况下洗脱,其次用阳离子洗涤剂洗脱缓冲液洗脱。将洗脱液通过SDS-PAGE解析,并且用蛋白染色剂染色以可视化条带。
免疫沉淀产生多个条带。用所鉴定出的抗体在免疫沉淀中富集大约220kDa和70-80kDa的条带。将条带切除,用胰蛋白酶在凝胶中单独消化,并通过串联质谱进行分析。分析从每个样品产生的光谱以进行蛋白质鉴定。通过将光谱计数(每种蛋白质的总肽计数)相加来估计蛋白质丰度。在来自Ovcar8和SKM1裂解物的免疫沉淀中,选择了用实施例1中鉴定出的抗体富集的前10种蛋白质,以进行进一步评价。
B.通过免疫沉淀和蛋白质印记进行靶标验证
用OvCar8细胞以及SKBR3(乳腺癌)和MIAPACA2(胰腺癌)细胞系重复使用所鉴定出的抗体进行的免疫沉淀。将洗脱液通过SDS-PAGE解析、进行转移以使用对在A部分中鉴定出的如下前10种候选蛋白具有特异性的兔多克隆抗体进行蛋白质印迹分析:RalGapa2、RalGapB、SPTAN1、IMPDH2、DNAJC13、SPTAN1、SNRNP200、PRPF8、CCT4、和CCT2。在来自所有评估的癌细胞系的免疫沉淀物中特异性地检测到CCT2和CCT4。没有检测到对应于其他蛋白质的条带。CCT2和CCT4两者都是TCP1环复合物(TRiC)的一部分。
C.通过对总免疫沉淀洗脱液的质谱进行靶标验证
使用实施例1中鉴定出的抗体、具有已知靶标的对照抗体或单独的珠,通过SDS-PAGE解析来自OvCar8、MIAPaCa2、SKM-1和SKBR3细胞系的免疫沉淀洗脱液。将每个泳道分为两个部分,进行消化,并通过如上所述的串联质谱进行分析。在消除从单独的珠或对照抗体条件中鉴定出的肽后,确定由实施例1中鉴定出的抗体特异性富集的蛋白质。
用实施例1中鉴定出的抗体富集的大多数蛋白质是TRiC蛋白质复合物的一部分,这表明抗体特异性地免疫沉淀该复合物。
D.通过肽阵列进行靶标验证
采用使用覆盖所有人类蛋白质的肽阵列的肽阵列分析用于抗体特异性的分析(
E.通过ELISA进行靶标确认
将来自TriC环复合物的重组蛋白固定化并用实施例1中鉴定出的抗体或对照非靶标抗体探测。如图1A和图1B中所示,实施例1中鉴定出的抗体仅以剂量依赖性方式结合蛋白CCT5,但不结合来自复合物的任何其他蛋白。阴性对照抗体不结合来自TriC环复合物的任何固定化重组蛋白。
F.通过蛋白质印迹进行靶标确认
用实施例1中鉴定出的抗体、或阴性对照抗体帕尼单抗(Panitumumab)免疫沉淀后,通过针对CCT5的蛋白质印记探测SK-BR-3和OvCar3细胞的胞浆和质膜(表面)裂解物制剂。如图2中所示,在SK-BR-3的质膜和胞浆裂解物级分两者以及OvCar3中的质膜级分中,通过用来自实施例1的示例性抗体进行的免疫沉淀检测到TRiC蛋白CCT5。阴性对照抗体在SK-BR-3的胞浆裂解物级分中显示出轻微的CCT5检测,但在质膜裂解物级分中未检测到。
在EF1a启动子(SEQ ID NO:82)或MND启动子(SEQ ID NO:27)的调节下,将实施例1中鉴定出的示例性抗CCT5抗体的VH和VL链克隆到含有嵌合抗原受体(CAR)的编码序列的慢病毒骨架中。产生了六种形式的CAR,其包括VH和VL链的两种取向以及三种不同的间隔子,每种间隔子具有不同的长度。所编码的CAR含有抗原结合结构域,所述抗原结合结构域含有由(Gly
将含有在Nur77启动子控制下的编码红色荧光蛋白报告物的核酸的示例性Jurkat报告细胞系用于评估在各种条件下表达实施例3中描述的示例性CAR的T细胞的活性。
如实施例3中所述,用单独编码CAR构建体的慢病毒载体转导示例性Nur77报告细胞系的细胞的各种组合物。
用编码各种抗CCT5 CAR的慢病毒构建体转导报告T细胞,每种抗CCT5 CAR的不同之处在于细胞外间隔子,所述细胞外间隔子具有:IgG4铰链、IgG4铰链-CH3、或IgG4/IgG2铰链-IgG2/IgG4 CH2-IgG4 CH3。此外,还用有着具有IgG4/IgG2铰链-IgG2/IgG4 CH2-IgG4CH3(对照)的细胞外间隔子的抗EGFR CAR转导报告T细胞。所有构建体的表达均处于EF1a启动子下。将CAR表达报告细胞与抗体已显示对其具有反应性的肿瘤细胞系共培养。然后通过流式细胞术评估Nur77报告物和CD69的表面表达。对于每种条件,确定观察到对CD69的表面表达和Nur77报告物信号呈阳性的细胞的百分比(高于在用单独培养基培养的细胞(即无靶细胞)中观察到的百分比),以作为激活水平的指标。
观察到所有CAR表达Jurkat T细胞均响应于靶细胞数量增加展现出激活水平增加(如通过报告物和CD69水平指示的)。当孔达到汇合时,抗CCT5 CAR表达Jurkat细胞在每孔约20,000个靶细胞时展现出最大激活。表达具有IgG4铰链间隔子的抗CCT5 CAR的报告细胞展现出最高水平的激活。表达抗EGFR CAR的细胞在每孔2,500个靶细胞时实现100%激活。表达具有IgG4铰链间隔子的抗EGFR CAR的报告细胞在大约750个靶细胞/孔时接近100%激活。
将含有已被各种抗CCT5 CAR(各自在EF1a启动子的控制下表达)转导的细胞的Jurkat报告T细胞与各种细胞系或原代细胞一起孵育。使用流式细胞术确定报告物和CD69的表达。通过基于GFP表达和/或抗IgG染色的流式细胞术确定CAR阳性细胞。针对每种条件计算被检测为对表面CD69表达和报告物信号均为阳性的CAR表达细胞的百分比(以及该百分比高于对于在单独培养基中(即在没有靶细胞的情况下)培养的细胞所观察到的信号的差异)以作为激活的指标。
A.人细胞
将抗CCT5 CAR Jurkat报告细胞在96孔细胞培养板中与以下示例性人肿瘤细胞系一起孵育2天:乳腺癌(SK-BR-3、MCF7、HCC 1806、HCC 2218、BT549和MDA-MB-231)、胰腺癌(MIA PaCa-2、PANC-1、BxPC-3、SU86.86和Panc10.05)、卵巢癌(OVCAR-8、Caov-3、ES-2、NIH:OVCAR-3和OVCAR-4)、肺癌(A549、NCI-H1975、NCI H1299、NCI H1573和NCI H1915)、头颈部鳞状细胞癌(HNSCC;UPCI:SCC152)、宫颈癌(CaSki)、皮肤癌(SV-80)、急性髓性白血病(AML;Kasumi-1、SH-2、HT-93、HL60、ML-2、BDCM、KG-1、SKM-1、THP-1和OCI-M1)或慢性髓性白血病(CML;K-562)。在此实验中,粘附细胞在汇合时使用,并与转导的细胞一起孵育。对于非粘附细胞,使用目标1:1E:T比率。表达抗CCT5 CAR的Jurkat报吿细胞在与代表每种适应症的至少一种细胞系一起孵育后展现出应答。
在另一项研究中,将抗CCT5 CAR Jurkat报告细胞与如下正常人细胞一起孵育:原代皮肤成纤维细胞,人脐静脉细胞(HUVEC),胰腺内皮、脑内皮和一组上皮细胞样品,包括从表皮角质形成细胞、肾、乳腺、前列腺、宫颈、结肠、胰腺、卵巢表面、肺泡和食道产生的样品。也将抗CCT5 CAR Jurkat报告细胞与从健康人供体获得的原代细胞一起孵育,所述原代细胞包括来自单采术样品的细胞、来自单采术样品的外周血单核细胞(PBMC)、或CD4+ T细胞、CD8+ T细胞或来自已经通过基于免疫亲和力的选择富集的阴性血液级分的细胞(例如CD4-和CD8-T细胞)。在此测定中,当与十种人原代上皮细胞样品中的六种(包括表皮角质形成细胞和乳腺、前列腺、宫颈、结肠和卵巢表面上皮细胞)一起孵育时,在CAR表达T细胞中观察到表面CD69和Nur77报告物信号的增加。没有观察到CAR表达T细胞对测试的其他人细胞的活性。
B.非人细胞
在进一步的研究中,在B16-F10(黑色素瘤)细胞中,还通过免疫沉淀和蛋白质印迹确认了抗CCT5抗体与鼠类CCT5的结合。为了进一步评估与鼠类细胞的结合,将已经转导为表达抗CCT5 CAR的Jurkat报告细胞与示例性鼠类细胞系一起孵育,所述示例性鼠类细胞系包括:原代小鼠肾上皮细胞、原代小鼠乳腺上皮细胞和A20(B淋巴瘤)、CT26(结肠)、LL/2(肺)、B16-F10(黑色素瘤)、B16-F1(黑色素瘤)、NIH3T3(胚胎成纤维细胞)、ID8(卵巢)和EpH4-1424(乳腺上皮肿瘤)永生小鼠系。在此报告物测定中,在与各种评估的靶细胞一起孵育后,未观察到增加的报告物信号(与未与靶细胞一起孵育的含CAR Jurkat细胞相比),或观察到低水平增加的报告物信号。
还将上述抗CCT5 CAR Jurkat报告细胞与示例性非人灵长类(NHP)细胞一起孵育,所述示例性非人灵长类细胞包括4MBr-5恒河猴(Macaca mulatta)肺上皮细胞系和一组食蟹猴(Macaca fascicularis)原代上皮细胞样品,包括从肾、小气道和大气道上皮细胞产生的那些。仅与4MBr-5或食蟹猴肾上皮细胞相比,在与食蟹猴小气道和大气道上皮细胞一起孵育后,观察到明显更高的报告物信号。这些结果与抗CCT5 CAR表达细胞展现出对某些非人细胞的一些反应性的发现是一致的。
响应于来自TRiC环的其他成员,测试了抗CCT5 CAR表达T细胞的激活。如以上在实施例4中所述,将已经用各种抗CCT5 CAR转导的Jurkat报告T细胞铺板在未包被的孔中或含有来自TRiC环复合物的固定化重组蛋白(CCT1、CCT2、CCT3、CCT4、CCT5、CCT8和CCTr1)的孔中。通过流式细胞术确定基于GFP表达的报告物和CAR阳性细胞的表达。仅与重组CCT5一起孵育产生高于基线的抗CCT5 CAR表达报告T细胞的激活。
通过共聚焦荧光显微镜,对在实施例5中产生抗CCT5 CAR活性(如通过报告物/CD69水平所确定)的来自乳腺癌细胞系的细胞以及在实施例5中表达抗CCT5 CAR的报告T细胞不产生应答的卵巢癌细胞系检查CCT5定位。使用多克隆抗CCT5抗体检测CCT5,用麦胚凝集素(WGA)标记膜,并且使用DAPI(4',6-二脒基-2-苯基吲唑)鉴定细胞核。在实施例5中未观察到抗CCT5 CAR产生应答的细胞展现出CCT5的弥漫性胞质定位和/或核周定位。诱导来自抗CCT5 CAR细胞的应答的细胞展现出增加的CCT5染色,所述染色呈小聚集体形式分布,所述小聚集体可能与整个细胞表面上的膜相关或定位于所述膜上。在这些细胞中还观察到了CCT5的一些弥漫性胞质染色。
将来自人供体的原代人T细胞(CD4+和CD8+ T细胞)用如实施例3中所述产生的编码抗CCT5 CAR的慢病毒构建体进行刺激和转导,所述慢病毒构建体包括在EF1a或MND启动子的调节下的构建体,并且所述抗CCT5 CAR具有IgG4铰链间隔子、IgG4铰链-CH3间隔子、或IgG4/IgG2铰链-IgG2/IgG4CH2-IgG4CH3细胞外间隔子。在感染后5和14天时通过流式细胞术评估转导效率和CAR表达。还在原代人T细胞中测试了转导效率和CAR表达,将所述原代人T细胞用在EF1a或MND启动子调节下的编码抗EGFR CAR的慢病毒构建体进行刺激和转导以作为对照,所述抗EGFR CAR具有IgG4/IgG2铰链-IgG2/IgG4 CH2-IgG4 CH3间隔子。
慢病毒构建体含有通过充当转导标记的T2A自切割肽与CAR序列分开的GFP序列。通过荧光标记的抗IgG4铰链抗体检测CAR表达。将事件以GFP(感染)相对于抗IgG4铰链(CAR表达)作图。CAR在原代人T细胞中的表达如图3A中所示。如图3B中所示,在此测定中,某些MND启动子构建体展现出较低的转导效率,但是表达较高水平的CAR。
将来自以上实施例8的表达抗CCT5和抗EGFR CAR的原代人T细胞与SK-BR-3(乳腺癌)、MIA PaCA-2(胰腺癌)和OvCar4(卵巢癌)靶细胞一起孵育。也将来自以上实施例9的表达抗CCT5和抗EGFR CAR的原代人T细胞与UPCI:SCC152(头颈部鳞状细胞癌)以4:1和1:1的效应子与靶标(E:T)比率一起孵育。还将靶细胞与作为对照的模拟处理的T细胞或无细胞一起孵育。为了进行细胞溶解测定,将靶细胞用NucLight Red(NLR)标记,以允许通过显微镜检查追踪靶细胞。通过测量如通过红色荧光信号(使用
未经处理或与模拟处理的CAR T细胞一起孵育的SK-BR-3和MIA PaCa-2靶细胞在研究过程中展现出逐渐生长。未经处理或与模拟处理的CAR T细胞一起孵育的OvCar4靶细胞展现出如下生长,所述生长在约30小时达到峰值,并在约48小时回到基线或低于基线,并在研究的剩余部分中保持稳定水平。未经处理或与模拟处理的CAR T细胞一起孵育的UPCI:SCC152靶细胞展现出在约60小时达到峰值的生长。
与未处理或模拟处理的T细胞处理条件相比,与在EF1a启动子的调节下表达具有IgG4铰链间隔子、IgG4铰链-CH3间隔子或IgG4/IgG2铰链-IgG2/IgG4 CH2-IgG4 CH3间隔子的抗CCT5 CAR的CAR T细胞一起孵育的靶细胞展现出相似或稍微降低的生长。与表达抗EGFR CAR的T细胞一起孵育导致所有三种靶细胞系的靶细胞数量逐渐减少。
与未处理或模拟处理的T细胞处理条件相比,与在MND启动子的调节下,具有IgG4铰链间隔子、IgG4铰链-CH3间隔子或IgG4/IgG2铰链-IgG2/IgG4CH2-IgG4 CH3间隔子的抗CCT5 CAR一起孵育的MIA PaCa-2靶细胞展现出降低的生长。与在MND启动子的调节下,具有IgG4铰链间隔子、IgG4铰链-CH3间隔子或IgG4/IgG2铰链-IgG2/IgG4 CH2-IgG4 CH3间隔子的抗CCT5 CAR一起孵育的SK-BR-3、UPCI:SCC152和OvCar4靶细胞展现出靶细胞数量的下降,这证实在这些条件下的细胞死亡。在此测定中,在评估的抗CCT5 CAR中,与包含其他间隔子或在不同启动子的控制下的CAR相比,在MND启动子的调节下的具有IgG4铰链-CH3间隔子的抗CCT5 CAR最有效地减少靶细胞的增殖或杀伤靶细胞。
如以上在实施例8所述,将表达抗CCT5 CAR或抗EGFR的CD4+和CD8+原代人T细胞与A549(腺癌)、SK-BR-3(乳腺癌)、MIA PaCA-2(胰腺癌)、OvCar4(卵巢癌)和UPCI:SCC152(头颈部鳞状细胞癌)靶细胞和仅培养基一起孵育2.5天。还将靶肿瘤细胞与作为对照的非处理T细胞一起孵育。孵育后,分析T细胞的对应于幼稚T(T
共培养24小时后,收集上清液并分析IL-2、IFNγ和TNFα的释放。在含有所有五种癌细胞类型的共培养物的上清液中检测到所有三种细胞因子,将所述五种癌细胞类型与在MND启动子的调节下表达具有IgG4铰链-CH3间隔子的抗CCT5 CAR的T细胞一起孵育。在含有癌细胞的共培养物的上清液中也观察到了可检测的细胞因子产生,所述癌细胞已经与在MND启动子的调节下表达具有IgG4-铰链间隔子的抗CCT5 CAR的T细胞一起孵育。
将如以上在实施例8所述产生的在MND启动子的调节下表达抗CCT5 CAR或抗EGFR的CD4+和CD8+原代人T细胞用增殖染料CellTrace
本发明在范围上并不旨在限于具体公开的实施方案,提供具体公开的实施方案例如是为了说明本发明的各个方面。根据本文的描述和传授,对所述组合物和方法的各种修改将变得清楚。可以在不背离本公开文本的真实范围和精神的情况下实践此类变化,并且此类变化旨在落入本公开文本的范围内。
序列表
<110> 朱诺治疗学股份有限公司
S·伯恩
R·沙利文
F·维尼奥特
<120> 抗CCT5结合分子及其使用方法
<130> 73504-20146.40
<140> 尚未分配
<141> 同时随同提交
<150> US 62/599,682
<151> 2017-12-15
<160> 86
<170> 用于Windows 4.0版的FastSEQ
<210> 1
<211> 133
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> 抗体可变重 (VH)链 (aa)
<400> 1
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ser Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Ser Ser Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Asp Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Phe Lys Gly Asp Cys Ser Ser Thr Ser Cys Tyr Arg Gly
100 105 110
Gly Tyr Tyr Tyr Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr
115 120 125
Val Thr Val Ser Ser
130
<210> 2
<211> 106
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223>抗体可变轻 (VL)链 (aa)
<400> 2
Ser Tyr Glu Leu Thr Gln Pro Pro Ser Val Ser Val Ser Pro Gly Gln
1 5 10 15
Thr Ala Ser Ile Thr Cys Phe Gly Asp Gln Leu Gly Asp Lys Tyr Val
20 25 30
Ser Trp Tyr Gln Lys Lys Pro Gly Gln Ser Pro Val Leu Val Ile Tyr
35 40 45
Gln Asp Ala Asn Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Arg Gly Thr Gln Asn Leu
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Thr Trp Gly Thr Thr Thr Ala Leu
85 90 95
Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 3
<211> 399
<212> DNA
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> 抗体可变重 (VH)链 (nt)
<400> 3
gaggtgcagc ttgtggagtc aggcggaggg cttgtacagc ccggcggcag tcttagactc 60
agttgtgccg cctctggctt tactttctca tcttactcca tgaactgggt gagacaggcc 120
cctggaaaag gacttgagtg ggttagttat atttcatctt caagcagcac aatatattat 180
gcagactcag tgaagggcag attcaccatt agtcgggaca atgcaaaaaa cagtctgtac 240
ttgcagatga attccctcag ggatgaagat acagcagtgt actattgtgc cagagacttc 300
aaaggcgatt gctcctctac gtcctgctat cgcggtggat actactatta ttatggaatg 360
gacgtttggg gccagggtac cacagtgacc gtgtcttcc 399
<210> 4
<211> 318
<212> DNA
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223>抗体可变轻 (VL)链 (nt)
<400> 4
agctatgagc tgacccagcc cccctccgtt agcgtcagtc ccggtcaaac cgccagcatc 60
acctgtttcg gggaccagct gggagataag tatgtgagct ggtatcagaa aaaaccaggt 120
cagtctcccg tgcttgtcat ttatcaggat gccaacagac caagcgggat ccctgaacga 180
ttctcaggga gcaacagcgg gaatactgcc acgcttacta tcagggggac ccagaatctg 240
gacgaggccg attactactg ccaaacctgg gggacaacaa ctgcgctgtt cggcgggggc 300
acaaagctga ccgttctg 318
<210> 5
<211> 228
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> IgG4/IgG2铰链- IgG2/IgG4 CH2- IgG4 CH3
细胞外间隔子
<400> 5
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Pro Val
1 5 10 15
Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
20 25 30
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
35 40 45
Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu
50 55 60
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Gln Ser Thr
65 70 75 80
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
85 90 95
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser
100 105 110
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
115 120 125
Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val
130 135 140
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
145 150 155 160
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
165 170 175
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr
180 185 190
Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val
195 200 205
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
210 215 220
Ser Leu Gly Lys
225
<210> 6
<211> 12
<212> PRT
<213> 智人(Homo sapiens)
<220>
<223> IgG4铰链 细胞外间隔子
<400> 6
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro
1 5 10
<210> 7
<211> 27
<212> PRT
<213> 智人(Homo sapiens)
<220>
<223> CD28跨膜结构域
<400> 7
Phe Trp Val Leu Val Val Val Gly Gly Val Leu Ala Cys Tyr Ser Leu
1 5 10 15
Leu Val Thr Val Ala Phe Ile Ile Phe Trp Val
20 25
<210> 8
<211> 42
<212> PRT
<213> 智人(Homo sapiens)
<220>
<223> 4-1BB来源的细胞内共信号传导序列
<400> 8
Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln Pro Phe Met
1 5 10 15
Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser Cys Arg Phe
20 25 30
Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu
35 40
<210> 9
<211> 112
<212> PRT
<213> 智人(Homo sapiens)
<220>
<223> CD3-ζ来源的细胞内信号传导结构域
(aa)
<400> 9
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly
1 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
50 55 60
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
65 70 75 80
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
85 90 95
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<210> 10
<211> 20
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> (Gly4Ser)4接头
<400> 10
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser
20
<210> 11
<211> 5
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> CDR-H1
<400> 11
Ser Tyr Ser Met Asn
1 5
<210> 12
<211> 17
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> CDR-H2
<400> 12
Tyr Ile Ser Ser Ser Ser Ser Thr Ile Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 13
<211> 24
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> CDR-H3
<400> 13
Asp Phe Lys Gly Asp Cys Ser Ser Thr Ser Cys Tyr Arg Gly Gly Tyr
1 5 10 15
Tyr Tyr Tyr Tyr Gly Met Asp Val
20
<210> 14
<211> 7
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> CDR-H1
<400> 14
Gly Phe Thr Phe Ser Ser Tyr
1 5
<210> 15
<211> 6
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> CDR-H2
<400> 15
Ser Ser Ser Ser Ser Thr
1 5
<210> 16
<211> 10
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> CDR-H1
<400> 16
Gly Phe Thr Phe Ser Ser Tyr Ser Met Asn
1 5 10
<210> 17
<211> 14
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> CDR-H2
<400> 17
Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser
1 5 10
<210> 18
<211> 6
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> CDR-H1
<400> 18
Ser Ser Tyr Ser Met Asn
1 5
<210> 19
<211> 13
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> CDR-H2
<400> 19
Trp Val Ser Tyr Ile Ser Ser Ser Ser Ser Thr Ile Tyr
1 5 10
<210> 20
<211> 25
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> CDR-H3
<400> 20
Ala Arg Asp Phe Lys Gly Asp Cys Ser Ser Thr Ser Cys Tyr Arg Gly
1 5 10 15
Gly Tyr Tyr Tyr Tyr Tyr Gly Met Asp
20 25
<210> 21
<211> 11
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> CDR-L1
<400> 21
Phe Gly Asp Gln Leu Gly Asp Lys Tyr Val Ser
1 5 10
<210> 22
<211> 7
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> CDR-L2
<400> 22
Gln Asp Ala Asn Arg Pro Ser
1 5
<210> 23
<211> 9
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> CDR-L3
<400> 23
Gln Thr Trp Gly Thr Thr Thr Ala Leu
1 5
<210> 24
<211> 7
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> CDR-L1
<400> 24
Asp Lys Tyr Val Ser Trp Tyr
1 5
<210> 25
<211> 10
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> CDR-L2
<400> 25
Leu Val Ile Tyr Gln Asp Ala Asn Arg Pro
1 5 10
<210> 26
<211> 8
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> CDR-L3
<400> 26
Gln Thr Trp Gly Thr Thr Thr Ala
1 5
<210> 27
<211> 399
<212> DNA
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> MND启动子
<400> 27
tttatttagt ctccagaaaa aggggggaat gaaagacccc acctgtaggt ttggcaagct 60
aggatcaagg ttaggaacag agagacagca gaatatgggc caaacaggat atctgtggta 120
agcagttcct gccccggctc agggccaaga acagttggaa cagcagaata tgggccaaac 180
aggatatctg tggtaagcag ttcctgcccc ggctcagggc caagaacaga tggtccccag 240
atgcggtccc gccctcagca gtttctagag aaccatcaga tgtttccagg gtgccccaag 300
gacctgaaat gaccctgtgc cttatttgaa ctaaccaatc agttcgcttc tcgcttctgt 360
tcgcgcgctt ctgctccccg agctcaataa aagagccca 399
<210> 28
<211> 20
<212> RNA
<213> 智人(Homo sapiens)
<220>
<223> 人Nur77 gRNA 1靶向结构域
<400> 28
caugaagauc uugucaauga 20
<210> 29
<211> 19
<212> RNA
<213> 智人(Homo sapiens)
<220>
<223> 人Nur77 gRNA 2靶向结构域
<400> 29
ugcacacgug uucccaggc 19
<210> 30
<211> 3341
<212> DNA
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> Nur77敲入构建体序列
<400> 30
cagcctccta aagtgctggg attacaggtg tgagccacca cgcctagccc ttcactgtga 60
cttctgacag tgcagatcag attggttgtg cctgttttgg actttatgta aatgtagttc 120
tgcaggatgg aatctggtgt tgaatgcaga ggttttcaga tttctctgtt ttttaaagga 180
aagaatccac cctcgttcat tttttcactt aaattgcaca ggggacccaa cgatatagaa 240
cacaatcaga ggtactctgg gctgagggag tgctgagttc tgaggctggg tttctcagaa 300
cagtctagat tttaaaaacc caatgatcta gccagaaaac gtaggttagg attttatttc 360
ccgtttgtga ccctgggcaa gtcattagcc tcctgggcct cgggttctca cttggagtat 420
gaggataatg agggttactg cttctcagac ttgtgacgat gcttactaat ggccaacatg 480
tgaatgcgct tttgtgaagt gccagcagag catgaggggt ggtcaggggc agcagtttta 540
ggggcctggg ggaggctggg gctttggggg cctggttctc agatgtacag ctaatcctgt 600
acccttcccg cagaccggca tgggctgcag gagccgcggc gggtggagga gctgcagaac 660
cgcatcgcca gctgcctgaa ggagcacgtg gcagctgtgg cgggcgagcc ccagccagcc 720
agctgcctgt cacgtctgtt gggcaaactg cccgagctgc ggaccctgtg cacccagggc 780
ctgcagcgta tcttctacct caagctggag gacttggtgc cccctccacc tatcatcgac 840
aagatcttca tggacacgct gcccttcgga tccggagaag gcagaggctc tctcctcaca 900
tgtggggatg ttgaagaaaa tccaggtccc ggtgtgagca agggcgagga ggtgatcaag 960
gagtttatga gattcaaagt ccggatggag ggcagcatga acggacatga gttcgaaatt 1020
gagggagaag gcgagggacg accttacgag ggaacacaga ccgccaaact gaaagtgaca 1080
aaaggcggac ctctgccatt tgcttgggac atcctgagtc cacagttcat gtatggctct 1140
aaggcttacg tgaaacaccc tgccgatatt cccgactaca aaaaactgag tttccctgaa 1200
ggcttcaaat gggaacgagt gatgaacttt gaggacggag gcctggtgac agtgacacag 1260
gactctagtc tccaggacgg cacactcatc tacaaagtga aaatgagggg caccaatttc 1320
cctcccgatg gacctgtcat gcagaaaaaa acaatgggat gggaggcttc taccgaacga 1380
ctgtacccac gggatggagt gctgaaaggc gagatccatc aggcactgaa actgaaggat 1440
ggcggccatt acctggtcga gttcaaaacc atctatatgg ccaaaaaacc cgtccagctg 1500
cctggctact attacgtgga taccaaactg gacattacct ctcacaatga agactacaca 1560
atcgtcgagc agtacgagag gagtgagggc cgacaccacc tcttcctcgg gcatggcacc 1620
ggcagcaccg gcagcggcag ctccggcacc gctagttccg aggacaacaa catggccgtc 1680
atcaaagagt tcatgcgctt caaggtgcgc atggagggct ccatgaacgg ccacgagttc 1740
gagatcgagg gcgagggcga gggccgcccc tacgagggca cccagaccgc caagctgaag 1800
gtgaccaagg gcggccccct gcccttcgcc tgggacatcc tgtcccccca gttcatgtac 1860
ggctccaagg cgtacgtgaa gcaccccgcc gacatccccg attacaagaa gctgtccttc 1920
cccgagggct tcaagtggga gcgcgtgatg aacttcgagg acggcggtct ggtgaccgtg 1980
acccaggact cctccctgca ggacggcacg ctgatctaca aggtgaagat gcgcggcacc 2040
aacttccccc ccgacggccc cgtaatgcag aagaagacca tgggctggga ggcctccacc 2100
gagcgcctgt acccccgcga cggcgtgctg aagggcgaga tccaccaggc cctgaagctg 2160
aaggacggcg gccactacct ggtggagttc aagaccatct acatggccaa gaagcccgtg 2220
caactgcccg gctactacta cgtggacacc aagctggaca tcacctccca caacgaggac 2280
tacaccatcg tggaacagta cgagcgctcc gagggccgcc accacctgtt cctgtacggc 2340
atggacgagc tgtacaaatg actcgagcct gggaacacgt gtgcacatgc gcactctcat 2400
atgccacccc atgtgccttt agtccacgga cccccagagc acccccaagc ctgggcttga 2460
gctgcagaat gactccacct tctcacctgc tccaggaggt ttgcagggag ctcaagccct 2520
tggggagggg gatgccttca tgggggtgac cccacgattt gtcttatccc ccccagcctg 2580
gccccggcct ttatgttttt tgtaagataa accgttttta acacatagcg ccgtgctgta 2640
aataagccca gtgctgctgt aaatacagga agaaagagct tgaggtggga gcggggctgg 2700
gaggaaggga tgggccccgc cttcctgggc agcctttcca gcctcctgct ggctctctct 2760
tcctaccctc cttccacatg tacataaact gtcactctag gaagaagaca aatgacagat 2820
tctgacattt atatttgtgt attttcctgg atttatagta tgtgactttt ctgattaata 2880
tatttaatat attgaataaa aaatagacat gtagttggaa ctgagattca gtctgtctct 2940
gatgccccct ccccactccc ccaccagaca caccccatca ttacataaga gatgggctgc 3000
tcaagatgaa acttggatgt taccagcctg agctgtcagg cctcagtgta ctcatttgta 3060
aaaggcggat aataatgaca cctgcttcac gaggttgtta tgcaaagcac ttagactaat 3120
ttctaacacg tgggaagcct gcattagctg tgcctggcta gctgtgcctg gctcattgct 3180
ggggtctgca gtggctgact agcccagggg tcactgcagg gccctagcaa tagacttagc 3240
cgcagatctc agggttgtca tgtttcctaa actggacata tattctctga ttcttgattt 3300
ccacatccat aaaacaagaa tagacccagc ctcacagagc t 3341
<210> 31
<211> 54
<212> DNA
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> T2A DNA
<400> 31
gaaggcagag gctctctcct cacatgtggg gatgttgaag aaaatccagg tccc 54
<210> 32
<211> 18
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> T2A肽(aa)
<400> 32
Glu Gly Arg Gly Ser Leu Leu Thr Cys Gly Asp Val Glu Glu Asn Pro
1 5 10 15
Gly Pro
<210> 33
<211> 21
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> T2A肽(aa)
<400> 33
Gly Ser Gly Glu Gly Arg Gly Ser Leu Leu Thr Cys Gly Asp Val Glu
1 5 10 15
Glu Asn Pro Gly Pro
20
<210> 34
<211> 24
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> T2A肽(aa)
<400> 34
Leu Glu Gly Gly Gly Glu Gly Arg Gly Ser Leu Leu Thr Cys Gly Asp
1 5 10 15
Val Glu Glu Asn Pro Gly Pro Arg
20
<210> 35
<211> 19
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> P2A肽(aa)
<400> 35
Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn
1 5 10 15
Pro Gly Pro
<210> 36
<211> 22
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> P2A肽(aa)
<400> 36
Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val
1 5 10 15
Glu Glu Asn Pro Gly Pro
20
<210> 37
<211> 20
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> E2A肽(aa)
<400> 37
Gln Cys Thr Asn Tyr Ala Leu Leu Lys Leu Ala Gly Asp Val Glu Ser
1 5 10 15
Asn Pro Gly Pro
20
<210> 38
<211> 23
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> E2A肽(aa)
<400> 38
Gly Ser Gly Gln Cys Thr Asn Tyr Ala Leu Leu Lys Leu Ala Gly Asp
1 5 10 15
Val Glu Ser Asn Pro Gly Pro
20
<210> 39
<211> 22
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> F2A肽(aa)
<400> 39
Val Lys Gln Thr Leu Asn Phe Asp Leu Leu Lys Leu Ala Gly Asp Val
1 5 10 15
Glu Ser Asn Pro Gly Pro
20
<210> 40
<211> 25
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> F2A肽(aa)
<400> 40
Gly Ser Gly Val Lys Gln Thr Leu Asn Phe Asp Leu Leu Lys Leu Ala
1 5 10 15
Gly Asp Val Glu Ser Asn Pro Gly Pro
20 25
<210> 41
<211> 1422
<212> DNA
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> tdTomato DNA
<400> 41
gtgagcaagg gcgaggaggt gatcaaggag tttatgagat tcaaagtccg gatggagggc 60
agcatgaacg gacatgagtt cgaaattgag ggagaaggcg agggacgacc ttacgaggga 120
acacagaccg ccaaactgaa agtgacaaaa ggcggacctc tgccatttgc ttgggacatc 180
ctgagtccac agttcatgta tggctctaag gcttacgtga aacaccctgc cgatattccc 240
gactacaaaa aactgagttt ccctgaaggc ttcaaatggg aacgagtgat gaactttgag 300
gacggaggcc tggtgacagt gacacaggac tctagtctcc aggacggcac actcatctac 360
aaagtgaaaa tgaggggcac caatttccct cccgatggac ctgtcatgca gaaaaaaaca 420
atgggatggg aggcttctac cgaacgactg tacccacggg atggagtgct gaaaggcgag 480
atccatcagg cactgaaact gaaggatggc ggccattacc tggtcgagtt caaaaccatc 540
tatatggcca aaaaacccgt ccagctgcct ggctactatt acgtggatac caaactggac 600
attacctctc acaatgaaga ctacacaatc gtcgagcagt acgagaggag tgagggccga 660
caccacctct tcctcgggca tggcaccggc agcaccggca gcggcagctc cggcaccgct 720
agttccgagg acaacaacat ggccgtcatc aaagagttca tgcgcttcaa ggtgcgcatg 780
gagggctcca tgaacggcca cgagttcgag atcgagggcg agggcgaggg ccgcccctac 840
gagggcaccc agaccgccaa gctgaaggtg accaagggcg gccccctgcc cttcgcctgg 900
gacatcctgt ccccccagtt catgtacggc tccaaggcgt acgtgaagca ccccgccgac 960
atccccgatt acaagaagct gtccttcccc gagggcttca agtgggagcg cgtgatgaac 1020
ttcgaggacg gcggtctggt gaccgtgacc caggactcct ccctgcagga cggcacgctg 1080
atctacaagg tgaagatgcg cggcaccaac ttcccccccg acggccccgt aatgcagaag 1140
aagaccatgg gctgggaggc ctccaccgag cgcctgtacc cccgcgacgg cgtgctgaag 1200
ggcgagatcc accaggccct gaagctgaag gacggcggcc actacctggt ggagttcaag 1260
accatctaca tggccaagaa gcccgtgcaa ctgcccggct actactacgt ggacaccaag 1320
ctggacatca cctcccacaa cgaggactac accatcgtgg aacagtacga gcgctccgag 1380
ggccgccacc acctgttcct gtacggcatg gacgagctgt ac 1422
<210> 42
<211> 474
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> tdTomato蛋白
<400> 42
Val Ser Lys Gly Glu Glu Val Ile Lys Glu Phe Met Arg Phe Lys Val
1 5 10 15
Arg Met Glu Gly Ser Met Asn Gly His Glu Phe Glu Ile Glu Gly Glu
20 25 30
Gly Glu Gly Arg Pro Tyr Glu Gly Thr Gln Thr Ala Lys Leu Lys Val
35 40 45
Thr Lys Gly Gly Pro Leu Pro Phe Ala Trp Asp Ile Leu Ser Pro Gln
50 55 60
Phe Met Tyr Gly Ser Lys Ala Tyr Val Lys His Pro Ala Asp Ile Pro
65 70 75 80
Asp Tyr Lys Lys Leu Ser Phe Pro Glu Gly Phe Lys Trp Glu Arg Val
85 90 95
Met Asn Phe Glu Asp Gly Gly Leu Val Thr Val Thr Gln Asp Ser Ser
100 105 110
Leu Gln Asp Gly Thr Leu Ile Tyr Lys Val Lys Met Arg Gly Thr Asn
115 120 125
Phe Pro Pro Asp Gly Pro Val Met Gln Lys Lys Thr Met Gly Trp Glu
130 135 140
Ala Ser Thr Glu Arg Leu Tyr Pro Arg Asp Gly Val Leu Lys Gly Glu
145 150 155 160
Ile His Gln Ala Leu Lys Leu Lys Asp Gly Gly His Tyr Leu Val Glu
165 170 175
Phe Lys Thr Ile Tyr Met Ala Lys Lys Pro Val Gln Leu Pro Gly Tyr
180 185 190
Tyr Tyr Val Asp Thr Lys Leu Asp Ile Thr Ser His Asn Glu Asp Tyr
195 200 205
Thr Ile Val Glu Gln Tyr Glu Arg Ser Glu Gly Arg His His Leu Phe
210 215 220
Leu Gly His Gly Thr Gly Ser Thr Gly Ser Gly Ser Ser Gly Thr Ala
225 230 235 240
Ser Ser Glu Asp Asn Asn Met Ala Val Ile Lys Glu Phe Met Arg Phe
245 250 255
Lys Val Arg Met Glu Gly Ser Met Asn Gly His Glu Phe Glu Ile Glu
260 265 270
Gly Glu Gly Glu Gly Arg Pro Tyr Glu Gly Thr Gln Thr Ala Lys Leu
275 280 285
Lys Val Thr Lys Gly Gly Pro Leu Pro Phe Ala Trp Asp Ile Leu Ser
290 295 300
Pro Gln Phe Met Tyr Gly Ser Lys Ala Tyr Val Lys His Pro Ala Asp
305 310 315 320
Ile Pro Asp Tyr Lys Lys Leu Ser Phe Pro Glu Gly Phe Lys Trp Glu
325 330 335
Arg Val Met Asn Phe Glu Asp Gly Gly Leu Val Thr Val Thr Gln Asp
340 345 350
Ser Ser Leu Gln Asp Gly Thr Leu Ile Tyr Lys Val Lys Met Arg Gly
355 360 365
Thr Asn Phe Pro Pro Asp Gly Pro Val Met Gln Lys Lys Thr Met Gly
370 375 380
Trp Glu Ala Ser Thr Glu Arg Leu Tyr Pro Arg Asp Gly Val Leu Lys
385 390 395 400
Gly Glu Ile His Gln Ala Leu Lys Leu Lys Asp Gly Gly His Tyr Leu
405 410 415
Val Glu Phe Lys Thr Ile Tyr Met Ala Lys Lys Pro Val Gln Leu Pro
420 425 430
Gly Tyr Tyr Tyr Val Asp Thr Lys Leu Asp Ile Thr Ser His Asn Glu
435 440 445
Asp Tyr Thr Ile Val Glu Gln Tyr Glu Arg Ser Glu Gly Arg His His
450 455 460
Leu Phe Leu Tyr Gly Met Asp Glu Leu Tyr
465 470
<210> 43
<211> 927
<212> DNA
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> Nur77左同源臂
(chr12:52,058,015-52,058,941 hg38组装),具有沉默突变
<400> 43
aatctcacta tgttgcccga gctggtctcg aactcctggg ctcaaatgat cctcctgtct 60
cagcctccta aagtgctggg attacaggtg tgagccacca cgcctagccc ttcactgtga 120
cttctgacag tgcagatcag attggttgtg cctgttttgg actttatgta aatgtagttc 180
tgcaggatgg aatctggtgt tgaatgcaga ggttttcaga tttctctgtt ttttaaagga 240
aagaatccac cctcgttcat tttttcactt aaattgcaca ggggacccaa cgatatagaa 300
cacaatcaga ggtactctgg gctgagggag tgctgagttc tgaggctggg tttctcagaa 360
cagtctagat tttaaaaacc caatgatcta gccagaaaac gtaggttagg attttatttc 420
ccgtttgtga ccctgggcaa gtcattagcc tcctgggcct cgggttctca cttggagtat 480
gaggataatg agggttactg cttctcagac ttgtgacgat gcttactaat ggccaacatg 540
tgaatgcgct tttgtgaagt gccagcagag catgaggggt ggtcaggggc agcagtttta 600
ggggcctggg ggaggctggg gctttggggg cctggttctc agatgtacag ctaatcctgt 660
acccttcccg cagaccggca tgggctgcag gagccgcggc gggtggagga gctgcagaac 720
cgcatcgcca gctgcctgaa ggagcacgtg gcagctgtgg cgggcgagcc ccagccagcc 780
agctgcctgt cacgtctgtt gggcaaactg cccgagctgc ggaccctgtg cacccagggc 840
ctgcagcgta tcttctacct caagctggag gacttggtgc cccctccacc tatcatcgac 900
aagatcttca tggacacgct gcccttc 927
<210> 44
<211> 975
<212> DNA
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> Nur77右同源臂
(chr12:52,058,950-52,059,924 hg38组装)
<400> 44
gcctgggaac acgtgtgcac atgcgcactc tcatatgcca ccccatgtgc ctttagtcca 60
cggaccccca gagcaccccc aagcctgggc ttgagctgca gaatgactcc accttctcac 120
ctgctccagg aggtttgcag ggagctcaag cccttgggga gggggatgcc ttcatggggg 180
tgaccccacg atttgtctta tcccccccag cctggccccg gcctttatgt tttttgtaag 240
ataaaccgtt tttaacacat agcgccgtgc tgtaaataag cccagtgctg ctgtaaatac 300
aggaagaaag agcttgaggt gggagcgggg ctgggaggaa gggatgggcc ccgccttcct 360
gggcagcctt tccagcctcc tgctggctct ctcttcctac cctccttcca catgtacata 420
aactgtcact ctaggaagaa gacaaatgac agattctgac atttatattt gtgtattttc 480
ctggatttat agtatgtgac ttttctgatt aatatattta atatattgaa taaaaaatag 540
acatgtagtt ggaactgaga ttcagtctgt ctctgatgcc ccctccccac tcccccacca 600
gacacacccc atcattacat aagagatggg ctgctcaaga tgaaacttgg atgttaccag 660
cctgagctgt caggcctcag tgtactcatt tgtaaaaggc ggataataat gacacctgct 720
tcacgaggtt gttatgcaaa gcacttagac taatttctaa cacgtgggaa gcctgcatta 780
gctgtgcctg gctagctgtg cctggctcat tgctggggtc tgcagtggct gactagccca 840
ggggtcactg cagggcccta gcaatagact tagccgcaga tctcagggtt gtcatgtttc 900
ctaaactgga catatattct ctgattcttg atttccacat ccataaaaca agaatagacc 960
cagcctcaca gagct 975
<210> 45
<211> 541
<212> PRT
<213> 智人(Homo sapiens)
<220>
<223> 人CCT5
(Uniprot P48643)
<400> 45
Met Ala Ser Met Gly Thr Leu Ala Phe Asp Glu Tyr Gly Arg Pro Phe
1 5 10 15
Leu Ile Ile Lys Asp Gln Asp Arg Lys Ser Arg Leu Met Gly Leu Glu
20 25 30
Ala Leu Lys Ser His Ile Met Ala Ala Lys Ala Val Ala Asn Thr Met
35 40 45
Arg Thr Ser Leu Gly Pro Asn Gly Leu Asp Lys Met Met Val Asp Lys
50 55 60
Asp Gly Asp Val Thr Val Thr Asn Asp Gly Ala Thr Ile Leu Ser Met
65 70 75 80
Met Asp Val Asp His Gln Ile Ala Lys Leu Met Val Glu Leu Ser Lys
85 90 95
Ser Gln Asp Asp Glu Ile Gly Asp Gly Thr Thr Gly Val Val Val Leu
100 105 110
Ala Gly Ala Leu Leu Glu Glu Ala Glu Gln Leu Leu Asp Arg Gly Ile
115 120 125
His Pro Ile Arg Ile Ala Asp Gly Tyr Glu Gln Ala Ala Arg Val Ala
130 135 140
Ile Glu His Leu Asp Lys Ile Ser Asp Ser Val Leu Val Asp Ile Lys
145 150 155 160
Asp Thr Glu Pro Leu Ile Gln Thr Ala Lys Thr Thr Leu Gly Ser Lys
165 170 175
Val Val Asn Ser Cys His Arg Gln Met Ala Glu Ile Ala Val Asn Ala
180 185 190
Val Leu Thr Val Ala Asp Met Glu Arg Arg Asp Val Asp Phe Glu Leu
195 200 205
Ile Lys Val Glu Gly Lys Val Gly Gly Arg Leu Glu Asp Thr Lys Leu
210 215 220
Ile Lys Gly Val Ile Val Asp Lys Asp Phe Ser His Pro Gln Met Pro
225 230 235 240
Lys Lys Val Glu Asp Ala Lys Ile Ala Ile Leu Thr Cys Pro Phe Glu
245 250 255
Pro Pro Lys Pro Lys Thr Lys His Lys Leu Asp Val Thr Ser Val Glu
260 265 270
Asp Tyr Lys Ala Leu Gln Lys Tyr Glu Lys Glu Lys Phe Glu Glu Met
275 280 285
Ile Gln Gln Ile Lys Glu Thr Gly Ala Asn Leu Ala Ile Cys Gln Trp
290 295 300
Gly Phe Asp Asp Glu Ala Asn His Leu Leu Leu Gln Asn Asn Leu Pro
305 310 315 320
Ala Val Arg Trp Val Gly Gly Pro Glu Ile Glu Leu Ile Ala Ile Ala
325 330 335
Thr Gly Gly Arg Ile Val Pro Arg Phe Ser Glu Leu Thr Ala Glu Lys
340 345 350
Leu Gly Phe Ala Gly Leu Val Gln Glu Ile Ser Phe Gly Thr Thr Lys
355 360 365
Asp Lys Met Leu Val Ile Glu Gln Cys Lys Asn Ser Arg Ala Val Thr
370 375 380
Ile Phe Ile Arg Gly Gly Asn Lys Met Ile Ile Glu Glu Ala Lys Arg
385 390 395 400
Ser Leu His Asp Ala Leu Cys Val Ile Arg Asn Leu Ile Arg Asp Asn
405 410 415
Arg Val Val Tyr Gly Gly Gly Ala Ala Glu Ile Ser Cys Ala Leu Ala
420 425 430
Val Ser Gln Glu Ala Asp Lys Cys Pro Thr Leu Glu Gln Tyr Ala Met
435 440 445
Arg Ala Phe Ala Asp Ala Leu Glu Val Ile Pro Met Ala Leu Ser Glu
450 455 460
Asn Ser Gly Met Asn Pro Ile Gln Thr Met Thr Glu Val Arg Ala Arg
465 470 475 480
Gln Val Lys Glu Met Asn Pro Ala Leu Gly Ile Asp Cys Leu His Lys
485 490 495
Gly Thr Asn Asp Met Lys Gln Gln His Val Ile Glu Thr Leu Ile Gly
500 505 510
Lys Lys Gln Gln Ile Ser Leu Ala Thr Gln Met Val Arg Met Ile Leu
515 520 525
Lys Ile Asp Asp Ile Arg Lys Pro Gly Glu Ser Glu Glu
530 535 540
<210> 46
<211> 540
<212> PRT
<213> 智人(Homo sapiens)
<220>
<223> 人CCT5
(Uniprot P48643)
<400> 46
Ala Ser Met Gly Thr Leu Ala Phe Asp Glu Tyr Gly Arg Pro Phe Leu
1 5 10 15
Ile Ile Lys Asp Gln Asp Arg Lys Ser Arg Leu Met Gly Leu Glu Ala
20 25 30
Leu Lys Ser His Ile Met Ala Ala Lys Ala Val Ala Asn Thr Met Arg
35 40 45
Thr Ser Leu Gly Pro Asn Gly Leu Asp Lys Met Met Val Asp Lys Asp
50 55 60
Gly Asp Val Thr Val Thr Asn Asp Gly Ala Thr Ile Leu Ser Met Met
65 70 75 80
Asp Val Asp His Gln Ile Ala Lys Leu Met Val Glu Leu Ser Lys Ser
85 90 95
Gln Asp Asp Glu Ile Gly Asp Gly Thr Thr Gly Val Val Val Leu Ala
100 105 110
Gly Ala Leu Leu Glu Glu Ala Glu Gln Leu Leu Asp Arg Gly Ile His
115 120 125
Pro Ile Arg Ile Ala Asp Gly Tyr Glu Gln Ala Ala Arg Val Ala Ile
130 135 140
Glu His Leu Asp Lys Ile Ser Asp Ser Val Leu Val Asp Ile Lys Asp
145 150 155 160
Thr Glu Pro Leu Ile Gln Thr Ala Lys Thr Thr Leu Gly Ser Lys Val
165 170 175
Val Asn Ser Cys His Arg Gln Met Ala Glu Ile Ala Val Asn Ala Val
180 185 190
Leu Thr Val Ala Asp Met Glu Arg Arg Asp Val Asp Phe Glu Leu Ile
195 200 205
Lys Val Glu Gly Lys Val Gly Gly Arg Leu Glu Asp Thr Lys Leu Ile
210 215 220
Lys Gly Val Ile Val Asp Lys Asp Phe Ser His Pro Gln Met Pro Lys
225 230 235 240
Lys Val Glu Asp Ala Lys Ile Ala Ile Leu Thr Cys Pro Phe Glu Pro
245 250 255
Pro Lys Pro Lys Thr Lys His Lys Leu Asp Val Thr Ser Val Glu Asp
260 265 270
Tyr Lys Ala Leu Gln Lys Tyr Glu Lys Glu Lys Phe Glu Glu Met Ile
275 280 285
Gln Gln Ile Lys Glu Thr Gly Ala Asn Leu Ala Ile Cys Gln Trp Gly
290 295 300
Phe Asp Asp Glu Ala Asn His Leu Leu Leu Gln Asn Asn Leu Pro Ala
305 310 315 320
Val Arg Trp Val Gly Gly Pro Glu Ile Glu Leu Ile Ala Ile Ala Thr
325 330 335
Gly Gly Arg Ile Val Pro Arg Phe Ser Glu Leu Thr Ala Glu Lys Leu
340 345 350
Gly Phe Ala Gly Leu Val Gln Glu Ile Ser Phe Gly Thr Thr Lys Asp
355 360 365
Lys Met Leu Val Ile Glu Gln Cys Lys Asn Ser Arg Ala Val Thr Ile
370 375 380
Phe Ile Arg Gly Gly Asn Lys Met Ile Ile Glu Glu Ala Lys Arg Ser
385 390 395 400
Leu His Asp Ala Leu Cys Val Ile Arg Asn Leu Ile Arg Asp Asn Arg
405 410 415
Val Val Tyr Gly Gly Gly Ala Ala Glu Ile Ser Cys Ala Leu Ala Val
420 425 430
Ser Gln Glu Ala Asp Lys Cys Pro Thr Leu Glu Gln Tyr Ala Met Arg
435 440 445
Ala Phe Ala Asp Ala Leu Glu Val Ile Pro Met Ala Leu Ser Glu Asn
450 455 460
Ser Gly Met Asn Pro Ile Gln Thr Met Thr Glu Val Arg Ala Arg Gln
465 470 475 480
Val Lys Glu Met Asn Pro Ala Leu Gly Ile Asp Cys Leu His Lys Gly
485 490 495
Thr Asn Asp Met Lys Gln Gln His Val Ile Glu Thr Leu Ile Gly Lys
500 505 510
Lys Gln Gln Ile Ser Leu Ala Thr Gln Met Val Arg Met Ile Leu Lys
515 520 525
Ile Asp Asp Ile Arg Lys Pro Gly Glu Ser Glu Glu
530 535 540
<210> 47
<211> 5
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> 4GS接头 (aa)
<400> 47
Gly Gly Gly Gly Ser
1 5
<210> 48
<211> 4
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> 3GS接头 (aa)
<400> 48
Gly Gly Gly Ser
1
<210> 49
<211> 15
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> (4GS)3接头 (aa)
<400> 49
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 50
<211> 18
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223>接头 (aa)
<400> 50
Gly Ser Thr Ser Gly Ser Gly Lys Pro Gly Ser Gly Glu Gly Ser Thr
1 5 10 15
Lys Gly
<210> 51
<211> 60
<212> DNA
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> (4GS)3接头 (nt)
<400> 51
ggaggcggag gatctggtgg cggaggaagt ggcggaggcg gtagtggtgg tggtggatct 60
<210> 52
<211> 259
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> CCT5 scFv (aa)
<400> 52
Ser Tyr Glu Leu Thr Gln Pro Pro Ser Val Ser Val Ser Pro Gly Gln
1 5 10 15
Thr Ala Ser Ile Thr Cys Phe Gly Asp Gln Leu Gly Asp Lys Tyr Val
20 25 30
Ser Trp Tyr Gln Lys Lys Pro Gly Gln Ser Pro Val Leu Val Ile Tyr
35 40 45
Gln Asp Ala Asn Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
50 55 60
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Arg Gly Thr Gln Asn Leu
65 70 75 80
Asp Glu Ala Asp Tyr Tyr Cys Gln Thr Trp Gly Thr Thr Thr Ala Leu
85 90 95
Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Gly Gly Gly Ser Gly
100 105 110
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val
115 120 125
Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu
130 135 140
Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr Ser Met
145 150 155 160
Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Tyr
165 170 175
Ile Ser Ser Ser Ser Ser Thr Ile Tyr Tyr Ala Asp Ser Val Lys Gly
180 185 190
Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu Gln
195 200 205
Met Asn Ser Leu Arg Asp Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg
210 215 220
Asp Phe Lys Gly Asp Cys Ser Ser Thr Ser Cys Tyr Arg Gly Gly Tyr
225 230 235 240
Tyr Tyr Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr
245 250 255
Val Ser Ser
<210> 53
<211> 777
<212> DNA
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> CCT5 scFv (nt)
<400> 53
agctatgagc tgacccagcc cccctccgtt agcgtcagtc ccggtcaaac cgccagcatc 60
acctgtttcg gggaccaact gggagataaa tatgtgagct ggtatcagaa aaaaccaggc 120
cagtctcccg tgcttgtcat ttatcaagac gccaacagac caagcgggat ccctgaacga 180
ttctcaggga gcaacagcgg gaatactgcc acgcttacta tccgggggac ccagaatctg 240
gacgaggccg attactactg ccaaacctgg gggacaacaa ctgcgctgtt cggcgggggc 300
acaaagctga ccgttctggg aggcggagga tctggtggcg gaggaagtgg cggaggcggt 360
agtggtggtg gtggatctga ggtgcagctt gtggagtcag gcggagggct tgtacagccc 420
ggcggcagtc ttagactcag ttgtgccgcc tctggcttta ctttctcatc ttactccatg 480
aactgggtca gacaggcccc tggaaaagga cttgagtggg ttagttatat ttcatcttca 540
agcagcacaa tatattatgc agactcagtg aagggcagat tcaccattag tcgggacaat 600
gcaaaaaaca gcctgtactt gcaaatgaat tccctccggg atgaagatac agcagtgtac 660
tattgtgcca gagacttcaa aggcgattgc tcctctacgt cctgctatcg cggtggatac 720
tactattatt atggaatgga cgtttggggc cagggtacca cagtgaccgt gtcttcc 777
<210> 54
<211> 685
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> CCT5 CAR
<400> 54
Met Pro Leu Leu Leu Leu Leu Pro Leu Leu Trp Ala Gly Ala Leu Ala
1 5 10 15
Ser Tyr Glu Leu Thr Gln Pro Pro Ser Val Ser Val Ser Pro Gly Gln
20 25 30
Thr Ala Ser Ile Thr Cys Phe Gly Asp Gln Leu Gly Asp Lys Tyr Val
35 40 45
Ser Trp Tyr Gln Lys Lys Pro Gly Gln Ser Pro Val Leu Val Ile Tyr
50 55 60
Gln Asp Ala Asn Arg Pro Ser Gly Ile Pro Glu Arg Phe Ser Gly Ser
65 70 75 80
Asn Ser Gly Asn Thr Ala Thr Leu Thr Ile Arg Gly Thr Gln Asn Leu
85 90 95
Asp Glu Ala Asp Tyr Tyr Cys Gln Thr Trp Gly Thr Thr Thr Ala Leu
100 105 110
Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Gly Gly Gly Ser Gly
115 120 125
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Val
130 135 140
Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu
145 150 155 160
Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr Ser Met
165 170 175
Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ser Tyr
180 185 190
Ile Ser Ser Ser Ser Ser Thr Ile Tyr Tyr Ala Asp Ser Val Lys Gly
195 200 205
Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu Gln
210 215 220
Met Asn Ser Leu Arg Asp Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg
225 230 235 240
Asp Phe Lys Gly Asp Cys Ser Ser Thr Ser Cys Tyr Arg Gly Gly Tyr
245 250 255
Tyr Tyr Tyr Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr
260 265 270
Val Ser Ser Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala
275 280 285
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
290 295 300
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
305 310 315 320
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
325 330 335
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
340 345 350
Gln Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
355 360 365
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
370 375 380
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
385 390 395 400
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
405 410 415
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
420 425 430
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
435 440 445
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
450 455 460
Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
465 470 475 480
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
485 490 495
Leu Ser Leu Ser Leu Gly Lys Met Phe Trp Val Leu Val Val Val Gly
500 505 510
Gly Val Leu Ala Cys Tyr Ser Leu Leu Val Thr Val Ala Phe Ile Ile
515 520 525
Phe Trp Val Lys Arg Gly Arg Lys Lys Leu Leu Tyr Ile Phe Lys Gln
530 535 540
Pro Phe Met Arg Pro Val Gln Thr Thr Gln Glu Glu Asp Gly Cys Ser
545 550 555 560
Cys Arg Phe Pro Glu Glu Glu Glu Gly Gly Cys Glu Leu Arg Val Lys
565 570 575
Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Gln Gln Gly Gln Asn Gln
580 585 590
Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr Asp Val Leu
595 600 605
Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys Pro Arg Arg
610 615 620
Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys Asp Lys Met
625 630 635 640
Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg Arg Arg Gly
645 650 655
Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala Thr Lys Asp
660 665 670
Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
675 680 685
<210> 55
<211> 2055
<212> DNA
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> CCT5 CAR (nt)
<400> 55
atgccgctgc tgctactgct gcccctgctg tgggcagggg ctctagccag ctatgagctg 60
acccagcccc cctccgttag cgtcagtccc ggtcaaaccg ccagcatcac ctgtttcggg 120
gaccaactgg gagataaata tgtgagctgg tatcagaaaa aaccaggcca gtctcccgtg 180
cttgtcattt atcaagacgc caacagacca agcgggatcc ctgaacgatt ctcagggagc 240
aacagcggga atactgccac gcttactatc cgggggaccc agaatctgga cgaggccgat 300
tactactgcc aaacctgggg gacaacaact gcgctgttcg gcgggggcac aaagctgacc 360
gttctgggag gcggaggatc tggtggcgga ggaagtggcg gaggcggtag tggtggtggt 420
ggatctgagg tgcagcttgt ggagtcaggc ggagggcttg tacagcccgg cggcagtctt 480
agactcagtt gtgccgcctc tggctttact ttctcatctt actccatgaa ctgggtcaga 540
caggcccctg gaaaaggact tgagtgggtt agttatattt catcttcaag cagcacaata 600
tattatgcag actcagtgaa gggcagattc accattagtc gggacaatgc aaaaaacagc 660
ctgtacttgc aaatgaattc cctccgggat gaagatacag cagtgtacta ttgtgccaga 720
gacttcaaag gcgattgctc ctctacgtcc tgctatcgcg gtggatacta ctattattat 780
ggaatggacg tttggggcca gggtaccaca gtgaccgtgt cttccgaatc taaatacgga 840
ccgccttgtc ctccatgtcc tgctcctcca gttgccggac cttccgtgtt cctgtttcct 900
ccaaagccta aggacaccct gatgatcagc agaacccctg aagtgacctg cgtggtggtg 960
gacgtgtccc aagaggatcc tgaggtgcag ttcaactggt atgtggacgg cgtggaagtg 1020
cacaacgcca agaccaagcc tagagaggaa cagttccaga gcacctacag agtggtgtcc 1080
gtgctgacag tgctgcacca ggattggctg aacggcaaag agtacaagtg caaggtgtcc 1140
aacaagggcc tgcctagcag catcgagaaa accatcagca aggccaaggg ccagccaaga 1200
gaaccccagg tgtacacact gcctccaagc caagaggaaa tgaccaagaa ccaggtgtcc 1260
ctgacctgcc tggtcaaggg cttctaccct tccgatatcg ccgtggaatg ggagagcaat 1320
ggccagcctg agaacaacta caagaccaca cctcctgtgc tggacagcga cggctcattc 1380
ttcctgtaca gccggctgac cgtggacaag agcagatggc aagagggcaa cgtgttcagc 1440
tgcagcgtga tgcacgaggc cctgcacaac cactacaccc agaagtctct gagcctgagc 1500
ctgggcaaga tgttctgggt gctcgttgtt gttggcggcg tgctggcctg ttactccctg 1560
ctggttaccg tggccttcat catcttttgg gtcaagcggg gcagaaagaa gctgctctac 1620
atcttcaagc agcccttcat gcggcccgtg cagaccacac aagaggaaga tggctgctcc 1680
tgcagattcc ccgaggaaga agaaggcggc tgcgagctga gagtgaagtt cagcagatcc 1740
gccgacgctc cagcctatca gcagggacag aaccagctgt acaacgagct gaacctgggg 1800
agaagagaag agtacgacgt gctggataag cggagaggca gagatcctga gatgggcggc 1860
aagcccagac ggaagaatcc tcaagagggc ctgtataatg agctgcagaa agacaagatg 1920
gccgaggcct acagcgagat cggaatgaag ggcgagcgca gaagaggcaa gggacacgat 1980
ggactgtacc agggactgag caccgccacc aaggatacct atgacgcact gcacatgcag 2040
gccctgccac ctaga 2055
<210> 56
<211> 20
<212> PRT
<213> 智人(Homo sapiens)
<220>
<223> 人IgG -κ信号传导序列 (aa)
<400> 56
Met Val Leu Gln Thr Gln Val Phe Ile Ser Leu Leu Leu Trp Ile Ser
1 5 10 15
Gly Ala Tyr Gly
20
<210> 57
<211> 60
<212> DNA
<213> 智人(Homo sapiens)
<220>
<223> 人IgG -κ信号传导序列 (nt)
<400> 57
atggtgctgc agacccaggt gttcatcagc ctgctgctgt ggatctccgg agcatacgga 60
<210> 58
<211> 541
<212> PRT
<213> 黑鼠(Rattus rattus)
<220>
<223> 大鼠CCT5 (aa) (UniProt Q68FQ0)
<400> 58
Met Ala Ser Val Gly Thr Leu Ala Phe Asp Glu Tyr Gly Arg Pro Phe
1 5 10 15
Leu Ile Ile Lys Asp Gln Asp Arg Lys Ser Arg Leu Met Gly Leu Glu
20 25 30
Ala Leu Lys Ser His Ile Met Ala Ala Lys Ala Val Ala Asn Thr Met
35 40 45
Arg Thr Ser Leu Gly Pro Asn Gly Leu Asp Lys Met Met Val Asp Lys
50 55 60
Asp Gly Asp Val Thr Val Thr Asn Asp Gly Ala Thr Ile Leu Ser Met
65 70 75 80
Met Asp Val Asp His Gln Ile Ala Lys Leu Met Val Glu Leu Ser Lys
85 90 95
Ser Gln Asp Asp Glu Ile Gly Asp Gly Thr Thr Gly Val Val Val Leu
100 105 110
Ala Gly Ala Leu Leu Glu Glu Ala Glu Gln Leu Leu Asp Arg Gly Ile
115 120 125
His Pro Ile Arg Ile Ala Asp Gly Tyr Glu Gln Ala Ala Arg Ile Ala
130 135 140
Ile Gln His Leu Asp Lys Ile Ser Asp Asn Val Leu Val Asp Ile Asn
145 150 155 160
Asn Pro Glu Pro Leu Ile Gln Thr Ala Lys Thr Thr Leu Gly Ser Lys
165 170 175
Val Val Asn Ser Cys His Arg Gln Met Ala Glu Ile Ala Val Asn Ala
180 185 190
Val Leu Thr Val Ala Asp Met Glu Arg Arg Asp Val Asp Phe Glu Leu
195 200 205
Ile Lys Val Glu Gly Lys Val Gly Gly Arg Leu Glu Asp Thr Lys Leu
210 215 220
Ile Lys Gly Val Ile Val Asp Lys Asp Phe Ser His Pro Gln Met Pro
225 230 235 240
Lys Glu Val Leu Asn Ala Lys Ile Ala Ile Leu Thr Cys Pro Phe Glu
245 250 255
Pro Pro Lys Pro Lys Thr Lys His Lys Leu Asp Val Thr Ser Val Glu
260 265 270
Asp Tyr Lys Ala Leu Gln Lys Tyr Glu Lys Glu Lys Phe Glu Glu Met
275 280 285
Ile Ala Gln Ile Lys Glu Thr Gly Ala Asn Leu Ala Ile Cys Gln Trp
290 295 300
Gly Phe Asp Asp Glu Ala Asn His Leu Leu Leu Gln Asn Gly Leu Pro
305 310 315 320
Ala Val Arg Trp Val Gly Gly Pro Glu Ile Glu Leu Ile Ala Ile Ala
325 330 335
Thr Gly Gly Arg Ile Val Pro Arg Phe Ser Glu Leu Thr Ser Glu Lys
340 345 350
Leu Gly Phe Ala Gly Val Val Arg Glu Ile Ser Phe Gly Thr Thr Lys
355 360 365
Asp Lys Met Leu Val Ile Glu Gln Cys Lys Asn Ser Arg Ala Val Thr
370 375 380
Ile Phe Ile Arg Gly Gly Asn Lys Met Ile Ile Glu Glu Ala Lys Arg
385 390 395 400
Ser Leu His Asp Ala Leu Cys Val Ile Arg Asn Leu Ile Arg Asp Asn
405 410 415
Arg Val Val Tyr Gly Gly Gly Ala Ala Glu Ile Ser Cys Ala Leu Ala
420 425 430
Val Ser Gln Glu Ala Asp Lys Cys Pro Thr Leu Glu Gln Tyr Ala Met
435 440 445
Arg Ala Phe Ala Asp Ala Leu Glu Val Ile Pro Met Ala Leu Ser Glu
450 455 460
Asn Ser Gly Met Asn Pro Ile Gln Thr Met Thr Glu Val Arg Ala Arg
465 470 475 480
Gln Val Lys Glu Ser Asn Pro Ala Leu Gly Ile Asp Cys Leu His Lys
485 490 495
Gly Ser Asn Asp Met Gln Tyr Gln His Val Ile Glu Thr Leu Ile Gly
500 505 510
Lys Lys Gln Gln Ile Ser Leu Ala Thr Gln Met Val Arg Met Ile Leu
515 520 525
Lys Ile Asp Asp Ile Arg Lys Pro Gly Glu Ser Glu Glu
530 535 540
<210> 59
<211> 540
<212> PRT
<213> 黑鼠(Rattus rattus)
<220>
<223> 大鼠 CCT5 (aa) (UniProt Q68FQ0)
<400> 59
Ala Ser Val Gly Thr Leu Ala Phe Asp Glu Tyr Gly Arg Pro Phe Leu
1 5 10 15
Ile Ile Lys Asp Gln Asp Arg Lys Ser Arg Leu Met Gly Leu Glu Ala
20 25 30
Leu Lys Ser His Ile Met Ala Ala Lys Ala Val Ala Asn Thr Met Arg
35 40 45
Thr Ser Leu Gly Pro Asn Gly Leu Asp Lys Met Met Val Asp Lys Asp
50 55 60
Gly Asp Val Thr Val Thr Asn Asp Gly Ala Thr Ile Leu Ser Met Met
65 70 75 80
Asp Val Asp His Gln Ile Ala Lys Leu Met Val Glu Leu Ser Lys Ser
85 90 95
Gln Asp Asp Glu Ile Gly Asp Gly Thr Thr Gly Val Val Val Leu Ala
100 105 110
Gly Ala Leu Leu Glu Glu Ala Glu Gln Leu Leu Asp Arg Gly Ile His
115 120 125
Pro Ile Arg Ile Ala Asp Gly Tyr Glu Gln Ala Ala Arg Ile Ala Ile
130 135 140
Gln His Leu Asp Lys Ile Ser Asp Asn Val Leu Val Asp Ile Asn Asn
145 150 155 160
Pro Glu Pro Leu Ile Gln Thr Ala Lys Thr Thr Leu Gly Ser Lys Val
165 170 175
Val Asn Ser Cys His Arg Gln Met Ala Glu Ile Ala Val Asn Ala Val
180 185 190
Leu Thr Val Ala Asp Met Glu Arg Arg Asp Val Asp Phe Glu Leu Ile
195 200 205
Lys Val Glu Gly Lys Val Gly Gly Arg Leu Glu Asp Thr Lys Leu Ile
210 215 220
Lys Gly Val Ile Val Asp Lys Asp Phe Ser His Pro Gln Met Pro Lys
225 230 235 240
Glu Val Leu Asn Ala Lys Ile Ala Ile Leu Thr Cys Pro Phe Glu Pro
245 250 255
Pro Lys Pro Lys Thr Lys His Lys Leu Asp Val Thr Ser Val Glu Asp
260 265 270
Tyr Lys Ala Leu Gln Lys Tyr Glu Lys Glu Lys Phe Glu Glu Met Ile
275 280 285
Ala Gln Ile Lys Glu Thr Gly Ala Asn Leu Ala Ile Cys Gln Trp Gly
290 295 300
Phe Asp Asp Glu Ala Asn His Leu Leu Leu Gln Asn Gly Leu Pro Ala
305 310 315 320
Val Arg Trp Val Gly Gly Pro Glu Ile Glu Leu Ile Ala Ile Ala Thr
325 330 335
Gly Gly Arg Ile Val Pro Arg Phe Ser Glu Leu Thr Ser Glu Lys Leu
340 345 350
Gly Phe Ala Gly Val Val Arg Glu Ile Ser Phe Gly Thr Thr Lys Asp
355 360 365
Lys Met Leu Val Ile Glu Gln Cys Lys Asn Ser Arg Ala Val Thr Ile
370 375 380
Phe Ile Arg Gly Gly Asn Lys Met Ile Ile Glu Glu Ala Lys Arg Ser
385 390 395 400
Leu His Asp Ala Leu Cys Val Ile Arg Asn Leu Ile Arg Asp Asn Arg
405 410 415
Val Val Tyr Gly Gly Gly Ala Ala Glu Ile Ser Cys Ala Leu Ala Val
420 425 430
Ser Gln Glu Ala Asp Lys Cys Pro Thr Leu Glu Gln Tyr Ala Met Arg
435 440 445
Ala Phe Ala Asp Ala Leu Glu Val Ile Pro Met Ala Leu Ser Glu Asn
450 455 460
Ser Gly Met Asn Pro Ile Gln Thr Met Thr Glu Val Arg Ala Arg Gln
465 470 475 480
Val Lys Glu Ser Asn Pro Ala Leu Gly Ile Asp Cys Leu His Lys Gly
485 490 495
Ser Asn Asp Met Gln Tyr Gln His Val Ile Glu Thr Leu Ile Gly Lys
500 505 510
Lys Gln Gln Ile Ser Leu Ala Thr Gln Met Val Arg Met Ile Leu Lys
515 520 525
Ile Asp Asp Ile Arg Lys Pro Gly Glu Ser Glu Glu
530 535 540
<210> 60
<211> 112
<212> PRT
<213> 智人(Homo sapiens)
<220>
<223> CD3-ζ来源的细胞内信号传导结构域
(aa)
<400> 60
Arg Val Lys Phe Ser Arg Ser Ala Asp Ala Pro Ala Tyr Lys Gln Gly
1 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
50 55 60
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
65 70 75 80
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
85 90 95
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<210> 61
<211> 41
<212> PRT
<213> 智人(Homo sapiens)
<220>
<223> CD28 (P10747的氨基酸180-220)智人
<400> 61
Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr
1 5 10 15
Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro
20 25 30
Pro Arg Asp Phe Ala Ala Tyr Arg Ser
35 40
<210> 62
<211> 16
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> CD3-ζ来源的细胞内信号传导结构域
(aa)
<400> 62
Met Pro Leu Leu Leu Leu Leu Pro Leu Leu Trp Ala Gly Ala Leu Ala
1 5 10 15
<210> 63
<211> 41
<212> PRT
<213> 智人(Homo sapiens)
<220>
<223> CD28 (LL至GG) 智人
<400> 63
Arg Ser Lys Arg Ser Arg Gly Gly His Ser Asp Tyr Met Asn Met Thr
1 5 10 15
Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro
20 25 30
Pro Arg Asp Phe Ala Ala Tyr Arg Ser
35 40
<210> 64
<211> 4
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> 肽接头
<400> 64
Ala Leu Ala Ala
1
<210> 65
<211> 357
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> EGFRt
<400> 65
Met Leu Leu Leu Val Thr Ser Leu Leu Leu Cys Glu Leu Pro His Pro
1 5 10 15
Ala Phe Leu Leu Ile Pro Arg Lys Val Cys Asn Gly Ile Gly Ile Gly
20 25 30
Glu Phe Lys Asp Ser Leu Ser Ile Asn Ala Thr Asn Ile Lys His Phe
35 40 45
Lys Asn Cys Thr Ser Ile Ser Gly Asp Leu His Ile Leu Pro Val Ala
50 55 60
Phe Arg Gly Asp Ser Phe Thr His Thr Pro Pro Leu Asp Pro Gln Glu
65 70 75 80
Leu Asp Ile Leu Lys Thr Val Lys Glu Ile Thr Gly Phe Leu Leu Ile
85 90 95
Gln Ala Trp Pro Glu Asn Arg Thr Asp Leu His Ala Phe Glu Asn Leu
100 105 110
Glu Ile Ile Arg Gly Arg Thr Lys Gln His Gly Gln Phe Ser Leu Ala
115 120 125
Val Val Ser Leu Asn Ile Thr Ser Leu Gly Leu Arg Ser Leu Lys Glu
130 135 140
Ile Ser Asp Gly Asp Val Ile Ile Ser Gly Asn Lys Asn Leu Cys Tyr
145 150 155 160
Ala Asn Thr Ile Asn Trp Lys Lys Leu Phe Gly Thr Ser Gly Gln Lys
165 170 175
Thr Lys Ile Ile Ser Asn Arg Gly Glu Asn Ser Cys Lys Ala Thr Gly
180 185 190
Gln Val Cys His Ala Leu Cys Ser Pro Glu Gly Cys Trp Gly Pro Glu
195 200 205
Pro Arg Asp Cys Val Ser Cys Arg Asn Val Ser Arg Gly Arg Glu Cys
210 215 220
Val Asp Lys Cys Asn Leu Leu Glu Gly Glu Pro Arg Glu Phe Val Glu
225 230 235 240
Asn Ser Glu Cys Ile Gln Cys His Pro Glu Cys Leu Pro Gln Ala Met
245 250 255
Asn Ile Thr Cys Thr Gly Arg Gly Pro Asp Asn Cys Ile Gln Cys Ala
260 265 270
His Tyr Ile Asp Gly Pro His Cys Val Lys Thr Cys Pro Ala Gly Val
275 280 285
Met Gly Glu Asn Asn Thr Leu Val Trp Lys Tyr Ala Asp Ala Gly His
290 295 300
Val Cys His Leu Cys His Pro Asn Cys Thr Tyr Gly Cys Thr Gly Pro
305 310 315 320
Gly Leu Glu Gly Cys Pro Thr Asn Gly Pro Lys Ile Pro Ser Ile Ala
325 330 335
Thr Gly Met Val Gly Ala Leu Leu Leu Leu Leu Val Val Ala Leu Gly
340 345 350
Ile Gly Leu Phe Met
355
<210> 66
<211> 335
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> EGFRt
<400> 66
Arg Lys Val Cys Asn Gly Ile Gly Ile Gly Glu Phe Lys Asp Ser Leu
1 5 10 15
Ser Ile Asn Ala Thr Asn Ile Lys His Phe Lys Asn Cys Thr Ser Ile
20 25 30
Ser Gly Asp Leu His Ile Leu Pro Val Ala Phe Arg Gly Asp Ser Phe
35 40 45
Thr His Thr Pro Pro Leu Asp Pro Gln Glu Leu Asp Ile Leu Lys Thr
50 55 60
Val Lys Glu Ile Thr Gly Phe Leu Leu Ile Gln Ala Trp Pro Glu Asn
65 70 75 80
Arg Thr Asp Leu His Ala Phe Glu Asn Leu Glu Ile Ile Arg Gly Arg
85 90 95
Thr Lys Gln His Gly Gln Phe Ser Leu Ala Val Val Ser Leu Asn Ile
100 105 110
Thr Ser Leu Gly Leu Arg Ser Leu Lys Glu Ile Ser Asp Gly Asp Val
115 120 125
Ile Ile Ser Gly Asn Lys Asn Leu Cys Tyr Ala Asn Thr Ile Asn Trp
130 135 140
Lys Lys Leu Phe Gly Thr Ser Gly Gln Lys Thr Lys Ile Ile Ser Asn
145 150 155 160
Arg Gly Glu Asn Ser Cys Lys Ala Thr Gly Gln Val Cys His Ala Leu
165 170 175
Cys Ser Pro Glu Gly Cys Trp Gly Pro Glu Pro Arg Asp Cys Val Ser
180 185 190
Cys Arg Asn Val Ser Arg Gly Arg Glu Cys Val Asp Lys Cys Asn Leu
195 200 205
Leu Glu Gly Glu Pro Arg Glu Phe Val Glu Asn Ser Glu Cys Ile Gln
210 215 220
Cys His Pro Glu Cys Leu Pro Gln Ala Met Asn Ile Thr Cys Thr Gly
225 230 235 240
Arg Gly Pro Asp Asn Cys Ile Gln Cys Ala His Tyr Ile Asp Gly Pro
245 250 255
His Cys Val Lys Thr Cys Pro Ala Gly Val Met Gly Glu Asn Asn Thr
260 265 270
Leu Val Trp Lys Tyr Ala Asp Ala Gly His Val Cys His Leu Cys His
275 280 285
Pro Asn Cys Thr Tyr Gly Cys Thr Gly Pro Gly Leu Glu Gly Cys Pro
290 295 300
Thr Asn Gly Pro Lys Ile Pro Ser Ile Ala Thr Gly Met Val Gly Ala
305 310 315 320
Leu Leu Leu Leu Leu Val Val Ala Leu Gly Ile Gly Leu Phe Met
325 330 335
<210> 67
<211> 112
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> CD3-ζ来源的细胞内信号传导结构域
(aa)
<400> 67
Arg Val Lys Phe Ser Arg Ser Ala Glu Pro Pro Ala Tyr Gln Gln Gly
1 5 10 15
Gln Asn Gln Leu Tyr Asn Glu Leu Asn Leu Gly Arg Arg Glu Glu Tyr
20 25 30
Asp Val Leu Asp Lys Arg Arg Gly Arg Asp Pro Glu Met Gly Gly Lys
35 40 45
Pro Arg Arg Lys Asn Pro Gln Glu Gly Leu Tyr Asn Glu Leu Gln Lys
50 55 60
Asp Lys Met Ala Glu Ala Tyr Ser Glu Ile Gly Met Lys Gly Glu Arg
65 70 75 80
Arg Arg Gly Lys Gly His Asp Gly Leu Tyr Gln Gly Leu Ser Thr Ala
85 90 95
Thr Lys Asp Thr Tyr Asp Ala Leu His Met Gln Ala Leu Pro Pro Arg
100 105 110
<210> 68
<211> 8
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> 表位
<220>
<221> 变体
<222> 1, 5, 6, 8
<223> Xaa =任何氨基酸
<400> 68
Xaa Ser Val Glu Xaa Xaa Lys Xaa
1 5
<210> 69
<211> 8
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> 表位
<220>
<221> 变体
<222> 1
<223> Xaa = Thr、Ser或Asp
<220>
<221> 变体
<222> 2
<223> Xaa = Asp或Ala
<220>
<221> 变体
<222> 3
<223> Xaa = Tyr、Phe或Ile
<220>
<221> 变体
<222> 4
<223> Xaa = Ala或Arg
<400> 69
Xaa Ser Val Glu Xaa Xaa Lys Xaa
1 5
<210> 70
<211> 8
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> 表位
<400> 70
Thr Ser Val Glu Asp Tyr Lys Ala
1 5
<210> 71
<211> 8
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> 表位
<400> 71
Ser Ser Val Glu Ala Phe Lys Arg
1 5
<210> 72
<211> 8
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> 表位
<400> 72
Asp Ser Val Glu Ala Ile Lys Ala
1 5
<210> 73
<211> 245
<212> PRT
<213> 人工序列
<220>
<223>异株泻根毒蛋白
<400> 73
Asp Val Ser Phe Arg Leu Ser Gly Ala Thr Thr Thr Ser Tyr Gly Val
1 5 10 15
Phe Ile Lys Asn Leu Arg Glu Ala Leu Pro Tyr Glu Arg Lys Val Tyr
20 25 30
Asn Ile Pro Leu Leu Arg Ser Ser Ile Ser Gly Arg Tyr Thr Leu Leu
35 40 45
His Leu Thr Asn Tyr Ala Asp Glu Thr Ile Ser Val Ala Val Asp Val
50 55 60
Thr Asn Val Tyr Ile Met Gly Tyr Leu Ala Gly Asp Val Ser Tyr Phe
65 70 75 80
Phe Asn Glu Ala Ser Ala Thr Glu Ala Ala Lys Phe Val Phe Lys Asp
85 90 95
Ala Lys Lys Lys Val Thr Leu Pro Tyr Ser Gly Asn Tyr Glu Arg Leu
100 105 110
Gln Thr Ala Ala Gly Lys Ile Arg Glu Asn Ile Pro Leu Gly Leu Pro
115 120 125
Ala Leu Asp Ser Ala Ile Thr Thr Leu Tyr Tyr Tyr Thr Ala Ser Ser
130 135 140
Ala Ala Ser Ala Leu Leu Val Leu Ile Gln Ser Thr Ala Glu Ser Ala
145 150 155 160
Arg Tyr Lys Phe Ile Glu Gln Gln Ile Gly Lys Arg Val Asp Lys Thr
165 170 175
Phe Leu Pro Ser Leu Ala Thr Ile Ser Leu Glu Asn Asn Trp Ser Ala
180 185 190
Leu Ser Lys Gln Ile Gln Ile Ala Ser Thr Asn Asn Gly Gln Phe Glu
195 200 205
Ser Pro Val Val Leu Ile Asp Gly Asn Asn Gln Arg Val Ser Ile Thr
210 215 220
Asn Ala Ser Ala Arg Val Val Thr Ser Asn Ile Ala Leu Leu Leu Asn
225 230 235 240
Arg Asn Asn Ile Ala
245
<210> 74
<211> 39
<212> PRT
<213> 人工序列
<220>
<223> CD28胞外结构域间隔子(aa)
<400> 74
Ile Glu Val Met Tyr Pro Pro Pro Tyr Leu Asp Asn Glu Lys Ser Asn
1 5 10 15
Gly Thr Ile Ile His Val Lys Gly Lys His Leu Cys Pro Ser Pro Leu
20 25 30
Phe Pro Gly Pro Ser Lys Pro
35
<210> 75
<211> 274
<212> PRT
<213> 人工序列
<220>
<223> 皂草素-6
<400> 75
Val Thr Ser Ile Thr Leu Asp Leu Val Asn Pro Thr Ala Gly Gln Tyr
1 5 10 15
Ser Ser Phe Val Asp Lys Ile Arg Asn Asn Val Lys Asp Pro Asn Leu
20 25 30
Lys Tyr Gly Gly Thr Asp Ile Ala Val Ile Pro Pro Ser Lys Glu Lys
35 40 45
Phe Leu Arg Ile Asn Phe Gln Ser Ser Arg Gly Thr Val Ser Leu Gly
50 55 60
Leu Lys Arg Asp Asn Leu Tyr Val Val Ala Tyr Leu Ala Met Asp Asn
65 70 75 80
Thr Asn Val Asn Arg Ala Tyr Tyr Phe Arg Ser Glu Ile Thr Ser Ala
85 90 95
Glu Ser Thr Ala Leu Phe Pro Glu Ala Thr Thr Ala Asn Gln Lys Ala
100 105 110
Leu Glu Tyr Thr Glu Asp Tyr Gln Ser Ile Glu Lys Asn Ala Gln Ile
115 120 125
Thr Gln Gly Asp Gln Ser Arg Lys Glu Leu Gly Leu Gly Ile Asp Leu
130 135 140
Leu Ser Thr Ser Met Glu Ala Val Asn Lys Lys Ala Arg Val Val Lys
145 150 155 160
Asp Glu Ala Arg Phe Leu Leu Ile Ala Ile Gln Met Thr Ala Glu Ala
165 170 175
Ala Arg Phe Arg Tyr Ile Gln Asn Leu Val Ile Lys Asn Phe Pro Asn
180 185 190
Lys Phe Asn Ser Glu Asn Lys Val Ile Gln Phe Glu Val Asn Trp Lys
195 200 205
Lys Ile Ser Thr Ala Ile Tyr Gly Asp Ala Lys Asn Gly Val Phe Asn
210 215 220
Lys Asp Tyr Asp Phe Gly Phe Gly Lys Val Arg Gln Val Lys Asp Leu
225 230 235 240
Gln Met Gly Leu Leu Met Tyr Leu Gly Lys Pro Lys Ser Ser Asn Glu
245 250 255
Ala Asn Ser Thr Val Arg His Tyr Gly Pro Leu Lys Pro Thr Leu Leu
260 265 270
Ile Thr
<210> 76
<211> 41
<212> PRT
<213> 人工序列
<220>
<223> CD28胞内结构域 (aa)
<400> 76
Arg Ser Lys Arg Ser Arg Leu Leu His Ser Asp Tyr Met Asn Met Thr
1 5 10 15
Pro Arg Arg Pro Gly Pro Thr Arg Lys His Tyr Gln Pro Tyr Ala Pro
20 25 30
Pro Arg Asp Phe Ala Ala Tyr Arg Ser
35 40
<210> 77
<211> 250
<212> PRT
<213> 人工序列
<220>
<223> 抗病毒蛋白 MAP
<400> 77
Ala Pro Thr Leu Glu Thr Ile Ala Ser Leu Asp Leu Asn Asn Pro Thr
1 5 10 15
Thr Tyr Leu Ser Phe Ile Thr Asn Ile Arg Thr Lys Val Ala Asp Lys
20 25 30
Thr Glu Gln Cys Thr Ile Gln Lys Ile Ser Lys Thr Phe Thr Gln Arg
35 40 45
Tyr Ser Tyr Ile Asp Leu Ile Val Ser Ser Thr Gln Lys Ile Thr Leu
50 55 60
Ala Ile Asp Met Ala Asp Leu Tyr Val Leu Gly Tyr Ser Asp Ile Ala
65 70 75 80
Asn Asn Lys Gly Arg Ala Phe Phe Phe Lys Asp Val Thr Glu Ala Val
85 90 95
Ala Asn Asn Phe Phe Pro Gly Ala Thr Gly Thr Asn Arg Ile Lys Leu
100 105 110
Thr Phe Thr Gly Ser Tyr Gly Asp Leu Glu Lys Asn Gly Gly Leu Arg
115 120 125
Lys Asp Asn Pro Leu Gly Ile Phe Arg Leu Glu Asn Ser Ile Val Asn
130 135 140
Ile Tyr Gly Lys Ala Gly Asp Val Lys Lys Gln Ala Lys Phe Phe Leu
145 150 155 160
Leu Ala Ile Gln Met Val Ser Glu Ala Ala Arg Phe Lys Tyr Ile Ser
165 170 175
Asp Lys Ile Pro Ser Glu Lys Tyr Glu Glu Val Thr Val Asp Glu Tyr
180 185 190
Met Thr Ala Leu Glu Asn Asn Trp Ala Lys Leu Ser Thr Ala Val Tyr
195 200 205
Asn Ser Lys Pro Ser Thr Thr Thr Ala Thr Lys Cys Gln Leu Ala Thr
210 215 220
Ser Pro Val Thr Ile Ser Pro Trp Ile Phe Lys Thr Val Glu Glu Ile
225 230 235 240
Lys Leu Val Met Gly Leu Leu Lys Ser Ser
245 250
<210> 78
<211> 66
<212> PRT
<213> 智人(Homo sapiens)
<220>
<223> CD28 (登录号P10747的氨基酸114-179 )
<400> 78
Ile Glu Val Met Tyr Pro Pro Pro Tyr Leu Asp Asn Glu Lys Ser Asn
1 5 10 15
Gly Thr Ile Ile His Val Lys Gly Lys His Leu Cys Pro Ser Pro Leu
20 25 30
Phe Pro Gly Pro Ser Lys Pro Phe Trp Val Leu Val Val Val Gly Gly
35 40 45
Val Leu Ala Cys Tyr Ser Leu Leu Val Thr Val Ala Phe Ile Ile Phe
50 55 60
Trp Val
65
<210> 79
<211> 293
<212> PRT
<213> 人工序列
<220>
<223>志贺毒素A链
<400> 79
Lys Glu Phe Thr Leu Asp Phe Ser Thr Ala Lys Thr Tyr Val Asp Ser
1 5 10 15
Leu Asn Val Ile Arg Ser Ala Ile Gly Thr Pro Leu Gln Thr Ile Ser
20 25 30
Ser Gly Gly Thr Ser Leu Leu Met Ile Asp Ser Gly Thr Gly Asp Asn
35 40 45
Leu Phe Ala Val Asp Val Arg Gly Ile Asp Pro Glu Glu Gly Arg Phe
50 55 60
Asn Asn Leu Arg Leu Ile Val Glu Arg Asn Asn Leu Tyr Val Thr Gly
65 70 75 80
Phe Val Asn Arg Thr Asn Asn Val Phe Tyr Arg Phe Ala Asp Phe Ser
85 90 95
His Val Thr Phe Pro Gly Thr Thr Ala Val Thr Leu Ser Gly Asp Ser
100 105 110
Ser Tyr Thr Thr Leu Gln Arg Val Ala Gly Ile Ser Arg Thr Gly Met
115 120 125
Gln Ile Asn Arg His Ser Leu Thr Thr Ser Tyr Leu Asp Leu Met Ser
130 135 140
His Ser Gly Thr Ser Leu Thr Gln Ser Val Ala Arg Ala Met Leu Arg
145 150 155 160
Phe Val Thr Val Thr Ala Glu Ala Leu Arg Phe Arg Gln Ile Gln Arg
165 170 175
Gly Phe Arg Thr Thr Leu Asp Asp Leu Ser Gly Arg Ser Tyr Val Met
180 185 190
Thr Ala Glu Asp Val Asp Leu Thr Leu Asn Trp Gly Arg Leu Ser Ser
195 200 205
Val Leu Pro Asp Tyr His Gly Gln Asp Ser Val Arg Val Gly Arg Ile
210 215 220
Ser Phe Gly Ser Ile Asn Ala Ile Leu Gly Ser Val Ala Leu Ile Leu
225 230 235 240
Asn Cys His His His Ala Ser Arg Val Ala Arg Met Ala Ser Asp Glu
245 250 255
Phe Pro Ser Met Cys Pro Ala Asp Gly Arg Val Arg Gly Ile Thr His
260 265 270
Asn Lys Ile Leu Trp Asp Ser Ser Thr Leu Gly Ala Ile Leu Met Arg
275 280 285
Arg Thr Ile Ser Ser
290
<210> 80
<211> 319
<212> PRT
<213> 人工序列
<220>
<223>志贺样毒素亚基 A (Vero毒素2)
<400> 80
Met Lys Cys Ile Leu Phe Lys Trp Val Leu Cys Leu Leu Leu Gly Phe
1 5 10 15
Ser Ser Val Ser Tyr Ser Arg Glu Phe Thr Ile Asp Phe Ser Thr Gln
20 25 30
Gln Ser Tyr Val Ser Ser Leu Asn Ser Ile Arg Thr Glu Ile Ser Thr
35 40 45
Pro Leu Glu His Ile Ser Gln Gly Thr Thr Ser Val Ser Val Ile Asn
50 55 60
His Thr Pro Pro Gly Ser Tyr Phe Ala Val Asp Ile Arg Gly Leu Asp
65 70 75 80
Val Tyr Gln Ala Arg Phe Asp His Leu Arg Leu Ile Ile Glu Gln Asn
85 90 95
Asn Leu Tyr Val Ala Gly Phe Val Asn Thr Ala Thr Asn Thr Phe Tyr
100 105 110
Arg Phe Ser Asp Phe Thr His Ile Ser Val Pro Gly Val Thr Thr Val
115 120 125
Ser Met Thr Thr Asp Ser Ser Tyr Thr Thr Leu Gln Arg Val Ala Ala
130 135 140
Leu Glu Arg Ser Gly Met Gln Ile Ser Arg His Ser Leu Val Ser Ser
145 150 155 160
Tyr Leu Ala Leu Met Glu Phe Ser Gly Asn Thr Met Thr Arg Asp Ala
165 170 175
Ser Arg Ala Val Leu Arg Phe Val Thr Val Thr Ala Glu Ala Leu Arg
180 185 190
Phe Arg Gln Ile Gln Arg Glu Phe Arg Gln Ala Leu Ser Glu Thr Ala
195 200 205
Pro Val Tyr Thr Met Thr Pro Gly Asp Val Asp Leu Thr Leu Asn Trp
210 215 220
Gly Arg Ile Ser Asn Val Leu Pro Glu Tyr Arg Gly Glu Asp Gly Val
225 230 235 240
Arg Val Gly Arg Ile Ser Phe Asn Asn Ile Ser Ala Ile Leu Gly Thr
245 250 255
Val Ala Val Ile Leu Asn Cys His His Gln Gly Ala Arg Ser Val Arg
260 265 270
Ala Val Asn Glu Glu Ser Gln Pro Glu Cys Gln Ile Thr Gly Asp Arg
275 280 285
Pro Val Ile Lys Ile Asn Asn Thr Leu Trp Glu Ser Asn Thr Ala Ala
290 295 300
Ala Phe Leu Asn Arg Lys Ser Gln Phe Leu Tyr Thr Thr Gly Lys
305 310 315
<210> 81
<211> 119
<212> PRT
<213> 智人(Homo sapiens)
<220>
<223> IgG4铰链-CH3间隔子(aa)
<400> 81
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Gly Gln Pro Arg
1 5 10 15
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
20 25 30
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
35 40 45
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
50 55 60
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
65 70 75 80
Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
85 90 95
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
100 105 110
Leu Ser Leu Ser Leu Gly Lys
115
<210> 82
<211> 554
<212> DNA
<213> 人工序列
<220>
<223> 合成构建体
<220>
<223> EF1a启动子 (修饰的EF1a启动子)
<400> 82
ggatctgcga tcgctccggt gcccgtcagt gggcagagcg cacatcgccc acagtccccg 60
agaagttggg gggaggggtc ggcaattgaa ccggtgccta gagaaggtgg cgcggggtaa 120
actgggaaag tgatgtcgtg tactggctcc gcctttttcc cgagggtggg ggagaaccgt 180
atataagtgc agtagtcgcc gtgaacgttc tttttcgcaa cgggtttgcc gccagaacac 240
agctgaagct tcgaggggct cgcatctctc cttcacgcgc ccgccgccct acctgaggcc 300
gccatccacg ccggttgagt cgcgttctgc cgcctcccgc ctgtggtgcc tcctgaactg 360
cgtccgccgt ctaggtaagt ttaaagctca ggtcgagacc gggcctttgt ccggcgctcc 420
cttggagcct acctagactc agccggctct ccacgctttg cctgaccctg cttgctcaac 480
tctacgtctt tgtttcgttt tctgttctgc gccgttacag atccaagctg tgaccggcgc 540
ctacggctag cgcc 554
<210> 83
<211> 541
<212> PRT
<213> 小家鼠(Mus musculus)
<220>
<223> 小鼠CCT5 (aa) (UniProt P80316)
<400> 83
Met Ala Ser Val Gly Thr Leu Ala Phe Asp Glu Tyr Gly Arg Pro Phe
1 5 10 15
Leu Ile Ile Lys Asp Gln Asp Arg Lys Ser Arg Leu Met Gly Leu Glu
20 25 30
Ala Leu Lys Ser His Ile Met Ala Ala Lys Ala Val Ala Asn Thr Met
35 40 45
Arg Thr Ser Leu Gly Pro Asn Gly Leu Asp Lys Met Met Val Asp Lys
50 55 60
Asp Gly Asp Val Thr Ile Thr Asn Asp Gly Ala Thr Ile Leu Ser Met
65 70 75 80
Met Asp Val Asp His Gln Ile Ala Lys Leu Met Val Glu Leu Ser Lys
85 90 95
Ser Gln Asp Asp Glu Ile Gly Asp Gly Thr Thr Gly Val Val Val Leu
100 105 110
Ala Gly Ala Leu Leu Glu Glu Ala Glu Gln Leu Leu Asp Arg Gly Ile
115 120 125
His Pro Ile Arg Ile Ala Asp Gly Tyr Glu Gln Ala Ala Arg Ile Ala
130 135 140
Ile Gln His Leu Asp Lys Ile Ser Asp Lys Val Leu Val Asp Ile Asn
145 150 155 160
Asn Pro Glu Pro Leu Ile Gln Thr Ala Lys Thr Thr Leu Gly Ser Lys
165 170 175
Val Ile Asn Ser Cys His Arg Gln Met Ala Glu Ile Ala Val Asn Ala
180 185 190
Val Leu Thr Val Ala Asp Met Glu Arg Arg Asp Val Asp Phe Glu Leu
195 200 205
Ile Lys Val Glu Gly Lys Val Gly Gly Arg Leu Glu Asp Thr Lys Leu
210 215 220
Ile Lys Gly Val Ile Val Asp Lys Asp Phe Ser His Pro Gln Met Pro
225 230 235 240
Lys Lys Val Val Asp Ala Lys Ile Ala Ile Leu Thr Cys Pro Phe Glu
245 250 255
Pro Pro Lys Pro Lys Thr Lys His Lys Leu Asp Val Met Ser Val Glu
260 265 270
Asp Tyr Lys Ala Leu Gln Lys Tyr Glu Lys Glu Lys Phe Glu Glu Met
275 280 285
Ile Lys Gln Ile Lys Glu Thr Gly Ala Asn Leu Ala Ile Cys Gln Trp
290 295 300
Gly Phe Asp Asp Glu Ala Asn His Leu Leu Leu Gln Asn Gly Leu Pro
305 310 315 320
Ala Val Arg Trp Val Gly Gly Pro Glu Ile Glu Leu Ile Ala Ile Ala
325 330 335
Thr Gly Gly Arg Ile Val Pro Arg Phe Ser Glu Leu Thr Ser Glu Lys
340 345 350
Leu Gly Phe Ala Gly Val Val Gln Glu Ile Ser Phe Gly Thr Thr Lys
355 360 365
Asp Lys Met Leu Val Ile Glu Lys Cys Lys Asn Ser Arg Ala Val Thr
370 375 380
Ile Phe Ile Arg Gly Gly Asn Lys Met Ile Ile Glu Glu Ala Lys Arg
385 390 395 400
Ser Leu His Asp Ala Leu Cys Val Ile Arg Asn Leu Ile Arg Asp Asn
405 410 415
Arg Val Val Tyr Gly Gly Gly Ala Ala Glu Ile Ser Cys Ala Leu Ala
420 425 430
Val Ser Gln Glu Ala Asp Lys Cys Pro Thr Leu Glu Gln Tyr Ala Met
435 440 445
Arg Ala Phe Ala Asp Ala Leu Glu Val Ile Pro Met Ala Leu Ser Glu
450 455 460
Asn Ser Gly Met Asn Pro Ile Gln Thr Met Thr Glu Val Arg Ala Arg
465 470 475 480
Gln Val Lys Glu Ser Asn Pro Ala Leu Gly Ile Asp Cys Leu His Lys
485 490 495
Gly Ser Asn Asp Met Gln Tyr Gln His Val Ile Glu Thr Leu Ile Gly
500 505 510
Lys Lys Gln Gln Ile Ser Leu Ala Thr Gln Met Val Arg Met Ile Leu
515 520 525
Lys Ile Asp Asp Ile Arg Lys Pro Gly Glu Ser Glu Glu
530 535 540
<210> 84
<211> 540
<212> PRT
<213> 小家鼠(Mus musculus)
<220>
<223>小鼠CCT5 (aa) (UniProt P80316)
<400> 84
Ala Ser Val Gly Thr Leu Ala Phe Asp Glu Tyr Gly Arg Pro Phe Leu
1 5 10 15
Ile Ile Lys Asp Gln Asp Arg Lys Ser Arg Leu Met Gly Leu Glu Ala
20 25 30
Leu Lys Ser His Ile Met Ala Ala Lys Ala Val Ala Asn Thr Met Arg
35 40 45
Thr Ser Leu Gly Pro Asn Gly Leu Asp Lys Met Met Val Asp Lys Asp
50 55 60
Gly Asp Val Thr Ile Thr Asn Asp Gly Ala Thr Ile Leu Ser Met Met
65 70 75 80
Asp Val Asp His Gln Ile Ala Lys Leu Met Val Glu Leu Ser Lys Ser
85 90 95
Gln Asp Asp Glu Ile Gly Asp Gly Thr Thr Gly Val Val Val Leu Ala
100 105 110
Gly Ala Leu Leu Glu Glu Ala Glu Gln Leu Leu Asp Arg Gly Ile His
115 120 125
Pro Ile Arg Ile Ala Asp Gly Tyr Glu Gln Ala Ala Arg Ile Ala Ile
130 135 140
Gln His Leu Asp Lys Ile Ser Asp Lys Val Leu Val Asp Ile Asn Asn
145 150 155 160
Pro Glu Pro Leu Ile Gln Thr Ala Lys Thr Thr Leu Gly Ser Lys Val
165 170 175
Ile Asn Ser Cys His Arg Gln Met Ala Glu Ile Ala Val Asn Ala Val
180 185 190
Leu Thr Val Ala Asp Met Glu Arg Arg Asp Val Asp Phe Glu Leu Ile
195 200 205
Lys Val Glu Gly Lys Val Gly Gly Arg Leu Glu Asp Thr Lys Leu Ile
210 215 220
Lys Gly Val Ile Val Asp Lys Asp Phe Ser His Pro Gln Met Pro Lys
225 230 235 240
Lys Val Val Asp Ala Lys Ile Ala Ile Leu Thr Cys Pro Phe Glu Pro
245 250 255
Pro Lys Pro Lys Thr Lys His Lys Leu Asp Val Met Ser Val Glu Asp
260 265 270
Tyr Lys Ala Leu Gln Lys Tyr Glu Lys Glu Lys Phe Glu Glu Met Ile
275 280 285
Lys Gln Ile Lys Glu Thr Gly Ala Asn Leu Ala Ile Cys Gln Trp Gly
290 295 300
Phe Asp Asp Glu Ala Asn His Leu Leu Leu Gln Asn Gly Leu Pro Ala
305 310 315 320
Val Arg Trp Val Gly Gly Pro Glu Ile Glu Leu Ile Ala Ile Ala Thr
325 330 335
Gly Gly Arg Ile Val Pro Arg Phe Ser Glu Leu Thr Ser Glu Lys Leu
340 345 350
Gly Phe Ala Gly Val Val Gln Glu Ile Ser Phe Gly Thr Thr Lys Asp
355 360 365
Lys Met Leu Val Ile Glu Lys Cys Lys Asn Ser Arg Ala Val Thr Ile
370 375 380
Phe Ile Arg Gly Gly Asn Lys Met Ile Ile Glu Glu Ala Lys Arg Ser
385 390 395 400
Leu His Asp Ala Leu Cys Val Ile Arg Asn Leu Ile Arg Asp Asn Arg
405 410 415
Val Val Tyr Gly Gly Gly Ala Ala Glu Ile Ser Cys Ala Leu Ala Val
420 425 430
Ser Gln Glu Ala Asp Lys Cys Pro Thr Leu Glu Gln Tyr Ala Met Arg
435 440 445
Ala Phe Ala Asp Ala Leu Glu Val Ile Pro Met Ala Leu Ser Glu Asn
450 455 460
Ser Gly Met Asn Pro Ile Gln Thr Met Thr Glu Val Arg Ala Arg Gln
465 470 475 480
Val Lys Glu Ser Asn Pro Ala Leu Gly Ile Asp Cys Leu His Lys Gly
485 490 495
Ser Asn Asp Met Gln Tyr Gln His Val Ile Glu Thr Leu Ile Gly Lys
500 505 510
Lys Gln Gln Ile Ser Leu Ala Thr Gln Met Val Arg Met Ile Leu Lys
515 520 525
Ile Asp Asp Ile Arg Lys Pro Gly Glu Ser Glu Glu
530 535 540
<210> 85
<211> 4
<212> PRT
<213> 人工序列
<220>
<223> 合成构建体
<220>
<221> 变体
<222> 1
<223> Xaa = Lys或Arg
<220>
<221> 重复序列
<222> (1)...(4)
<223> XDEL 重复1至6 次
<220>
<223> 示例性分选信号
<400> 85
Xaa Asp Glu Leu
1
<210> 86
<211> 247
<212> PRT
<213> 人工序列
<220>
<223> 天花粉蛋白
<400> 86
Asp Val Ser Phe Arg Leu Ser Gly Ala Thr Ser Ser Ser Tyr Gly Val
1 5 10 15
Phe Ile Ser Asn Leu Arg Lys Ala Leu Pro Asn Glu Arg Lys Leu Tyr
20 25 30
Asp Ile Pro Leu Leu Arg Ser Ser Leu Pro Gly Ser Gln Arg Tyr Ala
35 40 45
Leu Ile His Leu Thr Asn Tyr Ala Asp Glu Thr Ile Ser Val Ala Ile
50 55 60
Asp Val Thr Asn Val Tyr Ile Met Gly Tyr Arg Ala Gly Asp Thr Ser
65 70 75 80
Tyr Phe Phe Asn Glu Ala Ser Ala Thr Glu Ala Ala Lys Tyr Val Phe
85 90 95
Lys Asp Ala Met Arg Lys Val Thr Leu Pro Tyr Ser Gly Asn Tyr Glu
100 105 110
Arg Leu Gln Thr Ala Ala Gly Lys Ile Arg Glu Asn Ile Pro Leu Gly
115 120 125
Leu Pro Ala Leu Asp Ser Ala Ile Thr Thr Leu Phe Tyr Tyr Asn Ala
130 135 140
Asn Ser Ala Ala Ser Ala Leu Met Val Leu Ile Gln Ser Thr Ser Glu
145 150 155 160
Ala Ala Arg Tyr Lys Phe Ile Glu Gln Gln Ile Gly Lys Arg Val Asp
165 170 175
Lys Thr Phe Leu Pro Ser Leu Ala Ile Ile Ser Leu Glu Asn Ser Trp
180 185 190
Ser Ala Leu Ser Lys Gln Ile Gln Ile Ala Ser Thr Asn Asn Gly Gln
195 200 205
Phe Glu Ser Pro Val Val Leu Ile Asn Ala Gln Asn Gln Arg Val Thr
210 215 220
Ile Thr Asn Val Asp Ala Gly Val Val Thr Ser Asn Ile Ala Leu Leu
225 230 235 240
Leu Asn Arg Asn Asn Met Ala
245
