一种龙葵醛/龙葵醇的生产方法及其生产系统
文献发布时间:2023-06-19 19:28:50
技术领域
本发明涉及精细品化工技术领域,具体地说,是涉及一种龙葵醛/龙葵醇的生产方法及其生产系统。
背景技术
龙葵醛(2-苯基丙醛)其外观呈无色液体,微溶于水,溶于乙醇等有机溶剂。目前主要作为香料使用,其具有强烈的风信子清新花香香气,主要用于风信子、紫丁香、百合等日用香精中,在食用香精中也可微量使用。同时龙葵醛还广泛应用于医药、染料及农药等行业。目前自然界中尚未发现天然的龙葵醛来源,需要通过人工合成。龙葵醇(2-苯基丙醇)也具有金银花和风信子香气,可以用于配制香精。龙葵醇通常由龙葵醛用醇铝还原等方法得到。
目前,常用的合成龙葵醛的方法主要有三种:
一是采用苯乙酮和氯乙酸乙酯发生Dazens反应的方法,具体过程是苯乙酮和氯乙酸乙酯在强碱如乙醇钠的作用下制得甲基苯基环氧丙酸酯,该酯经皂化、中和、水解成酸,再将酸加热分解得龙葵醛。该方法是目前工业生产龙葵醛最常用的工艺路线,但是在反应中需要用到乙醇钠,生产条件比较苛刻。而且反应过程中会生成大量酸碱废水。
二是以苯并咪唑盐与格氏试剂为原料合成龙葵醛。苯并咪唑盐与苯基乙基溴化镁加成生成苯并咪唑烷中间体,在酸性条件下水解便可得到龙葵醛。但该方法使用的苯并咪唑盐原料和格氏试剂制备步骤多,路线长,条件苛刻。致使这种合成方法不太容易应用于实际生产。
三是通过环氧化α-甲基苯乙烯得到2-苯基-1,2环氧丙烷(α-甲基环氧苯乙烷),2-苯基-1,2环氧丙烷经异构化为龙葵醛。环氧化甲基苯乙烯采用过氧乙酸为氧化剂。该路线较之传统的苯乙酮经环氧丙酸酯的合成路线来说优势在于步骤少、原料价廉易得、成本低、总产率高。但是由于过氧乙酸需要通过双氧水制备,并且具有强腐蚀性和强刺激性,对化工设备要求较高,这个工艺在实际应用上困难较多。
除以上三种方法外,也可以用2-苯基-1,2丙二醇为原料,经氧化生成2-苯基-1,2环氧丙烷,再分解生成龙葵醛,该方法产率较高,但是反应温度要求苛刻(-78℃),实用化的难度更高。
从现有技术看,龙葵醛的生产路线或者需要比较特殊的反应原料和催化剂,或者条件比较苛刻。其中,α-甲基苯乙烯环氧化路线相对来说具有一定的优势,但是氧化剂选择过氧乙酸仍有较多问题,可以进一步改进。
发明内容
针对现有技术中存在的上述问题,本发明提出一种龙葵醛/龙葵醇的生产方法,以异丙苯为主要原料,可用于生产龙葵醛和龙葵醇。
本发明目的之一为提供一种龙葵醛/龙葵醇的生产方法,包括以下步骤:
a)将异丙苯氧化为过氧化氢异丙苯;
b)以异丙苯作为溶剂,过氧化氢异丙苯作为氧化剂,将α-甲基苯乙烯氧化为2-苯基-1,2环氧丙烷,同时得到α,α-二甲基苄醇;
c)对步骤b)得到的产物进行异构化反应和脱水反应,以将2-苯基-1,2环氧丙烷生成龙葵醛和将α,α-二甲基苄醇生成α-甲基苯乙烯;
d)将步骤c)得到的产物中的龙葵醛、α-甲基苯乙烯、异丙苯进行分离;
任选地,e)将完全经过步骤c)的物料或仅经过步骤c)异构化反应的物料中的一部分进行选择性氢解反应,得到龙葵醇和异丙苯。
本发明生产方法中,步骤a)中,采用气液反应,使用空气或者富氧空气将异丙苯氧化得到过氧化氢异丙苯溶液,其中所述过氧化氢异丙苯溶液的浓度优选为1~85wt%,更优选为10~55wt%。
本发明生产方法中,步骤a)中,异丙苯中的一部分可来源于步骤d)和步骤e)返回的异丙苯。
本发明生产方法中,步骤b)中,采用液相反应,优选在催化剂存在下进行氧化反应将α-甲基苯乙烯氧化为2-苯基-1,2环氧丙烷,其中所述催化剂可采用烯烃环氧化反应中比较常见的催化剂,优选为含钛和/或钼的分子筛、杂多酸、复合氧化物、可溶性配合物中的至少一种;所述催化剂的用量为通常用量。
本发明生产方法中,步骤b)中,所述液相反应的温度优选为40~120℃;反应压力优选为1~5MPaG。
本发明生产方法中,步骤b)中,α-甲基苯乙烯与过氧化氢异丙苯的摩尔比为(1:1)~(10:1),优选为(3:1)~(6:1)。
本发明生产方法中,步骤b)中,α-甲基苯乙烯来源于新鲜的α-甲基苯乙烯、以及步骤d)返回的α-甲基苯乙烯。
本发明生产方法中,步骤c)中,2-苯基-1,2环氧丙烷的异构化反应和α,α-二甲基苄醇的脱水反应可以一步同时进行,也可以分步进行。2-苯基-1,2环氧丙烷的异构化反应可以不需要催化剂,α,α-二甲基苄醇的脱水反应需要酸性催化剂。
当两个反应一步同时进行时,在酸性催化剂存在下进行,其中反应优选在150~250℃下进行。
当两个反应分步进行时,优选先进行2-苯基-1,2环氧丙烷的异构化反应,再进行α,α-二甲基苄醇的脱水反应,其中脱水反应在酸性催化剂存在下进行。其中,2-苯基-1,2环氧丙烷的异构化反应优选在80~250℃下进行;α,α-二甲基苄醇的脱水反应优选在150~250℃下进行。
以上所述酸性催化剂采用通常脱水反应常用的非均相的固体酸催化剂,优选为γ-Al
本发明生产方法中,步骤d)中,优选通过精馏将龙葵醛与α-甲基苯乙烯和异丙苯分离。
其中,将得到的α-甲基苯乙烯和异丙苯进行完全分离,或者进行部分分离以保留一部分异丙苯溶解α-甲基苯乙烯;其中,分离的α-甲基苯乙烯返回步骤b);分离的异丙苯返回步骤a)或者流出。
本发明生产方法中,步骤e)中,可以将完全经过步骤c)异构化反应和脱水反应后的物料(即包含龙葵醛、α-甲基苯乙烯和异丙苯)中的一部分进行选择性氢解反应,得到龙葵醇和异丙苯;
或者也可以将仅经过步骤c)异构化反应的物料(即包含龙葵醛、α,α-二甲基苄醇、α-甲基苯乙烯和异丙苯)中的一部分进行选择性氢解反应,得到龙葵醇和异丙苯。
所述氢解反应优选在选择性氢解催化剂的存在下进行得到龙葵醇和异丙苯,其中所述选择性氢解催化剂采用通常的氢解反应催化剂,优选为Pd/Al
本发明生产方法中,进一步地通过精馏将龙葵醇与异丙苯分离。其中,异丙苯可返回步骤a)或者流出。
本发明目的之二为提供一种龙葵醛/龙葵醇的生产系统,用于所述的生产方法,包括:
第一反应器;其配置成接收异丙苯、和空气或富氧空气,以及排放包含异丙苯和过氧化氢异丙苯的第一反应物流。其中,第一反应器还可以配置成能够排放尾气;所述异丙苯包括新鲜异丙苯和返回的异丙苯。
第二反应器;其配置成接收第一反应物流和α-甲基苯乙烯,以及排放第二反应物流;其中所述第二反应物流主要包含2-苯基-1,2环氧丙烷、α,α-二甲基苄醇、α-甲基苯乙烯和异丙苯。其中,所述α-甲基苯乙烯包括新鲜α-甲基苯乙烯和返回的α-甲基苯乙烯。
第三反应系统;其配置成接收第二反应物流,以及排放第三反应物流;其中所述第三反应物流包含龙葵醛、α-甲基苯乙烯和异丙苯。
第一分离装置;其配置成接收第三反应物流,以及排放龙葵醛和包含α-甲基苯乙烯和异丙苯的物流。
第二分离装置;其配置成接收第一分离装置流出的包含α-甲基苯乙烯和异丙苯的物流,以及排放α-甲基苯乙烯和异丙苯。
其中,所述第三反应系统包括第三反应器,其配置成接收第二反应物流,以及排放包含龙葵醛、α-甲基苯乙烯和异丙苯的第三反应物流;
或者所述第三反应系统包括第三反应器和第四反应器,其中第三反应器,其配置成接收第二反应物流,以及排放包含龙葵醛、α,α-二甲基苄醇、α-甲基苯乙烯和异丙苯的物流;第四反应器,其配置成接收第三反应器排放的物流,以及排放包含龙葵醛、α-甲基苯乙烯和异丙苯的第三反应物流。
本发明所述生产系统还可进一步包括:
第五反应器;其配置成接收氢气和第三反应系统流出的包含龙葵醛、α-甲基苯乙烯和异丙苯的物流或者包含龙葵醛、α,α-二甲基苄醇、α-甲基苯乙烯和异丙苯的物流,以及排放包含龙葵醇和异丙苯的物流;
第三分离装置;其配置成接收第五反应器排放的包含龙葵醇和异丙苯的物流,以及排放龙葵醇和异丙苯。
本发明所述生产系统中,优选地,第一分离装置、第二分离装置、第三分离装置为精馏塔。
本发明所述生产系统中,优选地,设置将第二分离装置排出的α-甲基苯乙烯返回第二反应器的管线。
本发明所述生产系统中,优选地,设置将第二分离装置排出的异丙苯返回第一反应器的管线。
本发明所述生产系统中,优选地,设置将第三分离装置排出的异丙苯返回第一反应器的管线。
本发明与现有的龙葵醛生产技术相比,具有以下优势:
所述生产方法以异丙苯为单一化学品原料,除此外仅消耗空气、氢气以及一定量的α-甲基苯乙烯(装置开始运行时,在工艺循环实现后可以不用或者只需少量补充甲基苯乙烯),这些也都是廉价易得的产品。
本发明工艺中各主要反应步骤均有可靠的实现方案,反应条件比较温和简单。在优化条件下,反应副产物可以有效控制,产物收率较高。反应的各种产物以及溶剂相互之间易于分离。
附图说明
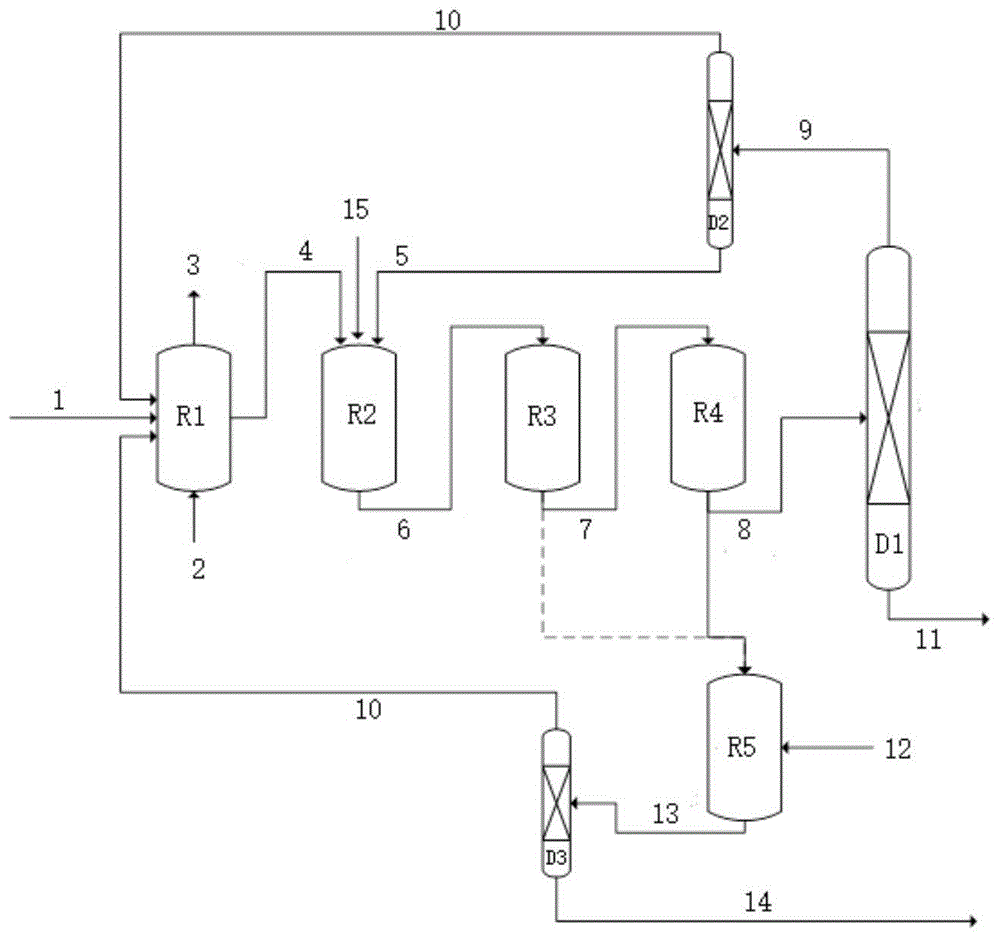
图1为本发明龙葵醛/龙葵醇的生产方法的实施方式的流程示意图。
附图标记说明:
1-异丙苯;
2-富氧空气;
3-尾气;
4-第一反应物流;
5-回收的α-甲基苯乙烯;
6-第二反应物流;
7-包含龙葵醛、α,α-二甲基苄醇、α-甲基苯乙烯和异丙苯的物流;
8-第三反应物流;
9-包含α-甲基苯乙烯和异丙苯的物流;
10-回收的异丙苯;
11-龙葵醛;
12-氢气;
13-包含龙葵醇和异丙苯的物流;
14-龙葵醇;
15-新鲜α-甲基苯乙烯;
R1-第一反应器;
R2-第二反应器;
R3-第三反应器;
R4-第四反应器;
R5-第五反应器;
D1-第一精馏塔;
D2-第二精馏塔;
D3-第三精馏塔。
图1中,异丙苯1经富氧空气2氧化为过氧化氢异丙苯,尾气3排出第一反应器R1。包含过氧化氢异丙苯和异丙苯的第一反应物流进入第二反应器R2,异丙苯作为溶剂,过氧化氢异丙苯作为氧化剂,氧化新鲜α-甲基苯乙烯15生成2-苯基-1,2环氧丙烷,同时过氧化氢异丙苯自身转化为α,α-二甲基苄醇。包含2-苯基-1,2环氧丙烷、α,α-二甲基苄醇、α-甲基苯乙烯和异丙苯的第二反应物流6流入第三反应器R3,2-苯基-1,2环氧丙烷异构化为龙葵醛。包含龙葵醛、α,α-二甲基苄醇、α-甲基苯乙烯和异丙苯的物流7流入第四反应器R4,α,α-二甲基苄醇脱水生成α-甲基苯乙烯。包含龙葵醛、α-甲基苯乙烯和异丙苯的第三反应物流8可以全部流入第一精馏塔D1,分离出龙葵醛11和包含α-甲基苯乙烯和异丙苯的物流9,物流9经过第二精馏塔D2分离成回收的异丙苯10和回收的α-甲基苯乙烯5,回收的异丙苯10流入第一反应器R1,回收的α-甲基苯乙烯5流入第二反应器R2。或者包含龙葵醛、α-甲基苯乙烯和异丙苯的第三反应物流8可以一部分流入第一精馏塔D1,另一部分流入第五反应器R5,龙葵醛、α-甲基苯乙烯通过选择性氢解反应,转化为龙葵醇和异丙苯。
以上流程中,根据另外一种实施方式,包含龙葵醛、α,α-二甲基苄醇、α-甲基苯乙烯和异丙苯的物流7中的一部分流入第四反应器R4,另一部分也可以流入第五反应器R5,龙葵醛、α,α-二甲基苄醇通过选择性氢解反应,转化为龙葵醇和异丙苯。
从第五反应器R5流出的包含龙葵醇和异丙苯的物流13经过第三精馏塔D3,分离出回收的异丙苯10和龙葵醇14,回收的异丙苯10流入第一反应器R1。
具体实施方式
下面结合具体实施例和附图对本发明进行具体的描述,有必要在此指出的是以下实施例只用于对本发明的进一步说明,不能理解为对本发明保护范围的限制,本领域技术人员根据本发明内容对本发明做出的一些非本质的改进和调整仍属本发明的保护范围。
根据本发明一种优选的实施方式,所述生产方法可包括以下步骤:
a)异丙苯经空气氧化为过氧化氢异丙苯。
b)异丙苯作为溶剂,过氧化氢异丙苯作为氧化剂,氧化α-甲基苯乙烯为2-苯基-1,2环氧丙烷,同时过氧化氢异丙苯自身转化为α,α-二甲基苄醇。
c)对步骤b)得到的产物进行异构化反应和脱水反应,其中2-苯基-1,2环氧丙烷异构化为龙葵醛,α,α-二甲基苄醇脱水生成α-甲基苯乙烯,这两个反应可以一步同时进行,也可以分步进行。
d)α-甲基苯乙烯分离出来回到步骤b)中使用,剩下龙葵醛和作为溶剂的异丙苯作为产物,也可以将部分异丙苯同α-甲基苯乙烯一起分离回用。
e)经过或部分经过c)步骤的物料(即其中包含龙葵醛、α,α-二甲基苄醇和α-甲基苯乙烯等组分的物料),可将其一部分通过选择性氢解反应,转化为龙葵醇和异丙苯,再将异丙苯分离回用。
在本方案中所得到的产品龙葵醛和(或)龙葵醇,溶解在异丙苯中,其中可能包含极少量的苯乙酮、苯酚、2,3-二甲基-2,3-二苯基丁烷等杂质组份,这些杂质是方案主张的各个反应环节中难以避免的副产物。对于异丙苯溶剂和副产物杂质,可根据下游应用的实际场景脱除或者保留,本方案不限定和要求根据下游需求精制龙葵醛和(或)龙葵醇产品的具体的方式。
在本方案中,虽然龙葵醛是通过将α-甲基苯乙烯氧化为2-苯基-1,2环氧丙烷再进一步异构化得到,但是氧化反应同时会产生等量或更多的α,α-二甲基苄醇,α,α-二甲基苄醇可以脱水转化成α-甲基苯乙烯循环使用。
异丙苯是比较常见和易得的化工原料。工业异丙苯中可能包含苯、甲苯、乙苯、正丙苯、二异丙苯等芳烃以及烷烃和环烷烃等微量杂质。部分杂质有可能进入最终产品中,但是以上杂质并不阻碍本方案所主张的工艺路线的实现,当然,从异丙苯原料或者最终产品中脱除这些杂质组分也是允许和可行的操作,并不影响本方案的权利主张。
本方案中的工艺步骤a),即将异丙苯氧化为过氧化氢异丙苯的过程,在本领域属于公开技术,细节上可以参考多种现有方案。根据本发明一种优选的实施方式,选择气液反应的形式,使用空气或者富氧空气将异丙苯氧化为过氧化氢异丙苯溶液,氧化液中的过氧化氢异丙苯浓度允许在1wt%~85wt%范围,进一步的优选范围是10wt%~55wt%。可以通过本领域内公开的技术方法调整过氧化氢异丙苯的浓度,例如通过蒸发提浓等。
本方案中的工艺步骤b),以过氧化氢异丙苯为氧化剂,氧化α-甲基苯乙烯为2-苯基-1,2环氧丙烷,同时过氧化氢异丙苯转化为α,α-二甲基苄醇。根据本发明一种优选的实施方式,采用在环氧化催化剂作用下的液相反应,高度选择性地将α-甲基苯乙烯环氧化为2-苯基-1,2环氧丙烷,过氧化氢异丙苯转化为α,α-二甲基苄醇,从而减少苯酚和苯乙酮等副产物的生成。
进一步的,本发明优选使用的环氧化催化剂,包括但不限于含钛和/或钼等元素的分子筛、杂多酸、复合氧化物、可溶性配合物或者它们的组合。这几类催化剂在烯烃环氧化过程,如丙烯、1-丁烯、环己烯环氧化过程中都有应用,属于本领域的公开技术。
更进一步的,本发明优选使用含钛和/或钼元素的非均相催化剂,特别优选是载有钛和/或钼元素的介孔硅分子筛型催化剂。
更进一步的,采用上述含钛和/或钼介孔分子筛催化剂时,反应温度优选40~120℃,例如40℃、50℃、60℃、70℃、80℃、90℃、100℃、110℃、120℃等;反应压力只要求保持反应体系维持液相,优选1~5MPaG,例如1MPaG、2MPaG、3MPaG、4MPaG、5MPaG等;反应原料中α-甲基苯乙烯相对过氧化氢异丙苯的比例为1:1~10:1(mol:mol),例如1:1、2:1、3:1、4:1、5:1、6:1、7:1、8:1、9:1、10:1等。
本方案中的工艺步骤c),将2-苯基-1,2环氧丙烷经异构化反应得到龙葵醛,而α,α-二甲基苄醇则经过脱水反应生成α-甲基苯乙烯。这两个反应均可以使用本领域内常见的酸性催化剂,优选是一些非均相的固体酸催化剂,包括但不限于γ-Al
进一步的,本方案主张先将2-苯基-1,2环氧丙烷异构化为龙葵醛,这个反应可以使用或者不使用催化剂,得到以龙葵醛、异丙苯、α,α-二甲基苄醇以及α-甲基苯乙烯(反应原料中过量的α-甲基苯乙烯)为主要成分的物流。然后处理这股物流,令α,α-二甲基苄醇脱水为α-甲基苯乙烯,脱水反应需要使用如上所述的一些酸性催化剂,得到以龙葵醛、异丙苯、以及α-甲基苯乙烯为主要成分的物流。
本方案中的工艺步骤d),需要将α-甲基苯乙烯分离出来回到步骤b)中使用,优选通过精馏手段从龙葵醛中分离出α-甲基苯乙烯,在精馏时,大部分异丙苯也会随α-甲基苯乙烯蒸出,再进一步将异丙苯与α-甲基苯乙烯分离,可以选择保留一部分异丙苯溶解α-甲基苯乙烯返回步骤b),这样的好处是降低α-甲基苯乙烯聚合的可能,蒸出的异丙苯可选择返回步骤a)或者作为溶剂溶解龙葵醛等产品。
本方案中的工艺步骤e),即氢解反应,主要目的是为平衡步骤b)消耗的和步骤c)生成的α-甲基苯乙烯。通常情况下因为过氧化氢异丙苯有分解反应,所以产物中α,α-二甲基苄醇的量实际比反应消耗的α-甲基苯乙烯多,这也造成步骤c)生成的α-甲基苯乙烯比较多,为了平衡,可以将步骤c)物流中的一部分,携带着多余部分的α-甲基苯乙烯,经过氢解反应转化为异丙苯。
进一步的,上述氢解反应可以使用一些催化剂保证氢解产物的选择性。这些催化剂包括但不限于Pd/Al
进一步的,在上述氢解催化剂和氢解反应的条件下,龙葵醛可以同时转化为龙葵醇。步骤e)得到以龙葵醇和异丙苯为主要成分的物流,可以通过精馏将异丙苯分离出来去步骤a)回用。
本发明提出一种生产龙葵醛和龙葵醇的工艺路线,下面以具体实施例来说明所主张工艺的可行性。但是实施例的具体参数并不限制本发明所主张的权利范围。
【实施例1】
实施例采用分步操作以说明工艺主要步骤的可行性。
a)异丙苯氧化:这一步因为在工业上已有非常成熟的技术装置(如苯酚丙酮的生产过程),在本实施例中直接使用外购的过氧化氢异丙苯试剂(浓度70wt%,国药沪试),用商品异丙苯试剂稀释到30wt%浓度。
b)取100g过氧化氢异丙苯(30wt%)和93gα-甲基苯乙烯混合,(α-甲基苯乙烯对过氧化氢异丙苯相当于4mol:1mol)加入10g Ti-HMS催化剂(参考公开号为CN104437636A的专利中实施例2制备),投入搅拌釜中,封闭并用氮气充分置换釜内空间,保持60转/分的搅拌速度,升温反应,釜内温度维持80℃左右,初期反应放热较大,应适当降低反应器加热温度,保证釜内不超过120℃,反应压力为1.0MPaG。反应6h后自然降温,冷却后取出液相产物,其组成见下表1:
表1
产物中少量的龙葵醛是因为2-苯基-1,2环氧丙烷在受热情况下直接发生异构化反应生成。
c)将b)中反应产物与Ti-HMS催化剂分离后,倒入装有温度计、搅拌和冷凝柱的三口烧瓶中,搅拌升温到140℃,保持回流约12小时以充分进行异构化反应,直至2-苯基-1,2环氧丙烷基本完全转化为龙葵醛。反应结束后冷却产物,称重并分析产物中龙葵醛含量,见表4。将剩余产物以1mL/min的速率通过一个固定床反应器,反应器中装填10gγ-Al
表2
d)将c)中产物(油相)取出一半约80g,在玻璃容器中减压蒸馏,在约30kPaA的压力下,逐渐提高温度到150℃左右,蒸出馏分主要为异丙苯和α-甲基苯乙烯;剩下组分中主要是龙葵醛,含量约为9.5g。
e)将c)中产物(油相)取出另一半约80g,在固定床反应器中进行氢解反应。反应器中装填10mL Pd/Al
表3
【实施例2】
参照实施例1中步骤a)到c)操作,但是在步骤a)中将过氧化氢异丙苯稀释至50wt%浓度。步骤b)中50wt%过氧化氢异丙苯的用量调整为60g,其它试剂和催化剂用量不变。后续步骤操作不变。
【实施例3】
参照实施例1中步骤a)到c)操作,但是在步骤b)中不使用催化剂,改为100~110℃下反应并延长反应时间到24h。后续步骤操作不变。
【实施例4】
参照实施例1中操作,但是在步骤c)中异构化反应和脱水反应一步同时进行,具体如下:直接将步骤b)的产物通过装有10gγ-Al
【实施例5】
重复实施例1中步骤a)到c),得到约160g的混合产物。在玻璃容器中减压蒸馏,在约30kPaA的压力下,逐渐提高温度,沸程低于115℃的馏分以异丙苯为主,集中收集沸程115℃~150℃的馏分,这股馏分约97g,其中α-甲基苯乙烯含量约95%。取这股回收的α-甲基苯乙烯,与100g过氧化氢异丙苯(30wt%)混合,加入10g Ti-HMS催化剂,按照实施例1中步骤b)和c)再次进行反应。在步骤c)异构化反应完成后测量产物中龙葵醛的含量。
因为蒸馏过程中有较多的不确定损失,这里以步骤c)中异构化反应后的产物中龙葵醛的含量来计算龙葵醛的收率,根据过氧化氢异丙苯的消耗量折算异丙苯原料的消耗,实施例1-5的比较结果如下表4:
表4
表4中产物龙葵醛的计算收率公式为:
从结果中可以看出,使用恰当的环氧化催化剂和优化的反应条件,可以保证较高的龙葵醛收率。通过蒸馏回收的α-甲基苯乙烯,可以再次作为环氧化反应原料来制备2-苯基-1,2环氧丙烷并最终得到龙葵醛。
【实施例6】
重复实施例1中步骤a)到b),但是步骤c)中在异构化反应结束后不进行脱水反应,这时产物组成见表5:
表5
将未脱水产物直接在固定床反应器中进行氢解反应。反应器中装填10mL Pd/Al
表6
从该实施例6可以看出,未脱水的α,α-二甲基苄醇亦可以直接氢解反应得到异丙苯,同时龙葵醛转变为龙葵醇。
- 一种连续精馏生产醇酯十二系统及其生产醇酯十二的方法
- 一种99级季戊四醇的生产系统及其生产工艺
- 在醇生产过程中蒸馏醇的方法和系统
- 一种龙葵醛的生产方法
- 一种制备龙葵醛的方法
