活细胞膜整合素αvβ3聚糖的原位糖链延长方法
文献发布时间:2023-06-19 19:28:50
一、技术领域
本发明介绍了一种活细胞膜整合素α
二、背景技术
糖基化是普遍存在于真核生物中的蛋白质翻译后修饰模式。细胞表面的聚糖参与了一系列重要的生物过程。异常的糖基化与多种疾病的发生和发展密切相关,因此对活细胞表面特定蛋白的聚糖结构进行编辑,是一种重要的疾病干预手段,已被用于增强赫赛汀对乳腺癌的治疗效果。
整合素α
本发明结合可以特异性识别α
三、发明内容
本发明的内容是:构建特定蛋白的聚糖重构探针,在活细胞表面原位靶向整合素α
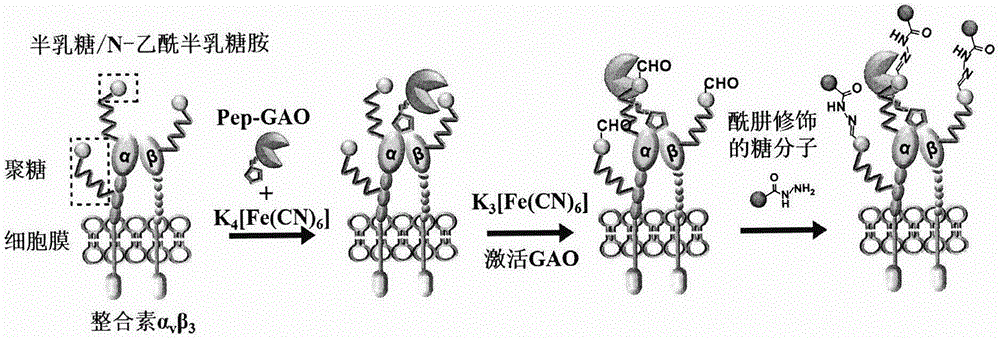
该方法首先以琥珀酰亚胺酯和马来酰亚胺双修饰的聚乙二醇1000(NHS-PEGl000-MAL)作为连接分子,偶联巯基修饰的c(RGDfK)多肽(Pep)和GAO的氨基,制备聚糖重构探针Pep-GAO,如图1所示。
本发明提出的活细胞膜整合素αvβ3聚糖的原位糖链延长方法如图2所示,将Pep-GAO与K4[Fe(CN)6]混合后加入活细胞,探针可在Pep的引导下特异性结合αvβ3,而在此过程中探针的GAO活性被K4[Fe(CN)6]抑制。识别结束后洗掉未结合探针,加入K3[Fe(CN)6]激活GAO,由于GAO被限域在αvβ3上,只能特异性氧化αvβ3糖链末端的Gal/GalNAc生成生物正交基团醛基。通过己二酸二酰肼与糖分子反应制得酰肼修饰的糖分子,进而与活细胞表面αvβ3糖链上生成的醛基发生连接反应生成腙键,实现整合素αvβ3聚糖的原位糖链延长。
本发明通过以下技术方案来实现:
1)如图1所示,以特异性识别整合素α
2)如图2所示,将Pep-GAO与K
3)在80℃磁力搅拌下,将己二酸二酰肼与糖分子(24mM∶2.4mM)在乙腈/水溶液(体积比1∶1)中冷凝回流反应8h后,用硅胶柱层析得到酰肼修饰的糖分子,洗脱液为体积比为6∶3∶1∶1的异丙醇,水,氨水和乙腈的混合液。
4)如图2所示,在10mM苯胺的催化下,细胞表面上生成的醛基与300μM酰肼修饰糖分子在4℃条件下反应1h,实现活细胞膜整合素α
本发明与现有技术相比,具有以下特点:
本发明设计首次提出了活细胞膜整合素α
与基于糖修饰酶的聚糖编辑技术相比,本方法由于在糖修饰酶上修饰了可以特异性识别目标蛋白的多肽,赋予了方法蛋白特异性;与基于聚糖新陈代谢技术的糖编辑技术相比,本方法无需经过细胞内的代谢过程,耗时大大缩短,同时方法具有蛋白特异性。同时本方法合成的聚糖重构探针具有良好的细胞相容性,方法可以在活细胞上进行。
本方法对给体糖分子的结构没有限制,在对糖分子进行一步酰肼功能化后,即可通过与目标蛋白上氧化生成的醛基的生物正交化学反应快速连接在目标蛋白糖链上。
该方法实现了对活细胞表面目标蛋白糖链的编辑,为理解聚糖的生物学功能,通过干预聚糖进行疾病治疗提供了工具。
四、附图说明
图1.聚糖重构探针Pep-GAO制备示意图
图2.活细胞膜整合素α
图3.酰肼修饰甘露三糖制备示意图
五、具体实施方式
实施例1:结合图1,制备聚糖重构探针Pep-GAO
在pH 7.4的PBS(10mM)中按照浓度比10μM∶1mM∶1mM混合GAO、NHS-PEG1000-MAL和Pep,在25℃,800rpm/h的条件下恒温振荡2h,之后用PBS超滤8次(超滤管截留分子量:30kDa),制得Pep-GAO。
实施例2:结合图2,乳腺癌细胞系MDA-MB-231膜蛋白整合素α
将1×10
实施例3:结合图3,制备酰肼修饰的甘露三糖
将己二酸二酰肼和甘露三糖溶解在等体积混合的乙腈/水溶液中,使其浓度分别为24mM和2.4mM。在80℃磁力搅拌下将混合物冷凝回流反应8h,然后用硅胶柱层析制得酰肼修饰的甘露三糖(Man3-H)。洗脱液为将异丙醇,水,氨水和乙腈按体积比6∶3∶1∶1配制的混合液。
实施例4:根据实施例2和3,乳腺癌细胞系MDA-MB-231膜蛋白整合素α
将含300μM Man
