乙型肝炎病毒抗原的胸腺依赖性淋巴细胞抗原表位肽及其应用
文献发布时间:2023-06-19 19:28:50
本案是针对发明名称为乙型肝炎病毒抗原的胸腺依赖性淋巴细胞抗原表位肽及其应用,申请号为2019112846358,申请日为2019.12.13的案件所做的分案。
技术领域
本发明属于医学免疫学和感染病学领域,特别涉及189种乙型肝炎病毒抗原的胸腺依赖性淋巴细胞抗原表位肽及其应用。
背景技术
乙型肝炎病毒(Hepatitis B virus,HBV)感染是最常见感染性疾病之一,严重危及人类的健康。世界卫生组织2015年7月统计数据显示,预计全球1/3的人口感染过HBV,约2.48亿HBV携带者,后期可发展为肝硬化和原发性肝细胞癌。每年约78万HBV感染的患者因疾病进展为肝硬化、肝衰竭或是肝癌而导致死亡。流行病学调查显示在中国约8亿人感染过HBV,乙肝表面抗原(hepatitis B surface antigen,HBsAg)携带率高达10.34%,即我国目前约有1.2亿人为HBV携带者,占全球慢性感染人数的一半。另外,我国也是一个肝癌大国,约占全球肝癌人数的55%以上。
HBV基因组由不完全双链环状DNA组成,长的为负链,含3020-3320个碱基,短的为正链,含1700-2800个碱基。包括四个开放阅读框(ORF),分别称为C、X、P和S编码区。C区由pre-C和C基因组成,分别由不同的起始密码子调控,在相同的终止密码子处结束,pre-C和C基因共同编码pre-C蛋白,Pre-C蛋白再经过切割加工后形成e抗原(HBeAg)。C基因编码病毒的衣壳蛋白,即HBcAg。S区由S基因、PreS1和PreS2基因组成,由3个不同的起始密码子启动翻译,在同一个终止密码子处终止翻译,分别编码表面抗原(HBsAg)蛋白、PreS1蛋白和PreS2蛋白。P区基因编码的HBV的聚合酶蛋白(HBpol)。X区的基因编码X蛋白(HBx),包含154个氨基酸,是最小的一个开放阅读框。
细胞毒性T细胞(Cytotoxic T lymphocyte,CTL)是介导适应性免疫应答的核心细胞,在抗感染、抗肿瘤以及超敏反应和自身免疫病的发生中起着至关重要的作用,其细胞膜上的T细胞受体(T cell receptor,TCR)能够特异性识别并结合抗原递呈细胞表面MHC I类分子与抗原肽的复合物,即MHC/抗原肽复合体分子。CTL表位是指与MHC I类分子结合的抗原肽,是抗原分子中能被TCR特异性识别的线性片段或空间构象性结构,是引起免疫应答反应的基本抗原单位,在CTL活化过程中扮演着关键角色。
MHC系统指主要组织相容性复合体(major histocompatibility complex,MHC),是脊椎动物基因组中一组紧密连锁的基因群,编码表达MHC I类和II类蛋白分子。HLA(human leukocyte antigen)是人类的MHC系统,是人体最复杂的基因群,在人群中具有高度多态性。HLA在抗原识别、抗原呈递等机体免疫过程中发挥重要作用,是影响人体免疫反应的主要因素。HLA I类分子主要负责将内源性HBV抗原呈递给CD8
但是,目前已明确的被各种HLA分子所提呈并能刺激机体引起T细胞应答反应的HBV抗原肽仍然很少,从而限制了对携带不同HLA等位基因的乙肝患者开展特异性T细胞检测,也限制了HBV特异性T细胞在乙肝发生发展中的作用研究,更限制了基于HLA基因个体差异性及其提呈的HBV抗原肽差异性的个性化检测和精准免疫治疗。
发明内容
本发明解决现有技术中存在的上述技术问题,提供乙型肝炎病毒抗原的胸腺依赖性淋巴细胞抗原表位肽及其应用。
为解决上述问题,本发明的技术方案如下:
乙型肝炎病毒抗原的胸腺依赖性淋巴细胞抗原表位肽,其氨基酸序列为如下所示表位肽序列中的任一种:
/>
/>
/>
/>
/>
/>
/>
由上述的表格可看出,上述序列分别为乙肝病毒e抗原HBeAg、表面抗原HBsAg、聚合酶蛋白HBpol或X蛋白(HBx)的抗原肽序列,上述序列分别与HLA-A0201、A1101、A2402、A3101、A0206、A0207、A3303、A3001、A0203、A1102、A0301、A0101、A2601分子呈高亲和力结合,在抗原提呈细胞表面组成MHC/抗原肽复合体分子,与抗原肽特异性CD8
所述乙型肝炎病毒抗原的胸腺依赖性淋巴细胞抗原表位肽序列可用于制备乙型肝炎多肽疫苗或基因疫苗:多肽疫苗制备:按照本发明的抗原表位肽序列人工合成一种或多种抗原肽,与佐剂混合制成可溶性制剂,或者由生物纳米材料装载制成纳米多肽疫苗,注入乙肝病毒感染者或乙型肝炎患者体内,激发患者乙肝病毒抗原特异性T细胞活化、增殖,并增强其杀瘤细胞活性,从而制备成乙肝多肽疫苗。基因疫苗制备:按照本分明的多肽序列,构建一种多肽或多种多肽的重组DNA基因片段、重组质粒或者重组病毒载体,注入乙肝病毒感染者或乙型肝炎患者体内,使该重组基因在体内表达一种或多种多肽,激发乙肝病毒抗原特异性T细胞活化、增殖,并增强其杀病毒感染细胞的活性,从而制备成乙肝基因疫苗。
所述乙型肝炎病毒抗原的胸腺依赖性淋巴细胞抗原表位肽序列可用于制备检测乙型肝炎病毒抗原特异性T细胞的检测制剂或试剂盒:按照本发明的抗原表位肽序列,人工合成一种或多种抗原肽,在酶联免疫斑点法、胞内细胞因子荧光染色法和酶联免疫吸附试验中,作为抗原制剂,与患者外周血单个核细胞(PBMC)混合培养,刺激乙肝病毒抗原特异性T细胞活化、增殖和分泌细胞因子,进而通过其他组合试剂检测该细胞因子的合成量,从而反应特异性T细胞的数量和反应活性;也可以利用这些多肽通过基因工程技术和蛋白工程技术制备人类白细胞抗原与多肽的复合体(peptide-HLA complex)及其多聚体,再进一步制备成荧光素标记的制剂,用流式细胞分析法检测患者外周血PBMC细胞群中乙肝病毒抗原特异性T细胞的数量。相关试剂盒则是指由上述制剂与不同检测方法中常用的其他试剂组装而成的乙肝病毒抗原特异性T细胞检测试剂盒。
所述乙型肝炎病毒抗原的胸腺依赖性淋巴细胞抗原表位肽序列可用于制备治疗乙型肝炎的药物:将上述基于本发明抗原表位肽序列的多肽疫苗或基因疫苗与其他免疫治疗制剂或化学治疗制剂组合,制备成治疗乙肝的临床药物。
本发明利用六种在线表位预测数据库虚拟预测HLA-A分子限制性的HBV特异性抗原表位肽序列,获得一组能分别与HLA-A0201、A1101、A2402、A3101、A0206、A0207、A3303、A3001、A0203、A1102、A0301、A0101、A2601分子呈高亲和力结合的HBV特异性抗原表位肽序列,然后通过ELISPOT功能性实验验证了其免疫原性,为制备HBV感染的治疗和预防性疫苗以及研制HBV抗原特异性T细胞检测试剂等提供了特异性抗原肽。
1.选择乙肝病毒e抗原(HBeAg,包括HBcAg的序列)、表面抗原(HBsAg)、聚合酶蛋白(HBpol)和X蛋白(HBx)氨基酸序列为靶向序列;
2.选择预测结果获得研究者公认的、具有较高准确性的、常用的六种表位预测数据库:SYFPEITHI、BIMAS、SVMHC、IEDB、NETMHC和EPIJEN预测上述两种HLA-A分子限制性的HBV特异性抗原表位肽序列;
3.根据一定的预测标准,对六个在线表位预测网站的预测结果进行整合分析,获得六个网站预测结果较一致的候选抗原肽序列。
4.通过IFN-γELISPOT细胞功能性实验验证HBV抗原表位肽的免疫原性。
本发明为乙肝病毒e抗原(HBeAg,包括HBcAg的序列)、表面抗原(HBsAg)、聚合酶蛋白(HBpol)和X蛋白(HBx)中能分别与HLA-A0201、A1101、A2402、A3101、A0206、A0207、A3303、A3001、A0203、A1102、A0301、A0101、A2601分子呈高亲和力结合并且具有免疫原性的抗原肽序列;还涉及到以上述抗原肽为基础的乙型肝炎多肽疫苗、基因疫苗、乙型肝炎的治疗与预防方法,以及以上述抗原肽为基础的检测乙型肝炎病毒抗原特异性T细胞的试剂和方法。
相对于现有技术,本发明的优点如下,
经在线虚拟预测和功能性实验验证获得的HLA-A0201、A1101、A2402、A3101、A0206、A0207、A3303、A3001、A0203、A1102、A0301、A0101、A2601分子限制性的HBV特异性抗原表位肽以前没有被报道过。这些HLA-A分子以前也没有被报道有限制性的HBV抗原肽。因此这些新的抗原表位肽序列将为研制针对乙型肝炎治疗性和预防性多肽疫苗和基因疫苗、设计检测乙型肝炎病毒抗原特异性T细胞的试剂和方法等提供所需的关键抗原组分,即抗原表位肽序列;同时这些抗原表位肽也为针对这些特定HLA-A等位基因的乙型肝炎患者进行个体化检测和精准医疗提供了关键的抗原组分。
附图说明
图1为HLA-A0201分子限制的HBV抗原T细胞表位肽;(A)IFN-γELISPOT方法鉴定HLA-A0201分子限制性HBV抗原T细胞表位肽的检测孔、阴性对照孔和阳性对照孔斑点图;(B)检测孔与阴性对照孔斑点数统计图;(C)检测孔与阴性对照孔斑点数比值(P/N)统计图;
图2为HLA-A1101分子限制的HBV抗原T细胞表位肽;(A)IFN-γELISPOT方法鉴定HLA-A1101分子限制性HBV抗原T细胞表位肽的检测孔、阴性对照孔和阳性对照孔斑点图;(B)检测孔与阴性对照孔斑点数统计图;(C)检测孔与阴性对照孔斑点数比值(P/N)统计图;
图3为HLA-A2402分子限制的HBV抗原T细胞表位肽;(A)IFN-γELISPOT方法鉴定HLA-A2402分子限制性HBV抗原T细胞表位肽的检测孔、阴性对照孔和阳性对照孔斑点图;(B)检测孔与阴性对照孔斑点数统计图;(C)检测孔与阴性对照孔斑点数比值(P/N)统计图;
图4为HLA-A3101分子限制的HBV抗原T细胞表位肽;(A)IFN-γELISPOT方法鉴定HLA-A3101分子限制性HBV抗原T细胞表位肽的检测孔、阴性对照孔和阳性对照孔斑点图;(B)检测孔与阴性对照孔斑点数统计图;(C)检测孔与阴性对照孔斑点数比值(P/N)统计图;
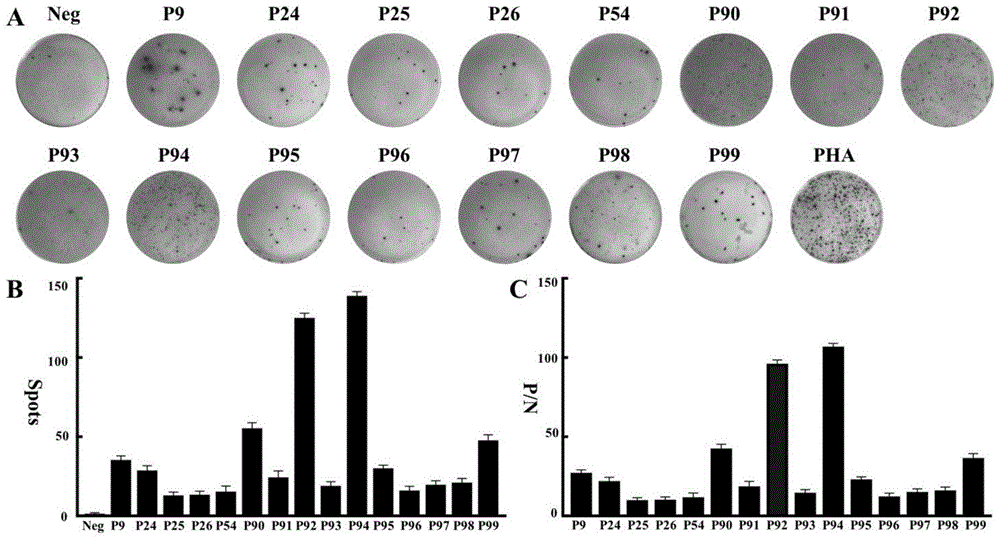
图5为HLA-A0206分子限制的HBV抗原T细胞表位肽;(A)IFN-γELISPOT方法鉴定HLA-A0206分子限制性HBV抗原T细胞表位肽的检测孔、阴性对照孔和阳性对照孔斑点图;(B)检测孔与阴性对照孔斑点数统计图;(C)检测孔与阴性对照孔斑点数比值(P/N)统计图;
图6为HLA-A0207分子限制的HBV抗原T细胞表位肽;(A)IFN-γELISPOT方法鉴定HLA-A0207分子限制性HBV抗原T细胞表位肽的检测孔、阴性对照孔和阳性对照孔斑点图;(B)检测孔与阴性对照孔斑点数统计图;(C)检测孔与阴性对照孔斑点数比值(P/N)统计图;
图7为HLA-A3303分子限制的HBV抗原T细胞表位肽;(A)IFN-γELISPOT方法鉴定HLA-A3303分子限制性HBV抗原T细胞表位肽的检测孔、阴性对照孔和阳性对照孔斑点图;(B)检测孔与阴性对照孔斑点数统计图;(C)检测孔与阴性对照孔斑点数比值(P/N)统计图;
图8为HLA-A3001分子限制的HBV抗原T细胞表位肽;(A)IFN-γELISPOT方法鉴定HLA-A3001分子限制性HBV抗原T细胞表位肽的检测孔、阴性对照孔和阳性对照孔斑点图;(B)检测孔与阴性对照孔斑点数统计图;(C)检测孔与阴性对照孔斑点数比值(P/N)统计图;
图9为HLA-A0203分子限制的HBV抗原T细胞表位肽;(A)IFN-γELISPOT方法鉴定HLA-A0203分子限制性HBV抗原T细胞表位肽的检测孔、阴性对照孔和阳性对照孔斑点图;(B)检测孔与阴性对照孔斑点数统计图;(C)检测孔与阴性对照孔斑点数比值(P/N)统计图;
图10为HLA-A1102分子限制的HBV抗原T细胞表位肽;(A)IFN-γELISPOT方法鉴定HLA-A1102分子限制性HBV抗原T细胞表位肽的检测孔、阴性对照孔和阳性对照孔斑点图;(B)检测孔与阴性对照孔斑点数统计图;(C)检测孔与阴性对照孔斑点数比值(P/N)统计图;
图11为HLA-A0301分子限制的HBV抗原T细胞表位肽;(A)IFN-γELISPOT方法鉴定HLA-A0301分子限制性HBV抗原T细胞表位肽的检测孔、阴性对照孔和阳性对照孔斑点图;(B)检测孔与阴性对照孔斑点数统计图;(C)检测孔与阴性对照孔斑点数比值(P/N)统计图;
图12为HLA-A0101分子限制的HBV抗原T细胞表位肽;(A)IFN-γELISPOT方法鉴定HLA-A0101分子限制性HBV抗原T细胞表位肽的检测孔、阴性对照孔和阳性对照孔斑点图;(B)检测孔与阴性对照孔斑点数统计图;(C)检测孔与阴性对照孔斑点数比值(P/N)统计图;
图13为HLA-A2601分子限制的HBV抗原T细胞表位肽;(A)IFN-γELISPOT方法鉴定HLA-A2601分子限制性HBV抗原T细胞表位肽的检测孔、阴性对照孔和阳性对照孔斑点图;(B)检测孔与阴性对照孔斑点数统计图;(C)检测孔与阴性对照孔斑点数比值(P/N)统计图;
图14为实施例1中待鉴定表位肽免疫原性验证的实验技术路线图。
具体实施方式
实施例1:
本发明的HLA-A0201、A1101、A2402、A3101、A0206、A0207、A3303、A3001、A0203、A1102、A0301、A0101、A2601分子限制性HBV特异性抗原肽,序列通过以下步骤筛选和鉴定:
1、在线虚拟预测13种HLA-A分子限制的4种HBV抗原的优势T细胞表位肽
选取4种HBV蛋白:表面抗原(HBsAg)、e抗原(HBeAg,包括HBcAg的序列)、DNA多聚酶(HBpol)和X蛋白(HBx),通过UniProt全球蛋白资源数据库检索获得其氨基酸序列,选择了中国感染最多的HBV C型HBV蛋白序列;再通过SYFPEITHI、BIMAS、SVMHC、IEDB、NETMHC、EPIJEN等六种常用的表位肽预测数据库对HLA-A0201、A1101、A2402、A3101、A0206、A0207、A3303、A3001、A0203、A1102、A0301、A0101、A2601分子限制的针对上述每种HBV蛋白的T细胞表位肽进行虚拟预测,其中SVMHC数据库包括MHCPEP model和SYFEPITHI model两种预测算法;IEDB数据库包括了ANN、SMM和ARB三种方法,本实验选择其中具有更好统计学意义的ANN和SMM方法。这些表位肽预测数据库网站见表1。
HLA I类分子的抗原结合凹槽两端封闭,接纳的抗原肽长度为8-11个氨基酸残基,其中以9和10个氨基酸最为常见,因此,本实验分别选择9和10个氨基酸长度的多肽作为研究对象。分别将每种HBV蛋白的氨基酸序列输入到预测数据库网站的相应氨基酸序列输入框,再分别选择表位肽的长度为9和10个氨基酸,然后选择特定的HLA-A分子,对HBV抗原的T细胞表位肽进行在线虚拟预测。
表1表位肽预测数据库网站
针对每种HLA-A分子和每种HBV蛋白,将不同数据库预测出的9肽和10肽分别按评分从高到低进行排列,再从中选择至少满足两种以上预测方法评分标准的表位肽作为候选表位肽。每种HLA-A分子,针对每种HBV蛋白,再从候选表位肽中选出评分最高(亲和力最高)的1-4种多肽作为待鉴定表位肽。
2、分离HBV慢性感染患者外周血PBMC
取室温保存的新鲜抗凝全血,用无菌PBS适当稀释;将1倍原血体积的人淋巴细胞分离液(达科为生物,深圳)加入15mL离心管;将稀释后的血液缓缓平铺于分离液上,室温离心20min,2500rpm;吸取单个核细胞(PBMCs)层,离心洗涤2次;用无血清培养基(达科为生物,深圳)重悬,细胞计数,调整细胞浓度为2×10
3、用IFN-γELISPOT法鉴定HBV抗原T细胞表位肽的免疫原性
技术路线如图14所示:
首先筛选出对混合肽组有阳性反应的HBV慢性感染者:将每种HLA-A分子限制的针对4种HBV蛋白的待鉴定表位肽混合为一组,每组8-9种表位肽;取预包被抗人IFN-γ抗体的ELISPOT板(达科为生物,深圳),用无血清培养基(200μL/well)活化8min,每孔加入HBV慢性感染者PBMC悬液(100μL/well);然后在检测孔中补加每种HLA-A分子限制的混合肽,混合肽中单种多肽为30μg/mL,在阳性对照孔补加PHA(2.5μg/mL),在阴性对照孔补加与检测孔相同浓度的DMSO多肽溶解液;置37℃,5%CO
鉴定单种表位肽的免疫原性:重新收集对混合肽有CTL阳性反应的HBV慢性感染者外周血PBMC,加入上述ELISPOT板中,每个检测孔中补加阳性混合肽中的单种HBV多肽(30μg/mL),同上设置阳性对照孔和阴性对照孔,置37℃,5%CO
HLA-A限制性的确定:对每位HBV感染者进行HLA-A等位基因分型,结合该表位肽的虚拟亲和力,初步确定其被哪种HLA-A分子所限制和提呈。从HBV感染者中分别选取这13种HLA-A等位基因的纯合子感染者,取其PBMC,与上述所有已被验证具有免疫原性的且该HLA-A分子限制的表位肽,重新进行ELISPOT检测,进一步确定每种表位肽的HLA-A分子限制性。
4、HLA-A等位基因分型
选择在表位肽鉴定实验中呈CTL阳性反应的HBV慢性感染者,取200μL抗凝血,利用人全血基因组DNA提取试剂盒(天根生物,北京)提取基因组DNA;采用HLA-A位点特异性引物A1和A3进行PCR,扩增A位点的外显子2、内含子2、外显子3以及部分内含子l和3的DNA序列,产物大小为985bp。扩增条件为:95℃预变性3min;95℃变性15s;62℃退火15s;72℃延伸90s;35个循环;72℃延伸5min。扩增产物经1%琼脂糖凝胶电泳鉴定大小,并送上海桑尼生物科技公司进行纯化和双向测序。PCR试剂购自南京诺唯赞生物科技公司,见表2。
表2 HLA-A位点特异性的PCR扩增引物
通过Lasergene程序的Seqman软件把外显子2和外显子3的测序结果拼成一条完整的HLA-A重叠序列(Contig),仔细检查双向测序的碱基是否完整一致,找出杂合子的碱基并用兼并碱基代替,例如M表示A和C,R表示A和G,W表示A和T,S表示C和G,Y表示C和T,K表示G和T,最终确定扩增出来的HLA-A等位基因的序列片段。利用Nucleotide BLAST工具,将拼接好的HLA-A碱基序列与数据库中所有HLA-A等位基因的外显子2和外显子3序列进行比对,直到获得完全匹配的基因组合,从而确定HLA-A的等位基因。
通过IFN-γELISPOT方法从612例HBV慢性感染患者中筛选出288例对HBV混合肽有CTL阳性反应的患者。再重新收集这些患者的PBMC,用ELISPOT法进行单种表位肽免疫原性的验证,然后结合患者的HLA-A等位基因以及表位肽与这些等位基因的虚拟预测亲和力进行综合分析。结果显示:有26种HBV表位肽(P1-P26)能刺激HLA-A*02:01阳性患者的PBMC呈现CTL阳性反应(图1);有23种HBV表位肽(P27-P49)能刺激HLA-A*11:01阳性患者的PBMC呈现CTL阳性反应(图2);有25种HBV表位肽(P50-P74)能刺激HLA-A*24:02阳性患者的PBMC呈现CTL阳性反应(图3);有17种HBV表位肽(P36、P54、P75-P89)能刺激HLA-A*31:01阳性患者的PBMC呈现CTL阳性反应(图4);有15种HBV表位肽(P9、P24-P26,P54,P90-P99)能刺激HLA-A*02:06阳性患者的PBMC呈现CTL阳性反应(图5);有14种HBV表位肽(P20、P100-P112)能刺激HLA-A*02:07阳性患者的PBMC呈现CTL阳性反应(图6);有16种HBV表位肽(P36、P42、P46、P48、P79,P86、P113-P122)能刺激HLA-A*33:03阳性患者的PBMC呈现CTL阳性反应(图7);有16种HBV表位肽(P9、P34、P123-P136)能刺激HLA-A*30:01阳性患者的PBMC呈现CTL阳性反应(图8);有11种HBV表位肽(P95、P137-P146)能刺激HLA-A*02:03阳性患者的PBMC呈现CTL阳性反应(图9);有13种HBV表位肽(P86、P117、P127、P147-P156)能刺激HLA-A*11:02阳性患者的PBMC呈现CTL阳性反应(图10);有13种HBV表位肽(P78、P85、P115、P151、P153、P155、P157-P164)能刺激HLA-A*03:01阳性患者的PBMC呈现CTL阳性反应(图11);有16种HBV表位肽(P47、P50、P115、P158,P164-P175)能刺激HLA-A*01:01阳性患者的PBMC呈现CTL阳性反应(图12);有15种HBV表位肽(P31、P176-P189)能刺激HLA-A*26:01阳性患者的PBMC呈现CTL阳性反应(图13)。在每种HLA-A分子限制的HBV表位肽之间,免疫原性存在明显差异。
需要说明的是上述实施例仅仅是本发明的较佳实施例,并没有用来限定本发明的保护范围,在上述基础上做出的等同替换或者替代均属于本发明的保护范围。
附:
四种被用来预测抗原表位的乙型肝炎病毒抗原的氨基酸序列如下:
HBsAg(Q913A6):
序列的分子类型:PRT
科学命名的生物属种:人体乙型肝炎病毒
HBeAg(Q913A8):
序列的分子类型:PRT
科学命名的生物属种:人体乙型肝炎病毒
HBpol(Q913A7):
序列的分子类型:PRT
科学命名的生物属种:人体乙型肝炎病毒
HBx(Q913A9):
序列的分子类型:PRT
科学命名的生物属种:人体乙型肝炎病毒
/>
