一种PLA2R重组蛋白及其应用
文献发布时间:2024-04-18 19:53:33
技术领域
本发明属于生物医药工程技术领域,具体涉及PLA2R重组蛋白及其应用。
背景技术
原发性膜性肾病又称特发性膜性肾病、自发性膜性肾病,是导致肾衰竭的重要原因之一,也是造成肾病综合症的首要原因(童孟立.原发性膜性肾病的诊治进展[J].浙江医学,2021,43(04):352-357.)。虽然不超过30%原发性膜性肾病可能自发缓解,但仍有30%患者肾功能在10年左右时间缓慢进展到肾衰竭,对人民生命健康造成严重威胁。近年来的基础研究证实原发性膜性肾病是一种肾脏特异性自身免疫性疾病,身体的自身免疫抗原在疾病条件下激活了免疫系统,产生了自身免疫抗体。自身免疫抗体与肾小球足细胞上的自身免疫抗原结合,导致免疫系统对足细胞及周围组织的攻击,造成炎症与肾小球的损伤。
原发性膜性肾病的自身免疫抗原目前研究较为清楚的有PLA2R和THSD7A。约70%-80%的原发性膜性肾病为PLA2R型,不到10%的原发性膜性肾病为THSD7A型。PLA2R抗体(PLA2R-Ab)在PLA2R型膜性肾病的发生发展中起到了重要作用。PLA2R-Ab在血清中的水平可以作为PLA2R型膜性肾病的预测性标志物。较高的PLA2R-Ab滴度意味着更低的自发缓解几率。PLA2R-Ab滴度降低常常伴随着自发缓解,并在疾病完全缓解的患者中低至无法检测。免疫抑制治疗可以降低PLA2R-Ab滴度。当前PLA2R型膜性肾病的诊断标准为肾脏穿刺样品免疫荧光或免疫组化。这一方法事实上是一个小手术,具有一些缺点如:1)病人痛苦较大;2)某些情况无法进行;3)不能重复进行,对疾病的治疗效果无法提供参考。
PLA2R是一种高表达于肾小球足细胞表面的膜蛋白,包含CysR结构域、Fibronectin type-II结构域、8个序列相似度非常高的C-type lectin结构域、跨膜结构域和胞内结构域组成。由于其含有跨膜的疏水结构,重组表达时容易形成包涵体,产量非常低。德国欧蒙的诊断试剂盒采用了人重组PLA2R作为捕获分子,价格较高。完整的人重组PLA2R是该膜蛋白的胞外区,含有1300多个氨基酸残基,分子量很大,约185kD。这一分子的表达难度较大,产物易聚集,产量低且不易纯化。因此无论是表达PLA2R的全长蛋白还是胞外区都难以获得大量蛋白,阻碍了PLA2R型膜性肾病诊断试剂的开发,且推高了其成本。
开发出分子量小,蛋白表达水平高的重组蛋白,又不影响其抗体结合能力,是在研发PLA2R重组蛋白中需要面临的问题。
发明内容
本发明的目的之一在于,提供一种PLA2R重组蛋白,以及提供能编码该重组蛋白的基因该重组蛋白能够检测血浆中PLA2R抗体。
本发明的目的之一在于,提供能编码所述PLA2R重组蛋白的基因、含有该基因的质粒、含有该质粒的细胞株,以及获得该重组蛋白的工艺方法。
本发明目的之一在于,提供该PLA2R重组蛋白在制备PLA2R抗体检测试剂盒中的应用。
本发明目的之一在于,提供该PLA2R重组蛋白在制备原发性膜性肾病诊断和/或用于原发性膜性肾病患者预后评估的试剂中的应用。
本发明提供了如下技术方案:
一种PLA2R重组蛋白,其氨基酸序列如SEQ ID No.1或SEQ ID No.2所示。
所述PLA2R重组蛋白为PLA2R-CC1H重组蛋白或PLA2R-CC2H重组蛋白,其氨基端末端包含连续6个组氨酸形成的标签。
本发明还提供了编码所述PLA2R重组蛋白的基因,其核苷酸序列如SEQ IDNo.3或SEQ ID No.4所示。
具体的,所述的PLA2R-CC1H重组蛋白具有如SEQ ID No.1所示的氨基酸序列,PLA2R-CC2H重组蛋白具有SEQ ID No.2所示的氨基酸序列。
具体的,所述PLA2R-CC1H重组蛋白基因具有如SEQ ID No.3所示的核苷酸序列;所述PLA2R-CC2H重组蛋白基因具有如SEQ ID No.4所示的核苷酸序列。
所述的PLA2R重组蛋白可按如下方法制备:
(1)获取PLA2R重组蛋白目的片段:确定PLA2R重组蛋白基因酶切位点和特异性引物,人工合成基因为模板,利用特异性引物进行PCR扩增,得到PLA2R-CC1H和PLA2R-CC2H目的片段;
(2)构建PLA2R重组表达质粒:将所述PLA2R-CC1H/PLA2R-CC2H目的片段和pcDNA3.4载体进行同源重组,并将连接产物转化到感受态细胞E.coli DH5α中培养,筛选出阳性克隆,经鉴定后得到pcDNA3.4-PLA2R-CC1H和pcDNA3.4-PLA2R-CC2H重组表达质粒;
(3)制备PLA2R重组蛋白:重组表达质粒pcDNA3.4-PLA2R-CC1H和pcDNA3.4-PLA2R-CC2H转化至CHO-S细胞中,进行重组蛋白的表达,后纯化、鉴定,得到PLA2R重组蛋白。
上述制备方法中,采用Bradford法测定PLA2R重组蛋白浓度,采用SDS-PAGE检测PLA2R重组蛋白纯度。
进一步,所述的PLA2R重组蛋白在制备PLA2R抗体检测试剂盒中的用途。其包括所述PLA2R重组蛋白、ELISA板、TBST缓冲液、封闭液、检测抗体、显色液以及终止液。
所述的PLA2R重组蛋白和/或本发明所述试剂盒在制备膜性肾病诊断试剂中的用途。
所述试剂为原发性膜性肾病的诊断和/或原发性膜性肾病患者预后评估的试剂。
所述原发性膜性肾病是一种肾脏特异性自身免疫性疾病,血循环抗体靶向结合肾小球足细胞抗原,导致基底膜上皮下免疫复合物沉积,进而激活补体系统导致肾小球滤过屏障受损和蛋白尿产生。
本发明还提供了一种PLA2R抗体检测试剂盒的检测方法,包括以下步骤:
(1)将抗原加入固相表面,或抗原已被包被并固定于固相表面;
(2)加入血液样品;
(3)清洗去除未结合的杂质;
(4)加入经标记分子标记的并且与PLA2R抗体有反应性的检测抗体;
(5)清洗去除未结合的检测抗体;
(6)检测标记分子的信号;基于信号获得待测血液样品中是否存在PLA2R抗体和/或PLA2R抗体水平。
所述的检测抗体,其上的标记分子任选自酶,荧光基团或化学发光基团。
优选地,所述的检测抗体优选为HRP标记的小鼠抗人IgG单克隆抗体。
本发明的有益效果是:
1、本发明提供的PLA2R重组蛋白纯度高、分子量小,能够在体外大量表达。PLA2R-CC1H产量高达1780mg/L,PLA2R-CC2H的产量高达1260mg/L。而且纯化工艺简单,生产成本低。
附图说明
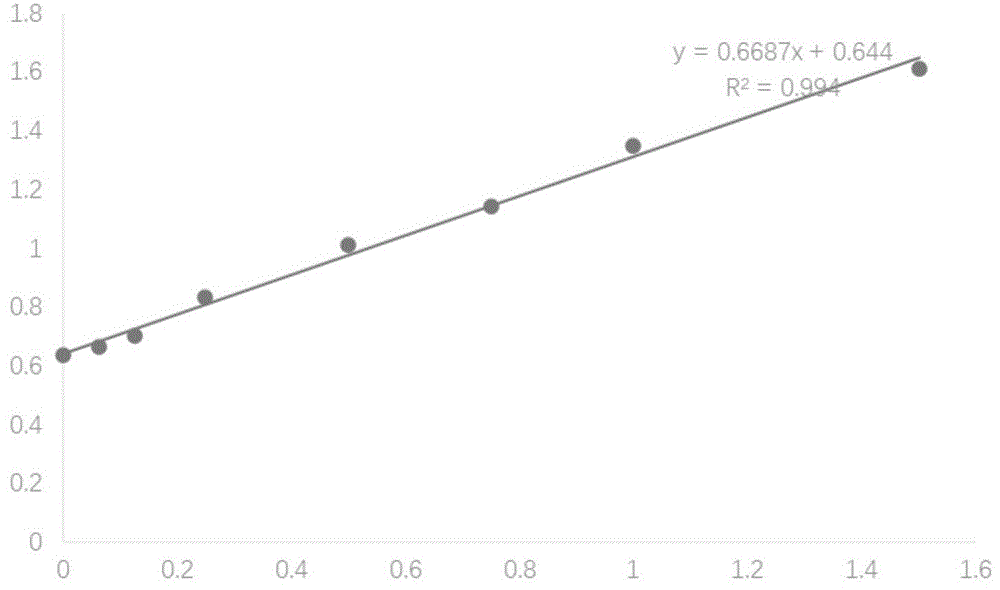
图1为蛋白标准曲线。
图2为PLA2R-CC1H重组蛋白纯化图;其中,1:13μg非还原PLA2R-CC1H;2:13μg还原PLA2R-CC1H;3:35μg非还原PLA2R-CC1H;4:35μg还原PLA2R-CC1H;M:蛋白Maker。
图3为PLA2R-CC2H重组蛋白纯化图;1:13μg非还原PLA2R-CC2H;2:13μg还原PLA2R-CC2H;3:35μg非还原PLA2R-CC2H;4:35μg还原PLA2R-CC2H;M:蛋白Maker。
图4为ELISA方法血浆滴定实验PLA2R-CC1H检测血浆中PLA2R抗体。
图5为ELISA方法血浆滴定实验PLA2R-CC2H检测血浆中PLA2R抗体。
具体实施方式
以下实施例仅用于进一步说明本发明,但不限制本发明。下述实施例中未注明具体条件的实验方法,均按照常规条件。
实施例1:本发明所述PLA2R重组蛋白的重组表达
1、PLA2R重组蛋白基因重组表达质粒的构建
(1)获取目的基因:
确定PLA2R重组蛋白基因酶切位点和特异性引物,其中PLA2R-CC1H基因上游引物为5'-GCCTCCGGACTCTAGAGGGCCACCATGCTGCTGTCG-3'(SEQ ID NO:5),下游引物为5'-CATTACTAACCGGTAGGGTTAGTGATGGTGATGGTGATGACCTCCT-3'(SEQ ID NO:6);PLA2R-CC2H基因上游引物为5'-GCCTCCGGACTCTAGAGGGCCACCATGCTGCTGTCG-3'(SEQ ID NO:5),下游引物为5'-CATTACTAACCGGTAGGGTTAGTGATGGTGATGGTG ATGACCTCC-3'(SEQ ID NO:7)。PCR以表1合成基因为模板,其中SEQ ID No.8为信号肽序列。PCR反应体系采用的是TAKARA的KOD反应体系(Cat.KFX-101),扩增体系如表2所示。PCR反应条件:94℃2min;98℃10s,60℃30s,68℃2min,30个循环;10℃保温。
表1PCR模板
表2KOD反应体系
(2)制备重组质粒pcDNA3.4-PLA2R-CC1H和pcDNA3.4-PLA2R-CC2H:
将胶回收的PLA2R-CC1H、PLA2R-CC2H目的片段和pcDNA3.4载体进行同源重组,利用NEB的试剂盒(
表3同源重组
2、PLA2R重组蛋白的表达
(1)培养悬浮CHO-S细胞至活率大于95%,用新鲜的ExpiCHO表达培养基(GIBCO)调整活细胞密度至6x10
(2)37℃、5% CO
3、PLA2R重组蛋白的纯化
(1)按照表4配置蛋白纯化所用的试剂。
表4蛋白纯化所用的试剂及其配置方法
(2)将样品4℃,7000rpm离心15min,留上清经0.22um针头滤器过滤。首先用Nisepharose 6FF柱进行纯化。用Buffer A1洗平后用0-100% Buffer B1洗脱,收集洗脱蛋白。将含目的蛋白的洗脱峰经30kD超滤离心管中进行超滤,4℃离心10min,截留上清。由于PLA2R-CC1H和PLA2R-CC2H预测等电点均低于7.0,因此选用DEAE柱进行纯化。将上一步纯化得到的样品进行10倍体积的Buffer A2稀释以降低离子强度,平衡后用0-100%的BufferB2洗脱,收集洗脱峰样品。洗脱液经超滤浓缩至<1.5mL后用Super dex 200柱纯化。平衡后用120mL最终溶剂洗脱。最后将洗脱峰经30kD超滤离心管进行超滤,截留上清分别记为PLA2R-CC1H洗脱超滤和PLA2R-CC2H洗脱超滤。
实施例2:PLA2R-CC1H重组蛋白或PLA2R-CC2H重组蛋白的浓度、纯度鉴定1、Bradford法测定PLA2R-CC1H重组蛋白或PLA2R-CC2H蛋白质含量以表5的浓度梯度制备蛋白标准曲线,获得的标准曲线如图1,R
表5:制备标准曲线(单位mg/mL)
以5mg/mL BSA为标准品,估计体积。PLA2R-CC1H稀释2倍测定OD值为1.239,PLA2R-CC1H稀释2倍测定OD值为1.064(表6)。根据测定OD值,利用蛋白标准曲线(图1),获得样品PLA2R-CC1H测得浓度为1.78mg/mL,样品PLA2R-CC2H测得浓度为1.26mg/mL(表6)。
表6:PLA2R-CC1H重组蛋白和PLA2R-CC2H蛋白质含量测定
2、纯化产物经SDS-PAGE进行纯度测定
将超滤后的PLA2R-CC1H重组蛋白和PLA2R-CC2H重组蛋白定量后,各取13μg、35μg蛋白进行电泳。电泳条件为SDS-PAGE,预制胶,10孔。150V,50min。样品90℃加热5min。PLA2R-CC1H重组蛋白和PLA2R-CC2H重组蛋白的蛋白大小如表7。
表7:PLA2R-CC1H重组蛋白和PLA2R-CC2H重组蛋白的分子量
从图1和图2可知PLA2R-CC1H、PLA2R-CC2H蛋白分子量大小正确、没有杂带,蛋白较纯。
实施例3:PLA2R-CC1H重组蛋白或PLA2R-CC2H重组蛋白作为捕获抗原检测膜性肾病患者pMN-1,pMN-2的血浆抗体。
1、PLA2R-CC1H和PLA2R-CC2H捕获抗原准备
PLA2R-CC1H浓度0.359mg/mL,PLA2R-CC2H浓度0.424mg/mL。使用包被液调整PLA2R-CC1H,PLA2R-CC2H浓度为10μg/mL,每孔加入100μL。按照表8准备样品和阴性对照所需捕获抗原。
表8捕获抗原
2、血清样品准备
样品1来自pMN-1患者,样品2来自pMN-2患者,阴性对照为健康人1,健康人2和健康人3的血浆。收集的全血经过1000g,5min离心后,取上清后分装并进行本实验。各组血浆建立浓度梯度,分别稀释5倍,50倍,500倍,5000倍,50000倍,500000倍,5000000倍,每个浓度梯度设置复孔。
3、ELISA法中各种缓冲液、试剂及加样方案
(1)按照表7配置ELISA法的试剂。
表7ELISA法所用的试剂及其配置方法
(2)检测抗体:HRP标记的小鼠抗人IgG单克隆抗体(Genscript)。
(3)加样方案(如表7):将不同浓度的患者或健康人血浆与抗原PLA2R-CC1H或PLA2R-CC2H反应。
表7抗原与血浆加样组合方案
4、临床标本检测实验
ELISA法测定血清中PLA2R抗体的浓度:
(1)加入100μL捕获抗原到ELISA板反应孔中,封板,于4℃过夜;
(2)使用200μL 1X洗液洗板,静置1min后弃液体,重复3次,弃掉孔内液体;
(3)加入100μL 5% BSA,37℃温育30min,按照(2)的方法洗板,弃掉孔内液体;
(4)按照加样方案每孔加入100μL对应浓度血浆,封板,37℃温育1h,按照(2)的方法洗板,弃掉孔内液体;
(5)加入100μL经标记分子标记的并且与PLA2R抗体有反应性的检测抗体,封板,37℃温育1h,按照(2)的方法洗板,弃掉孔内液体;
(6)加入100μL TMB,25℃避光温育15min;
(7)加入100μL终止液并于450nm检测OD值。
从图2和图3可知,和阴性对照相比,pMN-1和pMN-2患者血浆中都存在IgG抗体,且pMN-2患者血液中的抗体含量比pMN-1高;分析PLA2R-CC1H重组蛋白和PLA2R-CC2H重组蛋白的抗体结合能力可知两者相似。
/>
/>
/>
/>
/>
/>
