一种新的吗啉衍生物的制备方法
文献发布时间:2024-04-18 19:59:31
本申请要求申请日为2022年8月1日的中国专利申请CN202210914696.3的优先权,本申请引用上述中国专利申请的全文。
技术领域
本发明属于药物化学领域,具体涉及一种新的吗啉衍生物的制备方法。
背景技术
3CLPro(3C-like protease,又称3C样蛋白酶)是新型冠状病毒(COVID-19,SARS-CoV-2)产生的主要蛋白酶,冠状病毒大多数功能蛋白(非结构蛋白)由ORF1ab基因编码,先翻译成一个多蛋白体(7096aa),再由3CLPro切割成多个有活性的蛋白如病毒复制蛋白RdRp。此外,该蛋白可能切割胞内蛋白NEMO从而抑制干扰素信号途径的活化。因此抑制3CLPro能够有效抑制病毒的感染与复制。
WO2023036140A记载了一种3CLPro蛋白酶抑制剂,其中化合物(5-溴-2-((R)-1-(5-(甲氨基)烟碱酰)哌啶-3-基)氨基)-3-硝基苯基((2R,6S)-2,6-二甲基吗啉基)甲酮对SARS-CoV-23CLpro/Mpro蛋白酶具有良好的抑制作用,且在小鼠体内具有较高的暴露量和生物利用度,有望开发为临床药物,其结构如下所示:
发明内容
本发明提供式(IV)所示化合物或其药学上可接受的盐的制备方法,其特征在于:
式(II)化合物在缚酸剂下,
与式(III)化合物发生烷基化反应得到式(IV)化合物
本发明某些实施方案,所述缚酸剂选自选自三乙胺、N,N-二异丙基乙胺、N-甲基吗啉、吡啶、碳酸钾或碳酸钠中的一种或多种任意组合。
本发明某些实施方案,所述烷基化反应所用溶剂选自乙腈、乙醇、异丙醇、正丙醇、丙酮、丁酮、水、N,N-二甲基甲酰胺或N,N-二甲基乙酰胺中的一种或多种任意组合。
本发明某些实施方案,所述的式(II)化合物:式(III)化合物的摩尔比为1:0.9~1:2。
本发明某些实施方案,所述的式(II)化合物:式(III)化合物的摩尔比为1:0.9~1:1.5,优选1:1.2。
本发明某些实施方案,所述的式(II)化合物:缚酸剂的摩尔比为1:1~1:5。
本发明某些实施方案,所述的式(II)化合物:缚酸剂的摩尔比为1:2~1:4,优选1:3。
本发明某些实施方案,将所制备的式(IV)化合物作为制备由下式(I)所示化合物或其药学上可接受的盐的合成中间体:
本发明某些实施方案,制备的式(IV)化合物如下使用:
使式(IV)化合物与式(V)化合物
在缩合剂、有机碱条件下反应以便获得由下式(VI)所示的化合物
以及式(VI)所示的化合物脱除Boc保护基得到式(VII)所示的化合物或其盐
以及式(VII)所示的化合物或其盐与式(VIII)所示的化合物
发生酰化反应得到式(I)化合物或其药学上可接受的盐
本发明某些实施方案,其中所述的缩合剂选自2-(7-偶氮苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(HATU)、O-苯并三氮唑-四甲基脲六氟磷酸酯(HBTU)、6-氯苯并三氮唑-1,1,3,3-四甲基脲六氟磷酸酯(HCTU)、六氟磷酸苯并三唑-1-基-氧基三吡咯烷基磷(PyBOP)或1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐(EDCI)。
本发明一些实施方案,其中所述的有机碱选自三乙胺、N,N-二异丙基乙胺或N-甲基吗啉中的一种或多种任意组合。
本发明一些实施方案,其中所述缩合反应还加入催化剂,所述的催化剂选自4-N,N-二甲基吡啶(DMAP)或1-羟基苯并三氮唑(HOBt)。
解释和定义
除非另有说明,本文所用的下列术语和短语旨在具有下列含义。一个特定的术语或短语在没有特别定义的情况下不应该被认为是不确定的或不清楚的,而应该按照普通的含义去理解。
“烷基”是指直链或支链的饱和烃基。优选C
“卤素”表示氟、氯、溴或碘原子。
本发明中,酰胺反应用到缩合剂和有机碱,缩合剂包括但不限于碳二亚胺类缩合剂、碳鎓盐类的缩合剂、鏻鎓盐类缩合剂、有机磷类缩合剂等。
碳二亚胺类缩合剂选自二环己基碳二亚胺(DCC)、二异丙基碳二亚胺(DIC)和1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐(EDCI);
使用碳二亚胺类缩合剂时一般需要加入催化剂或活化剂,所述的催化剂或活化剂选自4-N,N-二甲基吡啶(DMAP)、1-羟基苯并三氮唑(HOBt)等;
所述的碳鎓盐类的缩合剂包括但不限于2-(7-偶氮苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(HATU)、O-苯并三氮唑-四甲基脲六氟磷酸酯(HBTU)、6-氯苯并三氮唑-1,1,3,3-四甲基脲六氟磷酸酯(HCTU)、O-(7-氮杂苯并三氮唑-1-基)-二(四氢吡咯基)碳鎓六氟磷酸盐(HAPyU)、O-(苯并三氮唑-1-基)-二(四氢吡咯基)碳鎓六氟磷酸盐(HBPyU)、O-(苯并三氮唑-1-基)-二(二甲胺基)碳鎓四氟硼酸盐(TBTU)、O-(N-丁二酰亚胺基)-二(二甲胺基)碳鎓四氟硼酸盐(TSTU)等;
鏻鎓盐类缩合剂包括但不限于六氟磷酸苯并三唑-1-基-氧基三吡咯烷基磷(PyBOP)、六氟磷酸7-偶氮苯并三氮唑-1-基-氧基三吡咯烷基磷(PyAOP)、苯并三氮唑-1-基氧-三(二甲胺基)鏻鎓六氟磷酸盐(BOP);
有机磷类缩合剂包括但不限于二苯基磷酰氯(DPP-Cl)、氰代磷酸二乙酯(DECP)、叠氮化磷酸二苯酯(DPPA)、硫代二甲基磷酰基叠氮(MPTA)、二(2-氧-3-唑烷基)磷酰氯(BOP-Cl)等。
本发明中,缚酸剂包括有机碱或无机碱,其中无机碱包括但不限于碳酸钾、碳酸钠、氢氧化钾、氢氧化钠、氢氧化锂、氢氧化钙、碳酸氢钠等。
本发明中,有机碱包括但不限于三乙胺(TEA)、N,N-二异丙基乙胺(DIPEA)、N-甲基吗啉(NMM)、吡啶(Py)、乙二胺(EDA)、一乙醇胺(MEA)、4-N,N-二甲氨基吡啶(DMAP)、1,8-二氮杂二环十一碳-7-烯(DBU)、叔丁醇钾、叔丁醇钠、正丁基锂、叔丁基锂、二(三甲基硅基)氨基钠(NaHMDS)、二异丙基氨基锂(LDA)等。
本发明所述的异构体包含几何异构体和立体异构体,例如顺反异构体、对映异构体、非对映异构体、及其外消旋混合物和其他混合物,所有这些混合物都属于本发明的范围之内。
术语“对映异构体”是指互为镜像关系的立体异构体。
术语“非对映异构体”是指分子具有两个或多个手性中心,并且分子间为非镜像的关系的立体异构体。
除非另有说明,用楔形实线键
本发明中,4M的氯化氢-1,4-二氧六环溶液中的M为浓度单位,代表mol/L,氯化氢为HCl。
附图说明
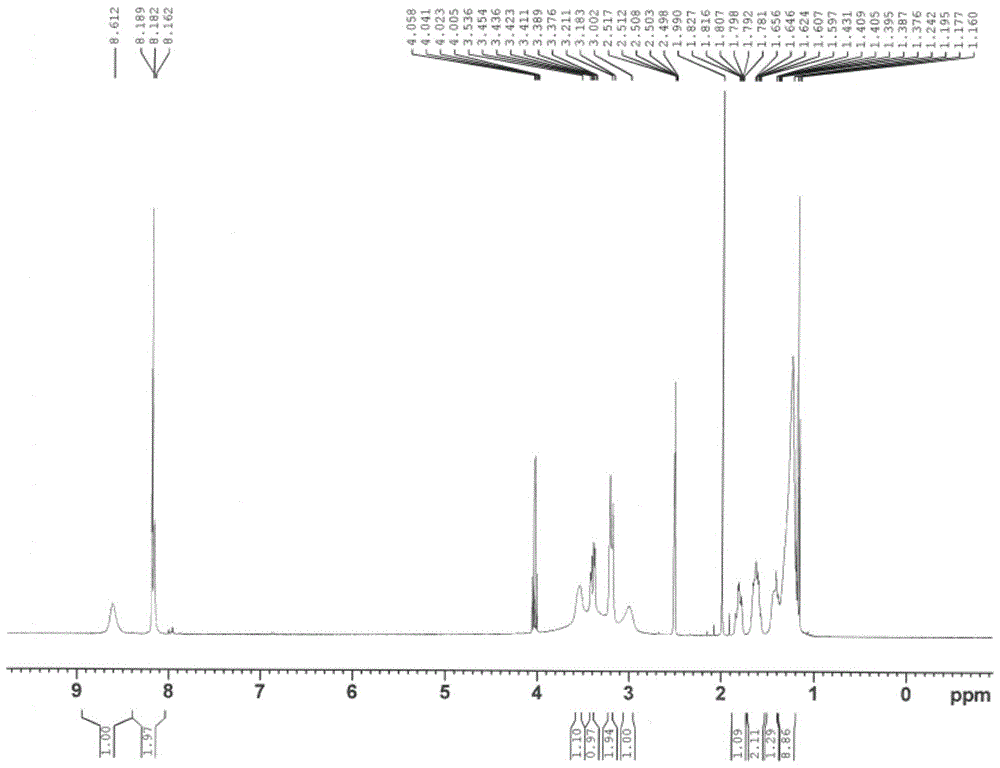
图1为式(IV)化合物的核磁氢谱图
具体实施方式
下面通过实施例对本发明进行详细描述,但并不意味着对本发明任何不利限制。本文已经详细地描述了本发明,其中也公开了其具体实施例方式,对本领域的技术人员而言,在不脱离本发明精神和范围的情况下针对本发明具体实施方式进行各种变化和改进将是显而易见的。
实验仪器汇总:
本发明的化合物结构是通过核磁共振(NMR)或/和液质联用色谱(LC-MS),或超高效液质联用色谱(UPLC-MS)来确定的。NMR化学位移(δ)以百万分之一(ppm)的单位给出。NMR的测定是用Bruker Neo 400M或者Bruker Ascend 400核磁仪器,测定溶剂为氘代二甲基亚砜(DMSO-d6),氘代甲醇(CD
液质联用色谱LC-MS的测定用Agilent 1260-6125B single quadrupole massspectrometer,柱子为Welch Biomate column(C18,2.7μm,4.6×50mm)或者waters H-Class SQD2,柱子为Welch Ultimate column(XB-C18,1.8μm,2.1×50mm)质谱仪(离子源为电喷雾离子化)。
超高效液质联用色谱UPLC-MS的测定用Waters UPLC H-class SQD质谱仪(离子源为电喷雾离子化)。
HPLC的测定使用Waters e2695-2998或Waters ARC和Agilent 1260或AgilentPoroshell HPH高效液相色谱。
薄层层析硅胶板使用烟台江友硅胶开发有限公司GF254硅胶板或乳山市上邦新材料有限公司GF254硅胶板,TLC采用的规格是0.15mm~0.20mm,制备型20×20cm,柱层析一般使用于成化工200~300目硅胶为载体。
本发明实施例中的起始原料是已知的并且可以在市场上买到,或者可以采用或按照本领域已知的方法来合成。
在无特殊说明的情况下,本发明的所有反应均在连续的磁力搅拌下,在干燥氮气或氩气气氛下进行,溶剂为干燥溶剂,反应温度单位为摄氏度或℃。如无特别说明,室温指25±5℃。
实施例1
(5-溴-2-((R)-1-(5-(甲氨基)烟碱酰)哌啶-3-基)氨基)-3-硝基苯基((2R,6S)-2,6-二甲基吗啉基)甲酮的制备
反应路线:
第一步:式(IV)化合物的制备
在室温条件下,氮气保护,将式(II)化合物(10g,37.9mmol)溶于乙腈(100mL),加入N,N-二异丙基乙胺(14.3g,111mmol),加入式(III)化合物(8.3g,41.7mmol),升温至80℃,搅拌反应1h。
LCMS监测显示原料消失后,降温至50℃,减压蒸馏;向减蒸母液中加入乙酸乙酯(100mL)搅拌溶解,有机相用饱和碳酸氢钠水溶液(100mL×2)、饱和食盐水(50mL×2)洗涤,无水硫酸钠干燥,过滤,减压浓缩得到式(IV)化合物,(16.1g,收率95.7%)。
1
MS(ESI)M/Z:442.0[M-H]
第二步:式(VI)化合物的制备
在室温条件下,氮气保护,将式(IV)化合物(15g,34mmol),溶于DMF(120mL),降温至0℃,依次加入N,N-二异丙基乙胺(13.1g,101mmol)、(2-(7-偶氮苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(缩写HATU,19.3g,51mmol)和(2R,6S)-2,6-二甲基吗啉(4.7g,41mmol)。反应体系在0℃下继续搅拌15分钟。
LCMS监测显示原料消失后,向反应液中加入水(200mL)淬灭,混合液用乙酸乙酯(100mL×3)萃取,合并有机相,有机相用饱和食盐水(100mL×2)洗涤,无水硫酸钠干燥,过滤,减压浓缩,得到式(VI)化合物,(17.3g,94.6%)。
MS(ESI)M/Z:441.0[M-99]
第三步:式(VII)化合物的制备
在室温条件下,氮气保护,将式(VI)化合物(17g,31mmol)溶于4M的盐酸-1,4-二氧六环溶液(85mL)。然后该反应体系在室温下搅拌1小时。
LCMS监测显示原料消失后,将反应液减压蒸馏浓缩,加入甲基叔丁基醚(350ml),搅拌析晶1h,过滤,烘干得到式(VII)化合物,(14.2g,94.7%)。
MS(ESI)M/Z:441.0[M+H-HCl]
第四步:式(I)化合物的制备
在室温条件下,氮气保护,将式(VIII)化合物(5.3g,35mmol)溶于N,N-二甲基甲酰胺(140mL)中。随后,将上述溶液降温至0℃,依次加入式(VII)化合物(14g,29mmol)、2-(7-偶氮苯并三氮唑)-N,N,N',N'-四甲基脲六氟磷酸酯(16.7g,44mmol)和N,N-二异丙基乙胺(11.4g,88mmol)。该反应体系在0℃下搅拌15分钟。
LCMS监测显示原料消失后,向反应液中加入水(500mL)淬灭,混合液用乙酸乙酯(500mL×3次)萃取,合并有机相,有机相用饱和食盐水(200mL×2次)洗涤。然后用无水硫酸钠干燥,过滤,减压浓缩,得到式(I)化合物,(14.3g,84.8%)。
MS(ESI)M/Z:575.0[M+H]
1
生物学测试评价
测试例1:评价式(I)化合物对SARS-CoV-2 3CLpro/Mpro靶点的抑制效果
本实验采用荧光共振能量转移的方法来检测SARS-CoV-2 3CLpro/Mpro蛋白酶的活性,并得出化合物对SARS-CoV-2 3CLpro/Mpro蛋白酶的半数抑制浓度IC
新型冠状病毒Mpro/3CLpro抑制剂筛选试剂盒(P0315M)购自Beyotime公司。
用反应缓冲液配置酶溶液,在各孔中加49.5μL的酶溶液;在Min孔中加49.5μL的反应缓冲溶液。化合物检测IC50,测试终浓度为10μM起始,3倍稀释,10个浓度,每个浓度设置复孔测试。将待测化合物稀释成200倍终浓度的溶液,使用D300e(TECAN)超微量加样器加入250nL梯度稀释的待测化合物到384孔反应板中。Max孔和Min孔中均转移250nL的100%DMSO。置冰上孵育10分钟。用D300e(TECAN)在各孔中加入250nL底物溶液。将反应板1000rpm离心1min,使用Envision酶标仪(PerkinElmer)连续读取30分钟的荧光信号。使用GraphPadPrism 8软件进行数据分析,计算化合物的IC
实验测得,式(I)化合物的IC
测试例2:CD1小鼠的体内药代动力学实验
以雄性CD1小鼠为受试动物,研究本发明化合物对雄性CD1小鼠在剂量为10mg/kg时经口服给药后的体内药代动力学行为。
供试品:对照化合物和式(I)化合物。
试验动物
种属:雄性CD1小鼠(3只/组)
等级:SPF级
体重:约20~30g
年龄:6~8周
来源:维通利华
雄性CD1小鼠灌胃给予供试品溶液,给药剂量为10mg/kg,给药体积为10mL/kg。
供试品溶液的配制:供试品采用溶媒(10%DMSO+50%PEG400+40%纯净水)溶解,配制时依次加入DMSO、PEG400和纯净水。
对照组:CN113072497A专利化合物2,其结构式如下:
实验组:式(I)化合物。
分别于给药前(0h)和给药后0.25h,0.5h,1h,2h,4h,8h,24h,按照设置的采血时间点,从小鼠足背静脉采集约0.025~0.03mL全血(用EDTA-K2抗凝),置于湿冰条件下,并在采集后30min内以4000g离心力、4℃、离心5min,分离血浆并转移到检测管中。
药代动力学主要参数用WinNonlin(PhoenixTM,version 6.1)计算得到,药代动力学参数参见如表1和表2。
表1 CD1小鼠口服给药的药代动力学参数
备注:NA代表无相应数据。
表2 CD1小鼠静脉给药的药代动力学参数
结果显示:与对照组相比,式(I)化合物在小鼠体内具有较高的暴露量和生物利用度,具有良好的药代动力学性质。
测试例3:食蟹猴的体内药代动力学实验
以雄性食蟹猴为受试动物,研究式(I)化合物在10mg/kg下口服给药在食蟹猴体内血浆的药代动力学行为。
1.试验方案
1.1供试品:
式(I)化合物。
1.2试验动物
动物基本信息
种属:食蟹猴
等级:普通级
数量:18只食蟹猴(雄)用于给药实验
体重:约2.5~4.5kg
年龄:约3~5岁
来源:从化市华珍动物养殖场(普通合伙)
1.3给药:
9只雄性食蟹猴,3只/组,共3组。动物给药前禁食12小时,灌胃给药供试品溶液(10mg/kg),给药体积2.5mL/kg。
供试品溶液的配制:供试品采用10%DMSO+50%PEG400+40%纯净水溶解,配制时依次加入DMSO、PEG400和纯净水。
1.4样品采集:
分别于给药前(0min)、给药后0.25h,0.5h,1h,2h,4h,6h,8h,12h,24h和48h(11个)。
按照设置的采血时间点,由从猴后肢静脉采血约1.5mL,置于湿冰条件下,并在采集后
1.5h内离心,以1700g离心力,4℃,离心10min。离心之后,取血浆加入到检测管中。离心后2小时内可将血浆样本置于-20℃以下的冰箱中保存。
2.实验结果与分析
药代动力学主要参数用WinNonlin 8.1.0.3530计算得到,结果显示,式(I)化合物具有良好的药代动力学性质。
表3食蟹猴口服给药的药代动力学参数
