一种治疗肝癌的联合用药物
文献发布时间:2023-06-19 09:47:53
技术领域
本发明涉及抗癌药物领域,具体涉及一种治疗肝癌的联合用药物。
背景技术
近年来,随着人们生活方式的不断西化及肝炎疫苗的普及,非酒精性脂肪性肝病已经成为当今全球第一大肝脏疾病,并替代病毒性和酒精性相关肝脏疾病成为肝癌最主要的病因促进因子。既往研究表明高脂可以通过炎症,内质网应激,肠内菌群失调来促进肝癌的进展。但肝癌如何调节脂代谢来适应高脂环境,并避免脂毒性的研究还很少。因此靶向脂代谢是治疗肝癌的一种新策略。
SOAT1,是一种胆固醇酰基转移酶,可以将胞内游离脂肪酸和胆固醇转移到胆固醇酯,从而形成一种脂滴储存起来。阿伐麦布是一种SOAT1的抑制剂,CAS:166518-60-1,分子式:C
CPT1A,肉毒碱棕榈酰基转移酶1A,是脂肪酸由胞浆转移到线粒体氧化供能的关键限速酶。乙莫克舍是一种CPT1A的抑制剂,CAS:124083-20-1,分子式:C
发明内容
本发明要解决的问题是:提供一种疗效优良的治疗肝癌的联合用药物。
本发明的技术方案如下:
一种治疗肝癌的联合用药物,所述联合用药物是分别或同时给药的SOAT1抑制剂和CPT1A抑制剂的联合用药物。
如前述的联合用药物,所述SOAT1抑制剂是阿伐麦布,所述CPT1A抑制剂是乙莫克舍。
进一步地,所述SOAT1抑制剂和CPT1A抑制剂的摩尔比是1:0.977~1:5。
一种治疗肝癌的药物组合物,它由SOAT1抑制剂和CPT1A抑制剂组成。
进一步地,所述SOAT1抑制剂是阿伐麦布,所述CPT1A抑制剂是乙莫克舍。
进一步地,所述SOAT1抑制剂和CPT1A抑制剂的摩尔比是1:0.977~1:5。
一种治疗肝癌的药物,所述药物以前述的药物组合物为活性成分,加上药学上可接受的辅助性成分制备而成。
SOAT1抑制剂和CPT1A抑制剂同时作为抗癌活性成分,在制备治疗肝癌的药物中的用途。
进一步地,所述SOAT1抑制剂是阿伐麦布,所述CPT1A抑制剂是乙莫克舍。
进一步地,所述SOAT1抑制剂和CPT1A抑制剂的摩尔比是1:0.977~1:5。
有益效果:
本发明的联合用药物及药物组合物中,SOAT1抑制剂和CPT1A抑制剂可发挥协同抗肿瘤作用,优于单独使用SOAT1抑制剂或CPT1A抑制剂,因而其能更好地治疗肝癌,应用前景良好。
显然,根据本发明的上述内容,按照本领域的普通技术知识和惯用手段,在不脱离本发明上述基本技术思想前提下,还可以做出其它多种形式的修改、替换或变更。
以下通过实施例形式的具体实施方式,对本发明的上述内容再作进一步的详细说明。但不应将此理解为本发明上述主题的范围仅限于以下的实例。凡基于本发明上述内容所实现的技术均属于本发明的范围。
附图说明
图1:阿伐麦布和乙莫克舍体外协同抑制肝癌细胞增殖;CI<1。
图2:克隆形成实验。
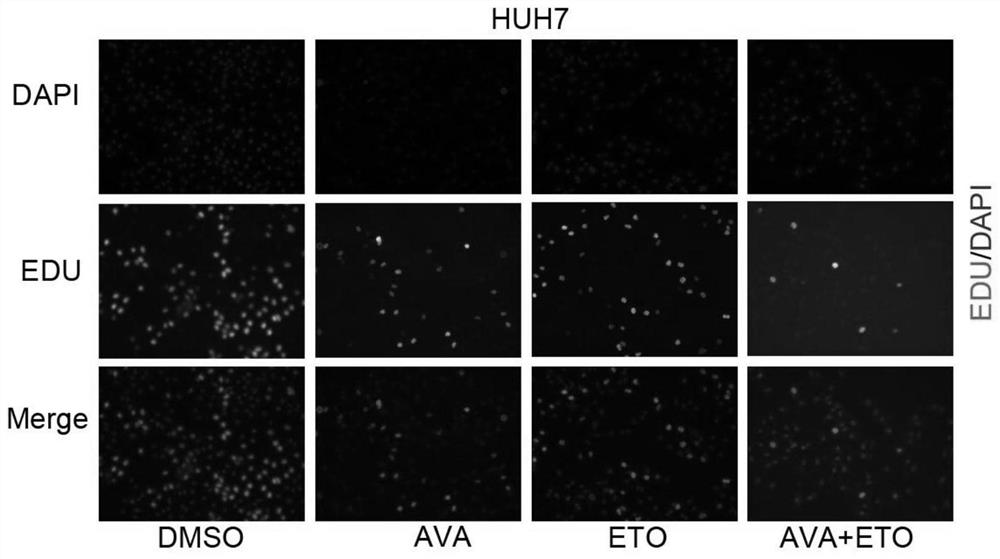
图3:EDU测癌细胞增殖。
图4:蛋白免疫印迹。
图5:阿伐麦布和/或乙莫克舍体内抑制肿瘤效果。
图6:阿伐麦布和/或乙莫克舍体内抑制肿瘤体积及体重统计图。
说明:附图中,AVA代表阿伐麦布;ETO代表乙莫克舍;*表示显著差异(p<0.05);**表示极显著差异(p<0.01);***表示非常显著的差异(p<0.001);免疫印迹图中:-表示没用药;+表示用药。
具体实施方式
实施例1 SOAT1抑制剂联合CPT1A抑制剂在体外抑制肝癌细胞
肝癌细胞株:HepG2,HUH7。
SOAT1抑制剂:阿伐麦布。
CPT1A抑制剂:乙莫克舍。
1.实验方法
1.1实验处理:分别使用生理盐水(对照)、阿伐麦布、乙莫克舍或阿伐麦布+乙莫克舍处理两种肝癌细胞。
1.2检测:
(1)CCK8检测细胞数量
阿伐麦布与乙莫可舍摩尔浓度比为1:5,如同所示处理肝癌细胞,3天后,采用CCK8检测细胞数量,结果运用Chou-Talalay公式计算协同指数(CI)。
(2)观察细胞克隆形成
实验处理7天后,使用结晶紫染色,观察克隆数量。
(3)EDU测癌细胞存活率
实验处理48h后,采用EDU试剂盒检测。
(4)蛋白免疫印迹
实验处理48h后,提取细胞总蛋白,进行蛋白免疫印迹,检测CDK4、CDK6、Cyclin D1(增殖相关蛋白)和GAPDH(作为内参)。
2.实验结果
2.1 CCK8检测细胞数量,其结果用Chou-Talalay公式计算协同指数(combinationindex:CI),其中CI<1表示有协同作用,CI=1表示只有单纯的叠加作用,CI>1表示拮抗作用。
如图1所示,阿伐麦布(AVA)+乙莫克舍(ETO)组的CI值低于1,表示阿伐麦布联合乙莫可舍有协同抗肿瘤作用;Fa(fraction affect)表示抑制率。
2.2细胞克隆数
如图2所示,阿伐麦布+乙莫克舍组的细胞克隆数明显少于单独使用阿伐麦布或乙莫克舍的组别。
2.3癌细胞存活率
EDU试剂检测癌细胞存活率的结果如图3所示,可见,阿伐麦布+乙莫克舍组的活的癌细胞(视野内7个细胞),明显少于单独使用阿伐麦布(视野内24个细胞)或乙莫克舍(视野内40个细胞)的组别,更明显地少于对照组(视野内86个细胞)。
2.4蛋白免疫印迹
蛋白免疫印迹结果如图4所示,在HepG2和HUH7,联合用药都显著降低了CDK4、CDK6、Cyclin D1(均为增殖相关蛋白)的表达,与CCK8和克隆形成实验的结果一致。
3.结论
阿伐麦布和乙莫克舍具有协同抗肿瘤作用。
实施例2阿伐麦布联合乙托克舍在体内抑制肝癌细胞
肝癌细胞株:HepG2。
SOAT1抑制剂:阿伐麦布。
CPT1A抑制剂:乙莫克舍。
动物模型构建:将肝癌细胞株异种移植到裸鼠体内。
1.实验方法
1.1实验处理:对动物模型分为对照组、阿伐麦布、乙莫克舍和联合用药组。阿伐麦布组通过腹腔注射阿伐麦布15mg/kg,每天一次;乙莫克舍组通过腹腔注射乙莫克舍10mg/kg,每天一次;联合用药组腹腔注射阿伐麦布15mg/kg和乙莫克舍10mg/kg(阿伐麦布与乙莫克舍药物摩尔比为1:0.977),每天一次。
1.2检测:
测定小鼠体重和移植肿瘤体积、重量,并在第14天分批处死动物模型。
2.结果
小鼠体重方面,各组均无显著差别。
肿瘤体积方面,小鼠荷瘤状态如图5所示,肿瘤体积与重量随时间变化趋势如图6所示。可见,联合用药(阿伐麦布+乙莫克舍)组的肿瘤体积最小,增长趋势缓慢,与对照组有显著差异;阿伐麦布组与乙莫克舍组的体积稍大,与对照组有减小趋势。
3.结论
联合使用阿伐麦布和乙莫克舍,相比阿伐麦布或乙莫克舍单独使用,能在体内发挥更为有效的抑制肝癌的能力。
综上,本发明所公开的联合用药物可显著抑制肝癌细胞的增殖,具有良好的应用前景。
- 一种治疗肝癌的联合用药物
- 一种治疗肝癌的联合用药物
