一种强化毕赤酵母表达外源蛋白的方法
文献发布时间:2023-06-19 11:55:48
技术领域
本发明涉及发酵工程技术领域,尤其涉及一种强化毕赤酵母表达外源蛋白的方法。
背景技术
人源溶菌酶(hLYZ)作为一种天然的抑菌活力物质,在畜牧、医药及食品等行业具有潜在的应用价值。利用甲醇营养型重组毕赤酵母进行发酵是生产人源溶菌酶的有效手段,人源溶菌酶可全部分泌于发酵液中。在完成重组工程菌的构建以及摇瓶工艺优化的基础上,研究重点已转移到发酵罐规模发酵工艺的优化上。
一般而言,利用重组毕赤酵母生产外源蛋白的发酵过程可分为细胞生长期和甲醇诱导期两个阶段。其中,细胞生长阶段的主要目的是以甘油为唯一碳源、短时间内获得高密度的毕赤酵母细胞。后续甲醇诱导阶段的主要目的则是采用适当的甲醇流加策略以实现外源蛋白的高效表达。
近年来,大量研究表明利用重组毕赤酵母表达外源蛋白过程中,外源蛋白的表达能力与能否获取高密度且细胞骨架完整的重组毕赤酵母细胞直接相关。为此,在细胞生长阶段,通过实施合适的甘油流加策略,可以在短时间内获得高密度的细胞骨架完整的毕赤酵母细胞。甘油流加速度过慢、细胞生长速度缓慢;甘油流加速度过快则会出现“葡萄糖效应(Crabtree effect)”,导致乙醇等有毒代谢副产物的积累。尽管积累的乙醇在进入到甲醇诱导期时,也会被完全消耗殆尽,但其在细胞生长阶段长时间/高浓度的积累,破坏了重组菌的细胞骨架,不可逆地抑制了AOX相关编码基因的转录水平,导致毕赤酵母无法正常表达、严重影响毕赤酵母表达外源蛋白的发酵稳定性。甘油流加速度控制策略主要有定速流加、指数流加、DO-stat等。以上的甘油流加控制策略的实施都是为了实现“氧气充足-甘油受限”的生长环境,通过甘油受限可以在短时间内获得高密度细胞和抑制有毒副产物的积累(乙醇等)。但是,当毕赤酵母细胞长时间处于氧气充足的环境下,大量的活性氧(ROS)会在细胞中积累,当累积的ROS攻破细胞抗氧化防御系统时,可引起脂质、蛋白质、核酸等结构的损伤,进而导致细胞生长能力丧失甚至凋亡。据此,Xiao等人[Xiao AF,Zhou XS,Zhou Let al.Appl Microbiol Biotechnol,2006,72:837-844]适时地提出添加昂贵抗氧化剂(抗坏血酸等)的方式、以消除胞内ROS的积累胁迫,最终恢复了细胞的代谢活性和外源蛋白合成效率。但是采用该方法存在需要加入昂贵的抗氧化剂的缺点,会在无形之中增加发酵生产的成本的同时,由于没有在线检测抗坏血酸浓度的设备和模型,无法实时反馈抗坏血酸的匮乏情况。
通过多变量聚类分析可知,在细胞生长阶段,如果细胞结构和功能受到了不可逆转的损伤,即使诱导阶段的甲醇浓度控制在最优水平也不能实现外源蛋白的高效表达。
发明内容
本发明旨在解决现有技术中存在的技术问题。为此,本发明提供一种强化毕赤酵母表达外源蛋白的方法,目的是确保细胞在短时间内高速生长的同时,有效抑制细胞内ROS的积累胁迫。
基于上述目的,本发明提供了一种强化毕赤酵母表达外源蛋白的方法,所述方法包括当Mut
作为一种优选的实施方式,所述间歇性控制甘油流加工艺参数使细胞在ROS快速积累胁迫生长环境和ROS未积累胁迫生长环境之间循环5次,所述ROS快速积累胁迫生长环境中发酵液的溶解氧浓度为20-40%,甘油浓度0-1g/L,维持4.5h;所述ROS未积累胁迫生长环境中发酵液的溶解氧浓度为~0%,甘油浓度为2-5g/L,维持1h。
作为一种优选的实施方式,在甘油流加结束后,继续培养直至发酵液中残留的甘油完全耗尽,之后在发酵液中流加含有甲醇的诱导培养基启动甲醇诱导培养,甲醇诱导培养结束后,Mut
作为一种优选的实施方式,所述ROS快速积累胁迫生长环境是通过基于溶解氧电极在线监测溶解氧浓度进行调控甘油流加速度的调控方法得到的。
作为一种优选的实施方式,所述调控方法为初始发酵培养基中的甘油耗尽时,启动甘油流加控制程序,预设溶解氧浓度的设定值为30%,当溶解氧浓度高于设定值时,增大甘油流加速度;当溶解氧浓度低于设定值时,减小甘油流加速度。
所述ROS快速积累胁迫生长环境中甘油的流加速度采用如下计算公式得到:
其中,Y
作为一种优选的实施方式,所述ROS快速积累胁迫生长环境中溶解氧浓度的控制方法为利用工控机和其内置的AD-DA数据接口/转化卡,驱动程序可调式蠕动泵,以所述计算公式在发酵液中流加甘油。
作为一种优选的实施方式,所述ROS未积累胁迫生长环境是基于离线测量的甘油浓度并通过手动控制甘油流加速度的方法得到的。
作为一种优选的实施方式,所述Mut
作为一种优选的实施方式,在发酵起始培养时,通气速度为3-5vvm,温度为29-31℃,pH为5.8-6.2。
本发明的有益效果:
(1)采用本发明的方法,在细胞生长阶段结束时,ROS的浓度处于最低水平,实现了短时间内获得大量的结构完整、功能健全的毕赤酵母细胞。
(2)采用本发明的方法,在甘油流加阶段,维持细胞生长所需的甘油处于最低水平。
(3)采用本发明的方法,诱导期内毕赤酵母细胞的甲醇代谢途径中相关酶(AOX、FLD和FDH)的比活性得到了大幅地增强。
(4)利用本发明可以将毕赤酵母适应甲醇诱导环境的时间缩短一半。
(5)采用本发明的方法,当采用相同的甲醇诱导策略时,人源溶菌酶的活性达到了2.45×10
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
图1为对比例1中Mut
图2为对比例1中Mut
图3为对比例2中Mut
图4为对比例2中Mut
图5为实施例中Mut
图6为实施例中Mut
图7为Mut
图8为Mut
图9为Mut
图10为Mut
图11为Mut
图12为对比例1、对比例2以及实施例中Mut
图13为Mut
图14为Mut
图15为Mut
图16为Mut
图17为Mut
具体实施方式
为使本发明的目的、技术方案和优点更加清楚明白,以下结合具体实施例,并参照附图,对本发明进一步详细说明。
需要说明的是,除非另外定义,本发明实施例使用的技术术语或者科学术语应当为本公开所属领域内具有一般技能的人士所理解的通常意义。“包括”或者“包含”等类似的词语意指出现该词前面的元件或者物件涵盖出现在该词后面列举的元件或者物件及其等同,而不排除其他元件或者物件。
本发明中,在宿主菌株毕赤酵母KM71H中构建至少含有一个表达人源溶菌酶的基因拷贝和共表达Hac1p转录因子的重组毕赤酵母(hLYH4-3/Hac1p)菌株。
在本发明中,携带外源溶菌酶(human lysozyme,hLYZ)基因的甲醇利用慢型重组Pichia pastoris KM71H菌株由武汉轻工大学构建。
在发酵生产过程中所使用的的培养基的原料及使用量可以基于本研究领域中毕赤酵母表达人源溶菌酶的情况而定,只要能满足基本的细胞生长和维持代谢且在不产生不良影响(抑制细胞生长)和副作用(有毒副产物)即可。本发明所使用的培养基完全按照已经报道的培养基配方进行配制。
菌种
携带外源溶菌酶(human lysozyme,hLYZ)基因的甲醇利用慢型重组Pichiapastoris KM71H菌株由武汉轻工大学构建,构建方法参考文献:陈珊珊,丁健,李鑫等.江苏农业学报,2018,34:20-28。
培养基的组分
平板活化培养基(g/L):酵母粉10,葡萄糖20,蛋白胨20,琼脂20,pH自然。
种子培养基(g/L):酵母提取物10,葡萄糖20,蛋白胨20,pH自然。
分批发酵初始培养基(g/L):甘油20mL/L,硫酸镁1,硫酸钾1,硫酸铵5,硫酸钙0.1,磷酸2%(v/v),微量盐溶液(PTM
流加培养基(g/L):甘油500mL/L,(NH
诱导培养基(g/L):甲醇(分析纯,纯度99.5%),PTM
PTM
本发明高密度发酵表达人源溶菌酶的过程如下:
整个发酵过程都是在一个5L的发酵罐中进行。初始发酵培养基为1.5L,接种量为20%(v/v),温度控制在30℃,使用氨水和磷酸控制pH为6,通气量为4vvm。在分批培养阶段,通过调整转速控制DO在20%以上。当初始培养基中的甘油耗尽时,DO急剧上升,进入甘油流加阶段。当甘油流加阶段进行约25h时,停止甘油流加,饥饿1-2h直到耗尽发酵中残留的甘油,添加甲醇进入诱导阶段。
对比例1
“ROS快速积累胁迫”生长环境
具体步骤如下:以较低速度(F)流加甘油
对比例2
“ROS未积累胁迫”生长环境
具体步骤如下:在分批培养阶段,当DO急剧上升即为初始培养基中甘油耗尽,启动甘油定值控制策略,基于离线测量的甘油浓度手动控制甘油流加速度,将甘油浓度控制在2-5g/L,DO在甘油流加开始后自然而然地降至~0%(图3)。
实施例
“基于实验室自适应进化技术解除活性氧积累胁迫”生长环境
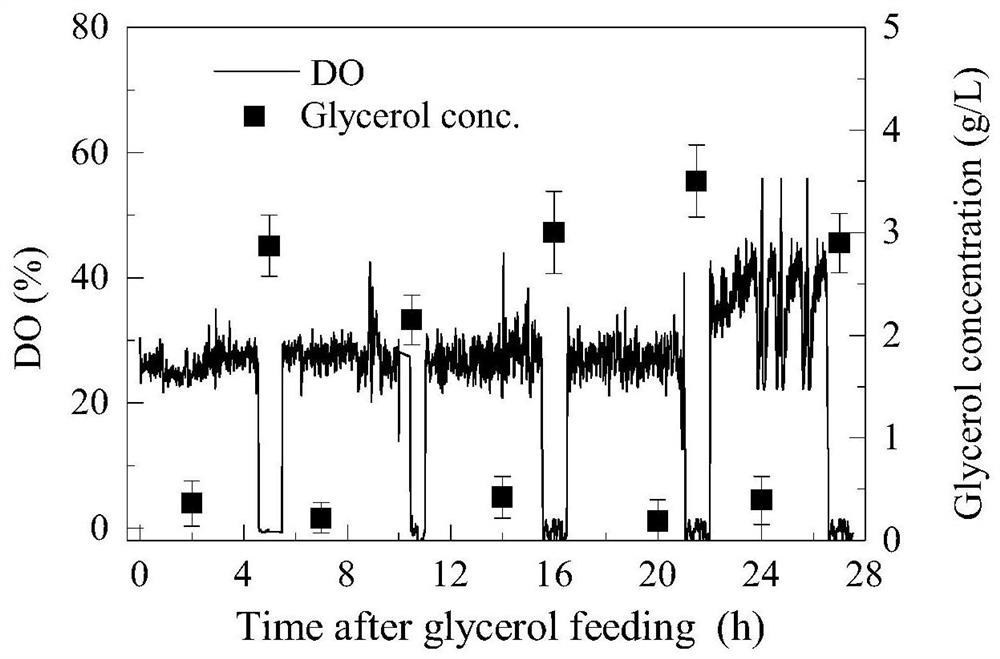
具体步骤如下:结合对比例1和对比例2的控制策略,间歇性控制甘油流加使细胞内ROS在“快速积累胁迫”(DO 20-40%,甘油浓度0-1g/L,4.5h)和“未积累胁迫”(DO~0%,甘油浓度2-5g/L,1h)之间循环5次(图5)。
上述实施例及对比例涉及的分析方法如下:
菌浓测定:参见参考文献:Yu RS,Dong SJ,Zhu YM,et al.Bioprocess BiosystEng,2010,33:473-483。
甘油浓度测定:参见参考文献:Bondioli P,Della Bella L.Eur J Lipid SciTechnol,2005,107:153-157。
离线甲醇浓度测定:参见参考文献:Gao MJ,Li Z,Yu RS,et al.BioprocessBiosyst Eng,2012,35:1125-1136。
胞内ROS浓度测定:参见参考文献:Li X,Hu HY,Zhang YP.Bioresour Technol,2011,102:3098-3102。
AOX、FLD、FDH比酶活性测定:参见参考文献:Gao MJ,Li Z,Yu RS,etal.Bioprocess Biosyst Eng,2012,35:1125-1136。
甲醇比消耗速率测定:参见参考文献:Jia LQ,Tu TY,Huai QQ,et al.PLoS ONE,2017,12:e0184602。
人源溶菌酶活性测定:参见参考文献:赵玉萍,张灏,杨严俊.食品科学,2002,23:116-119。
甘油流加阶段、不同生长环境下的细胞浓度和胞内ROS积累情况
利用重组毕赤酵母表达人源溶菌酶,在甘油流加阶段,甘油浓度与DO相耦合,难以同时处于最优水平。当处于对比例1(ROS积累胁迫)所述的细胞生长环境时,可将DO维持在20-40%,甘油浓度在整个甘油流加阶段都停留在0-1g/L的水平(图1)。甘油流加进行18h,ROS达到了162.95荧光强度/g-DCW的最高水平,此时细胞生长几乎停止(图2)。当处于对比例2(ROS未积累胁迫)的细胞生长环境时,基于离线测量的甘油浓度手动控制甘油流加速度,将甘油浓度控制在2-5g/L,DO在甘油流加开始后自然而然地降至~0%(图3)。此时,ROS浓度维持在零水平,而最终的细胞浓度仅为46.25g-DCW/L(图4)。当毕赤酵母处于高浓度的氧气环境中,虽然能获得一定密度的毕赤酵母细胞,但同时也会在细胞内积累大量的ROS,引起细胞结构和功能的损伤。虽然毕赤酵母处于低浓度的氧气环境中,可以有效抑制ROS的积累,但是太低的氧气浓度无法满足细胞的基本代谢需求。而采用本发明的实施例策略,当处于实施例所述的细胞生长环境时,发酵液中最终细胞浓度达到了143.02g-DCW/L的最高水平,ROS浓度处于48.39荧光强度/g-DCW的较低水平(图6)。
不同生长环境下维持细胞代谢所需甘油情况
为了维持细胞基本生长代谢需求,当细胞处于对比例1所述的ROS严重积累胁迫的细胞生长环境时,甘油流向细胞的维持系数处于0.0650 1/h的最高水平(图9);此时,在实施例所述的环境中,由于较低的ROS浓度水平,使得甘油流向细胞的维持系数处于较低的水平(0.0400 1/h)(图9)。
不同生长环境下的细胞表达人源溶菌酶情况
在甲醇诱导阶段,当采用相同的甲醇诱导策略时,细胞浓度在整个过程中都处于稳定水平(图10)。如图11和12所示,甘油流加阶段结束时高密度细胞的获得是甲醇诱导阶段人源溶菌酶高效表达的一个关键因素。当细胞处于实施例所述的生长环境时,细胞浓度达到了143.02g-DCW/L,甲醇诱导期最终hLYZ活性达到了2.45×10
不同生长环境下的细胞对甲醇环境的适应时间
当发酵阶段进入甲醇诱导阶段时,重组毕赤酵母需要很长一段时间去适应甲醇环境。一般而言,甲醇适应阶段的结束可以通过DO的下降和OUR的上升来直接反应。如图13所示,当细胞处于实施例所述的生长环境时,对于甲醇环境的适应时间约为3h,在相同的甲醇诱导条件下,仅为对比例1所需时间的一半。当细胞处于对比例2所述生长环境时,在整个诱导阶段内DO和OUR没有显著的下降和上升,导致人源溶菌酶表达的失败。
不同生长环境下的细胞甲醇代谢相关酶比活性及甲醇比消耗速率
重组毕赤酵母的甲醇代谢途径主要包括醇氧化酶(AOX)、甲醛脱氢酶(FLD)和甲酸脱氢酶(FDH)这三个关键酶。这三种酶在甲醇代谢过程中所起的作用如下:甲醇代谢的第一步反应(CH
综上,本发明在很大程度上抑制了胞内ROS的积累,强化了人源溶菌酶蛋白的表达。相较于传统的“ROS快速积累胁迫”的细胞生长环境,本发明的细胞生长环境可以:1)在甘油流加阶段结束后,细胞密度达到了143.02g-DCW/L的最高水平的同时、控制胞内ROS浓度在48.39荧光强度/g-DCW以下;2)毕赤酵母细胞对于甲醇诱导环境的适应时间缩短了一半;3)甲醇代谢途径中关键酶(AOX、FLD和FDH)的活性得到了大幅度地增强;4)在相同的甲醇诱导条件下,人源溶菌酶的活性达到了2.45×10
所属领域的普通技术人员应当理解:以上任何实施例的讨论仅为示例性的,并非旨在暗示本公开的范围(包括权利要求)被限于这些例子;在本发明的思路下,以上实施例或者不同实施例中的技术特征之间也可以进行组合,步骤可以以任意顺序实现,并存在如上所述的本发明的不同方面的许多其它变化,为了简明它们没有在细节中提供。
本发明的实施例旨在涵盖落入所附权利要求的宽泛范围之内的所有这样的替换、修改和变型。因此,凡在本发明的精神和原则之内,所做的任何省略、修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 一种强化毕赤酵母表达外源蛋白的方法
- 表达外源蛋白的毕赤酵母、其构建方法及其诱导表达方法
