一种检测HPV整合基因位点的引物组合及试剂盒
文献发布时间:2023-06-19 12:18:04
技术领域
本发明涉及生物检测技术领域,具体涉及一种检测HPV整合基因位点的引物组合及试剂盒。
背景技术
宫颈癌在全世界范围内每年有570,000新发病例,311,000死亡病例,其中我国每年有超过130,000的新发病例。高危型人乳头瘤病毒(HPV)的持续性感染被认为是宫颈癌的首要病因。随着高通量测序技术的不断发展,科学研究发现宫颈癌的发生是一个长期的过程,HPV基因组整合到宿主基因组上被认为是宫颈癌发生的一个关键步骤,由于HPV DNA整合后持续表达癌蛋白并使宿主基因组不稳定性增加,诱导正常宫颈上皮发展为癌前病变,最终致癌。目前,HPV基因组整合是宫颈上皮内瘤变向宫颈癌恶性转化的一个重要标志已得到一致认可,在HPV导致的良性病变中,细胞内的病毒DNA通常位于宿主基因组外,在高级别内瘤变和宫颈癌中,HPV和DNA通常以整合的形式存在于宿主细胞基因组中,且整合率随着宫颈病变的严重程度而显著增加;同时多项高通量测序研究发现,尽管在癌前病变和宫颈癌样本中都有HPV整合事件发生,但统计结果显示宫颈癌样本的HPV整合事件发生率(81%)明显高于CINs样本(48%),这表明HPV整合事件发生从癌前病变到癌变的过程是一个递增的过程。因此,HPV整合事件的检测可以作为宫颈病变发生风险的一个重要评估因素,对于HPV与人基因组整合位点可作为评估HPV阳性患者的宫颈癌发生风险的分子标记物。
基于HPV整合位点可以预测宫颈癌的风险评估,通过采用高通量测序法进行病毒整合检测,计算并绘制了HPV频繁整合位点图谱,确定了HPV阳性患者中LSIL、HSIL以及宫颈癌中HPV整合位点。选取其中位点作为预测宫颈癌发生风险的分子标记物,因此,本发明旨在于发现一种检测HPV整合基因位点的引物组合及试剂盒,用于评估HPV阳性患者的宫颈癌发生风险。
发明内容
针对现有技术存在的问题,本发明利用高通量测序法和荧光PCR法研究揭示了与宫颈癌发生相关的五个新的HPV整合位点(ARAP2、CASC21、CDH13、CNTN5、CNTNAP2),根据HPV整合至上述位点,来制备检测宫颈癌发生风险的试剂盒,具有快速、方便、准确等优点。
本发明解决上述技术问题的技术方案如下:
一种检测HPV整合基因位点的引物组合,所述引物组合包括SEQ ID NO:6至SEQ IDNO:15全部序列。
优选地,所述HPV整合基因位点分别为ARAP2、CASC21、CDH13、CNTN5、CNTNAP2。
上述这5种整合位点,是HPV16、18、56、66的部分或全部序列插入人基因组序列,形成整合的基因位点。
HPV的序列的网址如下:
HPV16的网址为https://www.ncbi.nlm.nih.gov/nuccore/NC_001526.2;
HPV18的网址为https://www.ncbi.nlm.nih.gov/nuccore/AY262282.1;
HPV56的网址为https://www.ncbi.nlm.nih.gov/nuccore/EF177176.1;
HPV66的网址为https://www.ncbi.nlm.nih.gov/nuccore/LC511686.1。
人染色体所对应的网址如下:
Chr4的网址为http://www.ncbi.nlm.nih.gov/nuccore/NC_000004.11;
Chr7的网址为http://www.ncbi.nlm.nih.gov/nuccore/NC_000007.13;
Chr8的网址为http://www.ncbi.nlm.nih.gov/nuccore/NC_000008.10;
Chr11的网址为http://www.ncbi.nlm.nih.gov/nuccore/NC_000011.9;
Chr16的网址为http://www.ncbi.nlm.nih.gov/nuccore/NC_000016.9。
表1为HPV的基因组序列在人基因组上整合的位点,其中第三列所示的“HPV断点”分别相应的插入第一列所示的“基因”的第二列所示的“人基因组上的断点”处,具体“基因”、“人基因组上的断点”、“HPV断点”如表1所示:
表1 HPV的基因组序列在人基因组上整合的位点
上表中以“Chr4:35694937”为例,表示HPV整合在人4号染色体35694937位点;以“HPV56:5500”为例,指整合在人基因组HPV的断点是第5500个碱基。
所述整合位点ARAP2的上、下游引物序列如SEQ ID NO:6和SEQ ID NO:7所示;
所述整合位点CASC21的上、下游引物序列如SEQ ID NO:8和SEQ ID NO:9所示;
所述整合位点CDH13的上、下游引物序列如SEQ ID NO:10和SEQ ID NO:11所示;
所述整合位点CNTN5的上、下游引物序列如SEQ ID NO:12和SEQ ID NO:13所示;
所述整合位点CNTNAP2的上、下游引物序列如SEQ ID NO:14和SEQ ID NO:15所示。
用于检测HPV整合位点的PCR扩增上、下游引物组合,具体见下表2所示。
表2用于检测HPV整合位点的PCR扩增上、下游引物组合
本领域技术人员可以根据表2的上、下游引物序列,进行适当的增加、减少或改变,例如增加不同的限制性酶切位点序列、保护碱基等,减少表2中引物序列的长度(删除部分碱基、只保留3’的部分或全部序列),对于个别碱基进行改变;上述操作只要不影响PCR扩增,均在本发明的保护范围内。
优选地,所述整合位点ARAP2的序列如SEQ ID NO:1所示;
所述整合位点CASC21的序列如SEQ ID NO:2所示;
所述整合位点CDH13的序列如SEQ ID NO:3所示;
所述整合位点CNTN5的序列如SEQ ID NO:4所示;
所述整合位点CNTNAP2的序列如SEQ ID NO:5所示。
HPV基因组插入人基因组后形成的整合位点的序列如下表3所示。
表3 HPV基因组插入人基因组后形成的整合序列
上表中整合序列指的是HPV部分或全部基因组序列融合后人染色体上得到的序列,即一部分是HPV的序列,一部分是人基因组序列。本领域技术人员可以根据表3中的整合序列,进行适当的增加、减少或改变,例如增加不同的限制性酶切位点序列、保护碱基等,减少表3的整合序列长度(如删除部分碱基),对于个别碱基进行改变;上述操作只要仍然保留了表3中整合序列的大部分碱基,均在本发明的保护范围内。
上述与宫颈癌发生相关的HPV整合位点以及在检测过程中所使用的引物和试剂可以组装成检测宫颈癌高危人群的试剂盒中,用于宫颈癌高危人群的检测。
一种检测HPV整合基因位点的试剂盒,包括所述引物组合,序列如SEQ ID NO:6至SEQ ID NO:15所示。
优选地,上述试剂盒中,还包含DNA提取试剂和PCR扩增用试剂。
优选地,上述试剂盒中,所述DNA提取试剂为:Buffer ACL、RNaseA、Proteinase K、Buffer ACL、Buffer WA、Buffer WB和Elution buffer,购自南京诺唯赞生物科技股份有限公司,货号为DC112。更具体的,所述DNA提取试剂可以购买商品化的DNA提取试剂盒,也可以参照精编分子生物学实验指南第五版(F.M.奥斯伯等著)中所述的DNA提取试剂或适当调整后来用于提取人宫颈脱落细胞DNA。
优选地,上述试剂盒中,所述PCR扩增试剂为:DNA聚合酶、与DNA聚合酶配套使用的缓冲液以及含镁离子的溶液、荧光染料和双蒸水。更具体的,所述荧光染料为SYBR Green。
优选地,上述试剂盒中,所述PCR扩增试剂为2×Taq Pro Universal SYBR qPCRMaster Mix,购自南京诺唯赞生物科技股份有限公司。
上述试剂盒的使用方法,包括以下步骤:
1)宫颈脱落细胞DNA提取,采集人宫颈脱落细胞作为样本并利用DNA提取试剂提取脱落细胞DNA;本发明对于人宫颈脱落细胞DNA提取方法并无特别限制,只需保证DNA浓度应大于15ng/μL,纯度A260/A280不低于1.5,A260/A230不低于1即可。
2)高通量测序法病毒整合检测:
①病毒整合检测:设计含有18种亚型的HPV全长探针(HPV16、HPV18、HPV26、HPV31、HPV33、HPV35、HPV39、HPV45、HPV51、HPV52、HPV53、HPV56、HPV58、HPV59、HPV66、HPV68、HPV73、HPV82)。根据Illumina的要求构建DNA的测序文库,采用酶切的方式将样品基因组DNA酶切为小片段,然后将这些小片段末端修复和加A处理;确保构建好的DNA文库总量应≥1500ng,且文库片段长度的主峰应约为350~550bp;根据液相探针杂交捕获技术,应用含有18种亚型的HPV探针,与基因组DNA文库在65℃杂交16~24h,捕获目标产物洗脱未杂交的DNA片段。获取的片段通过16轮PCR扩增,纯化再进行二次杂交捕获,获得的纯化后的扩增产物为测序文库,确保文库浓度应≥1ng/μL,且文库片段长度的主峰约为350~550bp;把测序文库加入到基因测序仪Nextseq CN500进行测序;
②病毒整合检测结果分析:对接头,低质量和重复序列进行过滤,并对过滤前后的序列质量进行评估。保证过滤后的序列Q30大于80%,且序列长度大于100bp。将经过预处理的测序数据,采用序列比对软件,将序列快速比对到HPV病毒和人类基因组参考序列上。基于比对结果,从中识别出嵌合体的序列(一条序列,部分比对上HPV基因组,部分比对上人类基因组)。针对这些嵌合序列,按照在人类基因组上的位置,进行局部的聚类,并将聚类的序列与参考基因组进行局部的比对,根据比对结果确定样品是否整合了HPV的部分序列,以及是否在基因ARAP2、CASC21、CDH13、CNTN5、CNTNAP2中整合了HPV部分序列。
3)荧光PCR法检测HPV整合位点:利用SEQ ID N0:6至SEQ ID NO:15所示序列对步骤2)获得的整合序列进行荧光PCR检测。
4)结果分析:步骤3)扩增为阳性,即检测到整合位点说明结果为阳性,即属于宫颈癌高危人群;否则,结果为阴性,即不属于宫颈癌高危人群。
本发明对于PCR扩增方法无特殊限制,试剂操作时可以根据PCR扩增试剂选择合适的扩增条件,只要能够保证扩增阳性即可,优先的所述PCR扩增方法为95℃30s,95℃7s,60℃20s,95℃15s,60℃60s,95℃15s,40个循环,可以根据实际条件对上述参数进行适当调整。
与现有技术相比,本发明的有益效果是:提供检测宫颈癌发生风险的试剂盒,具有快速、方便、准确、假阳性率低等优点;利用高通量测序法和荧光PCR法获得了与宫颈癌发生相关的HPV整合位点ARAP2、CASC21、CDH13、CNTN5、CNTNAP2,根据宫颈脱落细胞DNA中HPV整合至上述基因位点,可作为评估HPV阳性患者的宫颈癌发生风险的分子标记物;利用HPV整合来组装的试剂盒并应用于评估HPV感染阳性患者的宫颈癌发生风险评估,创新性好,对临床诊断有帮助。
附图说明
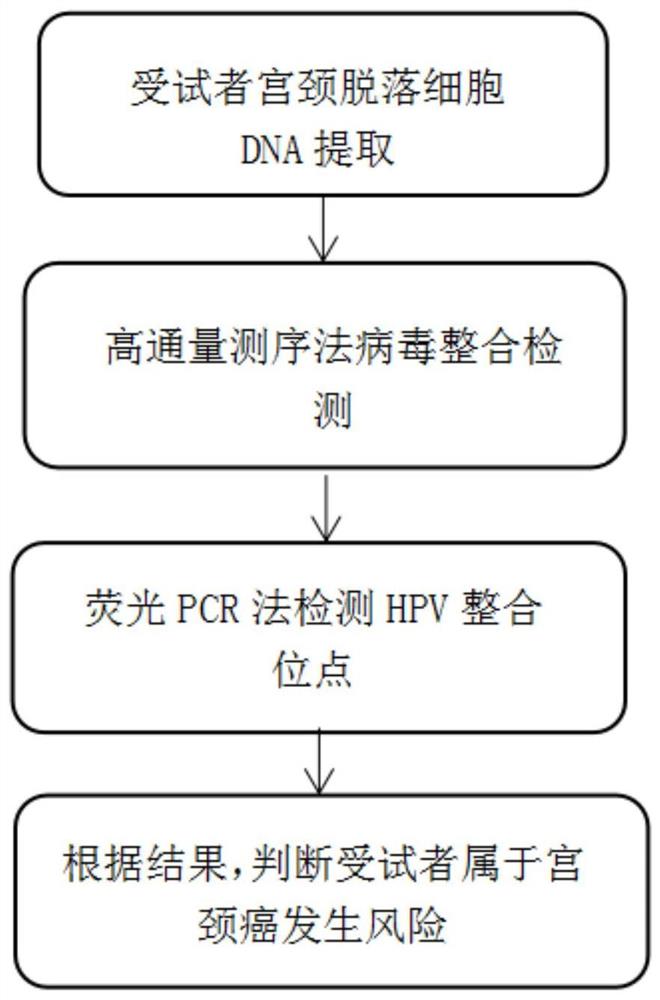
图1为本发明所述的检测宫颈癌高危人群试剂盒使用方法的流程图;
图2为LSIL、HSIL、宫颈癌样本中所有整合基因位点的HPV整合阳性率分布图;
图3为5个整合基因位点在所有样本中检测阳性率分布图,其中A表示5个基因位点检出阳性率。
具体实施方式
以下将结合附图对本发明各实施例的技术方案进行清楚、完整的描述,显然,所描述实施例仅仅是本发明的一部分实施例,而不是全部的实施例。基于本发明的实施例,本领域普通技术人员在没有做出创造性劳动的前提下所得到的所有其它实施例,都属于本发明所保护的范围。
实施例1
分别选择988例LSIL患者的宫颈脱落细胞、358例HSIL患者的宫颈脱落细胞、126例宫颈癌患者的宫颈脱落细胞作为样本。
本发明所述的LSIL指低度鳞状上皮内病变,HSIL指高度鳞状上皮内病变,为宫颈上皮内瘤变的不同的病理分期。
1)取宫颈脱落细胞样本离心5min收集细胞,弃上清液。依次加入200μl PBS、20μlProteinase K,振荡混匀。
2)加入200μl Buffer BCL,振荡混匀,56℃水浴10min,期间上下颠倒混匀数次,过柱子纯化。加入150μl无水乙醇,振荡混匀,短暂离心以收集管盖内壁上的液体。
3)将FastPure gDNA Mini ColumnsⅡ吸附柱置于2ml Collection Tubes收集管中,转移上述混合液(包括絮状沉淀)至吸附柱中。12,000rpm(13,400×g)离心1min。弃滤液,将吸附柱置于收集管中。沿管壁加入500μl Buffer WA至吸附柱,12,000rpm(13,400×g)离心1min。
4)弃滤液,将吸附柱置于收集管中。沿管壁加入600μl Buffer WB,12,000rpm(13,400×g)离心1min,弃滤液。
5)重复步骤4。
6)将吸附柱置于收集管中。12,000rpm(13,400×g)空柱离心2min。
7)将吸附柱转移至新的1.5ml离心管中。向吸附柱膜中央滴加50-200μl ElutionBuffer,室温放置2-5min。12,000rpm(13,400×g)离心1min。
8)弃吸附柱,DNA产物于-20℃保存备用。
实施例2
利用高通量测序法检测宫颈组织基因组DNA中HPV的整合位点。
1)宫颈脱落细胞的基因组DNA样品的病毒整合检测:设计含有18种亚型的HPV全长探针(HPV16、HPV18、HPV26、HPV31、HPV33、HPV35、HPV39、HPV45、HPV51、HPV52、HPV53、HPV56、HPV58、HPV59、HPV66、HPV68、HPV73、HPV82,探针的序列详细内容参见本申请人已申报的专利CN202011260519.5一种用于人乳头瘤病毒HPV分型和整合检测的探针组及其试剂盒。根据Illumina的要求构建DNA的测序文库,采用酶切的方式将样品基因组DNA酶切为小片段,然后将这些小片段末端修复和加A处理;确保构建好的DNA文库总量应≥1500ng,且文库片段长度的主峰应约为350~550bp;根据液相探针杂交捕获技术,应用含有18种亚型的HPV探针,与基因组DNA文库在65℃杂交16~24h,捕获目标产物洗脱未杂交的DNA片段。获取的片段通过16轮PCR扩增,纯化再进行二次杂交捕获,获得的纯化后的扩增产物为测序文库,确保文库浓度应≥1ng/μL,且文库片段长度的主峰约为350~550bp。把测序文库加入到基因测序仪Nextseq CN500进行测序;
2)病毒整合检测结果分析:首先,去除质量低、重复和接头引物污染的序列,剩余的序列同时向人基因组(NCBI build 37,HG19)和HPV基因组(HPV16:NC_001526.2,HPV18:AY262282.1,HPV26:NC_001583.1,HPV31:HQ537666.1,HPV33:HQ537688.1,HPV35:HQ537708.1,HPV39:M62849.1 HPV45:EF202156,HPV51:KF436882.1,HPV52:GQ472848.1,HPV53:NC_001593.1,HPV56:EF177176.1,HPV58:HQ537777.1,HPV59:EU918767.1,HPV66:LR862085.1,HPV68:EU918769.1,HPV73:LR862011.1,HPV82:LR862056.1)比对。
其次,去除完全比对到人基因组或HPV病毒基因组的序列,只保留同时部分比对到人和部分比对到HPV基因组的嵌合序列。把嵌合序列进行末端配对的组装确定准确的整合位点。应用BWA v0.7.17、Samtools v1.9和Picard v2.20.6软件再次比对末端配对组装后的序列,在人基因组DNA和HPV基因组DNA的序列的连接处即为HPV的整合位点。根据比对结果可以确定样品是否有整合,以及是否有ARAP2、CASC21、CDH13、CNTN5、CNTNAP2基因位点中的整合。
实施例3
利用荧光PCR法检测HPV整合位点。
1.荧光PCR扩增
设计能扩增HPV整合位点的上下游引物,引物如表2所示,按表4体系配制:
表4引物体系
每管分别混匀,放到标准的PCR仪扩增并使用表5程序:
表5 PCR扩增程序
2.结果分析:若扩增为阳性,即检测到整合位点,即HPV整合到ARAP2、CASC21、CDH13、CNTN5、CNTNAP2中任一基因位点,则可判断宫颈癌高危人群;否则,结果为阴性,即不属于宫颈癌高危人群。
实施例4
将来自HPV感染的LSIL、HSIL、宫颈癌样本按照实施例1所述的方法提取基因组DNA,按照实施例2所述的方法利用高通量测序法检测宫颈组织基因组DNA中HPV的整合位点,经过结果分析后获得了所有整合的基因位点,经统计获得整合位点。
实验结果分析
图1为本发明所述检测宫颈癌高危人群试剂盒使用方法的流程图。本发明所述的检测宫颈癌高危人群试剂盒使用方法包括以下步骤:提取受试者宫颈脱落细胞基因组DNA,通过高通量测序法病毒整合检测和荧光PCR检测出HPV整合位点,通过检测结果作出受试者判断HPV阳性患者宫颈癌发生风险评估。
图2不同病理分期样本所有整合基因位点的HPV整合阳性率分析结果。本发明所述的“所有整合基因位点”指发明人利用实施例1和实施例2所述的方法对宫颈脱落细胞DNA进行检测的过程中发现的所有的HPV整合的基因位点,大部分出现频率都比较低。本发明所述的ARAP2、CASC21、CDH13、CNTN5、CNTNAP2整合位点出现的频率较高。该样本分为LSIL、HSIL、宫颈癌样本,所述整合阳性即检测到同时部分含有人基因组序列和部分含有HPV基因组序列。所述整合阳性率的计算方法,分母是某一病理分期检测的总病人数,分子是这一病理分期病人中检测出整合阳性的病人数。在统计的896例LSIL样本、339例HSIL样本和114例宫颈癌样本中,检测出的所有HPV整合阳性率表现为从LSIL的HPV整合阳性率为61.27%到HSIL的68.14%、再到宫颈癌的HPV整合阳性率为92.98%,呈现出一个不断上升的趋势,上述结果说明了说明HPV整合阳性率和宫颈病变恶性化程度密切相关,宫颈病变恶性化程度越高,HPV整合阳性率越高,因此HPV整合可以作为评价宫颈病变恶性化程度,预测宫颈癌风险的一个指标。
图3为荧光PCR法检测所有样本中基因位点的HPV整合阳性率图,本发明所述的五个整合基因位点ARAP2、CASC21、CDH13、CNTN5、CNTNAP2。在1472例样本中,5个基因位点检出阳性率6.13%,上述结果说明基因位点检出阳性率较高,该基因位点整合可以作为评价宫颈病变恶性化程度,预测宫颈癌风险的一个指标。
以上所述,仅为本发明的具体实施方式,但本发明的保护范围并不局限于此,任何属于本技术领域的技术人员在本发明揭露的技术范围内,可轻易想到的变化或替换,都应涵盖在本发明的保护范围之内。因此,本发明的保护范围应该以权利要求的保护范围为准。
序列表
<110> 武汉凯德维斯生物技术有限公司
<120> 一种检测HPV整合基因位点的引物组合及试剂盒
<160> 15
<170> SIPOSequenceListing 1.0
<210> 1
<211> 166
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 1
gtggaaggct ttataggtaa gtgtgcagaa ggtgtagcaa ctgactggct agacaaacca 60
ggtgcttcat catctatatt tgcataaata tcatataggc catcaaatgc cttgagaaca 120
tcttggcaag tgaaaagagc cactcttttt tttttttttt ttttga 166
<210> 2
<211> 340
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 2
cctgcctcgg ccttccaaag tgctaggatt ataggcatga gccaccatgc cctgcctgac 60
aaatcttgag tcagatatta gtaaatgcaa acattacaca tacatacagt catacaacac 120
agacaacaaa tacacacata cagtacacac aataaataaa tagtacataa tacaaccata 180
catatacaat acagacacac aacatactat ttgcgtttgc gcttggagga gggggctgag 240
gtagatgtag taggagcaga gcgtttctta gaggatacag gaggtttagt acggacccca 300
acctgcatta aaaacttcct gccaagaggg aactgatcca 340
<210> 3
<211> 150
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 3
gttttcgtaa catgtaataa ctaggatgta aataaaagtc acctgcatca gcaataattg 60
tatattgtgg agaccctgga actataggaa gtaatgaagg agcttggtca gttatattaa 120
tgggtatatc aggacctgat actaaaggaa 150
<210> 4
<211> 899
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 4
tgggactaca ggcgcccgcc accgcgcccg gctaattttt tgtattttta gtagagacgg 60
ggtttcacct tgttagccag gatggtctcg atctcctgac ctcatgatcc acccgcctcg 120
gcctcccaga gtgctgggat tacaggcgtg agccaccgcg cccggccctc gccaactttt 180
aatttttaaa agttatttaa aacaaaaaga cccagctagt atcactattc taaaagagaa 240
agtttacaga aatacacaca cacacataca cgcgtgcgca catgctaaaa agagcaggcg 300
ctgagctctg agttaaggtt aactttatga tatcattaca ttgtcctgct tactcttcca 360
tttcaccaag gcccagtgaa aactttctca ctaaccagca ccaatccaca gctacagata 420
cacttgctcc tgtaagaccc cctttaacag tagatcctgt gggcccttct gatccttcta 480
tagtttcttt agtggaagaa actagtttta ttgatgctgg tgcaccaaca tctgtacctt 540
ccattccccc agatgtatca ggatttagta ttactacttc aactgatacc acacctgcta 600
tattagatat taataatact gttactactg ttactacaca taataatccc actttcactg 660
acccatctgt attgcagcct ccaacacctg cagaaactgg agggcatttt acactttcat 720
catccactat tagtacacat aattatgaag aaattcctat ggatacattt attgttagca 780
caaaccctaa cacagtaact agtagcacac ccataccagg gtctcgccca gtggcacgcc 840
taggattata tagtcgcaca acacaacaag ttaaagttgt agaccctgct tttgtaacc 899
<210> 5
<211> 150
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 5
ataacgatta tttttaaaaa tattcagaat taggtgttgg atagtaagct gacccaacca 60
aataaatatg tttctggctt tgaaatttgg tttgtctagc cagtcagttg ctacaccttc 120
tgcacactta cctataaagc cttccacatt 150
<210> 6
<211> 21
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 6
agtgtgcaga aggtgtagca a 21
<210> 7
<211> 20
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 7
tgccaagatg ttctcaaggc 20
<210> 8
<211> 21
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 8
tatttgcgtt tgcgcttgga g 21
<210> 9
<211> 20
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 9
gcaggttggg gtccgtacta 20
<210> 10
<211> 21
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 10
aaagtcacct gcatcagcaa t 21
<210> 11
<211> 22
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 11
accaagctcc ttcattactt cc 22
<210> 12
<211> 20
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 12
gtgggccctt ctgatccttc 20
<210> 13
<211> 20
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 13
ccctggtatg ggtgtgctac 20
<210> 14
<211> 22
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 14
ggatagtaag ctgacccaac ca 22
<210> 15
<211> 20
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 15
aggtgtagca actgactggc 20
- 一种检测HPV整合基因位点的引物组合及试剂盒
- 一种用于荧光定量PCR检测15型HPV的特异性引物和探针的组合以及试剂盒
