兰索拉唑肠溶微丸及其制备方法
文献发布时间:2023-06-19 19:27:02
技术领域
本发明属于药物制剂技术领域,特别涉及一种快速释放的兰索拉唑肠溶微丸及其制备方法。
背景技术
兰索拉唑是第二代质子泵抑制类抗溃疡药,主要用于治疗胃溃疡、十二指肠溃疡、反流性食管炎、Zollinger-Ellison综合征(胃泌素瘤)等,可广泛用于治疗与胃酸分泌有关的各种消化功能紊乱性疾病。化学名称为∶2-[[[3-甲基-4-(2,2,2-三氟乙氧基)-2-吡啶基]甲基]-亚磺酰基]-1H-苯并咪唑;其结构式为:
兰索拉唑于1991年由日本武田公司研制开发成功,主要剂型有肠溶胶囊、片剂和注射剂,兰索拉唑肠溶胶囊以商品名为“Takepron”在日本上市。在我国上市的品种有兰索拉唑肠溶胶囊、兰索拉唑口崩片和注射用兰索拉唑。武田中国分公司上市生产的兰索拉唑肠溶胶囊商品名为“达克普隆”。
兰索拉唑在酸性条件下不稳定,在胃酸中容易被破坏,现有技术制备的兰索拉唑肠溶微丸,其肠溶层在胃液中至少保持2小时把酸液隔离在药丸外;以免被酸破坏,而当到达小肠时其肠溶层逐渐化开,之后隔离层、药芯逐个溶解释放。整个过程缓慢,10分钟药物释放50%以下。需要发现新的兰索拉唑肠溶微丸制备技术,以使兰索拉唑在肠液中能够快速释放。
发明内容
本发明的目的之一在于提供一种快速释放的兰索拉唑肠溶微丸。
本发明的目的之二在于提供一种上述快速释放的兰索拉唑肠溶微丸的制备方法,以使兰索拉唑在肠液中能够快逮释放,缩短药物起效时间,大幅度提高了生物利用度。
根据本发明的一个方面,提供一种快速释放的兰索拉唑肠溶微丸,其包括载药层、隔离层和肠溶层,所述载药层,以重量份计,包括:
空白丸芯90~210份,
兰索拉唑15~30份,
崩解剂A 1~3份,
十二烷基硫酸钠0.4~2.4份,
填充剂0~10份,
碱保护剂5~15份,
粘合剂A 1~4份,
10%~50%乙醇水溶液 100~250份。
其中,将所述兰索拉唑、崩解剂A、十二烷基硫酸钠、填充剂、碱保护剂、粘合剂A与10%~50%乙醇水溶液制成混悬液,采用流化床底喷包衣技术喷至空白丸芯上制成载药层。
进一步地,所述空白丸芯选自蔗糖丸芯、淀粉蔗糖丸芯的至少一种,粒径优选为0.71~0.9mm。
进一步地,所述崩解剂A为水溶性的崩解剂,优选为羧甲淀粉钠、大豆多糖中的至少一种。
进一步地,所述填充剂选自甘露醇、蔗糖中的至少一种。
进一步地,所述碱保护剂选自碳酸镁、碳酸氢钠中的至少一种。
进一步地,所述粘合剂A选自羟丙甲纤维素、羟丙纤维素中的至少一种。
进一步地,所述隔离层,以所述载药层组成的含活性成分的微丸芯200份为基准,以重量份计,包括:
崩解剂B 1~3份,
粘合剂B 3~6份,
碳酸镁15~21份,
纯化水120~200份。
其中,将所述崩解剂B、粘合剂B、碳酸镁与纯化水制成混悬液,采用流化床底喷包衣技术喷至所述载药层组成的含活性成分的微丸芯上制成隔离层。
进一步地,所述崩解剂B为水溶性的崩解剂,优选为羧甲淀粉钠、大豆多糖中的至少一种。
进一步地,所述粘合剂B选自羟丙甲纤维素、羟丙纤维素中的至少一种。
进一步地,所述肠溶层,以包覆隔离层的微丸200份为基准,以重量份计,包括:
甲基丙烯酸和丙烯酸乙酯水分散体125~150份,
聚乙二醇3~4.5份,
滑石粉18~22.5份,
纯化水180~230份。
根据本发明的另一个方面,提供一种快速释放的兰索拉唑肠溶微丸的制备方法,所述兰索拉唑肠溶微丸包括载药层、隔离层和肠溶层,其中,所述载药层的制备方法包括以下步骤:
将粘合剂A和崩解剂A加入10%~50%乙醇水溶液中,搅拌溶解;
加入碱保护剂、十二烷基硫酸钠,可选地加入填充剂,搅拌均匀,加入兰索拉唑,搅拌均匀,得包衣液1;
将包衣液1采用流化床底喷包衣技术喷至空白丸芯上,形成含活性成分的微丸芯。
进一步地,在载药层的制备时,所述流化床底喷包衣的操作参数为:物料温度:35~50℃;进风温度:60~90℃;喷液速度:8~40rpm;喷枪压力:1.5~2.5bar;风量:60~100m³/h。
进一步地,所述隔离层的制备方法包括以下步骤:
将粘合剂B、崩解剂B加入纯化水中,搅拌溶解,再加入碳酸镁,搅拌均匀,得包衣液2;
将包衣液2采用流化床底喷包衣技术喷至所述含活性成分的微丸芯上,形成包覆隔离层的微丸。
进一步地,所述包覆隔离层的微丸相对于含活性成分的微丸芯,增重约为9%~15%。
进一步地,在所述隔离层的制备时,所述流化床底喷包衣的操作参数为:物料温度:35~50℃;进风温度:60~90℃;喷液速度:8~20rpm;喷枪压力:1.5~2.5bar;风量:60~100m³/h。
进一步地,所述肠溶层的制备方法包括以下步骤:
将甲基丙烯酸和丙烯酸乙酯水分散体、聚乙二醇、滑石粉加入中纯化水中,分散均匀,得包衣液3;
将包衣液3采用流化床底喷包衣技术喷至所述包覆隔离层的微丸上,形成所述兰索拉唑肠溶微丸。
进一步地,所述兰索拉唑肠溶微丸相对于包覆隔离层的微丸,增重约为29%~36%。
进一步地,在所述肠溶层的制备时,所述流化床底喷包衣的操作参数为:物料温度:25~35℃;进风温度:30~50℃;喷液速度:8~22rpm;喷枪压力:1.5~2.5bar;风量:60~100m³/h。
本发明的有益效果:
原研是采用离心式粉末层积上药制备兰索拉唑肠溶微丸,其对设备要求高,因国内离心造粒机容积较小,干燥效率低,气流难以控制,粉末进料系统技术不成熟,导致离心造粒法的应用受限。本发明开发了一种新的兰索拉唑微丸制剂的制备方法,首次将水溶性崩解剂溶于水或低浓度乙醇水溶液,采用流化床底喷包衣技术进行上药、包衣,首次将崩解剂以溶液的形式在流化床底喷包衣技术中进行上粉。与流化床法不加崩解剂相比,解决了难溶性药物微丸制剂溶出迟缓,溶出度偏低的问题。
本发明开发了一种新的适合难溶性药物制备成微丸的制备方法,解决了难溶性药物制备成微丸时对离心造粒设备的依赖问题,有效提高了微丸制备的生产效率,缩短了生产周期,降低了生产成本,并且可以满足小颗粒的包衣需求。
附图说明
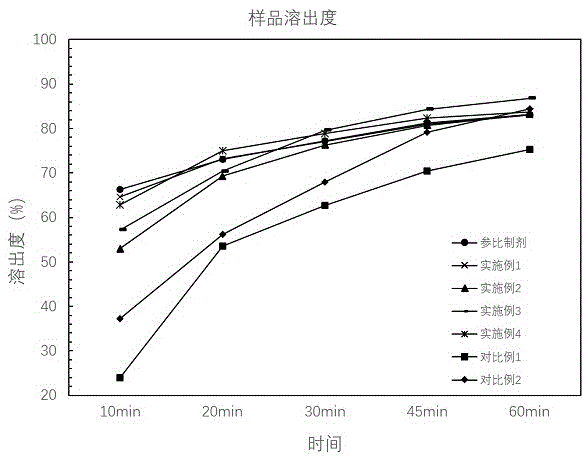
图1是实施例1~4和对比例1~2制备的肠溶微丸的溶出度对比图。
具体实施方式
下面通过具体实施例对本申请作进一步详细说明。
本发明的快速释放的兰索拉唑肠溶微丸,包括载药层、隔离层和肠溶层,其中,载药层,以重量份计,包括:
空白丸芯90~210份,
兰索拉唑15~30份,
崩解剂A 1~3份,
十二烷基硫酸钠0.4~2.4份,
填充剂0~10份,
碱保护剂5~15份,
粘合剂A 1~4份,
10%~50%乙醇水溶液 100~250份。
空白丸芯选自蔗糖丸芯或淀粉蔗糖丸芯的至少一种,粒径优选为0.71~0.9mm。
崩解剂A为水溶性的崩解剂,优选为羧甲淀粉钠、大豆多糖中的至少一种。检索到的公开文献中,仅离心式粉末层积法制备微丸会加入崩解剂,崩解剂以粉末形式上药。现有技术中没有将崩解剂溶解后再上药制备肠溶微丸的先例,普遍认为崩解剂吸收足够多的水后,完全溶胀,干燥之后将会丧失崩解性能。本发明首次将水溶性崩解剂溶于低浓度乙醇水溶液,采用流化床底喷包衣技术进行上药,使载药层中含有崩解剂,将水溶性崩解剂溶于水溶液,采用流化床底喷包衣技术进行隔离层包衣,使隔离层中含有崩解剂,解决了难溶性药物微丸制剂溶出迟缓,溶出度偏低的问题,克服了崩解剂吸水溶胀后再干燥将会丧失崩解性能的技术偏见。
填充剂选自甘露醇或蔗糖中的至少一种。本发明中,填充剂是非必要成分。加入一定量的填充剂,有利于提高上粉率。
碱保护剂优选为碳酸镁、碳酸氢钠中的至少一种;粘合剂A选自羟丙甲纤维素、羟丙纤维素中的至少一种。乙醇水溶液的作用是对原料药进行润湿和混悬,同时也是消泡剂,浓度为10~50%,优选为20~40%,其浓度过低,消泡效果较差,浓度过高,崩解剂的溶解性变差,上粉率降低。
其中,隔离层,以上述载药层组成的含活性成分的微丸芯200份为基准,以重量份计,包括:
崩解剂B 1~3份,
粘合剂B 3~6份,
碳酸镁15~21份,
纯化水120~200份。
载药层组成的含活性成分的微丸芯的粒径优选为0.75~0.95mm。
崩解剂B选自羧甲淀粉钠、大豆多糖中的至少一种。水溶性崩解剂溶于纯化水中,采用流化床底喷包衣技术进行上药,隔离层和载药层中均含有崩解剂,进一步解决了难溶性药物微丸制剂溶出迟缓,溶出度偏低的问题。粘合剂B选自羟丙甲纤维素、羟丙纤维素中的至少一种。
其中,肠溶层,以上述包覆隔离层的微丸200份为基准,以重量份计,包括:
甲基丙烯酸和丙烯酸乙酯水分散体125~150份,
聚乙二醇3~4.5份,
滑石粉18~22.5份,
纯化水180~230份。
包覆隔离层的微丸的粒径优选为0.8~1.0mm。
本发明的快速释放的兰索拉唑肠溶微丸的制备方法,其中,载药层的制备方法包括以下步骤:
将粘合剂A和崩解剂A加入10%~50%乙醇水溶液中,搅拌溶解;
加入碱保护剂、十二烷基硫酸钠,可选地加入填充剂,搅拌均匀,加入兰索拉唑,搅拌均匀,得包衣液1;兰索拉唑预先进行微粉化。
将包衣液1采用流化床底喷包衣技术喷至空白丸芯上,形成含活性成分兰索拉唑的微丸芯。含活性成分兰索拉唑的微丸芯相对于空白丸芯增重约为23%~28%。
现有技术中微丸制剂如需要添加崩解剂提高溶出速率主要采用以下两种方法:1、采用挤出制粒将崩解剂粉末内加制备成含药丸芯;2、采用离心造粒法一边加入液体粘合剂一边喷洒药粉,将崩解剂以粉末的形式层积在微丸上面。原研即是采用离心式粉末层积上药制备兰索拉唑肠溶微丸,其对设备要求高,因国内离心造粒机容积较小,干燥效率低,气流难以控制,粉末进料系统技术不成熟,导致离心造粒法的应用受限。现有的流化床法混悬上药制备肠溶微丸制剂尚无使用崩解剂的先例。这是因为崩解剂大多都具有较强的吸水性和膨胀性,不适合溶解或分散在水或其他溶剂中应用。
本发明开发了一种新的兰索拉唑微丸制剂的制备方法,首次将水溶性崩解剂溶于水或低浓度乙醇水溶液,采用流化床底喷包衣技术进行上药、包衣,首次将崩解剂以溶液的形式在流化床底喷包衣技术中进行上粉。与流化床法不加崩解剂相比,解决了难溶性药物微丸制剂溶出迟缓,溶出度偏低的问题。
制备载药层时,流化床底喷包衣操作参数为:物料温度:35~50℃;进风温度:60~90℃;喷液速度:8~40rpm;喷枪压力:1.5~2.5bar;风量:60~100m³/h。
其中,隔离层的制备方法包括以下步骤:
将粘合剂B、崩解剂B加入纯化水中,搅拌溶解,再加入碳酸镁,搅拌均匀,得包衣液2;
将包衣液2采用流化床底喷包衣技术喷至所述含活性成分的微丸芯上,形成包覆隔离层的微丸。包覆隔离层的微丸相对于含活性成分的微丸芯,增重约为9%~15%。隔离层用于将原料药兰索拉唑与酸性肠溶材料隔离,该增重量可以满足将酸性肠溶材料与原料药(遇酸不稳定)隔离的效果,增重太低隔离效果不好,增重太大溶出速率会下降,同时生产成本会增加。
制备隔离层时,流化床底喷包衣的操作参数为:物料温度:35~50℃;进风温度:60~90℃;喷液速度:8~20rpm;喷枪压力:1.5~2.5bar;风量:60~100m³/h。
其中,肠溶层的制备方法包括以下步骤:
将甲基丙烯酸和丙烯酸乙酯水分散体、聚乙二醇、滑石粉加入中纯化水中,分散均匀,得包衣液3;
将包衣液3采用流化床底喷包衣技术喷至所述包覆隔离层的微丸上,形成兰索拉唑肠溶微丸,兰索拉唑肠溶微丸相对于包覆隔离层的微丸,增重约为29%~36%。肠溶层增重主要是从耐酸和溶出速率考虑,增重过小耐酸能力差,增重过大溶出会延迟。
制备肠溶层时,流化床底喷包衣的操作参数为:物料温度:25~35℃;进风温度:30~50℃;喷液速度:8~22rpm;喷枪压力:1.5~2.5bar;风量:60~100m³/h。
以下实施例仅对本申请进行进一步说明,不应理解为对本申请的限制。本发明所用的试剂和原辅料均市售可得。
实施例1
(1)制备含兰索拉唑的微丸芯,处方如下:
。
载药层的制备方法为:
将羟丙甲纤维素、羧甲淀粉钠加入30%乙醇溶液中,搅拌溶解,再依次加入甘露醇、碳酸镁、十二烷基硫酸钠,搅拌均匀,加入兰索拉唑,搅拌30~60分钟,得包衣液1。
将包衣液1采用流化床底喷包衣技术喷至淀粉蔗糖丸芯上,形成含活性成分兰索拉唑的微丸芯。
流化床底喷包衣的主要操作参数为:物料温度:35~50℃;进风温度:60~90℃;喷液速度:8~40rpm;喷枪压力:1.5~2.5bar;风量:60~100m³/h。
制得白色小丸即含活性成分兰索拉唑的微丸芯226.4g,微丸芯增重25.8%,收率为97.8%。
(2)制备包覆隔离层的微丸
取步骤(1)制备的含兰索拉唑的微丸芯200g,隔离层的处方如下:
。
隔离层的制备方法为:
将羟丙甲纤维素E5、羧甲淀粉钠加入纯化水中,搅拌溶解,再加入碳酸镁,搅拌均匀,得包衣液2;
将包衣液2采用流化床底喷包衣技术喷至含兰索拉唑的微丸芯上,形成包覆隔离层的微丸。
流化床底喷包衣的操作参数为:物料温度:35~50℃;进风温度:60~90℃;喷液速度:8~20rpm;喷枪压力:1.5~2.5bar;风量:60~100m³/h。
制得白色小丸即包覆隔离层的微丸221.8g,微丸增重为10.9%,收率为98.7%。
(3)制备兰索拉唑肠溶微丸
取步骤(2)制备的包覆隔离层的微丸200g,肠溶层的处方如下:
。
肠溶层的制备方法为:
将甲基丙烯酸和丙烯酸乙酯水分散体、聚乙二醇、滑石粉加入中纯化水中,分散均匀,得包衣液3;
将包衣液3采用流化床底喷包衣技术喷至所述包覆隔离层的微丸上,形成兰索拉唑肠溶微丸。
流化床底喷包衣的操作参数为:物料温度:25~35℃;进风温度:30~50℃;喷液速度:8~22rpm;喷枪压力:1.5~2.5bar;风量:60~100m³/h。
制得白色小丸即兰索拉唑肠溶微丸263.2g,微丸芯增重31.6%,收率为99.7%。
实施例2
(1)制备含兰索拉唑的微丸芯,处方如下:
。
载药层的制备方法为:
将羟丙甲纤维素、羧甲淀粉钠加入50%乙醇溶液中,搅拌溶解,再依次加入碳酸镁、十二烷基硫酸钠,搅拌均匀,加入兰索拉唑,搅拌30~60分钟,得包衣液1。
将包衣液1采用流化床底喷包衣技术喷至淀粉蔗糖丸芯上,形成含活性成分兰索拉唑的微丸芯。
流化床底喷包衣的主要操作参数为:物料温度:35~50℃;进风温度:60~90℃;喷液速度:8~40rpm;喷枪压力:1.5~2.5bar;风量:60~100m³/h。
制得白色小丸即含活性成分兰索拉唑的微丸芯111.9g,微丸芯增重24.3%,收率为99.6%。
(2)制备包覆隔离层的微丸
取步骤(1)制备的含兰索拉唑的微丸芯200g,隔离层的处方如下:
。
隔离层的制备方法为:
将羟丙甲纤维素E5、羧甲淀粉钠加入纯化水中,搅拌溶解,再加入碳酸镁,搅拌均匀,得包衣液2;
将包衣液2采用流化床底喷包衣技术喷至含活性成分兰索拉唑的微丸芯上,形成包覆隔离层的微丸。
流化床底喷包衣的操作参数为:物料温度:35~50℃;进风温度:60~90℃;喷液速度:8~20rpm;喷枪压力:1.5~2.5bar;风量:60~100m³/h。
制得白色小丸即包覆隔离层的微丸222.3g,微丸增重为11.15%,收率为98.8%。
(3)制备兰索拉唑肠溶微丸
取步骤(2)制备的包覆隔离层的微丸200g,肠溶层的处方如下:
。
肠溶层的制备方法为:
将甲基丙烯酸和丙烯酸乙酯水分散体、聚乙二醇、滑石粉加入中纯化水中,分散均匀,得包衣液3;
将包衣液3采用流化床底喷包衣技术喷至所述包覆隔离层的微丸上,形成兰索拉唑肠溶微丸。
流化床底喷包衣的操作参数为:物料温度:25~35℃;进风温度:30~50℃;喷液速度:8~22rpm;喷枪压力:1.5~2.5bar;风量:60~100m³/h。
制得白色小丸即兰索拉唑肠溶微丸258.2g,微丸增重为29.1%,收率为99.9%。
实施例3
(1)制备含兰索拉唑的微丸芯,处方如下:
。
载药层的制备方法为:
将羟丙纤维素、大豆多糖加入10%乙醇溶液中,搅拌溶解,再依次加入甘露醇、碳酸氢钠、十二烷基硫酸钠,搅拌均匀,加入兰索拉唑,搅拌30~60分钟,得包衣液1。
将包衣液1采用流化床底喷包衣技术喷至淀粉蔗糖丸芯上,形成含活性成分兰索拉唑的微丸芯。
流化床底喷包衣的主要操作参数为:物料温度:35~50℃;进风温度:60~90℃;喷液速度:8~40rpm;喷枪压力:1.5~2.5bar;风量:60~100m³/h。
制得白色小丸即含活性成分兰索拉唑的微丸芯259.7g,增重为23.7%,收率为99.3%。
(2)制备包覆隔离层的微丸
取步骤(1)制备的含活性成分兰索拉唑的微丸芯200g,隔离层的处方如下:
。
隔离层的制备方法为:
将羟丙纤维素、大豆多糖加入纯化水中,搅拌溶解,再加入碳酸镁,搅拌均匀,得包衣液2;
将包衣液2采用流化床底喷包衣技术喷至含活性成分兰索拉唑的微丸芯上,形成包覆隔离层的微丸。
流化床底喷包衣的操作参数为:物料温度:35~50℃;进风温度:60~90℃;喷液速度:8~20rpm;喷枪压力:1.5~2.5bar;风量:60~100m³/h。
制得白色小丸即包覆隔离层的微丸222.0g,增重为11.0%,收率为99.1%。
(3)制备兰索拉唑肠溶微丸
取步骤(2)制备的包覆隔离层的微丸200g,肠溶层的处方如下:
。
肠溶层的制备方法为:
将甲基丙烯酸和丙烯酸乙酯水分散体、聚乙二醇、滑石粉加入中纯化水中,分散均匀,得包衣液3;
将包衣液3采用流化床底喷包衣技术喷至所述包覆隔离层的微丸上,形成兰索拉唑肠溶微丸。
流化床底喷包衣的操作参数为:物料温度:25~35℃;进风温度:30~50℃;喷液速度:8~22rpm;喷枪压力:1.5~2.5bar;风量:60~100m³/h。
制得白色小丸即兰索拉唑肠溶微丸269.8g,增重为34.9%,收率为99.2%。
实施例4
(1)制备含兰索拉唑的微丸芯,处方如下:
。
载药层的制备方法为:
将羟丙甲纤维素、羧甲淀粉钠加入30%乙醇溶液中,搅拌溶解,再依次加入甘露醇、碳酸氢钠、碳酸镁、十二烷基硫酸钠,搅拌均匀,加入兰索拉唑,搅拌30-60分钟,得包衣液1。
将包衣液1采用流化床底喷包衣技术喷至淀粉蔗糖丸芯上,形成含活性成分兰索拉唑的微丸芯。
流化床底喷包衣的主要操作参数为:物料温度:35~50℃;进风温度:60~90℃;喷液速度:8~40rpm;喷枪压力:1.5~2.5bar;风量:60~100m³/h。
制得白色小丸即含活性成分兰索拉唑的微丸芯248.1g,增重为24.05%,收率为98.5%。
(2)制备包覆隔离层的微丸
取步骤(1)制备的含活性成分兰索拉唑的微丸芯200g,隔离层的处方如下:
。
隔离层的制备方法为:
将羟丙甲纤维素E5、羧甲淀粉钠加入纯化水中,搅拌溶解,再加入碳酸镁,搅拌均匀,得包衣液2;
将包衣液2采用流化床底喷包衣技术喷至含活性成分兰索拉唑的微丸芯上,形成包覆隔离层的微丸。
流化床底喷包衣的操作参数为:物料温度:35~50℃;进风温度:60~90℃;喷液速度:8~20rpm;喷枪压力:1.5~2.5bar;风量:60~100m³/h。
制得白色小丸即包覆隔离层的微丸222.6g,增重为11.3%,收率为98.9%。
(3)制备兰索拉唑肠溶微丸
取步骤(2)制备的包覆隔离层的微丸200g,肠溶层的处方如下:
。
肠溶层的制备方法为:
将甲基丙烯酸和丙烯酸乙酯水分散体、聚乙二醇、滑石粉加入中纯化水中,分散均匀,得包衣液3;
将包衣液3采用流化床底喷包衣技术喷至所述包覆隔离层的微丸上,形成兰索拉唑肠溶微丸。
流化床底喷包衣的操作参数为:物料温度:25~35℃;进风温度:30~50℃;喷液速度:8~22rpm;喷枪压力:1.5~2.5bar;风量:60~100m³/h。
制得白色小丸即兰索拉唑肠溶微丸264.2g,增重为32.1%,收率为99.8%。
对比例1
(1)制备含兰索拉唑的微丸芯,处方如下:
。
载药层的制备方法为:
将羟丙甲纤维素加入30%乙醇溶液中,搅拌溶解,再依次加入甘露醇、碳酸镁、十二烷基硫酸钠搅拌均匀,加入兰索拉唑,搅拌30-60分钟,得包衣液1。
将包衣液1采用流化床底喷包衣技术喷至淀粉蔗糖丸芯上,形成含活性成分兰索拉唑的微丸芯。
流化床底喷包衣的主要操作参数为:物料温度:35~50℃;进风温度:60~90℃;喷液速度:8~40rpm;喷枪压力:1.5~2.5bar;风量:60~100m³/h。
制得白色小丸即含兰索拉唑的微丸芯212.7g,收率为92.7%。
(2)制备包覆隔离层的微丸
取步骤(1)制备的含活性成分兰索拉唑的微丸芯200g,隔离层的处方如下:
。
隔离层的制备方法为:
将羟丙甲纤维素E5加入纯化水中,搅拌溶解,再加入碳酸镁,搅拌30-60分钟,得包衣液2;
将包衣液2采用流化床底喷包衣技术喷至含活性成分兰索拉唑的微丸芯上,形成包覆隔离层的微丸。
流化床底喷包衣的主要操作参数为:物料温度:35~50℃;进风温度:60~90℃;喷液速度:8~20rpm;喷枪压力:1.5~2.5bar;风量:60~100m³/h。
制得白色小丸即包覆隔离层的微丸216.7g,收率为97.0%。
(3)制备兰索拉唑肠溶微丸
取步骤(2)制备的包覆隔离层的微丸200g,肠溶层的处方如下:
。
肠溶层的制备方法为:
将甲基丙烯酸和丙烯酸乙酯水分散体、聚乙二醇、滑石粉加入中纯化水中,分散均匀,得包衣液3;
将包衣液3采用流化床底喷包衣技术喷至包覆隔离层的微丸上,形成兰索拉唑肠溶微丸。
流化床底喷包衣的操作参数为:物料温度:25~35℃;进风温度:30~50℃;喷液速度:8~22rpm;喷枪压力:1.5~2.5bar;风量:60~100m³/h。
制得白色小丸即兰索拉唑肠溶微丸261.9g,收率为99.2%。
对比例2
(1)制备含兰索拉唑的微丸芯,处方如下:
。/>
载药层的制备方法为:
将羟丙甲纤维素加入30%乙醇溶液中,搅拌溶解,再依次加入低取代羟丙纤维素、甘露醇、碳酸镁、十二烷基硫酸钠搅拌均匀,加入兰索拉唑,搅拌30-60分钟,得包衣液1。
将包衣液1采用流化床底喷包衣技术喷至淀粉蔗糖丸芯上,形成含活性成分兰索拉唑的微丸芯。
流化床底喷包衣的主要操作参数为:物料温度:35~50℃;进风温度:60~90℃;喷液速度:8~40rpm;喷枪压力:1.5~2.5bar;风量:60~100m³/h。
制得白色小丸即含兰索拉唑的微丸芯208.1g,收率为89.9%。
(2)制备包覆隔离层的微丸
取步骤(1)制备的含活性成分兰索拉唑的微丸芯200g,隔离层的处方如下:
。
隔离层的制备方法为:
将羟丙甲纤维素E5加入纯化水中,搅拌溶解,再加入低取代羟丙纤维素、碳酸镁,搅拌30~60分钟,得包衣液2;
将包衣液2采用流化床底喷包衣技术喷至含活性成分兰索拉唑的微丸芯上,形成包覆隔离层的微丸。
流化床底喷包衣的主要操作参数为:物料温度:35~50℃;进风温度:60~90℃;喷液速度:8~20rpm;喷枪压力:1.5~2.5bar;风量:60~100m³/h。
制得白色小丸即包覆隔离层的微丸214.5g,收率为95.5%。
(3)制备兰索拉唑肠溶微丸
取步骤(2)制备的包覆隔离层的微丸200g,肠溶层的处方如下:
。
肠溶层的制备方法为:
将甲基丙烯酸和丙烯酸乙酯水分散体、聚乙二醇、滑石粉加入中纯化水中,分散均匀,得包衣液3;
将包衣液3采用流化床底喷包衣技术喷至包覆隔离层的微丸上,形成兰索拉唑肠溶微丸。
流化床底喷包衣的操作参数为:物料温度:25~35℃;进风温度:30~50℃;喷液速度:8~22rpm;喷枪压力:1.5~2.5bar;风量:60~100m³/h。
制得白色小丸即兰索拉唑肠溶微丸260.1g,收率为98.5%。
溶出度测定
分别取实施例1~4和对比例1~2制备的兰索拉唑肠溶微丸,取相当于30mg兰索拉唑的微丸重量进行试验,照溶出度与释放度测定法(中国药典2020年版四部通则0931第一法方法2)测定,以氯化钠盐酸溶液(取氯化钠2.0g,加盐酸7.0ml,加水溶解并稀释至1000ml)500ml为溶出介质,转速为每分钟150转,依法操作,经60分钟时,立即将转篮升出液面,弃去上述各溶出杯中酸液,立即加入预热至37℃的pH 6.8磷酸盐缓冲液(取0.1mol/L盐酸溶液和0.2mol/L磷酸钠溶液,按3:1混合均匀,必要时用2mol/L盐酸溶液或2mol/L氢氧化钠溶液调节pH值至6.8)900ml,继续依法操作,经60分钟时取样,滤过,精密量取续滤液5ml,置10ml量瓶中,用磷酸盐缓冲液(pH 6.8)稀释至刻度,摇匀,做为供试品溶液;取兰索拉唑对照品约20mg,精密称定,置25ml量瓶中,加甲醇溶解并定量稀释至刻度,摇匀,精密量取2ml,置100ml量瓶中,用磷酸盐缓冲液(pH 6.8)稀释至刻度,摇匀,作为对照品溶液;取供试品溶液与对照品溶液,照紫外-可见分光光度法(中国药典2020年版四部通则0401),在284nm的波长处分别测定吸光度,计算各时间点的溶出量,如表1和图1所示。
表1 各样品在各时间点的溶出度(%)
。
由表1和图1可得出:实施例1~4的兰索拉唑肠溶微丸由于在流化床底喷制备含药丸芯和包覆隔离层时在底喷悬浮液中加入了水溶性的崩解剂,其溶出速度明显比未加入崩解剂及加入非水溶性的崩解剂的兰索拉唑肠溶微丸的溶出速度快,本发明制备的兰索拉唑肠溶微丸与参比制剂的溶出速度基本一致,避免了使用离心造粒机,缩减了设备投入,降低了生产成本。
以上内容是结合具体的实施方式对本申请所作的进一步详细说明,不能认定本申请的具体实施只局限于这些说明。对于本申请所属技术领域的普通技术人员来说,在不脱离本申请构思的前提下,还可以做出若干简单推演或替换,都应当视为属于本申请的保护范围。
- 兰索拉唑肠溶微丸及其制备方法
- 一种稳定的兰索拉唑肠溶微丸及其制备方法
