一种含S-S键的共价有机框架及其制备方法与应用
文献发布时间:2024-04-18 20:01:23
技术领域
本发明属于催化剂制备技术领域,具体涉及一种含S-S键的共价有机框架及其制备方法与应用。
背景技术
公开该背景技术部分的信息仅仅旨在增加对本发明的总体背景的理解,而不必然被视为承认或以任何形式暗示该信息构成已经成为本领域一般技术人员所公知的现有技术。
具有有序多孔结构的共价有机框架(COFs)已成为最有前途的多孔材料之一。它们由有机构件通过强共价键通过热力学控制的可逆聚合而构建的。考虑到其高比表面积、预先设计的结构、优异的化学稳定性以及规则的孔径和简便的功能,COFs已经可以作为催化领域的功能平台。最近的研究表明,具有特定功能化的COFs可以成为催化各种反应的高效催化剂,例如在化学催化、光催化、电催化等领域。此外,为了提高其性能,各种定制的官能团,如-SCH
一般采用直接合成(也称为从头策略)和后合成两种各种定制的官能团集成到COFs的骨架中。例如,采用具有硫醚官能团的分子构建单体直接制备目标材料硫醚官能化COF,合成乙炔基功能化COFs后修饰硫醇接枝亚胺基得到硫醇接枝亚胺基COF(TPB-DMTP-COF-SH)。然而,无论是直接合成还是后合成,硫功能化的COF的合成过程需高温高压等反应条件,存在反应条件苛刻,反应步骤复杂的缺点。因此,开发一种简单、低成本且方便高效的合成策略来制备无法直接获得的硫功能化COF是非常必要的。
发明内容
为了解决现有技术的不足,本发明的目的是提供一种含S-S键的共价有机框架及其制备方法与其在催化亚胺和杂环卡宾硼烷的逆硼氢化反应中的应用。本发明的含S-S键的共价有机框架性能稳定,作为异相催化剂催化逆硼氢化反应时利用率高,反应条件温和,能够有效降低催化成本。
为了实现上述目的,本发明的技术方案为:
本发明的第一方面,提供一种含S-S键的共价有机框架的制备方法,包括以下步骤:
将醛类化合物、胺类化合物在溶剂中混合均匀,再加入乙酸,室温下搅拌反应,得到含S-S键的共价有机框架材料;
所述醛类化合物、胺类化合物分别为2,4,6-三羟基苯-1,3,5-三甲醛、4,4'-二硫代二苯胺;
或,所述醛类化合物、胺类化合物分别为2,4,6-三(4-醛基苯基)-1,3,5-三嗪、4,4'-二硫代二苯胺;
或,所述醛类化合物、胺类化合物分别为1,3,6,8-四(4-甲醛基苯基)芘、4,4'-二硫代二苯胺。
本发明采用简单的室温下的合成方法制备共价有机框架材料,反应温度低,方法简单,易于推广。
在本发明的一些实施例中,2,4,6-三羟基苯-1,3,5-三甲醛、4,4'-二硫代二苯胺的摩尔比为1~3:2~4,优选为2:3,以提高反应效率和产率。
在本发明的一些实施例中,2,4,6-三(4-醛基苯基)-1,3,5-三嗪、4,4'-二硫代二苯胺的摩尔比为1~3:2~4,优选为2:3,以提高反应效率和产率。
在本发明的一些实施例中,1,3,6,8-四(4-甲醛基苯基)芘、4,4'-二硫代二苯胺的摩尔比为1~2:2~4,优选为1:2,以提高反应效率和产率。
在本发明的一些实施例中,所述溶剂为邻二氯苯、正丁醇和甲醇中的一种或多种。
优选的,所述溶剂为体积比为1:1的邻二氯苯和正丁醇混合液,或,所述溶剂为体积比为1:1的邻二氯苯和甲醇的混合液。
进一步优选的,4,4'-二硫代二苯胺与所述溶剂的用量比为:4~8:3~5,mg:mL,优选为4.96:4或7.45:4,mg:mL,以有效地溶解醛类化合物、胺类化合物。
本发明的一些实施例中,所述室温温度为15-25℃,在不同的季节和地区,都可以进行反应。
在本发明的一些实施例中,反应时间为2~4天,优选为3天。
本发明的第二个方面,提供一种上述的制备方法制备的含S-S键的共价有机框架,所述共价有机框架具有式Ⅰ、式Ⅱ或式Ⅲ所示的结构单元;
本发明的第三个方面,提供一种上述的含S-S键的共价有机框架在催化亚胺和杂环卡宾硼烷的逆硼氢化反应中的应用,所述含S-S键的共价有机框架具有式Ⅰ所示的结构单元。
上述的亚胺和杂环卡宾硼烷的逆硼氢化反应的机理如下:
在起始步骤中,在可见光照射条件下,二硫化物(即本发明中的含S-S键的共价有机框架)形成巯基自由基A。巯基自由基从NHC-硼烷2(即杂环卡宾硼烷)中夺取氢,得到NHC-硼基自由基B。在关键步骤中,,NHC-硼基自由基B加成到亚胺1上,得到α-NHC硼基氨基自由基C。由于NHC-硼基自由基的亲核性,相比于亚胺的N原子加成,NHC-硼基自由基B更易加成到亚胺的C原子上。最后,α-NHC硼基氨基自由基C从硫醇中夺取氢,得到化合物3和另一个硫基自由基A。
本发明的第四个方面,提供一种亚胺和杂环卡宾硼烷的逆硼氢化反应,包括以下步骤:
将(E)-N-苄烯苯胺、(1,3-二甲基-1H-咪唑-3-鎓-2-基)三硼氢化物和异相催化剂在有机溶剂中、室温、氮气氛围、光照条件下反应,反应结束后,得到相应的产物;
所述异相催化剂为上述具有式Ⅰ所示的结构单元的含S-S键的共价有机框架。
在本发明的一些实施例中,反应结束后,离心去除所述异相催化剂,得到相应的产物。
在本发明的一些实施例中,所述光照条件为CFL(白炽灯)或白光(可见光),功率为12W。
在本发明的一些实施例中,所述室温为24-26℃,优选为25℃。
在本发明的一些实施例中,所述有机溶剂为乙腈。乙腈与(E)-N-苄烯苯胺的用量比为2:40~50,mL:mg,进一步优选为2:46,mL:mg。
在本发明的一些实施例中,反应时间为12~24h,优选为16h。
在本发明的一些实施例中,(E)-N-苄烯苯胺、(1,3-二甲基-1H-咪唑-3-鎓-2-基)三硼氢化物和异相催化剂的摩尔比为:1:2~2.5:0.01,优选为1:2.4:0.01。
采用本发明的上述具有式Ⅰ所示的结构单元的含S-S键的共价有机框架催化亚胺和杂环卡宾硼烷的逆硼氢化反应,实现了异相催化,并且催化剂用量少,回收容易,提高了催化剂的利用率,降低了成本。
从以上技术方案可以看出,本发明的有益效果为:
本发明提供的含S-S键的共价有机框架的制备方法,反应条件为室温搅拌,相较于此前的硫功能化COF的合成,本发明的合成步骤简便且无需严苛的反应条件。
本发明提供了三种新型含S-S键的共价有机框架材料,该含S-S键的共价有机框架材料的合成反应温度低,反应效果好,减少了能耗,方法简单、成本低、实用性强,易于推广。其中具有式Ⅰ所示的结构单元的含S-S键的共价有机框架材料可作为异相催化剂,催化亚胺和杂环卡宾硼烷的逆硼氢化反应,实现了异相催化,并且性能稳定,循环四次使用后,产物产率在65%左右,用量少,回收容易,提高了催化剂的利用率,降低了成本。
附图说明
构成本发明的一部分的说明书附图用来提供对本发明的进一步理解,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。
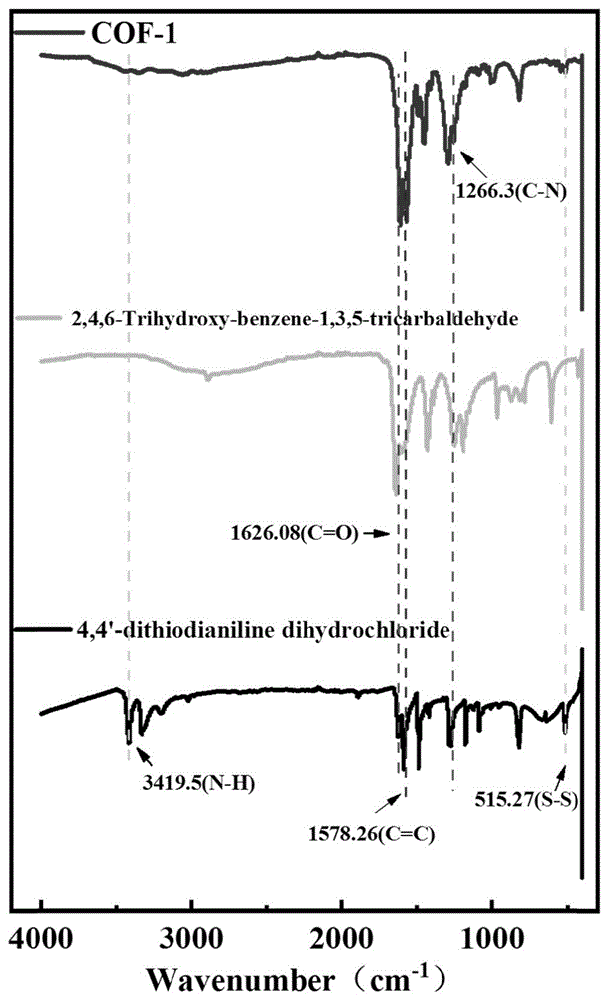
图1是本发明实施例1制备的COF-1与配体的红外光谱图;
图2是本发明实施例2制备的COF-2与配体的红外光谱图;
图3是本发明实施例3制备的COF-3与配体的红外光谱图;
图4是本发明实施例1制备的COF-1的PXRD图谱;
图5是本发明实施例2制备的COF-2的PXRD图谱;
图6是本发明实施例3制备的COF-3的PXRD图谱;
图7是本发明实施例4中的COF-1催化4次的PXRD图谱;
图8是本发明实施例4中的COF-1催化4次的产率统计图。
具体实施方式
为了使得本领域技术人员能够更加清楚地了解本发明的技术方案,以下将结合具体的实施例详细说明本发明的技术方案。
实施例1:具有式Ⅰ所示结构单元的含S-S键的共价有机框架材料COF-1的合成
合成路线如下:
将4.2mg(0.02mmol)2,4,6-三羟基苯-1,3,5-三甲醛、7.45mg(0.03mmol)4,4'-二硫代二苯胺置于10mL EP管中,加入2mL邻二氯苯、2mL正丁醇,搅拌溶解,接着加入500μL浓度为6M的乙酸水溶液,搅拌反应3days。反应结束,用DMF、甲醇和乙醇各洗三遍,得到含S-S键的共价有机框架材料,命名为COF-1,产率为76%。
通过FT-IR,PXRD表征了该聚合物,结果分别见图1、图4。
实施例2:具有式Ⅱ所示结构单元的含S-S键的共价有机框架材料COF-2的合成
合成路线如下:
将7.87mg(0.02mmol)2,4,6-三(4-醛基苯基)-1,3,5-三嗪、7.45mg(0.03mmol)4,4'-二硫代二苯胺置于10mL EP管中,加入2mL邻二氯苯和2mL甲醇,搅拌溶解,接着加入500μL浓度为6M的乙酸水溶液,搅拌反应3天。反应结束,用DMF、甲醇、乙醇各洗三遍,得到含S-S键的共价有机框架材料,命名为COF-2,产率为88.5%。
通过FT-IR、PXRD表征了该聚合物,结果分别见图2、图5。
实施例3:具有式Ⅲ所示结构单元的含S-S键的共价有机框架材料COF-3的合成
合成路线如下:
将6.18mg(0.01mmol)1,3,6,8-四(4-甲醛基苯基)芘、4.96mg(0.02mmol)4,4'-二硫代二苯胺置于10mLEP管中,加入2mL邻二氯苯、2mL正丁醇,搅拌溶解,接着加入500μL浓度为6M的乙酸水溶液,搅拌反应3days。反应结束,用DMF、甲醇和乙醇各洗三遍,得到含S-S键的共价有机框架材料,命名为COF-3产率为57.8%。
通过FT-IR、PXRD表征了该聚合物,结果分别见图3、图6。
实施例4:亚胺和杂环卡宾硼烷的逆硼氢化反应
所述亚胺和杂环卡宾硼烷的逆硼氢化反应的反应路线如下:
在25℃下,将(E)-N-苄烯苯胺(46mg,0.25mmol)、(1,3-二甲基-1H-咪唑-3-鎓-2-基)三硼氢化物(66mg,0.6mmol)、实施例1的COF-1(20mg,1mol%)置于反应容器中,并抽真空通氮气三次,加入2mL乙腈,氮气氛围、光照条件下反应16h,反应结束后,通过离心将催化剂滤出。旋蒸除去溶剂后,将产物通过硅胶柱纯化,得到相应的产物。
所得产物及产率如表1所示。
实施例5:亚胺和杂环卡宾硼烷的逆硼氢化反应
与实施例4的区别在于亚胺分别为含有不同取代基的亚胺。所采用的亚胺结构如表1所示。所得产物及产率如表1所示。
表1亚胺和杂环卡宾硼烷的逆硼氢化反应的产物及产率
将实施例4滤出的催化剂重新加入亚胺和杂环卡宾硼烷的逆硼氢化反应,重复四次,亚胺和杂环卡宾硼烷的逆硼氢化反应结束后,每次产率如图7所示,产率依旧维持在65%左右,可见,实施例1的COF-1作为催化剂使用时,具有较为良好的稳定性。
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
