制备姜油酮的方法、包含姜油酮的组合物和其用途
文献发布时间:2024-05-31 01:29:11
相关申请
本申请要求于2021年8月11日提交的第779010号新西兰临时申请的权益,其全部内容通过引用并入本文。
发明的领域
本公开涉及制备姜油酮的方法和包含姜油酮的组合物。特别指出的是药物组合物以及这些组合物的用途。
发明的背景
生姜(Zingiber officinale)是一种开花植物,其根茎被广泛用作香料和传统药物。如果食用量合理,生姜几乎没有负面副作用。它被列入FDA的“公认安全”名单。
生姜特有的香味和风味来自于占新鲜生姜重量的1-3%的挥发油,其主要由姜油酮、姜烯酚和姜酚组成,姜酚包含[6]-姜酚(1-[4'-羟基-3'-甲氧基苯基]-5-羟基-3-癸酮)作为主要的刺激性化合物。
据Li等人的2016,“Chemical Characterisation and antioxidant activitiescomparison in fresh,dried,stir frying and carbonized ginger”Journal ofChromatography B Analyt.Technol.Biomed.Life Sci.1011:223-232报道的,姜油酮(也称为姜酮)是由姜酚在约40摄氏度的温度下干燥或热处理过程中产生的。姜油酮具有较低的刺激性和辛甜香味。姜油酮也称为香草基丙酮,是一种结晶固体,据报道微溶于水,可溶于乙醚。FoodB化合物数据库中描述了姜油酮的水溶性值为0.57g/L,LogP值为2.02 1.92,logS为-2.5;见https://foodb.ca/compounds/FDB010527。
新鲜生姜含有极少量的姜油酮,已知姜油酮是通过蒸煮或干燥生姜根而产生的,这引起姜酚通过失去水分子而脱水,以产生姜油酮和己醛。见,例如,Gopi等人的2016,“Study on temperature dependent conversion of active components of ginger”Int.J.of Pharma Sciences 6(1):1344-1347。
姜烯酚更具刺激性,具有更高的抗氧化活性,在原始生姜中没有发现,但在加热、储存过程中或通过酸性由姜酚形成。
姜烯酚是姜酚的脱水形式。
1917年Hiroshi Nomura首次从生姜根中分离出姜油酮。Nomura发现了合成姜油酮的方法,并在后来获得了专利(1918年4月23日授权的US1,263,796),其中香草醛和丙酮在碱性条件下反应形成脱氢姜油酮。该化合物以约95%的量获得。该反应之后,对中间体化合物进行催化氢化,以形成姜油酮,以约100%的量获得。
生姜化合物已被证明能够有效对抗产肠毒素性大肠杆菌不耐热肠毒素引起的腹泻。这种类型的腹泻是发展中国家婴儿死亡的主要原因。据报道,姜油酮可能是生姜止泻功效的活性成分。该研究得出结论,生姜的生物活性化合物显著阻断了产肠毒素性大肠杆菌不耐热肠毒素与细胞表面受体G M1的结合,从而抑制了小鼠闭合的回肠袢中的液体积聚。参见,例如Chen等人的2007,“Ginger and its bioactive component inhibitenterotoxigenic Escherichia coli heat-labile enterotoxin-induced diarrhoea inmice”Journal of Agricultural and Food Chemistry 55(21):8390-7。
据Kumar等人报道,姜油酮在腹膜炎小鼠模型中显示出对肝脏炎症具有抗炎作用。参见Kumar等人的“Zingerone suppresses liver inflammation induced by antibioticmediated endotoxemia through down regulating hepatic mRNAexpression ofinflammatory markers in Pseudomonas aeruginosa peritonitis mouse model”PLOSONE 9(9):e106536。
Kumar等人也报道了姜油酮可以增强铜绿假单胞菌(Pseudomonas aeruginosa)细胞对抗生素的敏感性。见Kumar等人的2014,Life Sciences 117:24-32。Kumar等人得出结论,发现姜油酮引起铜绿假单胞菌细胞表面性质的改变,从而增加了铜绿假单胞菌细胞对抗生素的敏感性。
关于优化从天然来源生产姜油酮的研究有限。鉴于目前对源自天然来源的组合物的重视,需要新的组合物,其包括基于植物的组合物,尤其是具有抗微生物活性的组合物。本申请旨在满足这些需求和其他需求。
发明概述
一方面,本公开涵盖通过以下生产姜油酮的方法:(i)在碱性溶液中对生姜根进行碱处理;或者(ii)在碱性溶液中对从生姜根获得的汁液进行碱处理。
在具体方面:
生姜根是新鲜的。
生姜根是干燥的。
生姜根在约40至约70摄氏度、或约55至约65摄氏度、或约60摄氏度下干燥。
汁液通过浸渍和/或压榨生姜根获得。
将生姜根切成小块,然后进行碱处理。
将生姜根切成小块,干燥,然后进行碱处理。
碱处理在约40至约70摄氏度下进行。
碱处理在约50至约60摄氏度下进行。
碱处理在约55至约65摄氏度下进行。
碱处理在约60摄氏度下进行。
碱处理进行约1-72小时。
碱处理进行约1-48小时。
碱处理进行约1-24小时。
碱处理进行约1-30小时,或约1-20小时,或约1-10小时,或约1-5小时。
碱处理进行约0.5至约3小时,或约0.5至约2小时,或约1至约2小时。
碱处理进行约2小时。
碱处理进行约1小时。
使用氢氧化钾(KOH)。
使用液体形式的氢氧化钾(KOH)。
使用约0.1%至约1.0% KOH(v/v)。使用约0.5%至约0.7% KOH(v/v)。
使用约1%至约3% KOH(v/v)。使用约1.5%至约2.5% KOH(v/v)。使用约2% KOH(v/v)。
使用氢氧化钙Ca(OH)
使用约0.5%至约4% Ca(OH)
碱处理后,中和碱性溶液。
中和碱性溶液以获得约6.5至约7.5的pH。
将中和后的碱性溶液冷冻干燥。
对中和后的碱性溶液进行姜油酮的提取。
对中和后的碱性溶液进行干燥,然后进行姜油酮的提取。
干燥在约60摄氏度下进行长达24小时。
姜油酮任选地通过一个或多个醇提取步骤来提取。姜油酮通过一个或多个乙醇提取步骤来提取。
乙醇提取进行至少7天。
乙醇提取进行24小时或少于24小时。
姜油酮使用超临界流体萃取来提取。
姜油酮通过超临界流体萃取、随后进行醇提取步骤来提取。
所述方法生产的产物主要由姜油酮组成。
所述方法生产的产物不含或基本不含醛。
在一方面,本公开涵盖了通过对生姜根提取物进行碱处理来生产姜油酮的方法。
生姜根提取物是通过对生姜根进行超临界流体萃取而获得的。
生姜根提取物是通过对生姜根进行醇提取而获得的。
生姜根提取物是通过对生姜根进行榨汁而获得的。
榨汁包括浸渍和/或压榨生姜根。
碱处理在约30至约70摄氏度下进行。
碱处理在约50至约60摄氏度下进行。
碱处理在约55至约65摄氏度下进行。
碱处理在约60摄氏度下进行。
碱处理进行约1-72小时。
碱处理进行约1-48小时。
碱处理进行约1-24小时。
碱处理进行约1-30小时,或约1-20小时,或约1-10小时,或约1-5小时。
碱处理进行约0.5至约3小时,或约0.5至约2小时,或约1至约2小时。
碱处理进行约2小时。
碱处理进行约1小时。
使用氢氧化钾(KOH)。
使用液体形式的氢氧化钾(KOH)。
使用约0.1%至约5.0% KOH(v/v)。使用约0.5%至约0.7% KOH(v/v)。
使用约1%至约3% KOH(v/v)。使用约1.5%至约2.5% KOH(v/v)。使用约2% KOH(v/v)。
使用氢氧化钙Ca(OH)
使用约0.5%至约4% Ca(OH)
碱处理后,中和碱性溶液。
中和碱性溶液以获得约6.5至约7.5的pH。
中和碱性溶液后,进一步提取姜油酮。
姜油酮任选地通过一个或多个醇提取步骤来进一步提取。
姜油酮任选地通过一个或多个乙醇提取步骤来进一步提取。
乙醇提取进行至少7天。
乙醇提取进行24小时或少于24小时。
姜油酮任选地使用超临界流体萃取来进一步提取。
姜油酮任选地通过超临界流体萃取、随后进行醇提取步骤来进一步提取。
所述方法生产的产物主要由姜油酮组成。
所述方法生产的产物不含或基本不含醛。
所述方法包括:(i)在碱性溶液中对生姜根进行碱处理;或者(ii)在碱性溶液中对从生姜根获得的汁液进行碱处理,其中该碱性溶液包含约1.5%至约2.5% KOH(v/v),其中该碱处理进行约1至约2小时,并且其中在碱处理后,中和碱性溶液至约6.5至约7.5的pH。
还涵盖了包含姜油酮的组合物,该姜油酮通过前述任一方面的方法制备。
进一步涵盖了主要由姜油酮组成的组合物,该姜油酮通过前述任一方面的方法制备。
在一方面,本公开涵盖了治疗或预防微生物感染的方法,包括:向个体施用前述任一方面的组合物,从而治疗或预防感染。
在另一个方面,本公开涵盖了前述任一方面的组合物用于制备用于治疗或预防微生物感染的药物的用途。
还涵盖了用于治疗或预防微生物感染的包含姜油酮的组合物。
在各个方面:
包含姜油酮的组合物通过前述任一方面的方法获得。
包含姜油酮的组合物从生姜根中获得。
包含姜油酮的组合物从新鲜的生姜根中获得。
包含姜油酮的组合物从干燥的生姜根中获得。
包含姜油酮的组合物从由生姜根制备的汁液中获得。
汁液通过浸渍和/或压榨生姜根制备。
使用碱转化步骤以将生姜根中的姜酚或来自生姜根的汁液中的姜酚转化成姜油酮获得包含姜油酮的组合物。
包含姜油酮的组合物不含或基本不含醛。
包含姜油酮的组合物被配制成粉末。
包含姜油酮的组合物被配制成酊剂。
组合物进一步包含一种或多种抗微生物剂。
组合物进一步包含一种或多种氨基糖苷类抗生素或一种或多种糖肽类抗生素。
组合物进一步包含万古霉素。
组合物进一步包含庆大霉素。
微生物选自由以下组成的组:细菌和真菌。
细菌是革兰氏阳性菌或革兰氏阴性菌。
细菌选自由以下组成的组:芽孢杆菌属(Bacillus)、梭菌属(Clostridium)、埃希氏菌属(Escherichia)、支原体属(Mycoplasma)、奈瑟菌属(Neissaria)、假单胞菌属(Pseudomonas)、沙门氏菌属(Salmonella)、志贺氏菌属(Shigella)、链球菌属(Streptococcus)、葡萄球菌属(Staphylococcus)和弧菌属(Vibrio)的细菌。
细菌选自由以下组成的组:大肠杆菌(Escherichia coli)、金黄色葡萄球菌(Staphylococcus aureus)、肺炎链球菌(Streptococcus pneumoniae)、铜绿假单胞菌(Pseudomonas aeruginosa)和肺炎克雷伯杆菌(Klebsiella pneumoniae)。
真菌选自由以下组成的组:曲霉菌属(Aspergillus)、念珠菌属(Candida)、球孢子菌属(Coccidioides)、隐球菌属(Cryptococcus)、组织胞浆菌属(Histoplasma)、肺孢菌属(Pneumocystis)和葡萄穗霉菌(Stachybotrys)属的真菌。
真菌选自由以下组成的组:白色念珠菌(Candida albicans)、曲霉菌(Aspergillus species)、荚膜组织胞浆菌(Histoplasma capsulatum)、粗球孢子菌(Coccidioides immitis)、卡氏肺孢菌(Pneumocystis carinii)和癣真菌。
在组合物的各个方面:
组合物被配制用于局部给药或口服给药。
组合物被配制成液体、粉末、片剂或胶囊。
组合物包含约1mg至约5000mg的剂量的姜油酮。
组合物包含约1mg至约1500mg的剂量的姜油酮。
组合物包含约5mg至约500mg的剂量的姜油酮。
组合物包含约1mg至约150mg的剂量的姜油酮。
组合物包含约5mg至约50mg的剂量的姜油酮。
组合物包含约1mg至约15mg的剂量的姜油酮。
组合物包含约1mg至约10mg的剂量的姜油酮。
组合物以小袋形式提供。
组合物被配制成与一种或多种抗微生物剂共同给药。
组合物被配制成与一种或多种氨基糖苷类抗生素或一种或多种糖肽类抗生素共同给药。
组合物被配制成与庆大霉素或万古霉素共同给药。
微生物感染是影响以下的一种或多种的感染:皮肤、眼睛、耳朵、鼻子、口腔、喉咙、食道、肺、循环系统、胃肠系统或泌尿生殖系统。
前述简要概述广泛地描述了本公开的某些实施方案的特征和技术优点。进一步的技术优点将在下面的详细描述和实施例中描述。
当结合任何附图和实施例来考虑时,被认为是特有的新颖性特征将从详细描述中得到更好的理解。然而,本文提供的附图和实施例旨在帮助示例性说明所公开的内容或帮助理解所公开的内容,而非旨在限制本公开的范围。
附图的简要说明
图1.描绘了新鲜生姜根的照片。
图2.经碱处理的生姜的HPLC UV色谱图迹线(280nm)。
图3.示出处理比较的示意图。
图4A:描绘了榨汁机和榨汁前原始生姜的照片。
图4B:描绘了正在进行原始生姜的榨汁的照片。
图5A:生姜汁用KOH(0.5%)处理并通过HPLC分析。所示为姜油酮(Z)和姜酚(G)的峰面积。
图5B:生姜汁用KOH(1%)处理并通过HPLC分析。所示为姜油酮(Z)和姜酚(G)的峰面积。
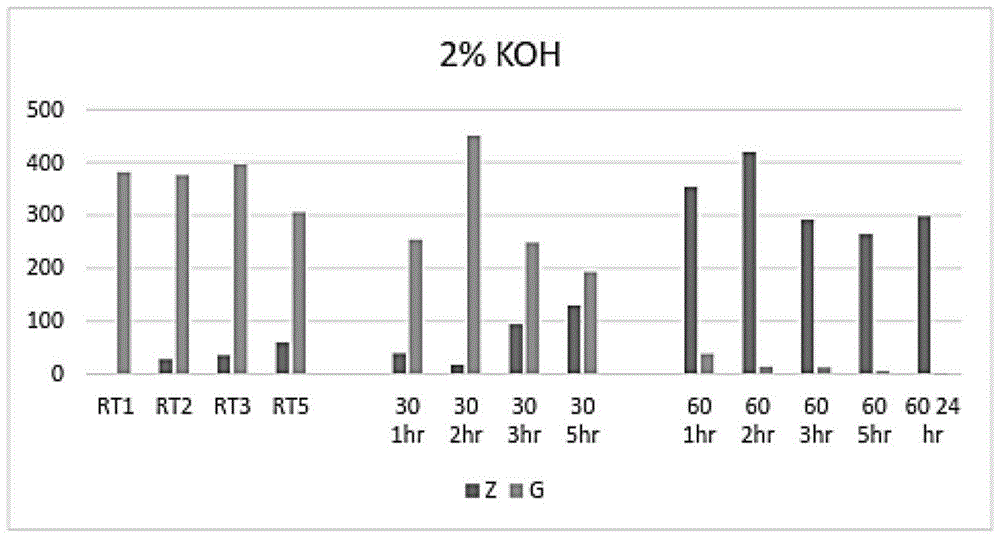
图5C:生姜汁用KOH(2%)处理并通过HPLC分析。所示为姜油酮(Z)和姜酚(G)的峰面积。
图6A:通过压榨产生的生姜渣。
图6B:通过压榨产生的生姜汁。
图7:示出乙醇提取工艺和蒸发的示意图。
图8A:乙醇提取物的GCMS TIC分析。
图8B:乙醇提取物与己醛标准品的比较。示出的是色谱图的2-7分钟区域。
图9A:姜油酮和庆大霉素的组合的棋盘格试验。
图9B:姜油酮和万古霉素的组合的棋盘格试验。
图9C:姜油酮和头孢噻肟的组合的棋盘格试验。
详细描述
以下描述阐述了许多示例性配置、参数等。然而,应当认识到,这种描述并不旨在限制本公开的范围,而是作为示例性实施方案的描述而提供。
本说明书中引用的所有参考文献(包括专利和专利申请)在此通过引用并入本文。不承认任何参考文献构成现有技术。对任何参考文献的讨论也不构成承认该参考文献在新西兰或任何其他国家构成本领域公知常识的一部分。
定义
在本文的每个实例中,在本公开的描述、实施方案和实施例中,术语“包含”、“包括”等应做广义理解,而不受限制。因此,除非上下文另有明确要求,否则在整个说明书和权利要求中,词语“包括”、“包含”等应被解释为包含性意义,而不是排他性意义,也就是说是“包括但不限于”的意义。
在本说明书中,使用冠词“一个/一种”是指该冠词的语法对象为一个/一种或多个/多种(即至少一个/一种)。举例来说,“元件”可以用来表示一个元件或多于一个的元件。
在整个说明书中,术语“约”用于表示数值包括用于测定该数值的方法的误差的标准偏差,例如如本文详细描述的化合物的水平或剂量水平。特别地,术语“约”包括所述数值或范围中至多10%的偏差(正偏差和负偏差)。
本文所用的术语“包含”可以指组合物中存在姜油酮或姜油酮提取物。作为示例,姜油酮或姜油酮提取物按重量计可以占组合物的至少0.1%、至少0.2%、至少0.3%、至少0.4%、至少0.5%、至少0.6%、至少0.7%、至少0.8%、至少0.9%、至少1%、至少2%、至少5%、至少10%、至少20%、至少30%、至少40%、至少50%、至少60%、至少70%、至少80%或至少90%(%w/w)。对于液体,姜油酮或姜油酮提取物可以按体积计占组合物的至少0.1%、至少0.2%、至少0.3%、至少0.4%、至少0.5%、至少0.6%、至少0.7%、至少0.8%、至少0.9%、至少1%、至少2%、至少5%、至少10%、至少20%、至少30%、至少40%、至少50%、至少60%、至少70%、至少80%或至少90%(%v/v)。
本文使用的术语“基本上由...组成”可以指产物中存在姜油酮。该产物可以是例如本文所述的组合物,或者可以是例如通过本文所述的方法产生的产物。作为示例,姜油酮可以占产物重量的至少90%,或者占产物重量的至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%、至少99%(%w/w)。对于液体,姜油酮可以占产物体积的至少90%,或者占产物体积的至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%、至少99%、至少99.5%、至少99.8%或至少99.9%(%v/v)。
与醛相关的术语“基本上不含”是指醛的水平可忽略不计的产物。该产物可以是例如本文所述的组合物,或者可以是例如通过本文所述的方法产生的产物。作为示例,醛的水平可以小于20ppm、小于15ppm、小于10ppm、小于7.5ppm、小于5ppm、小于2ppm、小于1.5ppm、小于1ppm、小于0.75ppm、小于0.5ppm、小于0.2ppm、小于0.1ppm、小于0.05ppm、小于0.005ppm或小于0.0005ppm。
本文使用的术语“碱处理”是指将生姜或生姜提取物的样品暴露于pH值大于7的含碱的水溶液中。包括但不限于包含氢氧化钠、氢氧化钾、氢氧化钙、氢氧化镁及其任意组合的溶液。应当理解,碱处理可以在本文所述的温度范围内进行,并且可以在暴露于包含生姜或来自生姜的提取物的样品之前或期间加热碱性溶液。碱性溶液将具有化学有效量的碱,以将样品中存在的至少一些姜酚转化为姜油酮。本文详细描述了特定的方法论。
从生姜根制备的“提取物”是指其中根的一种或多种液体、固体或化学成分已被分离或浓缩的组合物。例如,可以从生姜根中获得液体、固体或半固体提取物。提取物可通过以下的一种或多种方法获得:榨汁、压榨、浸渍、捣碎、研磨或其他已知方法。还包括基于溶剂的提取。特别指出的是固体提取物,例如通过干燥或蒸发获得的粉末。作为具体的示例,提取物可以制备成干燥形式,或者可以制备成溶液形式。“姜油酮提取物”是指从生姜根制备/产生的包含姜油酮或基本上由姜油酮组成的提取物。本文详细描述了特定的提取物及其产生方法。
“药物组合物”是指施用于个体以例如治疗或预防感染的组合物。
本文使用的“微生物(microbe)”或“微生物(microbial organism)”包括致病性生物,例如细菌、真菌、原生动物和病毒。这包括所有有害的微生物,包括与各种感染和其他健康状况(例如人类和非人类疾病)相关的生物。
本文使用的“细菌”包括但不限于:芽孢杆菌属(Bacillus)、巴尔通体属(Bartonella)、鲍特菌属(Bordetella)、疏螺旋体属(Borrelia)、布鲁氏菌属(Brucella)、弯曲菌属(Campylobacter)、衣原体属(Chlamydia)、嗜衣原体属(Chlamydophila)、梭菌属(Clostridium)、棒状杆菌属(Corynebacterium)、肠球菌属(Enterococcus)、埃希氏菌属(Escherichia)、弗朗西丝菌属(Francisella)、嗜血杆菌属(Haemophilus)、螺杆菌属(Helicobacter)、军团菌属(Legionella)、钩端螺旋体属(Leptospira)、李斯特菌属(Listeria)、分枝杆菌属(Mycobacterium)、支原体属(Mycoplasma)、奈瑟菌属(Neisseria)、假单胞菌属(Pseudomonas)、立克次体属(Rickettsia)、沙门氏菌属(Salmonella)、志贺氏菌属(Shigella)、葡萄球菌属(Staphylococcus)、链球菌属(Streptococcus)、密螺旋体属(Treponema)、脲原体属(Ureaplasma)、弧菌属(Vibrio)和耶尔森菌属(Yersinia)的细菌。包括革兰氏阳性菌和革兰氏阴性菌。本文详细描述了特定的细菌生物。
本文使用的“真菌”包括但不限于:曲霉菌属、念珠菌属、隐球菌属、组织胞浆菌属、肺孢菌属和葡萄穗霉菌属的真菌。特别包括癣真菌。本文详细描述了特定的真菌生物。
本文使用的“原生动物”包括但不限于:棘阿米巴属(Acanthamoeba)、隐孢子虫属(Cryptosporidium)、内阿米巴属(Entamoeba)、贾第鞭毛虫属(Giardia)、利什曼原虫属(Leishmania)、疟原虫属(Plasmodium)、锥虫属(Trypanosoma)和弓形体属(Toxoplasma)的原生动物。本文详细描述了特定的原生动物。
“抗微生物剂”是指阻止微生物生长或感染的成分,例如药物、草药组合物、精油以及各种其他有助于抑制或消除微生物的成分。这样的药剂可以与本公开的化合物和提取物组合使用。
如本文所用,“个体”可以是人类或非人类动物,特别是哺乳动物,包括牛、绵羊、山羊、猪、马和其他家畜,也包括狗、猫和其他家养宠物。在特定方面,个体是人类。
本文使用的“治疗”是指减轻或消除感染,或治疗由感染引起的疾病或其他病况。预期治疗将导致减少和/或消除感染。治疗可以阻止、减少或减缓感染的进展。
本文所用的“预防”是指阻止感染的发作或由感染引起的疾病或其他病况的发作。预期预防性措施将阻止或延迟感染的发生,或者如果出现感染则降低感染的严重程度。应当理解,术语“治疗或预防”不排除在任何给定个体中(例如,在同一时间或不同时间)获得病症的治疗和预防的可能性。
本文所用的“抑制”或“阻止”生长是指减缓或停止一种或多种微生物的生长。这可以通过杀死所述一种或多种微生物来实现,例如根除或减少存在的微生物,或根除或减少微生物的繁殖单元,例如孢子。可替代地或除此之外,抑制或阻止生长还可以通过部分或完全防止微生物的分裂或复制来实现。
制备组合物的方法
发明人已经发现,根据所公开的方法从生姜根制备的姜油酮组合物具有显著的抗微生物活性。因此,本公开总体上涉及由生姜根制备的姜油酮组合物及其制备方法。
在一方面,本公开提供了通过对生姜根进行碱处理来从生姜根产生姜油酮的方法。如本文所述,碱处理可包括在碱性溶液中孵育。作为原料,生姜根可以是新鲜的生姜根。例如,为了有助于制备,优化收获前生姜根在土壤中的保留时间可能会有所帮助。这样,所使用的生姜根将是新鲜的,并且将保持新鲜的生姜根的有利特征。
举例来说,为了优化新鲜度,生姜根可以在处理前少于48小时、处理前少于24小时、处理前少于12小时、处理前少于6小时或处理前少于3小时收获。例如,新鲜生姜以湿基计可以具有约80%至约95%、约81%至约95%、或约82%至约95%、或约83%至约95%、或约85%至约95%的含水量。
或者,生姜根可以在处理前干燥。例如,生姜根可以在约40℃至约70℃、或约55℃至约65℃、或在约60℃下干燥。干燥可以进行约1-72小时、或约1-48小时、或约1-24小时、或约1-20小时、或约1-18小时、或约1-10小时、或约1-5小时。
在某些方面,所选的用于所公开的方法的生姜根可以具有最低水平的姜酚,例如6-姜酚。例如,生姜根(例如,新鲜的生姜根)可以具有约0.3至约10mg/g、或约0.3至约9mg/g、或约0.3至约8mg/g、或约0.3至约7mg/g、或约0.3至约6mg/g、或约0.4至约5mg/g的6-姜酚。作为进一步的示例,生姜根可以含有至少1mg/g、至少2mg/g、至少3mg/g、至少4mg/g或至少5mg/g的6-姜酚。因此,在某些情况下,在开始本文所公开的方法之前,测试原料中姜酚(例如6-姜酚)的水平可以是有利的。
在一方面,所述方法包括将来自生姜根的汁液进行碱处理。生姜汁可以通过浸渍和/或压榨获得。浸渍可以包括用搅拌机、食品加工机或类似机器进行均质化。对于压榨,可以使用机器或手动压榨。特别注意螺旋压榨。榨汁后剩余的固体物质(生姜渣)可以再次榨汁以获得生姜汁。这可以根据需要重复进行。可以在碱处理前混合各种汁液样品。
任选地,可以将生姜渣进行热水处理以获得稀释的汁液。例如,水可以以约6比约1(~6∶1)、或约5比约1(~5∶1)、或约4比约1(~4∶1)、或约3比约1(~3∶1)的重量比加入渣中。水可以是例如在约40℃至约80℃,或在约50℃至约70℃,或在约55℃至约65℃,或在约60℃下。水中的孵育时间可以是约5分钟至约60分钟,或约10分钟至约30分钟,或约15分钟至约20分钟,或约15分钟。然后可以对稀释的汁液样品进行碱处理。在碱处理之前,稀释的汁液样品可以与其他汁液样品混合。
在一方面,氢氧化钾(KOH)可用于碱处理。例如,在碱性溶液中可以使用液体形式的KOH。处理混合物中使用的KOH的浓度可以是例如约0.1%至约1.0%、或约0.5%至约0.7%、或约1%至约3%、或约1.5%至约2.5%、或约2%(v/v)。作为替代方案,氢氧化钙Ca(OH)
在某些方面,碱处理可以使处理溶液的pH水平达到约pH 9至约pH 14、或约pH 9.5至约pH 13.5、或约pH 10至约pH 13、或约pH10.5至约pH 12.5、或约pH 11至约pH 12。碱处理可以在充分高的温度下进行充足的时间,以获得所需水平的姜油酮。例如,碱处理可以进行约1-72小时,或约1-48小时,或约1-24小时。进一步的实例包括处理约1至约30小时、或约1至约20小时、或约1至约10小时、或约1至约15小时、或约1至约7小时、或约1至约6小时、或约1至约5小时、或约1至约4小时、或约0.5至约3小时、或约0.5至约2小时、或约1至约2小时、或约2小时、或约1小时。作为具体的实例,碱处理可以在约40℃至约70℃、或约50℃至约60℃、或约55℃至约65℃、或约60℃下进行。应当理解,较低的温度可以允许较长的处理时间。例如,在室温下进行的碱处理可以进行约3天至约9天,或约5天至约9天,或约5天至约7天。
碱处理后,处理混合物可以例如通过以下的一种或多种进行进一步处理:中和、提取和干燥。对于中和,可以使用柠檬酸或其他酸组合物。作为示例,中和可以实现约6.4至约7.4、或约6.5至约7.5、或约6.6至约7.6、或约6.9至约7.4、或约6.6、约6.7、约6.8、约6.9、约7.0、约7.1、约7.2、约7.3、约7.4或约7.5的pH。例如,可以使用约10至约700g/L的柠檬酸,或者可以使用约10至约600g/L、或约10至约500g/L、或约10至约400g/L、或约10至约300g/L、或约10至约200g/L、或约10至约100g/L、或约10至约50g/L、或约10至约40g/L、或约10至约30g/L、或约10至约20g/L、或约15至约16g/L的柠檬酸。
对于提取,姜油酮提取可以通过一次或多次醇提取,例如一次或多次乙醇提取来实现。作为示例,醇提取(例如乙醇提取)可以进行约1-72小时、或约1-48小时、或约1-24小时、或约6-24小时、或约8-24小时、或约12-24小时、或约18-24小时。在一个具体方面,室温下的乙醇提取可以持续24小时或低于24小时。在提取之前和/或之后可以使用一个或多个干燥步骤。例如,可以利用冷冻干燥。
所述组合物可以制备成抗菌组合物或药物组合物。所述组合物还可以制备成功能性食品或饮料、天然成分(例如天然添加剂)或天然补充剂(例如膳食补充剂)。在各个方面,组合物可以以液体或固体形式、或半固体形式制备。本公开包括各种制剂。在某些方面,可能希望将组合物配制成粉末。粉末可以以自由流动的形式或以固体块状提供。该组合物可以以用于形成悬浮液的粉末、用于形成溶液的粉末、散装颗粒(bulk granule)或散装粉末(bulk powder)的形式提供。如本文详细描述的,粉末可以制成片剂或胶囊、或其他药物制剂。
作为初始处理的一部分,生姜根可以进行清洗或消毒。植物组成部分(例如,果实或种子)可以通过具有一个或多个滚筒刷的组件,以去除任何附着的异物。然后可以使用常规的洗涤技术。例如,可以使用一系列喷嘴来洗涤所述组成部分。根据当地法规和要求,可以使用有助于清洁或减少植物组成部分上的细菌数的洗涤添加剂。例如,可以通过氯洗涤和/或臭氧浸渍的水洗涤,然后用清水漂洗来洗涤植物组成部分。
如上所述,从生姜根制备液体或半固体姜油酮组合物可能是理想的。如本文所述,可以通过化学方法(例如,基于溶剂的提取)提取姜油酮组分。基于溶剂的提取可以利用以下的一种或多种:水、甲醇、乙醇或2-丙醇的提取。超临界流体萃取,例如CO
在具体方面,本公开包括用于从生姜根中提取姜油酮的机械手段(例如,诸如浸渍和/或压榨的榨汁手段)。在一个实施方案中,压榨组件可适于执行制浆或粉碎过程。与常规的果实制浆技术相比,这种方法相对轻柔和温和(“软制浆”)。对于软制浆,没有利用细胞的显著分解或裂解。压榨带可以是围绕一系列滑轮旋转的多个环。分隔压榨带的距离可沿植物组成部分的行进方向减小。以这种方式,当植物组成部分沿着压榨组件的长度行进时,可以对植物组成部分施加增大的力。在特定方面,如本文所述,可以使用压榨组件或机械压榨机从生姜根中获得汁液。可替代地,或除此之外,机械浸渍还可用于获得汁液。例如,可以使用商业榨汁设备。
生姜根组分(例如姜油酮或姜油酮提取物)可以通过冷冻步骤进行处理。随后可以进行干燥或蒸发步骤,或与干燥或蒸发步骤结合使用。在替代实施方案中,将组分干燥或蒸发,然后加工成粉末,而没有中间的冷冻步骤。可以使用涉及空气干燥或热辅助干燥(例如烘箱干燥)的方法。可以例如通过以下的一种或多种获得干燥:日光或太阳能干燥、热空气干燥、分批干燥、旋转干燥、隧道干燥、带式干燥、流化床干燥、冲击干燥、膨化干燥、转鼓干燥、喷雾干燥、真空干燥、冷冻干燥或渗透干燥。用于干燥的示例性温度包括约50℃-70℃、约55℃-65℃、或至少50℃、至少55℃、至少60℃、或至少65℃。可以例如通过以下的一种或多种获得蒸发:盘式蒸发、分批蒸发、管式蒸发、升膜蒸发、降膜蒸发、升-降膜蒸发或搅拌膜蒸发。可以使用各种干燥和蒸发方法的组合。例如,可以使用过滤,然后冷冻干燥。
如果使用冷冻,可能需要在生姜根组分产生后尽快冷冻生姜根组分(例如姜油酮或姜油酮提取物)以保持新鲜。然而,根据需要,冷冻可以在24或48小时内进行。冷冻方法为本领域技术人员所熟知的。鼓风冷冻特别适用于本公开。组分可以在标准尺寸的托盘(pale)中冷冻,该托盘用于收集加工后的冷冻产物。例如,组分可以冷冻保存(例如在-18℃下)直到需要时。任选地,然后可以将该组分冷冻干燥,即冻干。冷冻干燥技术是众所周知和普遍使用的。冷冻干燥周期可能长达48小时。在特定方面,可以进行该工艺以避免水的形成,并且在加工过程中将含水量最小化。应当理解,冷冻干燥/冻干不排除使用较高的温度(即高于冷冻温度)。例如,在冻干/冷冻干燥程序的二次干燥阶段,可以使用较高的温度来去除残留水分。
然后可以将所得的干燥或蒸发的来自生姜根的组分(例如姜油酮或姜油酮提取物)研磨成粉末,然后可以酌情使用。研磨方法是本领域技术人员众所周知并广泛使用的。可以使用标准筛目尺寸来生产粉末,例如,可以使用US20、US23、US 30、US 35、US 40、US 45或US 50筛目尺寸。粉末的筛分粒度可以为1.0至0.3mm;或0.84至0.4mm;或0.71至0.5mm;或者可以是约1.0mm、约0.84mm、约0.71mm、约0.59mm、约0.5mm、约0.47mm、约0.465mm、约0.437mm、约0.4mm、约0.355mm或约0.3mm。
应当理解,对于从生姜根获得的任何液体或半固体产物,该液体/半固体可以以这种形式使用,或者可以进行干燥或蒸发以获得用作如本文所述的抗菌组合物或药物组合物的粉末形式。以同样的方式,应当理解,对于从生姜根获得的任何固体产物,固体可以原样使用(例如,通过研磨、过筛或其他处理),或者可以重新悬浮以获得液体或半固体形式,以用作如本文所述的抗菌组合物或药物组合物。
组合物
本发明人已经发现,根据本文公开的方法由生姜根制备的姜油酮组合物具有显著的抗微生物特性,其可用于抑制或阻止微生物的生长,以及用于治疗或预防来自这些生物的感染。
本公开的组合物可以制备为以下的一种或多种:抗菌组合物或药物组合物。作为非限制性实例,组合物中姜油酮或姜油酮提取物的百分比可为约0.01%至约0.5%、或约0.02%至约0.2%、或约0.03%至约0.1%、或约0.04%至约0.09%、或约0.05%至约0.08%、或约0.06%至约0.07%、或至少约1%、至少约5%、至少约6%、至少约10%、至少约12%、至少约15%、至少约20%、至少约23%、至少约25%、或至少约30%的百分比,或约6.25%、约12.5%、或约25%的百分比,这些百分比代表液体组合物的v/v值或固体或者半固体组合物的w/w值。
例如,固体或半固体组合物可以包括约1至约100mg/g姜油酮、或约5至50mg/g姜油酮、或约5至约25mg/g姜油酮、或约5至约20mg/g姜油酮、或约5至约15mg/g姜油酮、或约10至约15mg/g姜油酮、或约10至约13mg/g姜油酮、或约12mg/g姜油酮(w/w)。类似地,液体组合物可以包括约1至约100mg/ml姜油酮、或约5至50mg/ml姜油酮、或约5至约25mg/ml姜油酮、或约5至约20mg/ml姜油酮、或约5至约15mg/ml姜油酮、或约10至约15mg/ml姜油酮、或约10至约13mg/ml姜油酮、或约12mg/ml姜油酮(w/v)。
在各个方面,可以制备抗菌组合物,例如:用于手部(例如,洗手液)、术前组织(例如,用于皮肤的手术准备)、粘膜(例如,用于膀胱、尿道或阴道感染的治疗,或医疗程序前这些腔体的清洁)、伤口或烧伤(例如,抗菌膏、绷带或敷料)、或口腔或咽喉(例如,漱口水或抗菌含片)。抗菌制剂及其制备在本领域是众所周知的。参见,例如,Antiseptic Prophylaxisand Therapy in Ocular Infections:Principles,Clinical Practice and InfectionControl,2002,Karger,Basel。
作为非限制性实例,抗菌组合物可包含以下的一种或多种:稀释剂(例如乙醇或其他醇)、润肤剂(例如PEG-45、棕榈仁甘油酯或肉豆蔻酸异丙酯)、湿润剂(例如甘油或甲基丙二醇)、载体(例如一种或多种油)、闭塞剂(例如矿物油或二甲基硅油)、其他调理剂(例如山嵛基三甲基铵甲基硫酸盐或聚季铵盐-7)和表面活性剂(例如温和的表面活性剂(例如两性基乙酸盐、羟乙基磺酸盐、磺基琥珀酸盐,特别是月桂酰两性基乙酸钠、椰油酰羟乙基磺酸钠、油酰氨基磺基琥珀酸二钠、十二烷基硫酸钠、C14-16烯基磺酸钠)。示例性油包括橄榄油、椰子油(例如椰子衍生的MCT油)、棕榈油(例如棕榈仁衍生的MCT油)、任何其他MCT油(中链甘油三酯油)及其任意组合。其他可能的载体包括卵磷脂(例如液体形式)和丙二醇。还注意到本文阐述的载体的任何组合。
在其他方面,药物组合物可以制备成各种给药途径,包括局部制剂或口服制剂。还包括为其他肠内或肠胃外给药途径制备的组合物。肠内制剂包括但不限于:口服、直肠、舌下、唇下和口腔的制剂。肠胃外制剂包括但不限于:鼻腔、眼内、阴道、病灶内、经皮和经粘膜的制剂。配制药物组合物的方法是本领域众所周知的。参见,例如,Remington:Essentialsof Pharmaceutics,2012,Pharmaceutical Press,London。
在特定方面,本公开的组合物可以制备成粉末或任何其他合适的剂型。局部制剂可以制备成例如气溶胶、香膏、乳膏、敷料、滴剂、乳剂、膜剂、泡沫、凝胶、液体、洗剂、面罩、油、软膏、糊剂、粉末、油膏、皂、喷雾剂、悬浮液、溶液、酊剂和蒸气。其他局部制剂包括绷带、敷料、贴剂、衬垫、海绵、条剂、带和本文提到的其他局部制剂。
如本文所述,组合物可以配制成半固体或液体组合物,例如用于口服给药,或者配制成用于肠内或肠胃外给药的溶液。或者,该组合物可以配制成粉末,用于封装、压片或者添加或掺入其他产品中。
口服制剂可以制备成例如饮剂(draught)、滴剂、酏剂、乳剂、液体、药糖剂(linctus)、溶液、喷雾剂、混悬液、糖浆、滋补剂,或者膜、凝胶、软糖、果冻、锭剂、块状物、糊剂、酱状物(puree)、渣状物(pomace)、粉末、丸剂或条状物。在其他方面,口服制剂可以制成片剂或胶囊,例如含有液体、半固体或固体内容物的片剂或胶囊。口服制剂可以小袋形式提供,例如粉末小袋或者凝胶或果冻小袋。还包括包含细条的口服制剂或包含胶囊中的固体以与食物或饮品混合的口服制剂。口服制剂可以作为注射器(shooter)或注射剂(shot)(通过口服)提供,例如液体注射剂、凝胶或果冻注射剂、糊状物注射剂或粉末注射剂。
特别包括延迟释放制剂、延长释放制剂以及快速崩解制剂。具体包括胶囊,例如凝胶胶囊,以及小袋和咀嚼片。此外,还包括组合制剂,其包括与其他有益药剂(例如一种或多种抗微生物剂)混合的本公开的粉末。如本文所述,其他制剂也是可能的。
为了快速起效或持续释放,可以改变口服制剂的溶出时间。口服制剂还可以包含缓释和速释的颗粒的混合物,以在相同剂量下产生快速和持续的吸收。特殊包衣可用于口服制剂,如片剂和胶囊,以给予对胃酸的抵抗力。口服制剂也可以涂有糖、清漆或蜡来改善味道。
因此,片剂可以制备成速溶片,胶囊可以制备成延长释放胶囊。片剂可以是刻痕片、咀嚼片、泡腾片、口腔崩解片或用于形成混悬液的片剂。胶囊可以是例如凝胶胶囊,并且可以包括粉末状内容物。这包括由单片凝胶封装和两片凝胶封装制成的凝胶胶囊。还包括非明胶胶囊以及囊片。
应当理解,某些制剂将适用于抗菌应用或药物应用。感兴趣的特定制剂是:眼部制剂(例如滴剂、软膏剂)、耳部制剂(例如滴剂、软膏剂)、鼻部制剂或呼吸道制剂(例如滴剂、喷雾剂、吹入组合物、吸入组合物、雾化组合物)、皮肤制剂(例如皂、喷雾、气溶胶、凝胶、糊剂、洗剂、乳膏剂、软膏剂、衬垫、贴剂、条带、绷带、敷料、海绵、蒸气)、咽喉或口腔制剂(例如滴剂、锭剂、漱口水、牙膏、喷雾、糊剂、凝胶)、粘膜制剂(例如喷雾、气溶胶、凝胶、糊剂、洗剂、乳膏剂、软膏剂、衬垫、敷料、海绵)。
固体和液体组合物可以将姜油酮或姜油酮提取物与一种或多种化合物组合以确保稳定且活性的组合物。例如,诸如片剂或胶囊的口服制剂可以包含:约5至约50%w/w的姜油酮或姜油酮提取物;至多约80%w/w的一种或多种填充剂、润滑剂、助流剂或粘合剂;和至多约10%w/w的化合物,以确保片剂在胃或肠中易于崩解、解聚和溶出。
因此,组合物可以包含各种赋形剂,例如以下的一种或多种:增溶剂、稳定剂、缓冲剂、张力调节剂、填充剂、增粘剂/降粘剂、表面活性剂、螯合剂、佐剂、抗粘剂、抗结块剂、粘合剂、包衣、崩解剂、润滑剂、助流剂、流动剂、吸附剂、矫味剂、着色剂、甜味剂或防腐剂。该组合物可包含小于1%的防腐剂,例如约0.005%至约0.5%,或约0.05%至约0.15%,或可包含约0.04%、约0.06%、约0.08%、约0.1%、约0.12%、约0.14%、约0.16%、约0.18%或约0.2%的防腐剂,这些百分比代表w/v值或w/w值。可用的防腐剂包括但不限于山梨酸、山梨酸钠、山梨酸钾、柠檬酸、抗坏血酸、苹果酸、酒石酸、丙酸和苯甲酸,例如其钠盐形式的苯甲酸,例如苯甲酸钠。
其他有用的赋形剂包括但不限于:硬脂酸甘油酯、硬脂酸镁和硬脂酸;糖类及其衍生物,例如二糖:蔗糖、乳糖;多糖及其衍生物,例如淀粉、纤维素或改性纤维素(如微晶纤维素)和纤维素醚(如羟丙基纤维素);糖醇,例如异麦芽酮糖醇(isomalt)、木糖醇、山梨醇和麦芽糖醇;蛋白质,例如明胶;合成聚合物,例如聚乙烯吡咯烷酮、聚乙二醇;脂肪酸、植物基表面活性剂;例如向日葵卵磷脂、蜡、虫胶、塑料和植物纤维(如玉米蛋白玉米醇溶蛋白);羟丙基甲基纤维素;交联聚合物,例如交联聚乙烯吡咯烷酮(交联聚维酮)和交联羧甲基纤维素钠(交联甲羧纤维素钠);羧基乙酸淀粉钠;二氧化硅、气相二氧化硅、滑石和碳酸镁。
液体组合物可以作为酊剂储存在小瓶、袋、安瓿、药筒或载药注射器中。组合物也可以从小瓶转移到更大的容器中并与其他材料混合。干燥或蒸发的组合物可以储存在小瓶、药筒、双腔注射器或预填充的混合系统中。在给药前,干形式的组合物可以在给药前重组为液体。
组合物的示例性单位剂量包含:约0.1mg至约1000mg姜油酮或姜油酮提取物、约1mg至约500mg姜油酮或姜油酮提取物、约1mg至约200mg姜油酮或姜油酮提取物、约1mg至约100mg姜油酮或姜油酮提取物。可以将剂量配制成每周给药一次、每周给药两次、每周给药三次、每隔一天给药一次、每天给药一次、每天给药两次或每天给药三次,或按需给药更多次。必要时,可针对儿童、老年人、超重者、体重不足者或其他患者调整剂量。剂量的改变可以根据已知的方法进行。欧洲食品安全局(EFSA)已根据128mg/kg/天的剂量将姜油酮归类为人类食用安全且无可见有害作用(NOAEL)(EFSA 2016;14(8):4557)。因此,应当理解,可以设想广泛的单位剂型。
使用组合物的方法
如上所述,所公开的组合物可用于减少微生物的流行和/或治疗或预防由这些微生物引起的各种健康状况。
在某些方面,所述组合物可包含通过本文所述方法产生的姜油酮或姜油酮提取物,或可基本上由其组成。本公开的组合物还可以配制用于以下的一种或多种:消毒、抗菌应用或治疗应用。另外,或作为其替代方案,该组合物还可以用作功能性食品或饮料、天然成分(例如天然添加剂)或天然补充剂(例如膳食补充剂)。
在各个方面,所公开的组合物可用于靶向一种或多种细菌、真菌或原生动物。特定真菌包括但不限于:烟曲霉(Aspergillus fumigatus)、黄曲霉(Aspergillus flavus)、白念珠菌(Candida albicans)、新型隐球菌(Cryptococcus neoformans)、格特隐球菌(Cryptococcus gattii)、荚膜组织胞浆菌(Histoplasma capsulatum)、耶氏肺孢菌(Pneumocystis jirovecii)、卡氏肺孢菌(Pneumocystis carinii)和黑葡萄穗霉菌(Stachybotryschartarum)。特别感兴趣的是耐药菌株。
特定原生动物包括但不限于:棘阿米巴(Acanthamoeba culbertsoni)、多噬棘阿米巴(Acanthamoeba polyphaga)、卡氏棘阿米巴(Acanthamoeba castellanii)、阿斯特罗尼棘阿米巴(Acanthamoeba astronyxis)、Acanthamoeba hatchetti、Acanthamoebagriffini、Acanthamoeba lugdenensis、多噬棘阿米巴(Acanthamoeba polyphaga)、Acanthamoeba rhysodes、狒狒巴拉姆希阿米巴(Balamuthia mandrillaris)、微小隐孢子虫(Cryptosporidium parvum)、溶组织内阿米巴(Entamoeba histolytica)、蓝氏贾第鞭毛虫(Giardia lamblia)、杜氏利什曼原虫(Leishmania donovani)、婴儿利什曼原虫(Leishmania infantum)、硕大利什曼(Leishmania major)、福氏耐格里阿米巴(Naegleriafowleri)、间日疟原虫(Plasmodium vivax)、三日疟原虫(Plasmodium malariae)、恶性疟原虫(Plasmodium falciparum)、卵形疟原虫(Plasmodium ovale)、诺氏疟原虫(Plasmodium knowlesi)、克氏锥虫(Trypanosomacruzi)、布氏冈比亚锥虫(Trypanosomabrucei gambiense)、布氏罗得西亚锥虫(Trypanosoma brucei rhodesiense)和刚地弓形体(Toxoplasma gondii)。特别感兴趣的是耐药菌株。
特定细菌包括但不限于:炭疽杆菌(Bacillus anthracis)、蜡样芽胞杆菌(Bacillus cereus)、汉赛巴尔通体(Bartonella henselae)、五日热巴尔通体(Bartonellaquintana)、百日咳杆菌(Bordetella pertussis)、伯氏疏螺旋体(Borreliaburgdorferi)、伽氏疏螺旋体(Borrelia garinii)、阿弗西尼疏螺旋体(Borreliaafzelii)、回归热螺旋体(Borrelia recurrentis)、牛布鲁氏杆菌(Brucella abortus)、犬种布鲁氏杆菌(Brucellacanis)、马耳他布鲁氏菌(Brucella melitensis)、猪布鲁氏菌(Brucella suis)、空肠弯曲菌(Campylobacter jejuni)、肺炎衣原体(Chlamydiapneumoniae)、沙眼衣原体(Chlamydia trachomatis)、鹦鹉热嗜衣原体(Chlamydophilapsittaci)、肉毒杆菌(Clostridium botulinum)、艰难梭菌(Clostridium difficile)、产气荚膜梭菌(Clostridium perfringens)、破伤风梭菌(Clostridium tetani)、白喉杆菌(Corynebacterium diphtheriae)、粪肠球菌(Enterococcus faecalis)、屎肠球菌(Enterococcus faecium)、大肠杆菌(Escherichia coli)、土拉热杆菌(Francisellatularensis)、流感嗜血杆菌(Haemophilus influenzae)、幽门螺旋杆菌(Helicobacter pylori)、嗜肺军团菌(Legionella pneumophila)、问号钩端螺旋体(Leptospira interrogans)、圣地罗西钩端螺旋体(Leptospira santarosai)、韦氏钩端螺旋体(Leptospira weilii)、野口钩端螺旋体(Leptospira noguchii)、李斯特菌(Listeriamonocytogenes)、麻风分枝杆菌(Mycobacterium leprae)、结核分枝杆菌(Mycobacteriumtuberculosis)、溃疡分枝杆菌(Mycobacterium ulcerans)、肺炎支原体(Mycoplasmapneumoniae)、奈瑟淋球菌(Neisseria gonorrhoeae)、脑膜炎奈瑟菌(Neisseriameningitidis)、铜绿假单胞菌(Pseudomonas aeruginosa)、立克次氏体(Rickettsia)、伤寒杆菌(Salmonella typhi)、鼠伤寒沙门氏菌(Salmonella typhimurium)、宋内志贺氏菌(Shigella sonnei)、金黄色葡萄球菌(Staphylococcus aureus)、表皮葡萄球菌(Staphylococcus epidermidis)、腐生葡萄球菌(Staphylococcus saprophyticus)、无乳链球菌(Streptococcus agalactiae)、肺炎链球菌(Streptococcus pneumoniae)、酿脓链球菌(Streptococcus pyogenes)、梅毒螺旋体(Treponema pallidum,)、解脲支原体(Ureaplasmaurealyticum)、霍乱弧菌(Vibrio cholerae)、鼠疫耶尔森氏菌(Yersiniapestis)、小肠结肠炎耶尔森菌(Yersinia enterocolitica)和假结核耶尔森菌(Yersiniapseudotuberculosis)。特别感兴趣的是耐药菌株,例如耐抗生素生物。
在特定方面,所公开的组合物可以与一种或多种抗微生物剂一起使用。例如,该组合物可以制备成与一种或多种抗微生物剂的组合制剂。或者,该组合物可以与一种或多种抗微生物剂一起作为分开的制剂使用。在使用分开的制剂的情况下(例如,姜油酮组合物和抗微生物剂),可以通过同时或依次应用/施用分开的制剂来协调使用。此外,本文所述的组合物可以与各种医疗或非医疗程序结合使用。组合物的使用可以在所述程序之前、期间或之后,或其任意组合进行。
作为示例,抗微生物剂包括但不限于:乙醇、异丙醇、戊二醛、甲醛、三氯卡班(triclocarbon)、苯酚、邻苯酚、氯酚、戊间甲酚、麝香草酚、甲酚、间苯二酚、氯二甲苯酚、三氯生、六氯酚、氯己定、普罗帕脒(propamidine)、次氯酸、氯胺、碘伏(iodophores)、碘、聚维酮碘、二溴巴比土酸(dibromin)、氯化汞、硫柳汞、硝酸银、磺胺嘧啶银、硫酸锌、氧化锌、过氧化氢、臭氧、过氧乙酸、西曲溴铵(cetrimide)、苯扎氯铵、龙胆紫、碱性品红、亚甲基蓝、吖啶黄、水杨酸凝集素(salactin)、红汞、硼酸、乙酸、壬二酸、硝基呋喃、环氧乙烷。
其他抗微生物剂包括天然产物,包括精油或植物提取物,例如来自金缕梅、啤酒花、百里香、牛至、金盏菊、茶树、薰衣草和茴香的精油或植物提取物,具体包括柠檬油、橙油、葡萄柚油、白柠檬油、橙花油、橘子油、香茅油、苦橙叶油、马郁兰油、迷迭香油、百里香油、麝香草酚、牛至油、罗勒油、丁香油、茶树油、杜松油、没药油、广藿香油、胡椒油、黑胡椒油、玫瑰油(例如,奥图玫瑰油)、甘松油、香根草油、马鞭草油、茴香油、柠檬草油、肉桂油、薰衣草油、天竺葵油、檀香油、桉树油、松木油、冷杉油、凤仙花油、雪松叶油、雪松木油、留兰香油、冬青油、薄荷油和薄荷醇。还包括蜂蜜(例如,麦卢卡蜂蜜)、活性炭、蓍草(例如,用于各种皮肤制剂)和紫草(例如,用于软膏剂或乳膏剂)。
还包括各种抗生素作为抗微生物剂,例如杆菌肽、头孢曲松、环丙沙星、克拉霉素、克林霉素、氯霉素、氨苯砜、地塞米松、氟氯西林、弗拉霉素、夫西地酸、庆大霉素、短杆菌肽、林可霉素、大环内酯、莫匹罗星、那氟沙星、新霉素、呋喃西林、多粘菌素B、瑞他莫林(retapamulin)、索夫霉素(soframycin)和磺胺嘧啶。其他抗生素包括,例如,氨苄青霉素、阿莫西林(例如,带有克拉维酸的阿莫西林)、阿莫西林克拉维酸盐(amoxicillinclavulanate)、阿奇霉素、头孢噻肟、头孢氨苄、环丙沙星、氯碘羟喹、双氯西林、多西环素、红霉素、氟米松、甲硝唑、萘夫西林、呋喃妥因(nitrofurantoin)、奥硝唑、苯唑西林、青霉素(例如,苄星青霉素、苯氧甲基青霉素、青霉素G钠、青霉素V钾、罗红霉素、磺胺甲恶唑、甲氧苄啶和万古霉素。其中值得注意的是糖肽类抗生素,例如达巴万星(dalbavancin)、奥利万星(oritavancin)、雷莫拉宁(ramoplanin)、替考拉宁(teicoplanin)、特拉万星(telavancin)和万古霉素。特别值得注意的是氨基糖苷类抗生素,如庆大霉素(例如,
如本文所述,本公开的组合物可用作抗微生物制剂。在特定方面,抗菌组合物可用于抑制或阻止微生物在某些组织上或某些组织中生长的方法中。这种组织包括:皮肤、指甲、耳、眼、鼻、口、牙龈、喉咙、阴道和尿道组织以及本文提到的其他组织。抗菌组合物可以用于例如烧伤,以减少感染的机会,或者在手术前用于皮肤,以对抗手术部位周围皮肤上的微生物。抗菌组合物可用作洗手剂(例如,皂或洗手液),可用水或无水使用。抗菌组合物可用于轻微的皮肤感染、割伤或擦伤。抗菌组合物可用作漱口剂(mouthwash)或含漱剂(gargle),例如以对抗口中或牙龈上的微生物。抗菌组合物也可以用作锭剂和咽喉喷雾剂,例如以缓解喉咙痛。抗菌滴眼剂或眼膏可用于对抗眼睛内或眼睛上的微生物。
如本文所述,本公开的组合物还可用作制剂,其可用于治疗或预防微生物感染或由感染引起的其他病况的方法中。感染可能影响一种或多种生理部分,包括以下的一个或多个部分:循环系统、呼吸系统、消化系统、肾脏系统、排泄系统、生殖系统、皮肤系统、神经系统、淋巴系统、内分泌系统、肌肉系统、骨骼系统和感觉系统。
如本文所述,各种施用途径可用于组合物,包括肠胃外(例如局部)和肠内(例如口服)给药。肠内给药可以通过十二指肠导管或胃管(包括鼻胃管)或其他已知方式进行。口服给药可以通过片剂、胶囊、小袋、滴剂、酏剂、药糖剂(linctus)、溶液、乳液、悬浮液、饮剂(draught)、酱状物、糊剂、渣状物、糖浆、凝胶、果冻、滋补剂或其他已知的方式进行。局部给药可以通过滴剂、喷雾剂、软膏剂、皂、衬垫、海绵、敷料、绷带或各种其他方式进行。不同的给药方式是本领域已知的,并且为技术人员可以使用。本文公开的组合物不限于特定的给药形式。
作为示例性剂量,对于平均70kg的人类个体,可以施用组合物以获得约1至5000mg剂量的姜油酮或姜油酮提取物,或者对于平均70kg的人类个体,获得约1至1500mg剂量的姜油酮或姜油酮提取物,或约5mg至约500mg剂量的姜油酮或姜油酮提取物,或约1mg至约500mg剂量的姜油酮或姜油酮提取物,或约1mg至约150mg剂量的姜油酮或姜油酮提取物,或约1mg至约100mg剂量的姜油酮或姜油酮提取物,或约1mg至约50mg剂量的姜油酮或姜油酮提取物,或约1mg至约30mg剂量的姜油酮或姜油酮提取物,或约1mg至约20mg剂量的姜油酮或姜油酮提取物,或约1mg至约15mg剂量的姜油酮或姜油酮提取物,或约1mg至约10mg剂量的姜油酮或姜油酮提取物。该剂量范围特别适用于干燥并研磨成粉末的生姜组分(例如姜油酮或姜油酮提取物)。上述剂量可以每天给药一次、每天给药两次、每天给药三次或者按需给药更少次或更多次。可以与食物一起服用,也可以在餐前服用。本领域技术人员可以容易地确定合适的剂量和剂型。
实施例
出于示例性说明具体实施方案的目的,提供本文所描述的实施例,其不旨在以任何方式限制本公开。
实施例1:姜油酮的制备
如图1所示的新鲜生姜的初始样品(400gm)来自新西兰,并清除了污物和泥土。然后将清洗过的生姜切成小块或切碎,并进行碱处理(800g的0.5%氢氧化钾的蒸馏水溶液)。搅拌所得混合物,并在60℃的烘箱中放置22小时。应当理解,也可以将所得混合物置于水浴中,并在约60℃下保持所需的时间。
然后通过加入浓柠檬酸将混合物的pH调节至pH 7,将经处理的植物材料铺展在金属托盘上,并在烘箱中在60℃下干燥20小时。所得干燥材料重35g,得到干产率为8.75%。然后将干燥的材料刮入烧瓶中,并用95%乙醇覆盖进行提取(210ml)。振荡烧瓶,并在烘箱中在40℃下放置16小时。使用带有玻璃棉塞的玻璃漏斗过滤出提取物(提取物1)。剩余的植物材料再次用95%乙醇提取(提取物2),然后用50%乙醇提取两次以上(提取物3和4)。
直接分析提取物中姜油酮的含量。还用2ml的乙醇对294mg切碎的新鲜生姜样品进行提取,并对该提取物进行分析。结果如表1所示。
表1.提取物组成
*提取物1和提取物2的干重通过干燥5ml份的每种提取物来估算。
结果
所提供的400g新鲜生姜根显示出含有260mg的6-姜酚(即0.65mg/g)。这将意味着从经处理的材料中得到的姜油酮的理论最大产量约为171mg(重量损失是由于姜油酮相对于6-姜酚的分子量较低而导致的)。大约50%的6-姜酚未转化。可以预见,进一步的研究可用于增加6-姜酚向姜油酮的碱性转化。
使用为了覆盖经处理的植物材料所需的最小体积进行乙醇提取。这意味着提取物1(最浓缩的提取物)的姜油酮含量为0.47mg/ml。可以预见,原则上可以使用多次浸泡方法或通过蒸发一些乙醇来增加该浓度。将乙醇体积减少80%将产生2.35mg姜油酮/mL的溶液。
预计完全干燥提取物将得到约16mg/g固体提取物的浓度。如果以更高的6-姜酚初始含量和/或更完全的转化开始,则可以预期更高的浓度。例如,通过将干燥的提取物直接配制到油或甘油载体中,以在一个或两个500mg的胶囊中提供所需的姜油酮剂量,从而可能达到理论上的25mg剂量。
大部分姜油酮在第一次提取中被提取出来。在某些情况下,两次提取会是有益的。第三次和第四次提取使总量略有增加。总的来说,乙醇提取作为制备方法被认为是非常有效的,并且是非常高效且廉价的。
实施例2:姜油酮的制备
概述:这些研究表明,对新鲜生姜进行水性碱处理随后进行冷冻干燥大大提高了转化率,使干燥生姜中姜油酮含量达到~1%。然后用超临界CO
干燥:将从斐济进口的新鲜生姜材料样品切成2-5mm的薄片,并放置在多孔烘箱托盘上的单层上。干燥在强制对流中进行。在中等温度(60℃)下进行干燥,目的是在不转化姜酚的情况下除去水分。当生姜的含水量达到7%时,这一过程就被认为完成了。将获得的干燥生姜冷藏储存,直到用于提取试验。
催化转化:通过用0.5% KOH(pH 14)、1% Ca(OH)
一旦选择了碱处理,就用立式切碎搅拌机(RobotCoupe R45)将5.2kg的新鲜生姜切碎。然后将生姜与3:1的液固比(体积:重量)的0.5%KOH(~0.1N)混合,得到pH~12.5。手动搅拌混合物,并将其置于60℃的烘箱中24小时。此后,通过添加浓柠檬酸(625g/L)将混合物中和至pH~7.2。然后将中和的混合物冷冻干燥,将在此过程中获得的生姜冷藏储存,直至用于提取试验。
催化转化结果:如前所述,测试了不同的碱:0.5%氢氧化钾或KOH(pH 14)、1%氢氧化钙或Ca(OH)
表2.经处理的样品中姜油酮和6-姜酚在280nm处的峰面积
将这种处理应用于更大的新鲜生姜样品(5.2kg),然后将得到的经处理的生姜中和并冷冻干燥。经冷冻干燥的生姜的产率为17%,即每100g切碎的原始生姜中有17g经处理的冻干的生姜。测得经冷冻干燥的生姜的姜油酮和6-姜酚的含量分别为10.2和3.3mg/g(干基)。见表2-1。姜油酮的含量至少比烘干的生姜的姜油酮的含量高10倍。
表2-1:经处理和冷冻干燥的生姜的组成
提取:使用经碱处理的生姜进行超临界萃取试验。将经碱处理的冷冻干燥的生姜用手轻轻碾碎,将其放入两端带有烧结滤盘的2L提取容器中,将容器完全装满。如上所述进行提取,直到观察到提取速率急剧下降,对应于CO
表3.提取参数总结
分析:根据需要,通过在中和后添加甲醇来制备用于分析的样品。将提取物直接溶解在甲醇中。用乙腈/0.1%甲酸梯度通过HPLC进行分析。在280nm下进行检测,使用的色谱柱为Phenomenex KinetexC18(150X 2.1mm)。姜油酮在约2分钟时洗脱,6-姜酚在5.2分钟时洗脱。姜油酮和6-姜酚的定量根据使用这些化合物的分析标准品制备的标准曲线中获得。
提取结果:如上所述,经碱处理并随后冷冻干燥的生姜用CO
表4.从经碱处理的生姜中获得的提取物的组成
表5.经碱处理的生姜的提取的姜油酮(Z)质量平衡
从结果可以看出,对于经碱处理的样品,CO
在另一个实验中,将从未经处理的生姜根中获得的CO
在另一个实验中,将未处理生姜的CO
样品1和样品2的这些值均低于采用早期处理获得的那些值,对于早期处理的姜油酮含量估计为150mg/g。在该工作中,树脂样品2已从水中分离出来并进行分析。随后,还对分离出的水进行了分析,并估计了每3g批次中还含有50-55mg(约25%)的姜油酮。据报道,姜油酮具有非常有限的水溶性,因此该结果非常出乎意料。因为看起来显著部分的姜油酮停留在水中而没有与树脂一起分离出来,所以这种方法与向粗制的中和产物中直接加入醇形成对比。
因为水能够从树脂中提取一些姜油酮,所以在通过干燥全部中和的碱处理产物进行处理后,也可能产生高产率的姜油酮。鉴于发现经碱处理后姜油酮似乎比先前报道的更易溶于水,将进行进一步的工艺优化以提高产率。
实施例3:进一步的反应方法和比较
概述:姜油酮并非天然存在于生姜中,而是由姜酚经过处理过程转化而来的产物。在这些研究中,从萨摩亚获得了经碱处理且干燥的生姜样品,并使用两组不同的提取条件用乙醇进行提取:在40℃下提取20小时(提取物A)和在室温下提取7天(提取物B)。结果发现,提取物A的所得的姜油酮浓度为41.4mg/g,提取物B的所得的姜油酮浓度为43.8mg/g。
提取A:将由SROS(萨摩亚科学研究组织)生产的经处理的生姜装在两个单独的塑料袋中。将两个袋子中的内容物合并,在-80℃下冷冻,随后使用带有2mm筛网的刀磨机(Wiley)进行研磨。然后将经研磨的材料(782.3g)与食品级乙醇以大约5:1的重量比一起放入圆底烧瓶中。然后将烧瓶置于40℃水浴中并以5rpm搅拌过夜(总提取时间为20h)。此后,在真空下过滤混合物,并在真空下通过旋转蒸发除去乙醇,以产生43.8g的具有特征性生姜香味的高粘性深棕色树脂。提取产率为5.6%。取出10g的该树脂(提取物A)并在氮气冲洗下冷藏储存,用于将来可能的生物测定。
提取B:如上所述,将生姜冷冻并研磨。将经研磨的材料(785.9g)与食品级乙醇以大约5:1的重量比一起放入桶中。将生姜在室温(22-29℃)下在乙醇中浸渍7天。在第1天、第3天和第7天取样。7天后,在真空下过滤混合物,并在真空下通过旋转蒸发除去乙醇,产生49.3g的具有特征性生姜香味的高粘性深棕色树脂(图1),非常类似于在提取A中获得的树脂。取出10g的该树脂(提取物B)并在氮气冲洗下冷藏储存,用于将来可能的生物测定。提取产率为6.3%。
姜油酮和醛分析:通过HPLC对起始材料(即经处理的姜)和最终的两种树脂以及提取B的第1天、第3天和第7天的样品中的姜油酮进行定量(注意,第7天的液体样品等同于最终的树脂样品)。HPLC定量方法包括在分析前加入甲醇并研磨样品。所有部分的姜油酮含量如表6所示。姜油酮的质量平衡和产率如表7所示。
表6.比较提取条件-不同部分的姜油酮含量
表7.姜油酮的质量平衡和产率
如上所述,提取物A是通过在40度下处理20小时获得的,而提取物B是通过在室温下处理7天获得的。表6和表7的结果表明,通过在室温下进行较长时间的处理获得较高水平的姜油酮,尽管通过将温度升高至40℃也可以获得高产率。
为了测定原料中的姜油酮含量,首先将其提取到合适的溶剂中。在一个方法中,用乙醇进行该提取,导致较低的姜油酮含量(1.44mg/g)。在第二方法中,使用甲醇进行该提取并在研钵和杵中研磨生姜与溶剂。这导致了更高的姜油酮含量(3.1mg/g)。作为参考,萨摩亚实验室报告的该材料的姜油酮含量为1.86mg/g。
基于此,提取A的姜油酮产率(即提取物中的姜油酮相对于进料中的姜油酮的量)估计为75%,并且提取B的姜油酮产率估计为89%。当测定姜油酮含量时,观察到HPLC分析中的6-姜酚峰始终为姜油酮峰面积的约1/8。这表明提取对姜油酮与姜酚的比例几乎没有影响。
将两种最终树脂的样品溶解在乙醇中,通过GCMS进行检查以用于醛分析。发现己醛水平非常低(太低而无法量化)。己醛是形成姜油酮的反应的副产物,但具有一定的挥发性。通过质谱数据的库匹配和己醛标准品的单独进样确认了己醛峰的身份。
讨论
本文所述研究中的每一项研究均可有效产生姜油酮。表8中提供了来自实施例2和实施例3的结果的比较。
表8.姜油酮产率的比较
Li等人获得了新鲜生姜和干燥生姜的相似值。参见Li等人2016年的“Chemicalcharacterization and antioxidant activities comparison in fresh,dried,stir-frying and carbonized ginger”J Chromatogr BAnalyt.Technol.Biomed.LifeSci.1011:223-32。如上所述,实施例2利用了逆羟醛反应。如上直接所述,实施例3利用了温度、pH调节和提取。
关于萨摩亚生姜,需要注意的是生姜没有在要求的时间(在地里9个月)收获,这影响了生姜中存在的姜酚的水平,进而影响了最终产物中姜油酮的含量。因此,预期可以获得进一步的收益。关于斐济生姜,与萨摩亚生姜相比,其姜油酮的含量明显更高(10.2:1.44=7.08x高)。这意味着如果应用实施例3的实验条件,斐济生姜的总产量可以推测为310mg/g。即:43.8mg/g(实施例3中从萨摩亚生姜中获得的量)x7.08(斐济生姜中较高的起始含量)=310mg/g。
实施例2中的表5显示了经pH处理的生姜随后进行CO
实施例4:使用榨汁和碱处理的处理方法
概述:对生姜根进行机械榨汁,并测定汁液和残余固体中6-姜酚的水平。大多数6-姜酚存在于汁液中。用碱处理汁液,显示在60℃下所有的6-姜酚在5-6小时内有效地转化为姜油酮。
关于榨汁的概述:将新鲜生姜(500至1000g)通过混合/浸渍和压榨生姜进行预处理。保留液体部分,对渣进一步用温水(4份水比1份生姜)在55-60℃下洗涤10-15分钟。这是在有盖的容器中完成的。然后再次进行压榨。分析每个部分的6-姜酚含量(总共5次分析),即:1)处理前立即取样的新鲜生姜样品;2)初始混合/浸渍后的液体部分;3)初始混合/浸渍后的生姜渣;4)进一步洗涤初始渣后收集的第二液体部分;5)如上所述洗涤并压榨后的最终生姜渣。在最终压榨后(即上述的样品3)和5)),对每批生姜渣进行含水量读取。
关于碱处理的概述:对液体部分进行碱处理,以实现向姜油酮的转化。在一系列时间点取样并分析姜油酮含量。将样品用KOH(如前所述为5%)进行小规模处理。在室温、30℃和60℃下使用1ml样品在1、2、3和5小时时进行处理。此外,一个样品在60℃下处理24小时。对多达15个样品进行分析。
榨汁方法:获得了两个新鲜生姜根样品,一个是本地的(有机的,来自Petone的Evithe),另一个从奥克兰的Phil Rasmussen获得。两个样品似乎都比普通超市的生姜根更饱满/多汁。含水量通过将每个根切成约10g的薄片,用液态空气冷冻,然后进行冷冻干燥来测定。用甲醇进行根的提取来测定6-姜酚含量。为此,将约5g的每个样品切成4-5块,并使用小型厨房大蒜压榨机破碎。破碎的根和汁液用甲醇(2×15ml)在60℃下提取20分钟。随后进行HPLC分析,并在280nm处检测。结果如下表9所示。
表9.生姜的含水量
选择奥克兰样品进行榨汁工作。为此,使用家用榨汁机处理635g生姜根。这包括带有网状汁液过滤器和可调固体喷嘴的旋转螺杆驱动器(见图4A-4B)。榨汁机去除了516.3g(81%)的液体(汁液1,J1),收集了101.5g的固体(渣1,M1)。取出一些干燥固体用于分析,并用360ml的热自来水提取了90.5g。将其静置15分钟,然后将该材料放入榨汁机中。从该步骤中,回收了350g的汁液(汁液2,J2)和70.2g的固体(渣2,M2)。
将这两种液体冷藏过夜。两者都是浑浊的,有固体沉淀。将这些样品在分析或处理前摇匀。通过将样品与乙醇混合(1:1)、离心并直接注射上清液来分析汁液样品的6-姜酚含量。两种经压榨的固体M1和M2的固体含量分别为37%和26.3%。
结果如下表10所示。姜酚值乘以重量,得到每种材料中姜酚的总量。发现汁液含有81.6%的测得的姜酚。计算出的进料的总姜酚低于回收量,表明从根中提取了部分姜酚。姜酚的百分比是基于渣和汁液中姜酚的总测量值(而不是进料测量值)。
表10.重量和姜酚含量
/>
碱处理:该工作是在榨汁过程中回收的第一汁液(J1)上进行的(如上)。将汁液样品(在振荡以混悬所有固体后)在室温、30℃或60℃下与KOH反应1小时、2小时、3小时、5小时,还有在60℃下反应24小时。还试验了三种浓度的KOH:0.5%、1.0%和2.0%。制备2N KOH溶液(5.6g KOH在50ml水中)。为了在每个样品中产生0.5%、1%和2%的KOH浓度,将0.25ml、0.5ml或1ml的2N KOH加入5.5ml汁液中并振荡。然后将样品置于RT(实验室)、30℃(水浴)或60℃(干燥烘箱)下。通过从每个样品中取出200μl,加入200μl的1N HCl,然后加入500μl的乙醇完成用于HPLC分析的取样。离心后,将样品直接注入HPLC。比较了姜油酮和姜酚的峰面积(见下文)。
这些结果表明,用2% KOH处理能够在5小时内实现完全转化为姜油酮。参见图5C。60℃下的孵育特别有利。参见图5C。结果以姜油酮(Z)和姜酚(G)的峰面积表示。注意到经KOH处理的样品有固体存在,其沉淀在试管中。为了进行分析,振荡试管,并用宽口吸头取样以避免堵塞。
实施例5:使用榨汁和碱处理的附加处理方法
概述:目的是产生具有通过碱催化的逆羟醛反应将6-姜酚转化为姜油酮的来自生姜的提取物。目前的工艺寻求减少处理时间和用水量。该工艺在大约40kg的规模上进行了试验,然后将以200kg的规模进行进一步生产。
简而言之,接收新鲜生姜,先用碱处理,然后冷冻干燥,以产生经处理的生姜粉。该粉末在室温下用乙醇提取3天,在24小时、48小时和72小时时取样以评估该提取的进展。实施例6中详细描述了乙醇提取。
方法论:对进口的新鲜生姜进行了碱预处理和干燥。为此,将新鲜生姜(36.67kg)在Vincent Corporation CP-4螺旋压榨机中压榨以制成两股料流:生姜汁和渣。螺旋压榨机的设置是VSD速度为50%,锥形气压为2巴。将经初始压榨的渣第二次压榨以除去任何残留的汁液。
将两份汁液合并。将汁液加热至60℃,加入KOH至最终浓度为2%w/w。碱化的汁液在60℃下保持5小时,以将姜酚转化为姜油酮。通过加入无水柠檬酸将汁液中和至pH 7.2。对现在含有姜油酮的汁液进行冷冻干燥并研磨。
样品取自:新鲜生姜(ZINGO);两份渣(GMARC和GMARC2);加入KOH之前的汁液(GKOH0);处理2小时、3小时和5小时后的汁液(GKOH2、GKOH3、GKOH5);最终的干燥提取物(GPE)。
此外,GMARC2的样品用热水进行如下提取。将水以5:1w:w的比率加入到GMARC2中。将混合物加热至60℃并在此温度下保持15分钟。采用与上述相同的设置,通过螺旋压榨将提取物与固体分离。样品取自:提取物(GMARC2 HWEX);渣(HW MARC)。通过HPLC分析每个样品的总固体(LOD,16小时100℃)和姜酚或姜油酮的含量。
样品分析:使用HPLC在280nm处用UV检测进行分析。样品制备如下:(1)液体样品(例如汁液)用乙醇进行1:1稀释并离心。含有碱的过程中液体样品用1N HCl和乙醇进行1:1:1稀释;(2)通过用乙醇进行两次提取(超声波处理、在60℃下加热20分钟、涡旋并离心)并合并上清液来提取固体样品(例如原始生姜或生姜渣)。固体提取物(约5g)通常制成50mL用于分析。将原始新鲜生姜粗略切碎,然后使用
压榨:收到36.67kg的原始斐济生姜并压榨。压榨是有效的,产生大量浅绿色汁液和纤维状渣。从第一次压榨中回收了28.92kg的汁液。然后将6.6kg的渣进行第二次压榨以回收额外的2.18kg的汁液。汁液的总产量为31.1kg,按质量计相当于进料原始生姜的86%。最终回收的渣质量为4.05kg。在一次运行结束时,螺旋压榨机中通常有1-2kg的滞留量。这使得进料质量与渣和汁液的合并质量之间存在微小差异。
热水提取:将3.62kg的GMARC2和18.1kg的水加热至60℃,然后在60℃下提取15分钟后通过螺旋压榨进行分离。然后,压榨21.18kg的混合物。注意到在提取过程中约有500g的水由于蒸发而损失。从中回收了17.62kg的提取物,并进行二次取样分析。此外,回收了2.69kg的渣。
碱处理:为此,将1.236kg的50% KOH溶液添加到31.1kg的生姜汁中,以达到2%的目标KOH浓度。加入KOH后的pH为12.18。加入KOH后,汁液的颜色由浅绿色变为红棕色。将汁液在60℃下保持5小时,然后通过加入500g无水柠檬酸进行中和。添加柠檬酸后的pH为7.23。
冷冻干燥:将经处理的汁液转移到冷冻干燥机托盘中并冷冻过夜,然后转移到Cuddon FD80冷冻干燥机中。将总共28.51kg的汁液装载到托盘上并干燥。由于人工处理,冷冻干燥前损失了约3kg的汁液。干燥后,收集到2.86kg的干燥提取物-总计干燥了汁液质量的10%。将其研磨并作二次取样。在研磨、作二次取样和处理损失后,总共将2.19kg装入箔袋储存,直至进一步处理。其中约1.6kg被送去进行乙醇提取(见实施例6)。
质量平衡总结如下所示。
榨汁
碱处理
冷冻干燥
如上所述测量姜酚和姜油酮的水平。结果如下表11所示。
表11.姜酚和姜油酮水平
该表示出了预处理和处理过程中不同部分的姜酚含量。根据这些测量,在36.67kg的原始生姜进料中总共有19.1g的6-姜酚。干燥的生姜提取物(GPE)的姜油酮含量为5.7mg/g。因此,2.86kg的干燥粉末中的姜油酮总量(损失和研磨损失前)为16.30g。转化前汁液(GKOH-0)中姜酚的浓度为6.9mg/g(以干基计)。当转换回湿基时,使用6.67%的固体浓度(在添加KOH和无水柠檬酸将总固体含量增加到约10%之前),汁液中的总姜酚为14.32g。6-姜酚的GKOH-2、-3、-5值有待确认。
在汁液中的姜酚和最终粉末提取物中的姜油酮之间的质量平衡并不精确地一致。这可能归因于测量值的变化。从总质量平衡计算来看,渣的数量似乎有所提高。当用热水提取渣时,提取物中的6-姜酚含量为0.22mg/g,对应于该提取物中总共有5.7g的6-姜酚,约占进料中的6-姜酚的25%。对于水提取,这总共需要18kg的水。这反过来会增加KOH和柠檬酸的质量,并使干燥负荷增加58%。因此,在某些情况下,可能需要省略水提取。
值得注意的是,这些实验表明实现了最终产物中的6-姜酚(以姜油酮的形式)的几乎全部回收。在转化反应过程中采集的样品-GKOH2、GKOH3和GKOH5-显示从6-姜酚到姜油酮的转化发生在处理的前两个小时,在处理的2小时后采集的样品中的姜油酮水平没有显著增加。考虑到转化似乎在2小时后完成,这一孵育时间(或甚至更短的孵育时间)将是足够的。
得出的结论是,包括先压榨然后在汁液相中用KOH处理的加工方法是有效的生产方法。进一步的实验将使用多于200kg的生姜作为原料。该批次中的6-姜酚水平为1.1mg/g,预期这将反映在相应的姜油酮水平中。
实施例6:乙醇提取工艺及分析
概述:接收新鲜生姜,先用碱处理,然后冷冻干燥,以产生经处理的生姜粉(见上文实施例5)。该粉末在室温下用乙醇提取3天,在24小时、48小时和72小时时取样以评估提取过程。
方法论:如上产生的经处理的生姜(实施例5)冷藏储存直至使用。在室温下,用XNS食品级乙醇提取约一半的接收的生姜。将经处理的生姜与乙醇(使用生姜与乙醇的重量比为1∶5)一起放入配备有顶部不锈钢搅拌器的10L玻璃容器中。将混合物搅拌72小时,搅拌速度足以使固体不沉积在底部。
经过24小时后,关闭搅拌器,使固体沉降10分钟,然后从顶部取出50ml样品。又经过24小时后,用同样的程序取出第二样品。经过总共72小时后,停止搅拌,用滤纸在真空下过滤混合物。从滤饼中取样,从滤液中取出代表72小时的最终酊剂样品。剩余的滤液标记为ZINGOEE。取样~300ml的ZINGOEE样品,冷藏储存在玻璃瓶中。在进一步的步骤中,蒸发所有ZINGOEE以产生43.5g的总树脂体积,其值为88.9mg/g姜油酮。
使用在50毫巴和40℃下操作的Buchi R220SE旋转蒸发器在真空下蒸发剩余的乙醇酊剂,直到达到体积减少约31倍。然后对所得的浓缩提取物(ZINGOCE)进行分析,一旦确认了姜油酮的含量,就通过用食品级乙醇将其稀释,使用少量的该浓缩提取物样品产生每克含有~12mg姜油酮的标准化酊剂。这种标准化酊剂的两个单独样品被送至SCU(澳大利亚)进行分析,第三个样品留在现场进行姜油酮分析。
结果:方法和结果如图7所示。对于这些实验,801.5g的收到的经处理的生姜与4007.3g的食品级乙醇一起用于乙醇提取。在室温(16-20℃)下搅拌72小时后,过滤混合物,获得3556.7g的澄清棕色的芳香乙醇酊剂[ZINGOEE],以及1033.4g的滤饼(即,废生姜固体)。大约140g的乙醇在提取过程中因蒸发而损失。产生的乙醇酊剂的总重量为3631.7g,其中包括在24小时和48小时时采集的样品
通过HPLC对原料(即经处理的姜,GPE)和室温下在乙醇提取24、48和72小时后的样品中的姜油酮进行定量。还分析了废生姜固体(即过滤过程中产生的滤饼)。所有部分的姜油酮含量如表12所示。HPLC结果显示三次提取时间之间的差异很小,表明24小时足以进行提取。
表12.样品的姜油酮含量(mg/g)
滤液[ZINGOEE]的姜油酮浓度为1.1mg/g,即液体中存在3.88g姜油酮,或85%的起始姜油酮,表明合理的回收。滤饼中的姜油酮浓度为0.61mg/g,即滤饼中存在0.63g的姜油酮。然而,注意到滤饼仍然具有一定量的乙醇溶液。在今后的加工中,可以用干净的乙醇洗涤滤饼,以尽可能多地冲洗出提取物。
乙醇提取方法的姜油酮质量平衡为98.5%。这是基于提取物中的3.88g,加上滤饼中的0.63g,除以进料中的4.58g。经测定,室温提取提供了有利的姜油酮回收。升高提取温度可能会导致较高的姜油酮回收,但室温提取显然是有效的。
在取出~300ml ZINGOEE样品后,将剩余的提取物(3249g)在真空下蒸发,以产生104.9g的浓缩提取物[ZINGOCE],其中姜油酮含量为33mg/g(3.46g的姜油酮)。该浓缩提取物的总固体含量为37.1%(以110℃下干燥时的损耗量测量),这表明如果除去所有乙醇,则可以实现的最终的油树脂重量将为38.9g。如果将该数字推算为所产生的ZINGOEE的总量,则所得的该方法的提取产率约为5.4%。通过将25.5g的ZINGOCE与44.5g的食品级乙醇混合来制备含有12mg/g的生姜油酮的标准化酊剂。该酊剂的样品被送去做进一步检测。
此外,进一步分析表明,最终产物中不存在醛。参见图8A-8B。为了进行这些评估,使用GCMS分析经处理的生姜的乙醇提取物样品中醛类的存在。如果存在,则预计将(主要)是衍生自6-姜酚的己醛。预计粉末制剂(如上述实施例4和实施例5中的预提取粉末)也不含醛。接下来的步骤将包括蒸发乙醇酊剂以产生浓稠的乙醇糊剂。
结论:所提出的方法包括螺旋压榨,然后在汁液相中进行KOH处理,用柠檬酸中和,然后冷冻干燥,该方法被证明非常有效,实现了汁液相中的6-姜酚的几乎全部回收,在60℃下用2% KOH处理5小时后,6-姜酚全部转化为姜油酮。经过预处理的干燥粉末目前含有5.32mg/g姜油酮,比以前的制造技术至少提高了两倍。
室温下24小时的乙醇提取是实现至少85%的姜油酮回收率的可选步骤。提取后用新鲜乙醇洗涤固体可进一步提高回收率。在这些方法中,蒸发乙醇提取物[ZINGOEE]以实现显著的体积减少,然后用新鲜乙醇重组浓缩提取物[ZINGOCE]以产生含有目标剂量为12mg/g姜油酮的标准化酊剂。
对于提取方法,总的Z质量平衡(出/入)为98.5%。滤液(ZINGOEE)中的姜油酮含量为1.1mg/g,浓缩提取物(ZINGOCE)中的姜油酮含量为33mg/g。该方法以33mg/g产生104.9g的ZINGOCE,剩余3.46g姜油酮。该数值低于ZINGOCE中的3.88g,因为~400g的ZINGOCE在蒸发前被去除(用于测试,加上~300mL保留样品)。考虑到这一点,计算结果非常吻合。蒸发前的总姜油酮质量平衡被计算为98.5%(=(0.63+3.88)/4.58)。
该工作中获得的结果表明,6-姜酚含量为0.5mg/g的100kg的新鲜生姜将产生3.6kg的姜油酮含量为12mg/g的标准化酊剂。
实施例7:姜油酮和抗微生物剂的组合
庆大霉素是氨基糖苷类抗生素,用于治疗严重的革兰氏阴性菌感染。它有多种剂型可供选择,包括可注射溶液、静脉内制剂和口服制剂。侵袭性金黄色葡萄球菌细菌通常对采用庆大霉素的抗生素单一疗法产生耐药性。数种金黄色葡萄球菌菌株通过表达介导庆大霉素细菌耐药性的抗生素修饰酶对庆大霉素和其他氨基糖苷类产生耐药性。
万古霉素是糖肽类抗生素,是治疗成人、儿童和新生儿的革兰氏阳性感染最广泛使用的糖肽类抗生素。它有多种剂型可供选择,包括口服(例如胶囊或溶液)和静脉注射。然而,耐万古霉素的肠球菌已经出现,使治疗更加困难。屎肠球菌(E.faecium)是获得万古霉素耐药性的最常见菌株。肠球菌中对糖肽(例如万古霉素)耐药性的主要机制涉及肽聚糖合成途径的改变,特别是D-丙氨酸-D-丙氨酸(D-Ala-D-Ala)替代为D-丙氨酸-D-乳酸(D-Ala-D-Lac)或D-丙氨酸-D-丝氨酸(D-Ala-D-Ser)。
棋盘格分析用于确定与每种单个化合物相比,化合物是否可以组合以降低金黄色葡萄球菌的MIC。在本实验中,测试了姜油酮加庆大霉素、姜油酮加万古霉素和姜油酮加头孢噻肟的组合。在该测试中,将96孔板接种金黄色葡萄球菌,然后在37℃下与测试化合物一起孵育24小时。对于姜油酮,添加量为0、0.78、1.56、3.125、6.26、12.5和25mg/ml。对于庆大霉素,添加量为0、4、8、16、32、64、128和256μg/ml。对于万古霉素,添加量为0、4、8、16、32、64、128和256μg/ml。对于头孢噻肟,添加量为0、8、16、32、64、128、256和512μg/ml。将MRSA细胞(耐甲氧西林的金黄色葡萄球菌)引入含有2%NaCl的Mueller Hinton培养基中。使用10
表13.用于对抗金黄色葡萄球菌的单个化合物的最低抑制浓度
表14.庆大霉素和姜油酮的组合降低了对金黄色葡萄球菌的MIC
表15.万古霉素和姜油酮的组合降低了对金黄色葡萄球菌的MIC
表16.头孢噻肟和姜油酮的组合用于对抗金黄色葡萄球菌
从这些结果可以确定,与单独添加的庆大霉素、万古霉素和姜油酮相比,庆大霉素联合姜油酮和万古霉素联合姜油酮降低了对金黄色葡萄球菌的MIC(见图9A-9B)。对于姜油酮和庆大霉素的组合,该活性是协同增效的:FICI=0.5=(MIC
庆大霉素和万古霉素分别是氨基糖苷类抗生素和糖肽类抗生素的代表。姜油酮和庆大霉素的组合(协同增效活性)以及姜油酮和万古霉素的组合(显著增加/接近协同增效作用)的抑制活性的有利增加提供了用于对抗感染的有价值的工具,特别是用于对抗耐抗生素菌株,包括金黄色葡萄球菌的耐抗生素菌株。这种联合治疗提供了增加的效力和降低的耐药性的可能性,并且作为治疗方式是极其有益的。
普通技术人员可以利用本文的公开和教导来产生其他实施方案和变化,而无需过度的实验。所有这些实施方案和变化都被认为是本公开的一部分。
因此,本领域普通技术人员将从本公开中容易地理解,根据这样的相关实施方案,可以利用实施与本文描述的实施方案基本相同的功能或实现与本文描述的实施方案基本相同的结果的后续修改、替换和/或变化。因此,本公开旨在在其范围内涵盖对本文公开的工艺、制造、物质组成、化合物、手段、方法和/或步骤的修改、替换和变化。
本文的描述可能包含超出所要求保护的发明范围的主题。包含该主题是为了帮助理解本发明。
在本说明书中,参考了外部信息源,包括专利说明书和其他文件,这通常是出于提供讨论本公开特征的背景的目的。除非另有说明,否则在任何司法管辖区内,对这种信息源的引用都不应被解释为承认这种信息源是现有技术或构成本领域公知常识的一部分。
- 用于制备聚酮化合物的催化剂组合物、钯混合催化剂体系、利用其的聚酮化合物制备方法及聚酮聚合物
- 甘草水提取物、包含其的组合物及其制备方法和用途
- 小茴香水提取物、包含其的组合物及其制备方法和用途
- 包含具有可交换交联点的交联有机硅的聚合物组合物、制备方法和用途
- 一种包含左卡尼汀的药用组合物及其制备方法和用途
- 一类基于喹诺酮的化合物、其制备方法、包含其的药物组合物及其用途
- 一种包含非瑟酮的药物组合物、其制备方法及用途
