有机电致发光化合物及包含其的有机电致发光装置
文献发布时间:2023-06-19 11:21:00
技术领域
本公开涉及一种有机电致发光化合物以及一种包含其的有机电致发光装置。
背景技术
电致发光(EL)装置是自发光装置,它的优点在于它提供更宽的视角、更大的对比率和更快的响应时间。有机EL装置首先是由伊士曼柯达公司(Eastman Kodak)于1987年通过使用小的芳香族二胺分子和铝络合物作为用于形成发光层的材料而开发的[Appl.Phys.Lett.[应用物理学快报]51,913,1987]。
有机电致发光装置(OLED)通过向有机发光材料施加电力而将电能转换为光,并且通常包括阳极、阴极和在这两个电极之间形成的有机层。OLED的有机层可以包含空穴注入层、空穴传输层、空穴辅助层、发光辅助层、电子阻挡层、发光层(含有主体和掺杂剂材料)、电子缓冲层、空穴阻挡层、电子传输层、电子注入层等。有机层中使用的材料可以根据功能分为空穴注入材料、空穴传输材料、空穴辅助材料、发光辅助材料、电子阻挡材料、发光材料、电子缓冲材料、空穴阻挡材料、电子传输材料、电子注入材料等。在OLED中,由于施加电压,将空穴从阳极注入发光层,将电子从阴极注入发光层,并且高能量的激子是通过空穴和电子的再结合而形成。通过此能量,有机发光化合物达到激发态,并且通过从由于所述激发态的有机发光化合物恢复到基态的能量发射光而发生发光。
最近,根据显示器的较大面积,需要可以展现出更精美且鲜艳的颜色的发光材料。具体地,在发射蓝光的材料的情况下,材料如ADN和DPVBi用作主体材料,并且材料如基于芳香族胺的化合物、铜酞菁化合物、基于咔唑的衍生物、基于苝的衍生物、基于香豆素的衍生物和基于芘的衍生物用作掺杂剂材料。然而,这些材料难以获得具有高颜色纯度的深蓝色,并且由于随着波长变得更短具有更短的发光寿命是有问题的。
因此,在实现全色显示器方面,需要开发具有长寿命的深蓝色的发光材料和具有与发射蓝光的材料相匹配的能级的其他有机材料。
美国专利号8,759,818和美国专利申请公开号2014/0001459公开了包含蒽部分的有机电致发光化合物,其中一些氢原子被氘取代。然而,这些参考文献未具体公开包含蒽部分的有机电致发光化合物,其中一些氢原子被氘取代,并且其中二苯并呋喃在一定位置被取代。
发明内容
技术问题
本公开的目的首先是提供一种有机电致发光化合物,其对于生产具有优异的寿命特征的有机电致发光装置是有效的;并且其次是提供一种包含所述有机电致发光化合物的有机电致发光装置。
问题的解决方案
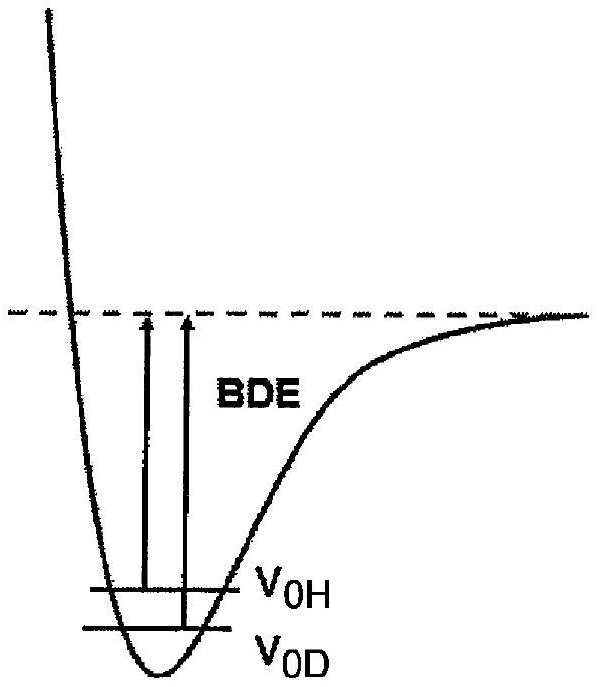
在有机电致发光装置中,重要的是改善发射蓝光材料或发射蓝光装置。然而,从开发有机电致发光装置的时间开始,在使用具有蒽的主要部分的化合物作为蓝色主体材料方面就没有改变。因此,在改善发射蓝光材料或发射蓝光装置的寿命特征方面存在限制。为了改善寿命特征,可以增加包含在蓝色主体材料中的蒽化合物的稳定性。方法之一是氘化。当氘化蒽化合物时,可以降低化合物的零点振动能,从而增加化合物的键离解能(BDE)。因此,可以增加蒽化合物的稳定性。图1是示出由于氘化引起的键离解能增加的图。具体地,本发明的诸位发明人发现,当氘化具有下式1的特定结构的有机电致发光化合物时,与具有其他结构的蒽化合物相比,产生寿命的更显著的改善。通过将杂芳基而不是芳基键合至蒽核,可以改善空穴和/或电子的迁移率,从而降低驱动电压。
其中
R
R
Ar
D
N表示8至50的整数。
本发明的有益效果
通过使用根据本公开的有机电致发光化合物,可以生产具有改善的发射蓝光寿命的有机电致发光装置。
附图说明
图1是示出由于氘化引起的键离解能增加的图。
具体实施方式
在下文中,将详细描述本公开。然而,以下描述旨在解释本发明,并不意味着以任何方式限制本发明的范围。
本公开中的术语“有机电致发光化合物”意指可以用于有机电致发光装置中并且如有需要可以包含在构成有机电致发光装置的任何层中的化合物。
本公开中的术语“有机电致发光材料”意指可以用于有机电致发光装置中并且可以包含至少一种化合物的材料。如有需要,有机电致发光材料可以包含在构成有机电致发光装置的任何层中。例如,有机电致发光材料可以是空穴注入材料、空穴传输材料、空穴辅助材料、发光辅助材料、电子阻挡材料、发光材料、电子缓冲材料、空穴阻挡材料、电子传输材料、电子注入材料等。
本公开的有机电致发光材料可以包含至少一种由式1表示的化合物。由式1表示的化合物可以包含在发光层或空穴传输层中,但不限于此。例如,当包含在发光层中时,由式1表示的化合物可以作为主体如用于发射蓝光的主体被包含。根据本公开的一个实施例,具有式1的化合物可以是荧光主体,例如用于发射蓝光的荧光主体。
在下文中,将更详细地描述由式1表示的化合物。
在本文中,术语“(C1-C30)烷基”意指具有1至30个构成链的碳原子的直链或支链烷基,其中碳原子的数目优选地是1至20,并且更优选地是1至10。上述烷基可以包括甲基、乙基、正丙基、异丙基、正丁基、异丁基、叔丁基等。术语“(C2-C30)烯基”意指具有2至30个构成链的碳原子的直链或支链烯基,其中碳原子的数目优选地是2至20,并且更优选地是2至10。上述烯基可以包括乙烯基、1-丙烯基、2-丙烯基、1-丁烯基、2-丁烯基、3-丁烯基、2-甲基丁-2-烯基等。术语“(C2-C30)炔基”意指具有2至30个构成链的碳原子的直链或支链炔基,其中碳原子的数目优选地是2至20,并且更优选地是2至10。上述炔基可以包括乙炔基、1-丙炔基、2-丙炔基、1-丁炔基、2-丁炔基、3-丁炔基、1-甲基戊-2-炔基等。术语“(C3-C30)环烷基”意指具有3至30个环骨架碳原子的单环烃或多环烃,其中碳原子的数目优选地是3至20,并且更优选地是3至7。上述环烷基可以包括环丙基、环丁基、环戊基、环己基等。术语“(3元至7元)杂环烷基”意指具有3至7个、优选5至7个环骨架原子并且包含至少一个杂原子的环烷基,所述杂原子选自由B、N、O、S、Si和P组成的组、并且优选地由O、S和N组成的组。上述杂环烷基可以包括四氢呋喃、吡咯烷、四氢噻吩(thiolan)、四氢吡喃等。术语“(C6-C30)芳基”意指衍生自具有6至30个环骨架碳原子的芳族烃的单环或稠环基团,其中环骨架碳原子的数目优选地是6至25,更优选地是6至18。上述芳基可以是部分饱和的,并且可以包含螺结构。上述芳基可以包括苯基、联苯基、三联苯基、萘基、联萘基、苯基萘基、萘基苯基、苯基三联苯基、芴基、苯基芴基、苯并芴基、二苯并芴基、菲基、苯基菲基、蒽基、茚基、三亚苯基、芘基、并四苯基、苝基、屈基、萘并萘基、荧蒽基、螺二芴基、薁基等。更具体地,所述芳基可以包括苯基、1-萘基、2-萘基、1-蒽基、2-蒽基、9-蒽基、苯并蒽基、1-菲基、2-菲基、3-菲基、4-菲基、9-菲基、萘并萘基、芘基、1-屈基、2-屈基、3-屈基、4-屈基、5-屈基、6-屈基、苯并[c]菲基、苯并[g]屈基、1-三亚苯基、2-三亚苯基、3-三亚苯基、4-三亚苯基、1-芴基、2-芴基、3-芴基、4-芴基、9-芴基、苯并芴基、二苯并芴基、2-联苯基、3-联苯基、4-联苯基、邻三联苯基、间三联苯-4-基、间三联苯-3-基、间三联苯-2-基、对三联苯-4-基、对三联苯-3-基、对三联苯-2-基、间四联苯基、3-荧蒽基、4-荧蒽基、8-荧蒽基、9-荧蒽基、苯并荧蒽基、邻甲苯基、间甲苯基、对甲苯基、2,3-二甲苯基、3,4-二甲苯基、2,5-二甲苯基、均三甲苯基、邻异丙苯基、间异丙苯基、对异丙苯基、对叔丁基苯基、对(2-苯基丙基)苯基、4'-甲基联苯基、4"-叔丁基-对三联苯-4-基、9,9-二甲基-1-芴基、9,9-二甲基-2-芴基、9,9-二甲基-3-芴基、9,9-二甲基-4-芴基、9,9-二苯基-1-芴基、9,9-二苯基-2-芴基、9,9-二苯基-3-芴基、9,9-二苯基-4-芴基等。
在本文中,术语“(3元至30元)杂芳基”是具有3至30个环骨架原子并且包括至少一个、优选地1至4个选自由B、N、O、S、Si和P组成的组的杂原子的芳基。上述杂芳基可以是单环、或与至少一个苯环缩合的稠环;可以是部分饱和的;可以是经由一个或多个单键将至少一个杂芳基或芳基与杂芳基连接而形成的杂芳基;并且可以包含螺结构。上述杂芳基可以包括单环型杂芳基,如呋喃基、噻吩基、吡咯基、咪唑基、吡唑基、噻唑基、噻二唑基、异噻唑基、异噁唑基、噁唑基、噁二唑基、三嗪基、四嗪基、三唑基、四唑基、呋咱基、吡啶基、吡嗪基、嘧啶基、哒嗪基等,以及稠环型杂芳基,如苯并呋喃基、苯并噻吩基、异苯并呋喃基、二苯并呋喃基、二苯并噻吩基、苯并萘并呋喃基、苯并萘并噻吩基、苯并咪唑基、苯并噻唑基、萘并噻唑基、苯并异噻唑基、苯并异噁唑基、苯并噁唑基、异吲哚基、吲哚基、苯并吲哚基、吲唑基、苯并噻二唑基、喹啉基、异喹啉基、噌啉基、喹唑啉基、苯并喹唑啉基、喹喔啉基、苯并喹喔啉基、萘啶基、咔唑基、苯并咔唑基、二苯并咔唑基、吩噁嗪基、吩噻嗪基、菲啶基、苯并二氧杂环戊烯基、二氢吖啶基等。更具体地,所述杂芳基可以包括1-吡咯基、2-吡咯基、3-吡咯基、吡嗪基、2-吡啶基、2-嘧啶基、4-嘧啶基、5-嘧啶基、6-嘧啶基、1,2,3-三嗪-4-基、1,2,4-三嗪-3-基、1,3,5-三嗪-2-基、1-咪唑基、2-咪唑基、1-吡唑基、1-吲哚啉基、2-吲哚啉基、3-吲哚啉基、5-吲哚啉基、6-吲哚啉基、7-吲哚啉基、8-吲哚啉基、2-咪唑并吡啶基、3-咪唑并吡啶基、5-咪唑并吡啶基、6-咪唑并吡啶基、7-咪唑并吡啶基、8-咪唑并吡啶基、3-吡啶基、4-吡啶基、1-吲哚基、2-吲哚基、3-吲哚基、4-吲哚基、5-吲哚基、6-吲哚基、7-吲哚基、1-异吲哚基、2-异吲哚基、3-异吲哚基、4-异吲哚基、5-异吲哚基、6-异吲哚基、7-异吲哚基、2-呋喃基、3-呋喃基、2-苯并呋喃基、3-苯并呋喃基、4-苯并呋喃基、5-苯并呋喃基、6-苯并呋喃基、7-苯并呋喃基、1-异苯并呋喃基、3-异苯并呋喃基、4-异苯并呋喃基、5-异苯并呋喃基、6-异苯并呋喃基、7-异苯并呋喃基、2-喹啉基、3-喹啉基、4-喹啉基、5-喹啉基、6-喹啉基、7-喹啉基、8-喹啉基、1-异喹啉基、3-异喹啉基、4-异喹啉基、5-异喹啉基、6-异喹啉基、7-异喹啉基、8-异喹啉基、2-喹喔啉基、5-喹喔啉基、6-喹喔啉基、1-咔唑基、2-咔唑基、3-咔唑基、4-咔唑基、9-咔唑基、氮杂咔唑基-1-基、氮杂咔唑基-2-基、氮杂咔唑基-3-基、氮杂咔唑基-4-基、氮杂咔唑基-5-基、氮杂咔唑基-6-基、氮杂咔唑基-7-基、氮杂咔唑基-8-基、氮杂咔唑基-9-基、1-菲啶基、2-菲啶基、3-菲啶基、4-菲啶基、6-菲啶基、7-菲啶基、8-菲啶基、9-菲啶基、10-菲啶基、1-吖啶基、2-吖啶基、3-吖啶基、4-吖啶基、9-吖啶基、2-噁唑基、4-噁唑基、5-噁唑基、2-噁二唑基、5-噁二唑基、3-呋咱基、2-噻吩基、3-噻吩基、2-甲基吡咯-1-基、2-甲基吡咯-3-基、2-甲基吡咯-4-基、2-甲基吡咯-5-基、3-甲基吡咯-1-基、3-甲基吡咯-2-基、3-甲基吡咯-4-基、3-甲基吡咯-5-基、2-叔丁基吡咯-4-基、3-(2-苯基丙基)吡咯-1-基、2-甲基-1-吲哚基、4-甲基-1-吲哚基、2-甲基-3-吲哚基、4-甲基-3-吲哚基、2-叔丁基-1-吲哚基、4-叔丁基-1-吲哚基、2-叔丁基-3-吲哚基、4-叔丁基-3-吲哚基、1-二苯并呋喃基、2-二苯并呋喃基、3-二苯并呋喃基、4-二苯并呋喃基、1-二苯并噻吩基、2-二苯并噻吩基、3-二苯并噻吩基、4-二苯并噻吩基、1-硅芴基(silafluorenyl)、2-硅芴基、3-硅芴基、4-硅芴基、1-锗芴基(germafluorenyl)、2-锗芴基、3-锗芴基、4-锗芴基等。“卤素”包括F、Cl、Br、以及I。
此外,“邻位(o-)”、“间位(m-)”和“对位(p-)”是前缀,其分别表示取代基的相对位置。邻位表示两个取代基彼此相邻,并且例如当苯衍生物中的两个取代基占据位置1和2时,被称为邻位。间位表示两个取代基在位置1和3处,并且例如当苯衍生物中的两个取代基占据位置1和3时,被称为间位。对位表示两个取代基在位置1和4处,并且例如当苯衍生物中的两个取代基占据位置1和4时,被称为对位。
在本文中,表述“取代或未取代的”中的“取代的”意指某个官能团中的氢原子被另一个原子或另一个官能团(即,取代基)替代。在R
由式1表示的化合物可以由下式1-1至1-3中的任一个表示:
其中
R
N表示8至30的整数。
在式1中,R
在式1中,Ar
在式1中,D
在本公开的一个实施例中,在式1中,未键合至
在本公开的另一个实施例中,在式1中,未键合至
在本公开的式中,如果相邻取代基彼此连接以形成环,则所述环可以是取代或未取代的单环或多环(3元至30元)脂环族环或芳香族环、或其组合,其中所形成的环可以含有至少一个选自B、N、O、S、Si和P,优选N、O和S的杂原子。根据本公开的一个实施例,环骨架原子的数目可以是5至20。根据本公开的另一个实施例,环骨架原子的数目可以是5至15。例如,稠环可以是取代或未取代的二苯并噻吩环、取代或未取代的二苯并呋喃环、取代或未取代的萘环、取代或未取代的菲环、取代或未取代的芴环、取代或未取代的苯并噻吩环、取代或未取代的苯并呋喃环、取代或未取代的吲哚环、取代或未取代的茚环、取代或未取代的苯环、或取代或未取代的咔唑环。
在本公开的式中,杂芳基各自独立地可以含有至少一个选自B、N、O、S、Si、以及P的杂原子。此外,杂原子可以与选自由以下组成的组的至少一个键合:氢、氘、卤素、氰基、取代或未取代的(C1-C30)烷基、取代或未取代的(C6-C30)芳基、取代或未取代的(5元至30元)杂芳基、取代或未取代的(C3-C30)环烷基、取代或未取代的(C1-C30)烷氧基、取代或未取代的三(C1-C30)烷基甲硅烷基、取代或未取代的二(C1-C30)烷基(C6-C30)芳基甲硅烷基、取代或未取代的(C1-C30)烷基二(C6-C30)芳基甲硅烷基、取代或未取代的三(C6-C30)芳基甲硅烷基、取代或未取代的单-或二-(C1-C30)烷基氨基、取代或未取代的单-或二-(C6-C30)芳基氨基、以及取代或未取代的(C1-C30)烷基(C6-C30)芳基氨基。
由式1表示的化合物包括以下化合物,但不限于此。
根据本公开的具有式1的化合物可以通过本领域技术人员已知的合成方法以及例如如以下反应方案所示制备,但不限于此。
[反应方案1]
[反应方案2]
[反应方案3]
在反应方案1至3中,Ar
此外,由式1表示的化合物的非氘化衍生物可以通过已知的偶联或取代反应制备。氘化衍生物可以通过类似的方法使用氘化前体材料,或更一般地,在路易斯酸如三氯化铝或乙基氯化铝、H/D交换催化剂如三氟甲磺酸或三氟甲磺酸-D等的存在下用氘化溶剂D6-苯等处理非氘化化合物来制备。此外,氘化度可以通过改变反应条件如反应温度来控制。例如,通过控制反应温度和时间、酸当量等,可以控制式1中的N的数目。
尽管以上描述了由式1表示的化合物的说明性合成实例,但是本领域技术人员将能够容易地理解它们全部基于布赫瓦尔德-哈特维希(Buchwald-Hartwig)交叉偶联反应、N-芳基化反应、酸化蒙脱土(H-mont)介导的醚化反应、宫浦(Miyaura)硼基化反应、铃木(Suzuki)交叉偶联反应、分子内酸诱导的环化反应、Pd(II)催化的氧化环化反应、格氏反应(Grignard reaction)、赫克反应(Heck reaction)、脱水环合反应(Cyclic Dehydrationreaction)、SN
本公开提供了一种包含由式1表示的有机电致发光化合物的有机电致发光材料,以及一种包含所述有机电致发光材料的有机电致发光装置。所述材料可以仅由根据本公开的有机电致发光化合物组成,或者可以进一步包含有机电致发光材料中包括的常规材料。
根据本公开的有机电致发光装置包括第一电极、第二电极、和在第一电极与第二电极之间的至少一个有机层,其中所述有机层可以包含至少一种由式1表示的有机电致发光化合物。
第一电极和第二电极中的一个可以是阳极,并且另一个可以是阴极。有机层可以包含发光层,并且可以进一步包含选自空穴注入层、空穴传输层、空穴辅助层、发光辅助层、电子传输层、电子缓冲层、电子注入层、中间层、空穴阻挡层、以及电子阻挡层的至少一个层。
第二电极可以是半透反射式电极或反射电极,并且根据形成的材料的种类,有机电致发光装置可以是顶部发光型、底部发光型、或两侧发光型。
第一电极和第二电极可以各自由透射式导电材料、半透反射式导电材料、或反射式导电材料形成。根据形成第一电极和第二电极的材料的种类,有机电致发光装置可以是顶部发光型、底部发光型、或两侧发光型。此外,空穴注入层可以进一步掺杂有p型掺杂剂,并且电子注入层可以进一步掺杂有n型掺杂剂。
本公开的由式1表示的有机电致发光化合物可以包含在发光层、空穴注入层、空穴传输层、空穴辅助层、发光辅助层、电子传输层、电子缓冲层、电子注入层、中间层、空穴阻挡层、以及电子阻挡层中的至少一个中,优选地,可以包含在发光层中。当在发光层中使用时,本公开的由式1表示的有机电致发光化合物可以作为主体材料被包含。优选地,发光层可以进一步包含至少一种掺杂剂。如果需要,本公开的有机电致发光化合物可以用作共主体材料。也就是说,发光层可以进一步包含除了本公开的由式1表示的有机电致发光化合物(第一主体材料)之外的化合物作为第二主体材料。第一主体材料与第二主体材料之间的重量比是1:99至99:1。
包含在本公开的有机电致发光装置中的掺杂剂是至少一种磷光掺杂剂或荧光掺杂剂,优选地是至少一种荧光掺杂剂。应用于本公开的有机电致发光装置的荧光掺杂剂材料不受特别限制。
有机层可以进一步包含至少一种选自由基于芳基胺的化合物和基于苯乙烯基芳基胺的化合物组成的组的化合物。
此外,在本公开的有机电致发光装置中,有机层可以进一步包含选自由以下组成的组的至少一种金属:周期表的第1族的金属、第2族的金属、第4周期的过渡金属、第5周期的过渡金属、镧系元素和d-过渡元素的有机金属,或至少一种包含所述金属的络合化合物。
除了本公开的有机电致发光化合物之外,本公开的有机电致发光装置可以通过进一步包括至少一个含有本领域已知的发射蓝光、红光或绿光的化合物的发光层来发射白光。此外,如果需要,它可以进一步包括发射黄光或橙光的层。
在本公开的有机电致发光装置中,可以优选将选自硫属化物层、金属卤化物层和金属氧化物层中的至少一个层(下文中,“表面层”)放置在一个或两个电极的一个或多个内表面上。具体地,优选将硅或铝的硫属化物(包括氧化物)层放置在电致发光介质层的阳极表面上,并且优选将金属卤化物层或金属氧化物层放置在电致发光介质层的阴极表面上。表面层可以为有机电致发光装置提供运行稳定性。优选地,硫属化物包括SiO
在阳极与发光层之间可以使用空穴注入层、空穴传输层、或电子阻挡层、或其组合。空穴注入层可以是多层以便降低从阳极到空穴传输层或电子阻挡层的空穴注入势垒(或空穴注入电压),其中多层中的每个可以同时使用两种化合物。空穴传输层或电子阻挡层也可以是多层。
在发光层与阴极之间可以使用电子缓冲层、空穴阻挡层、电子传输层、或电子注入层、或其组合。电子缓冲层可以是多层以控制电子的注入并改善发光层与电子注入层之间的界面特性,其中多层中的每个可以同时使用两种化合物。空穴阻挡层或电子传输层也可以是多层,其中多层中的每个可以使用多种化合物。
可以将发光辅助层放置在阳极与发光层之间,或放置在阴极与发光层之间。当将发光辅助层放置在阳极与发光层之间时,它可以用于促进空穴注入和/或空穴传输,或用于防止电子溢出。当将发光辅助层放置在阴极与发光层之间时,它可以用于促进电子注入和/或电子传输,或用于防止空穴溢出。此外,可以将空穴辅助层放置在空穴传输层(或空穴注入层)与发光层之间,并且可以有效促进或限制空穴传输速率(或空穴注入速率),从而使得能够控制电荷平衡。另外,可以将电子阻挡层放置在空穴传输层(或空穴注入层)与发光层之间,并且可以阻挡来自发光层的溢出电子并将激子限制在发光层中以防止漏光。当有机电致发光装置包括两个或更多个空穴传输层时,进一步包括的空穴传输层可以用作空穴辅助层或电子阻挡层。空穴辅助层和电子阻挡层可以具有改善有机电致发光装置的效率和/或寿命的作用。
在本公开的有机电致发光装置中,优选将电子传输化合物和还原性掺杂剂的混合区域、或空穴传输化合物和氧化性掺杂剂的混合区域放置在一对电极的至少一个表面上。在这种情况下,电子传输化合物被还原成阴离子,并且因此从混合区域向电致发光介质注入并且传输电子变得更容易。此外,空穴传输化合物被氧化成阳离子,并且因此从混合区域向电致发光介质注入并且传输空穴变得更容易。优选地,氧化性掺杂剂包括各种路易斯酸和受体化合物;并且还原性掺杂剂包括碱金属、碱金属化合物、碱土金属、稀土金属、及其混合物。还原性掺杂剂层可以用作电荷产生层,以制备具有两个或更多个发射白光的发光层的有机电致发光装置。
根据本公开的一个实施例,有机电致发光材料可以被用作用于白色有机发光装置的发光材料。根据R(红色)、G(绿色)、B(蓝色)、或YG(黄绿色)发光单元的布置,已经提出了呈各种结构的白色有机发光装置,如平行并排布置方法、堆叠布置方法、或CCM(颜色转换材料)方法等。此外,根据本公开的一个实施例,有机电致发光材料还可以应用于包含QD(量子点)的有机电致发光装置。
为了形成本公开的有机电致发光装置的每个层,可以使用干法成膜方法如真空蒸发、溅射、等离子体、离子镀等,或湿法成膜方法如喷墨印刷、旋涂、浸涂、流涂等。
当使用湿法成膜方法时,可以通过将形成每个层的材料溶解或扩散到任何合适溶剂如乙醇、氯仿、四氢呋喃、二噁烷等中来形成薄膜。对溶剂没有特别限制,只要形成每个层的材料在溶剂中是可溶的或可分散的,这在形成膜时不会引起任何问题。
可以通过使用本公开的有机电致发光装置来生产显示系统,例如用于智能手机、平板电脑、笔记本电脑、PC、TV或汽车的显示系统;或照明系统,例如室外或室内照明系统。
在下文中,将参考本公开的代表性化合物详细说明本公开的化合物的制备方法、及所述化合物的特性、以及包含所述化合物的有机电致发光装置的发光特性。然而,本公开不受限于以下实例。
将3.5g化合物1(8.3mmol)和100mL苯-D6引入烧瓶中,并且加热以溶解全部化合物1。将混合物冷却至室温后,向其中添加4.4mL三氟甲磺酸(49.8mmol)。在室温下搅拌混合物2小时30分钟后,向其中添加20mL重水。搅拌10分钟后,将混合物用K
如下生产包含根据本公开的有机电致发光化合物的OLED:使用于OLED的玻璃基板上的透明电极氧化铟锡(ITO)薄膜(10Ω/sq)(吉奥马有限公司(GEOMATEC CO.,LTD.),日本)经受依次用丙酮、乙醇和蒸馏水进行的超声洗涤,并且然后储存在异丙醇中。将ITO基板安装在真空气相沉积设备的基板支架上。将化合物HI-1引入真空气相沉积设备的小室中,并且然后将设备的腔室中的压力控制到10
结果,在2,000尼特下亮度从100%降低到95%所需的最短时间为76小时。
除了将化合物H-1用作发光层的主体材料以外,以与装置示例1中相同的方式生产OLED。
结果,在2,000尼特下亮度从100%降低到95%所需的最短时间为11小时。
除了将化合物H-2用作发光层的主体材料以外,以与装置示例1中相同的方式生产OLED。
结果,在2,000尼特下亮度从100%降低到95%所需的最短时间为25小时。
除了将化合物H-3用作发光层的主体材料以外,以与装置示例1中相同的方式生产OLED。
结果,在2,000尼特下亮度从100%降低到95%所需的最短时间为13小时。
在本公开中,通过用氘取代发光层的主体化合物的氢来生产有机电致发光装置,可以看出寿命特征远远优于使用常规化合物作为主体的有机电致发光装置。应理解的是,与未氘化或用较少的氘来氘化的化合物相比,OLED的寿命特征的此种改善是由于材料稳定性的改善,所述稳定性的改善是由于氘化化合物的零点振动能的降低。此外,不旨在受理论限制,为了改善发蓝光的荧光有机电致发光装置的寿命,需要控制电子迁移率,并且由于二苯并呋喃具有比芳基更快的空穴迁移,因此可以获得降低电子迁移率的类似效果。不旨在受理论限制,电子迁移率的降低可导致相邻层的降解的降低,从而增加寿命。在此种效果方面,与氘化其中蒽被芳基取代的化合物相比,氘化其中蒽被二苯并呋喃取代的化合物可能是有利的。
- 有机电致发光化合物和包含有机电致发光化合物的有机电致发光装置
- 有机电致发光化合物和包含所述有机电致发光化合物的有机电致发光装置
