基因检测用标本载玻片
文献发布时间:2023-06-19 11:26:00
技术领域
本发明涉及一种基因检测用标本载玻片。
背景技术
在基因检测中要处理各种检测材料(样品),也出现了癌症的伴随药物,现在最多的检测材料为未染色载玻片(将福尔马林固定石蜡包埋(FFPE)切片固定在玻璃载玻片上的玻片标本)。从未染色载玻片上提取核酸时,用手术刀从玻璃载玻片上刮取FFPE切片,将刮取的FFPE切片放入塑料制微型离心管中,提取核酸。当每片载玻片上的组织尺寸较小时(穿刺活检),无法提取充分的核酸,因此需要从每个样品的多片载玻片上刮取FFPE切片,当处理大量样品时,操作非常繁琐,需要大量的人力。此外,将刮取的PPFE切片放入微型离心管的行为因静电的影响而非常困难,是需要技巧的。进一步,还存在刮取的FFPE切片发生散落而混入(污染)样品间的风险。
此外,在癌症的检测中,检测材料的玻片标本中必须存在癌症部位。因此在制作标本时,制作连续切片,并使用其中1片进行HE染色,由病理医生确认存在癌症部位。通过仅对肿瘤组织进行选择性检测,可避免周围的正常组织的影响,得到更准确的检测结果。当为正常部位的比例较多的标本时,需要标记癌症部位以指示应为检测对象的区域。因此,有时将通过HE染色进行标记的标本作为参考,从未染载玻片上刮取与标记同等的区域。
作为刮取该标本的一部分的方法,已知有激光显微切割法,该方法将特殊的膜贴附在组织上,使用激光进行切取。本方法的技术问题在于,需要特殊的装置,且装置价格高昂;需要用于激光切取的专用玻璃载玻片或塑料膜,价格昂贵;从1片载玻片上选择性切取需要花费时间。不适合要处理大量样品的临床检测。
近年来出现一种较之激光显微切割法缩短了切取时间,专为检测而开发的组织切割法(样品预处理装置“AVENIO MilliSect”,Roche Diagnostics K.K.,非专利文献1)。所述装置在前端底部具备塑料制刀片(切断刀片),且使用在筒状主体内部具备切割试样回收管的专用枪头(tip),使枪头接触贴附了FFPE切片的玻璃载玻片,旋转枪头,从而物理性地切取载玻片上的切片,切片的碎片被回收至切割试样回收管内。在所述装置中使用的枪头价格高昂(约为4000日元/个),且一次性使用以防止污染,因此对处理大量样品的临床检测而言存在价格问题。
现有技术文献
非专利文献
非专利文献1:“AVENIO MilliSect”产品说明书,2017年8月编写(第1版)
发明内容
本发明要解决的技术问题
因此,本发明的技术问题在于提供一种样品预处理方法以及用于该方法的医疗器械及装置,所述样品预处理方法:(1)能够简化从未染色载玻片上刮取FFPE切片的工序且不会影响之后的核酸提取工序;(2)能够避免刮取时污染的风险;(3)能够以廉价且简便的设备选择性地分取癌症部位。
解决技术问题的技术手段
所述技术问题可通过以下的本发明解决:
[1]一种基因检测用标本载玻片,其为贴附样品切片的基因检测用标本载玻片,其中,载玻片的一部分与待分离的该样品切片能够一同以带有载玻片上表面与载玻片下表面的状态,与载玻片的除此以外的部分分离。
[2]一种基因检测用标本载玻片,其为贴附样品切片的基因检测用标本载玻片,其中,在该样品切片的贴附面和/或相反侧的面上,设有辅助分离载玻片的一部分与载玻片的除此以外的部分的标识(guide)。
[3]一种基因检测用标本载玻片,其为贴附样品切片的基因检测用标本载玻片,其中,在该样品切片的与贴附面为相反侧的面上,设有辅助分离载玻片的一部分与载玻片的除此以外的部分的槽。
[4]一种样品预处理用系统,其含有样品预处理装置与所述[1]~[3]中任一项所述的基因检测用标本载玻片,所述样品预处理装置具备能够将[1]~[3]中任一项所述的基因检测用标本载玻片的一部分与载玻片的除此以外的部分分离的分离设备。
[5]一种样品的预处理方法,其含有以下工序:
(1)准备样品切片的工序;
(2)在载玻片上贴附所述样品切片的工序;
(3)将载玻片的一部分和贴附在该区域的样品切片一起,与载玻片的除此以外的部分分离的工序。
[6]一种样品的预处理方法,其含有以下工序:
(1)准备石蜡包埋样品切片的工序;
(2)在载玻片上贴附所述样品切片的工序;
(3)将载玻片的一部分和贴附在该区域的样品切片一起,与载玻片的除此以外的部分分离的工序;
(4)从分离的载玻片上的样品切片中去除石蜡的工序。
发明效果
根据本发明,能够简化从未染色载玻片上刮取FFPE切片的工序且不会影响之后的核酸提取工序。此外,能够避免刮取时污染的风险。进一步,能够以廉价且简便的设备选择性地分取癌症部位。
附图说明
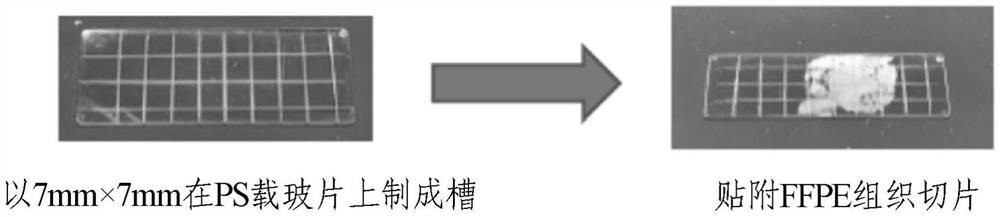
图1为代替附图的照片,示出了FFPE切片固定在聚苯乙烯(PS)载玻片上的状态,左侧示出了刻有7mm×7mm的格子状的槽的PS载玻片(固定FFPE切片前)的状态,右侧示出了固定FFPE切片后的PS载玻片的状态。
图2为在实施例2中使用的电热切割机的代替附图的照片。
图3为代替附图的照片,示出了对PS载玻片的下表面进行冷却并同时沿着槽切断PS载玻片的状态。
图4为代替附图的照片,示出了PS载玻片切断前后的状态。
图5为代替附图的照片,示出了脱蜡(Deparaffinization)处理(实施例3中的步骤(4))前后的状态。
图6为示出了为了确定从2个7mm×7mm的载玻片小片上提取时各区域的DNA提取量而实施了吸光度测定的结果的照片及图表,图表中从左至右为区域(2-AB)、区域(3-AB)、区域(4-AB)、区域(5-AB)。
图7为示出了为了确定从3个7mm×7mm的载玻片小片上提取时各区域的DNA提取量而实施了吸光度测定的结果的照片及图表,图表中从左至右为区域(2-ABC)、区域(3-ABC)、区域(4-ABC)、区域(5-ABC)。
具体实施方式
在本发明中,从组织样品或细胞样品(特别是病理组织/细胞样品)、优选从福尔马林固定石蜡包埋的组织样品或细胞样品中薄切出样品切片,并将该样品切片贴附在本发明的载玻片上,使用适宜的手段,仅将癌症部位等必要区域与和该区域对应的载玻片的部分区域一同,与除此以外的部分分离,然后从分离的载玻片上的样品切片中提取供于基因检测的核酸。
作为能够用本发明进行处理的样品,没有特别限定,可广泛处理用于进行病理诊断的通常的样品,例如可列举出组织样品、细胞样品等。优选为通过常规方法经福尔马林固定石蜡包埋的组织样品或细胞样品(FFPE组织样品或细胞样品)。
在本发明中,将通过常规方法(例如,切片机)从所述样品中薄切而得到的样品切片以展开的状态贴附在本发明的载玻片的样品切片贴附面上。
本发明的载玻片的形状及大小没有特别限定,优选操作感与以往一样且现有器械能够利用的、以以往公知的用于制作观察标本的显微镜载物片为基准的形状及大小。例如为长76mm左右、宽26mm左右、厚1mm左右的矩形形状。
本发明的载玻片的至少一个面为用于载置样品切片的贴附面,载玻片的一部分与待分离的样品切片能够一同,与载玻片的除此以外的部分分离。在本发明中,在将载玻片的一部分与载玻片的除此以外的部分分离时,在贴附面和/或其相反侧的面(以下,称为基底面)上设有用于辅助该分离的标识,从而能够以带有载玻片上表面与载玻片下表面的状态进行分离。所述标识可设置在载玻片的贴附面或基底面中的任意一面或两面,优选设置在进行分离时不会损伤样品切片的基底面。
为了载置样品切片,所述贴附面的载置样品切片的区域(以下,称为载置区域)优选为平滑面。另外,预设不载置样品切片的区域、例如载玻片的端部则无需为平滑面,例如可制成在夹持时不易打滑的粗糙面,或者也可设置适合记载信息的备注栏。
此外,为了使经石蜡包埋的样品切片容易贴附,贴附面优选为亲水性,例如可由亲水性材料形成整个载玻片,或者也可对用任意材料形成的载玻片的作为贴附面的表面进行亲水处理。此外,通过将整个作为贴附面的载玻片表面中除适合贴附的位置以外的部位制成疏水性或防水性,能够容易地贴附在所需位置上。
设置在本发明的载玻片中的贴附面和/或基底面上的标识只要为能够辅助分离载玻片的一部分与载玻片的除此以外的部分的结构,则没有特别限定,例如可列举出标记线、可降低分离所需的力的槽等。本发明的载玻片的特征在于,为了仅选择性分离贴附在贴附面上的样品切片中的必要区域(例如,癌症部位),以该区域所在的载玻片区域为单位进行分离。作为本发明的所述分离方法,例如可列举出利用冲压工具仅对必要区域进行冲压的方法、通过切开设备仅切取必要区域的方法、通过切开设备仅切分必要区域的方法、对载玻片施加力使必要区域与非必要区域弯折从而切分的方法等。
以下,以设有槽作为标识的方式为例对本发明进行说明,但本领域技术人员也可适当应用除槽以外的方式(例如,标记线)。作为设置在载玻片的基底面的槽的图案,例如能够以连续配置规定形状的区域的方式设置槽。例如,当所述区域为六边形形状时,能够以将六边形配置成蜂巢状的方式设置槽。此外,当所述区域为正方形形状时,能够以将正方形配置为棋盘格状的方式设置槽。作为其他形状,只要为从载玻片的贴附面观察时载置区域的内部被无空隙地包埋的形状,则没有特别限定,例如可列举出三角形形状、四边形形状(例如,正方形、长方形、平行四边形、梯形、菱形等)或这些形状的组合。这种连续配置能够分离(例如,冲压、切取、切分、弯折等)任意的一个或多个区域,因此具有可分离载置区域内的所需区域的优点。
作为设置在载玻片的基底面的槽的其他图案,例如,能够以非连续地配置规定形状的区域的方式(即,规定形状以浮于海中的岛的方式配置)设置槽。作为此时的形状,除了上文中对连续配置所列举的各形状以外,可采用任意的形状,例如可列举出圆形形状(正圆或椭圆)等。这种非连续配置具有能够采用任意的形状的优点。
作为设置在载玻片的基底面的槽的其他图案,例如,能够以任意间隔(优选等间隔)配置与载玻片的短边或长边(优选短边)平行的多根直线的方式、或者仅配置一根与载玻片的短边或长边(优选短边)平行的直线的方式设置槽。此时,通过对载玻片施加力进行弯折,能够切分必要区域与非必要区域,因此具有不需要特殊装置的优点。
设置在载玻片的基底面上的槽的深度、宽度只要为能够降低分离载玻片的一部分与载玻片的除此以外的部分时所需的力的深度,则没有特别限定。例如可根据载玻片的厚度、材料、分离时的力或方法等适当地确定。
相对于载玻片的厚度,槽的深度例如为25%以上,优选为50%以上,更优选为75%以上。另外,当槽过深时,有时载玻片的强度不充分,相对于载玻片的厚度,槽的深度优选为90%以下。
对于槽的宽度,只要能够在载玻片上形成槽且能够操作载玻片,则没有特别限定,但若槽的宽度过大,则选择性下降,因此优选为1mm以下的宽度。此外,考虑到在实施冲压等时对槽的选择性,优选为0.1mm以上。若考虑到切分时的容易度,则优选为0.5mm左右。
在设置于载玻片的基底面上的槽中,相邻的槽的间隔可根据分析目的进行设定,但若考虑肿瘤组织等的选择性,则为矩形时,例如为长10mm以下及宽10mm以下的间隔,优选为长5mm以下及宽5mm以下的间隔,更优选为2mm×2mm左右的间隔。下限没有特别限定,例如为0.5mm×0.5mm以上。本领域技术人员可考虑能够分离且切分后处理的容易度以及槽的宽度进行适当设计。
还可根据分析所需的间隔,由相邻的多个槽适当地选择分离的大小。
对于本发明的载玻片的材料,只要能够以在载玻片的贴附面上贴附有样品切片的状态,将样品切片及载玻片的一部分与除此以外的部分分离,且不会影响分离之后的核酸提取,则没有特别限定,例如可列举出玻璃或树脂等,作为树脂,可列举出有机树脂(例如,聚丙烯酸酯、聚酰胺、聚苯二甲酸丁二醇酯(Polybutylene phthalate)、聚碳酸酯、聚乙烯、聚苯二甲酸乙二醇酯(Polyethylene phthalate)、聚缩醛、聚丙烯、聚苯醚、聚苯硫醚、聚苯乙烯、聚氯乙烯、ABS树脂、AS树脂、氯三氟乙烯、偏氟乙烯、全氟烷氧基氟树脂等)等。例如特别优选在基因分析领域中通常使用的玻璃、聚丙烯、聚苯乙烯、聚乙烯、聚丙烯酸等,在显微镜观察等要求透明性的情况下,进一步优选玻璃或聚丙烯酸等。
另外,优选为能够在载玻片的贴附面上贴附样品切片的材料,但即使为无法在载玻片的贴附面上贴附样品切片的材料,其只要为能够通过适当的表面处理(例如,亲水处理)赋予相同特性的材料,则也可以使用。例如在通常将细胞组织切片固定在玻璃载玻片上时,可利用细胞表面的磷脂质的负电荷将其粘附。因此,为了提高粘附性,可在玻璃载玻片表面上涂布作为氨基酸的聚-L-赖氨酸或氨基硅烷。此外,若考虑到细胞组织片的伸展操作性,则表面为亲水性的材料的操作效率良好。
本发明的载玻片可通过与具备规定的分离设备的样品预处理装置进行组合,构成本发明的样品预处理用系统。
所述样品预处理装置的所述分离设备只要为能够将本发明的载玻片的一部分与载玻片的除此以外的部分分离的分离设备,则没有特别限定。
在通过冲压实施所述分离时,作为所述分离设备,可列举出能够仅对必要区域进行冲压的冲压工具。
在通过切取或切分实施所述分离时,作为所述分离设备,可列举出能够仅对必要区域进行切取或切分的切断设备。
在通过弯折实施所述分离时,作为所述分离设备,可列举出能够通过弯折切分必要区域与非必要区域的弯折设备。
本发明的预处理方法含有以下工序:
(1)准备样品切片(优选石蜡包埋样品切片)的工序;
(2)在载玻片上贴附所述样品切片的工序;
(3)将载玻片的一部分和贴附在该区域上的样品切片一起,与载玻片的除此以外的部分分离的工序。
此外,当所述样品为石蜡包埋样品切片时,除了所述工序(1)~(3)以外,本发明的预处理方法还可含有:
(4)从分离的载玻片上的样品切片中去除石蜡的工序。
在本发明方法的所述(1)的样品切片准备工序及所述(2)的样品切片贴附工序中,能够以与制作通常的观察标本相同的方式准备样品切片,并在载玻片(优选本发明的载玻片)上贴附样品切片。例如,在将福尔马林固定石蜡包埋样品切片(FFPE样品切片)用作样品切片时,例如可通过以下方式得到样品切片:对从患者等采集的组织样品或细胞样品用福尔马林进行固定之后,实施脱水、脱脂、石蜡渗透、石蜡包埋的各操作,通过切片机对得到的石蜡包埋块连续进行薄切。例如可通过使得到的样品切片浮在载置于载玻片上的蒸馏水上,升温使该样品切片伸展,直接对其进行干燥,由此将得到的样品切片贴附在载玻片上;或者通过将样品切片浮在温水中使其伸展后使用载玻片捞取,由此将得到的样品切片贴附在载玻片上。
在本发明方法的所述(3)的分离工序中,可通过使用适当的分离方法,将载玻片的一部分与载玻片的除此以外的部分分离,从而同时将载置于其之上的样品切片分离。作为所述分离方法,可使用对本发明的载玻片进行了说明的各种分离方法。对于分离区域,例如可通过对所述工序(2)中得到的贴附有样品切片的载玻片中的1片进行HE染色,标记必要区域(例如,癌症部位),由此将其特定为分离的相应区域。
在本发明方法的所述(4)的石蜡去除工序中,对在所述工序(3)中分离的载玻片上的样品切片实施脱蜡处理。作为所述脱蜡处理,例如可列举出使用有机溶剂的方法、使用矿物油的方法等。
在使用有机溶剂的脱蜡处理中,作为所述有机溶剂,使用不溶解样品切片且能够溶解石蜡的溶剂,例如可列举出二甲苯。例如,当使用二甲苯时,可通过在贴附有样品切片的载玻片上添加二甲苯,混合后进行离心处理,去除为上清的二甲苯,由此获得作为固体物质的样品切片。
更具体而言,添加充分浸泡样本的量(1mL的二甲苯),进行10秒钟涡旋搅拌。以室温(15~25℃)、15000rpm进行2分钟离心处理,制成脱蜡后的细胞团块(cell pellet)。在去除上清的二甲苯后,添加与二甲苯等量(1mL)的乙醇(96~100%),进行10秒钟涡旋,由此使用乙醇从样本中萃取残留的二甲苯。以室温、15000rpm进行2分钟离心处理,去除上清的乙醇,由此可得到可进行DNA提取处理的组织片。
在使用矿物油的脱蜡处理中,向贴附有样品切片的载玻片上添加充分浸泡样本的量的矿物油,进行混合后,加入含有蛋白酶的细胞裂解物,进行热处理(例如,在56℃下进行1小时),回收经两相分离的水相/油相中的水相,由此能够回收样品切片中的核酸(DNA)。
更具体而言,通过加入适量(300μL)的矿物油,以90℃进行20分钟的培养,可进行脱蜡,然后可使用通常的DNA提取试剂盒进行提取处理(Analytical Biochemistry,395(2009),265-267)。
此外,作为使用了相同原理的商品,市售有脱蜡试剂(脱蜡溶液;QIAGEN)。在该试剂中,加入适量(根据切片量分为:160μL或320μL)脱蜡溶液,进行10秒钟的涡旋搅拌后,以56℃培养3分钟,将培养后的样本恢复至室温,然后可使用通常的DNA提取试剂盒进行提取。
例如,若根据作为通常的提取试剂盒的一个例子的QIAGEN公司的提取试剂盒,则可在加入裂解缓冲液(180μL)并进行涡旋之后,进行离心处理,继续加入蛋白酶K(20μL),以56℃培养1小时之后,以90℃培养1小时,然后进行离心处理,回收下层的水相,使用提取试剂盒对回收的水相进行处理。
通过本发明的预处理方法得到的样品切片或来自样品切片的核酸溶液可根据常规方法作为基因检测的试样进行使用。
实施例
以下,通过实施例对本发明进行具体说明,但这些实施例并不限定本发明的范围。
<<实施例1:FFPE切片在聚苯乙烯(PS)载玻片上的固定>>
以7mm×7mm在PS载玻片(长76mm×宽26mm×厚1mm;KENIS,LTD.)的一个面上制成格子状的槽(图1左)。在制成槽时,使用了塑料切割机(OLFA CORPORATION)。此次虽然没有规定槽的深度,但通过肉眼估算将其制成0.5mm~0.7mm左右。
对于福尔马林固定石蜡包埋(FFPE)切片在载玻片上的固定,以与将FFPE切片固定在通常的玻璃载玻片上相同的步骤进行实施。首先,使以10μm的厚度从石蜡块中切取的FFPE切片浮在水浴中,以捞取的方式将其载置于PS载玻片的平坦的面(未开槽的一侧;贴附面)上。然后使其风干去除一定量的水分。
进一步,为了牢固地粘附PS载玻片上的FFPE切片与载玻片,将开槽的一侧(基底面)作为下表面,将载玻片放置在加热块上,升温至65℃。实施升温直至石蜡变得透明(熔化),然后使其自然冷却,使FFPE切片固定在载玻片上(图1右)。
<<实施例2:聚苯乙烯(PS)载玻片的切断>>
在PS载玻片的切断中,使用了将手术刀的替换刀片直接固定在树脂切割用电热切割机(TAIYO ELECTRIC IND.CO.,LTD.,HE-110)上自制而成的装置(图2)。另外,在PS载玻片的切断中,也可使用超声波切割机,可容易地切断载玻片。在使用电热切割机时,若直接与树脂接触,则有时树脂熔化,无法沿槽的线切断。因此,在本实施例中,从载玻片下表面(开槽的一侧)对载玻片进行冷却,从而防止树脂熔化。使用经低温(-20℃)下冷却的铁板,从下方对PS载玻片进行冷却,并同时从载玻片上表面(未开槽的一侧)沿着槽切断(图3)。将沿着槽切断的载玻片示于图4。
<<实施例3:从聚苯乙烯(PS)载玻片上提取DNA的研究1>>
在脱蜡处理中,使用了脱蜡试剂(脱蜡溶液;QIAGEN)。使用QIAamp DNA FFPE组织试剂盒(QIAGEN),对脱蜡后的回收溶液实施DNA提取处理。处理按照产品说明书中记载的步骤实施。只要没有特别说明,则后文中的DNA提取的研究以以下步骤进行。
(1)添加320μL的脱蜡试剂。
(2)以56℃升温3分钟,恢复至室温。
(3)添加180μL的裂解缓冲液(ATL缓冲液;QIAGEN),实施涡旋搅拌之后,以10,000rpm进行1分钟离心处理。
(4)添加20μL的蛋白酶K(蛋白酶K;QIAGEN)。
(5)使用振荡加热块(shake heat block)以56℃进行1小时升温反应。
(6)使用加热块以90℃升温1小时。
(7)添加200μL的试剂盒附带溶液(AL缓冲液;QIAGEN)。
(8)添加200μL的乙醇。
(9)回收下层的液相部分。
(10)使用QIAamp MinElute柱实施纯化回收。
本实施例的目的在于确认是否能够从溶液中回收FFPE切片、处理造成的PS载玻片小片的变化。将如图4所示的切断后的各PS载玻片小片(载玻片小片2、3、4、5)放入2mL的微型离心管(微量离心管)中,按照产品说明书记载的步骤,进行DNA提取操作。在所述步骤(4)之后,确认到固定在载玻片上的FFPE切片被完美地剥离(图5)。此外,若实施所述步骤(5)的90℃的热处理,则PS载玻片小片乳白色化,但形状仍保持不变。
<<实施例4:从聚苯乙烯(PS)载玻片上提取DNA的研究2>>
本实施例的目的在于确认是否对DNA提取造成影响。
以与实施例3相同的方式,使用图6及图7所示的各PS载玻片小片(载玻片小片2、3、4、5),使用QIAamp DNA FFPE组织试剂盒(QIAGEN),对脱蜡后的回收溶液实施DNA提取处理。DNA提取按照产品说明书记载的步骤实施。
使用30μL的洗脱液进行DNA的洗脱,洗脱后的DNA浓度使用Nanodrop超微量分光光度计(Thermo Fisher Scientific)进行测定。示出从两个7mm×7mm的载玻片小片上进行提取(图6)与从三个7mm×7mm的载玻片小片上进行提取(图7)的结果。
此外,根据此次提取的DNA量估算每单位体积组织的DNA量。将结果示于表1。虽然并非在用于提取的载玻片的整个面上都固定有组织,但此次的目的在于外推,以使用的载玻片的区域(7mm×7mm)计算组织区域。即,在为两个面时,以7mm×7mm×2面×10μm(FFPE切片厚度)进行计算,在为三个面时,以7mm×7mm×3面×10μm(FFPE切片厚度)进行计算。计算的结果与一般社团法人日本病理学会于平成30年3月1日发行的“ゲノム診療病理組織検体取り扱い規定”中记载的结果(实证数据3由日常诊疗中制作的FFPE块得到的DNA产量:在手术样品中中值约为0.5μg/mm
[表1]
<<实施例5:提取DNA的评价>>
在本实施例中,利用实时PCR检测评价是否能够由提取后的DNA扩增目标基因。扩增对象设为RHOA基因,将测定中使用的引物、探针的序列示于表2。
[表2]
以下示出实时PCR的反应组成与反应温度。
正向引物(F primer)与反向引物(R primer)各为200nmol/L,探针为100nmol/L,使用Premix Ex taq(探针法qPCR)预混合液(Takara)进行测定。对于样本,使用5μL的表1所示的各浓度的样本实施测定。实时PCR测定使用LC480(Roche)实施。对于反应温度,以95℃保持30秒,然后以95℃、3秒;62℃、30秒为1个循环,实施45个循环。在用于与树脂载玻片提取物的比较中,使用了通过以往的方法从玻璃载玻片上提取的FFPE切片。
其结果,相对于从现有的玻璃载玻片上的提取,图6中提取的DNA平均为115%,此外,图7中提取的DNA平均为95%。由此,实施实时PCR的情况下,对于现有的玻璃载玻片上提取的DNA与通过本方法提取的DNA,未观察到影响。
工业实用性
本发明能够用于基因检测的领域。
以上,以特定的方式对本发明进行了说明,但对于本领域技术人员而言,显而易见的变更或改良也包含在本发明的范围中。
序列表自由文本
序列表的SEQ ID NO:1~3分别为正向引物序列、反向引物序列、探针序列。
<110> 美迪恩斯生命科技株式会社(LSI Medience Corporation)
<120> 基因检测用标本载玻片
<130> KHP212110464.1
<150> JP 2018-211629
<151> 2018-11-09
<160> 3
<170> PatentIn version 3.5
<210> 1
<211> 22
<212> DNA
<213> 人工序列(Artificial Sequence)
<220>
<223> 对人工序列的描述:正向引物
<400> 1
cctatgactt cttgtgcatt gc 22
<210> 2
<211> 20
<212> DNA
<213> 人工序列(Artificial Sequence)
<220>
<223> 对人工序列的描述:反向引物
<400> 2
tacacctctg ggaactggtc 20
<210> 3
<211> 21
<212> DNA
<213> 人工序列(Artificial Sequence)
<220>
<223> 对人工序列的描述:探针
<400> 3
gctgccatcc ggaagaaact g 21
- 基因检测用标本载玻片
- 一种基因检测用载玻片清洗装置
