慢性创伤性脑病的治疗
文献发布时间:2023-06-19 11:27:38
相关申请的交叉引用
根据35U.S.C.§119(e),本专利申请要求在2018年7月10日提交的题为“慢性创伤性脑病的治疗”的美国临时申请第62/695,989号的优先权权益,其内容通过引用合并于此。
技术领域
本发明涉及慢性创伤性脑病(CTE)的治疗,并且更具体地涉及稳定、消退或排除CTE(并且更具体地是在患有创伤性脑损伤(TBI)的患者中的CTE)的发展和/或进展的化合物、组合物和方法。
背景技术
创伤性脑损伤(TBI)带来了严重的健康负担,每年有超过3千万的美国人患有TBI。即使是细微的,可能是无害的轻度TBI(这是TBI的最常见形式),也可能产生长期后果并导致巨大的医疗费用。直到最近,人们对伤害随着时间的流逝而扩大和进展的机制仍知之甚少。研究技术的技术进步允许对可能有助于认知下降的长期临床表现的研究进行改进。
TBI的症状表现在称为CTE的疾病中。CTE本质上是神经变性和进行性疾病。这种疾病可以存在于任何人中,特别是那些容易遭受重复性头部损伤的人,尤其是士兵和运动员。CTE的持续症状包括冲动性、攻击性和运动功能障碍。长期症状包括记忆力减退和认知下降。对来自CTE患者的脑(brain)进行的死后评估已显示,tau神经原纤维缠结在血管周围的积聚在不同的脑区域和沟深处。Tau神经原纤维缠结是调节微管结构的过度磷酸化tau蛋白的聚集形式。
已经存在对由于反复性脑震荡或亚脑震荡损伤的结果的CTE的发展的最低限度的理解。如前所述,CTE的特征在于存在聚集的tau神经原纤维缠结。然而,尚不清楚TBI如何导致过度磷酸化的tau的发展以及向CTE的进展。因此,迫切需要确定调节tau磷酸化和去磷酸化(分别为激酶和磷酸酶)的机制,以阐明TBI如何导致CTE,进而最小化或排除TBI向CTE的进展。
在针对阿尔茨海默氏病(AD)蛋白质聚集的研究中,已经确定了与tau磷酸化调控有关的机制。由蛋白质聚集诱导的一种机制是称为内质网(ER)应激的细胞应激反应。已显示在神经原纤维缠结发展之前,ER应激的标志物在AD模型中升高,并与过度磷酸化的tau共同定位或位于同一细胞中。一旦缠结形成,与ER应激的联系就会消失,这很可能是由于缠结的形成代表了不可逆的步骤。从治疗的角度来看,在早期时间点调整ER应激可能呈现一种可行的干预和保护策略。在AD的临床前研究中,salubrinal在调整ER应激方面已显示出令人鼓舞的结果。Salubrinal是充当eIF2α(真核翻译起始因子2α亚基)磷酸酶特异性抑制剂的药物,并且是ER应激诱导的凋亡的特异性抑制剂(a specific inhibitor or ER stressinduced apoptosis)。
本领域中需要发展有效治疗或减轻TBI作用,以治疗或减轻CTE进展的方法。此外,需要发展调节tau磷酸化和去磷酸化的机制,以使过度磷酸化的tau可以被最小化或排除,从而防止TBI和CTE的发展或减轻其作用。
发明内容
一方面,本发明涉及减轻人的创伤性脑损伤或减少人的慢性创伤性脑病的发展的方法。所述方法包括给人施用治疗有效量的具有如下结构I的3-苯基-N-[2,2,2-三氯-1-[[(8-喹啉基氨基)硫代甲基(thioxomethyl)]氨基]乙基]-2-丙烯酰胺或其药学上可接受的盐:
给人施用的步骤可以包括选自注射、肠胃外和口服的一种或多种技术。
在某些实施方案中,治疗有效量是每日剂量。
在某些实施方案中,治疗有效量是通过静脉注射10mg的剂量,通过腹腔内注射50mg的剂量和口服100mg的剂量。
在另一方面,本发明涉及减轻创伤性脑损伤或减少慢性创伤性脑病的发展的方法。所述方法包括制备药物组合物,其包括获得具有如下结构I的3-苯基-N-[2,2,2-三氯-1-[[(8-喹啉基氨基)硫代甲基]氨基]乙基]-2-丙烯酰胺的活性化合物或其药学上可接受的盐:
并将如上所述的活性化合物与药学上可接受的载体或赋形剂组合;并给患有创伤性脑损伤和慢性创伤性脑病中至少一种的人施用治疗有效量的药物组合物。
药学上可接受的载体或赋形剂可以是选自固体和液体的形式。优选的赋形剂是固体。
优选的赋形剂是1,4-二氢-N-甲基烟酸(二氢葫芦巴碱),其被选择来增强血脑屏障的渗透性。
载体或赋形剂可以选自惰性填充剂,稀释剂,粘合剂,润滑剂,崩解剂,溶液阻滞剂(solution retardant),吸收促进剂(resorption accelerator),吸收剂(absorptionagent),着色剂及其混合物或组合。粘合剂可以选自淀粉,明胶,葡萄糖,β-乳糖,玉米甜味剂,阿拉伯胶,黄芪胶,海藻酸钠,羧甲基纤维素,聚乙二醇,蜡及其混合物或组合。优选的混合物将是亲脂的,以增强对脑的渗透性。
药物组合物可以是片剂形式。
在某些实施方案中,药物组合物可包括按重量计0.05%至95%的活性化合物。
药物组合物可包括选自医药剂(medicinal agents),药物剂(pharmaceuticalagents),辅助剂,稀释剂,媒介物及其混合物或组合的添加剂。
本发明的另一方面是减轻人的创伤性脑损伤或减少人的CTE的发展的方法。该方法包括给人施用治疗有效量的选自以下的至少一种化合物:
(i)具有如下结构I的3-苯基-N-[2,2,2-三氯-1-[[(8-喹啉基氨基)硫代甲基]氨基]乙基]-2-丙烯酰胺或其药学上可接受的盐:
和
(ii)具有如下结构II的胍那苄或其药学上可接受的盐:
附图说明
当结合附图阅读时,可以从以下优选实施方案的描述中获得对本发明的进一步理解。
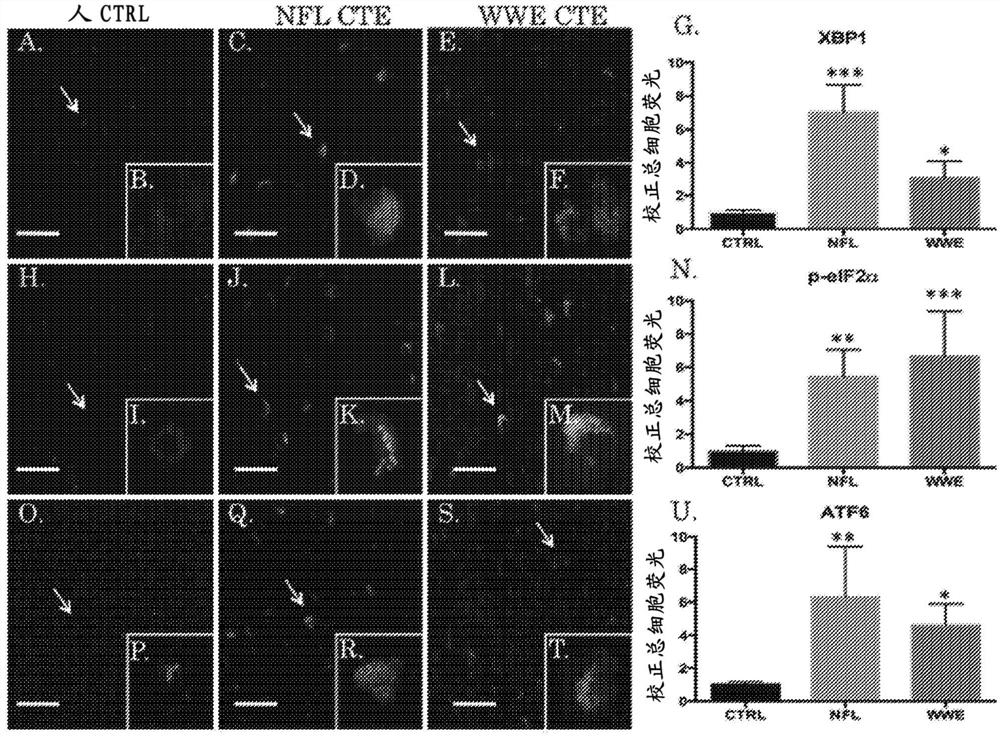
图1是显示被诊断为CTE的国家橄榄球联盟(NFL)球员,被诊断为CTE的WWE摔跤运动员以及对照(CTRL)样品的UPR脑的ER应激级联增加的图像和绘图(plot),其中Xbox结合蛋白1(XBP1)标记支路(arm)2,p-eIF2α标记支路1,且ATF6标记支路3。
图2是显示ER应激标志物肌醇需求酶1α(inositol requiring enzyme 1alpha)(IRE1α)与神经原纤维缠结标志物AT270在图1的相同CTE样品中显著共定位的图像。
图3是显示在病理性tau磷酸化的相同区域中tau激酶GSK3β增加的图像。
图4是显示用于产生数据的大鼠的空气加速性损伤模型的图像和绘图。
图5是阐明单次冲击伤后24小时salubrinal显著减少CHOP和GADD34(ER应激的标志物)的绘图。
图6是通过免疫组织化学显示salubrinal施用的冲击后保护益处的图像和绘图。
图7是显示salubrinal在损伤后24小时通过改变ER应激级联减少氧化应激的图像和绘图。
图8是阐明salubrinal在损伤后24小时通过成功地终止ER应激级联减少神经炎症的图像。
图9是显示在一个月(对冲性(contrecoup)脑半球(对侧)最终损伤后),重复冲击引起的tau蛋白病(tauopathy)标志物AT8和AT270增加的图像和绘图。
图10是显示了在重复性损伤后三周,ER应激的总体抑制剂(global inhibitor)(DHA)抑制了ER应激活化剂BiP和tau激酶GSK3β的图像和绘图。
图11是显示单次损伤后7天salubrinal减少冲动样行为的图像和绘图。
图12是显示重复损伤后72小时salubrinal通过防止在高架十字迷宫(elevatedplus maze)的开放支路中花费的时间而减少冲动样行为的图像和绘图。
图13是显示在的ER应激抑制如何改善损伤后认知学习(通过Morris水迷宫(Morris Water Maze)测量(图板(panel)D))和增强学习事件的保留(通过空间探索(probetrail)测量(图板E))的图像和绘图。
发明详述
本发明涉及治疗、减少或排除慢性创伤性脑病(CTE)的发展的化合物、组合物和方法。已经发现创伤性脑损伤(TBI)可能导致CTE的发展和进展。因此,本发明的目的是减轻TBI的进展,并使CTE的发展或进展最小化。
CTE的特征可能在于存在过度磷酸化的tau蛋白和神经原纤维缠结。因此,可通过确定调节或控制tau蛋白磷酸化的机制(从而减少或排除过度磷酸化)来减少或排除CTE的发展或进展。然而,总的来说,蛋白质磷酸化实际上调节着所有生物学过程,且尽管蛋白质激酶是众所周知的药物靶点,但已证明靶向蛋白质磷酸酶具有挑战性。
不受任何特定理论的束缚,据信内质网(ER)应激在TBI和CTE的发展和进展中起作用。ER是负责蛋白质折叠的细胞器。当由于新合成的未折叠或错误折叠的蛋白质在ER腔中积聚而使ER变得应激时,未折叠蛋白反应(UPR)被激活。UPR是在真核细胞中响应ER应激而激活的信号传导机制。UPR可以恢复和维持ER中的稳态,从而促进细胞存活,或者在ER应激保持不减轻的情况下诱导凋亡。
神经炎症和ER应激与许多神经系统疾病有关。因此,本发明的目的是给人(例如TBI患者)施用治疗有效量的ER应激抑制性化合物,以调节或抑制(例如减少或防止)ER应激,并进而稳定、消退或排除CTE。
根据本发明,确定了导致神经原纤维缠结发展的机制,并且靶向了有助于缠结的通路,即ER应激,从而减少了CTE患者的短期和长期症状和行为。ER应激具有三个不同的支路或信号分支,它们在多种形式的扰动后在恢复急性细胞稳态中发挥作用。第一、第二和第三支路如下:(1)蛋白激酶R(PKR)样内质网激酶(PERK),(2)肌醇需求酶-1(IRE-1);和(3)转录激活因子6(ATF6)。
通常,ER应激导致在ER腔中ER分子伴侣BiP与错误折叠的蛋白质的结合增加,从而导致BiP与ER应激转导物PERK、IRE-1和ATF6解离,从而导致其激活。激活的(磷酸化的)PERK使eIF2α磷酸化,并因此减弱蛋白质翻译以减轻应激过程中的ER工作量。同时,eIF2α磷酸化增强了ATF4翻译。ATF4诱导分子伴侣和CHOP的转录。CHOP诱导GADD34的表达。IRE-1激活(磷酸化)导致XBP1 mRNA剪接,产生转录因子sXBP1。
当ER应激持续存在或具有长期活性时,tau激酶GSK3β变得过度活跃,并充当tau过度磷酸化,后续聚集和细胞积聚的催化剂。该通路最终导致神经发炎,使损伤持续存在并随时间进展,并可能导致进行性神经变性。
根据本发明,已经发现,与没有患CTE的人脑相比,UPR的ER应激级联的所有三个支路在患有CTE的人的脑中可以增加。
在本发明的一个实施方案中,给人(例如患者)施用salubrinal,以治疗或减轻TBI的作用,防止或减少CTE发展的可能性,以及治疗或减轻CTE的进展。通常,salubrinal已主要在实验上用于研究真核细胞中与eIF2作用相关的应激反应。Salubrinal是eIF2去磷酸化的选择性抑制剂。已经用salubrinal进行了潜在治疗骨质疏松并加速骨愈合的研究。“Salubrinal”被用作市售药物的商品名。本发明中使用的“salubrinal”的化学名称是3-苯基-N-[2,2,2-三氯-1-[[(8-喹啉基氨基)硫代甲基]氨基]乙基]-2-丙烯酰胺(C
根据本发明,以治疗有效量给患者施用化学结构I(化合物I)或其药学上可接受的盐,并将化学结构I(化合物I)或其药学上可接受的盐用于安全地和选择性地靶向ER应激通路。化合物I的施用作为用于TBI和CTE的治疗可以稳定、消退、减少或排除在患者中的发展和进展。
如本领域技术人员将理解的,可以通过本领域已知的任何方式将治疗有效量的化合物I施用于患者,所述方式包括但不限于注射、肠胃外和口服。确定什么剂量以及该剂量的频率在本领域技术人员的技能范围内,这将构成每个患者的治疗有效量。
在某些实施方案中,化合物1的治疗有效量是1至100mg的剂量。在某些实施方案中,化合物1的治疗有效量是以10mg通过静脉(IV)注射,或以50mg通过腹腔内(IP)注射,或以100mg口服施用。此外,剂量可以以每天为基础。
可以将本发明的化合物配制成药物组合物,所述药物组合物通常包括常规的药物载体或赋形剂以及作为活性剂的化合物1(或其药学上可接受的盐)。另外,该组合物可以包括其他医药剂,药物剂,载体,辅助剂,稀释剂,媒介物或其组合。这样的药学上可接受的赋形剂,载体或添加剂以及制备用于各种模式或施用的药物组合物的方法是本领域技术人员众所周知的。在与组合物的其他成分相容的情况下,所使用的载体或赋形剂是可接受的,并且不得对患者有害。载体或赋形剂可以是固体或液体,或两者均可,并且优选与本发明化合物配制成单位剂量组合物,例如片剂,其可以含有按重量计0.05%至95%的活性化合物。这样的载体或赋形剂包括惰性填充剂或稀释剂,粘合剂,润滑剂,崩解剂,溶液阻滞剂,吸收促进剂,吸收剂和着色剂。合适的粘合剂包括淀粉,明胶,天然糖例如葡萄糖或β-乳糖,玉米甜味剂,天然的和合成的树胶例如阿拉伯胶,黄芪胶或海藻酸钠,羧甲基纤维素,聚乙二醇,蜡等。润滑剂包括油酸钠,硬脂酸钠,硬脂酸镁,苯甲酸钠,乙酸钠,氯化钠等。崩解剂包括淀粉,甲基纤维素,琼脂,膨润土,黄原胶等。
药学上可接受的载体和赋形剂涵盖所有上述添加剂等。
在某些实施方案中,药学上可接受的赋形剂优选是固体形式。
在某些实施方案中,优选的赋形剂是1,4-二氢-N-甲基烟酸(二氢葫芦巴碱),其被选择来增强血脑屏障的渗透性。
本文提供的说明书主要集中于化合物1。然而,本发明不限于化合物1的用途。应理解并考虑提供与化合物1相同或相似抑制活性(以靶向ER应激通路)的其他化合物或组合物可用作化合物1的代用品或替代物,或与化合物1的互补物。例如,本发明还包括具有如下化学结构的胍那苄(C
该化合物可以商品名WYTENSIN获得。化合物II是α-2肾上腺素能受体的α激动剂,且属于被称为抗高血压药的一般类别药物。已知使用化合物II通过控制沿某些神经通路的神经冲动,舒张血管并使血液更容易通过来治疗高的血液压力(high blood pressure)例如高血压(hypertension)。
尽管已经详细描述了本发明的特定实施例,但是本领域技术人员将理解,可以根据本公开的整体教导对这些细节进行各种修改和替换。因此,所公开的具体实施例仅是说明性的,并且不限制本发明的范围,本发明的范围由所附权利要求及其任何和所有等同形式的全部范围给出。
实施例
ER应激在TBI和CTE中的作用
使用动物模型评估TBI,并使用神经病理学标本(由脑损伤研究所脑库捐赠)评估CTE。TBI是在动物模型中冲击诱导的。对于冲击诱导的TBI(bTBI),测试数据显示ER应激急剧上调,即在损伤的前24小时内。损伤后给动物模型施用Salubrinal。ER应激是通过使用salubrinal来调整的。经发现,施用salubrinal导致减少了神经变性和凋亡的标志物。
还在动物模型中评估了bTBI之前施用salubrinal。使用saubrinal改善了以冲动样行为和空间记忆为形式的神经精神缺陷,所述冲动样行为通过高架十字迷宫测试/方案测量,所述空间记忆通过Morris水迷宫测试/方案测量。
使用用于CTE的神经病理学样品,测试数据显示,与不存在CTE的脑(即对照(“CTRL”)脑)相比,ER应激显著上调,并且发现ER应激与过度磷酸化tau共定位。
bTBI动物模型和CTE神经病理学标本的结果表明,ER应激代表TBI与CTE的发展之间的机制联系。此外,用salubrinal调整ER应激代表了用于减轻TBI的作用,和防止或减少CTE发展和进展的可能性的治疗方法。
实施例1
从被诊断为死后CTE的运动员的内嗅皮层收集人脑标本。对标本进行单独的ER应激标志物染色,并还与tau蛋白病标志物共定位。传统的免疫组织化学方法与对ER应激和病理性tau特异的一抗以及荧光二抗结合使用。用共定位软件(即ImageJ)检测重叠区域。ANOVA用于校正总细胞荧光分析。P<0.05被认为具有统计学意义。(*=p<0.05,**=p<0.01,和***=p<0.001)。
结果表明,人CTE标本中ER应激通路的所有三个支路都增加了。还发现在观察到tau蛋白病的相同区域内,ER应激增加,这暗示了在疾病过程中的ER应激。通过糖原合酶激酶β,即GSK3β(与ER应激有关的催化tau激酶)染色,以及发现GSK3β也与tau标志物共定位证实了这一点。
图1显示了分别在图像A-F,H-M和O-T以及相应的绘图G,N和U中的免疫组织化学结果,其阐明了与没有CTE的人对照(CTRL)样品相比,在被诊断为CTE的国家橄榄球联盟(NFL)球员的脑中和被诊断为CTE的WWE摔跤运动员的脑中,未折叠蛋白反应的ER应激级联的所有三个支路都增加了。A-G显示,与人CTRL样品相比,CTE样品中的X-box结合蛋白1(XBP1)增加(ER应激通路的第二支路)。H-N显示,与人CTRL样品相比,CTE样品中的磷酸化延伸起始因子2α(p-eIF2α)增加(ER应激通路的第一支路,也是salubrinal的靶点)。与人CTRL样品相比,O-U显示的CTE样品中激活的转录因子6(ATF6)也增加了(ER应激通路的第三支路)。p-eIF2α是重要的,因为它是抑制的主要靶点。
图2显示了图像M-R和A-F,其阐明了肌醇需求酶1α(IRE1α)是内质网应激的标志物,其与神经原纤维缠结标志物AT270(分别来自NFL球员和WWE摔跤运动员和人CTRL样品的相同CTE样品中)显著共定位。重叠图板中的染色(图像Aa-Dd)表明ER应激与相同神经元细胞中的tau蛋白病有关。对于NFL球员和WWE摔跤运动员,在二者CTE病例的脑中,重叠系数均为~0.9,这表明细胞内的共定位水平很高。
图3显示了图像M-R和A-F,其分别阐明了tau激酶GSK3β在观察到病理性tau磷酸化(AT100)的相同区域中显著增加。重叠图板中的染色(图像Aa-Dd)表明tau激酶与磷酸化有关。重叠系数为0.88,表明细胞内的共定位水平很高。通常,tau激酶导致tau过度磷酸化,这改变了构象形状并使其在细胞内积聚。
实施例2
该实施例评估了TBI后成功地靶向ER应激。如图4中的图像A和B所示,开发了桌面空气加速性损伤模型。将Sprague Dawley大鼠置于保护管中,以防止对周围器官的损伤,并产生加速度波并使其与大鼠的头骨碰撞。通过减小或增加用加压氮气爆炸的膜的厚度,以逐步的方式调节损伤的强度。选择了50PSI的损伤范式,它与人脑震荡相关,人脑震荡是与CTE相关的最常见损伤类型。在图4中,绘图D中的峰值示出了50PSI压力波。Sprague Dawley大鼠在两周内受到了一次或六次损伤。选择处死的各个时间点以观察ER应激和tau蛋白病的标记物。
损伤后给大鼠施用Salubrinal以靶向ER应激。损伤后30分钟通过IP注射用1mg/kg的剂量施用Salubrinal。经发现,salubrinal抑制GADD34以改变ER应激,并防止了促死亡信号(pro-death signal)CHOP的激增,这降低了GSK3β的活性,并因此防止了最初的tau蛋白病级联。salubrinal介导的CHOP减少可能与胱天蛋白酶-12的原形式的保存有关,而胱天蛋白酶-12的原形式(pro-form)被切割后与ER介导的凋亡或细胞死亡有关。用salubrinal减少CHOP也可能导致持续的氧化应激和神经炎症的减少。
如图5-9所示,在损伤后各个时间点使用了蛋白质印迹分析,免疫组织化学和PCR。使用LICOR蛋白质印迹方案,IHC世界免疫组织化学方案和Applied Biosystems PCR方案用于测定。使用ANOVA进行分析,p<0.05具有统计学意义。*=p<0.05,**=p<0.01,***=p<0.001。当将药物组与损伤组进行比较时,#=p<0.05,##=p<0.01,###=p<0.001。
图5显示了绘图,其阐明了单次冲击伤后24小时(bTBI24h),salubrinal(SAL+bTBI)显著减少了作为ER应激标志物的CHOP(参见绘图C)和GADD34(参见绘图E),从而有效终止了ER应激反应。
图6显示了图像和绘图,其通过免疫组织化学结果证实了冲击后施用salubrinal(SAL-bTBI)的保护益处。CHOP显著减少,这也与切割的胱天蛋白酶3(与凋亡相关的活性形式)减少有关。因此,如在绘图A和C中冲击诱导的TBI(bTBI)和bTBI后施用salubrinal(SAL-bTBI)所示,salubrinal减少了CHOP以及促凋亡标志物胱天蛋白酶-3。
图7显示了图像和绘图,其阐明了salubrinal在损伤后24小时通过改变ER应激级联减少氧化应激。测量的组分包括羰基(图A),超氧化物(图B),活性氧(ROS)(图C)和NADPH氧化酶4(NOX4)(图D)。如图A、B和D所示,施用salubrinal(sTBI+SAL)分别减少了蛋白质羰基,超氧化物和总氧化应激的产生。
图8显示了绘图,其阐明salubrinal在损伤后24小时通过成功地终止ER应激级联减少神经炎症。测量的组分包括NFκB(绘图A),可诱导一氧化氮合酶(iNOS)(绘图B),白介素1β(IL-1β)(绘图C)和肿瘤坏死因子α(TNFα)(绘图D)。如绘图A、C和D所示,施用salubrinal(sTBI+SAL)分别减少了促炎性标志物NFκB、IL-1β和TNFα。
图9显示了图像和绘图,其阐明了重复冲击在一个月和对冲性脑半球(对侧)中的最终损伤之后分别引起了tau蛋白病标志物AT8(绘图A和B)和AT270(绘图E和F)的增加。
图10显示了图像和绘图,其在绘图A和绘图B中分别阐明了在重复性损伤后三周,ER应激的总体抑制剂(DHA)抑制了ER应激活化剂BiP和tau激酶GSK3β。
实施例3
在此实施例中,通过利用损伤模型和用于Morris水迷宫和高架十字迷宫的标准方案研究了靶向(关掉(turning off))ER应激对改善行为的作用。Morris水迷宫检测到认知表现(cognitive performance)不足,而高架十字迷宫则评估了冲动样行为。结果表明,如果在损伤后提供靶向ER应激,其可以减少冲动样行为并改善认知行为。使用ANOVA进行统计学分析,其中*=p<0.05,**=p<0.01,***=p<0.001。当将药物与损伤组比较时,#=p<0.05,##=p<0.01,###=p<0.001。
图11显示了图像和绘图,其阐明了在单次损伤后7天损伤后施用salubrinal(SAL+bTBI)减少冲动样行为,这通过在高架十字迷宫的开放支路中减少的时间来测量。绘图A显示了在开放支路中较少的时间,例如行程。
图12显示了图像和绘图,其阐明了重复损伤后72小时,损伤后施用salubrinal(rTBI+SAL)通过防止在高架十字迷宫的开放支路中花费的时间减少冲动样行为。
图13显示了绘图,其阐明了ER应激(DHA)抑制如何改善损伤后的认知学习(通过Morris水迷宫测量(图板D))和增强学习事件的保留(通过空间探索测量(图板E))。
结果/结论
ER应激被确定为在人TBI后慢性神经变性发展中的关键通路。在实施例中,该通路是在啮齿动物模型(bTBI)中靶向的,并且结果证明了氧化应激和神经炎症的后续激活被阻止。通过施用salubrinal以有效地关闭(终止)ER应激通路,行为得到了改善。具体地,抑制ER应激级联可显著减少冲动样缺陷和认知下降。通过施用salubrinal来靶向ER应激的益处为TBI患者提供了潜在的诊断和治疗方法。
- 慢性创伤性脑病的治疗
- 用于预防和/或治疗II型慢性创伤性脑病的方法
