一种检测MET E14跳跃突变的方法
文献发布时间:2023-06-19 11:40:48
技术领域
本申请涉及生物技术领域,特别涉及一种检测MET E14跳跃突变的方法。
背景技术
研究发现MET基因14号外显子(MET exon 14,MET E14)跳跃缺失(skipping)突变多发生于非小细胞肺癌,并以其中的肺肉瘤样癌和肺腺癌更多见。在肺腺癌中的发生率约3~4%,在肺肉瘤样癌中的发生率可高达22%。MET E14突变已成为靶向治疗非小细胞肺癌的重要靶点。
目前现有的用于检测MET 14号外显子跳跃突变的方法主要包括c-MET免疫组化染色、直接针对DNA的Sanger测序以及下一代测序(next-generation sequencing,NGS,又称高通量测序)。c-MET免疫组化染色由于需要较多临床标本,且其用于检测MET 14号外显子跳跃突变的特异度较低,故临床较少应用。NGS是目前获得美国NCCN指南推荐的MET 14号外显子跳跃突变的检测方法,但成本较高、缺乏可靠统一临界值标准等因素限制了NGS检测MET 14号外显子跳跃突变的进一步应用。因此,急需一种能够精准、高效地检测MET14号外显子跳跃突变的方法,从而可以筛选出潜在的肺癌患者,并对其进行精准治疗。
发明内容
根据本申请的一方面,提供了一种用于检测MET基因14号外显子跳跃突变的试剂盒,其特征在于,所述试剂盒包括PCR扩增体系。PCR扩增体系包括以下引物和探针:如SEQID NO.1所示的上游引物,如SEQ ID NO.2所示的下游引物,以及如SEQ ID NO.3所示的用于特异性检测MET基因14号外显子跳跃突变的探针。
在一些实施例中,PCR扩增体系还可以包括用于特异性扩增和检测对照基因的引物和探针。
在一些实施例中,对照基因可以为GAPDH,所述用于特异性扩增和检测对照基因的引物和探针可以包括如SEQ ID NO.4所示的上游引物。
在一些实施例中,所述对照基因可以为GAPDH,所述用于特异性扩增和检测对照基因的引物和探针可以包括如SEQ ID NO.5所示的下游引物。
在一些实施例中,所述对照基因可以为GAPDH,所述用于特异性扩增和检测对照基因的引物和探针可以包括如SEQ ID NO.6所示的探针。
在一些实施例中,所述试剂盒中的PCR扩增体系中,各引物的终浓度可以为200-400nM。
在一些实施例中,所述试剂盒中的PCR扩增体系中,各探针的终浓度可以为200-400nM。
在一些实施例中,所述试剂盒中的PCR扩增体系还可以包括dNTP、模板、热启动Taq酶以及MgCl
在一些实施例中,所述试剂盒还可以包括反转录体系,所述反转录体系可以包括如SEQ ID NO.7所示的引物。
在一些实施例中,所述试剂盒还可以包括反转录体系,所述反转录体系包括如SEQID NO.8所示的引物。
在一些实施例中,所述试剂盒还可以包括反转录体系,所述反转录体系可以包括终浓度为200nM的反转录引物。
在一些实施例中,所述反转录体系还可以包括dNTP和super RT反转录酶。
在一些实施例中,所述如SEQ ID NO.3所示的用于特异性检测MET基因14号外显子跳跃突变的探针的5’端可以标记有荧光基团FAM,3’端可以标记有淬灭基团MGB。
根据本申请的另一方面,提供了一种检测MET基因14号外显子跳跃突变的试剂在制备用于鉴定受试者有利地响应卡马替尼或克唑替尼的可能性的试剂盒中的应用。所述检测MET基因14外显子跳跃突变的试剂可以包括:如SEQ ID NO.1所示的上游引物,如SEQ IDNO.2所示的下游引物,以及如SEQ ID NO.3所示的用于特异性检测MET基因14外显子跳跃突变的探针;所述应用包括以下步骤:1)获取受试者的样品;2)从所述样品中提取RNA;3)使用所述试剂盒,对所述提取出来的RNA进行逆转录得到样品cDNA;4)使用所述试剂盒,对所述样品cDNA进行荧光定量PCR反应;5)确定是否能检测到所述荧光定量PCR反应中对应于MET基因的Ct值,若能检测到CT值,则判定所述样品中存在MET基因14号外显子跳跃突变,并且鉴定为所述受试者有利地响应卡马替尼或克唑替尼的可能性较高。
附图说明
本申请将以示例性实施例的方式进一步说明,这些示例性实施例将通过附图进行详细描述。这些实施例并非限制性的,其中:
图1为根据本申请一些实施例所示的用于检测MET E14跳跃突变的系统100的应用场景示意图;
图2是根据本申请一些实施例所示的计算设备200的架构的示意图;
图3是根据本申请一些实施例所示的检测MET E14跳跃突变系统的模块图;
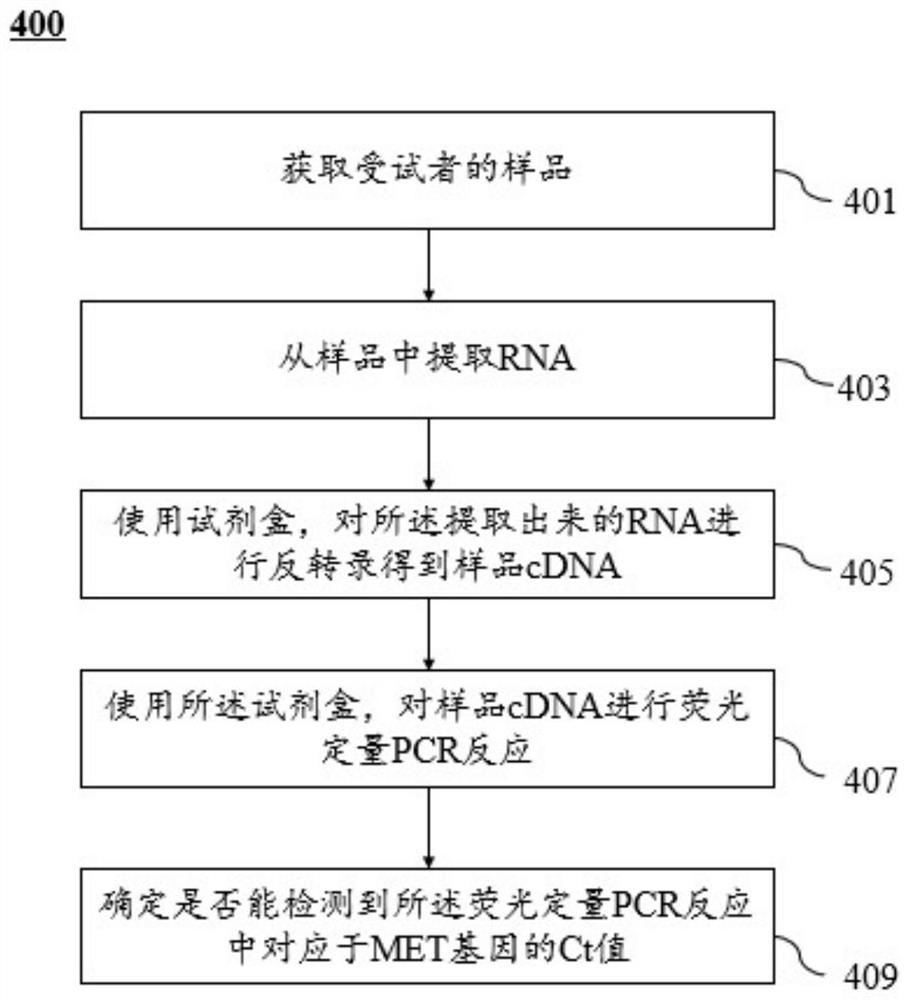
图4是根据本申请一些实施例所示的检测MET基因14号外显子跳跃突变的试剂在制备用于鉴定受试者有利地响应卡马替尼或克唑替尼的可能性的试剂盒中的应用方法;
图5是根据本申请一些实施例所示的MET E14具有Ct值和GAPDH的扩增曲线图;
图6是根据本申请一些实施例所示的MET E14无Ct值和GAPDH的扩增曲线图;
图7是根据本申请一些实施例所示的患者1的扩增曲线图;
图8是根据本申请一些实施例所示的患者2的扩增曲线图;
图9是根据本申请一些实施例所示的患者3的扩增曲线图。
具体实施方式
为了更清楚地说明本申请实施例的技术方案,下面将对实施例描述中所需要使用的附图作简单的介绍。显而易见地,下面描述中的附图仅仅是本申请的一些示例或实施例,对于本领域的普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图将本申请应用于其它类似情景。除非从语言环境中显而易见或另做说明,图中相同标号代表相同结构或操作。
应当理解,本文使用的“系统”、“装置”、“单元”和/或“模组”是用于区分不同级别的不同组件、元件、部件、部分或装配的一种方法。然而,如果其他词语可实现相同的目的,则可通过其他表达来替换该词语。
如本申请和权利要求书中所示,除非上下文明确提示例外情形,“一”、“一个”、“一种”和/或“该”等词并非特指单数,也可包括复数。一般说来,术语“包括”与“包含”仅提示包括已明确标识的步骤和元素,而这些步骤和元素不构成一个排它性的罗列,方法或者设备也可能包含其它的步骤或元素。
本申请中使用了流程图用来说明根据本申请的实施例的系统所执行的操作。应当理解的是,前面或后面操作不一定按照顺序来精确地执行。相反,可以按照倒序或同时处理各个步骤。同时,也可以将其他操作添加到这些过程中,或从这些过程移除某一步或数步操作。
以下是对本申请中一些术语的定义。
如本申请中所使用的,“受试者”(也可称为“个体”、“对象”)可以是人类或动物。在一些实施例中,受试者可以是脊椎动物。在一些实施例中,脊椎动物为哺乳动物。哺乳动物包括但不限于灵长类以及啮齿动物(例如,小鼠和大鼠)。在一些实施例中,受试者可以是人。在一些实施例中,受试者为患有肺癌的对象。例如,受试者可以是患有非小细胞肺癌(NSCLC)的对象。例如,受试者可以患有肺肉瘤样癌和肺腺癌。在一些实施例中,受试者可以接受MET基因14号外显子跳跃突变检测,从而确定受试者对药物产生有利响应的可能性。例如,所述药物可以是卡马替尼或克唑替尼。
术语“MET 14号外显子跳跃突变”(或MET 14号外显子跳跃缺失)指的是MET基因14号外显子在mRNA水平出现部分或完全跳跃缺失。造成的原因可能为:MET 14号外显子两侧剪接供体及受体位点的突变(例如,删除、插入和插入缺失突变、点突变)导致MET基因转录后前mRNA的剪接过程中14号外显子随其两端的内含子一同被剪接,从而产生缺少MET 14号外显子的成熟mRNA。
术语“引物”是指能够与核酸杂交并且通常通过提供游离3’-OH基团,允许互补核酸聚合的单链多核苷酸。
术语“聚合酶链式反应(PCR)”是一种用于放大扩增特定的DNA片段的分子生物学技术。
术语“实时荧光定量PCR(Quantitative Real-time PCR)”也可称为qPCR、RT-PCR。qPCR是一种在DNA扩增反应中,通过荧光化学物质检测每次聚合酶链式反应(PCR)循环后产物总量的方法,可通过内参或者外参法对待测样品中的特定DNA序列进行定量分析。
术语“探针”是指能够选择性结合靶生物分子(例如,与探针杂交的核酸序列)的任何分子。在一些实施例中,探针可检测地被标记,例如用荧光基团和淬灭基团标记。
术语“样品”是指从受试者分离出的含有核酸的任何组合物。该术语可以包括纯化的或分离的细胞、组织或血液的组分,例如,DNA、RNA、蛋白、无细胞部分或细胞裂解物。
本申请提供了一种用于检测MET基因14号外显子跳跃突变的试剂盒。该试剂盒可以包括PCR扩增体系和反转录体系。PCR扩增体系可以包括通过特异性设计的用于特异性检测MET基因14外显子跳跃突变的探针和上下游引物。从受试者的样品中可以提取出RNA,并使用该试剂盒对所述RNA进行逆转录得到cDNA,通过该试剂盒中的上下游引物以及探针对cDNA进行荧光定量PCR,能够检测出样品中的MET E14是否发生了跳跃突变。若检测到cDNA的Ct值,则可以判定样品中存在MET E14跳跃突变;若未能检测到Ct值,则可以判定受试者的样品中不存在MET E14跳跃突变。通过本申请的试剂盒,能够准确且快速地检测到MET 14号外显子跳跃突变的存在。
本申请还提供了一种检测MET基因14号外显子跳跃突变的试剂在制备用于鉴定受试者有利地响应卡马替尼或克唑替尼的可能性的试剂盒中的应用。通过使用上述试剂盒,能够判定出受试者的样品中存在MET E14跳跃突变,从而判定使用MET E14跳跃缺失的靶向药物(例如,卡马替尼、克唑替尼)对受试者进行治疗的效果可能较好,并进一步给予受试者精准治疗。
图1为根据本申请一些实施例所示的检测MET E14跳跃突变系统100的应用场景示意图。如图1所示,检测MET E14跳跃突变系统100可以包括处理设备110、网络120和存储设备130。在一些实施例中,存储设备130可以存储受试者(例如,受试者140)的基础信息、疾病史、治疗方案等数据,还可以存储受试者140的基因表达信息,例如受试者的MET E14和内参基因的Ct值等。存储设备130可以存储一项或多项数值(例如,荧光定量PCR反应的阈值线、反应的循环数)等数据。受试者的样品,例如样品145,可以保存在专门的储藏设备中以备进一步处理,例如进行RNA提取等。在一些实施例中,样品145可以是组织样品或体液样品。具体的,样品145可以是组织样品。处理设备110可以用于对相关信息进行处理、分析以生成判定结果。在一些实施例中,处理设备110可以从存储设备130中获取相关的信息和/或数据(例如,MET E14的Ct值等),也可以直接获取工作人员或者其他设备仪器对目标受试者140的样品145进行处理得到的相关信息和/或数据。
处理设备110可以处理从存储设备130处获得的数据和/或信息。例如,处理设备110可以对样品cDNA进行荧光定量PCR反应,并确定是否能检测到所述荧光定量PCR反应中对应于MET基因的Ct值,根据Ct值是否存在而判定样品中是否存在MET E14跳跃突变,并进一步鉴定受试者有利地响应卡马替尼或克唑替尼的可能性较高还是较低。在一些实施例中,处理设备110可以是一个单个的处理器或者一个处理器群组。该处理器群可以是集中式的或分布式的(例如,处理设备110可以是一个分布式的系统)。在一些实施例中,处理设备110可以是本地的或远程的。在一些实施例中,处理设备110可以通过网络120从存储设备130处获取信息和/或数据。在一些实施例中,处理设备110可以在一个云平台上实现。仅仅举个例子,该云平台可以包括私有云、公共云、混合云、社区云、分布云、云之间、多重云等或上述举例的任意组合。处理设备110可包含中央处理器(CPU)、专用集成电路(ASIC)、专用指令处理器(ASIP)、图形处理器(GPU)、物理处理器(PPU)、数字信号处理器(DSP)、现场可编程门阵列(FPGA)、可编辑逻辑电路(PLD)、控制器、微控制器单元、精简指令集电脑(RISC)、微处理器等或以上任意组合。
网络120可以提供信息交换的渠道。在一些实施例中,处理设备110和存储设备130之间可以通过网络120交换信息。例如,处理设备110可以通过网络120接收存储设备130中的数据。在一些实施例中,受试者140和/或样品145的相关信息可以通过网络120传输给处理设备110和/存储设备130。例如,受试者140的信息(如MET E14的Ct值等)可以通过网络120传输给处理设备110。在一些实施例中,网络120可以是任意类型的有线或无线网络。例如,网络120可包括一缆线网络、有线网络、光纤网络、电信网络、内部网络、网际网络、区域网络(LAN)、广域网络(WAN)、无线区域网络(WLAN)、都会区域网络(MAN)、公共电话交换网络(PSTN)、蓝牙网络、ZigBee网络、近场通讯(NFC)网络等或以上任意组合。
存储设备130可以用于存储数据和/或指令集。在一些实施例中,存储设备130可以存储从处理设备110获得的数据。在一些实施例中,存储设备130可存储供处理设备110执行或使用的信息和/或指令,以执行本申请中描述的示例性方法。在一些实施例中,存储设备130中可以存储基因表达数据。在一些实施例中,存储设备130可以包括大容量存储器、可移动存储器、易失性读写存储器、只读存储器(ROM)等或其任意组合。在一些实施例中,存储设备130可以在云平台上实现。仅作为示例,云平台可以包括私有云、公共云、混合云、社区云、分布式云、中间云、多云等或其任意组合。在一些实施例中,存储设备130可以是处理设备110的一部分。
在一些实施例中,受试者140可以是患有癌症(例如非小细胞肺癌)的受试者。在一些实施例中,受试者140可以是患有肺肉瘤样癌和肺腺癌的受试者。在一些实施例中,受试者140可以患有一种或多种癌症。在一些实施例中,受试者140患有的癌症可以处在各个阶段(如早期、中期、晚期等)。
在一些实施例中,样品145可以用于反映受试者140中MET E14的相关信息。一些实施例中,该样品可以包括组织样品或体液样品。在一些实施例中,体液样品可以包括血液、组织液、淋巴液或脑脊液样品的一种或几种的组合。在一些实施例中,样品可以是组织样品。在一些实施例中,哺乳动物可以为人。
在一些实施例中,受试者140和/或样品145的相关信息可以通过人工(如工作人员手动输入)或机器(如仪器设备等)传输给检测MET E14跳跃突变系统100的一个或多个组件(如处理设备110、存储设备130)。
图2是根据本申请一些实施例所示的计算设备200的架构的示意图。如图2所示,计算设备200可以包括处理器210、存储器220、输入/输出接口230和通信端口240。在该计算设备200上可以实现处理设备110和/或存储设备130。在一些实施例中,一种检测MET E14跳跃突变装置可以在计算设备200中实现。例如,处理设备110可以在计算设备200上实现并且被配置为执行本申请中处理设备110的功能。例如,处理设备110可以检测获取自目标受试者的样品中MET E14的Ct值。又例如,处理设备110可以基于该生物样品中MET E14的Ct值,判定样品中是否存在MET E14跳跃突变,以及鉴定受试者有利地响应卡马替尼或克唑替尼的可能性较高还是较低。
处理器210可以执行计算指令(程序代码)并执行本申请描述的处理设备110的功能。计算指令可以包括程序、对象、组件、数据结构、过程、模块和功能(功能指本申请中描述的特定功能)。例如,处理器210可以处理检测MET E14跳跃突变系统100中确定MET E14的Ct值的指令。在一些实施例中,处理器210可以包括微控制器、微处理器、精简指令集计算机(RISC)、专用集成电路(ASIC)、应用特定指令集处理器(ASIP)、中央处理器(CPU)、图形处理单元(GPU)、物理处理单元(PPU)、微控制器单元、数字信号处理器(DSP)、现场可编程门阵列(FPGA)、高级RISC机(ARM)、可编程逻辑器件以及能够执行一个或多个功能的任何电路和处理器等,或其任意组合。仅为了说明,图2中只描述了一个处理器210,但需要注意的是本申请可以包括多个处理器。
存储器220可以存储从检测MET E14跳跃突变系统100中任何组件获得的数据/信息。在一些实施例中,存储器220可以包括大容量存储器、可移动存储器、易失性读取和写入存储器和只读存储器(ROM)等,或其任意组合。示例性大容量存储器可以包括磁盘、光盘和固态驱动器等。可移动存储器可以包括闪存驱动器、软盘、光盘、存储卡、U盘、压缩盘和移动硬盘等。易失性读取和写入存储器可以包括随机存取存储器(RAM)。RAM可以包括动态RAM(DRAM)、双倍速率同步动态RAM(DDRSDRAM)、静态RAM(SRAM)、晶闸管RAM(T-RAM)和零电容(Z-RAM)等。ROM可以包括掩模ROM(MROM)、可编程ROM(PROM)、可擦除可编程ROM(PEROM)、电可擦除可编程ROM(EEPROM)、光盘ROM(CD-ROM)和数字通用盘ROM等。
输入/输出接口230可以用于输入或输出信号、数据或信息。在一些实施例中,输入/输出接口230可以用于实现用户(例如,受试者140、检测MET E14跳跃突变系统100的使用者等)与处理设备110的交互行为。在一些实施例中,用户可以通过输入/输出接口230输入患者的特征信息。在一些实施例中,输入/输出接口230可以包括输入装置和输出装置。示例性输入装置可以包括键盘、鼠标、触摸屏和麦克风等,或其任意组合。示例性输出设备可以包括显示设备、扬声器、打印机、投影仪等,或其任意组合。示例性显示装置可以包括液晶显示器(LCD)、基于发光二极管(LED)的显示器、平板显示器、曲面显示器、电视设备、阴极射线管(CRT)等,或其任意组合。
通信端口240可以连接到网络120以便数据通信。连接可以是有线连接、无线连接或两者的组合。有线连接可以包括电缆、光缆或电话线等,或其任意组合。无线连接可以包括蓝牙、WiFi、WiMax、WLAN、ZigBee、移动网络(例如,3G、4G或5G等)等,或其任意组合。在一些实施例中,通信端口240可以是标准化端口,如RS232、RS485等。在一些实施例中,通信端口240可以是专门设计的端口。
图3是根据本申请一些实施例所示的检测MET E14跳跃突变系统的模块图。如图3所示,该检测MET E14跳跃突变系统可以包括获取模块310、判定模块320、存储模块330。
获取模块310可以用于获取荧光定量PCR相关的数据,例如,阈值线、反应循环数等。在一些实施例中,获取模块310可以获取用户可以手动输入的数据。在一些实施例中,数据可以预先存储在存储设备(例如,存储设备130)中,获取模块310可以从存储设备(例如,存储设备130)获取数据。
判定模块320可以用于确定是否能检测到荧光定量PCR反应中对应于MET基因的Ct值。在一些实施例中,判定模块320可以基于荧光定量PCR反应的结果(例如,扩增曲线)确定是否具有对应于MET基因的Ct值。在一些实施例中,判定模块320可以从存储器130中获取数据(例如,扩增曲线)再确定对应于MET基因的Ct值。
若Ct值存在,判定模块320还可以判定样品中存在MET基因14号外显子跳跃突变,并且鉴定为所述受试者可能有利地响应MET抑制剂(例如,卡马替尼或克唑替尼)的可能性较高,从而可以为受试者提供精准化的治疗。
存储模块330可以用于存储与荧光定量PCR相关的数据,例如,阈值线、反应循环数、扩增曲线、反应得到的Ct值(例如,MET基因的Ct值和对照基因的Ct值)等。
应当理解,图3所示的系统及其模块可以利用各种方式来实现。例如,在一些实施例中,系统及其模块可以通过硬件、软件或者软件和硬件的结合来实现。其中,硬件部分可以利用专用逻辑来实现;软件部分则可以存储在存储器中,由适当的指令执行系统,例如微处理器或者专用设计硬件来执行。本领域技术人员可以理解上述的方法和系统可以使用计算机可执行指令和/或包含在处理器控制代码中来实现,例如在诸如磁盘、CD或DVD-ROM的载体介质、诸如只读存储器(固件)的可编程的存储器或者诸如光学或电子信号载体的数据载体上提供了这样的代码。本申请的系统及其模块不仅可以有诸如超大规模集成电路或门阵列、诸如逻辑芯片、晶体管等的半导体、或者诸如现场可编程门阵列、可编程逻辑设备等的可编程硬件设备的硬件电路实现,也可以用例如由各种类型的处理器所执行的软件实现,还可以由上述硬件电路和软件的结合(例如,固件)来实现。
需要注意的是,以上对于系统及其模块的描述,仅为描述方便,并不能把本申请限制在所举实施例范围之内。可以理解,对于本领域的技术人员来说,在了解该系统的原理后,可能在不背离这一原理的情况下,对各个模块进行任意组合,或者构成子系统与其他模块连接。例如,各个模块可以共用一个存储模块,各个模块也可以分别具有各自的存储模块。诸如此类的变形,均在本申请的保护范围之内。
图4是根据本申请一些实施例所示的检测MET基因14号外显子跳跃突变的试剂在制备用于鉴定受试者有利地响应卡马替尼或克唑替尼的可能性的试剂盒中的应用方法。在一些实施例中,流程400中的至少一部分步骤(例如步骤409)可以由计算设备(如图2所示的计算设备200,图1中的处理设备)完成。在一些实施例中,流程400可以利用未描述的一个或以上附加操作和/或未描述的一个或以上操作来完成。另外,图4所示和以下描述的过程的操作顺序并非旨在限制。
步骤401,获取受试者的样品。
在一些实施例中,受试者可以是哺乳动物,例如人。受试者可以是患有非小细胞肺癌的患者。关于受试者的详细信息可以参考图1及其描述,在此不再赘述。
在一些实施例中,受试者的样品可以包括受试者的组织样品、受试者的体液样品、体外培养的细胞(例如,肺细胞)等。组织样品可以包括新鲜的组织样品、福尔马林固定的石蜡包埋的组织(FFPET)等。例如,组织样品可以来自于肺部组织或其他人体组织(例如,肿瘤组织或肿瘤侵犯部位的组织)。液体样品可以包括但不限于胸水、血液(例如,血浆、血清、外周血等)、尿液、唾液、淋巴液、脑脊液、口腔/喉冲洗液、支气管肺泡灌洗液等。在一些实施例中,样品可以是新鲜的或者是冷冻的(例如,液氮保存、-80°冰箱保存、-20°冰箱保存)。可以从受试者中获取新鲜的样品后直接进行后续处理(例如,提取RNA等),也可以将样品进行冷冻保存后,待需要时再进行后续处理。
在一些实施例中,该样品可以是组织样品,例如石蜡肺组织样品。可以通过活检(例如,穿刺活检)、手术获取等方法来采集受试者的组织样品。在一些实施例中,可以在受试者所在医院获取生物样品。在一些实施例中,样品可以是胸水。可通过液体活检来采集受试者的胸水。
步骤403,从样品中提取RNA。
受试者的样品中可以含有MET基因转录得到的mRNA。在通常情况下,所述由MET基因转录得到的mRNA里含有对应于MET E14的RNA片段。在一些实施例中,MET E14发生跳跃突变,导致所述由MET基因转录得到的RNA里不含有对应于MET E14的RNA片段。所述对应于METE14的RNA片段也被称为目标RNA片段。在一些实施例中,样品中还含有对照RNA。对照RNA可以是对照基因所转录的RNA。如本文中所使用的,术语“对照基因”指生物体或者细胞中稳定表达的基因,其表达量几乎不变。一方面可以用来作为MET基因表达量的对照,另一方面其表达量可以用来作为荧光定量PCR的质控和参照,判断MET的PCR结果的准确性。对照基因可以包括但不限于核糖体蛋白(ribosomal protein,RPLO)、3-磷酸甘油醛脱氢酶(GAPDH)、β-肌动蛋白(β-actin,ACTB)、18sRNA、28sRNA、β2微球蛋白(B2M)、琥珀酸脱氢酶亚单位A(SDHA)、次黄嘌呤磷酸核糖转移酶1(hypoxanthine phosphoribosyltransferase1,HPRT1)、区结合蛋白(attachment region binding protein,ARBP)等中的一种或多种。例如,对照RNA可以由GAPDH基因经转录得到。
在一些实施例中,可以从样品中提取MET的RNA和对照基因的RNA。
提取RNA的方法可以包括异硫氰酸胍氯化铯超速离心法、盐酸胍-有机溶剂法、氯化锂-尿素法、热酚法、快速提取法、细胞质RNA提取法、酚-氯化锂法同时提取细胞RNA和DNA、一步快速热酚抽提法。在一些实施例中,通过提取RNA的方法可以在样品(例如,组织)中提取RNA。例如,将组织样品进行切片后进行RNA处理。
在一些实施例中,可以通过RNA提取试剂盒从样品中提取RNA。在一些实施例中,可以直接从样品(例如,石蜡组织样品)中提取RNA(例如,MET E14和对照基因的RNA)。在一些实施例中,提取MET E14的RNA和对照基因的RNA的试剂盒可以为如表1所示的试剂盒。需要注意的是,表1中的试剂仅作为示例用于提取石蜡组织样品,本领域内技术人员可以对试剂的种类和用量进行变化和修改。表1中的RNA提取试剂盒也可以包括在本申请的用于检测MET基因14号外显子跳跃突变的试剂盒中。
表1.RNA提取试剂盒
应当注意的是,不同样品提取RNA方式和试剂盒可能是不同的,对于本领域技术人员而言可根据不同的RNA样品使用不同的RNA提取方式和试剂盒来提取RNA。
步骤405,使用试剂盒,对所述提取出来的RNA进行反转录得到样品cDNA。
反转录可以是以提取出来的RNA(即,MET的RNA和对照基因的RNA)为模板,通过反转录酶,合成互补的单链DNA(cDNA)。本申请的试剂盒为用于检测MET基因14号外显子跳跃突变的试剂盒。该试剂盒可以包括反转录体系。该反转录体系可以包括反转录MET E14以及对照基因(例如,GAPDH)的引物。通过该试剂盒的反转录体系,可以将提取出来的RNA反转录得到样品cDNA。
在一些实施例中,MET E14的RNA反转录使用的特异性反转录引物可以包括:与SEQID NO.:7所示序列的相似度≥70%的核苷酸,与SEQ ID NO.:7所示序列的相似度≥75%的核苷酸,与SEQ ID NO.:7所示序列的相似度≥80%的核苷酸,与SEQ ID NO.:7所示序列的相似度≥85%的核苷酸,与SEQ ID NO.:7所示序列的相似度≥90%的核苷酸,与SEQ IDNO.:7所示序列的相似度≥95%的核苷酸。在一些实施例中,该对照基因RNA反转录使用的特异性反转录引物可以包括:与SEQ ID NO.:8所示序列的相似度≥70%的核苷酸,与SEQID NO.:8所示序列的相似度≥75%的核苷酸,与SEQ ID NO.:8所示序列的相似度≥80%的核苷酸,与SEQ ID NO.:8所示序列的相似度≥85%的核苷酸,与SEQ ID NO.:8所示序列的相似度≥90%的核苷酸,与SEQ ID NO.:8所示序列的相似度≥95%的核苷酸。在一些实施例中,MET E14的RNA反转录使用的特异性反转录引物为如SEQ ID NO.7所示的引物,该对照基因RNA反转录使用的特异性反转录引物可以是如SEQ ID NO.8所示的引物。
在一些实施例中,反转录体系还可以包括反转录酶、适于反转录酶反应的缓冲液、dNTP、RNA和/或无RNase水(例如,DEPC水)。在一些实施例中,反转录体系的容量可以包括100μL、50μL、25μL、20μL、15μL、10μL等。反转录体系中反转录酶的用量可以是200U,引物终浓度可以是0.2μM,dNTP的浓度可以是1mM。
在一些实施例中,可以使用本申请试剂盒中的反转录体系(如下表2所示)对METE14和对照基因进行反转录,得到样品cDNA。样品cDNA包括MET E14的cDNA和对照基因的cDNA。
表2.反转录体系
需要注意的是,表2中的反转录体系仅作为示例,本领域内技术人员可以对试剂的种类和用量进行变化和修改。例如,反转录体系的总量可以是10μL;反转录酶的用量可以根据RNA的浓度变化。例如,引物的终浓度可以是0.2μM,dNTP的终浓度可以是1mM,反转录酶的用量可以是200U。
步骤407,使用所述试剂盒,对样品cDNA进行荧光定量PCR反应。
该试剂盒还包括PCR扩增体系。在一些实施例中,可以使用试剂盒中的PCR扩增体系对上述步骤中获得的样品cDNA进行荧光定量PCR反应。在一些实施例中,所述反转录体系和所述PCR扩增体系可以分别被包括在不同的试剂盒中。
该PCR扩增体系可以包括用于扩增MET E14的上游引物和下游引物以及用于特异性检测MET基因14号外显子跳跃突变的探针。在一些实施例中,该PCR扩增体系还包括用于特异性扩增和检测对照基因(例如,GAPDH)的引物(即,上游引物和下游引物)和探针。探针可以连接有荧光基团(或报告基团)和淬灭基团。荧光基团可以包括但不限于FAM、JOE、JA270、TET、Cal Fluor Gold 540、HEX、VIC、Cal Fluor Orang 560、TAMRA、花青3、Quasar570、Cal Fluor Red 590、Rox、德克萨斯红、花青5、Quasar 670和花青5.5。淬灭基团可以包括但不限于MGB、TAMRA、DABCYL、BHQl-3、Eclipse。
在一些实施例中,该MET E14的上游引物与SEQ ID NO.:1所示序列的相似度大于或等于70%、75%、80%、85%、90%或95%;或者该MET E14的下游引物序列与SEQ ID NO.:2所示序列的相似度大于或等于70%、75%、80%、85%、90%或95%,该MET E14的探针序列与SEQ ID NO.3所示序列的相似度大于或等于70%、75%、80%、85%、90%或95%。在一些实施例中,该PCR扩增体系可以包括如SEQ ID NO.1所示的上游引物,如SEQ ID NO.2所示的下游引物和/或如SEQ ID NO.3所示的探针。
在一些实施例中,荧光基团和淬灭基团可以分别位于探针序列的两端,例如,3’端标记有淬灭基团,5’端标记有荧光基团。在一些实施例中,淬灭基团还可以位于探针序列的中间。在一些实施例中,不同基因的荧光基团可以相同或不同,例如,荧光基团可以均为FAM,MET E14的荧光基团可以是FAM,对照基团的荧光基团可以是JOE。特异性扩增对照基因的上游引物可以与SEQ ID NO.4所示序列的相似度大于或等于70%、75%、80%、85%、90%或95%。特异性扩增对照基因的下游引物可以与SEQ ID NO.5所示序列的相似度大于或等于70%、75%、80%、85%、90%或95%。检测对照基因的探针可以与SEQ ID NO.6所示序列的相似度大于或等于70%、75%、80%、85%、90%或95%。在一些实施例中,该扩增体系可以包括如SEQ ID NO.4所示的上游引物、如SEQ ID NO.5所示的下游引物和/或如SEQ IDNO.6所示的探针。
MET基因包含MET 13号外显子(简称为MET E13)、MET 14号外显子以及MET 15号外显子(简称为MET E15),这些外显子按顺序连接。当MET E14跳跃缺失(例如,完全缺失)时,MET E13和MET E15相连。在一些实施例中,扩增MET E14的上游引物和下游引物分别位于MET E13和MET E15的序列处。用于检测MET E14跳跃突变的探针可以包括MET E13的至少一部分序列和MET E15的至少一部分序列,从而识别出MET E13和MET E15相连的情况。当进行荧光定量PCR时,仅对于出现MET E14跳跃缺失的样品,PCR可以检测到CT值。而MET E14未缺失的样品,探针则无法识别,PCR检测不到CT值,或者说CT值不存在。
试剂盒中的PCR扩增体系的容量可以包括100μL、50μL、25μL、20μL、15μL、10μL等。PCR扩增体系可以包括引物、探针、dNTP、模板、热启动Taq酶以及MgCl
可以通过表3中所示的PCR扩增体系对MET E14和对照基因进行qPCR。
表3.试剂盒的PCR扩增体系
需要注意的是,表3中的qPCR试剂盒仅作为示例,本领域内技术人员可以对试剂的种类和用量进行变化和修改。例如,容量可以是10μL。例如,可以将cDNA样本稀释三倍后,取5μL样本,加0.5μLTaq酶,混匀后,加入已分装好2μL MIX液(缓冲液、引物和探针的混合液)的八连管中,然后启动Q-PCR仪器。
在一些实施例中,荧光定量PCR反应的条件为:95℃10分钟;95℃10秒钟,60℃50秒钟,15个循环;95℃10秒钟,60℃50秒钟,35个循环。反应条件还可以进行各种变化和修改,例如,35个循环可以修改为35个循环到45个循环以内的任意数值,30个循环到45个循环以内的任意数值等。在一些实施例中,荧光定量PCR反应的条件可以由用户自行设定或可以是系统的默认值。
步骤409,处理设备(例如,判定模块320)确定是否能检测到所述荧光定量PCR反应中对应于MET基因的Ct值。
在反应结束后,处理设备可以输出扩增曲线。扩增曲线指的是以循环数为横坐标,以反应过程中实时荧光强度为纵坐标所做的曲线。基线指的是在PCR扩增反应的最初数个循环里,荧光强度变化不大而接近直线的一条线。阈值线例如可以是PCR前3-15个循环荧光强度标准差的10倍,阈值线可以设定在PCR扩增的指数期。在一些实施例中,荧光定量PCR反应的阈值线可以是系统根据样品的扩增曲线自动确定,还可以由用户自行设置(例如,设定为100000)。不同基因的阈值线可以是相同或不同的。Ct值表示每个PCR反应管内荧光信号到达设定的阈值线时所经历的循环数。处理设备可以根据扩增曲线来确定是否能检测到对应于MET基因的Ct值。当样品的MET E14和对照基因的扩增曲线为S形,曲线与阈值线的交点的横坐标即为Ct值,说明该样品中含有MET E14跳跃突变。对照基因的Ct值用于参照表明此次PCR结果正常可靠(见图5)。当对照基因的扩增曲线为S形而样品的MET E14的扩增曲线为一条直线时,MET E14则无Ct值,说明MET E14未缺失,对照基因的Ct值用于参照表明此次PCR结果正常可靠(见图6)。
若Ct值存在,则处理设备(例如,判定模块320)可以判定样品中存在MET基因14号外显子跳跃突变,并且鉴定为所述受试者有利地响应卡马替尼或克唑替尼的可能性较高。
在一些实施例中,可以将PCR反应后的数据(例如,扩增曲线)发送给处理设备110和/或存储设备130。数据可以包括对应于不同样品的MET E14和对照基因的扩增曲线、Ct值等。处理设备110可以基于扩增曲线来判定样品是否含有Ct值。
在一些实施例中,若处理设备检测到MET基因的Ct值存在,则可以判定受试者的样品中存在MET基因14号外显子跳跃突变。若处理设备检测不到MET基因的Ct值,则判定样品中不存在MET基因14号外显子跳跃突变。
处理设备可以根据受试者的样品中存在MET基因14号外显子跳跃突变,鉴定受试者有利地响应MET抑制剂的可能性较高,从而可以为受试者提供精准化的治疗。“响应MET抑制剂的可能性较高”指的是受试者响应MET抑制剂的可能性为70%以上,例如70%、75%、80%、85%、90%、95%、99%等。处理设备可以根据受试者MET基因14号外显子跳跃突变,鉴定受试者有利地响应MET抑制剂的可能性较低。“响应MET抑制剂的可能性较低”指的是受试者响应MET抑制剂的可能性为30%、25%、20%、15%、10%、5%等。
示例性的MET抑制剂可以包括但不限于卡马替尼、克唑替尼、替泊替尼、沃利替尼、梅沙替尼、卡博替尼、色瑞替尼等。在一些实施例中,MET抑制剂还可以包括INCB28060(Incyte)、AMG-458(Amgen)、PF-04217903(Pfizer)、PF-02341066(Pfizer)、E7050(Eisai)、MK-2461(Merck)、BMS-777607(BMS)、JNJ-38877605(Johnson&Johnson)、ARQ197(ArQule)、GSK/1363089/XL880(GSK/Exelexis)和XL184(BMS/Exelexis)、抗MET单克隆抗体、MET酪氨酸激酶抑制剂(Tivantinib)等。
应当注意的是,上述有关流程400的描述仅仅是为了示例和说明,而不限定本申请的适用范围。对于本领域技术人员来说,在本申请的指导下可以对流程400进行各种修正和改变。然而,这些修正和改变仍在本申请的范围之内。在一些实施例中,可以将上述数据(例如,扩增曲线、Ct值)存储在存储设备(例如存储器130)中。处理设备110可以从存储设备中获取MET E14是否含有Ct值,进而判断MET E14是否发生跳跃突变。
根据本申请的一方面,提供了一种用于检测MET基因14号外显子跳跃突变的试剂盒。该试剂盒包括前述PCR扩增体系和反转录体系。反转录体系用于对MET E14和对照基因进行反转录得到cDNA。反转录体系可以包括MET E14和对照基因的引物、反转录酶、dNTP等。PCR扩增体系用于对MET E14和对照基因的cDNA进行荧光定量PCR。PCR扩增体系可以包括用于扩增MET E14和对照基因的上下游引物、用于特异性检测MET基因14号外显子跳跃突变的探针以及特异性检测对照基因的探针、dNTP、模板、1U热启动Taq酶以及MgCl
下述实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的试验材料,如无特殊说明,均为自常规生化试剂公司购买得到的。以下实施例中的定量试验,均设置三次重复实验,结果取平均值。
实施例
实施例1、提取目标RNA和对照基因RNA。
1.1取石蜡组织样品切成5-10μm厚的片状,并迅速将切片置于离心管中,加入1ml二甲苯,剧烈涡旋10s。
1.2室温12000rpm离心2min,去上清液。
1.3向上述沉淀中加入1ml无水乙醇,轻柔混匀,室温12000rpm离心2min,去上清,室温放置10min至乙醇挥发。
1.4加入200μl的裂解液RF以及10μl的蛋白酶K于沉淀中,彻底涡旋混匀。
1.5 55℃孵育15min,之后80℃孵育15min,室温离心5min。
1.6将上清液转入新的离心管中,加入220μl的缓冲液RB,涡旋混匀,加入660μl的无水乙醇,涡旋混匀。
1.7将700μl溶液和沉淀转移到放入收集管的吸附柱中,12000rpm离心1min,弃废液,将吸附柱放回收集管中,重复这一步骤。
1.8向吸附柱中央加入80μl的DNase I工作液,室温放置15min,向吸附柱中加入500μl的去蛋白液RW1,12000rpm离心1min,弃废液。
1.9向吸附柱中加入500μl漂洗液RW(使用前请先检查是否已加入乙醇),室温静置2min,12,000rpm离心30-60sec,弃废液,将吸附柱放回收集管中,重复这一步骤并通风晾干。
2.0加30-100μl的RNase-Free ddH
实施例2、将该目标RNA和对照RNA分别反转录为目标cDNA和对照cDNA。
该反转录体系如下:
5×Buffer 2μL
10×ACE buffer 2μL
引物终浓度 200nM
dNTP 1mM
super RT 200U
样品RNA 12μL
RNA酶抑制剂 1μL。
2.1取样品RNA 12μL,super RT反转录酶1μL,反转录引物1μL,dNTP混合物1μL,5×buffer 2μL,10×ACE buffer 2μL,RNA酶抑制剂1μL,加入无菌离心管中,混匀。其中,目标RNA的反转录引物为:cagaggatactgcacttgtcg(SEQ ID NO.:7),对照RNA的反转录引物为:atacgaccaaatccgttgact(SEQ ID NO.:8)。
2.2启动PCR仪程序:55℃保温15min,85℃孵育10s;反应结束后,短暂离心,置于10℃冷却10分钟。
2.3反转录产物可直接用于后续PCR扩增反应。
实施例3、将该目标cDNA和对照cDNA进行PCR扩增反应。
PCR扩增体系如下:
10×PCR Buffer 稀释为1×
dNTP 0.2mM
模板 2uL
各引物 200-400nM
各探针 100-400nM
热启动Taq酶 1U
MgCL
总体积 20uL。
取混合液18μL,包括10×PCR Buffer、0.2μM的PCR特异引物和0.2μM的探针,反转录样品cDNA稀释3倍后取5μL,Taq酶0.5μL,加入无菌离心管中,混匀后分装,每个孔2μL。其中,目标基因MET E14的特异性引物为:tacttgggtttttcctgtgg(SEQ ID NO.:1,正向引物),cagaggatactgcacttgtcg(SEQ ID NO.:2,反向引物)。内参基因GAPDH的特异性引物为:ctctgctcctcctgttcgac(SEQ ID NO.:4,正向引物),atggtgtctgagcgatgtgg(SEQ ID NO.:5,反向引物)。目标基因MET E14的特异性探针的序列为:FAM-aggaaactgatctttaatttg-MGB(SEQ ID NO.:3),内参基因GAPDH的特异性探针的序列为:FAM-cgtcgccagccga-MGB(SEQ IDNO.:6)。
使用Q-PCR仪器ABI 7500,设置PCR扩增反应的条件如下:
表4.PCR扩增反应的条件
实施例4、确定受试者的目标RNA和对照RNA的Ct值。
选取20个患有非小细胞肺癌的患者,年龄范围为37-82岁,中位数为63岁。其中男性为11人,占55%,女性为9人,占45%。取这些患者的组织样品,进行上述实施例1到3的步骤。PCR扩增反应之后,可以手动调节荧光阈值线。根据调节的阈值线,确定受试者的血液样品中的是否含有MET E14和对照基因GAPDH的Ct值。结果显示,检测到了其中3名患者的Ct值,判定为这3名患者的样品中出现了MET E14跳跃缺失。这患者1-3的PCR的扩增曲线分别如图7-9所示。这3名患者的MET E14和GAPDH的Ct值如下表5所示:
表5.患者的MET E14和GAPDH的Ct值
当判定为患者出现MET E14跳跃缺失时,可为患者使用克唑替尼、卡马替尼、色瑞替尼等酪氨酸激酶抑制剂进行治疗。
本申请所披露的一种癌症预后预测的方法,可能带来的有益效果包括但不限于:(1)基于mRNA的qRT-PCR方法适合筛选MET E14跳跃突变,灵敏度高,特异性强,操作方便且成本较低;(2)利用MET E14跳跃缺失突变的检测,能够为非小细胞肺癌患者制定个体化临床治疗方案,精准治疗。需要说明的是,不同实施例可能产生的有益效果不同,在不同的实施例里,可能产生的有益效果可以是以上任意一种或几种的组合,也可以是其他任何可能获得的有益效果。
本领域的技术人员应当理解,以上实施例仅为说明本发明,而不对本发明构成限制。凡在本发明的精神和原则内所作的任何修改、等同替换和变动等,均应包含在本发明的保护范围之内。
序列表
<110> 嘉兴允英医学检验有限公司
<120> 一种检测MET E14跳跃突变的方法
<160> 8
<170> SIPOSequenceListing 1.0
<210> 1
<211> 20
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 1
tacttgggtt tttcctgtgg 20
<210> 2
<211> 21
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 2
cagaggatac tgcacttgtc g 21
<210> 3
<211> 21
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 3
aggaaactga tctttaattt g 21
<210> 4
<211> 20
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 4
ctctgctcct cctgttcgac 20
<210> 5
<211> 20
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 5
atggtgtctg agcgatgtgg 20
<210> 6
<211> 13
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 6
cgtcgccagc cga 13
<210> 7
<211> 21
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 7
cagaggatac tgcacttgtc g 21
<210> 8
<211> 21
<212> DNA
<213> 人工序列(Artificial Sequence)
<400> 8
atacgaccaa atccgttgac t 21
- MET基因外显子14跳跃突变检测的引物组、检测方法和试剂盒
- 一种MET基因14外显子跳跃缺失突变检测试剂盒
