增强化学发光的基材
文献发布时间:2023-06-19 12:19:35
技术领域
本发明涉及具有纳米结构表面的基材用于增强化学发光的用途。这种效应也称为“金属增强化学发光”(MEC)。
背景技术
化学发光是通过化学反应发射紫外线和/或可见光范围内的电磁辐射的过程。通常,氧化敏感化合物参与化学发光反应,首先氧化成为不稳定的中间化合物,从而在随后的反应中释放光。这种化合物也称为发光团(luminophore)。众所周知且经常使用的发光团是鲁米诺(luminol)。它尤其用于法医,因为鲁米诺可以检测血液残留物。这是基于这样一个事实,即在用氧化剂氧化后,鲁米诺会通过发出蓝光进行反应。然而,只有在催化剂(例如络合物结合的Fe
特别是在分析过程中,确定样品中的甚至少量的分析物是非常重要。用于确定和定量样品中分析物的常规方法通常具有无法检测纳克或皮克范围内的分析物浓度的缺点。
发明内容
因此,本发明的一个目的是提供能够提高前述分析方法的灵敏度的装置和方法。
该目的通过使用用于增强在化学发光反应中产生的一个或多个发光团的化学发光的基材来实现,该基材包含具有多个彼此分离的凹陷的固体聚合物载体,并且该固体载体至少部分地涂覆有金属。
已知可增强荧光的此类基材,例如见WO 2017/046320。利用这些基材的纳米结构表面,可以显著提高荧光化合物的荧光产率,从而通过所谓的MEF(“金属增强荧光”)效应急剧提高荧光测量的灵敏度。这允许测量非常低的荧光团浓度。然而,只有当荧光团与基材非常接近(小于50nm)时,才能观察到这种荧光增强(Hawa et al.,Analytical Biochemistry549(2018):39-44)。这种MEF效应只有在去除任何不与表面结合并因此包含非增强荧光团的溶液之后通过透明基材或直接在表面上测量荧光时才能观察到。因此不可能通过溶液中游离分子的MEF效应进行增强。
然而,令人惊讶地发现,能够增强荧光材料的荧光的表面结构也可用于增强在化学发光反应中产生的发光团的电磁发射。然而,已经发现,发光增强效应不仅在发光团与上述基材非常靠近(即小于50nm)时是可观察到的,而且该效应扩展到整个溶液。因此,当从上方测量整个本体溶液时也可以观察到。与测定间接结合到固体载体上的荧光团的荧光的分析方法(例如ELISA)相反,由间接结合到固体载体上的酶产生的发光团在溶液中是游离的,并且可以在待检测的水溶液中自由扩散。因此,反应体系中的大多数发光团并不靠近基材,而是从基材扩散开。尽管有这种扩散效应,仍然发现但本发明的基材出乎意料地显著增强了发光团的化学发光。鉴于Hawa et al.,的研究结果(Analytical Biochemistry 549(2018):39-44),这是出乎意料的,因为该出版文献的作者能够证明荧光增强效应只能在靠近本发明的基材的地方观察到。
本发明的包括凹陷的固体载体基本上可以用不同的方法生产,如WO 2017/046320中也提出的。
(a)包括凹陷的固体载体在一个单一步骤(例如注射成型)中制造
(b)在进一步的工艺步骤(例如热压印、电子束光刻或与反应离子蚀刻或激光烧蚀相关的“极紫外”(EUV))中将凹陷引入现有的固体载体中
(c)在固体载体上施加薄的可结构化聚合物层,在其中引入凹陷,例如在BD-50蓝光光盘的生产过程中(UV纳米压印光刻)
所谓的纳米压印光刻特别适用于生产这些结构(Chou S.et al.,Nanoimprintlithography,Journal of Vacuum Science&Technology B Volume 14,Nr.6,1996,S.4129-4133)。为了通过纳米压印光刻法生产纳米结构,需要正片(positive)(通常是单体或聚合物)和纳米结构印模(stamp)(“母版”)。印模本身可以通过纳米光刻制造,或者它可以通过蚀刻制造。正片被施加到基材上,然后加热到玻璃转移温度(glass temperature)以上,即在压印之前液化。为了实现可控(和短期)加热,经常使用激光或紫外线。由于加热过程中正片的粘性,印模的空隙被其完全填满。冷却后,移除印模。通过溅射方法用金属涂覆构成本发明的基材的固体载体的正片。
用于光刻的印模的结构化可以再次通过纳米压印来实现。在这里,使用的材料是玻璃或透光塑料。
特别优选的是通过注射成型生产包括凹陷的固体载体。在这里,模具嵌件通常是通过电镀镍从光刻生产的硅晶片得到的。
固体载体基本上可以具有任何形状(例如球形、平面),特别优选平面形状。
如本文所用,“凹陷”涉及围绕凹陷的固体载体的表面水平,并延伸到载体中而不是像隆起(elevation)或突起(bump)那样从载体延伸出来。本发明意义上的凹陷具有由侧壁限定的底部。因此,它的深度是从表面到凹陷底部的距离。固体载体上的凹陷可以具有不同的形状(例如圆形、卵形、方形、矩形)。
如本文所用的“多个”凹陷是指本发明的载体具有至少一个、优选至少两个、更优选至少5个、更优选至少10个、更优选至少20个、更优选至少30个、更优选至少50个、更优选至少100个、更优选至少150个、更优选至少200个凹陷。这些凹陷可以设置在1000μm
如本文所用,“彼此分离的凹陷”是指凹陷通过它们的侧限(side limit)彼此分离并且彼此不连接——甚至在固体载体的表面处也不彼此连接。
根据本发明的优选实施例,凹陷彼此之间的距离(“周期”)为0.2μm至2.5μm,优选0.3μm至1.4μm,更优选0.4μm至1.3μm。在本发明的另一优选实施例中,凹陷彼此之间的距离为0.2μm至2μm,优选0.2μm至1.8μm,优选0.2μm至1.6μm,优选0.2μm至1.5μm,优选0.2μm至1.4μm,优选0.2μm至1.3μm,优选0.3μm至2.5μm,优选0.3μm至2μm,优选0.3μm至1.8μm,优选0.3μm至1.6μm,优选0.3μm至1.5μm,优选0.3μm至1.3μm,优选0.4μm至2.5μm,优选0.4μm至2μm,优选0.4μm至1.8μm,优选0.4μm至1.6μm,优选0.4μm至1.5μm,优选0.4μm至1.4μm,优选0.5μm至2.5μm,优选0.5μm至2μm,优选0.5μm至1.8μm,优选0.5μm至1.6μm,优选0.5μm至1.5μm,优选0.5μm至1.4μm,优选0.5μm至1.3μm,优选0.6μm至2.5μm,优选0.6μm至2μm,优选0.6μm至1.8μm,优选0.6μm至1.6μm,优选0.6μm至1.5μm,优选0.6μm至1.4μm,优选0.6μm至1.3μm,优选0.7μm至2.5μm,优选0.7μm至2μm,优选0.5μm至1.8μm,优选0.7μm至1.6μm,优选0.7μm至1.5μm,优选0.7μm至1.4μm,优选0.7μm至1.3μm,其中凹陷最优选彼此之间的距离为0.2μm至1.4μm或0.3μm至1.3μm。凹陷之间的距离(“周期”)是从凹陷中心测量的。
根据本发明的优选实施例,固体载体的凹陷具有长度和宽度,其中长宽比为2:1至1:2,特别是约1:1。
基本上,固体载体上的凹陷可以具有任何形状。然而,特别优选的是具有2:1至1:2、优选1.8:1、优选1.6:1、优选1.5:1、优选1.4:1、优选1.3:1、优选1.2:1、优选1.1:1、优选1:1.8、优选1:1.6、优选1:1.5、优选1:1.4、优选1:1.3、优选1:1.2、优选1:1.1、特别是1:1的长宽比的凹陷。
根据本发明的另一优选实施例,凹陷的长度和宽度为0.1μm至2μm,优选0.2μm至2μm,优选0.3μm至2μm,优选0.1μm至1.8μm,优选0.2μm至1.8μm,优选0.3μm至1.8μm,优选0.1μm至1.5μm,优选0.2μm至1.5μm,优选0.3μm至1.5μm,优选0.1μm至1.2μm,优选0.2μm至1.2μm,优选0.2μm至1.2μm,优选0.1μm至1μm,优选0.2μm至1μm,优选0.3μm至1μm,优选0.1μm至0.8μm,优选0.2μm至0.8μm,优选0.3μm至0.8μm,优选0.1μm至0.6μm,优选0.2μm至0.6μm,优选0.3μm至0.6μm,特别是0.2μm至0.6μm。
特别地,本发明的固体载体的凹陷具有基本上圆形的形状,其中“基本上圆形”还包括卵形和椭圆形形状。凹陷的形状在固体载体的平面图中是可见的。
凹陷具有的深度为优选0.1μm至5μm,优选0.1μm至4μm,优选0.1μm至3μm,优选0.1μm至2μm,优选0.1μm至1.5μm,优选0.1μm至1.2μm,优选0.1μm至1μm,优选0.1μm至0.9μm,优选0.1μm至0.8μm,优选0.2μm至5μm,优选0.2μm至4μm,优选0.2μm至3μm,优选0.2μm至2μm,优选0.2μm至1.5μm,优选0.2μm至1.2μm,优选0.2μm至1μm,优选0.2μm至0.9μm,优选0.2μm至0.8μm,优选0.3μm至5μm,优选0.3μm至4μm,优选0.3μm至3μm,优选0.3μm至2μm,优选0.3μm至1.5μm,优选0.3μm至1.2μm,优选0.3μm至1μm,优选0.3μm至0.9μm,优选0.3μm至0.8μm。凹陷的深度是固体金属化载体表面到凹陷底部的距离。
根据本发明,固体聚合物载体“至少部分地”被金属覆盖。如本文所用,“至少部分地”是指包含凹陷的固体载体的任何区域的至少20%、优选至少30%、更优选至少40%、更优选至少50%、更优选至少60%、更优选至少70%、更优选至少80%、更优选至少90%、更优选至少95%、更优选至少98%、最优选100%被至少一种金属覆盖。由于MEF效应需要金属表面,因此特别优选固体载体的表面至少在凹陷区域中被至少一种金属覆盖。在此,固体载体还可以包括由相同或不同金属制成的相互层叠布置的几个(例如至少两个、至少三个、至少四个或至少五个)金属层。在固体载体上使用几个金属层的优点是直接施加到载体上的第一金属层(例如铬)可以提高其他金属层的粘附性。
如本文所用,术语“层叠布置”是指金属层直接或间接地布置在另一金属层上。这可获得相同金属或不同金属的金属层的多层系统。
金属层优选是连续的而不是不连续的。然而,根据本发明,发现固体聚合物载体上的一个或多个金属层可以是不连续的而不损害荧光增强效果。例如,不连续金属层可以通过对本发明的基材表面的电导率测量来确定。较低或没有电导率意味着金属层在基材表面是不连续的。不连续的金属层可以例如通过将基本上完全被金属覆盖的基材与优选的盐溶液,例如具有150mM NaCl的10mM磷酸盐缓冲液接触一段时间(10-90分钟)来产生。
本发明的固体载体“涂覆有至少一种金属”。优选地,金属层包含至少两种、更优选至少三种、更优选至少四种、更优选至少五种不同的金属。可以通过现有技术已知的方法将金属施加到固体载体上,其中优选使用溅射(阴极溅射)或热蒸发、电子束蒸发、激光束蒸发、电弧蒸发、分子束外延、离子束辅助沉积和离子镀。
根据本发明的一个优选实施例,所述金属选自银、金、铝、铬、铟、铜、镍、钯、铂、锌、锡和包含这些金属中的一种或多种的合金。
根据本发明,这些金属或其合金可用于涂覆本发明的固体载体。特别优选的是用银或含银合金涂覆固体载体,因为银及其合金具有特别强的增强作用。特别优选的是包含银、铟和锡的合金。含银合金的银含量优选大于10%,更优选大于30%,更优选大于50%,更优选大于70%,更优选大于80%,更优选大于90%。
在用至少一种金属涂覆固体载体之后或在使用本发明的基材或固体载体之前,优选用包含选自由氟、氯、溴和碘组成的组的卤素的至少一种酸或一种盐的水性组合物处理固体载体或基材。
已经表明,通过用包含至少一种卤素的酸或其盐的水溶液(例如缓冲液)预处理基材或固体载体,可以进一步增强荧光增强。因此,特别优选用含酸或含盐的溶液预处理固体载体或基材。或者,在测量期间也可以使用包含至少一种卤素的酸或盐的水溶液(例如缓冲液)代替其他溶液。根据本发明,卤素基团的任何酸或其任何盐都是合适的,然而,放射性卤素在实践中是不希望的。因此,氟、氯、溴和碘的卤素的酸或盐是特别优选的,并且最优选使用氯化物,特别是金属氯化物。特别优选,根据本发明使用的酸或盐是碱金属盐或碱土金属盐,特别是钠盐、钾盐或锂盐。
根据本发明的一个特别优选的实施例,水性组合物包含选自由HCl、HF、HBr、HI、NaCl、NaF、NaBr、NaI、KCl、KF、KBr和KI组成的组的至少一种酸或盐。除了所述至少一种酸或其盐之外,包含至少一种卤素的酸或其盐的水性组合物还可包含其他材料,例如其他酸或盐。特别优选的是具有缓冲功能的材料(例如磷酸氢二钠、磷酸二氢钾、碳酸盐)。
根据本发明的另一个优选实施例,固体载体用水性组合物处理至少1分钟,优选至少2分钟,更优选至少5分钟,更优选至少10分钟,更优选至少20分钟。根据本发明,已经显示,当固体载体与包含至少一种卤素的酸或其盐的水性组合物温育至少1分钟时,优选在室温(22℃),涂覆有至少一种金属的载体的荧光增强效果特别强。如果在较高温度(例如在30℃和40℃之间)进行温育,则可以相应缩短温育时间(例如至少30秒)。另一方面,如果在较低温度(例如在10℃和20℃之间)进行温育,则温育时间可能会相应延长(例如至少2分钟)。
根据本发明的另一优选实施例,固体载体上的金属层的厚度为10nm至200nm,优选为15nm至100nm。特别优选地,所述固体载体上金属层的厚度为10nm至190nm,优选10nm至180nm,优选10nm至170nm,优选10nm至160nm,优选10nm至150nm,优选10nm至140nm,优选10nm至130nm,优选10nm至120nm,优选10nm至110nm,优选10nm至100nm,优选10nm至90nm,优选10nm至80nm,优选10nm至70nm,优选10nm至60nm,优选10nm至50nm,优选15nm至200nm,优选15nm至190nm,优选15nm至180nm,优选15nm至170nm,优选15nm至160nm,优选15nm至150nm,优选15nm至140nm,优选15nm至130nm,优选15nm至120nm,优选15nm至110nm,优选15nm至90nm,优选15nm至80nm,优选15nm至70nm,优选15nm至60nm,优选15nm至50nm,优选20nm至200nm,优选20nm至190nm,优选20nm至180nm,优选20nm至170nm,优选20nm至160nm,优选20nm至150nm,优选20nm至140nm,优选20nm至130nm,优选20nm至120nm,优选20nm至110nm,优选20nm至100nm,优选20nm至90nm,优选20nm至80nm,优选20nm至70nm,优选20nm至60nm,优选20nm至50nm。
根据本发明,“固体载体”可以由任何聚合物材料组成,只要它可以用金属涂覆并且只要可以产生凹陷即可。例如,固体聚合物载体包括合成聚合物或由合成聚合物组成,例如聚苯乙烯、聚氯乙烯或聚碳酸酯、环烯烃、聚甲基丙烯酸甲酯、聚乳酸或它们的组合。基本上,非聚合物载体如金属、陶瓷或玻璃也是合适的,只要它们可以用金属涂覆并且只要可以产生凹陷即可。
固体载体优选包含至少一种选自由热塑性聚合物和缩聚物组成的组的材料。
根据本发明的优选实施例,热塑性聚合物选自由聚烯烃、乙烯基聚合物、苯乙烯聚合物、聚丙烯酸酯、聚乙烯咔唑、聚缩醛和含氟聚合物组成的组。
缩聚物优选选自由热塑性缩聚物、热固性缩聚物和聚加合物组成的组。
根据本发明的一个特别优选的实施例,聚合物固体载体的材料包括有机和/或无机添加剂和/或填料,这些优选地选自由TiO
根据一个优选的实施例,本发明的基材是毛细管、微量滴定板、微流体芯片、测试条(用于“侧流测定”)、用于荧光显微术的载玻片(例如目标载玻片)的一部分,特别是用于高分辨率方法,例如根据点扫描仪原理的共聚焦激光显微术以及4Pi显微术和STED(受激发射损耗)显微术、传感器阵列或任何其他光学检测器领域。
特别优选的是在微量滴定板中使用本发明的基材,其中微量滴定板可以包括6、12、24、48、96、384或1536个孔。微量滴定板用于各种测量和分析,通常还包括测量样品的荧光。通过在微量滴定板的孔中提供本发明的基材,可以显著增加样品的荧光产率。可以通过各种方法将基材引入并固定在孔中。此处,基材优选通过粘合、焊接技术(例如激光焊接)和热粘合固定在孔中。
根据本发明的一个特别优选的实施例,固体载体包含环烯烃共聚物或环烯烃聚合物或由环烯烃共聚物或环烯烃聚合物组成,并且是微量滴定板的一部分或微量滴定板的一部分孔。COP 1060R(Zeonor°1060R)已经显示是特别适合的。这里,载体优选涂覆有10至60nm,优选最多40nm的金属(例如银)。
用荧光物质(如荧光团)的某些测量是在毛细管中进行的。因此优选在毛细管中提供本发明的基材。一种示例性应用是细胞术或流式细胞术,其中荧光细胞或荧光标记细胞的数量或和类型通过荧光测量来确定。
许多荧光测量应用在微流体芯片中进行(例如作为“芯片实验室”应用),其中可以在此类芯片的检测区域中提供本发明的基材。本发明的基材也可以在常规的比色皿中提供。这也允许在荧光测量中显著增加荧光产率,从而可以测量样品中非常少量的荧光材料。根据本发明,可以使用任何比色皿形状。本发明的基材也可用于可用于快速测试或现场测试(护理点)的测试条系统(“侧流分析”)的检测区域(“检测线”),以增强标记分析物(例如荧光标记抗体)的荧光,从而提高测试的灵敏度。
根据本发明的优选实施例,发光团由酶产生。
发光团是在某些反应(例如用氧气或过氧化氢氧化)的情况下反应生成产物的化学化合物。在这种反应过程中,会发出紫外线和/或可见光范围内的电磁辐射。根据本发明,发光团可以在一种或多种酶的帮助下产生。在这里,这些酶能够与发光团的前体发生反应,以便将这些前体转化为富含能量且不稳定的发光团。
优选地,根据本发明使用的酶选自由过氧化物酶和加氧酶组成的组,优选选自由辣根过氧化物酶(HRP)、碱性磷酸酶(ALP)和荧光素酶组成的组。这些酶能够以某种方式与某些化合物发生反应,使得它们发出电磁辐射。合适的化学发光化合物是技术人员众所周知的(参见例如“Chemiluminescence in Organic Chemistry”,Karl-DietrichGundermann Frank McCapra,Springer-Verlag Berlin Heidelberg 1987,ISBN 978-3-642-71647-8)并且根据酶来选择。
根据本发明的另一个优选实施例,发光团选自由鲁米诺及其衍生物、1,2-二氧杂环丁烷、吖啶酯和荧光素组成的组。除了这些发光团中的一种或多种之外,可以使用草酸衍生物,优选草酸芳酯,例如双(2,4,6-三氯苯基)草酸酯(TCPO)、双(2,3-二硝基苯基)草酸酯(DNPO)或双(2,4,5-三氯苯基-6-戊氧羰基苯基)草酸酯(CPPO),从中已知它们可以在与过氧化物(例如过氧化氢)反应时形成不稳定的过氧草酸盐,例如1,3-二氧杂环丁酮,它们会在它们的分解反应过程中释放例如紫外线。
本发明的产生发光团的酶优选直接和/或间接结合到基材上。因此,本发明的基材可以例如包被有能够产生发光团的酶。这在确定表面上的分析物(例如酶联免疫吸附测定(ELISA))时特别有利。
根据应用领域,酶可以通过一种或多种其他分子直接或间接结合到基材上。将这些分子结合到金属结构上的方法是众所周知的。在最简单的情况下,结合是通过蛋白质对金属表面的物理化学吸附(通过离子和疏水相互作用介导)实现的(例如,Nakanishi K.etal.,J Biosci Bioengin 91(2001):233-244)。在金属表面衍生化之后用于固定蛋白质的共价方法也是已知的(例如GB Sigal et al.,Anal Chem 68(1996):490-7)。
根据本发明的一个优选实施例,酶通过选自由抗体、抗体片段,优选Fab、F(ab)
本发明的另一方面涉及一种增强在水溶液中化学发光反应中产生的一个或多个发光团的化学发光的方法,该方法包括使水溶液与如上限定的基材接触的步骤。
在本发明的方法中,可以通过使水溶液与本发明的基材接触来增强由该水溶液中的发光团发出的光。这例如通过产生发光团提高了反应的敏感性。例如,可以提到通过鲁米诺检测血液残留。在此,可以在仅包含非常少量血液的含水样品中或冲洗或溶解在水溶液中的样品中检测血液。
本发明的另一方面涉及一种用于测定或定量水性样品中至少一种分析物的方法,该方法包括以下步骤:
a)使样品与本发明的基材接触,该样品包含直接或间接结合到该基材的分析物结合分子,
b)添加至少一种额外的分析物结合分子,至少一种酶直接或间接结合到该分子上,所述酶在化学发光反应中从一个或多个基材产生一个或多个发光团,和
c)测量由步骤b)中的化学发光反应产生的光发射。
用于测定或定量水性样品中至少一种分析物的本发明的方法是基于技术人员熟知的检测方法(例如ELISA),不同之处在于具有待测定和/或定量的分析物的水性样品与WO2017/046320中也公开的本发明的基材接触。这种基材的存在可以显著增强化学发光反应过程中发出的光。
在优选的本发明方法中,水性样品与通过已知方法结合到基材的分析物结合分子(例如抗体或抗体片段)接触。因此,存在于水性样品中的分析物分子间接地结合到基材表面。在洗涤步骤的过程中,未间接结合到基材表面的分析物被去除。通过另外的分析物结合分子,至少一种酶也间接地结合到本发明的基材上。在进一步的洗涤步骤之后,其中未结合分析物的该另外的分析物结合分子被去除,添加基材,酶可以从该基材产生发光团,该发光团在该方法的最后步骤之一中发出光。这种光可以用常规方法定性或定量测定。
发光团-正如开头已经提到的-由酶在化学发光反应中产生。根据本发明的优选实施例,酶选自由辣根过氧化物酶、碱性磷酸酶、荧光素酶和通常地水解酶组成的组。
根据本发明的另一个优选实施例,发光团选自由鲁米诺及其衍生物、1,2-二氧杂环丁烷、吖啶酯或荧光素组成的组。
酶和基材的优选组合可选自由辣根过氧化物酶/鲁米诺、碱性磷酸酶/1,2-二氧杂环丁烷和荧光素酶/荧光素组成的组。
根据本发明的一个优选实施例,结合到基材的分析物结合分子和至少一种另外的分析物结合分子选自由抗体、抗体片段,优选Fab、F(ab)'
根据本发明的另一个优选实施例,酶通过选自由抗体和抗体片段,优选Fab、F(ab)'
根据本发明的优选实施例,在280nm至850nm的波长测量步骤b)中的光发射。
根据本发明的一个特别优选的实施例,步骤b)中的光发射在距基材大于40nm、优选大于50nm的距离处测量。
附图说明
将参考以下附图更详细地解释本发明,然而,本发明不限于这些。
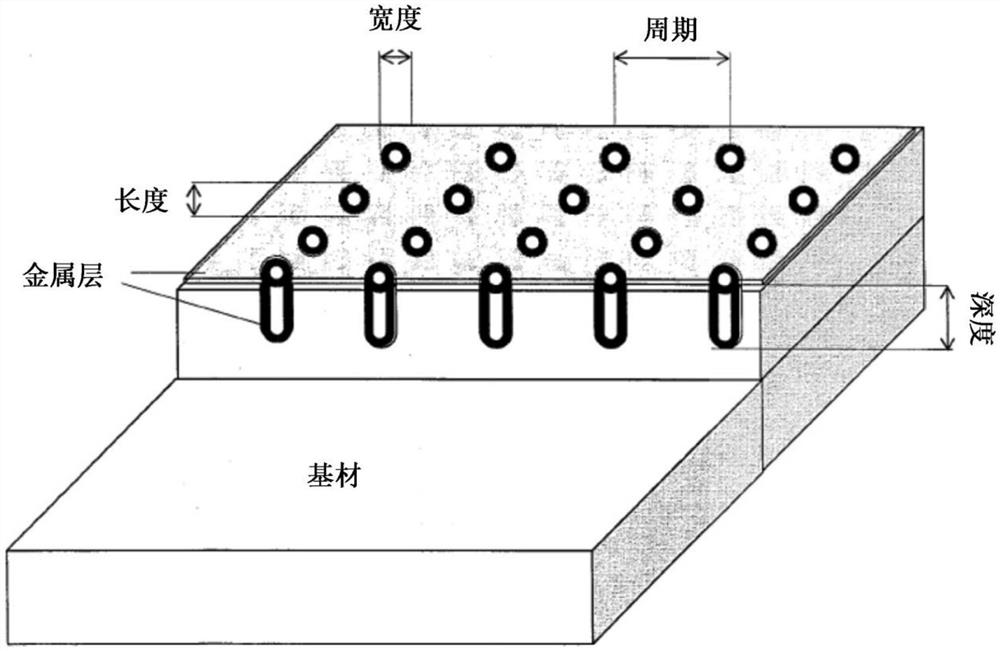
图1显示了包括涂覆有金属层的固体载体的本发明基材。固体载体具有有深度、宽度和长度的凹陷。凹陷以彼此相距的一定距离(周期)位于固体载体上。
图2显示了本发明固体载体的平面图(A)和横截面(B)。固体载体上的凹陷以宽度、长度和深度来表征并且彼此间隔一定距离(周期)。
图3显示了随抗体浓度变化的MEC增强。
图4显示了MEF和标准MTP在两步测定体系中的信噪比。表2和下图显示了实现的SNR或MEC增强随包被的山羊抗体浓度变化。
具体实施方式
实施例
通过下面描述的实施例,检查了为金属增强荧光开发的基材是否也适用于提高化学发光测量的信噪比。
对于以下实施例,使用底部具有AT 517 746中公开的结构的微量滴定板。具体地,将具有多个彼此分开、且直径为0.4μm、周期(即两个凹陷之间的距离)为1μm、深度为0.7μm的凹陷的银涂覆聚合物载体施加到该微量滴定板的底部。Greiner公司(奥地利)的商购微量滴定板用于比较目的,以确定所达到的增强效果的程度。
检测MEC(“金属增强化学发光”)增强效应的最简单方法是将酶标抗体吸附到上述微量滴定板底部,并在洗涤步骤后,通过用于相应酶的化学发光基材检测结合的抗体。
步骤
·50μl驴抗山羊抗体(Sigma,SAB3700287,1mg/ml)在50mM磷酸盐缓冲液/100mMNaCl中的稀释液,浓度为10
·弃去孔(微量滴定板上的凹陷)中的内容物,并用200μl 50mM磷酸盐缓冲液/100mM NaCl/0.1%TritonX100洗涤板3次。
·根据生产商说明书(BM Chemiluminescence ELISA Substrate Kit,Sigma,11759779001),将10μl化学发光基材与100μl增强剂和890μl测定缓冲液混合,两者均包含在试剂盒中。试剂盒中包含的基材为CSPD(3-(4-甲氧基螺{1,2-二氧杂环丁烷-3,2'-(5'-氯代)三环[3.3.1.1
·将150μl反应混合物用移液管移至MTP上,并使用TECAN的SPARK微量滴定板读数器监测出现的化学发光信号。
结果
信噪比(SNR,有抗体的孔的化学发光/无抗体的化学发光)的时间演变
从表1中可以看出,SNR在开头所述的具有结构化底部的微量滴定板(MEF-MTP)中仅随时间增加,而在Greiner的标准微量滴定板(“Greiner MTP”)上则停滞甚至降低。
表1:SNR随时间变化
这可以通过以下事实来解释:由于MEC增加了量子产率,防止了富含发光团的本体溶液的猝灭。因此,与标准MTP相比,MEF-MTP上吸附抗体的检测随着时间的推移变得越来越敏感,并允许将检测限降低至少10倍(a power of ten)。
浓度依赖和MEC程度
对增强程度进行量化的最简单方法是比较MEF和标准MTP的SNR。
这表明MEC的程度明显依赖于浓度(300秒测量时间后的数据),如图3所示。这种增强在浓度最高为10
MEF(“金属增强荧光”)效应的程度强烈取决于荧光团与纳米结构的距离(也见Hawa et al.,Analytical Biochemistry 549(2018):39-44)。
在酶催化的MEC测试的情况下,与例如直接用荧光标记的抗体的MEF测试相反,产生的发光团会从表面扩散开,因此只有在表面上时才会被增强。为了表明在两个蛋白质层(至少约10
步骤:
·50μl山羊抗体(Jackson,111-005-008,2mg/ml)在50mM磷酸盐缓冲液/100mMNaCl中的稀释液,浓度为0-1μg/ml,在MEF或Greiner 1×8HB strip MTP(VWR,737-0195)上在4℃避光温育过夜。
·弃去孔中的内容物,并用200μl 50mM磷酸盐缓冲液/100mM NaCl/0.1%TritonX100洗涤板3次。
·通过在室温与100μl 50mM磷酸盐缓冲液/100mM NaCl/0.1%TritonX100和5%聚乙烯吡咯烷酮(5%PBSPTx)温育2小时来阻断非特异性结合
·在进一步洗涤步骤后,将板与50μl 30ng/ml的ALP标记的抗山羊抗体溶液(也用于第2项)在室温温育2小时。
·在最后的洗涤步骤之后,再次加入150μl实施例1中描述的发光团反应混合物,并用TECAN的SPARK微量滴定板读数器监测出现的化学发光信号。
结果
通过比较MEF和标准MTP(Greiner MTP)的SNR,再次对增强程度进行了量化。表2和图4显示了获得的SNR值和MEC增强随包被的山羊抗体浓度而变化。
表2:两步检测体系中的信噪比
甚至在两个蛋白质层上可以观察到增强效果。这是令人惊讶的,因为与具有表面结合的荧光团的MEF相比,酶产生的发光团会扩散并远离表面。在任何情况下,灵敏度升高20-30倍在分析上被认为是有意义的,因为它们似乎随着涂层浓度的增加而上升。
讨论
因此,为金属增强的荧光开发的结构也适用于金属增强化学发光。
这是非常令人惊讶的,因为效果的范围(距表面的距离)只有40-50nm,并且酶产生的化学发光基材从表面扩散开。显然,增强是如此强烈,以至于随着时间的推移平均,在靠近表面的地方存在足够的分子。此外,所观察到的MEC范围是出乎意料的,目前尚未在文献中描述。
- 增强化学发光的基材
- 预浸料坯基材、层合基材、纤维增强塑料、预浸料坯基材的制造方法及纤维增强塑料的制造方法
