含铜治疗诊断性化合物及使用方法
文献发布时间:2023-06-19 19:28:50
相关申请的交叉引用
本申请要求2020年5月6日提交的美国临时专利申请No.63/020,838的权益,其全部公开内容出于任何和所有目的通过引用并入本文。
技术领域
本发明一般地涉及三功能构建体,其包括肿瘤靶向结构域(其中肿瘤靶向结构域包括能够识别肿瘤细胞表面上的分子靶标或与肿瘤细胞表面上的分子靶标相互作用的部分)、血液-蛋白结合结构域和含sarcophagine的结构域,其中肿瘤靶向结构域的部分位于血液-蛋白结合结构域的远端并且在空间上不受血液-蛋白结合结构域阻碍。本发明的化合物的含sarcophagine的结构域能够螯合
发明内容
在一方面,提供了化合物,其包括肿瘤靶向结构域(其中肿瘤靶向结构域包括能够识别肿瘤细胞表面上的分子靶标或与肿瘤细胞表面上的分子靶标相互作用的部分)、血液-蛋白结合结构域和含sarcophagine的结构域,其中肿瘤靶向结构域的部分位于血液-蛋白结合结构域的远端并且在空间上不受血液-蛋白结合结构域阻碍。本文的实施方式的肿瘤靶向结构域能够结合至肿瘤相关分子靶标,其包括以下中的一者或多者:肿瘤相关分子靶标,其为肿瘤特异性细胞表面蛋白或其他标记,例如前列腺特异性膜抗原(PSMA)、生长激素抑制素肽受体-2(SSTR2)、alphavbeta3(αvβ3)、αvβ6、胃泌素释放肽受体、seprase(例如成纤维细胞激活蛋白α(FAP-α))、肠促胰岛素受体、葡萄糖依赖性促胰岛素多肽受体、VIP-1、NPY、叶酸受体、LHRH、神经元转运体(例如去甲肾上腺素转运体(NET))、EGFR、HER-2、VGFR、MUC-1、CEA、MUC-4、ED2、TF-抗原、内皮特异性标记、神经肽Y、uPAR、TAG-72、密封蛋白、CCK类似物、VIP、铃蟾肽、VEGFR、肿瘤特异性细胞表面蛋白、GLP-1、CXCR4、Hepsin、TMPRSS2、caspace、cMET、或过表达肽受体。本文公开的任何实施方式的肿瘤靶向结构域可包括经修饰抗体、经修饰抗体片段、经修饰结合肽、前列腺特异性膜抗原(“PSMA”)结合肽、生长激素抑制素受体激动剂、铃蟾肽受体激动剂、seprase结合化合物、或其任一种或多种的结合片段。
在本发明所公开的任何实施方式中,化合物可以是式I至V中的任一者或其药学上可接受的盐和/或溶剂合物:
TTD-L
其中
TTD是本文公开的任何实施方式的肿瘤靶向结构域;
BBD是本文公开的任何实施方式的血液-蛋白结合结构域;
Sarc是本文公开的任何实施方式的含sarcophagine的结构域;
X
L
L
p在每次出现时独立为0、1、2、3、4或5;和
q在每次出现时独立为1或2。
在化合物的本文公开的任何实施方式中,含sarcophagine的结构域可以或不可以螯合
在一方面,提供了一种组合物,其包含本文公开的任何实施方式的化合物并且还包含药学上可接受的载体。
在一方面,提供了一种药物组合物,其中组合物包含有效量的本文公开的任何实施方式的化合物,其螯合
在一方面,提供了一种药物组合物,其中组合物包含有效量的螯合
附图说明
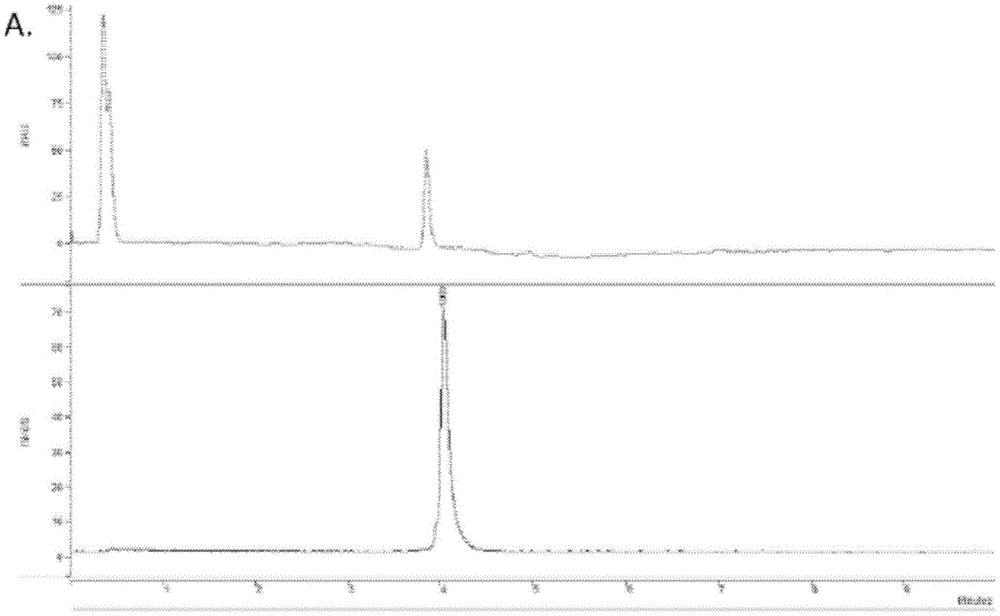
图1A-1B显示根据工作实施例的本发明的加标样品的HPLC色谱图,其中图1A是[
图2A-2B显示25℃下20分钟之后[
图3显示根据工作实施例的携带LNCaP异种移植肿瘤的雄性Balb/C nu/nu小鼠中的[
图4示出根据工作实施例的携带LNCaP异种移植物的雄性Balb/C nu/nu小鼠中的[
图5显示根据工作实施例的携带LNCaP异种移植物的雄性Balb/C nu/nu小鼠中[
图6显示根据工作实施例的雄性Balb/C nu/nu小鼠的LNCaP肿瘤和肾中[
具体实施方式
以下术语如下定义地全文使用。
如本文和所附权利要求中所使用,在描述要素的上下文中(特别是在以下权利要求的上下文中)的单数冠词,例如“一个”和“一种”和“所述”以及类似指代物应被解释为涵盖单数和复数,除非本文另有说明或与上下文明显矛盾。在本文列举值的范围仅仅意在用作一种单独地指代落在范围内的每个单独值的简略方法,除非本文另有说明,并且每个单独值被并入说明书中,就像在本文中单独列举一样。本文描述的所有方法都可以以任何合适的顺序执行,除非在本文中另有说明或除非与上下文明显矛盾。本文提供的任何和所有实例或示例性语言(例如,“例如”)的使用仅意在更好地阐明实施方式,并非不对权利要求的范围构成限制,除非另有说明。说明书中的任何语言都不应被解释为表明任何非要求保护的要素是必要的。
如本文所用,“约”将为本领域技术人员所理解,并将在一定程度上根据其使用的上下文所变化。如果本领域技术人员不清楚该术语的用途,则鉴于其使用的上下文,“约”将意指高达该特定术语的正负10%-例如,“约10重量%”将理解为意指“9重量%至11重量%”。当“约”位于术语之前时,该术语应被解释为公开“约”该术语以及未经“约”修改的术语-例如,“约10wt.%”公开了“9wt.%至11wt.%”以及公开了“10wt.%”。
如本发明中使用的短语“和/或”将被理解为意指所述成员中的任一个单独或其任两个或多个的组合-例如,“A、B和/或C”将意指“A、B、C,A和B,A和C,或B和C”。
如本文所用,术语“氨基酸”包括天然存在的α-氨基酸和合成的α-氨基酸(例如,2-氨基-2-苯乙酸,也称为苯甘氨酸),以及功能类似于天然存在的氨基酸的α-氨基酸类似物和氨基酸模拟物。该术语还包括此类α-氨基酸的L型和D型两者,除非指明了特定的立体异构体。天然存在的氨基酸是由遗传密码编码的那些,以及后来修饰的那些氨基酸,例如羟脯氨酸、γ-羧谷氨酸和O-磷酸丝氨酸。氨基酸类似物是指与天然存在氨基酸具有相同碱性化学结构的化合物,例如携带有机基团的α-碳,例如高丝氨酸、正亮氨酸、蛋氨酸亚砜、蛋氨酸甲基锍。此类类似物可以具有修饰的有机基团(例如,去亮氨酸)或修饰的肽骨架,但保留与自然存在的氨基酸相同的基本化学结构。氨基酸模拟物是指具有不同于氨基酸一般化学结构的结构但功能类似于天然存在的氨基酸的化学化合物。氨基酸在本文中可以用其通常已知的三个字母符号来指代,或用IUPAC-IUB生化命名委员会(IUPAC-IUB BiochemicalNomenclature Commission)推荐的一个字母符号来指代。
如本文所用,术语“多肽”、“肽”和“蛋白”在本文中可互换使用来意指包含由肽键或经修饰的肽键彼此连接两个或多个氨基酸的聚合物,即肽等排体。多肽既是指短链(通常称为多肽、糖肽或寡聚物),并且是指长链(通常称为蛋白质)两者。多肽可以含有20种基因编码氨基酸以外的氨基酸。多肽包括通过天然过程(例如翻译后加工)或通过本领域公知的化学修饰技术修饰的氨基酸序列,以及氨基酸。
通常,提及某种元素,例如氢或H,意在包括此元素的所有同位素。例如,如果R基团被定义为包括氢或H,它还包括氘和氚。因此,包含放射性同位素(例如氚、C
通常,“取代的”是指如下所定义的有机基团(例如烷基基团),其中至其中所含氢原子的一个或多个键被至非氢或非碳原子的键所替代。经取代的基团还包括其中至一个或多个碳原子或氢原子的一个或多个键被至杂原子的一个或多个键(包括双键或三键)所替代的基团。因此,除非另有说明,否则经取代的基团被一种或多种取代基取代。在一些实施方式中,经取代的基团被1、2、3、4、5或6个取代基取代。取代基基团的实例包括但不限于:卤素(即F、Cl、Br和I);羟基;烷氧基、烯氧基、芳氧基、芳烷氧基、杂环基、杂环烷基、杂环氧基和杂环烷氧基基团;羰基(氧代基);羧酸根;酯;尿烷;肟;羟胺;烷氧基胺;芳烷氧基胺;硫醇;硫化物;亚砜;砜;磺酰基;五氟硫烷基(即SF
经取代的环基团例如经取代的环烷基、芳基、杂环基和杂芳基基团,也包括其中至氢原子的键被至碳原子的键替代的环和环体系。因此,经取代的环烷基、芳基、杂环基和杂芳基基团还可被如下所定义的经取代或未取代的烷基、烯基和炔基基团取代。
如本文所用,C
烷基基团包括具有1至12个碳原子且通常1至10个碳、或在一些实施方式中1至8个、1至6个、或1至4个碳原子的直链和支链烷基基团。直链烷基基团的实例包括基团例如甲基、乙基、正丙基、正丁基、正戊基、正己基、正庚基和正辛基基团。支化烷基基团的实例包括但不限于异丙基、异丁基、仲丁基、叔丁基、新戊基、异戊基和2,2-二甲基丙基基团。烷基基团可以是取代的或未取代的。代表性取代的烷基基团可被取代基、例如以上列出的那些取代一次或多次,并且包括但不限于卤代烷基(例如三氟甲基)、羟烷基、硫代烷基、氨基烷基、烷基氨基烷基、二烷基氨基烷基、烷氧基烷基和羧基烷基。
环烷基基团包括在环中具有3至12个碳原子或在一些实施方式中具有3至10、3至8或3至4、5或6个碳原子的单环状、双环状或三环状烷基基团。示例性单环状环烷基基团包括但不限于环丙基、环丁基、环戊基、环己基、环庚基和环辛基基团。在一些实施方式中,环烷基基团具有3至8个环成员,而在其他实施方式中,环碳原子的数量范围为3至5、3至6或3至7。双环状和三环状环体系包括桥接环烷基基团和稠合环,例如但不限于双环[2.1.1]己烷、金刚烷基、十氢化萘基等。环烷基基团可以是取代的或未取代的。取代的环烷基基团可以用如上定义的非氢和非碳基团取代一次或多次。然而,取代的环烷基基团还包括被如上所定义的直链或支链烷基基团取代的环。代表性取代的环烷基基团可以是单取代的或取代多于一次,例如但不限于2,2-、2,3-、2,4-2,5-或2,6-二取代的环己基基团,其可被取代基例如以上列出的那些取代。
环烷基烷基基团是如上所定义的烷基基团,其中烷基基团的氢或碳键被至如上所定义的环烷基基团的键替代。在一些实施方式中,环烷基烷基基团具有4至16个碳原子、4至12个碳原子和通常4至10个碳原子。环烷基烷基基团可以是取代的或未取代的。取代的环烷基烷基基团可在基团的烷基、环烷基或烷基和环烷基两部分处被取代。代表性取代的环烷基烷基基团可以是单取代的或取代多于一次,例如但不限于被取代基例如以上列出的那些单取代、二取代或三取代。
烯基基团包括如上文定义的直链和支链烷基基团,除两个碳原子之间至少存在一个双键外。烯基基团具有2至12个碳原子且通常2至10个碳、或在一些实施方式中2至8个、2至6个、或2至4个碳原子的直链和支链烷基基团。在一些实施方式中,烯基基团具有一个、两个或三个碳-碳双键。实例尤其包括但不限于乙烯基、烯丙基、-CH=CH(CH
环烯基基团包括在两个碳键之间具有至少一个双键的如上所定义的环烷基基团。环烯基基团可以是取代的或未取代的。在一些实施方式中,环烯基基团可以有一个、两个或三个双键,但不包括芳族化合物。环烯基基团具有4至14个碳原子,或在一些实施方式中,5至14个碳原子、5至10个碳原子,或甚至5、6、7或8个碳原子。环烯基基团的实例包括环己烯基、环戊烯基、环己二烯基、环丁二烯基和环戊二烯基。
环烯基烷基基团是如上所定义的烷基基团,其中烷基基团的氢或碳键被至如上所定义的环烯基基团的键替代。环烯基烷基基团可以是取代的或未取代的。取代的环烯基烷基基团可在基团的烷基、环烯基或烷基和环烯基两部分处取代。代表性取代的环烯基烷基基团可被取代基例如以上列出的那些取代一次或多次。
炔基基团包括如上所定义的直链和支链烷基基团,除了两个碳原子之间存在至少一个三键之外。炔基基团具有2至12个碳原子,并且通常是2至10个碳原子,或在一些实施方式中,2至8、2至6、或2至4个碳原子。在一些实施方式中,炔基基团具有一个、两个或三个碳-碳三键。实例包括但不限于-C≡CH、-C≡CCH
芳基基团是不含杂原子的环状芳族烃。本文的芳基基团单环、双环和三环体系。因此,芳基基团包括但不限于苯基、薁基、庚烯基、联苯基、芴基、菲基、蒽烯基、茚基、茚满基、戊烯基和萘基基团。在一些实施方式中,芳基基团在基团的环部分中含有6至14个碳,并且在其他中,6至12或甚至6至10个碳原子。在一些实施方式中,芳基基团是苯基或萘基。芳基基团可以是取代的或未取代的。短语“芳基基团”包括含有稠环的基团,例如稠合芳族-脂族环体系(例如茚满基、四氢萘基等)。代表性取代的芳基基团可以是单取代的或取代多于一次。例如,单取代的芳基基团包括但不限于2-、3-、4-、5-或6-取代的苯基或萘基基团,其可被取代基例如以上列出的那些取代。
芳烷基基团是如上文所定义的烷基基团,其中烷基基团的氢或碳键被至如上所定义的芳基基团的键替代。在一些实施方式中,芳烷基基团含有7至16个碳原子、7至14个碳原子、或7至10个碳原子。芳烷基基团可以是取代的或未取代的。经取代的芳烷基基团可在基团的烷基、芳基或烷基和芳基两部分处取代。代表性芳烷基基团包括但不限于苄基和苯乙基基团,以及稠合(环烷基芳基)烷基基团、例如4-茚满基乙基。代表性取代的芳烷基基团可以被取代基、例如以上列出的那些取代一次或多次。
杂环基基团包括含有3或多个环成员的芳族(也称为杂芳基)和非芳族环化合物,其中的一个或多个是杂原子,例如但不限于N、O和S。在一些实施方式中,杂环基基团含有1、2、3或4个杂原子。在一些实施方式中,杂环基基团包括具有3至16个环成员的单环状环、双环状环和三环状环,而其他这种基团具有3至6个、3至10个、3至12个或3至14个环成员。杂环基基团涵盖芳族、部分不饱和的和饱和的环体系,例如咪唑基、咪唑啉基和咪唑烷基基团。短语“杂环基基团”包括稠环物质,包括包含稠合芳族和非芳族基团的那些,例如苯并三唑基、2,3-二氢苯并[1,4]二噁英基和苯并[1,3]二代基。短语还包括含有杂原子的桥接多环状环体系,例如但不限于奎宁环基(quinuclidyl)。杂环基基团可以是取代的或未取代的。杂环基基团包括但不限于氮丙啶基、吖丁啶基、吡咯烷基、咪唑烷基、吡唑烷基、噻唑烷基、四氢噻吩基、四氢呋喃基、间二氧杂环戊烯基、呋喃基、噻吩基、吡咯基、吡咯啉基、咪唑基、咪唑啉基、吡唑基、吡唑啉基、三唑基、四唑基、噁唑基、异噁唑基、噻唑基、噻唑啉基、异噻唑基、噻二唑基、噁二唑基、哌啶基、哌嗪基、吗啉基、硫代吗啉基、四氢吡喃基、四氢硫代吡喃基、氧硫杂环己烷、dioxyl、二噻烷基、吡喃基、吡啶基、嘧啶基、哒嗪基、吡嗪基、三嗪基、二氢吡啶基、二氢二硫杂环己二烯基(dihydrodithiinyl)、二氢二硫酮基基、高哌嗪基、奎宁环基、吲哚基、吲哚啉基、异吲哚基、氮杂吲哚基(吡咯并吡啶基)、吲唑基、吲哚嗪基、苯并三唑基、苯并咪唑基、苯并呋喃基、苯并噻吩基、苯并噻唑基、苯并噁二唑基、苯并噁嗪基、苯并二硫杂环己二烯基、苯并氧硫杂环己二烯基、苯并噻嗪基、苯并噁唑基、苯并噻唑基、苯并噻二唑基、苯并[1,3]间二氧杂环戊烯基、吡唑并吡啶基、咪唑并吡啶基(氮杂苯并咪唑基)、三唑并吡啶基、异噁唑并吡啶基、嘌呤基、黄嘌呤基、腺嘌呤基、鸟嘌呤基、喹啉基、异喹啉基、喹嗪基、喹喔啉基、喹唑啉基、噌啉基、酞嗪基、萘啶基、蝶啶基、硫杂萘基、二氢苯并噻嗪基、二氢苯并呋喃基、二氢吲哚基、二氢苯并二噁英基、四氢吲哚基、四氢吲唑基、四氢苯并咪唑基、四氢苯并三唑基、四氢吡咯并吡啶基、四氢吡唑并吡啶基、四氢咪唑并吡啶基、四氢三唑并吡啶基和四氢喹啉基基团。代表性取代的杂环基基团可以是单取代的或被取代多于一次,例如但不限于吡啶基或吗啉基基团,其是2-、3-、4-、5-或6-取代的,或被各种取代基例如以上列出的那些进行二取代。
杂芳基基团是含有5或多个环成员的芳族环化合物,其中一个或多个是杂原子例如但不限于N、O和S。杂芳基基团包括但不限于基团例如吡咯基、吡唑基、三唑基、四唑基、噁唑基、异噁唑基、噻唑基、吡啶基、哒嗪基、嘧啶基、吡嗪基、噻吩基、苯并噻吩基、呋喃基、苯并呋喃基、吲哚基、氮杂吲哚基(吡咯并吡啶基)、吲唑基、苯并咪唑基、咪唑并吡啶基(氮杂苯并咪唑基)、吡唑并吡啶基、三唑并吡啶基、苯并三唑基、苯并噁唑基、苯并噻唑基、苯并噻二唑基、咪唑并吡啶基、异噁唑并吡啶基、硫杂萘基、嘌呤基、黄嘌呤基、腺嘌呤基、鸟嘌呤基、喹啉基、异喹啉基、四氢喹啉基、喹喔啉基和喹唑啉基基团。杂芳基基团包括其中所有环都是芳族的稠环化合物,例如吲哚基基团;并且包括其中只有一个环是芳族的稠环化合物,例如2,3-二氢吲哚基基团。杂芳基基团可以是取代的或未取代的。因此,短语“杂芳基基团”包括稠环化合物,以及包括具有其他基团键合至环成员之一(例如烷基基团)的杂芳基基团。代表性取代的杂芳基基团可被各种取代基例如以上列出的那些取代一次或多次。
杂环基烷基基团是如上所定义的烷基基团,其中烷基基团的氢或碳键被至如上所定义的杂环基基团的键替代。杂环基烷基基团可以是取代的或未取代的。取代的杂环基烷基基团可以在基团的烷基、杂环基或烷基和杂环基两个部分处被取代。代表性杂环基烷基基团包括但不限于吗啉-4-基-乙基、呋喃-2-基-甲基、咪唑-4-基-甲基、吡啶-3-基-甲基、四氢呋喃-2-基-乙基和吲哚-2-基-丙基。代表性取代的杂环基烷基基团可以用取代基例如上文列出的那些取代一次或多次。
杂芳烷基基团是如上所定义的烷基基团,其中烷基基团的氢或碳键被至如上所定义的杂芳基基团的键替代。杂芳烷基基团可以是取代的或未取代的。经取代的杂芳烷基基团可以在基团的烷基、杂芳基或烷基和杂芳基两个部分处被取代。代表性取代的杂芳烷基基团可以用取代基例如以上列出的那些取代一次或多次。
本文所述的在本发明的化合物中具有两个或多个附接点(即二价、三价或多价)的基团通过使用后缀“ene”来指定。例如,二价烷基基团是亚烷基基团、二价芳基基团是亚芳基基团、二价杂环基基团是杂亚环基基团、二价杂芳基基团是亚杂芳基基团等。具有至本发明的化合物的单点附接的取代基团不使用“ene”命名指代。因此,如氯乙基在本文中不称为亚氯乙基。此类基团还可以被取代或不取代。
烷氧基基团是羟基基团(-OH),其中至氢原子的键被至如上定义的经取代或未取代的烷基基团的碳原子的键替代。线性烷氧基基团的实例包括但不限于甲氧基、乙氧基、丙氧基、丁氧基、戊氧基、己氧基等。支化烷氧基基团的实例包括但不限于异丙氧基、仲丁氧基、叔丁氧基、异戊氧基、异己氧基等。环烷氧基基团的实例包括但不限于环丙氧基、环丁氧基、环戊氧基、环己氧基等。烷氧基基团可以是取代的或未取代的。代表性取代的烷氧基基团可以用取代基例如上文列出的那些取代一次或多次。
如本文所用的语“烷酰基”和“烷酰基氧基”可分别是指–C(O)–烷基和–O–C(O)–烷基基团,其中在一些实施方式中,烷酰基或烷酰基氧基基团各自含有2–5个碳原子。类似地,术语“芳酰基”和“芳酰基氧基”分别是至–C(O)–芳基和–O–C(O)–芳基基团。
术语“芳基氧基”和“芳基烷氧基”分别是指键合至氧原子的经取代或未取代的芳基基团和键合至烷基处的氧原子的经取代或未取代的芳烷基基团。实例包括但不限于苯氧基、萘氧基和苄氧基。代表性取代的芳基氧基和芳基烷氧基基团可以用取代基例如上文列出的那些取代一次或多次。
如本文所用的术语“羧酸”是指具有–C(O)OH基团的化合物。如本文所用的术语“羧酸根”是指–C(O)O
如本文所用的术语“酯”是指–COOR
术语“酰胺”(或“酰氨基”)包括C-和N-酰胺基团,即分别是-C(O)NR
如本文所用的术语“腈”或“氰基”是指–CN基团。
尿烷基团分别包括N-和O-尿烷基团,即-NR
如本文所定义的术语“胺”(或“氨基”)是指–NR
术语“磺酰氨基”分别包括S-和N-磺酰胺基基团,即-SO
术语“巯基”是指–SH基团,而硫化物包括–SR
术语“脲”是指–NR
术语“脒”是指如本文所定义的–C(NR
术语“胍”是指–NR
术语“烯胺”是指–C(R
如本文所用的术语“卤素(halogen)”或“卤素(halo)”是指溴、氯、氟或碘。在一些实施方式中,卤素是氟。在其他实施方式中,卤素是氯或溴。
如本文所用的术语“羟基”可以是指–OH或其电离形式–O
术语“酰亚胺”是指–C(O)NR
术语“亚胺”是指–CR
如本文所用的术语“硝基”是指–NO
如本文所用的术语“三氟甲基”是指–CF
如本文所用的术语“三氟甲氧基”是指–OCF
术语“叠氮基”是指–N
术语“三烷基铵”是指–N(烷基)
术语“三氟甲基二氮环甲烷”是指
术语“异氰基”是指–NC。
术语“异硫代氰基”是指–NCS。
术语“五氟硫烷基”是指–SF
如本领域技术人员将理解,对于任何和所有目的,特别是在提供书面描述方面,本文公开的所有范围还涵盖任何和所有可能的子范围及其子范围的组合。任何列出的范围都可以很容易地识别为足够的描述,并使相同的范围被分解为至少相等的二分之一、三分之一、四分之一、五分之一、十分之一等。作为非限制性实例,本文讨论的每个范围都可以很容易地分解为下三分之一、中三分之一和上三分之一等。如本领域技术人员也将理解,例如“至多”、“至少”、“大于”、“小于”等的所有语言都包括所列举的数字,并且是指随后可分解为如上所讨论的子范围的范围。最终,如本领域技术人员所理解,范围包括每个单独的成员。因此,例如具有1至3个原子的基团是指具有1、2或3个原子的基团。类似地,具有1至5个原子的基团是指具有1、2、3、4或5个原子的基团,以此类推。
本文所述的化合物的药学上可接受的盐在本发明的范围内,并且包括保留所需药理活性并且在生物学上不是不可取的酸或碱加成盐(例如,盐没有不适当的毒性、致敏性或刺激性,并且是生物可利用的)。当本发明的化合物具有碱性基团,例如例如氨基基团时,药学上可接受的盐可以与无机酸(例如盐酸、氢硼酸、硝酸、硫酸和磷酸)、有机酸(例如海藻酸、甲酸、乙酸、苯甲酸、葡萄糖酸、富马酸、草酸、酒石酸、乳酸、马来酸、柠檬酸、琥珀酸、苹果酸、甲磺酸、苯磺酸、萘磺酸和对甲苯磺酸)或酸性氨基酸(例如天冬氨酸和谷氨酸)。当本发明的化合物含有酸性基团,例如例如羧酸基团时,它可以与金属例如碱金属和碱土金属(例如Na
本领域技术人员将认识到,本发明的化合物可以表现出互变异构、构象异构、几何异构和/或立体异构现象。由于说明书和权利要求中的式图只能表示可能的互变异构、构象异构、立体化学或几何异构形式中的一种,因此应该理解,本发明涵盖具有本文所述的一种或多种用途的化合物的任何互变异构、构象异构、立体化学和/或几何异构形式,以及这些各种不同形式的混合物。
“互变异构体”是指化合物的异构形式,它们彼此之间处于平衡。异构形式的存在和浓度将取决于化合物所处的环境,并且可能不同,例如,取决于化合物是固体,还是在有机或水溶液中。例如,在水溶液中,喹唑啉酮可表现出以下异构形式,它们被称为彼此的互变异构体:
作为另一个实例,胍在质子有机溶液中可以表现出以下异构形式,也称为彼此的互变异构体:
由于用结构式表示化合物的局限性,应理解,本文所述化合物的所有化学式都表示化合物的所有互变异构形式,并且在本发明的范围内。
化合物的立体异构体(也称为光学异构体)包括结构的所有手性、非对映异构体和外消旋形式,除非明确指出了特定的立体化学。因此,在本发明中使用的化合物包括在任何或所有不对称原子上的富集或拆分光学异构体,如从描述中很明显。外消旋和非对映异构体体混合物两者,以及单独的光学异构体都可以被分离或合成,从而基本上不含它们的对映异构体或非对映异构体伴侣,并且这些立体异构体都在本发明的范围内。
本发明的化合物可以以溶剂合物、特别是水合物存在。水合物可以在化合物或包含化合物的组合物的制造过程中形成,或者由于化合物的吸湿性质,水合物可以随着时间的推移而形成。本发明的化合物也可以作为有机溶剂存在,包括DMF、醚和醇溶剂合物等。任何特定溶剂合物的鉴定和制备都在合成有机化学或药物化学的普通技术人员的技能范围内。
在整个本发明中,各种出版物、专利和公布的专利说明书都通过识别引文引用。在本发明中还包括指代引用的引文的阿拉伯数字,其完整的书目细节在实施例内章节中提供。这些出版物、专利和公布的专利说明书的公开内容在此通过引用并入本发明,以更全面地描述本发明。
本发明
靶向前列腺特异性膜抗原(PSMA)的放射性配体在前列腺癌的临床成像和疗法中表现出令人鼓舞的功效。第一个进行临床评价的配体是靶向PSMA的抗体,但最近放射标记的PSMA小分子抑制剂因其在肿瘤中快速积累、从非靶组织中清除以及被认为是患者相当可接受的副作用特性而受到关注。这些化合物中的许多利用谷氨酸-脲-赖氨酸或谷氨酸-脲-谷氨酸部分来实现对PSMA的靶向和高亲和力结合。在目前临床研究中的一些PSMA-靶向配体中,有某些用氟-18或镓-68标记的诊断性化合物用于通过正电子发射断层扫描(PET)进行的肿瘤成像,或用碘-131、镥-177、铋-213或锕-225标记的治疗性化合物用于PSMA-表达癌症的靶向放射性配体疗法。
虽然小分子的组织分布和清除通常是快速的,但铜-64较长的半衰期(t
治疗诊断的概念描述了使用一对匹配的放射性核素来使得能够量化体内的放射性分布,然后使用相同的传递载体进行放射性配体疗法。在使用靶向PSMA的
铜-64(t
本发明提供了克服这些问题的新型化合物,特别是提供了具有多个结构域的三功能化合物,包括一个以相对高亲和力靶向并结合至肿瘤标记的结构域,和另一个以一系列中度至弱亲和力结合血蛋白(例如血清白蛋白)的结构域。这些化合物包括对铜具有高选择性的螯合部分–具体地说,是3,6,10,13,16,19-六氮杂双环[6.6.6]二十烷的衍生物,称为sarcophagine。
因此,在一方面,提供了一种化合物,其包括肿瘤靶向结构域(其中肿瘤靶向结构域包括能够识别肿瘤细胞表面上的分子靶标或与肿瘤细胞表面上的分子靶标相互作用的部分)、血液-蛋白结合结构域和含sarcophagine的结构域,其中肿瘤靶向结构域的部分位于血液-蛋白结合结构域的远端并且在空间上不受血液-蛋白结合结构域阻碍。
如上文所讨论,肿瘤靶向结构域(“TTD”)包括能够识别肿瘤细胞表面上的分子靶标或与肿瘤细胞表面上的分子靶标相互作用的部分。此类分子靶标包括细胞表面蛋白,例如受体、酶和抗原。例如,分子靶标可以是能够与肿瘤靶向结构域相互作用的在肿瘤细胞表面上表达的受体、酶和/或抗原(例如肿瘤特异性细胞表面蛋白)。此类肿瘤靶向结构域的实例是被在大多数前列腺癌细胞表面上表达的前列腺特异性膜抗原(PSMA)识别的谷氨酸-脲-赖氨酸基序。另一个实例是依多曲肽,被许多神经内分泌癌症表面上表达的生长激素抑制素受体识别。因此,本文的任何方面和实施方式的肿瘤靶向结构域可能能够结合至肿瘤相关分子靶标,其包括以下中的一者或多者:肿瘤相关分子靶标,其为肿瘤特异性细胞表面蛋白或其他标记,例如前列腺特异性膜抗原(PSMA)、生长激素抑制素肽受体-2(SSTR2)、alphavbeta3(αvβ3)、αvβ6、胃泌素释放肽受体、seprase(例如成纤维细胞激活蛋白α(FAP-α))、肠促胰岛素受体、葡萄糖依赖性促胰岛素多肽受体、VIP-1、NPY、叶酸受体、LHRH、神经元转运体(例如去甲肾上腺素转运体(NET))、EGFR、HER-2、VGFR、MUC-1、CEA、MUC-4、ED2、TF-抗原、内皮特异性标记、神经肽Y、uPAR、TAG-72、密封蛋白、CCK类似物、VIP、铃蟾肽、VEGFR、肿瘤特异性细胞表面蛋白、GLP-1、CXCR4、Hepsin、TMPRSS2、caspace、cMET或过表达肽受体。上述只是代表性的肿瘤相关分子靶标,并且其靶标和与之结合的化合物都存在详细的结构信息。对这些特定细胞靶标显示特定亲和力的各种抗体、多肽和化合物广泛描述在科学文献中,并且可以适应本发明作为肿瘤靶向结构域。本文的任何方面和实施方式的肿瘤靶向结构域能够以至少中度亲和力至高度亲和力结合至肿瘤相关分子靶标(如,平衡结合常数(K
因此,肿瘤靶向结构域的实例包括靶向并结合至PSMA的活性位点的部分,包括例如谷氨酸-脲基-氨基酸序列、在赖氨酸的ε胺处具有或不具有芳族取代基的谷氨酸-脲-赖氨酸序列,或可以中度至高度亲和力结合PSMA的活性位点的其任何衍生物。本文提供了示例性结构,然而可以靶向PSMA的其他区域,并且这些与本文详述的化合物中的PSMA肿瘤靶向结构域可互换。一个对PSMA具有亲和力的示例性含铜三功能化合物如下:
其中“Cu”可以是
Seprase(或成纤维细胞活化蛋白(FAP))是一种完整的膜丝氨酸肽酶。除了明胶酶活性外,seprase在肿瘤进展中具有双重功能。Seprase促进细胞对ECM的侵入,并且也支持肿瘤的生长和增殖。如上所讨论,肿瘤靶向结构域可包括结合至seprase的部分,例如seprase抑制剂。含铜三功能化合物的示例性结构如下所提供,其对FAP具有亲和力并且可用于大多数癌症的诊断和疗法中:
其中“Cu”可以是
生长激素抑制素是一种肽激素,其调控内分泌系统,并经由与G蛋白偶联生长激素抑制素受体相互作用和抑制许多次生激素释放来影响神经传递和细胞增殖。生长激素抑制素有由单个前原蛋白的交替切割产生的两种活性形式。有五种已知的生长激素抑制素受体,都是G蛋白偶联的7个跨膜受体:SST1(SSTR1);SST2(SSTR2);SST3(SSTR3);SST4(SSTR4);和SST5(SSTR5)。示例性生长激素抑制素受体激动剂包括生长激素抑制素自身、兰瑞肽、奥曲肽酸(octreotate)、奥曲肽、帕瑞肽和伐普肽。许多神经内分泌瘤表达SSTR2和其他生长激素抑制素受体。长效生长激素抑制激动剂(例如奥曲肽、兰瑞肽)用于刺激SSTR2受体,并从而抑制进一步的肿瘤增殖。参见Zatelli MC,等人,(2007年4月)."Control ofpituitary adenoma cell proliferation by somatostatin analogs,dopamineagonists and novel chimeric compounds".European Journal of Endocrinology/European Federation of Endocrine Societies.156增刊1:S29–35。奥曲肽是一种模仿天然生长激素抑制素但在体内具有明显较长的半衰期的八肽。奥曲肽用于治疗产生生长激素的肿瘤(肢端肥大症和巨人症),当手术是禁忌的时,分泌甲状腺刺激激素的垂体瘤(促甲状腺素瘤)、与类癌综合征相关的腹泻和潮红发作,及血管活性肠肽分泌肿瘤(VIPomas)患者的腹泻。兰瑞肽用于管理肢端肥大症和由神经内分泌瘤引起的症状,最显著的是类癌综合征。帕瑞肽是一种与其他生长激素抑制素激动剂相比对SSTR5具有更高的亲和力的生长激素抑制素类似物,并被批准用于治疗库欣病(Cushing's disease)和肢端肥大症。伐普肽用于治疗肝硬化病和AIDS-相关腹泻患者体内的食管静脉曲张出血。因此,就本发明而言,下面描述了基于兰瑞肽衍生物的含铜三功能化合物的示例结构,其对SSTR2具有亲和力并且可用于上述疾病的诊断和治疗:
其中“Cu”可以是
铃蟾肽是一种最初从欧洲火腹蟾蜍(红腹铃蟾(Bombina bombina))的皮肤中分离的肽。除了刺激G细胞释放胃泌素外,铃蟾肽还激活至少三种不同的G蛋白偶联受体:BBR1、BBR2和BBR3,其中这种活性包括大脑中此类受体的激动。铃蟾肽也是小细胞肺癌、胃癌、胆囊癌、胰腺癌和成神经细胞瘤的肿瘤标记。铃蟾肽受体激动剂包括但不限于BBR-1激动剂、BBR-2激动剂和BBR-3激动剂。含铜三功能化合物的示例性结构如下所提供,其对铃蟾肽具有亲和力并且可以用于以上癌症的诊断和疗法中:
其中“Cu”可以是
因此,本文公开的任何实施方式的肿瘤靶向结构域可包括经修饰抗体、经修饰抗体片段、经修饰结合肽、前列腺特异性膜抗原(“PSMA”)结合肽、生长激素抑制素受体激动剂、铃蟾肽受体激动剂、seprase结合化合物、或其任一种或多种的结合片段。本文公开的任何实施方式的肿瘤靶向结构域可包括贝利单抗、莫格利珠单抗、博纳吐单抗、替伊莫单抗、奥妥珠单抗、奥法木单抗、利妥昔单抗、奥英妥珠单抗、帕西妥莫单抗、维布妥昔单抗、达雷木单抗、伊匹单抗、西妥昔单抗、耐昔妥珠单抗、帕尼单抗、地努妥昔单抗、帕妥珠单抗、曲妥珠单抗、恩美曲妥珠单抗、司妥昔单抗、西米普利单抗、纳武单抗、派姆单抗、奥拉妥单抗、阿特珠单抗、阿维单抗、德瓦鲁单抗、喷地肽卡罗单抗、艾洛珠单抗、地诺单抗、Ziv-阿柏西普、贝伐珠单抗、雷莫芦单抗、托西莫单抗、奥加米星吉妥珠单抗、阿仑单抗、西妥木单抗、吉妥昔单抗、尼妥珠单抗、卡妥索单抗或埃达珠单抗。本文公开的任何实施方式的肿瘤靶向结构域可包括以下的抗原结合片段:贝利单抗、莫格利珠单抗、博纳吐单抗、替伊莫单抗、奥妥珠单抗、奥法木单抗、利妥昔单抗、奥英妥珠单抗、帕西妥莫单抗、维布妥昔单抗、达雷木单抗、伊匹单抗、西妥昔单抗、耐昔妥珠单抗、帕尼单抗、地努妥昔单抗、帕妥珠单抗、曲妥珠单抗、恩美曲妥珠单抗、司妥昔单抗、西米普利单抗、纳武单抗、派姆单抗、奥拉妥单抗、阿特珠单抗、阿维单抗、德瓦鲁单抗、喷地肽卡罗单抗、艾洛珠单抗、地诺单抗、Ziv-阿柏西普、贝伐珠单抗、雷莫芦单抗、托西莫单抗、奥加米星吉妥珠单抗、阿仑单抗、西妥木单抗、吉妥昔单抗、尼妥珠单抗、卡妥索单抗或埃达珠单抗。
血液-蛋白结合结构域“BBD”(例如白蛋白结合结构域;白蛋白结合部分)在调节对象中化合物的血液血浆清除率中起作用,从而增加循环时间和分隔含细胞毒素结构域的细胞毒性作用和/或含显像剂结构域在血浆空间中而不是可能表达抗原的正常器官和组织中的成像能力。不受理论所束缚,化合物的该组分被认为与血清蛋白(例如白蛋白和/或细胞要素)可逆地相互作用。该血液-蛋白结合结构域(例如白蛋白结合结构域;白蛋白结合部分)对血液的血浆或细胞组分的亲和力可以被配置为影响化合物在对象的血池中的滞留时间。在本文的任何实施方式中,血液-蛋白结合结构域(例如白蛋白结合结构域;白蛋白结合部分)可以被配置成当它在血液血浆中时可逆或不可逆地与白蛋白结合。
举例来说,本文的任何方面或实施方式的血液-蛋白结合结构域可包括短链脂肪酸、中链脂肪酸、长链脂肪酸、肉豆蔻酸、经取代或未取代的吲哚-2-羧酸、经取代或未取代的硫代酰胺、经取代或未取代的4-氧代-4-(5,6,7,8-四氢萘-2-基)丁酸、经取代或未取代的萘酰基磺酰胺、经取代或未取代的二苯基环己醇磷酸酯、经取代或未取代的4-碘代苯基烷酸、经取代或未取代的3-(4-碘代苯基)丙酸、经取代或未取代的2-(4-碘代苯基)乙酸、或经取代或未取代的4-(4-碘代苯基)丁酸。在本文公开的任何实施方式中,可能的是血液-蛋白结合结构域是
其中Y
/>
在本发明的任何实施方式中,化合物可以是式I至V中的任一者或其药学上可接受的盐和/或溶剂合物:
TTD-L
/>
其中
TTD是本文公开的任何实施方式的肿瘤靶向结构域;
BBD是本文公开的任何实施方式的血液-蛋白结合结构域;
Sarc是本文公开的任何实施方式的含sarcophagine的结构域;
X
L
L
p在每次出现时独立为0、1、2、3、4或5;和
q在每次出现时独立为1或2。
在本发明的任何实施方式中,肿瘤靶向结构域可以是
/>
其中W
本发明的化合物的含sarcophagine的结构域是能够螯合
本发明还提供了组合物和药物,该药物包含本发明化合物的任一个方面和实施方式以及药学上可接受的载体或一种或多种赋形剂或填料(除非另有说明,否则统称为“药学上可接受的载体”)。所述组合物可用于本文所述的方法和治疗中。本发明还提供了药物组合物,其包含药学上可接受的载体和有效量的用于使病症成像和/或治疗病症的本发明的化合物的方法和实施方式中任一种的化合物;并且其中病症可包括以下中的一者或多者:非小细胞肺癌、小细胞肺癌、膀胱癌、结肠癌、胆囊癌、胰腺癌、食道癌、黑素瘤、肝癌、原发性胃腺癌、原发性结直肠腺癌、肾细胞癌、前列腺癌、神经内分泌瘤、垂体瘤、血管活性肠肽分泌肿瘤、神经胶质瘤、乳腺癌、肾上腺皮质癌、宫颈癌、外阴癌、子宫内膜癌、原发性卵巢癌、转移性卵巢癌和转移癌。例如,这种病症可包括过表达PSMA的哺乳动物组织,例如表达PSMA的癌症(包括癌症组织、癌症相关的新血管或其组合)、克罗恩病或IBD。
在进一步相关的方面,提供了一种成像方法,其包括将本发明的化合物的任一方面和实施方式的化合物施用(例如施用有效量)或将包含有效量的本发明化合物的任一方面和实施方式的化合物的药物组合物施用给对象,并且在施用之后检测正电子发射、检测来自正电子发射和湮灭的伽马射线(例如通过正电子发射断层扫描),和/或检测由正电子发射导致的切伦科夫辐射(例如通过切伦科夫发光成像)。在成像方法的任何实施方式中,对象可疑似患有包括以下中的一者或多者的病症:非小细胞肺癌、小细胞肺癌、膀胱癌、结肠癌、胆囊癌、胰腺癌、食道癌、黑素瘤、肝癌、原发性胃腺癌、原发性结直肠腺癌、肾细胞癌、前列腺癌、神经内分泌瘤、垂体瘤、血管活性肠肽分泌肿瘤、神经胶质瘤、乳腺癌、肾上腺皮质癌、宫颈癌、外阴癌、子宫内膜癌、原发性卵巢癌、转移性卵巢癌、转移癌、过表达PSMA的哺乳动物组织,例如表达PSMA的癌症(包括癌症组织、癌症相关的新血管或其组合)、克罗恩病或IBD。检测步骤可以例如在对对象进行外科手术期间发生以去除过表达PSMA的哺乳动物组织。检测步骤可以包括使用手持设备来进行检测步骤。例如,切伦科夫发光图像可以通过使用超高灵敏度光学相机(例如电子倍增电荷耦合设备(EMCCD)相机)检测切伦科夫光来获得。
在以上实施方式的任一个中,有效量可以根据对象确定。“有效量”是指产生所想要效果所需的化合物或组合物的量。有效量或剂量的一个非限制性实例包括产生可接受的毒性和用于治疗(制药)用途的生物利用性水平的量或剂量,包括但不限于例如以下中的一者或多者的治疗:非小细胞肺癌、小细胞肺癌、膀胱癌、结肠癌、胆囊癌、胰腺癌、食道癌、黑素瘤、肝癌、原发性胃腺癌、原发性结直肠腺癌、肾细胞癌、前列腺癌(例如去势难治性前列腺癌)、神经内分泌瘤、垂体瘤、血管活性肠肽分泌肿瘤、神经胶质瘤、乳腺癌、肾上腺皮质癌、宫颈癌、外阴癌、子宫内膜癌、原发性卵巢癌、转移性卵巢癌和转移癌。有效量的另一个实例包括能够减少与如以下中的一者或多者相关的症状的量或剂量:非小细胞肺癌、小细胞肺癌、膀胱癌、结肠癌、胆囊癌、胰腺癌、食道癌、黑素瘤、肝癌、原发性胃腺癌、原发性结直肠腺癌、肾细胞癌、前列腺癌(例如去势难治性前列腺癌)、神经内分泌瘤、垂体瘤、血管活性肠肽分泌肿瘤、神经胶质瘤、乳腺癌、肾上腺皮质癌、宫颈癌、外阴癌、子宫内膜癌、原发性卵巢癌、转移性卵巢癌和转移癌,例如增殖和/或转移的减少。本发明的化合物的有效量可以包括足以能够检测该化合物与包括但不限于以下中的一者或多者的目标靶标的结合的量:非小细胞肺癌、小细胞肺癌、膀胱癌、结肠癌、胆囊癌、胰腺癌、食道癌、黑素瘤、肝癌、原发性胃腺癌、原发性结直肠腺癌、肾细胞癌、前列腺癌(例如去势难治性前列腺癌)、神经内分泌瘤、垂体瘤、血管活性肠肽分泌肿瘤、神经胶质瘤、乳腺癌、肾上腺皮质癌、宫颈癌、外阴癌、子宫内膜癌、原发性卵巢癌、转移性卵巢癌和转移癌。有效量的另一实例包括能够在具有组织的对象中从正电子发射和湮灭(高于背景)中提供可检测伽马射线发射的量或剂量,所述组织包括以下中的一者或多者:非小细胞肺癌、小细胞肺癌、膀胱癌、结肠癌、胆囊癌、胰腺癌、食道癌、黑素瘤、肝癌、原发性胃腺癌、原发性结直肠腺癌、肾细胞癌、前列腺癌(例如去势难治性前列腺癌)、神经内分泌瘤、垂体瘤、血管活性肠肽分泌肿瘤、神经胶质瘤、乳腺癌、肾上腺皮质癌、宫颈癌、外阴癌、子宫内膜癌、原发性卵巢癌、转移性卵巢癌、转移癌和过表达PSMA,例如统计学显著的发射高于背景。有效量的另一实例包括能够在具有组织的对象中提供由于正电子发射(高于背景)导致的可检测切伦科夫辐射发射的量或剂量,所述组织包括以下中的一者或多者:非小细胞肺癌、小细胞肺癌、膀胱癌、结肠癌、胆囊癌、胰腺癌、食道癌、黑素瘤、肝癌、原发性胃腺癌、原发性结直肠腺癌、肾细胞癌、前列腺癌(例如去势难治性前列腺癌)、神经内分泌瘤、垂体瘤、血管活性肠肽分泌肿瘤、神经胶质瘤、乳腺癌、肾上腺皮质癌、宫颈癌、外阴癌、子宫内膜癌、原发性卵巢癌、转移性卵巢癌、转移癌、和过表达PSMA,例如统计学显著的发射高于背景。有效量可为每克组合物中约0.01μg至约1mg化合物,并且优选为每克组合物中约0.1μg至约500μg化合物。
如本文所用,“对象”或“患者”是哺乳动物,例如猫、狗、啮齿动物或灵长类动物。通常,对象是人,并且优选是患有或疑似患有以下中的一者或多者的人:非小细胞肺癌、小细胞肺癌、膀胱癌、结肠癌、胆囊癌、胰腺癌、食道癌、黑素瘤、肝癌、原发性胃腺癌、原发性结直肠腺癌、肾细胞癌、前列腺癌(例如去势难治性前列腺癌)、神经内分泌瘤、垂体瘤、血管活性肠肽分泌肿瘤、神经胶质瘤、乳腺癌、肾上腺皮质癌、宫颈癌、外阴癌、子宫内膜癌、原发性卵巢癌、转移性卵巢癌和转移癌。术语“对象”和“患者”可以互换使用。
特别地,用于治疗癌症(例如以下中的一者或多者:非小细胞肺癌、小细胞肺癌、膀胱癌、结肠癌、胆囊癌、胰腺癌、食道癌、黑素瘤、肝癌、原发性胃腺癌、原发性结直肠腺癌、肾细胞癌、前列腺癌(例如去势难治性前列腺癌)、神经内分泌瘤、垂体瘤、血管活性肠肽分泌肿瘤、神经胶质瘤、乳腺癌、肾上腺皮质癌、宫颈癌、外阴癌、子宫内膜癌、原发性卵巢癌、转移性卵巢癌和转移癌)和/或过表达PSMA的哺乳动物组织的本文公开的任何实施方式的化合物的有效量可以是约0.1μg至约50μg/kg对象质量。因此,为了治疗癌症(如以下中的一者或多者:非小细胞肺癌、小细胞肺癌、膀胱癌、结肠癌、胆囊癌、胰腺癌、食道癌、黑素瘤、肝癌、原发性胃腺癌、原发性结直肠腺癌、肾细胞癌、前列腺癌(例如去势难治性前列腺癌)、神经内分泌瘤、垂体瘤、血管活性肠肽分泌肿瘤、神经胶质瘤、乳腺癌、肾上腺皮质癌、宫颈癌、外阴癌、子宫内膜癌、原发性卵巢癌、转移性卵巢癌和转移癌)和/或过表达PSMA的哺乳动物组织;本文所述的任何实施方式的化合物的有效量可为约0.1μg/kg、约0.2μg/kg、约0.3μg/kg、约0.4μg/kg、约0.5μg/kg、约0.6μg/kg、约0.7μg/kg、约0.8μg/kg、约0.9μg/kg、约1μg/kg、约2μg/kg、约3μg/kg、约4μg/kg、约5μg/kg、约6μg/kg、约7μg/kg、约8μg/kg、约9μg/kg、约10μg/kg、约11μg/kg、约12μg/kg、约13μg/kg、约14μg/kg、约15μg/kg、约16μg/kg、约17μg/kg、约18μg/kg、约19μg/kg、约20μg/kg、约22μg/kg、约24μg/kg、约26μg/kg、约28μg/kg、约30μg/kg、约32μg/kg、约34μg/kg、约36μg/kg、约38μg/kg、约40μg/kg、约42μg/kg、约44μg/kg、约46μg/kg、约48μg/kg、约50μg/kg或包括这些值的和/或这些值中任两个之间的任何范围。
特别地,用于使癌症(例如以下中的一者或多者:非小细胞肺癌、小细胞肺癌、膀胱癌、结肠癌、胆囊癌、胰腺癌、食道癌、黑素瘤、肝癌、原发性胃腺癌、原发性结直肠腺癌、肾细胞癌、前列腺癌(例如去势难治性前列腺癌)、神经内分泌瘤、垂体瘤、血管活性肠肽分泌肿瘤、神经胶质瘤、乳腺癌、肾上腺皮质癌、宫颈癌、外阴癌、子宫内膜癌、原发性卵巢癌、转移性卵巢癌和转移癌)和/或过表达PSMA的哺乳动物组织成像的本文任何实施方式的化合物的有效量可为约0.1μg至约50μg/kg对象质量。因此,为了治疗癌症(例如以下中的一者或多者:非小细胞肺癌、小细胞肺癌、膀胱癌、结肠癌、胆囊癌、胰腺癌、食道癌、黑素瘤、肝癌、原发性胃腺癌、原发性结直肠腺癌、肾细胞癌、前列腺癌(例如去势难治性前列腺癌)、神经内分泌瘤、垂体瘤、血管活性肠肽分泌肿瘤、神经胶质瘤、乳腺癌、肾上腺皮质癌、宫颈癌、外阴癌、子宫内膜癌、原发性卵巢癌、转移性卵巢癌和转移癌)和/或过表达PSMA的哺乳动物组织;本文所述的任何实施方式的化合物的有效量可为约0.1μg/kg、约0.2μg/kg、约0.3μg/kg、约0.4μg/kg、约0.5μg/kg、约0.6μg/kg、约0.7μg/kg、约0.8μg/kg、约0.9μg/kg、约1μg/kg、约2μg/kg、约3μg/kg、约4μg/kg、约5μg/kg、约6μg/kg、约7μg/kg、约8μg/kg、约9μg/kg、约10μg/kg、约11μg/kg、约12μg/kg、约13μg/kg、约14μg/kg、约15μg/kg、约16μg/kg、约17μg/kg、约18μg/kg、约19μg/kg、约20μg/kg、约22μg/kg、约24μg/kg、约26μg/kg、约28μg/kg、约30μg/kg、约32μg/kg、约34μg/kg、约36μg/kg、约38μg/kg、约40μg/kg、约42μg/kg、约44μg/kg、约46μg/kg、约48μg/kg、约50μg/kg、或包括这些值的和/或这些值中任两个之间的任何范围。
本发明的化合物还可连同可用于使以下中的一者或多者成像和/或治疗以下中的一者或多者的其他常规成像剂施用给患者:非小细胞肺癌、小细胞肺癌、膀胱癌、结肠癌、胆囊癌、胰腺癌、食道癌、黑素瘤、肝癌、原发性胃腺癌、原发性结直肠腺癌、肾细胞癌、前列腺癌(例如去势难治性前列腺癌)、神经内分泌瘤、垂体瘤、血管活性肠肽分泌肿瘤、神经胶质瘤、乳腺癌、肾上腺皮质癌、宫颈癌、外阴癌、子宫内膜癌、原发性卵巢癌、转移性卵巢癌、转移癌、或过表达PSMA的哺乳动物组织。这种哺乳动物组织包括但不限于表达PSMA的癌症(包括癌症组织、癌症相关的新血管,或其组合)、克罗恩病或IBD。因此,本发明的药物组合物和/或方法还可包括不同于本发明的化合物的成像剂;本发明的药物组合物和/或方法可包括不同于本发明的化合物的治疗剂;本发明的药物组合物和/或方法还可包括根据本发明的化合物的任何所述方案的成像剂和还根据本发明的化合物的任何实施方式的治疗剂。根据本发明的化合物可能既是一种治疗剂又是一种成像剂。施用可包括口服施用、肠胃外施用或经鼻施用。在这些实施方式的任一个中,施用可以包括皮下注射、静脉内注射、腹腔内注射或肌肉内注射。在这些实施方式的任一个中,施用可以包括口服施用。本发明的方法还可以包括按顺序或与本发明的一种或多种化合物联合施用常规成像剂,其量可以潜在地或协同地使以下中的一者或多者成像有效:非小细胞肺癌、小细胞肺癌、膀胱癌、结肠癌、胆囊癌、胰腺癌、食道癌、黑素瘤、肝癌、原发性胃腺癌、原发性结直肠腺癌、肾细胞癌、前列腺癌(例如去势难治性前列腺癌)、神经内分泌瘤、垂体瘤、血管活性肠肽分泌肿瘤、神经胶质瘤、乳腺癌、肾上腺皮质癌、宫颈癌、外阴癌、子宫内膜癌、原发性卵巢癌、转移性卵巢癌、转移癌和过表达PSMA的哺乳动物组织。
在本文所述的本发明的任何实施方式中,药物组合物可以以单位剂型包装。单位剂型可有效治疗以下中的一者或多者:非小细胞肺癌、小细胞肺癌、膀胱癌、结肠癌、胆囊癌、胰腺癌、食道癌、黑素瘤、肝癌、原发性胃腺癌、原发性结直肠腺癌、肾细胞癌、前列腺癌(例如去势难治性前列腺癌)、神经内分泌瘤、垂体瘤、血管活性肠肽分泌肿瘤、神经胶质瘤、乳腺癌、肾上腺皮质癌、宫颈癌、外阴癌、子宫内膜癌、原发性卵巢癌、转移性卵巢癌和转移癌。通常,包括本发明的化合物的单位剂量将根据患者的考虑而变化。此类考虑包括,例如年龄、方案、情况、性别、疾病程度、禁忌症、伴随疗法等。基于这些考虑的示例性单位剂量也可以由本领域技术人员调整或修改。例如,包含本发明的化合物的患者用单位剂量可以从1×10
药物组合物可以通过将本发明的一种或多种化合物与药学上可接受的载体、赋形剂、粘合剂、稀释剂等混合来制备,以预防和治疗与癌症相关的病症(例如,以下中的一者或多者:非小细胞肺癌、小细胞肺癌、膀胱癌、结肠癌、胆囊癌、胰腺癌、食道癌、黑素瘤、肝癌、原发性胃腺癌、原发性结直肠腺癌、肾细胞癌、前列腺癌(例如去势难治性前列腺癌)、神经内分泌瘤、垂体瘤、血管活性肠肽分泌肿瘤、神经胶质瘤、乳腺癌、肾上腺皮质癌、宫颈癌、外阴癌、子宫内膜癌、原发性卵巢癌、转移性卵巢癌和转移癌)。本文所述的化合物和组合物可用于制备制剂和药物,其治疗例如以下中的一者或多者:非小细胞肺癌、小细胞肺癌、膀胱癌、结肠癌、胆囊癌、胰腺癌、食道癌、黑素瘤、肝癌、原发性胃腺癌、原发性结直肠腺癌、肾细胞癌、前列腺癌(例如去势难治性前列腺癌)、神经内分泌瘤、垂体瘤、血管活性肠肽分泌肿瘤、神经胶质瘤、乳腺癌、肾上腺皮质癌、宫颈癌、外阴癌、子宫内膜癌、原发性卵巢癌、转移性卵巢癌和转移癌。此类组合物可以呈例如颗粒剂、粉剂、片剂、胶囊剂、糖浆剂栓剂、注射剂、乳剂、酏剂、混悬剂或溶液的形式。即时组合物可被配制为用于各种施用途径,例如通过口服、肠胃外、局部、经直肠、经鼻、经阴道施用或经由植入贮库。肠胃外或全身施用包括但不限于皮下、静脉内、腹膜内和肌肉内注射。以下剂型是作为示例给出的,并且不应被解释为限制即时本发明。
对于口服、经颊和舌下施用,粉剂、混悬剂、颗粒剂、片剂、丸剂、胶囊剂、凝胶盖和囊片剂可作为固体剂型接受。例如,可以通过将即时本发明的一种或多种化合物或药学上可接受的盐或其互变异构体与至少一种添加剂(例如淀粉或其他添加剂)混合来制备这些。合适的添加剂是蔗糖、乳糖、纤维素糖、甘露糖醇、麦芽糖醇、右旋糖酐、淀粉、琼脂、海藻酸盐、几丁质、壳聚糖、果胶、黄蓍胶、阿拉伯胶、明胶、胶原蛋白、酪蛋白、白蛋白、合成或半合成聚合物或甘油。任选地,口服剂型可以含有其他成分以帮助施用,例如非活性稀释剂,或润滑剂,例如硬脂酸镁,或防腐剂,例如对羟基苯甲酸酯或山梨酸,或抗氧化剂,例如抗坏血酸、生育酚或半胱氨酸,崩解剂、粘合剂、增稠剂、缓冲剂、甜味剂、调味剂或香料剂。片剂和丸剂可以用本领域已知的合适包衣材料进一步处理。
用于口服施用的液体剂型可以是可以含有非活性稀释剂例如水的药学上可接受的乳剂、糖浆剂、酏剂、混悬剂和溶液的形式。药物制剂和药物可以使用无菌液体(例如但不限于油、水、醇以及这些的组合)制备为液体混悬液或溶液。可加入药学上合适的表面活性剂、助悬剂、乳化剂以用于口服或肠胃外施用。
如上所述,混悬液可包含油。此类油包括但不限于花生油、芝麻油、棉籽油、玉米油和橄榄油。混悬液制剂还可含有脂肪酸酯,例如油酸乙酯、肉豆蔻酸异丙酯、脂肪酸甘油酯和乙酰化脂肪酸甘油酯。混悬液制剂可包含醇,例如但不限于乙醇、异丙醇、十六醇、甘油和丙二醇。醚,例如但不限于聚(乙二醇)、石油烃例如矿物油和凡士林;并且水也可以用于混悬液制剂中。
可注射剂型一般包括可使用合适的分散剂或润湿剂和助悬剂制备的水混悬液或油混悬液。可注射形式可以是溶液相或混悬液的形式,其用溶剂或稀释剂制备。可接受的溶剂或媒介物包括无菌水、林格氏溶液(Ringer's solution)或等渗盐水溶液。替选地,无菌油可用作溶剂或助悬剂。通常,油或脂肪酸是非挥发性的,包括天然油或合成油、脂肪酸、单甘油酯、二甘油酯或三甘油酯。
对于注射,药物制剂和/或药物可以是适合于用如上所述的适当溶液复溶的粉末。这些的实例包括但不限于冷冻干燥、旋转干燥或喷雾干燥的粉末、无定形粉末、颗粒、沉淀物或微粒。对于注射,制剂可任选地含有稳定剂、pH调节剂、表面活性剂、生物利用度调节剂及这些的组合。
本发明的化合物可通过经过鼻或口吸入施用至肺。适用于吸入的药物制剂包括含有任何适当溶剂和任选其他化合物(例如但不限于稳定剂、抗微生物剂、抗氧化剂、pH调节剂、表面活性剂、生物利用度调节剂及这些的组合)的溶液、喷雾剂、干粉或气溶胶。载体和稳定剂因特定化合物的要求而异,但通常包括非离子表面活性剂(Tween、Pluronic或聚乙二醇)、无害蛋白质(如血清白蛋白、山梨糖醇酯、油酸、卵磷脂)、氨基酸(例如甘氨酸)、缓冲液、盐、糖或糖醇。水性和非水性(如,在氟碳推进剂中)气溶胶通常用于通过吸入递送本发明的化合物。
除了上述那些代表性剂型之外,药学上可接受的赋形剂和载体通常为本领域技术人员所知,因此包括在即时本发明中。此类赋形剂和载体描述于例如“RemingtonsPharmaceutical Sciences”Mack Pub.Co.,新泽西(1991),其通过引用并入本文。即时组合物还可包括例如胶束或脂质体或某些其他囊封形式。
具体剂量可根据对象的疾病情况、年龄、体重、一般健康状况、性别和饮食、剂量间隔、施用途径、排泄率和药物组合进行调整。上述任一种含有有效量的剂型都完全在常规实验的范围内,并因此也完全在即时本发明的范围内。
可以很容易地使用各种测定和模型系统来确定根据本发明的治疗的治疗效果。
对于指定疾患,与安慰剂治疗或其他合适的对照对象相比,测试对象将表现出由对象体内的病症导致的或与对象体内的病症相关的一种或多种症状的10%、20%、30%、50%或更大的减少、高达75–90%、或95%或更大的减少。
本文提供的实施例是为了说明本发明的优点,并进一步帮助本领域的普通技术人员制备或使用本发明的化合物或盐、药物组合物、衍生物、前药或其互变异构形式。本文的实施例也被提出,以更充分地说明本发明的优选方面。实施例绝不应被解释为限制本发明的范围,如所附权利要求所定义的。实施例可以包括或合并上述本发明的任何变型、方面或实施方式。上述变型、方面或实施方式还可以进一步各自包括或合并本发明的任何或所有其他变型、方面或实施方式的变型。
实施例
材料和仪器.所有溶剂和试剂,除非另有说明,否则均从商业来源购买,并在收到后未经进一步纯化就使用。在
合成RPS-085、[
三功能骨架(((S)-5-(3-(3-(1-((14S,17S)-14-(4-氨基丁基)-17-羧基-24-(4-碘代苯基)-12,15,23-三氧代-3,6,9-三氧杂-13,16,22-三氮杂二十四基)-1H-1,2,3-三唑-4-基)苯基)脲基)-1-羧基戊基)氨基甲酰基)-L-谷氨酸如Kelly等人(Eur J Nucl MedMol Imaging.2018;45:1841-51)所述合成。将该胺(13mg,10μmol,1eq)溶解于无水DMF(1mL;Sigma Aldrich,USA)中,并在室温(rt)下用N,N-二异丙基乙胺(18μL,100μmol,10eq)搅拌5分钟。
通过MeCOSar的NHS酯衍生物和Lys的N
将MeCOSar的N-琥珀酰亚胺酯(6.2mg,12μmol,1.2eq)于DMF(0.5mL)中的溶液滴加至反应物,并将所得混合物在室温下搅拌5小时。将粗混合物通过HPLC使用配备有Phenomenex
产物纯度通过分析型HPLC使用配备有Agilent ProStar 325双波长UV-Vis检测器的双泵Agilent ProStar HPLC(Agilent Technologies,USA)确认。在220nm和280nm下监测紫外吸收。在XSelect
相对于母化合物RPS-063,所得的RPS-085化合物对PSMA的亲和力降低了大约一个数量级。无金属RPS-085抑制了PSMA,其IC
在20分钟内在25℃下在10X PBS(pH 7.4)和0.5M NH
[
化合物的稳定性测试
在25℃下一式三份地测定重新配制的[
[
细胞培养、体外测定IC
PSMA-表达性人前列腺癌细胞系LNCaP获自美国菌种保藏中心(American TypeCulture Collection)。除非另有说明,否则细胞培养用品均获自Invitrogen(USA)。将LNCaP细胞维持在37℃/5% CO
根据前述方法(Kelly等人,Eur J Nucl Med Mol Imaging.2018;45:1841-51),在针对
对人血清白蛋白的亲和力通过如前所述的高效亲和色谱进行测定(Kelly等人,JNucl Med.2019;60:656-63)。简单地说,[
LNCaP异种移植小鼠模型和microPET/CT成像
所有动物研究均经威尔康奈尔医学机构动物护理和使用委员会(InstitutionalAnimal Care and Use Committee of Weill Cornell Medicine)批准,并按照关于实验室动物人道护理和使用的USPHS政策(USPHS Policy on Humane Care and Use ofLaboratory Animals)规定的指导方针进行。将小鼠在标准条件下圈养在批准设施中,光照/黑暗周期为12小时。在整个研究过程中,自由提供食物和水。雄性BALB/c无胸腺nu/nu小鼠购自Jackson Laboratory(USA)。接种前,LNCaP细胞以4x10
LNCaP异种移植肿瘤用[
当肿瘤尺寸在200-500mm
生物分布和剂量测定
当肿瘤尺寸达到大约200mm
表1.剂量学
[
/>
[
/>
用于剂量学计算的数据基于注射后4、24和96小时的每个时间点平均4至5只动物。首先得到的是血液、心脏、肺、肝、小肠、大肠、胃、脾、胰腺、肾、肌肉、骨骼、肿瘤和尾巴中每个器官的注射剂量百分比。在前96小时内使用幂函数对生物分布数据进行拟合。每个器官的幂函数用于以2小时区间对浓度进行插值,以更好地估计动力学。积分时间又延长了96小时,假设前96小时后每个器官的注射剂量百分比恒定,并且96小时至192小时之间浓度的唯一变化是由于放射性衰变导致的。然后使用梯形近似来获得两小时区间内的积分。区间积分被缩放到完整积分的值,以给出更好的估计。这些滞留时间用来使用有成人男性模型和无膀胱清除的OLINDA程序来估计人对象的吸收剂量。对身体其他部位的剂量没有在该计算中使用。
在生物分布研究之后对[
图5显示了携带LNCaP异种移植物的雄性Balb/C nu/nu小鼠中的[
表2.全身和器官特异性有效剂量(mrem/mCi)和吸收剂量
/>
靶向PSMA的
表3.治疗诊断性放射性核素对的衰变特性.
用于PSMA治疗诊断的正电子发射放射性核素
用于PSMA治疗诊断的β
为了充分利用Cu-64/Cu-67治疗诊断的潜力,需要对这种射电金属进行有效和稳定的螯合。与可以作为
治疗诊断性配体开发的挑战性方面是需要平衡成像的最佳药代动力学,例如快速组织分布和从血液中清除,具有用于疗法的最佳特征,例如进行性和持续性的肿瘤负荷与同时从正常组织中清除。该挑战在先前描述的低分子量
小分子配体设计的第二个挑战方面是无法精确和全面地预测结构变化对化合物药代动力学的全面影响。之前,我们和其他人已经证明,改变缀合PSMA结合基团、金属螯合部分和白蛋白结合基团的接头的长度影响肿瘤摄取和滞留以及肾脏清除和滞留两者。此外,在固定的接头结构上的不同白蛋白结合基团也深刻地影响从血液中清除。在这里,我们证明了在固定结构平台上金属螯合部分的变化也影响配体的药代动力学,即使当不预测螯合剂有助于PSMA结合或白蛋白结合时。最近对更紧凑的分子支架描述了这一发现。相对于含有DOTA的类似物相比,螯合剂看起来导致对PSMA的亲和力降低了10倍。此外,Cu
基于RPS-085与其先前报道的同源配体的结构相似性,对血清白蛋白的亲和力以及因此在血液中的活性低于预测。因此,我们没有观察到随时间推移的进展性肿瘤负荷。然而,[
尽管RPS-085作为放射性配体疗法的潜在配体的有前景特性,但可以通过延长血浆半衰期来获得进一步的收益。该方法最近被用于开发[
据报道在唾液腺和泪腺中摄取大量PSMA-靶向配体,并且由于β
虽然已经说明和描述了某些实施方式,但本领域技术人员在阅读上述说明书后,可以对如本文所述的本发明的化合物或其盐、药物组合物、衍生物、前药、代谢物、互变异构体或外消旋混合物进行变化、等价物的取代和其他类型的改变。上面描述的每个方面和实施方式也可以包括或与之并入就任何或所有其他方面和实施方式所公开的此类变化或方面。
本发明也不限于本文所述的特定方面,所述方面旨在作为本发明的单个方面的单个说明。这种本发明的许多修改和变化可以在不偏离其精神和范围的情况下进行,这对于本领域的技术人员来说是明显的。本发明范围内的功能等效方法,除了在本文中列举的那些之外,对于本领域技术人员来说,从上述描述将是明显的。此类修改和变化旨在落在所附权利要求的范围内。应理解,该本发明并不局限于特定的方法、试剂、化合物、组合物、标记化合物或生物系统,当然它们可以变化。还应理解,本文使用的术语仅用于描述特定方面的目的,而不是有意限制。因此,本说明书意在仅被视为示例性,其本发明的广度、范围和精神仅由所附权利要求书、其中的定义及其任何等效方案所表明。
本文说明性地描述的实施方式可以在没有在本文中未具体公开的任一个或多个要素、一个或多个限制的情况下适当地实施。因此,例如,术语“包含”、“包括”、“含有”等应被广泛而不受限制地理解。此外,本文所使用的术语和表达只是用作描述术语,而不是限制术语,并且在使用此类术语和表达时不打算排除所示和所述的特征或其部分的任何等效方案,但是承认在所要求保护的技术范围内可以进行各种修改。此外,短语“基本上由……组成”将被理解为包括那些具体列举的要素和那些对所要求保护的技术的基本和新特征没有实质性影响的附加要素。短语“由……组成”排除不指定的任何要素。
此外,当以马库什组描述本发明的特征或方面时,本领域技术人员将认识到,本发明也因此以马库什组的任何单个成员或成员子组来描述。落入通用公开内容的范围内的每个较窄的种和亚属分组也构成本发明的一部分。这包括带有从属中移除任何主题的条件或否定限制的本发明的通用描述,无论所删除的材料是否在本文中具体列举。
如本领域技术人员将理解,对于任何和所有目的,特别是在提供书面描述方面,本文公开的所有范围还涵盖任何和所有可能的子范围及其子范围的组合。任何列出的范围都可以很容易地识别为足够的描述,并使相同的范围被分解为至少相等的二分之一、三分之一、四分之一、五分之一、十分之一等。作为非限制性实例,本文讨论的每个范围都可以很容易地分解为下三分之一、中三分之一和上三分之一等。如本领域技术人员也将理解,例如“至多”、“至少”、“大于”、“小于”等的所有语言都包括所列举的数字,并且是指随后可分解为如上所讨论的子范围的范围。最终,如本领域技术人员所理解,范围包括每个单独的成员。
本说明书中提到的所有出版物、专利申请、已发布的专利和其他文件(例如,期刊、文章和/或教科书)在此通过引用并入本文,如同每个单独的出版物、专利申请、已发布的专利或其他文件都被具体地且单独地表示通过引用整体并入一样。就其与本发明的定义相矛盾而言,排除通过引用并入的文本中所包含的定义。
本发明可以包括但不限于下列字母段落中所述的特征和特征组合,应理解,以下段落不应被解释为限制所附权利要求的范围或强制要求所有此类特征必须包含在此类权利要求中:
A.一种化合物,包含:
肿瘤靶向结构域,其包含能够识别肿瘤细胞表面上的分子靶标或与肿瘤细胞表面上的分子靶标相互作用的部分;
血液-蛋白结合结构域;和
含sarcophagine的结构域;其中,肿瘤靶向结构域的部分在血液-蛋白结合结构域的远端并且在空间上不受血液-蛋白结合结构域的阻碍。
B.如段落A所述的化合物,其中,肿瘤靶向结构域结合至选自以下中的一者或多者的肿瘤相关分子靶标:肿瘤特异性细胞表面蛋白、前列腺特异性膜抗原(PSMA)、生长激素抑制素肽受体-2(SSTR2)、alphavbeta3(αvβ3)、αvβ6、胃泌素释放肽受体、seprase、成纤维细胞激活蛋白α(FAP-α)、肠促胰岛素受体、葡萄糖依赖性促胰岛素多肽受体、VIP-1、NPY、叶酸受体、LHRH、神经元转运体(例如去甲肾上腺素转运体(NET))、EGFR、HER-2、VGFR、MUC-1、CEA、MUC-4、ED2、TF-抗原、内皮特异性标记、神经肽Y、uPAR、TAG-72、密封蛋白、CCK类似物、VIP、铃蟾肽、VEGFR、肿瘤特异性细胞表面蛋白、GLP-1、CXCR4、Hepsin、TMPRSS2、caspace、cMET或过表达肽受体。
C.如段落A或段落B所述的化合物,其中,肿瘤靶向结构域包含经修饰抗体、经修饰抗体片段、经修饰结合肽、前列腺特异性膜抗原(“PSMA”)结合肽、生长激素抑制素受体激动剂、铃蟾肽受体激动剂、seprase结合化合物、或其任一种或多种的结合片段。
D.如段落A-C中任一项所述的化合物,其中,肿瘤靶向结构域包含贝利单抗、莫格利珠单抗、博纳吐单抗、替伊莫单抗、奥妥珠单抗、奥法木单抗、利妥昔单抗、奥英妥珠单抗、帕西妥莫单抗、维布妥昔单抗、达雷木单抗、伊匹单抗、西妥昔单抗、耐昔妥珠单抗、帕尼单抗、地努妥昔单抗、帕妥珠单抗、曲妥珠单抗、恩美曲妥珠单抗、司妥昔单抗、西米普利单抗、纳武单抗、派姆单抗、奥拉妥单抗、阿特珠单抗、阿维单抗、德瓦鲁单抗、喷地肽卡罗单抗、艾洛珠单抗、地诺单抗、Ziv-阿柏西普、贝伐珠单抗、雷莫芦单抗、托西莫单抗、奥加米星吉妥珠单抗、阿仑单抗、西妥木单抗、吉妥昔单抗、尼妥珠单抗、卡妥索单抗或埃达珠单抗。
E.如段落A-C中任一项所述的化合物,其中,肿瘤靶向结构域包含以下的抗原结合片段:贝利单抗、莫格利珠单抗、博纳吐单抗、替伊莫单抗、奥妥珠单抗、奥法木单抗、利妥昔单抗、奥英妥珠单抗、帕西妥莫单抗、维布妥昔单抗、达雷木单抗、伊匹单抗、西妥昔单抗、耐昔妥珠单抗、帕尼单抗、地努妥昔单抗、帕妥珠单抗、曲妥珠单抗、恩美曲妥珠单抗、司妥昔单抗、西米普利单抗、纳武单抗、派姆单抗、奥拉妥单抗、阿特珠单抗、阿维单抗、德瓦鲁单抗、喷地肽卡罗单抗、艾洛珠单抗、地诺单抗、Ziv-阿柏西普、贝伐珠单抗、雷莫芦单抗、托西莫单抗、奥加米星吉妥珠单抗、阿仑单抗、西妥木单抗、吉妥昔单抗、尼妥珠单抗、卡妥索单抗或埃达珠单抗。
F.如段落A-E中任一项所述的化合物,其中,化合物是式I至V中任一者或其药学上可接受的盐和/或溶剂合物:
TTD-L
其中
TTD是肿瘤靶向结构域;
BBD是血液-蛋白结合结构域;
Sarc是含sarcophagine的结构域;
X
L
L
p在每次出现时独立为0、1、2、3、4或5;和
q在每次出现时独立为1或2。
G.如段落A-F中任一项所述的化合物,其中,肿瘤靶向结构域是
其中/>
W
r在每次出现时独立为1或2;
s在每次出现时独立为1或2;
P
o、o’和o”各自独立为0或1。
H.如段落G所述的化合物,其中,P
I.如段落G或段落H所述的化合物,其中,P
J.如段落A-I中任一项所述的化合物,其中,血液-蛋白结合结构域是
其中
Y
X
t在每次出现时独立为0、1或2;
u在每次出现时独立为0或1;
v在每次出现时独立为0或1;和
w在每次出现时独立为0、1、2、3或4,任选地其中u和v不能为相同的值。
K.如段落A-I中任一项所述的化合物,其中,血液-蛋白结合结构域包含肉豆蔻酸、经取代或未取代的吲哚-2-羧酸、经取代或未取代的硫代酰胺、经取代或未取代的4-氧代-4-(5,6,7,8-四氢萘-2-基)丁酸、经取代或未取代的萘酰基磺酰胺、经取代或未取代的二苯基环己醇磷酸酯、经取代或未取代的4-碘代苯基烷酸、经取代或未取代的3-(4-碘代苯基)丙酸、经取代或未取代的2-(4-碘代苯基)乙酸或经取代或未取代的4-(4-碘代苯基)丁酸。
L.如段落A-I中任一项所述的化合物,其中,血液-蛋白结合结构域是
M.如段落A-L中任一项所述的化合物,其中,含sarcophagine的结构域是
其中
R
R
L
R
N.如段落M所述的化合物,其中,R
O.如段落A-N中任一项所述的化合物,其中,含sarcophagine的结构域螯合
P.一种药物组合物,包含如段落A-O中任一项所述的化合物和药学上可接受的载体。
Q.一种药物组合物,所述组合物包含:
有效量的段落O的化合物用于使以下中的一者或多者成像和/或检测以下中的一者或多者:非小细胞肺癌、小细胞肺癌、膀胱癌、结肠癌、胆囊癌、胰腺癌、食道癌、黑素瘤、肝癌、原发性胃腺癌、原发性结直肠腺癌、肾细胞癌、前列腺癌、神经内分泌瘤、垂体瘤、血管活性肠肽分泌肿瘤、神经胶质瘤、乳腺癌、肾上腺皮质癌、宫颈癌、外阴癌、子宫内膜癌、原发性卵巢癌、转移性卵巢癌和转移癌;和
药学上可接受的载体。
R.如段落Q中任一项所述的药物组合物,其中,药物组合物配制用于静脉内施用,任选地包含无菌水、林格氏溶液或等渗盐水溶液。
S.如段落Q或段落R所述的药物组合物,其中,化合物的有效量是约0.01μg至约10mg化合物/g药物组合物。
T.如段落Q-S中任一项所述的药物组合物,其中,药物组合物以可注射剂型提供。
U.一种方法,包括:
向对象施用有效量的如段落O所述的化合物用于使癌症成像和/或检测癌症;和
在施用之后,检测正电子发射、来自正电子发射和湮灭的伽马射线以及由正电子发射引起的切伦科夫辐射中的一者或多者。
V.如段落U所述的方法,其中,癌症包括以下中的一者或多者:非小细胞肺癌、小细胞肺癌、膀胱癌、结肠癌、胆囊癌、胰腺癌、食道癌、黑素瘤、肝癌、原发性胃腺癌、原发性结直肠腺癌、肾细胞癌、前列腺癌、神经内分泌瘤、垂体瘤、血管活性肠肽分泌肿瘤、神经胶质瘤、乳腺癌、肾上腺皮质癌、宫颈癌、外阴癌、子宫内膜癌、原发性卵巢癌、转移性卵巢癌和转移癌。
W.如段落U或段落V所述的方法,其中,对象疑似患有过表达前列腺特异性膜抗原(“PSMA”)的哺乳动物组织。
X.如段落U-W中任一项所述的方法,其中,哺乳动物组织包括以下中的一者或多者:非小细胞肺癌、小细胞肺癌、膀胱癌、结肠癌、胆囊癌、胰腺癌、食道癌、黑素瘤、肝癌、原发性胃腺癌、原发性结直肠腺癌、肾细胞癌、前列腺癌、神经内分泌瘤、垂体瘤、血管活性肠肽分泌肿瘤、神经胶质瘤、乳腺癌、肾上腺皮质癌、宫颈癌、外阴癌、子宫内膜癌、原发性卵巢癌、转移性卵巢癌和转移癌。
Y.如段落X所述的方法,其中,施用化合物包括肠胃外施用或静脉内施用。
Z.一种药物组合物,包含:
有效量的如段落O所述的化合物用于治疗以下中的一者或多者:非小细胞肺癌、小细胞肺癌、膀胱癌、结肠癌、胆囊癌、胰腺癌、食道癌、黑素瘤、肝癌、原发性胃腺癌、原发性结直肠腺癌、肾细胞癌、前列腺癌、神经内分泌瘤、垂体瘤、血管活性肠肽分泌肿瘤、神经胶质瘤、乳腺癌、肾上腺皮质癌、宫颈癌、外阴癌、子宫内膜癌、原发性卵巢癌、转移性卵巢癌和转移癌;和
药学上可接受的载体。
AA.如段落Z所述的药物组合物,其中,药物组合物配制用于静脉内施用,任选地包含无菌水、林格氏溶液或等渗盐水溶液。
AB.如段落Z或段落AA所述的药物组合物,其中,化合物的有效量是约0.01μg至约10mg化合物/g药物组合物。
AC.如段落Z-AB中任一项所述的药物组合物,其中,药物组合物以可注射剂型提供。
AD.如段落Z-AC中任一项所述的药物组合物,其中,用于治疗非小细胞肺癌、小细胞肺癌、膀胱癌、结肠癌、胆囊癌、胰腺癌、食道癌、黑素瘤、肝癌、原发性胃腺癌、原发性结直肠腺癌、肾细胞癌、前列腺癌、神经内分泌瘤、垂体瘤、血管活性肠肽分泌肿瘤、神经胶质瘤、乳腺癌、肾上腺皮质癌、宫颈癌、外阴癌、子宫内膜癌、原发性卵巢癌、转移性卵巢癌和转移癌中的一者或多者的化合物的有效量还是用于使非小细胞肺癌、小细胞肺癌、膀胱癌、结肠癌、胆囊癌、胰腺癌、食道癌、黑素瘤、肝癌、原发性胃腺癌、原发性结直肠腺癌、肾细胞癌、前列腺癌、神经内分泌瘤、垂体瘤、血管活性肠肽分泌肿瘤、神经胶质瘤、乳腺癌、肾上腺皮质癌、宫颈癌、外阴癌、子宫内膜癌、原发性卵巢癌、转移性卵巢癌和转移癌中的一者或多者成像和/或检测的化合物的有效量。
AE.一种方法,包括:
向对象施用有效量的如段落O所述的化合物用于治疗癌症。
AF.如段落AE所述的方法,其中,癌症包括以下中的一者或多者:非小细胞肺癌、小细胞肺癌、膀胱癌、结肠癌、胆囊癌、胰腺癌、食道癌、黑素瘤、肝癌、原发性胃腺癌、原发性结直肠腺癌、肾细胞癌、前列腺癌、神经内分泌瘤、垂体瘤、血管活性肠肽分泌肿瘤、神经胶质瘤、乳腺癌、肾上腺皮质癌、宫颈癌、外阴癌、子宫内膜癌、原发性卵巢癌、转移性卵巢癌和转移癌。
AG.如段落AE或段落AF所述的方法,其中,施用化合物包括肠胃外施用。
AH.如段落AE-AG中任一项所述的方法,其中,施用化合物包括静脉内施用。
AI.如段落AE-AH中任一项所述的方法,其中,用于治疗癌症的化合物的有效量是约0.1μg至约50μg/kg对象质量。
AJ.如段落AE-AI中任一项所述的方法,其中,化合物的有效量也是用于使癌症成像和/或检测癌症的化合物的有效量。
其他实施方式列出在以下权利要求中,以及这些权利要求有权享有的等同方案的全部范围。
