胺碘酮药物组合物、注射液及其制备方法及含其的注射器
文献发布时间:2023-06-19 19:30:30
技术领域
本发明涉及一种胺碘酮药物组合物、注射液及其制备方法及含其的注射器。
背景技术
盐酸胺碘酮(Amiodarone Hydrochloride)又名乙胺碘呋酮,属于VaughanWillians抗心律失常药分类法中的第Ⅲ类抗心律失常药物。盐酸胺碘酮的分子式为C
胺碘酮延长心肌细胞3相动作电位,但不影响动作电位的高度和下降速率(Vaughan Williams分类Ⅲ类);单纯延长心肌细胞3相动作电位是由于钾离子外流减少所致,钠离子和钙离子外流不变。
目前,盐酸胺碘酮市售剂型包括片剂、胶囊剂、注射剂。静脉注射盐酸胺碘酮有三个特点:负性肌力作用、降低外周阻力、无Ⅲ类抗心律失常药物作用。注射剂由于具有药效迅速、作用可靠的特点,盐酸胺碘酮注射剂成为其主要剂型。
盐酸胺碘酮为高度脂溶性药物,几乎不溶于水,现有的注射剂产品需要加入助溶剂,国内外生产的盐酸胺碘酮注射液应用聚山梨酯-80为助溶剂,苯甲醇为抑菌剂。高浓度的聚山梨酯-80和苯甲醇易引起爆发性肝炎、低血压、静脉炎及新生儿致命性窒息综合征等毒副作用。苯甲醇可导致婴儿和3岁(含3岁)的儿童发生毒性反应和过敏反应。
胺碘酮目前作为在安瓿中的50mg/mL胺碘酮盐酸盐浓缩液上市和销售。该制剂在施用前用5%葡萄糖注射液稀释至0.5至2mg/mL的浓度。由于胺碘酮的注射形式通常在紧急状况下(例如心跳骤停)使用,因此提供以所需剂量浓度预混的即用型注射液是重要的。制备稀释液所需的额外时间可能延误治疗,并可能对患者产生严重和不利的结果。
β-环糊精包合技术在药学中研究及实际应用较为普遍。β-环糊精在药学中具有增加药物稳定性,提高难溶药物溶解度,掩盖不良气味,减少刺激等一系列优点。磺丁基醚-β-环糊精(SBE-β-CD)作为β-环糊精的衍生物,具有水溶性好、肾毒性低、溶血作用小及局部刺激性轻微等特点,在医药领域已受到广泛重视。
环糊精及其衍生物被广泛用在液体制剂中以提高疏水性化合物的水溶性。环糊精是源自于淀粉的环状糖类。未改性的环糊精的差异在于圆柱状结构中连在一起的吡喃葡萄糖单元的数量。母体环糊精含有6、7或8个吡喃葡萄糖单元,并分别被称为α-、β-和γ-环糊精。每个环糊精亚单元在2和3-位处具有仲羟基并在6-位处具有伯羟基。
到目前为止制备的大量取代环糊精中,有两种被包含在商品化注射药物制剂中;即2-羟丙基衍生物(“HP-β-CD”或“HPCD”),其是由Janssen公司等在商业上开发的中性分子,以及磺烷基醚衍生物(“SAE-B-CD”或“SAE-CD”),由CyDex公司等开发。SAE-CD是一类带负电荷的环糊精,其差异在于烷基连接物的性质、盐形式、取代度和起始的母体环糊精。负电荷的存在允许在溶液中与药物发生离子相互作用以及复合反应。磺丁基-β-环糊精是一种赋形剂,主要用于含氮类药物中。对于含氮类药物具有特殊的亲和力和包合性。分子:C
目前,本领域为了提高胺碘酮注射剂的溶解度、稳定性和安全性,选择用环糊精及其衍生物替换助溶剂,例如中国专利文献(CN103079559A)公开了包含胺碘酮及其盐的制剂及其制造和使用方法,该专利虽然使用了环糊精提高了胺碘酮的溶解度和稳定性,但是其包合速度和药物溶出速度低。
发明内容
本发明为了解决现有技术中使用环糊精类化合物包合胺碘酮存在的包合速度和药物溶出速度低的问题,提供了一种胺碘酮药物组合物、注射液及其制备方法及含其的注射器,该药物组合物的包合速度快,由该药物组合物制备得到的胺碘酮注射剂中药物溶出速度高。
本发明主要采用以下技术方案解决上述技术问题:
本发明提供了一种胺碘酮药物组合物,其包含药物活性成分、环糊精类化合物、助溶剂和水;
所述药物活性成分为胺碘酮和/或在药物上可接受的胺碘酮盐;
所述环糊精类化合物为环糊精和/或环糊精衍生物。
本发明中,所述胺碘酮药物组合物中所述药物活性成分的浓度较佳地为2~60g/L,更佳地为20~60g/L,进一步更佳地为30~60g/L,例如为50g/L。
本发明中,所述胺碘酮药物组合物中所述环糊精类化合物的浓度较佳地为1~650g/L,更佳地为200~500g/L,进一步更佳地为300~500g/L。
本发明中,所述胺碘酮药物组合物中所述助溶剂的浓度较佳地为5~50g/L,例如为10g/L。本发明所述胺碘酮药物组合物中的助溶剂添加量少,能够降低由助溶剂引起的各种毒性反应和过敏反应的风险,该药物组合物使用的安全性高。
本发明中,所述药物活性成分和所述环糊精类化合物的质量比较佳地为1:(1~10)。
本发明中,所述环糊精类化合物和助溶剂的用量比较佳地为(0.02~200):1,例如为25:1、30:1或40:1。
本发明中,所述助溶剂较佳地为聚山梨酯、乙醇和聚乙二醇中的一种或多种的混合物。
其中,所述聚山梨酯较佳地为聚山梨酯-80、聚山梨酯-20和聚山梨酯-40中的一种或多种的混合物。
其中,所述聚乙二醇较佳地为聚乙二醇400。
本发明中,所述在药物上可接受的胺碘酮盐较佳地为盐酸胺碘酮。
本发明中,所述环糊精类化合物较佳地为α-环糊精、β-环糊精和γ-环糊精中的一种或多种,例如为磺丁基醚-β-环糊精。
本发明中,所述胺碘酮药物组合物中一般还包括pH值调节剂,所述pH值调节剂可为本领域常规,较佳地为醋酸、盐酸、磷酸、硫酸和枸橼酸中的一种或多种的混合物。
本发明中,所述胺碘酮药物组合物的pH值较佳地为3.0~6.0,更佳地为4.0~6.0,进一步更佳地为4.5~6.0。
本发明中,所述水为本领域已知的注射用水,所述注射用水是指符合中国药典注射用水项下规定的水,其为蒸馏水或去离子水经蒸馏所得的水。
本发明较佳的实施例中,所述胺碘酮药物组合物以1L计,包括2~60g/L的药物活性成分、1~650g/L的环糊精类化合物、5~50g/L的助溶剂和注射用水;所述药物活性成分为胺碘酮和/或在药物上可接受的胺碘酮盐;所述环糊精类化合物为环糊精和/或环糊精衍生物。
本发明一较佳实施例中,所述胺碘酮药物组合物以1L计,包括20g/L的盐酸胺碘酮,5g/L的聚山梨酯80和200g/L的磺丁基醚-β-环糊精钠。
本发明一较佳实施例中,所述胺碘酮药物组合物以1L计,包括30g/L的盐酸胺碘酮,10g/L的聚山梨酯40和300g/L的磺丁基醚-β-环糊精钠。
本发明一较佳实施例中,所述胺碘酮药物组合物以1L计,包括50g/L的盐酸胺碘酮,20g/L的聚乙二醇400和500g/L的磺丁基醚-β-环糊精钠。
本发明还提供了一种胺碘酮注射液,其特征在于,其包含上述胺碘酮药物组合物。
本发明还提供了一种胺碘酮注射液的制备方法,其包括以下步骤:将所述环糊精类化合物和所述助溶剂的混合物溶解于水后,再加入所述药物活性成分即可。
其中,所述溶解的温度较佳地为25~40℃。
其中,所述溶解的方法可为本领域常规,例如超声法或饱或溶液搅拌法。
本发明还提供了一种由上述胺碘酮注射液的制备方法制备得到的胺碘酮注射液。
本发明还提供了一种含上述胺碘酮注射液的注射器。
本发明中,所述注射器可为本领域常规,较佳地为西林瓶、玻璃安瓿和预填充注射器。
其中,所述预填充注射器的材质可为本领域常规,较佳地为玻璃、不含酞酸二乙酯的聚氯乙烯、热塑性聚氨酯、聚烯烃热塑弹性体、聚氨酯、聚乙烯或聚丙烯。
本发明中,所述胺碘酮注射剂的制备方法可为本领域常规,较佳地包括以下步骤:将所述胺碘酮注射液经过滤后灌装,罐装前后通入惰性气体。
其中,本领域技术人员已知所述过滤的装置一般包含滤芯和/或滤膜。
其中,所述滤芯和/或滤膜的滤孔直径较佳地为0.2~0.45μm,例如0.2μm。
其中,所述过滤的次数较佳地为1~3,例如2次。
其中,所述惰性气体较佳地为氮气。
本发明中,所述环糊精类化合物可以被形象地描述为中空的截锥体,具有亲水性外表面和疏水性内部空腔。在水性溶液中,这些疏水性空腔为疏水性有机化合物提供了庇护,所述疏水有机化合物可以将它们结构的全部或一部分刚好放入这些空腔。这种被称为包合复合的过程可以引起复合的药物的表观水溶性和稳定性增加,复合物被疏水相互作用稳定化,并且不涉及任何共价键的形成。通过对母体环糊精的化学改性(通常在羟基组成部分处)可以产生有时具有提高安全性并同时保持或提高环糊精复合能力的取代环糊精。
本发明的积极进步效果在于:
通过将环糊精类化合物和助溶剂配合使用,能够提高胺碘酮药物活性成分的溶解度,制备得到的胺碘酮注射剂化学和物理性质稳定,在光照和高温下pH和浓度均没有发生明显改变,可见异物符合规定;本发明胺碘酮的包合速度和释放速度快,其包合速度快有利于提高注射剂的质量,其释放速度快有利于快速发挥治疗作用。
通过本发明的优选方案,降低助溶剂的使用量,能够有效提高胺碘酮注射液的安全性。
附图说明
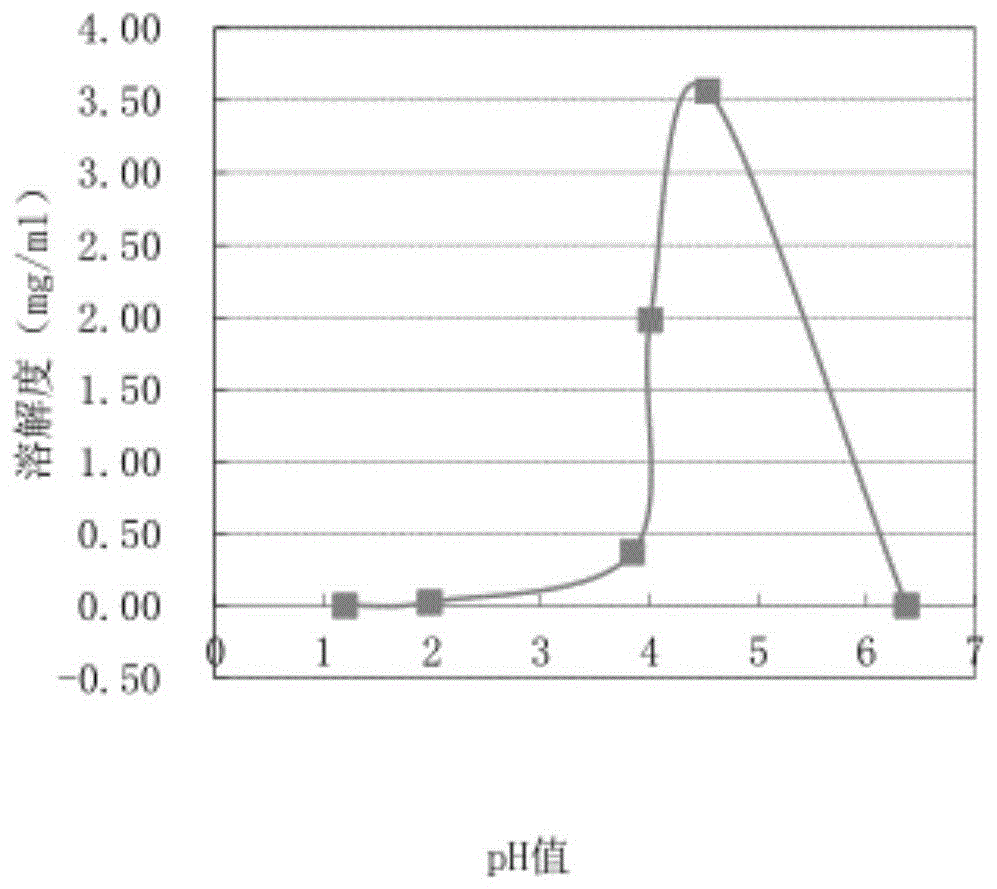
图1为实施例1~4和对比例1~2中使用的盐酸胺碘酮的pH溶解度曲线。
具体实施方式
下面通过实施例的方式进一步说明本发明,但并不因此将本发明限制在所述的实施例范围之中。下列实施例中未注明具体条件的实验方法,按照常规方法和条件,或按照商品说明书选择。
本发明的实施例1~4和对比例1~2中使用同一批市购的盐酸胺碘酮,其pH溶解度曲线如图1所示。
实施例1
在配制量70L~80L的注射用水中,加入20kg磺丁基醚-β-环糊精钠和0.5kg聚山梨酯80,搅拌溶解后用醋酸调节pH值至4.5-6.0,得混合溶液。在上述混合溶液中加入3mol的盐酸胺碘酮(约2kg),得饱和溶液,搅拌至饱和溶液澄明即为包合完全。然后用注射用水将药液稀释至100L,搅拌均匀。配制完毕药液经两道0.2μm滤芯过滤后,经灌装入西林瓶中,在灌装前后通入适量氮气,压塞、轧盖、灯检合格后得成品。
实施例2
在配制量70L~80L的注射用水中,加入30kg磺丁基醚-β-环糊精钠和1kg聚山梨酯40,搅拌溶解后用醋酸调节pH值至3.5-5.0,得混合溶液。在上述混合溶液中加入4mol的盐酸胺碘酮(约3kg),得饱和溶液,搅拌至饱和溶液澄明即为包合完全。然后用注射用水将药液稀释至100L,搅拌均匀。配制完毕药液经两道0.2μm滤芯过滤后,经灌装入玻璃安瓿中,在灌装前后通入适量氮气,压塞、轧盖、灯检合格后得成品。
实施例3
在配制量60L~70L的注射用水中,加入50kg磺丁基醚-β-环糊精钠和2kg聚乙二醇400,搅拌溶解后用盐酸调节pH值至4.0-5.5,得混合溶液。在上述混合溶液中加入7mol的盐酸胺碘酮(约5kg),得饱和溶液,搅拌至饱和溶液澄明即为包合完全。然后用注射用水将药液稀释至100L,搅拌均匀。配制完毕药液经两道0.2μm滤芯过滤后,经灌装入预填充注射器,在灌装前后通入适量氮气,压塞、轧盖、灯检合格后得成品。
实施例4
在配制量70L~80L的注射用水中,加入5kg磺丁基醚-β-环糊精钠和5kg乙醇,搅拌溶解后用盐酸调节pH值至4.5-5.5,得混合溶液。在上述混合溶液中加入7mol的盐酸胺碘酮(约5kg),得饱和溶液,搅拌至饱和溶液澄明即为包合完全。然后用注射用水将药液稀释至100L,搅拌均匀。配制完毕药液经两道0.2μm滤芯过滤后,经灌装入玻璃安瓿中,在灌装前后通入适量氮气,压塞、轧盖、灯检合格后得成品。
对比例1
在配制量80L~90L的注射用水中,加入10kg聚山梨酯80、2kg苯甲醇,搅拌溶解后用醋酸调节pH值至4.0-5.5,得混合溶液。在上述混合溶液中加入7mol的盐酸胺碘酮(约5kg),得饱和溶液,搅拌至饱和溶液澄明即为包合完全。然后用注射用水将药液稀释至配制总量,搅拌均匀。配制完毕药液经两道0.2μm滤芯过滤后,经灌装入玻璃安瓿中,在灌装前后通入适量氮气,压塞、轧盖、灯检合格后得成品。
对比例2
在配制量80L~90L的注射用水中,加入50kg磺丁基醚-β-环糊精钠,搅拌溶解后用盐酸调节pH值至4.0-5.5,得混合溶液。在上述混合溶液中加入7mol的盐酸胺碘酮(约5kg),得饱和溶液,搅拌至饱和溶液澄明即为包合完全。然后用注射用水将药液稀释至100L,搅拌均匀。配制完毕药液经两道0.2μm滤芯过滤后,经灌装入玻璃安瓿中,在灌装前后通入适量氮气,压塞、轧盖、灯检合格后得成品。
效果实施例1
对实施例1~4和对比例1和2在40℃、60℃和5000Lx条件下,同时进行高温和光照试验,分别在第5、10和30天测定注射液中胺碘酮的浓度,胺碘酮的浓度采用高效液相色谱(色谱柱:Symmetry C18,4.6*250mm,5μm)测定,结果列于表1。
表1高温和光照实验结果
/>
对比例1的胺碘酮浓度和pH在60℃放置期间发生了明显的变化,说明磺丁基醚-β-环糊精钠包合的盐酸胺碘酮能提高盐酸胺碘酮的稳定性。
效果实施例2
对实施例1~4和对比例1和2进行40℃±2℃/60% RH±5% RH的稳定性6个月考察,考察结果见表2。表中不溶性微粒含量的测试依据2020版《中国药典》第0903节不溶性微粒检查法的相关规定。不溶性微粒含量是指每10ml胺碘酮注射液中10μm及以上或者25μm及以上的不溶性微粒的粒数。
表2稳定性试验结果
/>
/>
在此放置条件,实施例1~4的胺碘酮浓度最大变化量为1.4mg/ml,而对比例为2.05mg/ml;实施例1~4中10μm及以上不溶性微粒6个月后最多仅含7,而对比例为15。说明本发明仅添加少量的助溶剂,与现有技术中添加大量的助溶剂相比,胺碘酮浓度稳定性更好,10μm及以上不溶性微粒更少,25μm及以上不溶性微粒与现有技术相当。
效果实施例3
对实施例1~4和对比例2进行包合时间和完全释放时间测试。包合时间的测定从加入胺碘酮后开始计时,直至饱和溶液澄明停止计时。此处溶液澄明的判断方法依据2020版《中国药典》第0902节澄清度检查法的相关规定。
完全释放时间按如下方法测试:准确称取实施例1~4和对比例2中100mg胺碘酮当量的注射液,分别加入装有500mL的pH值为6.8的缓冲水溶液的锥形瓶中,置于37±2℃的恒温振荡器中进行释放试验,设定转速为300r/min,分别每5min取样检测其吸光值。根据胺碘酮标准曲线计算胺碘酮包合物随时间变化的释放量,胺碘酮的释放量不随时间变化时停止计时。结果如表3所示:
表3实施例1~4和对比例2的各项参数
由包合时间和完全释放时间可知,实施例1~4加入了助溶剂,其注射液有更快的包合速度,释放速度也更快更完全。这是由于助溶剂能够增大胺碘酮在水中游离分子的溶解量,分子状态的胺碘酮更容易被环糊精类化合物包合,因此助溶剂的加入能促进胺碘酮包合在环糊精中,提高其包合速度。此外,助溶剂也能够加快包合物中胺碘酮的释放,胺碘酮用于抗心律失常,在患者心律失常期间可以迅速起效,有效的控制病情。因此加入助溶剂,更有利于胺碘酮包合物注射液的质量和疗效。
效果实施例4
(1)样品配置
阴性对照品:直接使用5%葡萄糖注射液。
实施例供试品:使用5%葡萄糖注射液将浓度为50mg/mL的实施例1~4溶液稀释成2mg/mL,用于实施例组动物给药。
对比例供试品:使用5%葡萄糖注射液将浓度为50mg/mL的对比例1和2溶液稀释成2mg/mL,用于对比例组动物给药。
(2)给药及观察
根据分组前(D-1)测定的动物体重,选取检疫合格、注射部位皮肤无明显异常、体重相近的12只动物用于试验。使用Provantis 9.4.3系统动物管理模块将动物随机分为2组,每组6只,分别为实施例组和对比例组。采用同体自身对照模型,给药剂量、浓度和容量见下表4:
表4
a:前4只/组用于末次给药后3天(D10)的解剖,后2只/组用于末次给药后14天(D21)的解剖。
b:体重和体表面积折算按照FDA推荐的折算系数12计算。
试验使用12只雄性新西兰兔,分成2组,6只/组,采用同体自身对照法进行给药,右耳静脉输注给予实施例或对比例样品,给药浓度均为2mg/mL,给药剂量均为20mg/kg,左耳静脉输注给予5%葡萄糖注射液。给药容量均为10mL/kg,输注速度为1.0mL/kg/min,每天给药l次,重复给药6天。试验期间,每天上午和下午各进行一次一般临床观察,观察内容包括但不限于死亡情况、精神状态、行为活动、呼吸、粪便以及饮食和饮水情况。给药前(D-1)、给药期间(D1~D7)每天给药前及给药后各局部观察1次,末次药后(D8~D21)每天局部观察1次。其中末次药后3天(D10)给药局部观察时间为药后72h(±2h)。局部观察注射部位是否有可见可触摸到的病变,包括但不限于肿胀、发热、水肿、充血、红斑、溃疡等。末次药后3天(D9)对前4只/组动物实施安乐死,末次药后14天(D20)对剩余动物实施安乐死,对注射局部组织取材并进行组织病理学检查。
(3)结果
实施例、对比例和阴性对照品在D1配制完成后,对实施例和对比例溶液进行浓度分析,配制后实施例和对比例理论浓度均为2mg/mL,准确度分别为106.07%和104.08%,在理论浓度的90~110%之间,阴性对照品中未检测到供试品,结果符合方案要求。试验期间,所有动物均未见死亡或濒死。试验期间,所有动物给药局部观察,实施例和对比例D2-D19陆续可见右耳变色(紫色)(发生率2/6、6/6),在D6-D12陆续可见右耳轻度破溃(发生率0/6、2/6),在D7-D19陆续可见右耳结痂(发生率0/6、1/6),在D6-D20陆续可见右耳坏死(发生率0/6、5/6),在D8-D9可见皮肤触摸较硬(发生率0/6、2/6)。5%葡萄糖注射液给药局部观察未见异常。末次药后3天(D9)安乐死动物大体观察可见,实施例1~4给药部位肿胀变硬、部分出现变硬、创口;对比例1和2给药部位均出现不同程度肿胀、变色(黑色)、变硬、结痂、创口。实施例1~4组织病理学表现为血管周围及皮下轻微炎症;对比例1组织病理学改变表现为静脉血栓、血管周围及皮下混合性炎症、皮下和/或血管周围出血、真皮和/或皮下组织和/或表皮坏死、表皮结痂。末次给药后14天(D20)安乐死动物,给药部位实施例1~4完全恢复,对比例1和2相关的病变仍可见部分炎症或皮下组织坏死。
本申请降低了助溶剂的浓度,配合着环糊精类化合物的使用,在保证了胺碘酮药物活性成分的溶解度高,包合速度快和溶出速率高的前提下,能够提高其安全性。
- 玻璃组合物、含该玻璃组合物的玻璃料浆,含该玻璃组合物的真空玻璃和电阻件及制备方法
- 一种含蜂胶提取物的治疗老年痴呆的药物组合物及其制备方法和用途
- 一种含亲水形式的阿哌沙班药物组合物及其制备方法
- 一种含蜂胶提取物的组合物及其制备方法和用途
- 一种含注射用水溶性维生素、脂溶性维生素注射液和中/长链脂肪乳注射液的药物组合物
- 一种含注射用水溶性维生素、脂溶性维生素注射液和中/长链脂肪乳注射液的药物组合物
