一种仿生膜包裹稀土掺杂无机纳米荧光探针及其制备方法和应用
文献发布时间:2024-04-18 20:01:55
技术领域
本发明属于纳米生物材料技术领域,涉及一种仿生膜包裹稀土掺杂无机纳米荧光探针及其制备方法和应用,具体涉及一种具有肿瘤靶向仿生膜包裹稀土掺杂无机纳米荧光探针及其制备方法和应用。
背景技术
癌症是全球范围内的重大公共卫生问题,灵敏高效的肿瘤诊断方式对于肿瘤发现与治疗具有重要意义。分子影像因其无创性、可视化等优点已经成为有效的诊断工具,例如荧光成像、PET成像、核磁共振成像(magnetic resonance imaging,MRI)、计算机断层扫描算法(computed tomography,CT)、光声成像(photoacoustic tomography,PAT)等。近红外二区成像(NIR-II,1000–1700nm)因其穿透深度大、自体荧光弱、背景干扰小等优点成为研究热点。稀土掺杂无机纳米材料具有较低的生物毒性、无背景荧光、抗光漂白性、较深的光穿透深度等特点,是一种具有前景的近红外二区生物荧光成像探针。
然而,当稀土掺杂无机纳米荧光探针应用于生物体内时,常常难以逃过免疫系统的吞噬与清除,从而降低其体内循环时间;同时传统的靶向肿瘤方式,是在纳米显影剂表面修饰具有靶向性的生物分子(如蛋白质、多肽或单克隆抗体),这些基于单一或几种靶点结合的方法难以实现多种肿瘤类型广泛适用。因此,制备一种简易低毒性的具有免疫逃逸及广泛靶向肿瘤能力的稀土掺杂无机纳米荧光探针,实现病灶精准诊断,在疾病的诊断中将具有重要实际的意义和临床价值。
发明内容
为了改善上述技术问题,本发明公开了一种仿生膜包裹稀土掺杂无机纳米荧光探针,所述纳米荧光探针包括水溶性的稀土掺杂无机纳米颗粒内核以及仿生膜壳层;
所述稀土掺杂无机纳米颗粒以化学式AREF
根据本发明,所述水溶性的稀土掺杂无机纳米颗粒可以采用配体氧化法、逐层沉积法、酸洗、配体交换等中的至少一种方法制备。示范性选用配体交换法。
根据本发明,所述配体交换法是采用两亲性配体对稀土掺杂无机纳米颗粒表面进行水溶性修饰,所述两亲性配体可以选择二硬脂酰磷脂酰乙醇胺(DSPE)、二硬脂酰基磷脂酰乙醇胺-聚乙二醇(DSPE-PEG)、二硬脂酰磷脂酰乙醇胺聚乙二醇羧基(DSPE-PEG-COOH)、二硬脂酰磷脂酰乙醇胺-聚乙二醇-氨基共聚物(DSPE-PEG-NH
根据本发明,所述稀土掺杂无机纳米颗粒与两亲性配体的质量比为1:(4~10),示例性地为1:4、1:5、1:6、1:7、1:8、1:9、1:10。
根据本发明,所述仿生膜为来自白细胞、红细胞、肿瘤细胞的细胞膜,其中肿瘤细胞包括原代肿瘤细胞、肿瘤细胞系、或工程化改造的肿瘤细胞等,可以选自乳腺癌、肝癌、食管癌、肺癌、胃癌等中的至少一种。示例性选自4T1小鼠乳腺癌肿瘤细胞。
根据本发明,所述内核的厚度为20~50nm,示例性为20nm、25nm、30nm、35nm、40nm、45nm或50nm。
根据本发明,所述壳层的厚度为3~10nm,优选8~10nm。
根据本发明,所述稀土掺杂无机纳米颗粒的制备方法可选为共沉淀法、热分解法、水热法或溶胶-凝胶法等制备纳米材料的方法,示例性为共沉淀法。
本发明还提供上述仿生膜包裹稀土掺杂无机纳米荧光探针的制备方法,其包括以下步骤:
(1)制备所述稀土掺杂无机纳米颗粒;
(2)对所述稀土掺杂无机纳米颗粒进行水溶性修饰;
(3)制备细胞膜囊泡;
(4)将步骤(2)制备的两亲性配体修饰的稀土掺杂无机纳米颗粒与步骤(3)中细胞膜囊泡混合,将得到的混合物通过聚碳酸酯膜,制备得到所述仿生膜包裹稀土掺杂无机纳米荧光探针。
根据本发明,步骤(1)中,所述稀土掺杂无机纳米颗粒的制备方法可选为共沉淀法、热分解法、水热法或溶胶-凝胶法等制备纳米材料的方法,示例性为共沉淀法。
根据本发明,步骤(1)中,所述稀土掺杂无机纳米颗粒通过共沉淀方法制备,具体包括:
(a)将稀土源在溶剂中混合,再加入碱金属源和氟源,经共沉淀反应,制备得到AREF
(b)将步骤(a)中AREF
根据本发明,步骤(a)中所述稀土源选自下述物质中的一种或多种:稀土离子的乙酸盐、稀土离子的氯化物和稀土离子的硝酸盐,优选为稀土离子的乙酸盐和稀土离子的氯化物,还优选为Yb、Er、Ce、Tm、Ho、Eu、Nd、Y和Lu的乙酸盐和/或氯化物,例如为Y的乙酸盐、Y的氯化物、Yb的乙酸盐、Yb的氯化物、Er的乙酸盐、Er的氯化物、Ce的乙酸盐、Ce的氯化物。
根据本发明,步骤(a)中,Yb离子、Er离子和Ce离子的摩尔比为(10~30):(0.5~4):(0.5~4),例如摩尔比为(15~20):(1~3):(0.5~4),示例性为20:2:4。
根据本发明,步骤(a)中,所述溶剂为油酸和十八烯中的至少一种。优选地,当所述溶剂为油酸和十八烯的混合溶剂时,所述油酸与十八烯的体积比例为6~12:8~20,示例性地为6:15。
根据本发明,步骤(a)中所述碱金属源选自含有碱金属的氢氧化物、含有碱金属的油酸盐、含有碱金属的乙酸盐、含有碱金属的氟化物和含有碱金属的氟氢化物中的一种或多种,优选为含有碱金属的的氢氧化物、含有碱金属的氟化物或含有碱金属的乙酸盐,示例性选自氢氧化钾、氢氧化钠、氟化钠、氟化钾、乙酸钠、乙酸钾中的至少一种。
根据本发明,所述氟源选自氟化铵、氟化钠、氟化钾、氟氢化钠、氢氧化钾和三氟乙酸盐中的一种或多种,优选为氟化铵、氟化钠、氟化钾、氟氢化钠或氢氧化钾。
根据本发明,所述步骤(a)中将碱金属源和氟源加入溶液之前,还包括将碱金属源和氟源溶于溶剂的步骤。优选地,所述溶剂为乙醇或甲醇,例如为甲醇。
根据本发明,所述步骤(a)中,所述碱金属源、氟源与溶剂的摩尔体积比例为(0.05~5)mmol:(0.2~7)mmol:(1~12)ml,优选地,所述碱金属源、氟源与溶剂的比例为(0.3~3)mmol:(2~4)mmol:(3~10)ml。
根据本发明,所述加热的温度为70-350℃,例如先在70℃-100℃下加热,在再200-350℃下加热。所述加热的时间为1h-6h,示例性地为1h、2h、3h、4h、5h或6h。
根据本发明,步骤(b)中,所述稀土源选自下述物质中的一种或多种:稀土离子的乙酸盐、稀土离子的氯化物和稀土离子的三氟乙酸盐,优选为稀土离子的三氟乙酸盐,还优选为Y、Yb、Er、Ce、Tm、Ho、Eu、Nd和Lu的三氟乙酸盐。
根据本发明,步骤(b)中所述碱金属源选自含有碱金属的氢氧化物、含有碱金属的油酸盐、含有碱金属的乙酸盐、含有碱金属的氟化物、含有碱金属的氟氢化物和含有碱金属的三氟乙酸盐中的一种或多种,优选为含有碱金属的三氟乙酸盐、含有碱金属的氯化物或含有碱金属的乙酸盐,示例性选自三氟乙酸钾、三氟乙酸钠、氯化钠、氯化钾、乙酸钠、乙酸钾中的至少一种。
根据本发明,步骤(b)中,所述溶剂为油酸和十八烯中的至少一种。优选地,当所述溶剂为油酸和十八烯的混合溶剂时,所述油酸与十八烯的摩尔比例为1:0.5-20,优选为1:1-12,示例性地为1:1。
根据本发明,步骤(b)中,所述加热的温度为200-350℃,示例性地为200℃、220℃、240℃、260℃、280℃、300℃、310℃、320℃、350℃。所述加热的时间为1h-6h,示例性地为1h、2h、3h、4h、5h或6h。
作为本发明示例性地实施方案,所述稀土掺杂无机纳米颗粒NaYF
(a)称取醋酸钇、醋酸镱、醋酸铒、醋酸铈于反应容器中,加入溶剂;在惰性气氛下加热至原料溶解,冷却至室温,加入碱金属溶液和含氟溶液,升温至70℃,去除甲醇,继续升温至310℃,保温1h后自然冷却至室温,得到NaYF
(b)将步骤(a)中含NaYF
根据本发明,步骤(2)中,稀土掺杂无机纳米材料表面进行水溶性修饰包括配体氧化法、逐层沉积法、酸洗、配体交换等方法中的至少一种。
根据本发明,步骤(2)中,当采用两亲性配体对所述稀土掺杂无机纳米材料的表面进行修饰时,具体方法为:
将所述稀土掺杂无机纳米材料与两亲性配体在三氯甲烷中混合,制备得到水溶性的稀土掺杂无机纳米材料。
根据本发明,步骤(2)中,所述稀土掺杂无机纳米材料与两亲性配体的质量比为1:(4~10),示例性地为1:4、1:5、1:6、1:7、1:8、1:9、1:10。
根据本发明,步骤(2)中,可以采用搅拌的方式将所述稀土掺杂无机纳米材料与两亲性配体在三氯甲烷中混合,搅拌时间10~48h;示例性地为10h、15h、20h、25h、30h、35h、40h、45h、48h。
根据本发明,步骤(2)中,混合的温度为15-35℃,例如室温。
根据本发明,步骤(2)中,还包括后处理步骤:对制备的产物进行旋蒸、超声、离心等。
示例性地,超声功率为100W,40Hz,超声时间为5min。
作为本发明示例性地实施方案,当采用二硬脂酰基磷脂酰乙醇胺-聚乙二醇-2000(DSPE-PEG-2000)对所述稀土掺杂无机纳米材料的表面进行修饰时,具体方法为:
在三氯甲烷中加入所述稀土掺杂无机纳米材料与DSPE-PEG-2000,室温搅拌,随后旋蒸除去溶剂;加入去离子水超声得水溶性内核,离心洗涤后低温保存,得到二硬脂酰基磷脂酰乙醇胺-聚乙二醇-2000修饰的稀土掺杂无机纳米材料,即水溶性的稀土掺杂无机纳米颗粒。
根据本发明,所述步骤(3)具体是通过低渗裂解,反复冻融,差速离心以及挤压,制备得到细胞膜囊泡;其具体步骤包括:
采用磷酸缓冲盐溶液清洗细胞膜,得到细胞沉淀;再采用低渗细胞裂解液重悬并放置于冰上,对细胞沉淀冻融;差速离心后,得到细胞膜沉淀,再将细胞膜沉淀挤压透过聚碳酸酯膜,得到细胞膜囊泡。
根据本发明,采用磷酸缓冲盐溶液清洗细胞膜的温度为0-5℃,示例性地为0、1℃、2℃、3℃、4℃、5℃。
根据本发明,冰上放置的时间为5-15min;示例性地为5min、6min、8min、10min、12min、13min、14min、15min。
根据本发明,所述冻融可以采用液氮和水浴冻融,例如水浴温度为25-38℃,例如为37℃。
根据本发明,所述低渗细胞裂解液为膜蛋白提取试剂A(Beyotime P0033-1)。
根据本发明,所述挤压可以采用挤压注射装置,挤压的次数为10-20次。
作为本发明示例性的实施方案,所述步骤(3)具体为:
4℃下,用提前预冷的磷酸缓冲盐溶液冲洗三次之后,收集细胞沉淀。用低渗细胞裂解液重悬并放置于冰上,反复冻融;随后进行差速离心,获得细胞膜沉淀;最后重悬细胞膜沉淀,并通过物理挤出得到细胞膜囊泡。
根据本发明,步骤(4)中,聚碳酸酯膜的孔径为50-400nm,示例性地为50nm、100nm、150nm、200nm、250nm、300nm、350nm、400nm。
根据本发明,步骤(4)中,采用挤压注射装置使混合物通过聚碳酸酯膜,挤压次数为10-20次。
本发明还提供上述仿生膜包裹稀土掺杂无机纳米荧光探针在近红外二区生物荧光成像中的应用。
本发明的有益效果:
本发明提供一种仿生膜包裹稀土掺杂无机纳米荧光探针,其制备工艺简单,全程无任何有毒材料,安全可靠。同时,所述仿生膜包裹稀土掺杂无机纳米荧光探针借助稳定的膜结构,可以实现免疫逃逸,延长其在血液循环中的驻留时间;并且生物体来源的仿生膜结构使荧光探针具有更高的生物安全性。因此,可以作为一种全新的近红外二区无机纳米荧光探针。
本发明制备的仿生膜包裹稀土掺杂无机纳米荧光探针可以采用肿瘤细胞作为仿生膜来源,可以实现对肿瘤的靶向性。
本发明制备的仿生膜包裹稀土掺杂无机纳米荧光探针在生物体内可维持高有效浓度。
附图说明
图1为实施例1配体修饰的NaYF
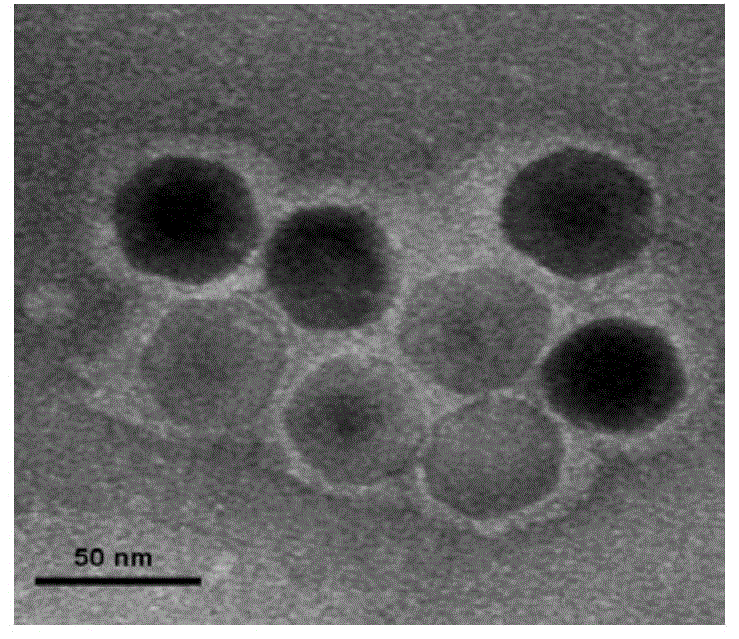
图2为实施例3中仿生膜包裹稀土掺杂无机纳米荧光探针的透射电镜图。
图3为实施例1配体修饰的NaYF
图4为实施例1配体修饰的NaYF
图5为实施例1配体修饰的NaYF
图6为实施例1配体修饰的NaYF
图7为用CCK8检测实施例1配体修饰的NaYF
图8为采用实施例1配体修饰的NaYF
具体实施方式
下文将结合具体实施例对本发明的技术方案做更进一步的详细说明。应当理解,下列实施例仅为示例性地说明和解释本发明,而不应被解释为对本发明保护范围的限制。凡基于本发明上述内容所实现的技术均涵盖在本发明旨在保护的范围内。
除非另有说明,以下实施例中使用的原料和试剂均为市售商品,或者可以通过已知方法制备。
实施例1:NaYF
(1)基于共沉淀法制备NaYF
室温下按照0.74mmol醋酸钇、0.2mmol醋酸镱、0.02mmol醋酸铒和0.04mmol醋酸铈的化学计量比放至三口烧瓶中,随后加入6ml油酸和16ml十八稀作为溶剂在惰性气氛下升温至150~160℃,将上述固体完全溶解后自然冷却到室温,得到澄清溶液;将溶有1.25mmol氢氧化钠和2mmol氟化铵的甲醇溶液10ml加到上述溶液中,在惰性气氛下升温至65~80℃,保温至甲醇除净,升温至100~110℃,保温至水除净,然后在惰性气氛下升温至310℃,保温1h后自然冷却到室温,沉淀并洗涤,得到NaYF
将NaYF
(2)对NaYF
称取15mg NaYF
实施例2:乳腺癌4T1肿瘤细胞膜囊泡制备
(1)小鼠乳腺癌肿瘤细胞系4T1的收集:收集约8×10
(2)4T1肿瘤细胞膜碎片的制备:膜蛋白抽提试剂A(Beyotime P0033-1)重悬细胞沉淀,随后冰上放置15min。采用冻融法破碎细胞,取少量液体显微镜下观察,绝大多数观察不到完整细胞形态时,说明破碎完全。接着4℃,700g离心10min,以除去细胞核和未破碎的细胞。取上清接着4℃,14000g离心30min,收集沉淀即为细胞膜。将沉淀重悬于适量生理盐水中备用。
(3)4T1肿瘤细胞膜囊泡的制备:通过物理挤出的方法制备细胞膜囊泡,具体为:将提取的细胞膜碎片通过反复挤压注射装置经过400nm聚碳酸酯膜,反复挤压20次,得到4T1肿瘤细胞膜囊泡。
实施例3:仿生膜包裹稀土掺杂无机纳米荧光探针的制备
将实施例1中配体修饰的NaYF
测试例1:仿生膜包裹稀土掺杂无机纳米荧光探针粒径电位及透射电镜测定
采用马尔文粒度仪分别测定实施例1中配体修饰的NaYF
测试例2:仿生膜包裹稀土掺杂无机纳米荧光探针透射电镜测定
将实施例3中仿生膜包裹稀土掺杂无机纳米荧光探针滴一滴于培养皿上,将200目铜网倒扣在液滴静置上30s,滤纸吸去多余液体;再滴一滴2%磷钨酸于培养皿上,将上述铜网倒扣在染液上避光染色30s,滤纸吸去多余染料,室温自然晾干,用生物投射电子显微镜观察样品,测试结果如图2所示,仿生膜包裹稀土掺杂无机纳米荧光探针具有明显核壳结构,其中内核的厚度为50nm,壳层细胞膜的厚度约为10nm。
测试例3:仿生膜包裹稀土掺杂无机纳米荧光探针体外靶向能力评估
将乳腺癌4T1细胞,以10
测试例4:仿生膜包裹稀土掺杂无机纳米生物荧光探针体外巨噬细胞吞能力评估
将小鼠巨噬细胞RAW264.7,以10
测试例5:仿生膜包裹稀土掺杂无机纳米生物荧光探针体内循环能力评估
小鼠尾静脉注射6mg/ml实施例1配体修饰的NaYF
测试例6:仿生膜包裹稀土掺杂无机纳米荧光探针体内靶向能力评估
小鼠尾静脉注射6mg/ml实施例1配体修饰的NaYF
测试例7:仿生膜包裹稀土掺杂无机纳米荧光探针生物安全性评估
(1)细胞毒性实验
利用CCK8法测定实施例1中配体修饰的NaYF
(2)不同器官组织切片HE染色安全性评估
为了确定实施例1中配体修饰的NaYF
以上,对本发明的实施方式进行了示例性的说明。但是,本发明的保护范围不拘囿于上述实施方式。凡在本发明的精神和原则之内,本领域技术人员所作出的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
