一种近红外发光的阳离子自由基细菌荧光成像抗菌剂及其制备与应用
文献发布时间:2024-04-18 19:58:26
技术领域
本发明属于医用材料的技术领域,具体涉及一种具有近红外发光的阳离子自由基的细菌荧光成像抗菌剂及其制备方法与应用。所述细菌荧光成像抗菌剂在细菌荧光成像以及监测细菌与免疫细胞的相互作用过程的应用。
背景技术
抗生素在现代细菌感染治疗中发挥了重要作用。但由于抗生素的滥用导致耐药性细菌的出现,细菌感染在全球范围内引发严重疾病。因此,开发新型抗菌剂,实现细菌的诊疗一体化至关重要。细菌膜带负电性,为了精确识别细菌的位置,必须在抗菌剂上进一步修饰靶向基团。目前开发了一系列基于带正电荷的细菌靶向试剂,如铵盐、抗菌肽和金属配合物等。但这些诊疗一体化的试剂通常会经历繁琐的合成过程。近年来,超分子主体化合物稳定自由基被用于光热疗法。然而,没有超分子主体化合物稳定的自由基作为细菌诊疗一体化的药物。因为大多数阳离子自由基的荧光量子产率较低。这可能是由于激发态和基态之间的低能隙以及激发能的快速非辐照衰减所致。
发明内容
为了克服现有技术的不足和缺陷,本发明的目的在于提供一种具有近红外发光的阳离子自由基细菌荧光成像抗菌剂及其制备方法。本发明的试剂为细菌诊疗一体化的试剂,可以实现细菌诊疗一体化。
本发明的另一目的在于提供上述抗菌剂的应用。所述阳离子自由基化合物在细菌诊疗一体化试剂或药物中的应用,所述诊疗一体化是指在针对革兰氏阳性菌的成像和杀灭。所述抗菌剂还可以用于监测体内和体外免疫细胞吞噬细菌的过程和针对革兰氏阴性菌的药物筛选。
本发明的目的通过下述技术方案实现:
一种具有近红外发光的阳离子自由基细菌荧光成像抗菌试剂,是由式II阳离子自由基化合物和葫芦[7]脲组成;
式Ⅱ化合物:
其中R
其中R
R
所述取代的芳基是指芳基环状上的氢被烷氧基、氨基、羧基中一种以上取代;
所述杂芳基指具有1-20个碳原子、1-4个选自N、S、O杂原子的单环或多环杂芳族基团,代表性的杂芳基包括:吡咯基、吡啶基、嘧啶基、咪唑基、噻唑基、吲哚基、氮杂萘基、氮杂蒽基、氮杂芘基。
R
所述取代的烷基是指烷基上的氢被羟基、甲氧基、羧基、卤素等基团取代。
所述芳基指具有6-20个碳原子的单环或多环芳族基团,代表性的芳基包括:苯基、萘基、蒽基、芘基;芳基氧基、芳基氨基和芳基硫基中的芳基各自独立的为具有6-20个碳原子的单环或多环芳族基团,代表性的芳基包括:苯基、萘基、蒽基、芘基。
所述杂芳基指具有1-20个碳原子、1-4个选自N、S、O杂原子的单环或多环杂芳族基团,代表性的杂芳基包括:吡咯基、吡啶基、嘧啶基、咪唑基、噻唑基、吲哚基、氮杂萘基、氮杂蒽基、氮杂芘基;所述杂芳基氧基、杂芳基氨基和杂芳基硫基中杂芳基各自独立的为具有1-20个碳原子、1-4个选自N、S、O杂原子的单环或多环杂芳族基团,代表性的杂芳基包括:吡咯基、吡啶基、嘧啶基、咪唑基、噻唑基、吲哚基、氮杂萘基、氮杂蒽基、氮杂芘基。
R
所述具有近红外发光的阳离子自由基细菌荧光成像抗菌剂具体是在葫芦[7]脲和有氧的条件下,式I化合物氧化,得到由式II阳离子自由基化合物和葫芦[7]脲组成的复合物,即阳离子自由基细菌荧光成像抗菌剂。
所述式Ⅰ化合物为:
R
所述CB[7]与式I化合物的摩尔比为1:(2~4)。
所述具有近红外发光的阳离子自由基化合物(式II)是将式I化合物与葫芦[7]脲在氧气中原位氧化得到。具体是在水溶液中氧化得到。
所述具有近红外发光的阳离子自由基细菌荧光成像抗菌剂的制备方法,包括以下步骤:将式I化合物和葫芦[7]脲在水中混合,式I化合物在有氧的条件下进行氧化反应,得到由式II阳离子自由基化合物和葫芦[7]脲组成的复合物,即阳离子自由基细菌荧光成像抗菌剂。
氧化反应的方程式:
所述水为超纯水;
所述有氧条件是指在氧化剂的作用下反应,氧化剂为氧气、含有氧气的气氛(如:空气);
在氧化剂的作用下进行反应时,可以光照或不光照。
当氧化剂为氧气或空气时,在进行氧化时,光照或不光照;
光照时,氧化反应称为光氧化。所述光氧化是指在有氧的条件下进行光照。
所述光照包括太阳光、紫外光。
所述式I化合物在水中的浓度为1μM~1000mM;所述CB[7]与式I化合物的摩尔比为1:(2~4)。
所述反应的时间为1~30min。
本发明的阳离子自由基细菌荧光成像抗菌试剂用作细菌荧光成像剂,进行细菌染色;特别是革兰氏阳性菌的荧光成像剂。
本发明的阳离子自由基细菌荧光成像抗菌剂用于革兰氏阳性菌和革兰氏阴性菌的区分鉴别,革兰氏阳性菌被染色发红色荧光,革兰氏阴性菌不染色;所述革兰氏阳性菌为金黄色葡萄球菌、耐甲氧西林金黄色葡萄球菌;所述革兰氏阴性菌为大肠杆菌、绿脓杆菌。
本发明的阳离子自由基细菌荧光成像抗菌剂用作鉴别革兰氏阳性菌和革兰氏阴性菌的试剂。
本发明的阳离子自由基细菌荧光成像抗菌试剂用于针对革兰氏阴性菌进行药物筛选;所述革兰氏阴性菌为大肠杆菌、绿脓杆菌。
本发明的阳离子自由基细菌荧光成像抗菌剂用于检测革兰氏阳性菌与免疫细胞相互作用。
本发明的阳离子自由基细菌荧光成像抗菌剂在抗菌上的应用,用于抑制和杀灭革兰氏阳性菌;所述革兰氏阳性菌为金黄色葡萄球菌、耐甲氧西林金黄色葡萄球菌。
本发明具有以下优异的效果:
本发明的阳离子自由基化合物通过原位反应生成,不需分离,具有近红外发光,生成效率高、稳定性好的优点,可直接用于细菌的荧光成像。能够对革兰氏阳性菌和革兰氏阴性菌进行有效的区分,同时对于革兰氏阳性菌具有良好的抗菌效果,从而实现细菌的诊疗一体化;还能实现对革兰氏阴性菌的药物筛选。此外,该阳离子自由基可以作为检测细菌与免疫细胞的相互作用的荧光探针。
附图说明
图1为I-1在CB[7]及空气作用下,原位氧化转变为阳离子自由基化合物I-1
图2为II-1在CB[7]及空气作用下,原位氧化转变为阳离子自由基化合物II-1
图3为III-1在CB[7]及空气作用下,原位氧化转变为阳离子自由基化合物III-1
图4为I-1
图5为不同浓度下I-1
图6为不同浓度的I-1
图7为I-1
图8为I-1
图9为不同浓度的I-1、CB[7]和I-1
图10为不同浓度的I-1、CB[7]、I-1
图11为100μM或者400μM的I-1
图12为革兰氏阴性菌经过不同药物处理后,I-1
图13为I-1
图14为I-1
图15为I-1
具体实施方式
下面结合实施例对本发明作进一步详细的描述,但本发明的实施方式不限于此。
本发明的实施例1~3所提供的化合物对革兰氏阳性菌具有良好的抗菌效果和选择性荧光成像,能够对革兰氏阳性菌和革兰氏阴性菌进行有效的区分;还能实现对革兰氏阴性菌的药物筛选。
实施例1:水溶液中化合物I-1
将化合物I-1(2,5-二甲基-3-羟亚甲基-1-苯基-1H-吡咯)(300μM),加入到葫芦[7]脲的水溶液中(100μM),吡咯化合物I-1迅速转变为相应的阳离子自由基化合物I-1
实施例2:水溶液中化合物II-1
将化合物II-1(1-(4-甲氧苯基)-2,5-二甲基-3-羟亚甲基-1H-吡咯)(300μM),加入到葫芦[7]脲的水溶液中(100μM),吡咯化合物II-1迅速转变为相应的阳离子自由基化合物II-1
实施例3:水溶液中化合物III-1
将化合物III-1(2,5-二乙基-3-羟亚甲基-1H-吡咯)(300μM),加入到葫芦[7]脲的水溶液中(100μM),吡咯化合物III-1迅速转变为相应的阳离子自由基化合物III-1
实施例4:
细菌的荧光成像应用(见图4~图5):
(1)细菌的培养
选取金黄色葡萄球菌(革兰氏阳性菌,S.aureus)的一个菌落转移到NB培养基中,在37℃,转速为180rpm的摇床上孵育8h。通过离心(8000rpm,3min)、洗涤(PBS,10mM,pH=7.4)3次得到细菌。最后重悬于PBS中,得到600nm处的光密度为1.0(OD
(3)细菌的荧光成像实验
活细菌成像:在细菌悬液(OD
死细菌成像:首先将200μL的细菌悬液离心(8000rpm,3min),弃去上清液,然后加入1mL的75%的EtOH重悬,在摇床上37℃孵育30min。再次离心(8000rpm,3min),并用磷酸盐缓冲盐水(PBS,10mM,pH=7.4)洗涤2次。最后用PBS重悬得到细菌悬液。然后加入10μL浓度为10mM的I-1
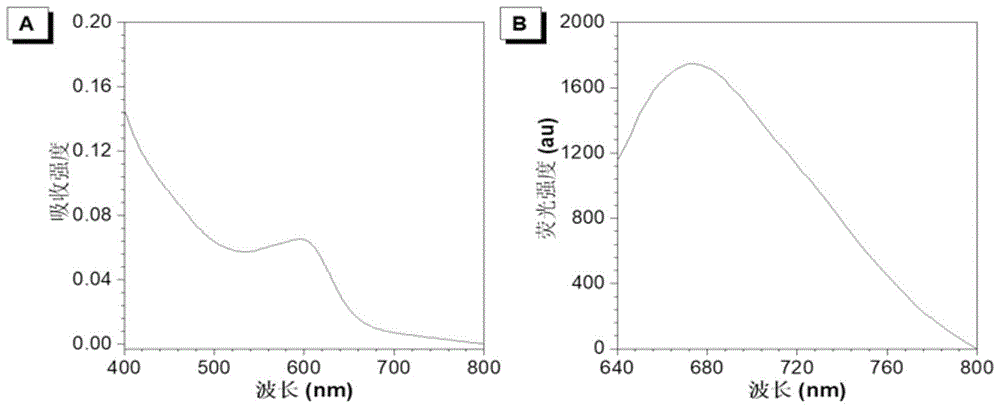
图4为I-1
荧光光谱和共聚焦成像结果都可以说明I-1
(4)细菌表面电位测试:
将200μL的OD
图5为不同浓度下I-1
实施例5
I-1
(1)SEM表征
在细菌悬液中加入PBS稀释,然后加入10,40μL的浓度为10mM的I-1
(2)TEM表征
在细菌悬液中加入PBS稀释,然后加入10,40μL的浓度为10mM的I-1
通过电镜可以进一步证明I-1
图6为不同浓度的I-1
实施例6
I-1
(1)普适性验证
通过激光共聚焦研究I-1
(2)细菌共孵育
将I-1
图7为I-1
图8为I-1
在混合菌液中,I-1
实施例7
抗菌实验(图9~图10)
利用平板计数法对抗菌性能进行表征。将浓度为~10
图9为不同浓度的I-1、CB[7]和I-1
图10为不同浓度的I-1、CB[7]、I-1
实施例8
抗菌机制实验(图11)
在细菌悬液(OD
图11为100μM或者400μM的I-1
实施例9
药敏性实验(图12)
I-1
图12为革兰氏阴性菌经过不同药物处理后,I-1
实施例10
监测免疫细胞与细菌相互作用的应用(图13-15)
(1)I-1
荧光成像实验:取200μL的OD
流式细胞仪:取200μL的OD
I-1
(2)体外实验
本实验中涉及的RAW 264.7细胞购自国家实验细胞资源共享服务平台。RAW 264.7细胞的完全培养基由10%FBS、1%双抗(青霉素和链霉素)和DMEM组成。细胞培养于37℃,CO
(3)体内实验
细菌悬液制备:将200μL的细菌悬液(OD
(2)注射针准备:在针头外径约为20μm的位置使用镊子折断针尖,使用光学显微镜目镜中的标尺。避免使用开口过大的针头,因为它们会影响胚胎的存活。
(3)细菌注射:受精后第3天,首先将胚胎放在含有0.02%(w/v)3-氨基苯甲酸的100mm培养皿中进行麻醉,然后用立体荧光显微镜选择表达绿色荧光蛋白的胚胎。将胚胎转移到覆盖有含有0.02%(w/v)3-氨基苯甲酸的E3培养基的琼脂糖平板上,在胚胎的体节上皮下用气压显微注射器注射约2nL的金黄色葡萄球菌悬液。对于斑马鱼的中心粒细胞或巨噬细胞:激发波长为488nm,发射波长为500-550nm;对于I-1
通过体外和体内实验证明了可以监测经过I-1
图13为I-1
图14为I-1
图15为I-1
- 具有聚集诱导发光性质的近红外二区荧光化合物及制备方法、纳米粒胶束及其应用
- 一种基于花菁结构测钯离子的近红外荧光探针、其制备方法及应用
- 一种近红外发光的自由基阳离子化合物及其制备与应用
- 一种通过原子转移自由基聚合制备的近红外二区荧光成像造影剂及其应用
