表羽扇豆碱及其衍生物在制备抗阿尔茨海默病的药物中的应用
文献发布时间:2024-04-18 19:59:31
技术领域
本发明涉及生物医药技术领域,尤其涉及表羽扇豆碱及其衍生物在制备抗阿尔茨海默病的药物中的应用。
背景技术
阿尔茨海默病(Alzheimer’s disease,AD)是一种以进行性认知功能障碍为主,逐渐影响日常生活能力的慢性中枢神经系统退行性疾病。全球65岁以上老年人群中患AD的概率为4%~7%,占所有痴呆病因的60%~80%,且平均每增加6.1岁,AD患病率增加1倍。随着社会人口老龄化,AD发病率和患病率急剧上升,由此造成的家庭和社会负担越发沉重。
然而AD的发病机制尚未明确,临床药物治疗方式也有限。目前临床上应用最广泛的抗阿尔茨海默病药物主要是乙酰胆碱酯酶抑制剂(ace-tylcholine esteraseinhibitors,AChEI)(如盐酸多奈哌齐、重酒石酸卡巴拉汀等)和N-甲基-D-天门冬氨酸(N-methyl-D-aspartate,NMDA)受体阻滞剂(如盐酸美金刚等),但这些药物的作用并不理想,它们只能减轻症状,并不能使病情得到控制,不能根治AD,甚至不能延缓AD的发展,并且药物副作用较大,临床上有些病人难以耐受。可见,研发安全有效的预防或干预AD的药物是现阶段AD研究的重点和热点。近年来,靶向Aβ蛋白的新药如阿杜卡尼单抗、仑卡奈单抗等也被批准用于AD治疗,但此类药物价格较为昂贵,短期内难以广泛普及。因此,寻找新的依从性好、副作用少、性价比高的抗AD药物具有重大的临床意义,也是抗AD药物研发的主要方向。
表羽扇豆碱(1-Epilupinine),又名表羽扇豆宁,是从豆科羽扇豆属植物羽扇豆(Lupinuspolyphyllus)中分离得到的。表羽扇豆碱是一种喹诺里西定类生物碱成分,分子式为C
发明内容
本发明的目的在于提供表羽扇豆碱及其衍生物在制备抗阿尔茨海默病的药物中的应用,为预防或治疗阿尔茨海默病,改善患者认知功能障碍,提高患者记忆力提供新的药物。
为了实现上述发明目的,本发明提供以下技术方案:
本发明提供了表羽扇豆碱及其衍生物在制备抗阿尔茨海默病的药物中的应用,所述表羽扇豆碱的结构式为:
优选的,所述衍生物包括表羽扇豆碱的有机酸型或无机酸盐型产物,及表羽扇豆碱11位羟基位点的酯化产物或醚化产物。
优选的,所述药物还包括对抗阿尔兹海默症有积极作用的药物成分。
优选的,所述对抗阿尔兹海默症有积极作用的药物成分包括乙酰胆碱酯酶抑制剂或N-甲基-D-天门冬氨酸受体阻滞剂。
优选的,所述乙酰胆碱酯酶抑制剂包括卡巴拉汀、加兰他敏或多奈哌齐。
优选的,所述N-甲基-D-天门冬氨酸受体阻滞剂包括美金刚。
优选的,所述对抗阿尔兹海默症有积极作用的药物成分还包括石杉碱甲或甘露特纳。
优选的,所述对抗阿尔兹海默症有积极作用的药物成分还包括Aβ或Tau蛋白靶向药。
优选的,所述Aβ或Tau蛋白靶向药包括阿杜卡尼单抗、Donanemab或仑卡奈单抗。
本发明提供了表羽扇豆碱(1-EPILUPININE)及其衍生物在预防或治疗阿尔茨海默病药物中的应用。本发明研究发现,应用剂量为2.5-5mg/kg的表羽扇豆碱或其衍生物可以改善AD模型小鼠的记忆力和空间学习能力,缩短AD模型小鼠在Morris水迷宫实验的空间探索实验中找到平台的潜伏期并且提高其穿过平台的次数。其次,在旷场实验中发现阳性对照药胆碱酯酶抑制剂(多奈哌齐)可显著降低小鼠在旷场中运动距离,影响小鼠运动能力,而表羽扇豆碱及其衍生物不影响小鼠的运动距离,对小鼠的运动能力影响小。同时表羽扇豆碱及其衍生物可增加小鼠进入中心区的次数和运动距离,缓解AD模型小鼠的焦虑情绪。进一步研究发现表羽扇豆碱及其衍生物可降低脑内AD模型小鼠脑内的促炎因子水平,改善AD模型小鼠脑内的炎症状态。
综上,表羽扇豆碱或其衍生物可用于预防或治疗阿尔茨海默病,改善患者认知功能障碍,提高患者记忆力,具有效果显著、用药量少、副作用小等优点。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据提供的附图获得其他的附图。
图1为试验例1中表羽扇豆碱的
图2为试验例1中表羽扇豆碱的
图3为试验例1中表羽扇豆碱的MS质谱图;
图4中(A)为试验例1中不同处理组小鼠穿越平台的次数,(B)为试验例1中不同处理组小鼠在平台上的潜伏时间;
图5中(A)为试验例2中不同处理组小鼠活动的总距离,(B)为试验例2中不同处理组小鼠在中心区停留的时间,(C)为试验例2中不同处理组小鼠穿越平台中心区的次数,(D)为试验例2中不同处理组小鼠在中心区活动的距离;
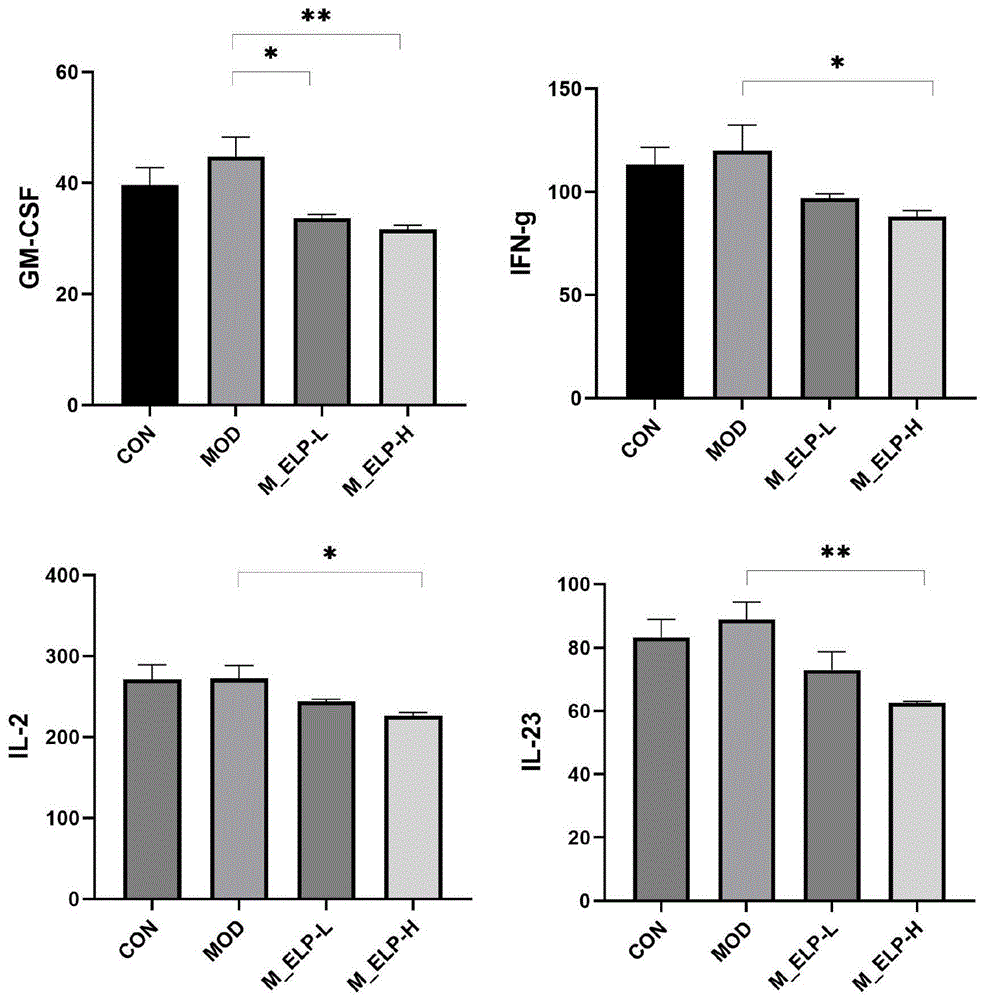
图6为试验例3中不同处理组小鼠脑内炎症因子的浓度。
具体实施方式
本发明提供了表羽扇豆碱及其衍生物在制备抗阿尔茨海默病的药物中的应用。
在本发明中,所述表羽扇豆碱为白色粉末,HRESI-MS m/z[M+H]
1
13
所述表羽扇豆碱的化学结构式如式1所示。
在本发明中,所述衍生物包括表羽扇豆碱的有机酸型或无机酸盐型产物,及表羽扇豆碱11位羟基位点的酯化产物或醚化产物。
在本发明中,所述药物还包括对抗阿尔兹海默症有积极作用的药物成分。
在本发明中,所述对抗阿尔兹海默症有积极作用的药物成分包括乙酰胆碱酯酶抑制剂或N-甲基-D-天门冬氨酸受体阻滞剂。
在本发明中,所述乙酰胆碱酯酶抑制剂包括卡巴拉汀、加兰他敏或多奈哌齐。
在本发明中,所述N-甲基-D-天门冬氨酸受体阻滞剂包括美金刚。
在本发明中,所述对抗阿尔兹海默症有积极作用的药物成分还包括石杉碱甲或甘露特纳。
在本发明中,所述对抗阿尔兹海默症有积极作用的药物成分还包括Aβ或Tau蛋白靶向药。
在本发明中,所述Aβ或Tau蛋白靶向药包括阿杜卡尼单抗、Donanemab或仑卡奈单抗。
在本发明中,所述药物的剂型包括粉剂、颗粒剂、片剂、胶囊剂、丸剂、溶液、悬浮液或注射液。
在本发明中,所述药物的给药剂型包括液体剂型或固体剂型。
在本发明中,所述液体剂型包括真溶液类、胶体类、微粒剂型、乳剂剂型、混悬剂型;所述固体剂型包括片剂、胶囊、滴丸、气雾剂、丸剂、粉剂、溶液剂、混悬剂、乳剂、颗粒剂、栓剂、冻干粉针剂。
在本发明中,所述片剂包括糖包衣片、薄膜包衣片、肠溶包衣片、双层片或多层片剂。
在本发明中,所述片剂的载体包括稀释剂、润湿剂、崩解剂、崩解抑制剂、吸收促进剂或润滑剂。
在本发明中,所述稀释剂包括淀粉、糊精、硫酸钙、乳糖、甘露醇、蔗糖、氯化纳、葡萄糖、尿素、碳酸钙、白陶土、微晶纤维素或硅酸铝;所述润湿剂包括水、聚乙二醇、乙醇、丙醇、淀粉浆、糊精、糖浆、蜂蜜、葡萄糖溶液、阿拉伯胶浆、明胶浆、羧甲基纤维素纳、紫胶、甲基纤维素、磷酸钾或聚乙烯吡咯烷酮;所述崩解剂包括干燥淀粉、海藻酸盐、琼脂粉、褐藻淀粉、碳酸氢钠与枸橼酸、碳酸钙、聚氧乙烯山梨糖醇脂肪酸酯、十二烷基磺酸钠、甲基纤维素或乙基纤维素;所述崩解抑制剂包括蔗糖、三硬脂酸甘油酯、可可脂或氢化油;所述吸收促进剂包括季铵盐或十二烷基硫酸钠;所述润滑剂包括滑石粉、二氧化硅、玉米淀粉、硬脂酸盐、硼酸、液体石蜡或聚乙二醇。
在本发明中,所述胶囊包括明胶胶囊、软胶囊或微囊剂。
在本发明中,所述丸剂的载体包括稀释剂、粘合剂或崩解剂。
在本发明中,所述稀释剂包括葡萄糖、乳糖、淀粉、可可脂、氢化植物油、聚乙烯吡咯烷酮、Gelucire、高岭土或滑石粉;所述粘合剂包括阿拉伯胶、黄蓍胶、明胶、乙醇、蜂蜜、液糖、米糊或面糊;所述崩解剂包括琼脂粉、干燥淀粉、海藻酸盐、十二烷基磺酸钠、甲基纤维素或乙基纤维素。
在本发明中,所述溶液剂、混悬剂、乳剂、或冻干粉针剂的载体包括稀释剂、粘合剂、润滑剂、防腐剂、表面活性剂或分散剂。
在本发明中,所述稀释剂包括水、乙醇、聚乙二醇、1,3-丙二醇、乙氧基化的异硬脂醇、多氧化的异硬脂醇或聚氧乙烯山梨醇脂肪酸酶。
在本发明中,所述栓剂的载体包括聚乙二醇、卵磷脂、可可脂、高级醇、高级醇的酶、明胶或半合成甘油酶。
在本发明中,所述注射液包括等渗注射液,所述等渗注射液的载体包括氯化钠、葡萄糖、甘油、助溶剂、缓冲剂或pH调节剂。
在本发明中,所述药物制剂中可包括着色剂、防腐剂、香料、矫味剂或甜味剂。
在本发明中,所述药物的给药途径包括肠道途径或非肠道途径。
在本发明中,所述肠道途径包括口服;所述非肠道途径包括肌肉注射、皮下注射、鼻腔、口腔粘膜、皮肤注射、穴位注射、腹膜或直肠途径。
在本发明中,所述药物可制成普通制剂、缓释制剂、控释制剂、靶向制剂及各种微粒给药系统。
在本发明中,抗阿尔茨海默病的药物包括预防阿尔茨海默病的药物和治疗阿尔茨海默病的药物。
在本发明中,所述预防阿尔茨海默病的药物的用量为0.001-5mg/kg·天;所述治疗阿尔茨海默病的药物的用量为0.01-30mg/kg·天。
在本发明中,所述抗阿尔茨海默病药物的给药方式为口服、鼻喷、滴注或注射;给药对象为哺乳动物,所述哺乳动物包括人。
下面结合实施例对本发明提供的技术方案进行详细的说明,但是不能把它们理解为对本发明保护范围的限定。表羽扇豆碱(1-EPILUPININE),CAS号:486-71-5,本实验室自制。
实施例1
表羽扇豆碱的制备方法:
取10kg羽扇豆(Lupinus micranthus)种子进行粉碎,将粉碎后的种子用95%乙醇加热回流提取3次,每次50L,每次提取2h,得到提取液;将提取液减压浓缩后获得浸膏,共2.5kg;将获得的2.5kg浸膏混悬于6L蒸馏水中,并用2mol/L的稀盐酸调节溶液pH为2,使用氯仿萃取3次,每次6L;萃取完成后,用2mol/L的NaOH溶液调节萃取后的溶液pH至10;调节完成后继续用氯仿萃取3次,每次6L。回收氯仿,得到80.0g总生物碱。
将得到的总生物碱用硅胶柱层析进行粗分,氯仿-甲醇系统(10:0-0:10)梯度洗脱,得到6个部分(Frs.A-F)。其中Fr.B(9.6g)经硅胶柱层析、Sephadex LH-20分离纯化得到2g表羽扇豆碱(1-Epilupinine)。
经测定,表羽扇豆碱的熔点为77-78℃,可溶于氯仿、甲醇、乙醇;HR-ESI-MS m/z[M+H]
实施例2
取表羽扇豆碱150g,以300g乳糖作为填充剂,2.25g硬脂酸镁作为润滑剂,4.5g二氧化硅作为抗结剂,过筛,混匀,装入胶囊,制成1000粒表羽扇豆碱胶囊。根据定量分析获得表羽扇豆碱的含量,作为服用量的依据。
实施例3
取表羽扇豆碱150g加水稀释并用0.15g甜菊甙矫味而制成10%的表羽扇豆碱口服液。根据定量分析获得表羽扇豆碱的含量,作为服用量的依据。
实施例4
取表羽扇豆碱100g,溶于500mL无水乙醇中,滴加3%的稀盐酸溶液至pH为6,放置析出表羽扇豆碱盐酸盐结晶,过滤,干燥,得到表羽扇豆碱盐酸盐;按常规加注射液用水,精滤,灌封、灭菌制成注射液。
实施例5
取表羽扇豆碱200g,溶于1000mL无水乙醇中,滴加5%的硫酸乙醇溶液至pH为6,放置析出结晶,过滤,干燥,得到表羽扇豆碱硫酸盐;将得到的表羽扇豆碱硫酸盐溶于无菌注射液用水中,加入5%葡萄糖作为赋形剂,搅拌使扇豆碱硫酸盐溶解,用无菌抽滤漏斗过滤,再无菌精滤,分装于2安瓿中,低温冷冻干燥后灭菌熔封得粉针剂。
实施例6
将表羽扇豆碱与赋形剂淀粉按重量比9:1混合,制成粉剂。
实施例7
将表羽扇豆碱与赋形剂淀粉按重量比为1:8的比例混合,制粒压片。
实施例8
将50g表羽扇豆碱溶于300mL无水乙醇中,滴加3%的磷酸乙醇溶液至pH为6,放置析出结晶,过滤,干燥,得到表羽扇豆碱磷酸盐;按常规口服液制法制成口服液。
实施例9
将表羽扇豆碱与辅料按重量比5:1混合,制成胶囊(辅料:乳糖10%+滑石粉1%+淀粉2%)或颗粒剂(辅料:水5%+淀粉5%+乳糖10%+滑石粉1%)或冲剂(辅料:乳糖10%+柠檬酸1%+氧化镁0.1%+薄荷油0.1%)。
实施例10
将表羽扇豆碱与辅料按重量比3:1混合,制成胶囊(辅料:乳糖10%+滑石粉1%+淀粉2%)或颗粒剂(辅料:水5%+淀粉5%+乳糖10%+滑石粉1%)或冲剂(辅料:乳糖10%+柠檬酸1%+氧化镁0.1%+薄荷油0.1%)。
实施例11
将46.6g表羽扇豆碱、600g淀粉、200g乳糖、3g薄荷醇、152g羧甲基淀粉钠混合,制成含片,作为功能食品。
试验例1表羽扇豆碱对AD小鼠模型Morris水迷宫探索实验的影响
实验动物:选择重量20-30克的C57BL/6雄性小鼠,(北京华阜康生物科技有限公司提供,许可证号:SCXK(京)2020-0004)。将小鼠分笼饲养,设置明暗周期12h/12h,温度20-22℃,食水自由(食物由北京汇霖泽古生物科技有限公司提供)。
实验药品:表羽扇豆碱(1-EPILUPININE)(由中国医学科学院药物研究所提取),表羽扇豆碱的化学纯度和结构分析如图1-3所示;盐酸多奈哌齐(5mg)购于卫材(中国)药业有限公司。
实验方法:将适应性饲养一周后的雄性小鼠分为空白对照组(CON)、模型组(MOD)、模型+阳性对照组(M_P)、模型+表羽扇豆碱低剂量组(M_ELP-L)和模型+表羽扇豆碱高剂量组(M_ELP-H)5组,每组10只。其中,M_P组腹腔注射多奈哌齐(溶剂为1%DMSO),注射剂量为5mg/kg;M_ELP-L组腹腔注射表羽扇豆碱(溶剂为1%DMSO),注射剂量为2.5mg/kg;M_ELP-H组腹腔注射表羽扇豆碱(溶剂为1%DMSO),注射剂量为5mg/kg,CON组和MOD组腹腔注射等量溶剂(1%DMSO)。所有小鼠每天给药1次,连续给药5天。
第6天开始进行Morris水迷宫实验。在行为学实验前1小时M_P组腹腔注射多奈哌齐(溶剂为1%DMSO),剂量为5mg/kg;M_ELP-L组腹腔注射表羽扇豆碱(溶剂为1%DMSO),剂量为2.5mg/kg;M_ELP-H组腹腔注射表羽扇豆碱(溶剂为1%DMSO),剂量为5mg/kg,CON组和MOD组腹腔注射等量溶剂(1%DMSO);在行为学实验前30分钟,所有处理组及模型组(M_P组、M_ELP-L组、M_ELP-H组、MOD组)均腹腔注射氢溴酸东莨菪碱(1mg/kg,溶剂为生理盐水),CON组注射等量生理盐水。
首先进行连续5天的Morris水迷宫隐藏平台实验,以探究小鼠的空间学习能力和空间记忆能力。隐藏平台实验要求将直径8cm的白色平台置于SW-III象限距离中心约15cm处,平台隐藏在水迷宫中液面1.5cm处,并保持平台位置在5天内没有任何变动。按照四个象限依次将每只小鼠面向池壁,轻轻放入水中,记录小鼠寻找到隐藏平台并所需要的时间,记作潜伏期(Latency,s),如果小鼠在1min内没有找到平台,则由实验人员将它引至平台上停留15s。每只小鼠每天按照四个象限进行一轮实验,每个象限入水间隔时间为20min,以保证小鼠有足够的休息时间。在进行最后一次隐藏平台的定位航行实验24h后,进行小鼠空间探索实验。保持对照物、水深、光照、温度、湿度等外界条件不变,只撤去水迷宫平台。将小鼠面向四个象限的水迷宫池壁,轻放入水中。记录4次小鼠60s内穿越平台位置的次数及潜伏期的总和。小鼠穿越平台位置的次数越多,潜伏期越短则意味着药物改善记忆力和空间学习能力越好。
统计方法:采用SPSS25.0软件进行统计学分析。符合正态分布的计量资料以均数±标准差(mean±SD)表示,非正态分布的计量资料以中位数(四分位距)形式表示。符合正态分布和方差齐性的多组间均数比较采用方差分析(one-way ANOVA),两组间比较采用最小显著差法(LSD);若不符合正态分布和方差齐性则进行非参数检验,多组间比较采用Kruskal-Wallis H秩和检验,两组间数据比较采用Mann-Whitney U检验。p<0.05为差异有统计学意义。统计结果如图4所示,其中,(A)为不同处理组小鼠穿越平台的次数,(B)为不同处理组小鼠在平台上的潜伏时间。
从图4可以看出,相比于空白对照组(CON),模型组(MOD)小鼠穿越平台位置的次数显著减少(p<0.001,图4(A)),且潜伏期增加(p<0.001,图4(B)),表明氢溴酸东莨菪碱(1mg/kg)可导致小鼠记忆力和空间学习能力下降。而模型+表羽扇豆碱高剂量组(M_ELP-H)相比于模型组(MOD)穿越平台位置的次数显著增加(p=0.007,图4(A)),且潜伏期缩短(p=0.009,图4(B)),表明5mg/kg的表羽扇豆碱可逆转氢溴酸东莨菪碱(1mg/kg)导致的小鼠记忆力和空间学习能力下降,且改善的效果不劣于阳性对照组使用的盐酸多奈哌齐。
试验例2小鼠旷场实验
Morris水迷宫结束后第二天进行小鼠旷场实验:在行为学实验前1小时M_P组腹腔注射多奈哌齐(溶剂为1%DMSO),剂量为5mg/kg,M_ELP-L组腹腔注射表羽扇豆碱(溶剂为1%DMSO),剂量为2.5mg/kg;M_ELP-H组腹腔注射表羽扇豆碱(溶剂为1%DMSO),剂量为5mg/kg,CON组和MOD组腹腔注射等量溶剂(1%DMSO);在行为学实验前30分钟,所有处理组及模型组(M_P组、M_ELP-L组、M_ELP-H组、MOD组)均腹腔注射氢溴酸东莨菪碱(1mg/kg,溶剂为生理盐水),CON组注射等量生理盐水。
实验开始时将小鼠放入旷场中,使用Any-maze软件记录10分钟内小鼠的活动情况,主要观察小鼠在中心区停留的时间和距离。实验完成后将小鼠取出,将旷场清理干净,喷洒酒精除去气味,再继续进行下一只小鼠实验。小鼠运动总距离可评估小鼠运动能力,运动总距离越长,活动能力越好。小鼠在中心区进入次数和距离与小鼠的焦虑情绪成负相关,停留时间越短,说明小鼠的焦虑情绪越严重。统计结果如图5所示,其中,(A)为不同处理组小鼠活动的总距离,(B)为不同处理组小鼠在中心区停留的时间,(C)为不同处理组小鼠穿越平台中心区的次数,(D)为不同处理组小鼠在中心区活动的距离。
结果显示:与MOD组相比,多奈哌齐处理后,小鼠运动总距离显著下降,而表羽扇豆碱两个剂量组无明显下降,即表羽扇豆碱处理不影响小鼠运动能力【图5(A)】。此外,与CON小鼠相比,AD小鼠造模后(MOD组)小鼠中心区进入次数、时间和距离均显著下降,这表明AD模型小鼠造模后可能存在焦虑样行为。多奈哌齐处理(M_P组)虽然可以改善模型小鼠记忆力但无法逆转这种焦虑样行为【图5(B)、(C)、(D)】。而表羽扇豆碱(2.5mg/kg)处理后小鼠中心区进入时间相比于造模组(MOD组)显著增加,同时与M_P组相比,表羽扇豆碱处理后小鼠中心区进入次数和距离显著增加,这意味着表羽扇豆碱可以缓解AD模型小鼠中的焦虑样行为【图5(B)、(C)、(D)】。
试验例3小鼠脑内炎症因子检测
行为学实验结束后立即处死小鼠,取脑,分离出前额叶,储存在-80℃冰箱内。
提取蛋白时将前额叶称重后剪碎,将剪碎的组织按每100mg组织加入500μL裂解液(按10μL蛋白酶抑制剂,990μL 1×Cell Lysis Buffer的比例配制)的比例混合,加入到玻璃匀浆器中,于冰上充分研磨。为了进一步裂解组织细胞,对匀浆液进行超声破碎。最后将匀浆液于5000×g离心10分钟,取上清,利用炎症因子抗体芯片进行检测,采用QAR-INF-1的数据分析软件来进行数据分析。检测分析结果如图6所示。
从图6可以看出,表羽扇豆碱高剂量和低剂量处理组小鼠的促炎因子GM-CSF、INF-g、IL-2、IL-23水平低于模型组小鼠,并且高剂量组与模型组间的差异具有显著性,说明表羽扇豆碱具有降低小鼠脑内炎症因子的作用。
由以上实施例可知,本发明提供了表羽扇豆碱及其衍生物在制备抗阿尔茨海默病的药物中的应用。表羽扇豆碱或其衍生物可用于预防或治疗阿尔茨海默病,改善患者认知功能障碍,提高患者记忆力,具有效果显著、用药量少、副作用小等优点。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
