一种含苯并呋喃咔唑叔丁基联苯胺类衍生物及其应用
文献发布时间:2023-06-19 10:10:17
技术领域
本发明涉及一种含苯并呋喃咔唑叔丁基联苯胺类衍生物及其应用,属于有机电致发光材料技术领域。
背景技术
1947美籍华裔教授邓青云在实验室中发现了有机发光二极体,也就是OLED,由此展开了对OLED的研究,1987年,邓青云教授和Van Slyke采用了超薄膜技术,用透明导电膜作阳极,Alq
OLED的特色在于其核心可以做得很薄,厚度为目前液晶的三分之一,加上OLED为全固态组件,抗震性好,能适应恶劣环境;OLED自发光的特性的让其几乎没有视角问题,与LCD技术相比,即使在大的角度观看,显示画面依然清晰可见,并且其响应时间为毫秒级,基本无滞后现象。此外,OLED的效率高,耗能较液晶略低还可以在不同材质的基板上制造,甚至能成制作成可弯曲的显示器,这些优点都使得OLED应用范围日渐增广。
现阶段OLED技术发展较为成熟,OLED产品已经渗透到我们身边各个角落,但是OLED也存在使用寿命不长、发光效率的等问题,解决这些问题成为当下研究的热点话题。
发明内容
本发明针对现有技术存在的不足,提供一种新型结构有机电致发光材料,本发明提供的化合物材料与商业应用中已知的化合物对比,应用在电致发光器件上表现出较好的热稳定性以及较长的使用寿命,并且在色纯度、发光效率、外部量子效率、驱动电压等方面都有明显的改善,具有广阔的市场前景。
本发明解决上述技术问题的技术方案如下:一种含苯并呋喃咔唑叔丁基联苯胺类衍生物,所述的含苯并呋喃咔唑叔丁基联苯胺类衍生物结构式如下式[I]:
其中,所述的R取代基为C6~C80之间的芳基或杂芳基及其衍生物。
优选的,所述的含苯并呋喃咔唑叔丁基联苯胺类衍生物选自如下结构式中的任意一种:
本发明还公开了所述含苯并呋喃咔唑叔丁基联苯胺类衍生物的应用,所述的含苯并呋喃咔唑叔丁基联苯胺类衍生物应用于有机电致发光器件。
进一步的,所述的含苯并呋喃咔唑叔丁基联苯胺类衍生物作为有机电致发光器件的空穴传输层材料。
进一步的,所述的含苯并呋喃咔唑叔丁基联苯胺类衍生物作为有机电致发光器件的发光层主体材料。
本发明的有益效果是:所述的含苯并呋喃咔唑叔丁基联苯胺类衍生物应用在有机电致发光器件上表现出较好的热稳定性以及较长的使用寿命,并且在色纯度、发光效率、外部量子效率、驱动电压等方面都有明显的改善,具有广阔的市场前景。
附图说明
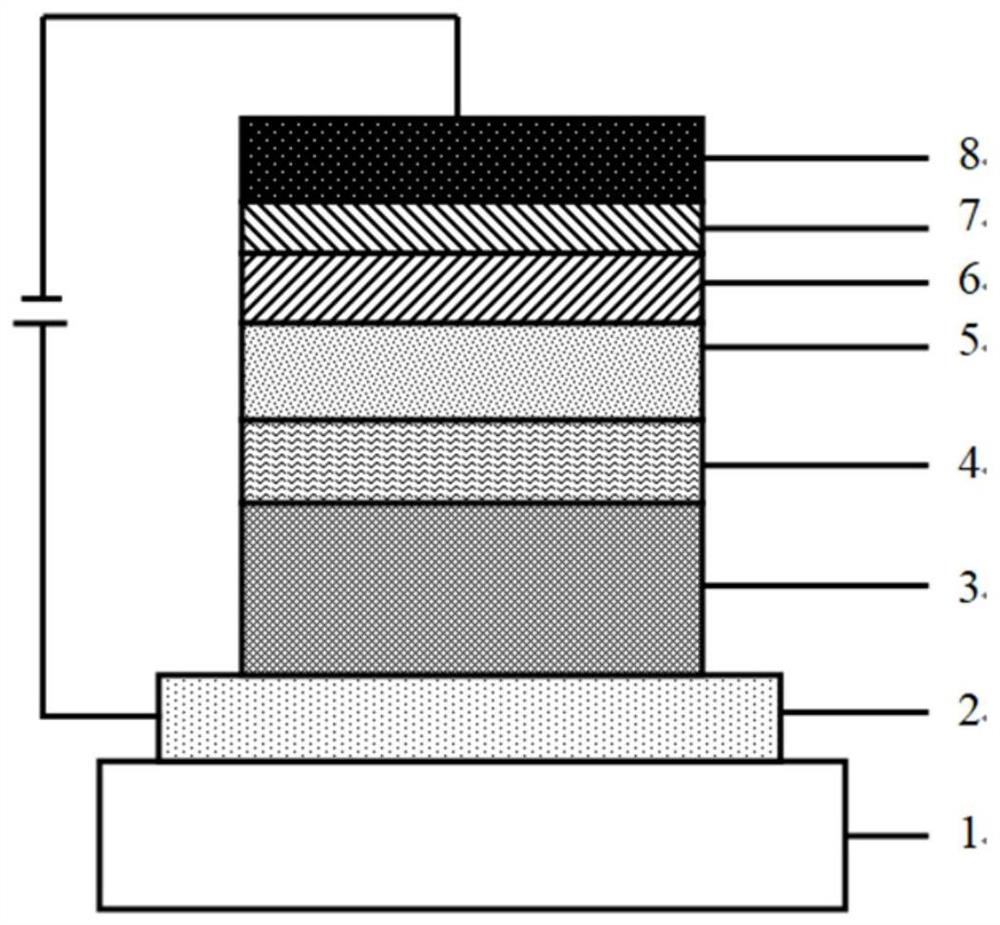
图1为实施例中的有机电致发光器件结构示意图;
图中,1透明基板,2透明电极层,3空穴注入层,4空穴传输层,5发光层,6电子传输层,7电子注入层,8阴极反射电极层。
具体实施方式
为使本发明的上述目的、特征和优点能够更加明显易懂,下面对本发明的具体实施方式做详细的说明。在下面的描述中阐述了很多具体细节以便于充分理解本发明。但是本发明能够以很多不同于在此描述的其它方式来实施,本领域技术人员可以在不违背本发明内涵的情况下做类似改进,因此本发明不受下面公开的具体实施例的限制。
除非另有定义,本文所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同。本文中在本发明的说明书中所使用的术语只是为了描述具体的实施方式的目的,不是旨在于限制本发明。
有机电致发光材料主体结构化合物E的合成方法包括以下步骤:
a:在惰性气体保护下向反应瓶中加入碳酸钾、纯化水、2-溴-3氟咔唑、甲苯,混合均匀后,加入四三苯基膦合钯,控温滴加邻甲氧基苯硼酸/四氢呋喃溶液,滴加毕保温5~30h反应完全,经水洗、过柱、重结晶得到化合物A,总收率:50~90%,GC:≥99.0%;
b:在惰性气体保护下向反应瓶中加入反应物A、二氯乙烷搅拌全溶后控温滴加三溴化硼,保温1~10h反应完全,经水解、水洗、过柱、重结晶得到化合物B,总收率:70~90%,GC:≥99.0%;
c:在惰性气体保护下一锅法向反应瓶中加入反应物B、DMF、碳酸铯,升温保温2~20h反应完全,经萃取水洗、过柱、重结晶得到化合物C,总收率:50~90%,GC:≥99.0%;
d:在惰性气体保护下一锅法向反应瓶中加入反应物C、2-溴-7氟-9,9-二甲基芴、DMF、碳酸铯,升温保温2~20h反应完全,经萃取水洗、过柱、重结晶得到化合物C,总收率:45~85%,HPLC:≥99.0%;
f:在惰性气体保护下向反应瓶中加入二甲苯、叔丁醇钠,搅拌均匀后加入醋酸钯/膦配体,控温滴加化合物D、4-叔丁基-2-联苯胺、二甲苯混合溶液,保温2~20h反应合格,经水洗、过柱、重结晶得到主体结构化合物E。
合成实施例1:化合物3的合成
具体合成路线:
在惰性气体保护下,称取9-溴蒽12.9g,主体化合物E 33.6g,甲苯400g,叔丁醇钠9.6g,醋酸钯0.2244g,膦配,0.879g于1L三口瓶中,升温至90~100℃保温10h,HPLC:93.2%,经水洗、过柱、甲苯重结晶得到31.8g类白色固体化合物3,总收率:75.1%,HPLC:99.9%,HPLC-MS:理论值:849.07,实测值:849.35。
H-NMR(400MHz,Chloroform-d):δ1.35(s,9H),1.72(s,6H,)6.37(d,1H),6.54(s,1H),6.61(d,1H),6.97(d,1H),7.08(d,2H),7.17(d,1H),7.25(dd,1H),7.32(dd,1H),7.33(dd,1H),7.34(s,1H),7.38(dd,5H),7.41(t,1H),7.51(dd,2H),7.59(d,1H),7.62(d,1H),7.66(dd,2H),7.77(s,1H),7.80(s,1H),7.87(d,1H),7.88(d,2H),7.89(d,1H),7.9(d,2H),7.94(d,1H),8.55(d,1H)
合成实施例2:化合物6的合成
具体合成路线:
在惰性气体保护下,称取3-溴联苯11.6g,主体化合物E 33.6g,甲苯400g,叔丁醇钠9.6g,醋酸钯0.2244g,膦配体:3 0.879g于1L三口瓶中,升温至90~100℃保温15h,HPLC:90.1%,经水洗、过柱、甲苯重结晶得到28.3g类白色固体化合物6,总收率:68.7%,HPLC:99.9%,HPLC-MS:理论值:825.05,实测值:825.20。
H-NMR(400MHz,Chloroform-d):δ1.35(s,9H),1.72(s,6H,)6.37(d,1H),6.54(s,1H),6.59(d,1H),6.61(d,1H),6.88(d,1H),6.89(s,1H),6.97(d,1H),7.08(d,2H),7.17(d,1H),7.25(dd,1H),7.32(dd,1H),7.33(dd,1H),7.34(s,1H),7.38(dd,1H),7.41(t,2H),7.44(dd,1H),7.51(dd,4H),7.59(d,1H),7.62(d,1H),7.66(dd,2H),7.77(s,1H),7.87(d,1H),7.89(d,1H),7.94(d,1H),8.55(d,1H)
合成实施例3:化合物11的合成
具体合成路线:
在惰性气体保护下,称取2-溴9,9-二甲基芴13.6g,主体化合物E 33.6g,甲苯400g,叔丁醇钠9.6g,醋酸钯0.2244g,C10104R:3 0.879g于1L三口瓶中,升温至90~100℃保温10h,HPLC:95.1%,经水洗、过柱、甲苯重结晶得到33.7g类白色固体化合物11,总收率:78.1%,HPLC:99.9%,HPLC-MS:理论值:865.11,实测值:865.51。
H-NMR(400MHz,Chloroform-d):δ1.35(s,9H),1.72(s,12H,)6.37(d,1H),6.54(s,1H),6.58(d,1H),6.75(s,1H),6.61(d,1H),6.97(d,1H),7.08(d,2H),7.17(d,1H),7.25(dd,1H),7.28(d,1H),7.32(dd,1H),7.33(dd,1H),7.34(s,1H),7.38(dd,2H),7.41(t,1H),7.51(dd,2H),7.55(d,1H),7.59(d,1H),7.62(d,2H),7.66(dd,2H),7.77(s,1H),7.87(d,2H),7.89(d,1H),7.94(d,1H),8.55(d,1H)
合成实施例4::化合物13的合成
具体合成路线:
在惰性气体保护下,称取2-([1,1'-联苯基]-3-yl)-4-氯-6-苯基-1,3,5-三嗪17.2g,主体化合物E 33.6g,甲苯400g,叔丁醇钠9.6g,醋酸钯0.2244g,膦配体0.879g于1L三口瓶中,升温至90~100℃保温10h,HPLC:87.3%,经水洗、过柱、甲苯重结晶得到34.3g类白色固体化合物13,总收率:70.0%,HPLC:99.9%,HPLC-MS:理论值:980.20,实测值:979.85。
H-NMR(400MHz,Chloroform-d):δ1.35(s,9H),1.72(s,6H,)6.37(d,1H),6.54(s,1H),6.61(d,1H),6.97(d,1H),7.08(d,2H),7.17(d,1H),7.25(dd,1H),7.32(dd,1H),7.33(dd,1H),7.34(s,1H),7.38(dd,1H),7.41(t,3H),7.48(d,H),7.51(dd,6H),7.52(d,2H),7.57(dd,1H),7.59(d,1H),7.62(d,1H),7.66(dd,2H),7.70(s,1H),7.77(s,1H),7.87d,1(H),7.89(d,1H),7.94(d,1H),8.24(d,1H),8.28(d,1H),8.55(d,1H)
本发明其它化合物的合成方法与具体实施方式案例相同或相近,不再进一步一一列举,本发明所列举的化合物FD-MS检测的m/Z值及理论值如下表1:
表1
应用对比例1
透明基板1采用玻璃基板,将涂满ITO的透明基板1(膜厚为200nm)放入洗涤剂中超声清洗30min,再用去离子水冲洗干净,再分别用异丙醇、甲苯、乙醇等溶剂超声清洗30min,然后在干净的环境下干燥,最后紫外线-臭氧洗涤以清除透明电极层2表面的有机残留物。
经过上述洗涤之后,对透明电极层2的阳极,利用真空蒸镀装置,蒸镀结构1(NBP)所示材料(钼坩锅、蒸镀速度0.1nm/s、真空度约5.0*10
在上述空穴传输材料蒸镀结束后,将结构3所示的材料和[2-(4,6-二氟苯基)吡啶-C2,N](吡啶)铱(Firpic)掺杂比例为94:6的重量比蒸镀至空穴传输层4之上(钼坩埚、蒸镀速度0.1nm/s,真空度约5.0*10
电子传输层6的制备是在上述发光层5之后,继续将电子传输层6材料结构4所示材料真空蒸镀至发光层5之上(钼坩埚、蒸镀速度0.1nm/s,真空度约5.0*10
电子注入层7是在电子传输层6上,通过真空蒸镀装置,制作膜厚为0.8nm的氟化锂(LiF)层。
阴极反射电极层8是通过真空蒸镀方式,在电子注入层7上,制备膜厚度为140nm的铝(Al)层。
如上所述地完成OLED发光器件后,用公知的驱动电路将阳极和阴极连接起来,测量器件的发光效率,发光光谱以及器件的电流-电压特性。
应用实施例1
应用实施例1与应用对比例1相比较,其不同之处在于OLED发光器件的空穴传输层4的材料改变为本发明合成实施例1制备得到的材料(化合物3)。
应用实施例2
应用实施例2与应用对比例1相比较,其不同之处在于OLED发光器件的空穴传输层4的材料改变为本发明合成实施例2制备得到的材料(化合物6)。
应用实施例3
应用实施例3与应用对比例1相比较,其不同之处在于OLED发光器件的空穴传输层4的材料改变为本发明合成实施例3制备得到的材料(化合物11)。
应用实施例4
应用实施例与应用对比例1相比较,其不同之处在于OLED发光器件的发光层5的材料改变为本发明合成实施例4制备得到的材料(化合物13)。
应用实施例1~4应用对比例1检测结果显示于表2中。
表2
根据表2数据对比得知,采用本发明化合物作为空穴传输材料或主体发光材料的OLED器件,其发光效率明显优于对比案例,且器件的色纯度、使用寿命、外部量子效率、驱动电压等性能均具有较大优势,利用本发明制备的化合物制备的OLED器件具有较大的商业价值和广阔的市场应用前景。
以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
- 一种含苯并呋喃咔唑叔丁基联苯胺类衍生物及其应用
- 一种含苯并呋喃咔唑叔丁基联苯胺类衍生物及其应用
