用于检测细胞外囊泡的试剂盒及其应用
文献发布时间:2023-06-19 10:57:17
技术领域
本发明涉及生物检测技术领域,具体而言,涉及一种用于检测细胞外囊泡的试剂盒及其应用。
背景技术
近年来,一些方法已被应用于外泌体液体活检,例如纳米粒子跟踪分析(NTA)、流式细胞术、免疫印迹、PCR分离、胶体金法和酶联免疫吸附法ELSA。由于在癌症早期外周血中肿瘤来源外泌体含量低,传统的定量检测方法灵敏度低。进一步,电化学发光、电化学免疫分析、荧光法和微流控传感器被用于肿瘤外泌体的定量。
Wang等人利用电化学方法开发了一种用于直接捕获外泌体的纳米四面体辅助传感器
这些方法可以检测出高灵敏度的外泌体,但是它们需要复杂的界面工程和复杂的纳米制造过程。Jin等人利用荧光法检测外泌体,使用氧化石墨烯纳米薄片吸附单链荧光配体,并形成淬灭纳米探针读出外泌体的存在
【1】Wang,S.;Zhang,L.;Wan,S.;Cansiz,S.;Cui,C.;Liu,Y.;Wu,Y.ACS Nano2017,11,3943-3949.
【2】Im,H.;Shao,H.;Park,Y.I.;Peterson,V.M.;Castro,C.M.;Weissleder,R.;Lee,H.Nat.Biotechnol.2014,32,490.
【3】Jin,D.;Yang,F.;Zhang,Y.;Liu,L.;Zhou,Y.;Wang,F.;Zhang,G.J.Anal.Chem.2018,90,14402-14411.
发明内容
为了实现本发明的上述目的,特采用以下技术方案:
本发明的第一方面涉及一种用于检测细胞外囊泡的试剂盒,包含AIE荧光染料及量子点;
所述AIE荧光染料含有能够与细胞外囊泡膜结合的配偶体;
所述量子点偶联有特异性地与所述细胞外囊泡表面的标志物结合的检测剂;
所述AIE荧光染料与所述量子点具有配对的发射峰与激发峰,能够实现荧光共振能量转移。
本发明的再一方面涉及一种检测细胞外囊泡的方法,包括:
a)将含有细胞外囊泡的组合物与AIE荧光染料、量子点共孵育;
b)在激发光下获取所述AIE荧光染料与所述量子点通过荧光共振能量转移所产生的目标信号;
其中,所述AIE荧光染料、所述量子点、所述细胞外囊泡为如上所定义的AIE荧光染料、量子点和细胞外囊泡。
本发明的有益效果为:
量子点可通过所述检测剂结合细胞外囊泡,该特定的AIE染料可以通过配偶体固定在细胞外囊泡膜表面。同时这两种荧光材料具有配对的发射与激发峰,能够实现荧光共振能量转移的供体-受体对。当且仅当二者同时标记上时,经过特定波长的光线激发能够观察到特定的信号,从而构建灵敏度高、信噪比高的荧光修饰体系,实现对外泌体的特异性检测。
附图说明
为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
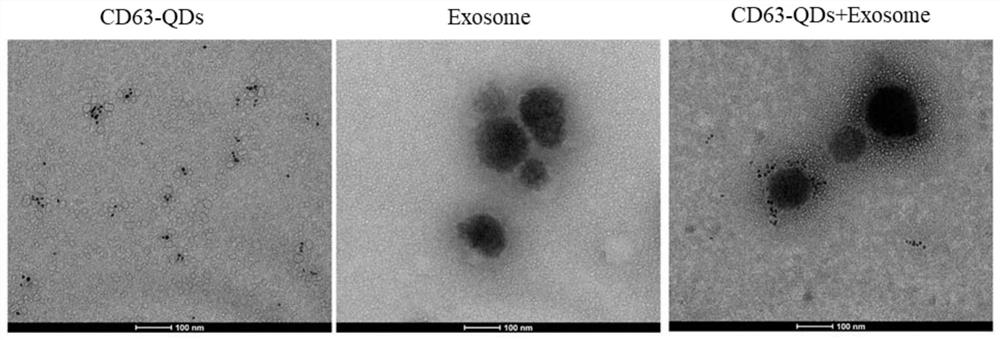
图1为本发明一个实施例中TEM表征结果:A)CD63-QDs(525nm);B)外泌体;C)CD63-QDs(525nm)标记的外泌体;
图2为本发明一个实施例中不同AIE荧光染料标记外泌体后,外泌体溶液的紫外-可见光吸收光谱和荧光发射光谱:A)AIE1;B)AIE2;
图3为本发明一个实施例中不同荧光染料标记外泌体的动力学:A)AIE1标记不同浓度外泌体溶液在1h内的荧光强度变化;B)AIE2标记不同浓度外泌体溶液在1h内的荧光强度变化;
图4为本发明一个实施例中不同荧光材料标记外泌体后,外泌体溶液在波长为380nm激光激发下的荧光光谱:A)AIE1与CD63-QDs(525nm)标记外泌体;B)AIE2与CD63-QDs(525nm)标记外泌体;C)AIE2与CD63-QDs(500nm)标记外泌体;D)AIE2与CD63-QDs(460nm)标记外泌体;
图5为本发明一个实施例中不同荧光材料标记外泌体后,外泌体溶液的荧光图像:A)CD63-QDs(525nm)标记的外泌体使用紫外光进行激发;B)AIE1标记的外泌体使用紫外光进行激发;C)AIE1标记的外泌体使用绿光进行激发;D)CD63-QDs(525nm)和AIE1共同标记的外泌体使用紫外光进行激发;
图6为本发明一个实施例中CD63-QDs(460nm)和AIE2共同标记不同浓度外泌体溶液后,紫外光激发下在600nm处发射的荧光强度随外泌体浓度的变化。
具体实施方式
现将详细地提供本发明实施方式的参考,其一个或多个实例描述于下文。提供每一实例作为解释而非限制本发明。实际上,对本领域技术人员而言,显而易见的是,可以对本发明进行多种修改和变化而不背离本发明的范围或精神。例如,作为一个实施方式的部分而说明或描述的特征可以用于另一实施方式中,来产生更进一步的实施方式。
因此,旨在本发明覆盖落入所附权利要求的范围及其等同范围中的此类修改和变化。本发明的其它对象、特征和方面公开于以下详细描述中或从中是显而易见的。本领域普通技术人员应理解本讨论仅是示例性实施方式的描述,而非意在限制本发明更广阔的方面。
本发明涉及一种用于检测细胞外囊泡的试剂盒,包含AIE荧光染料及量子点;
所述AIE荧光染料含有能够与细胞外囊泡膜结合的配偶体;
所述量子点偶联有特异性地与所述细胞外囊泡表面的标志物结合的检测剂;
所述AIE荧光染料与所述量子点具有配对的发射峰与激发峰,能够实现荧光共振能量转移。
量子点可通过所述检测剂结合细胞外囊泡,AIE荧光染料能够通过与细胞外囊泡膜结合的配偶体固定在细胞外囊泡的膜结构表面。同时这两种荧光材料具有配对的发射与激发峰,能够作为荧光共振能量转移的供体-受体对。当且仅当二者同时标记上时,经过特定波长的光线激发能够观察到特定的信号,从而构建灵敏度高、信噪比高的荧光修饰体系,实现对细胞外囊泡的特异性检测。
在本发明中,细胞胞外囊泡(Extracellular vesicles,EVs)被定义为20nm~1000nm大小的膜囊泡结构群体,其可包括外泌体(exosomes)、微泡(microvesicles)和凋亡小体(apoptosis body)等。
量子点三维尺寸通常在1nm~50nm范围内,例如2nm、3nm、4nm、5nm、6nm、7nm、8nm、9nm、10nm、15nm、20nm、30nm、40nm。量子点可选为元素周期表IV族、II-VI族、II-V族、III-V族、III-VI族、IV-VI族、I-III-VI族、II-IV-VI族、II-IV-V族的二元或多元半导体化合物或其中任意两种或以上的混合物。具体量子点材料的实例包括:IV族半导体化合物,例如包括单质Si、Ge和二元化合物SiC、SiGe;II-VI族半导体化合物,例如,其中二元化合物包括CdSe、CdTe、CdO、CdS、CdSe、ZnS、ZnSe、ZnTe、ZnO、HgO、HgS、HgSe、HgTe,三元化合物包括CdSeS、CdSeTe、CdSTe、CdZnS、CdZnSe、CdZnTe、CgHgS、CdHgSe、ZnSeS、ZnSeTe、ZnSTe、HgSeS、HgSeTe、HgSTe、HgZnS、HgSeSe,以及四元化合物包括CgHgSeS、CdHgSeTe、CgHgSTe、CdZnSeS、CdZnSeTe、HgZnSeTe、HgZnSTe、CdZnSTe、HgZnSeS;III-V族半导体化合物,例如,其中二元化合物包括AlN、AlP、AlAs、AlSb、GaN、GaP、GaAs、GaSb、InN、InP、InAs、InSb,三元化合物包括AlNP、AlNAs、AlNSb、AlPAs、AlPSb、GaNP、GaNAs、GaNSb、GaPAs、GaPSb、InNP、InNAs、InNSb、InPAs、InPSb,以及四元化合物包括GaAlNAs、GaAlNSb、GaAlPAs、GaInNP、GaInNAs、GaInNSb、GaInPAs、GaInPSb、InAlNP、InAlNAs、InAlNSb、InAlPAs、InAlPSb;IV-VI族半导体化合物,例如,其中二元化合物包括SnS、SnSe、SnTe、PbSe、PbS、PbTe,三元化合物包括SnSeS、SnSeTe、SnSTe、SnPbS、SnPbSe、SnPbTe、PbSTe、PbSeS、PbSeTe,以及四元化合物包括SnPbSSe、SnPbSeTe、SnPbSTe。
在一些实施方式中,量子点包含有II-VI族半导体材料,优选地,选自CdSe,CdS,CdTe,ZnO,ZnSe,ZnS,ZnTe,HgS,HgSe,HgTe,CdZnSe及其任意组合。在一个优选的实施例中,由于CdSe,CdS的合成相对成熟,而可以将此材料用作用于可见光的发光量子点。
在一些实施方式中,量子点包含有III-V族半导体材料,优选地,其选自InAs,InP,InN,GaN,InSb,InAsP,InGaAs,GaAs,GaP,GaSb,AlP,AlN,AlAs,AlSb,CdSeTe,ZnCdSe或其中任意两种或以上的混合物。
在一些实施方式中,量子点包含有IV-VI族半导体材料,优选地,选自PbSe,PbTe,PbS,PbSnTe,Tl2SnTe5或其中任意两种或以上的混合物。
在一些优选的实施例中,量子点为核壳结构。核与壳分别相同或不同地包括一种或多种半导体材料。
所述量子点的核可以选自上述的元素周期表IV族、II-VI族、II-V族、III-V族、III-VI族、IV-VI族、I-III-VI族、II-IV-VI族、II-IV-V族的二元或多元半导体化合物。具体的用于量子点核的实例包括,但不限于:ZnO、ZnS、ZnSe、ZnTe、CdO、CdS、CdSe、CdTe、MgS、MgSe、GaAs、GaN、GaP、GaSe、GaSb、HgO、HgS、HgSe、HgTe、InAs、InN、InSb、AlAs、AlN、AlP、AlSb、PbO、PbS、PbSe、PbTe、Ge、Si及其任意组合的合金或其中任意两种或以上的混合物。
所述量子点的壳包含有与核相同或不同的半导体材料。可用于壳的半导体材料包括元素周期表IV族、II-VI族、II-V族、III-V族、III-VI族、IV-VI族、I-III-VI族、II-IV-VI族、II-IV-V族二元或多元半导体化合物。具体的用于量子点核的实例包括但不限于ZnO、ZnS、ZnSe、ZnTe、CdO、CdS、CdSe、CdTe、MgS、MgSe、GaAs、GaN、GaP、GaSe、GaSb、HgO、HgS、HgSe、HgTe、InAs、InN、InSb、AlAs、AlN、AlP、AlSb、PbO、PbS、PbSe、PbTe、Ge、Si,及其任意组合的合金或其中任意两种或以上的混合物。
所述具有核壳结构的量子点中,其壳可以包括单层或多层的结构。所述壳可以包括一种或多种与核相同或不同的半导体材料。在一个优选的实施例中,壳具有约1~20层的厚度。在一个更为优选的实施例中,壳具有约5~10层的厚度。在某些实施例中,在量子点核的表面包含有两种或两种以上的壳。
合适的采用核壳结构的发光量子点的例子(但不限于)有:
红光:CdSe/CdS,CdSe/CdS/ZnS,CdSe/CdZnS等;
绿光:CdZnSe/CdZnS,CdSe/ZnS等;
蓝光:CdS/CdZnS,CdZnS/ZnS等。
量子点也可以为钙钛矿量子点和碳点。
优选的,所述量子点的激发波长选择:450-550nm;例如460nm、470nm、480nm、490nm、495nm、500nm、505nm、510nm、525nm、530nm。
AIE(Aggregation Induced Emission)荧光染料可以带有季铵、胆固醇、长烷基链、C18、四苯乙烯基中的至少一种。进一步的,所述AIE荧光染料可以选自TPE(四苯乙烯)或其衍生物、TPAFN【2,3-bis[4-(diphenylamino)phenyl]fumaronitrile】、TPETPAFN【2,3-bis(4-(phenyl(4-(1,2,2-triphenylvinyl)phenyl)amino)phenyl)fumaroni-trile】、TVP【(E)-4-(2-(5-(4-(diphenylamino)phenyl)thiophen-2-yl)vinyl)-1-methyl-pyridin-1-ium】、TTVP【(E)-4-(2-(5-(4-(diphenylamino)phenyl)-thiophen-2-yl)vinyl)-1-(3-(trimethylammonio)propyl)pyridine-1-ium】、Pent-TMP、TPA-OH、THBA。
所述AIE荧光染料能够通过与细胞外囊泡膜结合的配偶体固定在细胞外囊泡的膜表面并发光。可以理解,所述配偶体可与细胞外囊泡膜进行特异或非特异性的结合而固定,固定的方式可以是共价键或者亲和作用等。在一些实施方式中,所述AIE荧光染料带有季铵、胆固醇、长烷基链、C18、四苯乙烯基中的至少一种,荧光染料带有的上述结构能够与细胞膜上的脂质区域融合,插入细胞膜内发光;在一些实施例中,所述AIE荧光染料标记能够与细胞外囊泡膜结合的配偶体,所述配偶体含有脂质、配体、受体、抗体、抗原、互补序列、适配体或凝集素,所述配偶体与细胞膜成分或表面标志物融合和/或结合插入到细胞膜中;在一些优选的实施方式中,所述配偶体是与细胞膜结构具有相容性的物质,能在与细胞外囊泡共孵育时自发或在诱导条件(如温度变化,搅拌,细胞破膜剂等)下插入到细胞外囊泡中。在一些实施方式中,其为脂质,所述脂质选自磷脂酰乙醇胺(PE)、胆固醇(CHOL)、二酰基甘油(DAG)和脂肪酸(FA)。在一些实施方式中所述脂质选自DSPE、DPPE、DLPE、DMPE等,优选DSPE。在优选的实施方式中,所述细胞外囊泡膜结合的配偶体选自脂质聚乙二醇衍生物,例如DSPE-PEG。
在一些实施方式中,所述标志物为蛋白(例如受体或配体)和/或核酸。在一些实施方式中,所述标志物选自CD63、CD9、CD81、HSP70、Tsg101、EpCam、flotillin、Syntenin、Alix、HSP90、LAMP2B、LMP1、ADAM10、nicastrin、AChE、AQP2、RPL5以及a-1AT中的至少一种;优选的,所述标志物选自更为常见的蛋白,四次跨膜蛋白(CD9、CD63、CD81)、热休克蛋白70(heat shock protein70,HSP70)、肿瘤易感基因101蛋白(tumor susceptibility gene101,TSG101)、ALG-2相互作用蛋白X(ALG-2-interacting protein X,Alix)等可作为细胞外囊泡的标记物。
在本发明中,特异性地与所述细胞外囊泡表面的标志蛋白结合的检测剂是标志蛋白的配体或受体(如果存在的话)、标志蛋白的凝集素、标志蛋白的适配体或标志蛋白的抗体。特异性的结合剂对其相应的靶分子优选具有至少10
“抗体”此用语包括多克隆抗体及单克隆抗体,“抗体片段”此用语包括这些抗体的抗原化合物结合片段,包括Fab、F(ab’)
在一些实施方式中,所述检测剂选自所述标志物的配体或受体、抗体、抗原、互补序列、适配体或凝集素。
在一些实施方式中,所述量子点与所述细胞外囊泡表面的标志蛋白结合的抗体的氨基偶联。在一些实施方式中,量子点表面修饰有羧基。在一些实施方式中,偶联通过EDC催化进行。
根据本发明的再一方面,还涉及一种检测细胞外囊泡的方法,包括:
a)将含有细胞外囊泡的组合物与AIE荧光染料、量子点共孵育;
b)在激发光下获取所述AIE荧光染料与所述量子点通过荧光共振能量转移所产生的目标信号;
其中,所述AIE荧光染料、所述量子点、所述细胞外囊泡为如上所定义的AIE荧光染料、量子点和细胞外囊泡。
在一些实施方式中,所述激发光为紫外光;进一步的,其波长为370nm~390nm,例如380nm。
在一些实施方式中,所述组合物中的细胞外囊泡预先固定于固相载体上,再与AIE荧光染料、量子点共孵育。
由于细胞胞外囊泡存在于原核生物和真核生物中,并且跨越所有的进化,所以本发明可以使用得自原核生物、真核生物、细菌、真菌、酵母、无脊椎动物、脊椎动物、爬行动物、鱼、昆虫、植物或动物(包括哺乳动物,例如啮齿动物和灵长目动物)的任何组合物。例如组合物来源可以为鸡、小鼠、大鼠、兔、山羊、羔羊、绵羊、马、猪、牛(胎牛)和人类。组合物的优选的实例为鼠、牛或人类,其用于制备分别为鼠、牛或人类的细胞胞外囊泡;更优选的,所述组合物来源于人类。
所述方法包括诊断及非诊断目的。
在一些实施方式中,所述组合物衍生自肿瘤细胞或病原体感染的细胞。
示例性肿瘤包括但不限于肺癌、乳腺癌、卵巢癌、胃癌、胰腺癌、喉癌、食道癌、睾丸癌、肝癌、腮腺癌、胆道癌、结肠癌、直肠癌、子宫颈癌、子宫癌、子宫内膜癌、肾癌、膀胱癌、前列腺癌、甲状腺癌、鳞状细胞癌、腺癌、小细胞癌、黑素瘤、神经胶质瘤、胶质母细胞瘤、成神经细胞瘤等。从这些实例中,通常使用得自黑素瘤、结肠直肠癌、肺癌、胰腺癌、肝癌、前列腺癌、乳腺癌和卵巢癌的样品。
示例性的病原体包括但不限于病毒、细菌、寄生虫、真菌。
病原体的概念还可以理解为具有致病性/激活免疫功能的有机大分子,有机小分子,或无机分子。
在一些实施方式中,所述组合物选自细胞培养物上清液、全血、血清、血浆、腹水、脑脊液、骨髓穿刺液、支气管肺泡洗液、胸腔液、尿、精液、卵泡液、宫腔液、胆汁、羊水、阴道分泌物、唾液、痰或者从生物组织样品得到的澄清的裂解液。
所述组合物可以是新鲜的或事先冷冻的,然后解冻。
在一些实施方式中,所述组合物在基本上不破坏EVs形态学特征或功能特征或者细胞表面抗原的条件下被分离;
上述,EVs在所述组合物中应该保持了它们的原始抗原图谱,这样它们是“抗原性完整的”,由此被检测的EVs才能用以分析其浓度/粒径。
EVs的富集方式可通过密度梯度离心、超速离心、超滤、聚乙二醇沉淀中的任一种方法进行。
在一些实施方式中,所述组合物中EVs的浓度为10
在一些实施方式中,为减少细胞外囊泡中蛋白的降解,所述孵育在低温下进行,例如2℃~10℃,例如4℃、6℃、8℃。
下面将结合实施例对本发明的实施方案进行详细描述。
实施例
在本实施例中,AIE1为TPETPAFN,激发波长为525nm,AIE2为TVP,激发波长为460nm;量子点采用的是为ZnCdS/ZnS量子点,发射波长分别为460nm、500nm以及525nm。
1.CD63抗体与量子点(QDs)的偶联
本发明所使用的QDs表面富含羧基官能团,在在活化剂1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(EDC)作用下,与抗体的氨基反应形成稳定的酰胺键,从而将CD63抗体共价固定在量子点表面。
具体方法为:
首先在硼酸盐缓冲液溶液中加入EDC活化QDs的羧基1h,然后将量子点重悬于MES缓冲液中并加入抗体,室温反应2h,其中QDs:EDC:-NH
2.外泌体的标记
通过超离法提取HepG2细胞上清外泌体。取30μL外泌体溶液,加入1μL 5μg/mLAIE1或者3μg/mL AIE2溶液和1μL CD63-QDs溶液。在4℃混匀孵育过夜。
通过透射电镜观察量子点和AIE对外泌体的标记情况,结果如图1所示,可见CD63-QDs成功标记在了外泌体上。
通过酶标仪检测AIE对外泌体的荧光标记清况,结果见图2和图3,可见AIE1和AIE2均能很迅速地标记上外泌体,且荧光强度在1h内具有很好地稳定性。
通过酶标仪监测荧光能量转移情况结果见图4,不同荧光材料标记外泌体后,外泌体溶液在紫外激发下的荧光光谱不同。
使用荧光倒置显微镜观察荧光图像的变化情况如图5所示,CD63-QDs(525nm)标记外泌体后,在紫外光激发下,有绿色荧光信号点,AIE1标记的外泌体在紫外光下无荧光信号,而在绿色激光激发下发出红色荧光信号,当CD63-QDs(525nm)和AIE1共同标记时,紫外光激发下可以看到红色荧光信号与绿色荧光信号共同存在(图D中箭头所示点为红色荧光信号)。这个结果表明CD63-QDs(525nm)与AIE1的共同标记可以区分假阳性标记,同时放大了荧光信号。通过酶标仪测定不同浓度外泌体溶液在CD63-QDs(460nm)和AIE2共同标记,使用紫外光激发在600nm处的荧光强度变化情况如图6所示。
以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
- 一种分离细胞外囊泡的方法和检测细胞外囊泡的试剂盒
- 一种用于分离细胞外囊泡的离心管和提取细胞外囊泡的试剂盒
