植物性多糖作为佐剂在制备自身性免疫疾病药物中的应用
文献发布时间:2023-06-19 10:05:17
技术领域
本发明涉及自身性免疫疾病治疗技术领域,具体涉及一种植物性多糖作为佐剂在制备自身性免疫疾病药物中的应用。
背景技术
自身性免疫疾病主要包括类风湿性关节炎、自身免疫性糖尿病(也称为1型糖尿病)、自身免疫性脑脊髓炎(多发性硬化)和红斑狼疮。其具体发病原因至今不明,但通常是机体对于自身正常组织有非正常的免疫排斥反应,即免疫不耐受,引发的。如果可以通过一定手段使机体对这些自身抗原产生免疫耐受作用,避免自抗体的生成及T细胞对这些抗原的识别及攻击,就可以纠正免疫细胞对自体含抗原组织的攻击。
1型糖尿病是自身免疫疾病中的一种,是由于自身的免疫细胞在自身发育过程中阴性选择时发生障碍,导致自身抗原具有活化自体T细胞的作用,这些被活化的T细胞进而可对自体特异性抗原进行攻击。现被证明有可能触发1型糖尿病的多种自身抗原包括:β细胞释放的胰岛素或者前胰岛素、谷氨酸脱羧酶、一种B细胞特异性的蛋白脱羧酶、热休克蛋白65的P227段多肽、锌转运体Znt8等。1型糖尿病正是一种由自体活化的T细胞对体内分泌胰岛素的胰岛β细胞攻击而导致的自身免疫性疾病。现在治疗1型糖尿病的主要手段是注射外源性胰岛素,然而该方法只能够补充胰岛素的不足,却无法更正体内免疫细胞对胰岛细胞的破坏,因而不能根治或预防1型糖尿病的发生。另外,糖尿病人伤口本来不易愈合,频繁注射胰岛素和血糖监测对机体造成严重损伤,而且胰岛素用量难以精确调整,很容易造成低血糖的风险,且仍不能完全避免血糖升高造成的大血管和微血管并发症的发生。
免疫佐剂作为疫苗的重要组成部分,尤其是针对免疫原性较弱的抗原疫苗,其研究需求尤其迫切。佐剂不仅可以增强免疫反应的强度和速度以提高疫苗效率,减少抗原用量,降低疫苗生产成本,还可以使临床疫苗治疗过程简单化,降低患者的治疗费用。目前,将抗原与佐剂同时应用时新型疫苗的发展趋势,例如刚刚被美国FDA(Food and DrugAdministration)批转的Dynavax公司生产的HEPLISAV-B疫苗是将乙肝表面抗原与Dynavax专有佐剂Toll样受体9(TLR 9)激动剂相结合制成的承认乙肝疫苗。葛兰素史克公司的宫颈癌疫苗Cervarix和乙型肝炎疫苗Fendrix则是用新型佐剂系统AS04(含MPL的铝佐剂)制备而成。已有多项研究表明将抗原与多种佐剂及组合佐剂(如免疫刺激复合物ISCOMs、佐剂系统AS或三联佐剂组合体等)联合应用可以大大提高疫苗的疗效,具有免疫协同效应。因此,研究一种用于自身性免疫疾病的佐剂尤为关键。
发明内容
本发明的目的在于提供一种植物性多糖作为佐剂在制备自身性免疫疾病药物中的应用,以解决针对自身性免疫疾病佐剂匮乏的问题。
为了实现本发明的上述目的,特采用以下技术方案:
本发明第一方面提供一种植物性多糖作为佐剂在制备自身性免疫疾病药物中的应用。
研究表明,植物性多糖能够辅助自身性免疫疾病抗原功能,能够起到免疫佐剂的作用,有效降低机体内自抗体滴度,从而更有效地辅助抗原激活体内调节性T细胞增殖及其功能,诱导免疫耐受,防止和延缓自身性免疫疾病的发病。
优选地,所述自身性免疫疾病包括1型糖尿病、类风湿性关节炎、自身免疫性脑脊髓炎和红斑狼疮。
优选地,所述植物性多糖选自菊糖、葡甘露聚糖和β-1,3-D-葡聚糖中的任意一种。
本发明第二方面提供一种自身性免疫疾病的疫苗佐剂,所述疫苗佐剂包括上述植物性多糖。
优选地,所述疫苗佐剂中植物性多糖的质量浓度为0.5%~2.8%;所述植物性多糖的粒径为200~700nm。
本发明第三方面提供一种自身性免疫疾病的疫苗,所述疫苗包括包括上述植物性多糖或上述疫苗佐剂,以及抗原。
优选地,所述疫苗中植物性多糖的质量浓度为0.5%~2.8%;所述植物性多糖的粒径为200~700nm。
优选地,所述抗原的质量浓度为0.5%~5%。
优选地,所述抗原为胰岛素抗原或髓少突胶质细胞蛋白。
本发明第四方面提供一种上述疫苗的制备方法,所述制备方法包括如下步骤:
(a)将植物性多糖和抗原溶解于二甲基亚砜中,得到混合液;
(b)将混合液置于截留分子量为3000~5000的透析袋中进行透析,得到纳米微粒;
(c)将纳米微粒置于PBS缓冲液中配制相应浓度,即得所述疫苗。
与现有技术相比,本发明的有益效果至少包括:
本发明中植物性多糖能够辅助自身性免疫疾病抗原功能,能够起到免疫佐剂的作用,有效降低机体内自抗体滴度,从而更有效地辅助抗原激活体内调节性T细胞增殖及其功能,诱导免疫耐受,防止和延缓自身性免疫疾病的发病。
附图说明
为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍。在所有附图中,类似的元件或部分一般由类似的附图标记标识。附图中,各元件或部分并不一定按照实际的比例绘制。
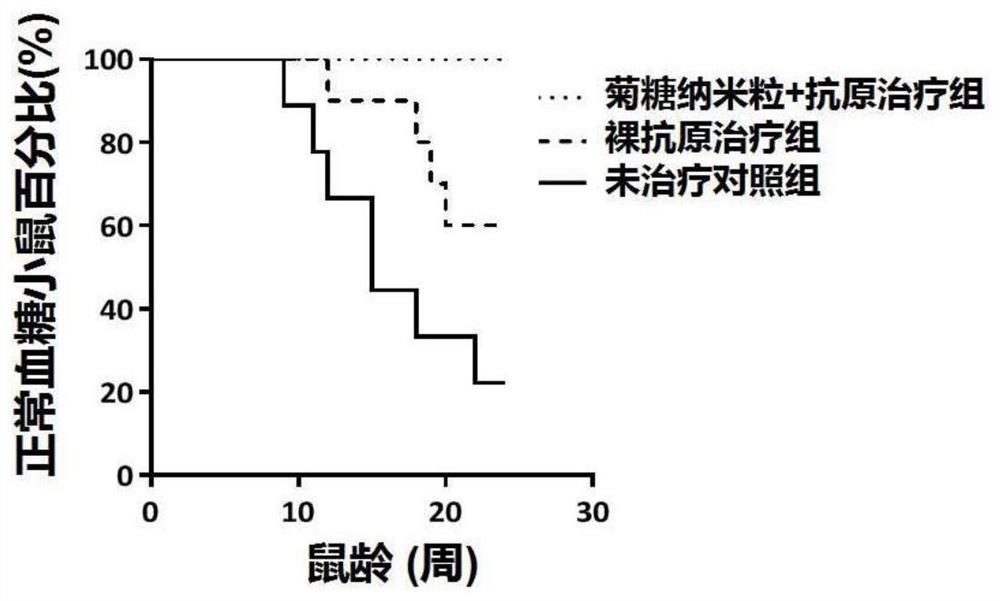
图1为本发明实验例1中不同治疗组24周龄内糖尿病发病比例;
图2为本发明实验例1中不同治疗组小鼠血清中自体抗胰岛素抗体水平;
图3为本发明实验例1中不同治疗组小鼠血清中胰岛素水平;
图4为本发明实验例2中不同治疗组24周龄内糖尿病发病比例。
具体实施方式
下面将结合实施例对本发明技术方案的实施例进行详细的描述。以下实施例仅用于更加清楚地说明本发明的技术方案,因此只作为示例,而不能以此来限制本发明的保护范围。
需要注意的是,除非另有说明,本申请使用的技术术语或者科学术语应当为本发明所属领域技术人员所理解的通常意义。
实施例1
一、自身性免疫疾病的疫苗
上述自身性免疫疾病的疫苗包括菊糖和胰岛素抗原,该疫苗中菊糖的质量浓度为2%,菊糖的粒径为250nm;
该疫苗中胰岛素抗原的质量浓度为2%。
二、制备方法
上述自身性免疫疾病的疫苗的制备方法,该制备方法包括如下步骤:
(a)将100mg菊糖和100mg胰岛素抗原溶解于10ml二甲基亚砜中,得到混合液;
(b)将混合液置于截留分子量为5000的透析袋中,并使用2000ml无菌水在室温下透析40h,透析过程中每小时进行换液,得到纳米微粒;
(c)将纳米微粒置于PBS缓冲液中配制相应浓度,即得上述自身性免疫疾病的疫苗。
实施例2
一、自身性免疫疾病的疫苗
上述自身性免疫疾病的疫苗包括葡甘露聚糖和胰岛素抗原,该疫苗中葡甘露聚糖的质量浓度为1%,葡甘露聚糖的粒径为200~700nm;
该疫苗中胰岛素抗原的质量浓度为4%。
二、制备方法
上述自身性免疫疾病的疫苗的制备方法,该制备方法包括如下步骤:
(a)将20mg葡甘露聚糖和80mg胰岛素抗原溶解于10ml二甲基亚砜中,得到混合液;
(b)将混合液置于截留分子量为5000的透析袋中,并使用2000ml无菌水在室温下透析40h,透析过程中每小时进行换液,得到纳米微粒;
(c)将纳米微粒置于PBS缓冲液中配制相应浓度,即得上述自身性免疫疾病的疫苗。
实施例3
一、自身性免疫疾病的疫苗
上述自身性免疫疾病的疫苗包括β-1,3-D-葡聚糖和胰岛素抗原,该疫苗中β-1,3-D-葡聚糖的质量浓度为2.5%,β-1,3-D-葡聚糖的粒径为200~700nm;
该疫苗中胰岛素抗原的质量浓度为1%。
二、制备方法
上述自身性免疫疾病的疫苗的制备方法,该制备方法包括如下步骤:
(a)将50mgβ-1,3-D-葡聚糖和20mg胰岛素抗原溶解于5ml二甲基亚砜中,得到混合液;
(b)将混合液置于截留分子量为3000的透析袋中,并使用1000ml无菌水在室温下透析30h,透析过程中每小时进行换液,得到纳米微粒;
(c)将纳米微粒置于PBS缓冲液中配制相应浓度,即得上述自身性免疫疾病的疫苗。
实施例4
一、自身性免疫疾病的疫苗
上述自身性免疫疾病的疫苗包括菊糖和髓少突胶质细胞蛋白,该疫苗中菊糖的质量浓度为2%,菊糖的粒径为250nm;
该疫苗中髓少突胶质细胞蛋白的质量浓度为2%。
二、制备方法
上述自身性免疫疾病的疫苗的制备方法,该制备方法包括如下步骤:
(a)将100mg菊糖和100mg髓少突胶质细胞蛋白原溶解于10ml二甲基亚砜中,得到混合液;
(b)将混合液置于截留分子量为3000的透析袋中,并使用2000ml无菌水在室温下透析40h,透析过程中每小时进行换液,得到纳米微粒;
(c)将纳米微粒置于PBS缓冲液中配制相应浓度,即得上述自身性免疫疾病的疫苗。
实施例5
一、自身性免疫疾病的疫苗
上述自身性免疫疾病的疫苗包括菊糖和胰岛素抗原,该疫苗中菊糖的质量浓度为1%,菊糖的粒径为250nm;
该疫苗中胰岛素抗原的质量浓度为2%。
二、制备方法
上述自身性免疫疾病的疫苗的制备方法,该制备方法包括如下步骤:
(a)将50mg菊糖和100mg胰岛素抗原原溶解于10ml二甲基亚砜中,得到混合液;
(b)将混合液置于截留分子量为3000的透析袋中,并使用2000ml无菌水在室温下透析40h,透析过程中每小时进行换液,得到纳米微粒;
(c)将纳米微粒置于PBS缓冲液中配制相应浓度,即得上述自身性免疫疾病的疫苗。
对照例1
本对照例公开了一种自身性免疫疾病的疫苗,该疫苗与实施例1中的疫苗基本相同,区别仅在于将菊糖替换壳聚糖;
对照例2
本对照例公开了一种自身性免疫疾病的疫苗,该疫苗的制备方法包括如下步骤:
(a)将100mg胰岛素抗原溶解于10ml二甲基亚砜中,得到混合液;
(b)将混合液置于截留分子量为5000的透析袋中,并使用2000ml无菌水在室温下透析40h,透析过程中每小时进行换液,得到纳米微粒;
(c)将纳米微粒置于PBS缓冲液中,配制得到胰岛素抗原质量浓度为2%的自身性免疫疾病的疫苗。
实验例1
取离乳雌性non-obese diabetic(NOD)小鼠,经体重、血糖测量正常后随机分为3组,每组20只,第1组采用实施例1中制备得到的疫苗进行灌胃治疗;第2组采用对照例2中制得的疫苗进行灌胃治疗;第3组为生理盐水灌胃对照组;在小鼠4-8周龄时,每周灌胃两次,每次剂量为每只鼠400μg抗原;干预时间共5周,干预后,小鼠从9周龄到24周龄,每周测量体重,尾静脉测量血糖。
统计24周龄内不同组中糖尿病发病比例,统计结果如图1所示;
由图1可知,菊糖纳米粒+抗原治疗组(即采用实施例1疫苗治疗组)小鼠在24周龄时,糖尿病发病率为0,明显优于裸抗原治疗组(即采用对照例2疫苗治疗组),其发病率达40%,P<0.01;未治疗对照组小鼠则在9周龄开始就陆续有小鼠出现血糖升高情况,24周时发病率高达80%。因此,采用菊糖纳米粒+抗原治疗组(即实施例1疫苗)小鼠1型糖尿病发病显著改善,明显优于裸抗原及未治疗对照组。
对各组小鼠血清中的自体抗胰岛素抗体水平进行检测:
于15周龄,通过眼眶取血对所有小鼠进行血样采集,凝血后收集小鼠血清,使用胰岛素自抗体(Insulin autoantigen IAA)ELISA检测试剂盒(Cloud-Clone Corp.),按照试剂盒步骤进行比色检测,检测结果如图2所示;
由图2可知:
菊糖纳米粒+抗原治疗组的小鼠血清中自体抗胰岛素抗体水平显著低于裸抗原治疗组以及未治疗对照组;而自体抗原抗体是自身性免疫疾病发病及病情的指症之一,其抗体滴度的降低则直接说明治疗方法对于自身性免疫细胞功能及抗体产生的抑制作用;可见,说明了菊糖的抗原佐剂作用。
于15周龄,通过眼眶取血对所有小鼠进行血样采集,凝血后收集小鼠血清,使用胰岛素ELISA检测试剂盒(Merck-Millipore EZRMI-13K Rat/Mouse Insulin ELISA Kit.),按照试剂盒步骤进行比色检测,检测结果如图3所示;
由图3可知:
菊糖纳米粒+抗原治疗组的小鼠血清中胰岛素水平比裸抗原治疗组以及未治疗对照组显著升高;血清胰岛素含量是检测糖尿病疾病进程的指标之一,在1型糖尿病胰岛被自身免疫系统攻击破坏的情况下,胰岛分泌胰岛素能力也会随之降低导致循环系统中胰岛素水平低下;因此,菊糖纳米粒+抗原治疗组小鼠血清中胰岛素水平稳定也能够说明书本申请疫苗能够稳定糖尿病病情。
实验例2
取离乳雌性non-obese diabetic(NOD)小鼠,经体重、血糖测量正常后随机分为4组,每组20只,第1组采用对照例1中制备得到的疫苗进行灌胃治疗;第2组采用对照例2中制得的疫苗进行灌胃治疗;第3组为生理盐水灌胃对照组;第4组为灌胃壳聚糖组,在小鼠4-8周龄时,每周灌胃两次,每次剂量为每只鼠400μg抗原;第4组的壳聚糖每次灌胃量为第1组灌胃疫苗中对应的壳聚糖含量;干预时间共5周,干预后,小鼠从9周龄到24周龄,每周测量体重,尾静脉测量血糖。
统计24周龄内不同组中糖尿病发病比例,统计结果如图4所示;
由图4可知:
壳聚糖包裹抗原组小鼠糖尿病发病率与裸抗原组相同,且无抗原的壳聚糖纳米粒治疗组小鼠发病率也高于裸抗原以及壳聚糖+裸抗原治疗组,说明壳聚糖在胰岛素抗原诱导免疫耐受延迟糖尿病发病中不具有明显作用。
最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围,其均应涵盖在本发明的权利要求和说明书的范围当中。
- 植物性多糖作为佐剂在制备自身性免疫疾病药物中的应用
- 一种活性多糖在制备增强免疫力药物、药物组合物或保健食品中的应用
