一种间歇性曝气式地下水氨氮、有机污染生物的修复方法
文献发布时间:2023-06-19 11:34:14
技术领域
本发明涉及一种修复方法,特别涉及一种间歇性曝气式地下水氨氮、有机污染生物的修复方法。
背景技术
2019年《中国生态环境状况公报》显示,中国地下水质量状况总体不容乐观,全国1万多个国家级地下水水质监测点位中,劣五类水体占比涨到18.8%,污染超标因子包括氟化物、氨氮、有机物等。大量研究表明,在一些典型污染场地,如垃圾填埋场、工矿企业污染场地,其地下水中氨氮、有机物已成为较普遍的特征污染物。受氨氮、有机污染的地下水作为饮用水源时,水处理系统会产生有害消毒副产物和不良气味,配水系统易出现硝化菌再生的问题;地下水中氨氮经过含水层氧化反应带后,可被转化为硝酸盐,当其被婴幼儿摄入后,会引起高铁血红蛋白症,即蓝婴综合症;有机污染更容易引起人体消化系统癌变。
近年来,厌氧微生物在地下环境中氨氮、有机污染物的自然衰减过程扮演的重要角色,引起了研究人员的广泛关注。含水层的一些氧化还原反应带中,微生物能够在厌氧或缺氧条件下利用硝酸盐、硫酸盐、或Fe(Ⅲ)(Mn)氧化物作为电子受体,以有机物为电子供体进行自身新陈代谢。在被污染含水层的一些厌氧区域,Fe(III)还原菌对苯、及其它芳香族化合物的自然降解能力非常显著,地杆菌在这一过程扮演着非常重要的角色。厌氧铁氨氧化是指在厌氧条件下,氨氧化过程耦合Fe(III)生物还原过程,这一过程能够将氨氮转化为氮气、亚硝酸盐或硝酸盐。厌氧铁氨氧化可在不同环境下发生,且不同条件下NH
由于一步脱氮对溶解氧等反应条件控制较为苛刻,目前还没有一种合适的反应条件能实现NH
发明内容
本发明实施例的目的是针对上述现有技术的缺陷,提供一种能够解决厌氧铁氨氧化产生的亚硝酸盐难题,实现地下水中氨氮和有机物的高效协同去除的间歇性曝气式地下水氨氮、有机污染生物的修复方法。
为了实现上述目的本发明采取的技术方案是:
一种间歇性曝气式地下水氨氮、有机污染生物的修复方法,包括以下步骤:
将源于淹水稻田土的原生土著微生物,经过室内驯化、筛选和培养,得到复合菌株的菌液,所述菌液里含有驯化培养的复合菌株,所述复合菌株为Fe(III)还原菌、反硝化菌和铁氨氧化菌,再通过挂膜的方式,将菌液里驯化培养后的复合菌株负载至颗粒粒径2-4mmFe(III)铁氧化矿物表面,形成生物膜,得到修复功能材料,将修复功能材料加入至受污染的地下水中;
在厌氧环境中,在经驯化培养的Fe(III)还原菌和铁氨氧化菌的作用下,将地下水中的铁氧化矿物表面Fe(III)转化为Fe(II),NH
通过间歇性好氧曝气,Fe(II)曝气氧化为Fe(III)、NO
在厌氧环境中,并在经驯化培养的反硝化菌和铁还原菌的作用下,使Fe(III)转化为Fe(II),NO
所述复合菌株的菌液体积与Fe(III)铁氧化矿物的重量比为8-12mL:1g。
所述驯化、筛选和培养所述复合菌株的菌液的步骤为:
厌氧处理去离子水:将去离子水置于厌氧反应瓶中,通入氮气,进行厌氧处理;
加入稻田土后恒温震荡:称取新鲜稻田土,加入到厌氧处理后的去离子水中,通入氮气,盖紧瓶塞,以100-150rpm的转速、20-25℃下恒温震荡1.5-2.5h;
所述去离子水与稻田土的用量比为40-60mL:2-4g;
装瓶:取震荡后的上层菌液,转移至装有培养基和Fe(III)铁氧化矿物颗粒的厌氧反应瓶中;
所述上层菌液、培养基和Fe(III)铁氧化矿物颗粒的体积质量比为:2mL:15-25mL:8-12g;
培养:给厌氧反应瓶通入3-6min N
传代培养:给培养菌液每月加入1次培养基,得到二代培养菌液,所述培养菌液与培养基的体积比:10:90-110,然后取10%体积(v/v)的二代培养菌液,接种至新鲜制备的培养基中,所述新鲜制备的培养基的体积为二代培养菌液体积的9-11倍,共传代3-5次,得到驯化培养的复合菌株的菌液。
所述培养基为微量元素混合溶液、Wolfe’s维生素溶液和碳酸氢盐缓冲液的混合液;每升培养基中微量元素混合溶液mL、Wolfe’s维生素溶液mL和碳酸氢盐缓冲液mmol的用量比为8-12:8-12:25-35;
1升微量元素混合溶液的组分含量为:0.05-0.1g CoCl
进一步地,装入瓶中的培养基为经过通入4-6min氮气和高压蒸汽灭菌处理的培养基。
所述高压蒸汽灭菌处理为100-130℃灭菌处理15-25min。
所述Fe(III)铁氧化矿物为赤铁矿、褐铁矿或针铁矿。
所述间歇性好氧曝气的方式包括采用地面式曝气风机,所述曝气风机连接曝气管;或采用地埋式曝气风机,通过自动化控制,改变曝气频率与曝气流量,从而实现地下水中溶解氧环境的可变式调控。
所述地下水的进水恒定流量为0.15-0.35mL·min
本发明实施例提供的技术方案带来的有益效果是:
(1)本发明针对基于Fe(III)生物还原厌氧氧化氨氮、有机物的去除不彻底这一特点,通过间歇性曝气,调控溶解氧环境,可以实现彻底反硝化、以及有机物的全量氧化,促进Fe(III)与Fe(II)的循环转化,实现氨氮向氮气的完全氧化,解决厌氧铁氨氧化产生的硝酸盐氮、亚硝酸盐氮去除不彻底的问题,进而实现地下水中氨氮和有机物的协同高效去除。
(2)能够实现有机物的进一步氧化,可实现大分子、中分子有机物向小分子有机物持续转变氧化的用途。
附图说明
图1是本发明实施例1中提供的修复方法的流程示意图;
图2为本发明实施例提供的试验装置示意图;
图3为本发明实施例提供的氨氮浓度变化曲线;
图4为本发明实施例提供的有机物浓度变化曲线;
图5为本发明实施例提供的反应介质渗透性曲线。
具体实施方式
为使本发明的目的、技术方案和优点更加清楚,下面将结合附图对本发明实施方式作进一步地详细描述。
实施例1
参见图1,一种间歇性曝气式地下水氨氮、有机污染生物的修复方法,包括以下步骤:
将源于淹水稻田土的原生土著微生物,经过室内驯化、筛选和培养,得到复合菌株的菌液,所述菌液里含有驯化培养的复合菌株,所述复合菌株为Fe(III)还原菌、反硝化菌和铁氨氧化菌,再通过挂膜的方式,将菌液里驯化培养后的复合菌株负载至颗粒粒径2-4mm赤铁矿表面,形成生物膜,得到修复功能材料,将修复功能材料加入至受污染的地下水中;驯化培养的Fe(III)还原菌、反硝化菌和铁氨氧化菌的菌液体积与赤铁矿的重量比为10mL:1g;
在厌氧环境中,在经驯化培养的Fe(III)还原菌和铁氨氧化菌的作用下,将地下水中的铁氧化矿物表面Fe(III)转化为Fe(II),NH
地下水的进水恒定流量为0.25mL·min
在厌氧环境中,并在经驯化培养的反硝化菌和铁还原菌的作用下,使Fe(III)转化为Fe(II),NO
本发明的Fe(III)生物还原厌氧过程,是指在典型的经驯化培养的Fe(III)还原菌的作用下,以Fe(III)为电子受体,以地下水中氨氮、有机物等特征污染物为电子供体,Fe(III)被还原为Fe(II),有机物被氧化,氨氮被厌氧氧化物为硝酸盐氮、亚硝酸盐氮的生物过程。Fe(III)作为电子受体,可采用溶解性Fe(III),即无定型Fe(III)氧化物;也可采用非溶解性Fe(III)氧化物,即弱晶型Fe(III)氧化物或强晶型Fe(III)氧化物。
本发明通过间歇性曝气调控溶解氧环境,进而控制厌氧铁氨氧化反应进程,修复地下水氨氮和有机污染。解决了厌氧铁氨氧化产生的亚硝酸盐难题,完全彻底脱氮,实现地下水中氨氮和有机物的高效协同去除。
进一步地,驯化培养复合菌株的大概流程为:富集培养淹水稻田土中土著微生物—异化Fe(III)还原菌、反硝化菌和铁氨氧化菌作为功能微生物,并在试验室内进一步筛选以获得生长活性最优的混合菌株。
所述驯化、筛选和培养复合菌株(主要包括Fe(III)还原菌、反硝化菌和铁氨氧化菌)的菌液的具体步骤为:
厌氧处理去离子水:将50mL去离子水置于100mL厌氧反应瓶中,通入5min氮气,进行厌氧处理;
加入新鲜稻田土后恒温震荡:称取3g新鲜稻田土,加入到50mL厌氧处理后的去离子水中,通入5分钟氮气,盖紧瓶塞,以120rpm的转速、25℃下恒温震荡2h;
装瓶:取震荡后的上层菌液2mL,转移至50mL规格的厌氧反应瓶中,厌氧反应瓶中装有20mL已通入5min氮气厌氧处理,并经过120℃灭菌20min高压蒸汽灭菌处理的培养基,以及10g清洗去除杂质后的Fe(III)铁氧化矿物颗粒;
培养:给厌氧反应瓶通入5min N
传代培养:给培养菌液每月加入1次培养基,得到二代培养菌液,培养菌液与培养基的体积比:10:100,然后取10%体积(v/v)的二代培养菌液,接种至新鲜制备的培养基中,所述新鲜制备的培养基的体积为二代培养菌液体积的10倍,共传代4次,得到驯化培养的复合菌株的菌液。
所述培养基为微量元素混合溶液10mL/L、Wolfe’s维生素溶液10mL/L和碳酸氢盐缓冲液30mmol L-1的混合液;
1升微量元素混合溶液的组分含量为:0.1g CoCl
实施例2
本实施例的修复方法与实施例1基本相同,所不同的是:
地下水的进水恒定流量为0.15mL·min
Fe(III)铁氧化矿物为针铁矿;
驯化培养的Fe(III)还原菌、反硝化菌、铁氨氧化菌的菌液体积与针铁矿的重量比为8mL:1g;
本实施例的间歇性好氧曝气采用地埋式曝气风机,通过自动化控制,改变曝气频率与曝气流量,从而实现地下水中溶解氧环境的可变式调控。
所述驯化、筛选和培养复合菌株(Fe(III)还原菌、反硝化菌和铁氨氧化菌)的菌液的具体步骤为:
厌氧处理去离子水:将50mL去离子水置于100mL厌氧反应瓶中,通入5min氮气,进行厌氧处理;
加入新鲜稻田土后恒温震荡:称取4g新鲜稻田土,加入到60mL厌氧处理后的去离子水中,通入5分钟氮气,盖紧瓶塞,以150rpm的转速、20℃下恒温震荡1.5h;
装瓶:取震荡后的上层菌液2mL,转移至50mL规格的厌氧反应瓶中,厌氧反应瓶中装有25mL已通入6min氮气厌氧处理,并经过100℃灭菌25min高压蒸汽灭菌处理的培养基,以及12g清洗去除杂质后的Fe(III)铁氧化矿物颗粒;
所述上层菌液、培养基和Fe(III)铁氧化矿物颗粒的体积质量比为:2mL:15-25mL:8-12g;
培养:给厌氧反应瓶通入6min N
传代培养:给培养菌液每月加入1次培养基,得到二代培养菌液,所述培养菌液与培养基的体积比:10:90,然后取10%体积(v/v)的二代培养菌液,接种至新鲜制备的培养基中,所述新鲜制备的培养基的体积为二代培养菌液体积的11倍,共传代3次,得到驯化培养的复合菌株的菌液。
所述培养基为微量元素混合溶液8mL/L、Wolfe’s维生素溶液12mL/L和碳酸氢盐缓冲液25mmol L-1的混合液;
1升微量元素混合溶液的组分含量为:0.05g CoCl
实施例3
本实施例的修复方法与实施例1基本相同,所不同的是:
地下水的进水恒定流量为0.35mL·min
Fe(III)铁氧化矿物为褐铁矿。
驯化培养的Fe(III)还原菌、反硝化菌或铁氨氧化菌的菌液体积与褐铁矿的重量比为12mL:1g;
所述驯化、筛选和培养复合菌株(Fe(III)还原菌、反硝化菌和铁氨氧化菌)的菌液的具体步骤为:
厌氧处理去离子水:将50mL去离子水置于100mL厌氧反应瓶中,通入5min氮气,进行厌氧处理;
加入新鲜稻田土后恒温震荡:称取2g新鲜稻田土,加入到40mL厌氧处理后的去离子水中,通入5分钟氮气,盖紧瓶塞,以100rpm的转速、23℃下恒温震荡2.5h;
装瓶:取震荡后的上层菌液2mL,转移至50mL规格的厌氧反应瓶中,厌氧反应瓶中装有15mL已通入6min氮气厌氧处理,并经过130℃灭菌15min高压蒸汽灭菌处理的培养基,以及8g清洗去除杂质后的Fe(III)铁氧化矿物颗粒;
所述上层菌液、培养基和Fe(III)铁氧化矿物颗粒的体积质量比为:2mL:15-25mL:8-12g;
培养:给厌氧反应瓶通入3min N
传代培养:给培养菌液每月加入1次培养基,得到二代培养菌液,所述培养菌液与培养基的体积比:10:110,然后取10%体积(v/v)的二代培养菌液,接种至新鲜制备的培养基中,所述新鲜制备的培养基的体积为二代培养菌液体积的9倍,共传代5次,得到驯化培养的复合菌株的菌液。
所述培养基为微量元素混合溶液12mL/L、Wolfe’s维生素溶液5mL/L和碳酸氢盐缓冲液35mmol L-1的混合液。
1升微量元素混合溶液的组分含量为:0.07g CoCl
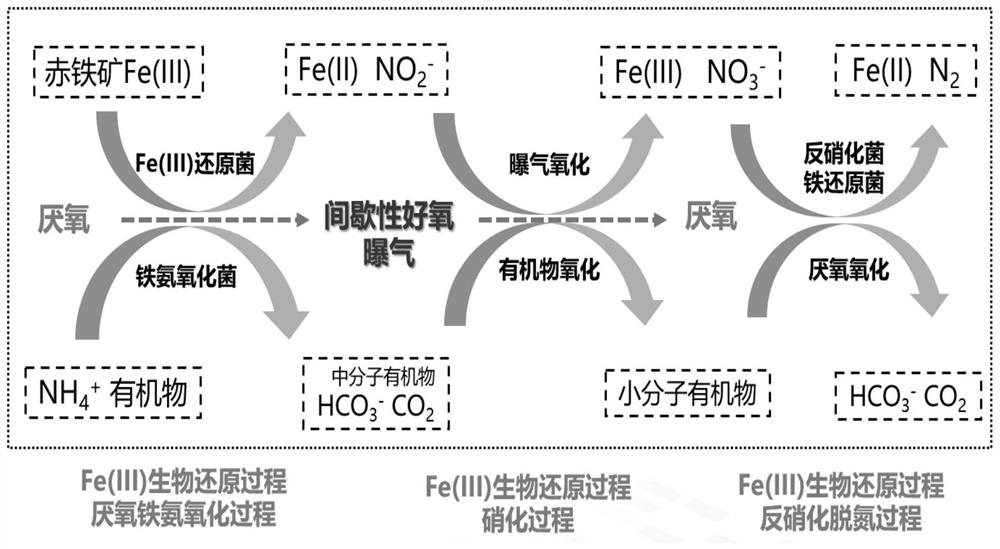
本发明采用的间歇性曝气式地下水氨氮、有机污染生物修复方法的原理在于:针对厌氧铁氨氧化产生的硝酸盐氮、亚硝酸盐氮(非彻底脱氮),通过间歇性曝气,构建厌氧好氧环境,实现地下水氨氮、有机污染同步生物修复。首先通过曝气创造好氧条件,曝气时可将曝气流量设置为0.01L/min,打开曝气阀门,使反应系统进行好氧状态,实现亚硝酸盐氮向硝酸盐氮的转变、Fe
对比实施例
(1)选择典型Fe(III)铁氧化矿物,以天然赤铁矿(α-Fe
(2)构建两套材质为有机玻璃的圆柱形试验装置,如图2所示,蠕动泵1通过管道连接进水通2,再通过进水管3连接生物反应柱4和对照试验柱5,生物反应柱4和对照试验柱5分别通过各自的出水管6连接相应的出水桶7,生物反应柱4和对照试验柱5上设有曝气口8,两个曝气口8通过曝气管道连接曝气泵9。本试验装置使用1台多通道蠕动泵1(Longerpump,BT100-2J/YZ1515x)为两套试验装置自下而上供水,一套为生物反应装置,在生物反应柱3内的赤铁矿上负载接种驯化培养的复合菌株,另一套为非生物反应装置,未负载接种驯化培养的Fe(III)还原菌、反硝化菌和铁氨氧化菌。两套试验装置分别装入100kg的填料介质赤铁矿,填料介质完全相同,均为上述颗粒状赤铁矿,区别在于生物反应装置内填料介质负载接种了复合菌株,而非生物反应装置内填料介质未负载接种复合菌株。
(3)通过富集培养淹水稻田土中土著微生物—异化Fe(III)还原菌、反硝化菌和铁氨氧化菌作为功能微生物,并按照实施例1的方法在试验室内进一步筛选以获得生长活性最优的混合菌株,得到驯化培养的复合菌株的菌液100L开展后续试验。所选用淹水稻田土取自于江西省中部(N 28°10′~28°45′,E 116°1′~116°34′),所用培养基为微量元素混合溶液10mL/L、Wolfe’s维生素溶液10mL/L和碳酸氢盐缓冲液30mmol L
(4)按照以下方法,将驯化培养的复合菌株负载挂膜至赤铁矿表面:将填充介质均匀填充至上述试验装置中,使用1台多通道蠕动泵,将100L实施例1制备的驯化培养的Fe(III)还原菌、反硝化菌和铁氨氧化菌的复合菌株的菌液输入至玻璃试验装置内,并使液面充满,之后将试验装置的进水口和出水口关闭,进行微生物的静态挂膜,为时1周。挂膜满1周后,打开玻璃试验装置出水口,排出玻璃试验装置内剩余的菌液,之后使用蠕动泵将生理盐水(0.90%氯化钠溶液)循环注入玻璃试验装置内,冲洗培养基内干扰性富营养离子,从而使驯化培养的Fe(III)还原菌、反硝化菌和铁氨氧化菌负载至赤铁矿螯合物表面。
(5)两套试验装置用水相同,取自某非正规生活垃圾填埋场受渗滤液污染的地下水,主要特征污染物为氨氮(重度污染)、有机物(轻度污染),氨氮浓度范围为16-18mg N/L(本底值为0.5mg N/L)。COD浓度为100-120mg/L(本底值为50mg/L),地下水碳氮比失调,属于典型的低碳高氮型污染。体系内硝酸盐氮浓度为1.50mg N/L、亚硝酸盐氮低于检出限。
(6)两套试验装置设定进水恒定流量为0.25mL·min
(7)试验装置运行时出水管接入废水桶,取样时接入封口的干燥锥形瓶中。为了评价填料的渗透性,通过监测水头管内水位高度,并根据达西定律(Darcy's law)对反应介质的渗透性进行换算,计算公式如下:Q=K*A*(△h)/L,式中Q为单位时间渗流量,K为反应介质的渗透系数,A为过水断面面积,L为渗流路径长度,△h为监测管水头差。
运行一段时间后,检测进出水水质指标,可发现:
由图3可看出,反应前10d,未进行间歇性曝气。地下水氨氮进水浓度为16-18mg N/L时,反应至第10d,生物反应试验装置出水氨氮浓度由18.50mg N/L降至5.85mg N/L,氨氮去除率为68.38%;与之相比,非生物反应试验装置出水氨氮浓度由16.05mg N/L降至13.60mg N/L,氨氮去除率仅为15.26%;这说明未负载功能性微生物条件下,赤铁矿作为填充介质,对氨氮的吸附截留去除效果一般。而负载微生物后,地下水流动状态下,氨氮的厌氧生物氧化效能仍旧较好(68.38%)。反应第10d之后,每天定时打开增氧泵,定时调节两套试验装置内的溶解氧条件(12h/d)。可以看出反应至第20d,两套试验装置出水氨氮浓度均呈现下降趋势,其中生物试验装置出水氨氮浓度下降至2mg N/L左右;非生物反应试验装置出水氨氮浓度下降至6mg N/L左右。之后通过调控反应体系内的碳源,可知反应55d后,生物反应试验装置出水氨氮浓度为0.42mg N/L,非生物反应试验装置出水氨氮浓度为9.51mgN/L,这表明负载功能微生物的赤铁矿填料,地下水中氨氮能够被有效去除,生物去除率为93%。
由图4可看出,在未曝气的前10d,两组试验装置出水COD浓度整体均呈现先上升后下降的趋势,且两组差异性不大,反应至第10d,生物试验装置COD浓度下降至50mg/L,这表明在功能微生物新陈代谢活动下,地下水中有机质逐渐被消耗。反应第10d后,反应体系内开始进行间歇性曝气,反应至第20d,生物反应试验装置出水COD浓度为20mg/L,非生物反应试验装置出水COD浓度为140mg/L,进一步表明生物反应体系内有机质被逐渐消耗殆尽。如前所述,反应20d后,两组试验装置的进水中均添加了葡萄糖,反应第20-38d,非生物反应试验装置出水COD出现了一定的上升,而生物反应试验试验装置出水COD仍维持在40-60mg/L,这表明外加葡萄糖作为碳源时,反应体系内微生物可以利用葡萄糖作为碳源,且并未出现有机碳积累现象,葡萄糖的外加很好地促进了反硝化过程的进行。反应第38至55d,两组试验装置内碳源均被替换为固相木屑,可看出,两根试验装置出水COD浓度均有所上升,且非生物反应试验装置出水COD浓度明显要高于生物反应试验装置,随着反应的进行,固相碳源缓慢释放,反应体系内还原态有机质和氨氮逐步被氧化降解,出水COD浓度最终整体维持在60mg/L。
由图5可看出,对赤铁矿反应介质的渗透系数进行了测定,即通过水头测定装置,根据达西公式计算渗透系数。两组试验装置整个运行周期内,赤铁矿填料的渗透系数K均比较稳定,K值范围在(0.11-2.85)×10
以上所述仅为本发明的较佳实施例,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 一种间歇性曝气式地下水氨氮、有机污染生物的修复方法
- 一种间歇性曝气式垃圾渗滤液氨氮、有机污染生物修复装置及方法
