肾小球滤过能力的确定方法
文献发布时间:2023-06-19 12:02:28
技术领域
本发明涉及肾小球滤过能力的确定方法、和确定肾小球滤过能力的血液分析系统。
背景技术
作为表示肾功能的代表性指标有肾小球滤过率(Glomerular Filtration Rate:GFR)。肾小球滤过率表示通过肾小球从血液中过滤1分钟的液量,菊粉清除率的测定是它的国际标准(金标准)。然而,菊粉清除率的测定需要经过2小时的菊粉的持续点滴、和经过多次的采尿和采血,受检者和实施者的负担大。因此,在日常临床中菊粉清除率的测定限于仅在活体肾移植时的供体这样有限的状况下实施,大部分以肌酐这样的其它标志物的测定代替。多数标志物的值与作为金标准的菊粉清除率等的实际的肾小球滤过率的背离大,从而成为肾脏病准确诊断的障碍。
肌酐作为肾功能的指标在临床现场通用地被测定。肌酐是肌肉收缩所必需的肌酸的最终代谢物。肝脏中生成的肌酸被摄入到肌细胞中,一部分代谢变成肌酐,介由血液运送到肾脏,经肾小球滤过后,没有经肾小管再吸收而排泄到尿中。在肾小球滤过能力降低的情况下,排出受到阻碍,留在血液中而数值升高,由此成为尿毒素蓄积有益的指标,因此用于评价肾功能。但是,如果GFR不降低50%以上,血液中的肌酐量就不会显示出明显的异常值,不能说是敏锐的标志物。
半胱氨酸蛋白酶抑制剂C是由全身的有核细胞以一定比例产生的分子量13.36kDa的蛋白质,在全部经肾小球滤过后,经过肾小管中的再吸收在肾脏中被分解,因此考虑根据滤过量而从血液中被除去,血液中的量成为GFR的指标。但是,在肾功能高度降低时,血液中半胱氨酸蛋白酶抑制剂C量的升高钝化,对于末期的肾脏病难以进行准确的肾功能评价。
如以上,能够充分满足想要不对受检者/患者带来大的负担、仅通过采血就能够在从早期到末期的广泛范围测定个别患者的准确的肾小球滤过率这种临床现场的要求的生物标志物尚不存在。
逐渐明确了以往认为在哺乳类的活体内不存在的D-氨基酸存在于各种各样的组织中,承担生理功能。另外显示血液中的D-丝氨酸、D-丙氨酸、D-脯氨酸、D-谷氨酸、D-天冬氨酸的量在肾功能衰竭患者中会变动,与肌酐相关,因此可以成为肾功能衰竭的标志物(非专利文献1、非专利文献2、非专利文献3、非专利文献4)。进而公开了选自D-丝氨酸、D-苏氨酸、D-丙氨酸、D-天冬酰胺、D-别苏氨酸、D-谷氨酰胺、D-脯氨酸以及D-苯丙氨酸中的氨基酸为肾脏病的病况指标值(专利文献1)。这些文献中,只不过公开了患有肾脏病的患者的血液中的D-氨基酸与健康正常者相比会变动,因此能够将这些变动作为指标来诊断肾脏病的主旨、或者仅对象的血液中的D-丝氨酸量与肌酐量或将肌酐量校正后的估计值相关,对于血液中的D-氨基酸量直接与作为金标准的菊粉清除率相关而能够确定(推断)肾小球滤过能力,没有任何记载和启示。此外,虽然近年来作为肾脏病的标志物,开发出了尿中L-FABP、血液中NGAL、尿中KIM-1等,但是它们不是与肾小球滤过能力相关的。
现有技术文献
专利文献
专利文献1:国际公开第2013/140785号
非专利文献
非专利文献1:Fukushima,T.等,Biol.Pharm.Bull.18:1130(1995)
非专利文献2:Nagata.Y Viva Origino Vol.18(No.2)(1990)第15次学术演讲会演讲要旨集
非专利文献3:Ishida等,北里医学23:51~62(1993)
非专利文献4:Yong Huang等,Biol.Pharm.Bull.21:(2)156-162(1998)
发明内容
发明要解决的课题
希望与到现在为止已知的血液中的肌酐量等肾功能标志物相比,以更广的范围准确地确定受检者的肾小球滤过能力的方法。
用于解决课题的手段
本发明者们着眼于血液中的D-丝氨酸,分析了与GFR(菊粉清除率)的关系后,令人惊奇地发现了在从健康正常开始到处于早期~末期阶段的肾脏病患者的血液样品中,血液中的D-丝氨酸量与肌酐量和/或半胱氨酸蛋白酶抑制剂C量相比,在全部阶段中相对于GFR(菊粉清除率)显示出更高的相关,从而完成了本发明。
于是本发明涉及下述发明:
[1]基于血液中的D-丝氨酸量的肾小球滤过能力的确定方法。
[2]根据项目1所述的方法,所述肾小球滤过能力是基于由菊粉清除率与血液中的D-丝氨酸量的相关计算出的方程而确定的肾小球滤过率。
[3]根据项目1或2所述的方法,所述血液是根据现有的检查判定为有疑似肾脏病的对象的血液。
[4]根据项目1~3中任一项所述的方法,对判定为肾小球滤过能力降低的对象进行治疗干预。
[5]根据项目4所述的方法,所述治疗干预选自生活习惯改善、膳食指导、血压管理、贫血管理、电解质管理、尿毒素管理、血糖值管理、免疫管理和脂肪管理。
[6]根据项目4或5所述的方法,作为所述治疗干预,包括对所述对象施与选自利尿剂、钙拮抗剂、血管紧张素转换酶抑制剂、血管紧张素受体拮抗剂、交感神经阻滞剂、SGLT2抑制剂、磺酰脲类药物、噻唑烷类药物、双胍类药物、α-葡糖苷酶抑制剂、格列奈类药物、胰岛素制剂、NRF2激活剂、免疫抑制剂、他汀类药物、贝特类药物、贫血治疗药、促红细胞生成素制剂、HIF-1抑制剂、铁剂、电解质调节剂、钙受体激动剂、磷吸附剂、尿毒素吸附剂、DPP4抑制剂、EPA制剂、烟酸衍生物、胆固醇转运蛋白抑制剂、PCSK9抑制剂中的至少一种药剂。
[7]一种血液分析系统,包括存储部、分析测定部、数据处理部和肾小球滤过能力输出部,
所述存储部存储D-丝氨酸量与肾小球滤过能力的相关方程;
所述分析测定部分离并定量所述血液中的D-丝氨酸量;
所述数据处理部将D-丝氨酸量代入到存储部所存储的相关方程中,计算出肾小球滤过能力;
所述病况信息输出部输出关于肾小球滤过能力的信息。
[8]根据项目7所述的血液分析系统,所述肾小球滤过能力是基于由菊粉清除率与血液中的D-丝氨酸量的相关计算出的方程而确定的肾小球滤过率。
[9]根据项目7或8所述的血液分析系统,所述血液是根据现有的检查判定为有疑似肾脏病的对象的血液。
发明的效果
在本发明的肾小球滤过能力的确定方法中使用的血液中的D-丝氨酸量相对于GFR(菊粉清除率)具有比血液中的肌酐量和半胱氨酸蛋白酶抑制剂C量更优异的相关。
附图说明
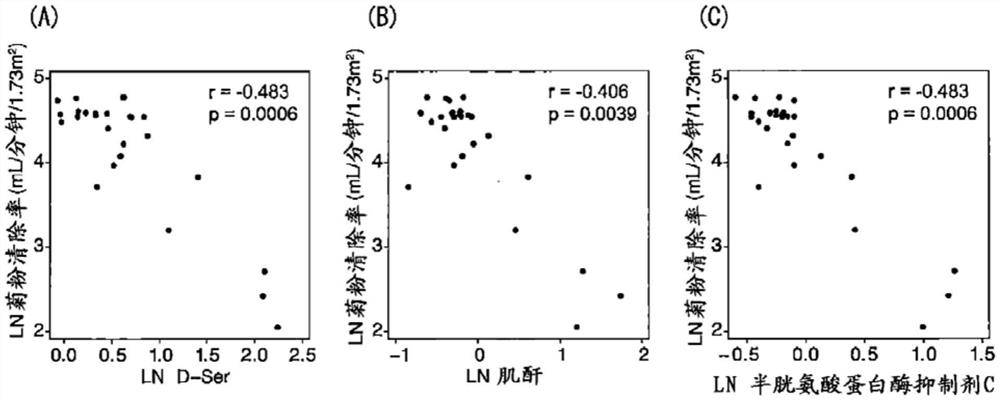
图1是在对象中测定的血液中的D-丝氨酸量(A)、肌酐量(B)、以及半胱氨酸蛋白酶抑制剂C量(C)与GFR(菊粉清除率)(经体表面积校正)的散点图。
图2是在对象中测定的血液中的D-丝氨酸量(A)、肌酐量(B)、以及半胱氨酸蛋白酶抑制剂C量(C)与GFR(菊粉清除率)(无体表面积校正)的散点图。
图3是健康正常者组(GFR>70)的数据中的血液中的D-丝氨酸量(A)、肌酐量(B)、以及半胱氨酸蛋白酶抑制剂C量(C)与体表面积(BSA)的散点图。
图4是分类成全部数据(All)、GFR(菊粉清除率)100以下、G3a以下(GFR(菊粉清除率)60以下)、G3b以下(GFR(菊粉清除率)45以下)、G4以下(GFR(菊粉清除率)30以下)、以及G5以下(GFR(菊粉清除率)15以下),显示各分类中的血液中的D-丝氨酸量(A)、肌酐量(B)、以及半胱氨酸蛋白酶抑制剂C量(C)与GFR(菊粉清除率)(经体表面积校正)的相关的图。
图5显示本发明的试样分析系统的构成图。
图6是显示用于通过本发明的程序确定肾小球滤过率的动作的例子的流程图。
具体实施方式
本发明涉及基于血液中的D-丝氨酸量的肾小球滤过能力的确定方法。
在本发明中,肾小球滤过能力是指肾小球过滤血液的能力。在一个方式中,用肾小球滤过率(GFR)表示,但实质上不限于肾小球滤过率,可以以任意单位确定肾小球滤过能力。作为一例,也可以将血液中的D-丝氨酸量直接或根据情况用任意的数值校正,作为肾小球滤过能力表示。在本发明中,肾小球滤过能力可以是进行了体表面积校正的肾小球滤过能力,也可以是没有进行体表面积校正的肾小球滤过能力。由于根据体格所需要的肾小球滤过能力不同,因此,在用于比较、统计处理、或筛选诊断的情况下,有时进行体表面积校正。
所谓肾小球滤过率,是指通过肾小球从血液中过滤1分钟的液量,以“mL/分钟”这样的单位表示。根据体格所需要的肾小球滤过率会变化,因此,在用于统计处理、比较、筛选诊断的情况下,校正为每1.73m
在本发明中,作为指标使用的D-丝氨酸是作为构成蛋白质的氨基酸的L-丝氨酸的光学异构体。D-丝氨酸量主要通过丝氨酸消旋酶和/或D-氨基酸氧化酶等代谢酶在各组织和/或血液中被精密控制,另一方面,在发生肾损伤的情况下,血液中的D-丝氨酸量会变动。
在本发明中,所谓“血液中的D-丝氨酸量”,可以是指特定的血液量中的D-丝氨酸量,可以以浓度表示。血液中的D-丝氨酸量作为对于采集的血液中进行离心分离、沉淀分离、或用于分析的前处理后的试样中的量来测定。因此,血液中的D-丝氨酸量可以作为采集的全血、血清、血浆等来自血液的血液试样中的量来测定。作为一例,利用HPLC的分析的情况下,规定量的血液所包含的D-丝氨酸量用色谱表示,可以根据对于峰的高度、面积、形状通过与标准品的比较和/或校准进行的分析来定量。D-丝氨酸浓度可以根据与已知样品的比较来测定血液中的D-丝氨酸浓度,可以使用血液中的D-丝氨酸浓度作为血液中的D-丝氨酸量。另外,可以利用酶法,通过利用标准品的标准曲线的定量分析而计算出氨基酸浓度。
D-丝氨酸和L-丝氨酸量可以通过任意方法测定,例如可以通过手性柱色谱、利用酶法的测定、以及利用识别氨基酸的光学异构体的单克隆抗体的免疫学手法来定量。本发明中的试样中的D-丝氨酸和L-丝氨酸量的测定可以利用本领域技术人员周知的任何方法来实施。例如有色谱法、酶法(Y.Nagata et al.,Clinical Science,73(1987),105.Analytical Biochemistry,150(1985),238.,A.D'Aniello et al.,ComparativeBiochemistry and Physiology Part B,66(1980),319.Journal of Neurochemistry,29(1977),1053.,A.Berneman et al.,Journal of Microbial&Biochemical Technology,2(2010),139.,W.G.Gutheil et al.,Analytical Biochemistry,287(2000),196.,G.Mollaet al.,Methods in Molecular Biology,794(2012),273.,T.Ito et al.,AnalyticalBiochemistry,371(2007),167.等)、抗体法(T.Ohgusu et al.,AnalyticalBiochemistry,357(2006),15.,等)、气相色谱(GC)(H.Hasegawa et al.,Journal of MassSpectrometry,46(2011),502.,M.C.Waldhier et al.,Analytical and BioanalyticalChemistry,394(2009),695.,A.Hashimoto,T.Nishikawa et al.,FEBS Letters,296(1992),33.,H.Bruckner and A.Schieber,Biomedical Chromatography,15(2001),166.,M.Junge et al.,Chirality,19(2007),228.,M.C.Waldhier et al.,Journal ofChromatography A,1218(2011),4537.等)、毛细管电泳法(CE)(H.Miao et al.,Analytical Chemistry,77(2005),7190.,D.L.Kirschner et al.,AnalyticalChemistry,79(2007),736.,F.Kitagawa,K.Otsuka,Journal of Chromatography B,879(2011),3078.,G.Thorsen and J.Bergquist,Journal of Chromatography B,745(2000),389.等)、高效液相色谱(HPLC)(N.Nimura and T.Kinoshita,Journal ofChromatography,352(1986),169.,A.Hashimoto et al.,Journal of Chromatography,582(1992),41.,H.Bruckner et al.,Journal of Chromatography A,666(1994),259.,N.Nimura et al.,Analytical Biochemistry,315(2003),262.,C.Muller et al.,Journal of Chromatography A,1324(2014),109.,S.Einarsson et al.,AnalyticalChemistry,59(1987),1191.,E.Okuma and H.Abe,Journal of Chromatography B,660(1994),243.,Y.Gogami et al.,Journal of Chromatography B,879(2011),3259.,Y.Nagata et al.,Journal of Chromatography,575(1992),147.,S.A.Fuchs et al.,Clinical Chemistry,54(2008),1443.,D.Gordes et al.,Amino Acids,40(2011),553.,D.Jin et al.,Analytical Biochemistry,269(1999),124.,J.Z.Min et al.,Journal ofChromatography B,879(2011),3220.,T.Sakamoto et al.,Analytical andBioanalytical Chemistry,408(2016),517.,W.F.Visser et al.,Journal ofChromatography A,1218(2011),7130.,Y.Xing et al.,Analytical and BioanalyticalChemistry,408(2016),141.,K.Imai et al.,Biomedical Chromatography,9(1995),106.,T.Fukushima et al.,Biomedical Chromatography,9(1995),10.,R.J.Reischl etal.,Journal of Chromatography A,1218(2011),8379.,R.J.Reischl and W.Lindner,Journal of Chromatography A,1269(2012),262.,S.Karakawa et al.,Journal ofPharmaceutical and Biomedical Analysis,115(2015),123.,等)。
本发明中的光学异构体的分离分析系统可以组合多种分离分析。更具体而言,可以通过利用光学异构体的分析方法来测定试样中的D-/L-氨基酸量,所述分析方法的特征在于包括以下步骤:使包含具有光学异构体的成分的试样,与作为流动相的第一液体一起通过作为固定相的第一柱填充剂,从而分离所述试样的所述成分的步骤;在多回路单元中分别保留所述试样的各个所述成分的步骤;将在所述多回路单元中各自保留的所述试样的各个所述成分,与作为流动相的第二液体一起,通过流路供于作为固定相的具有光学活性中心的第二柱填充剂,从而分割所述试样的各个成分所包含的所述光学异构体的步骤;以及检测所述试样的各个成分所包含的所述光学异构体的步骤(专利第4291628号)。HPLC分析有时会预先用邻苯二甲醛(OPA)、4-氟-7-硝基-2,1,3-苯并噁二唑(NBD-F)这样的荧光试剂将D-和L-氨基酸衍生物化、或用N-叔丁氧羰基-L-半胱氨酸(Boc-L-Cys)等进行非对映异构体化(浜濑健司和财津洁,分析化学,53卷,677-690(2004))。代替地可以通过利用识别氨基酸的光学异构体的单克隆抗体、例如与D-丝氨酸、L-丝氨酸等特异性结合的单克隆抗体的免疫学手法来测定D-氨基酸。另外,以D-型异构体和L-型异构体的合计量为指标的情况下,不需要分离D-型异构体和L-型异构体进行分析,可以不区别D-型异构体和L-型异构体地分析氨基酸。这种情况下也可以通过酶法、抗体法、GC、CE、HPLC分离和定量。
由于与本发明的比较中使用的血液中的肌酐量自来就强烈受到肌肉量的影响,所以在运动选手、肢端肥大症的患者和/或大量摄取肉时显示出高值,在神经肌肉疾病(肌营养不良等)和/或羸弱、长期卧床、衰弱、肌肉减少症、运动障碍综合征(locomotivesyndrome)、有截肢(anputation)的患者和/或蛋白质摄取限制时显示出低值,因此不能反映准确的肾功能。另外,对于血液中的肌酐量,确认了在早上显示高值的10%左右的日内变动,因此在它的处理中需要注意。由于在轻度的肾功能降低时,血液中的半胱氨酸蛋白酶抑制剂C量比血液中的肌酐量升高灵敏,因此认为适于初期肾功能障碍的发现。但是,已知类固醇和/或环孢菌素的使用、糖尿病、甲状腺功能亢进症、炎症、高胆红素血症、高甘油三酯血症等患者的状态会影响半胱氨酸蛋白酶抑制剂C量。所以,当诊查肾脏病时,需要结合其它标志物、例如尿素氮(BUN)和/或尿蛋白等数值联合诊断。
基于以血液中的肌酐量为代表的目前为止的肾功能标志物确定的肾小球滤过量的准确性低,另一方面,虽然金标准的菊粉清除率能够准确地测定肾小球滤过率,但其程序烦杂,受检者和医疗从业者的负担大,因此实施场地受到限定。本发明的肾小球滤过能力的确定方法至少与血液中的肌酐量相比,能够更准确地确定肾小球滤过能力,另外与血液中的半胱氨酸蛋白酶抑制剂C量相比,能够更准确地确定肾小球滤过能力。另外,在根据肾小球滤过量分类的组中进行与菊粉清除率的相关分析的情况下,在全部的组中,D-丝氨酸与血液中的半胱氨酸蛋白酶抑制剂C量和肌酐量两者相比,显示出相关系数r值更高,与菊粉清除率的相关更高。另外,关于其准确性,应该根据今后的实验弄清楚,但可以具有与作为国际标准测定法的利用菊粉清除率的肾小球滤过率确定方法相匹敌或更好的性能。因此,本发明的其他方式中,可以将血液中的D-丝氨酸量作为菊粉清除率的代用标志物使用。所谓代用标志物,是指能够科学地证明与最终评价的关联的标志物。因此,所谓菊粉清除率代用标志物,是指使用血液中的D-丝氨酸量统计性地显示与利用菊粉清除率的评价的关联,结果能够代替基于菊粉清除率的GFR确定方法,基于D-丝氨酸量来确定肾小球滤过率。
对于D-丝氨酸,不想要在理论上限定,但由于不会受到肌肉量的影响,因此有不需要如血液中的肌酐那样根据体格进行校正的优点。本发明的1个方式中,本发明的肾小球滤过率确定方法具有不进行基于与体格相关联的选自性别、年龄、以及肌肉量中的至少1种因素的校正。
观察到血液中的肌酐量(p=0.0074)、半胱氨酸蛋白酶抑制剂C量(p=0.043)与体表面积(BSA)相关,但D-丝氨酸量(p=0.17)与BSA不相关(实施例3)。这显示了肌酐和半胱氨酸蛋白酶抑制剂C受到以肌肉量为代表的体格的某些影响,为了测定准确的肾小球滤过能力,需要以人种、年龄、性别、体表面积等进行校正。另一方面意味着,通过D-丝氨酸量判定的肾小球滤过能力能够提供不受如高龄者那样肌肉衰退的体格的影响的准确的值。体表面积可以根据已知的方法确定,作为一例可以使用下述方程:
BSA=体重(kg)
在本发明的一个方式中,肾小球滤过能力可以通过将受检者的血液中的D-丝氨酸量代入到由菊粉清除率与血液中的D-丝氨酸量的相关计算出的方程、对应表或图中来确定。显示出菊粉清除率与D-丝氨酸量的相关,比菊粉清除率与血液中的肌酐量的相关高,通过将受检者的D-丝氨酸量代入到由菊粉清除率与血液中的D-丝氨酸量的相关计算出的方程、对应表或图中确定的肾小球滤过能力,与基于以往的血液中的肌酐量确定的肾小球滤过率相比更准确。相关的分析中使用的菊粉清除率可以是经体表面积校正的菊粉清除率,也可以是体表面积校正前的菊粉清除率。可以根据需要选择体表面积校正前和校正后的肾小球滤过能力的任一个。在由菊粉清除率与血液中的D-丝氨酸量的相关计算出的对应表中,可以记载与某个D-丝氨酸量对应的肾小球滤过能力的数值,也可以记载根据数值范围的肾脏病的疾病严重程度分类。
慢性肾脏病(CKD)的疾病严重程度分类中,根据肾小球滤过率的数值范围分类成G1、G2、G3a、G3b、G4、以及G5六个疾病严重程度。即,将90mL/分钟/1.73m
关于观察到与体格的相关的血液中的肌酐量、半胱氨酸蛋白酶抑制剂C量,研究出对于相关的人种和/或年龄、性别用大规模的患者数据将其校正而推算出肾小球滤过率的各种方程。作为主要的肾小球滤过率的推算公式,有Cockcroft-Gault公式、MDRD公式、CKD-EPI公式,现在日常诊疗中主要使用的日本人用的推算公式(eGFR)如下所述。
其中,这样确定的eGFR是以健康诊断中的筛选、和/或比较多数对象者这样的流行病学研究中的简单评价为着眼点而制作成的指标,以计算出由平均体格校正而得的值为目的,因此对于特别瘦的高龄者等个别患者的准确的肾功能评价,仍然推荐使用菊粉清除率。(日本肾脏学会指南)。
如果通过本发明的判定方法确定肾小球滤过能力,则可以基于此进行肾脏病的疾病严重程度的分类。作为一例,可以根据作为慢性肾脏病患者的分类的G1、G2、G3a、G3b、G4、以及G5六个疾病严重程度进行分类。对于分类到与G2~G5相对应的分类的对象,进行治疗干预。治疗干预可以根据各分类适当选择。将生活习惯改善、膳食指导、血压管理、贫血管理、电解质管理、尿毒素管理、血糖值管理、免疫管理、以及脂肪管理等独立或组合来指导治疗干预。作为生活习惯改善,推荐戒烟及向BMI值小于25的减重等。作为膳食指导,进行减盐及蛋白质限制。这些中特别对于血压管理、贫血管理、电解质管理、尿毒素管理、血糖值管理、免疫管理、脂肪管理,可以通过给药进行治疗。作为血压管理,管理以使其为130/80mmHg以下,可以根据情况施与高血压治疗药。作为高血压治疗药,可以使用利尿剂(噻嗪系利尿剂例如三氯噻嗪、苄氢氯噻嗪、氢氯噻嗪,类噻嗪系利尿剂例如美替克仑、吲达帕胺、曲帕胺、美夫西特,袢利尿剂例如呋塞米,保钾性利尿剂/醛固酮拮抗剂例如氨苯蝶啶、螺内酯、依普利酮等)、钙拮抗剂(二氢吡啶系例如硝苯地平、氨氯地平、依福地平、西尼地平、尼卡地平、尼索地平、尼群地平、尼伐地平、巴尼地平、非洛地平、贝尼地平、马尼地平、阿折地平、阿雷地平,苯二氮卓系、地尔硫卓等)、血管紧张素转换酶抑制剂(卡托普利、依那普利、阿拉普利、地拉普利、西拉普利、赖诺普利,贝那普利、咪达普利、替莫普利、喹那普利、群多普利、培哚普利叔丁胺等)、血管紧张素受体拮抗剂(血管紧张素Ⅱ受体拮抗剂例如氯沙坦、坎地沙坦、缬萨坦、替米沙坦、奥美沙坦、厄贝沙坦、阿齐沙坦等)、交感神经阻滞剂(β阻滞剂例如阿替洛尔、比索洛尔、倍他洛尔、美托洛尔、醋丁洛尔、塞利洛尔、普萘洛尔、纳多洛尔、卡替洛尔、吲哚洛尔、尼普地洛、氨磺洛尔、阿罗洛尔、卡维地洛、拉贝洛尔、贝凡洛尔、乌拉地尔、特拉唑嗪、哌唑嗪、多沙唑嗪、布那唑嗪等)等。作为贫血治疗药,使用促红细胞生成素制剂、铁剂、HIF-1抑制剂等。作为电解质调节剂,使用钙受体激动剂(西那卡塞、依特卡肽等)、磷吸附剂。作为尿毒素吸附剂,使用活性炭等。管理血糖值以使其小于Hba1c6.9%,根据情况施与降糖药。作为降糖药,使用SGLT2抑制剂(伊格列净、达格列净、鲁格列净、托格列净、坎格列净、恩格列净等)、DPP4抑制剂(西他列汀磷酸、维格列汀、沙格列汀、阿格列汀、利拉利汀、特力利汀、曲格列汀、阿拉格列汀、奥格列汀等)、磺酰脲类药物(甲苯磺丁脲、醋酸己脲、氯磺丙脲、格列吡脲、格列本脲、格列齐特、格列美脲等)、噻唑烷类药物(吡格列酮等)、双胍类药物(二甲双胍、丁福明等)、α-葡糖苷酶抑制剂(阿卡波糖、伏格列波糖、米格列醇等)、格列奈类药物(那格列奈、米格列奈、瑞格列奈等)、胰岛素制剂、NRF2激活剂(甲基巴多索隆等)等。作为免疫管理,使用免疫抑制剂(类固醇类、他克莫司、抗CD20抗体、放线酮、霉酚酸酯(MMF)等)。脂肪管理时,管理以使其小于LDL-C120mg/dL,根据情况使用脂质异常症治疗药,例如他汀类药物(瑞舒伐他汀、匹伐他汀、阿托伐他汀、西立伐他汀、氟伐他汀他汀、辛伐他汀他汀、普伐他汀、洛伐他汀、美伐他汀等)、贝特类药物(氯贝特、苯扎贝特、非诺贝特、克利贝特等)、烟酸衍生物(生育酚烟酸酯、尼可莫尔、戊四烟酯等)、胆固醇转运蛋白抑制剂(依泽替米贝等)、PCSK9抑制剂(依洛尤单抗等)EPA制剂等。任何药剂的剂型都可以是单剂也可以是合剂。根据肾功能降低的程度,可以施行腹膜透析、血液透析、持续血液透析滤过、血液置换(血浆交换、血浆吸附等)、肾移植这样的肾代替疗法。
本发明的其他方式可以涉及执行确定肾小球滤过能力的方法的试样分析系统、程序。图4是本发明的试样分析系统的构成图。图4所示的试样分析系统10以能够实施本发明的肾小球滤过能力的判定方法的方式构成。这样的试样分析系统10包括存储部11、和输入部12、分析测定部13、和数据处理部14、和输出部15,能够分析血液试样,输出肾小球滤过能力。
更具体而言,在本发明的试样分析系统10中,
存储部11能够存储从输入部12输入的由菊粉清除率与血液试样中的D-丝氨酸量的相关计算出的方程、对应表或图,
分析测定部13能够分离定量血液试样中的D-丝氨酸,
数据处理部14能够通过将D-丝氨酸量代入到由菊粉清除率与血液试样中的D-丝氨酸量的相关计算出的方程中、或者由对应表和/或图读出,由此确定肾小球滤过能力,
输出部15能够输出肾小球滤过能力。
进一步优选的方式中,本发明的试样分析系统可以进一步包括存储部11存储从输入部12输入的阈值的工序、和数据处理部14将分离定量而得的D-丝氨酸量与阈值进行比较的工序。该情况下,在D-丝氨酸量比阈值低的情况下,输出部15输出肾小球滤过能力高的主旨。在D-丝氨酸量比阈值高的情况下,数据处理部14通过将D-丝氨酸量代入到由菊粉清除率与血液试样中的D-丝氨酸量的相关计算出的方程中、或者从对应表或图中读出,从而确定肾小球滤过能力,输出部15输出肾小球滤过能力。
存储部11具有RAM、ROM、闪存等存储装置、硬盘驱动器等固定盘装置、或软盘、光盘等可移动的存储装置等。除经分析测定部测定的数据、从输入部输入的数据和指示、经数据处理部进行的演算处理结果等以外,存储部还存储信息处理装置的各种处理中使用的计算机程序、数据库等。计算机程序可以介由例如CD-ROM、DVD-ROM等计算机可读取的记录介质、和/或互联网安装。计算机程序用公知的安装程序等安装在存储部。存储部存储关于预先从输入部12输入的由菊粉清除率与血液试样中的D-丝氨酸量的相关计算出的方程、对应表或图的数据。另外,也可以存储根据肾小球滤过率的肾功能分类。
输入部12是接口(interface)等,也包括键盘、鼠标等操作部。由此输入部能够输入经分析测定部13测定的数据、由数据处理部14进行的演算处理的指示等。另外,例如在分析测定部13位于外部的情况下,输入部12可以与操作部分开地,包括能够介由网络和/或存储介质输入测定的数据等的接口部。
分析测定部13进行血液试样中的D-丝氨酸的测定工序。因此,分析测定部13具有能够分离和测定氨基酸的D-型异构体和L-型异构体的构成。氨基酸可以逐个分析,也可以对于一部分或全部种类的氨基酸汇总分析。没有意图要将分析测定部13限定于以下形式,例如可以是具备试样导入部、光学拆分率柱、检测部的手性色谱系统,优选为高速液相色谱系统。从仅检测特定的氨基酸量的观点来说,可以实施基于酶法和/或免疫学方法的定量。分析测定部13可以与试样分析系统分别地构成,也可以将测定数据等用网络和/或存储介质介由输入部12输入。
数据处理部14能够通过由测定的D-丝氨酸量代入到由菊粉清除率与血液试样中的D-丝氨酸量的相关计算出的方程中、或者通过由对应表或图读出,从而确定肾小球滤过能力。在由菊粉清除率与血液试样中的D-丝氨酸量的相关计算出的方程、对应表或图还进一步需要其它的校正值例如年龄、体重、性别、身高等的情况下,这样的信息预先从输入部输入,存储在存储部。在计算肾小球滤过率时,数据处理部能够调出所涉及的信息,代入到式中、或者由对应表或图读出,由此计算出肾小球滤过率。数据处理部14也能够由确定的肾小球滤过能力确定肾脏病和/或肾功能分类。数据处理部14根据存储部所存储的程序,对经分析测定部13测定而存储在存储部11中的数据执行各种演算处理。演算处理通过数据处理部所包含的CPU进行。该CPU包括控制分析测定部13、输入部12、存储部11、及输出部15的功能模块,能够进行各种控制。这些各部可以由各自独立的集成电路、微处理器、固件等构成。
输出部15以输出作为经数据处理部进行演算处理的结果的肾小球滤过能力的方式构成。输出部15可以是直接显示演算处理的结果的液晶显示器等显示装置、打印机等输出单元,也可以是用于向外部存储装置输出或介由网络输出的接口部。也能够与肾小球滤过能力一并、或独立地输出D-丝氨酸量和/或肾功能分类。
图5是显示用于通过本发明的程序确定肾小球滤过率的动作的例子的流程图。具体而言,本发明的程序是使包括输入部、输出部、数据处理部、存储部的信息处理装置确定肾小球滤过率的程序。本发明的程序包括用于使所述信息处理装置执行以下工序的指令:
使存储部存储从输入部输入的D-丝氨酸量,
读出预先存储在存储部的由菊粉清除率与血液试样中的D-丝氨酸量的相关计算出的方程、对应表或图、和D-丝氨酸量,使数据处理部确定肾小球滤过能力,
使存储部存储所确定的肾小球滤过能力,然后
使输出部输出所存储的肾小球滤过能力。
本发明的程序可以存储在存储介质中,也可以介由互联网或LAN等电信线路提供。
在信息处理装置具备分析测定部的情况下,代替从输入部输入D-丝氨酸量的值,可以包括用于使信息处理装置执行分析测定部从血液试样中测定该值并存储在存储部的指令。
本说明书中所提到的全部文献其整体通过引用援引到本说明书中。
以下说明的本发明的实施例仅以例示为目的,不是限定本发明的技术范围。本发明的技术范围仅通过权利要求范围的记载来限定。以不脱离本发明的主旨为条件,可以进行本发明的变更,例如本发明的构成要件的追加、删除及替换。
实施例
受检者集合
从由为了诊断和/或治疗目的在2016年~2017年之间在大阪大学医学部附属医院肾脏内科(Department of Nephrology,Osaka University Hospital))住院的慢性肾脏病(CKD)患者组成的组中,将11名患者用于回顾性研究。与此独立地,在国立医药基盘·健康·荣养研究所采用15名20岁以上的健康正常志愿者。试验方案经各设施中的伦理委员会承认,且从全部受检者获得了书面的知情同意。
健康正常者和慢性肾脏病患者的信息如下所述:
表1受检者的基线特征
值以中位数(IQR)或%(count)表示
菊粉清除率的测量方法
将受检者的菊粉清除率(Cin)按照Clin Exp Nephrol 13,50-54(2009)中记载的标准方法,由血液和尿中的菊粉浓度、以及尿体积计算出。简单记载则为在断食、推迟用药、及水负荷环境下,在2小时的连续静脉滴注1%的菊粉(菊粉注:株式会社富士药品)期间,在不同的三个时间点采集血液和尿样品。受检者在滴注30分钟前经口饮用500mL的水。为了保持水负荷,菊粉滴注开始后,在40、60、90分钟饮用60mL的水。点滴的初期速度在最初的30分钟为300mL/h,在接着的90分钟为100mL/h。菊粉滴注开始后,在45、75、及105分钟采集血液试样。受检者点滴开始后30分钟排尿直到完全排空膀胱。接着,在30分钟~60分钟之间、60分钟~90分钟之间、和90~120分钟之间采集尿样品。菊粉利用酶法测量。用三个Cin值的平均作为由标准方法得到的Cin(Cin-ST)。
血液中D-氨基酸的测定
样品制备
来自人血浆的样品制备如下所述进行:
将20倍体积的甲醇添加到血浆中完全混合。离心后,将由甲醇匀浆得到的上清10μL的转移到褐色管中,使其减压干燥。在残渣中添加20μL的200mM硼酸钠缓冲液(pH8.0)和5μL的荧光标记试剂(无水MeCN中有40mM的4-氟-7-硝基-2,1,3-苯并噁二唑(NBD-F)),接着在60℃加热2分钟。加入75μL的0.1%TFA水溶液(v/v)终止反应,然后将2μL的反应混合液供于二维HPLC。
利用二维HPLC的氨基酸光学异构体的定量
用以下二维HPLC系统定量氨基酸光学异构体。用反相柱(KSAA RP,1.0mmi.d.×400mm;株式会社资生堂)通过流动相(5~35%MeCN、0~20%THF、及0.05%TFA)分离、溶出氨基酸的NBD衍生物。设定柱温为45℃,流动相的流速为25μL/分钟。对分离出来的氨基酸的级分用多回路阀进行分级,连续用手性柱(KSAACSP-001S,1.5mmi.d.×250mm;资生堂)进行光学拆分。根据氨基酸的保留使用包含柠檬酸(0~10mM)或甲酸(0~4%)的MeOH-MeCN的混合用液作为流动相。NBD-氨基酸用470nm的激发光在530nm下进行荧光检测。NBD-氨基酸的保留时间通过氨基酸光学异构体的标准品鉴定,通过标准曲线定量。
与GFR(菊粉清除率)的相关分析
(1)有体表面积校正
对于26名受检者,将进行了体表面积校正的GFR(菊粉清除率)、与血液中的D-丝氨酸量(A)、肌酐量(B)、及半胱氨酸蛋白酶抑制剂C量(C)制图成散点图,计算出相关系数r值和p值。结果示于图1。血液中的D-丝氨酸量相对于GFR(菊粉清除率)显示出与血液中的半胱氨酸蛋白酶抑制剂C量同等的相关。
(2)无体表面积校正
对于26名受检者,将没有进行体表面积校正的GFR(菊粉清除率)、与血液中的D-丝氨酸量(A)、肌酐量(B)、及半胱氨酸蛋白酶抑制剂C量(C)制图成散点图,计算出相关系数r值和p值。结果示于图2。血液中的D-丝氨酸在无体表面积校正的条件下,相对于GFR(菊粉清除率)显示出最高的相关。
与体表面积(BSA)的相关
对于健康正常者(GFR>70)的数据,将体表面积(BSA)、与测定的血液中的D-丝氨酸量、半胱氨酸蛋白酶抑制剂C量、及肌酐量表示成散点图,计算出相关系数r值和p值。结果示于图3。血液中的肌酐量和/或半胱氨酸蛋白酶抑制剂C量与体表面积相关,而血液中的D-丝氨酸量与体表面积不相关。
基于GFR的分类的比较
基于由菊粉清除率得到的GFR,将26名受检者分类到以下的组(全部数据(All);GFR100以下;G3a以下:GFR60以下;G3b以下:GFR45以下;G4以下:GFR30以下;G5以下:GFR15以下)。GFR100以下为21名、G3a以下为8名、G3b以下为5名、G4以下为4名、G5以下为3名。计算出各数据中没有进行体表面积校正的GFR(菊粉清除率)、与血液中的D-丝氨酸量(A)、肌酐量(B)、及半胱氨酸蛋白酶抑制剂C量(C)的相关系数r值和p值。结果示于图3。在分组的情况下,各组中D-丝氨酸量显示出与GFR(菊粉清除率)的相关高。特别是血液中的肌酐量在G3a以下和/或G3b以下显示出比较良好的相关,但在全部数据(All)和/或GFR100以下则显示出相关低,这是显示肾功能降低为轻度时无法反映这样的肌酐的缺点的结果。另一方面,半胱氨酸蛋白酶抑制剂C量在GFR100以下、G3a以下等肾功能比较优异的数据中,与GFR(菊粉清除率)的相关高,另一方面如G3b以下那样,显示出随着肾功能恶化,与GFR(菊粉清除率)的相关降低。血液中的D-丝氨酸量在各组中显示出良好地与GFR(菊粉清除率)相关。
- 肾小球滤过能力的确定方法
- 用于估算肾小球滤过率(GFR)的血代谢标记物及其应用
