改善生物传感器光收集效率的方法和结构
文献发布时间:2023-06-19 12:07:15
相关申请的交叉引用
本申请要求于2018年12月1日提交的名称为“Methods And Structures ToImprove The Light Collection Efficiency”的美国临时专利申请No.62/774,239的优先权,该临时专利被共同转让并通过引用整体并入本文,以用于所有目的。
技术领域
本发明通常涉及用于光电二极管和生物传感器以用于生物或化学分析的方法和结构。
背景技术
发现CMOS图像传感器可用于电子成像设备,包括用于数码相机、医学成像设施、雷达设备等。CMOS图像传感器使用集成电路和一系列光电二极管,可以捕获光并将其转换为电信号。
CMOS图像传感器通常在集成电路芯片上实现。芯片可以具有用于每个像素的放大器。虽然在芯片中包含许多放大器可能导致用于捕获光的区域较少,但是可以将其他部件集成到芯片上以将更多光引导到光电二极管中。例如,可以将微透镜放置在光电二极管的前面以将光引导到光电二极管中。为了进一步增加撞击光电二极管的光量,可以使用背面照射(BSI)。BSI有效地将光电二极管放置在更靠近光源的位置,而不是在集成电路布线之下和之间,从而减少了破坏性干扰。BSI CMOS传感器还具有其他优点。例如,BSI CMOS传感器可具有低工作电压、低功耗、高效率和低噪声。
BSI CMOS图像传感器通常具有两个功能区域:光感测区域和电子电路区域。光感测区域包括以阵列布置的光电二极管,其耦合到检测光强度的金属氧化物半导体(MOS)晶体管。电子电路区域在MOS晶体管和外部连接之间提供连接,例如与用于处理来自MOS晶体管的数据的其他器件的连接。
在实践中,BSI CMOS图像传感器可以采用将入射光分成不同波长的光带的滤光器。光被基底上的光电二极管接收并转换成不同强度的电信号。例如,入射光束可以被分成红色、绿色和蓝色光,并且由每个颜色的相应光电二极管接收。每个光电二极管将检测到的光强度转换成电信号。这是通过光电二极管累积电荷来实现的。例如,光的强度越高,光电二极管中累积的电荷越多。然后可以将累积的电荷与颜色和亮度相关联。
除了上述用途之外,CMOS图像传感器还可以用于生物或化学分析。对于这样的分析,可以将生物或化学样品放置在光电二极管上方,并且可以将生物或化学样品发射的光引导到光电二极管。可以通过光电二极管检测样品的荧光或化学发光,并且可以确定颜色和亮度。该颜色和亮度可用于识别生物或化学样品。
发明内容
本发明的实施方案通过提供可以改善用于生物或化学分析的生物传感器中的光收集效率的光电二极管解决了与先前方法相关的缺点。
根据本发明的实施方案,BSI CMOS图像传感器可用于有效分析和测量样品的荧光或化学发光。该测量的值可用于帮助识别样品。本发明的实施方案还提供制备用于生物或化学分析的改进的生物传感器的方法。如本文所用,术语“生物传感器”可用于指用于确定生物分子(特别是以DNA和支链的或其他衍生化核酸为例的核酸大分子)内或附接于其上的发光物质的设备。如本文所使用的,术语“核酸大分子”可以指例如DNB或单链实施方案。
根据本发明的一些实施方案,提供了用于增加由样品的荧光或化学发光发射的光的收集的方法和结构。在某些实施方案中,一种光电二极管可以包含具有第一表面和第二表面的半导体基板以及位于第一表面附近的光敏结。所述第二表面定位成与所述第一表面相对,所述第二表面包含覆盖所述半导体基板中的凹陷区域的凹入表面。
在上述光电二极管的一些实施方案中,所述凹陷区域的尺寸和功能被设置以容纳核酸大分子。
在一些实施方案中,所述半导体基板包含硅材料。
在一些实施方案中,所述光敏结包含P-N结。
在一些实施方案中,所述光敏结包含在N型基板中的P+区。
在一些实施方案中,所述光敏结包含在P型基板中的N+区。
在一些实施方案中,所述光电二极管还包含:金属氧化物层,其覆盖在所述半导体基板的所述第二表面上;以及氧化物层,其覆盖在所述金属氧化物层上。
在一些实施方案中,所述金属氧化物层包括夹心的氧化钽(Ta
在一些实施方案中,所述的光电二极管还包含:一个或多个金属氧化物层,其覆盖在所述半导体基板的所述第二表面上;以及氧化硅层,其覆盖在所述金属氧化物层上。
在一些实施方案中,所述金属氧化物层包含氧化铪(HfO
在一些实施方案中,所述金属氧化物层包含阳极氧化铝(Al
在一些实施方案中,使用干法蚀刻工艺形成所述半导体基板中的所述凹陷区域。
在一些实施方案中,所述干法蚀刻工艺包括基于氯的蚀刻工艺或基于氟的干法蚀刻工艺。
在一些实施方案中,使用湿法蚀刻工艺形成所述半导体基板中的所述凹陷区域。
在一些实施方案中,所述湿法蚀刻工艺包含依赖于晶体取向的湿法各向异性蚀刻。
在一些实施方案中,所述湿法蚀刻工艺包含使用KOH的蚀刻工艺。
根据一些实施方案,一种生物传感器可以具有背面照射互补金属氧化物半导体(CMOS)图像传感器,其包括电子电路层;和在所述电子电路层上的光敏层。所述光敏层包括多个光电二极管,所述多个光电二极管覆盖所述电子电路层。所述光电二极管中的每一个具有与所述电子电路层相邻的光敏结和与所述电子电路层相对的光接收表面。所述光接收表面包括覆盖所述光电二极管的背面中的凹陷区域的凹入表面,并且所述凹陷区域的尺寸和功能被设置以容纳核酸大分子。
在以上生物传感器的一些实施方案中,每个光电二极管包括如本文所述的光电二极管。
在一些实施方案中,所述电子电路层包括:介电层;和形成在所述第一介电层中的金属布线,其中所述金属布线被配置为将所述多个光电二极管耦合到外部设备。
在一些实施方案中,所述生物传感器还包括:在所述背面照射CMOS图像传感器上的钝化层。
在上述生物传感器的一些实施方案中,所述多个光电二极管中的每个光电二极管被配置为检测从所述多个核酸大分子中的核酸大分子上的荧光或化学发光标记发射的光。
在一些实施方案中,所述光从荧光标记的寡核苷酸探针发射,所述荧光标记的寡核苷酸探针与固定在斑点上的核酸扩增子杂交。
在一些实施方案中,所述光从与固定所述斑点上的核酸扩增子杂交的荧光标记的引物延伸产物发射。
在一些实施方案中,所述核酸扩增子来自基因组DNA片段或cDNA文库。
在一些实施方案中,所述扩增子通过滚环扩增或桥聚合酶链式反应(PCR)形成。
在一些实施方案中,所述生物传感器还包括激发光源。
一些实施方案提供一种方法,其包括:提供背面照射互补金属氧化物半导体(CMOS)图像传感器。提供所述背面照射CMOS图像传感器包括:提供电子电路层;以及在所述电子电路层上提供光敏层。所述光敏层包括:电子电路层;和在所述电子电路层上的光敏层。所述光敏层包括多个光电二极管,所述多个光电二极管覆盖所述电子电路层。所述光电二极管中的每一个具有与所述电子电路层相邻的光敏结和由所述多个光电二极管的与所述电子电路层相对的表面限定的光接收表面。所述光接收表面包含覆盖所述光电二极管的背面中的凹陷区域的凹入表面。所述凹陷区域的尺寸和功能被设置以容纳核酸大分子。
在以上方法的一些实施方案中,每个光电二极管包括如本文所述的光电二极管。
在一些实施方案中,从所述斑点中包含的所述核酸大分子发射的所述光被一个光电二极管的所述光接收表面接收。
在一些实施方案中,从所述斑点中包含的所述核酸大分子发射的所述光从多于一个的光电二极管的所述光接收表面接收。
在一些实施方案中,提供所述电子电路层包括:沉积介电层;以及在所述介电层中形成金属布线。所述金属布线被配置为将所述多个光电二极管耦合到外部设备。
在一些实施方案中,所述方法还包括:在所述背面照射CMOS图像传感器上沉积钝化层。
在一些实施方案中,所述方法还包括:将所述多个核酸大分子中的核酸大分子附接于所述斑点中的斑点。
在一些实施方案中,所述方法还包括:使用所述多个光电二极管中的光电二极管检测从所述核酸大分子上的荧光或化学发光标记发射的光。
在一些实施方案中,所述光从与固定在所述斑点上的核酸扩增子杂交的荧光标记的寡核苷酸探针发射。
在一些实施方案中,所述光从与固定在所述斑点上的核酸扩增子杂交的荧光标记的引物延伸产物发射。
在一些实施方案中,所述核酸扩增子来自基因组DNA片段或cDNA文库。
在一些实施方案中,所述扩增子通过滚环扩增或桥聚合酶链式反应(PCR)形成。
在一些实施方案中,所述方法还包括:用激发光源照射所述核酸大分子。
根据一些实施方案,一种核酸测序方法包括迭代地执行过程,该过程包括以下步骤:
用荧光标记来标记核酸大分子,所述荧光标记识别所述核酸大分子中特定位置处的核苷酸碱基;
检测与所述核酸大分子相关的所述荧光标记,其中检测所述荧光标记包括:
用激发光照射所述核酸大分子,其中所述核酸大分子吸收所述激发光并使发射的光传输到达背面照射(BSI)互补金属氧化物半导体(CMOS)图像传感器的光电二极管上;
测量在所述光电二极管处接收的所述发射的光的至少一个参数;以及
将所述发射的光的所述至少一个参数与所述荧光标记相关联;以及
从所述核酸大分子中除去所述荧光标记。
在以上方法的一些实施方案中,每个光电二极管包括如本文所述的光电二极管。
根据一些实施方案,一种核酸测序方法包括迭代地执行过程,该过程包括以下步骤:
用化学发光标记来标记核酸大分子,所述化学发光标记识别所述核酸大分子中特定位置处的核苷酸碱基;
改变所述核酸大分子化学发光的环境,以使所述标记发射光;
其中使所发射的所述光传输到达背面照射(BSI)互补金属氧化物半导体(CMOS)图像传感器的光电二极管上;
测量在所述光电二极管处接收的所述发射的光的至少一个参数;以及
将所述发射的光的所述至少一个参数与所述化学发光标记相关联;以及
从所述核酸大分子中除去所述化学发光标记。
在以上方法的一些实施方案中,每个光电二极管包括如本文所述的光电二极管。
根据一些实施方案,一种生物传感器具有背面照射互补金属氧化物半导体(CMOS)图像传感器,其包括:电子电路层;以及在所述电子电路层上的光敏层。所述光敏层包括多个光电二极管,所述多个光电二极管覆盖所述电子电路层。所述光电二极管中的每一个具有与所述电子电路层相邻的光敏结和由所述多个光电二极管的与所述电子电路层相对的表面限定的光接收表面。所述光接收表面包含覆盖在所述光电二极管的背面中的凹陷区域的凹入表面。在所述光接收表面上方的保护层,其尺寸和功能被设置为包含多个核酸大分子。
在以上方法的一些实施方案中,每个光电二极管包括如本文所述的光电二极管。
通过参考以下说明、权利要求和附图,前述以及其他特征和实施方案将变得更加明显。
附图说明
图1是根据本发明一些实施方案的包含多个背面照射(BSI)CMOS图像传感器的半导体晶片的截面图。
图2是根据本发明一些实施方案的光电二极管的剖视图。
图3是图2的光电二极管的截面图,其示出了根据本发明的一些实施方案的由生物样品发射的光的收集效率。
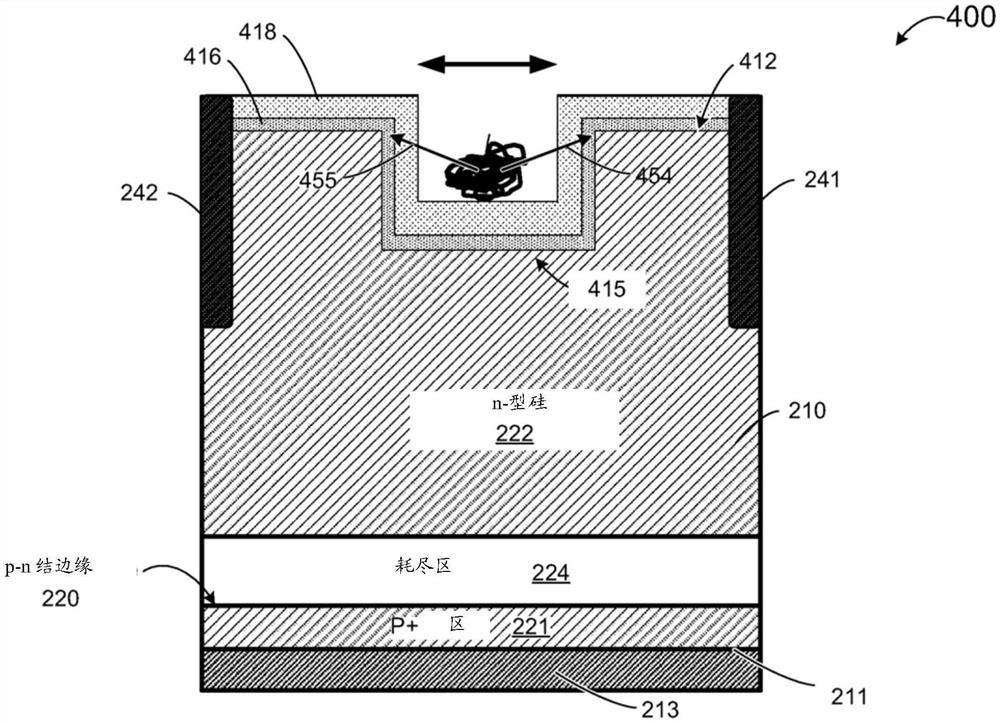
图4是根据本发明一些实施方案的具有改善的对生物样品发射的光的光收集效率的光电二极管的截面图。
图5是根据本发明的替代实施方案的具有改善的对生物样品发出的光的光收集效率的光电二极管的截面图。
图6是根据本发明的一些实施方案的另一光电二极管的截面图,该光电二极管具有改善的对生物样品发射的光的光收集效率。
具体实施方式
图1是根据本发明的一些实施方案的包含多个背面照射(BSI)CMOS图像传感器的半导体晶片的截面图。在基于半导体的测序池的制造中,晶片可具有数千个管芯,每个管芯代表晶片的将被制造成包含多个池阵列(例如,数百个或更多池)的测序芯片的部分。为了简单起见,图1仅示出了半导体晶片100中的区域11和12,其被设计用于两个单独的管芯中的两个流通池,并且每个区域被示出为仅具有两个池区域,如图1所示。区域11包含池区域151-1和151-2,区域12包含池区域152-1和152-2。
如图1所示,半导体晶片100包含CMOS图像传感器层10、CMOS处理电路层20和堆叠层30。在堆叠技术中,CMOS图像传感器层10和CMOS处理电路层20可以分别制造,然后在3-D堆叠设备中通过堆叠接口层30接合在一起。
CMOS图像传感器层10包含形成在半导体层110中的光感测部件,例如,光电二极管112。半导体层110可以由任何合适的材料制成,诸如,例如,由硅、硅上III-V族、硅上石墨烯、绝缘体上硅、它们的组合等制成。尽管这里相对于光电二极管112进行了描述,但是预期可以使用任何合适的光敏部件。光电二极管112可以配置为将所测得的光转换成电流。光电二极管112可以包括MOS晶体管(未示出)的源极和漏极,其可以将电流传输到其他部件,例如其他MOS晶体管。其他部件可以包括复位晶体管、电流源跟随器或用于将电流转换为数字信号的行选择器等。尽管描述为电介质,但是预期,介电层可以包含任何合适的电绝缘材料。
CMOS图像传感器层10还包含形成在介电层104中的金属布线105。金属布线115可以包含用于集成电路材料的互连和外部连接。
为了简单起见,CMOS处理电路层20被示为硅基板层101。然而,应当理解,CMOS处理电路层20可以包含测序操作所需的CMOS电路。例如,CMOS处理电路层20可以包含用于图像处理、信号处理以及用于排序操作和外部通信的控制功能的电路。
如图1所示,CMOS图像传感器层10被配置用于背面照射(BSI)。CMOS图像传感器层10和CMOS处理电路层20可以分别制造,然后在3-D堆叠器件中通过堆叠层30接合在一起。堆叠层30可以包含介电层102和在介电层102中形成的通孔103。通孔103用于连接CMOS图像传感器层10和CMOS处理电路层20。
图1还示出了钝化层121,其覆盖在CMOS图像传感器层10上。钝化层121可以通过常规的半导体处理技术(例如,低温等离子体化学气相沉积、PECVD、溅射、ALD、旋涂、浸涂等)沉积在基板层110和光电二极管112上。钝化层121可以包含任何合适的保护材料。例如,钝化层121可以包含诸如氮化硅、氧化硅、其他介电材料或其组合等等材料。钝化层121可以用作随后的蚀刻步骤的蚀刻停止层,如本文进一步所述的。钝化层121可以可替代地或附加地起到保护有源器件(即,背面照射CMOS传感器)的作用。钝化层121可以可替代地或附加地起到保护光电二极管112免受由频繁使用引起的磨损的作用。钝化层121可以是透明的。
可以在第一钝化层121上方或之内形成离散区域,有时称为“斑点”或孔(未示出),分析物分子可以定位或固定在该离散区域上。化学或生物样品可以放置在离散区域上或上方以进行分析。通常,对于DNA测序,生物样品包含DNA测序文库。DNA测序文库的DNB或其他成员或其克隆种群位于离散区域中。
在一些实施方案中,CMOS图像传感器层10可以适于检测来自相应生物分子阵列的光信号(例如,荧光或化学发光发射),其中各个生物分子可以位于(例如,在斑点或孔中)一个或多个光电二极管上方,使得一个或多个光电二极管接收来自生物分子的光。如本文所使用的,化学发光包含生物发光,例如荧光素酶报道分子产生的生物发光。
图2是根据本发明的一些实施方案的光电二极管的截面图。光电二极管200是可以在图2中描述的背面照射(BSI)CMOS图像传感器中使用的光电二极管的示例。在该示例中,光电二极管200是硅P-N结光电二极管。光电二极管200包含具有第一表面211和第二表面212的半导体基板210。第二表面212与第一表面211相对定位。光电二极管200包含与第一表面211相邻的光敏结220。在该示例中,光敏结220是由重掺杂p+区221在n型基板区222中形成的硅PN结220。耗尽区224形成在结附近,其中载流子可以由入射的光子产生并且可以作为电信号感测。第一表面也可以被称为光电二极管的前表面,第二表面也可以被称为光电二极管的后表面。光电二极管200还可具有分别覆盖第一表面211和第二表面212的介电层231和232。
在正面照射(FSI)感测中,入射光从正表面或第一表面211入射。在背面照射(BSI)感测中,入射光从后表面或第二表面212入射。如图2所示,光电二极管200用于背面照射(BSI),并且入射光入射在第二表面212上。光电二极管200还可具有深沟槽隔离(DTI)区域241和242,以将一个光电二极管与相邻的光电二极管隔离。在一些实施方案中,沟槽241和242可以填充有金属,例如钨(W)。钨深沟槽隔离(W DTI)可以减少进入相邻的光电二极管的入射光。
图3是图2的光电二极管200的截面图,其示出了根据本发明一些实施方案的由生物样品发射的光的收集效率。如图3所示,生物样品250设置在光电二极管200的背面。光信号(例如,荧光或化学发光发射)在来自生物样品250的所有方向,如光线252所示。但是,仅一部分发射光能由光电二极管200收集到,如由光线254和255所指示的。结果,大部分发射的光没有被收集并且不能对被感测的信号做出贡献。
图4是根据本发明一些实施方案的具有改善的对生物样品发射的光的光收集效率的光电二极管的截面图。如图4所示,光电二极管400类似于图2的光电二极管200,并且,相似的部件用相同的附图标记表示。然而,光电二极管400具有与图2中的第二表面212不同的第二表面或背表面412。在图2中,第二表面212具有基本平坦的表面。然而,图4中的第二表面412是非平坦的表面。非平坦的表面可以是覆盖半导体基板中的凹陷区域415的凹入表面。凹陷区域的尺寸和功能被设置为包含生物样品450,例如核酸大分子。如图4中的光线454和455所示,生物样品450发射的大部分光可以被光电二极管400收集。可以大大改善光的收集效率。
凹陷区域可以是在硅基板中蚀刻的沟槽。图4中的凹陷区域415为基本矩形的形状。第二表面412被金属氧化物层416覆盖。诸如氧化硅层之类的氧化物层418设置在金属氧化物层416上方。在一些实施方案中,金属氧化物层可以是夹心的HfO
半导体基板中的凹陷区域可以使用干法蚀刻工艺形成。例如,干法蚀刻工艺可以包含等离子体蚀刻、反应离子蚀刻(RIE)等。干法蚀刻工艺可以包含不同的化学过程,例如,基于氯的蚀刻工艺或基于氟的干法蚀刻工艺。备选地,使用湿法蚀刻工艺形成半导体基板中的凹陷区域。例如,湿法蚀刻工艺可以是各向同性蚀刻工艺或依赖于晶体取向的湿法各向异性蚀刻。作为依赖于晶体取向的湿法各向异性蚀刻的示例,湿法蚀刻工艺包含使用KOH的蚀刻工艺。使用水性KOH蚀刻硅会产生V形凹槽、金字塔形凹陷区域等。
图5是根据本发明的替代实施方案的具有改善的对生物样品发出的光的光收集效率的光电二极管的截面图。如图5所示,通过使用KOH,利用蚀刻工艺,通过依赖于晶体取向的湿法各向异性蚀刻来蚀刻硅,以形成金字塔形状的凹陷区域515。类似于图4中的光电二极管400,在图5的光电二极管500中,第二表面512被金属氧化物层516覆盖。诸如氧化硅层之类的氧化物层518被布置在金属氧化物层516之上。在一些实施方案中,金属氧化物层可以是夹心的HfO
如上所述,凹陷区域的尺寸和功能被设置以容纳核酸大分子。例如,在图4中的光电二极管400中,可以使用氧化物层上的化学物质使氧化物层418的表面功能化以固定DNB。替代地,可以使用在氧化物层上形成的附加金属氧化物层来对氧化物层的表面进行功能化。如图6所示,在氧化物层618上形成金属氧化物层619。表面层的功能化以保留生物样品的更多细节描述于例如在2018年9月11日提交的、名称为“WAFER LEVEL SEQUENCING FLOWCELL FABRICATION,”的美国专利申请No.16/128,120,其通过引用整体并入本文。
在一些实施方案中,凹陷区域包含具有基本矩形的横截面的沟槽。在一些实施方案中,凹陷区域可包含具有基本正方形的横截面的沟槽。凹陷区域可以是具有基本金字塔形的横截面、基本圆形的横截面、基本椭圆形的横截面、基本金字塔形的横截面、基本圆形的横截面、或基本椭圆形的横截面的蚀刻区域。
在一些实施方案中,凹陷区域包含具有顶部开口的沟槽,该顶部开口具有基本矩形的横截面。在一些实施方案中,凹陷区域可包含具有顶部开口的沟槽,该顶部开口具有基本正方形的横截面。所述凹陷区域可以是具有顶部开口的蚀刻区域,所述顶部开口具有基本为金字塔形的横截面、基本为圆形的横截面、基本为椭圆形的横截面、基本为金字塔形的横截面、基本为圆形的横截面或基本为椭圆形的横截面。
在一些实施方案中,沟槽可以具有从200nm至300nm的宽度和从200至300nm的深度。在一些实施方案中,沟槽可具有从100nm至500nm的宽度和从100至600nm的深度。在一些实施方案中,沟槽可具有从20nm至500nm的宽度和从20至600nm的深度。在其他实施方案中,沟槽可具有基于生物样品的大小选择的宽度和深度,以提高光收集的效率。
在一些实施方案中,光敏结在p型基板中包含n+区。
在一些实施方案中,光电二极管可以包含覆盖在半导体基板的第二表面上的含金属层,以及覆盖含金属层的介电层。含金属层可以包含金属层或金属氧化物层。介电层可以包含氮化硅、氧化硅、其他介电材料或其组合。在一些实施方案中,光电二极管可以包含覆盖在半导体基板的第二表面上的金属氧化物层和覆盖在金属氧化物层上的硅氧化物层。
在一些实施方案中,含金属的层(例如,金属氧化物层)的厚度可以在50-150nm的范围内。在其他实施方案中,含金属层的厚度可以在20-400nm的范围内。介电层(例如,氧化物层)的厚度可以在50-150nm之间。在其他实施方案中,金属氧化物的厚度可以在20-400nm的范围内。
可以通过常规的半导体薄膜技术(例如化学气相沉积(CVD)、低温等离子体化学气相沉积(LPCVD)、等离子体增强化学气相沉积(PECVD)、溅射、物理气相沉积(PVD)和原子层沉积(ALD)等)形成如上所述的各种薄膜。
在一些实施方案中,光电二极管可包含覆盖半导体基板的第二表面的一个或多个介电层、覆盖一个或多个介电层的金属氧化物层以及覆盖金属氧化物层的氧化硅层。
在一些实施方案中,光电二极管可以包含具有氧化铪(HfO
在一些实施方案中,所述金属氧化物层包含阳极氧化铝(Al
根据一些实施方案,一种生物传感器可以具有背面照射互补金属氧化物半导体(CMOS)图像传感器,其包括电子电路层;和在所述电子电路层上的光敏层。所述光敏层包括多个光电二极管,所述多个光电二极管覆盖所述电子电路层。所述光电二极管中的每一个具有与所述电子电路层相邻的光敏结和与所述电子电路层相对的光接收表面。所述光接收表面包括覆盖所述光电二极管的背面中的凹陷区域的凹入表面,并且所述凹陷区域的尺寸和功能被设置以容纳核酸大分子。
在以上生物传感器的一些实施方案中,每个光电二极管都包含如本文所述的光电二极管。例如,图1示出了多个背面照射(BSI)CMOS生物传感器。在图1中,CMOS图像传感器层10包含多个光电二极管112。每个光电二极管都可以具有一种结构,该结构与以上结合图4-6描述的光电二极管相似,具有凹入表面,该凹入表面覆盖光电二极管的背面中的凹陷区域以用于接收样品,该凹入表面可以改善用于生物或化学分析的生物传感器中的光收集效率。
在一些实施方案中,所述电子电路层包括:介电层;和形成在所述第一介电层中的金属布线,其中所述金属布线被配置为将所述多个光电二极管耦合到外部设备。
在一些实施方案中,所述生物传感器还包括:在所述背面照射CMOS图像传感器上的钝化层。
在上述生物传感器的一些实施方案中,所述多个光电二极管中的每个光电二极管被配置为检测从所述多个核酸大分子中的核酸大分子上的荧光或化学发光标记发射的光。
在一些实施方案中,所述光从荧光标记的寡核苷酸探针发射,所述荧光标记的寡核苷酸探针与固定在所述斑点上的核酸扩增子杂交。
在一些实施方案中,所述光从与固定在所述斑点上的核酸扩增子杂交的荧光标记的引物延伸产物发射。
在一些实施方案中,所述核酸扩增子来自基因组DNA片段或cDNA文库。
在一些实施方案中,所述扩增子通过滚环扩增或桥聚合酶链式反应(PCR)形成。
在一些实施方案中,所述生物传感器还包括激发光源。
一些实施方案提供一种方法,其包括:提供背面照射互补金属氧化物半导体(CMOS)图像传感器。提供所述背面照射CMOS图像传感器包括:提供电子电路层;以及在所述电子电路层上提供光敏层。所述光敏层包括:电子电路层;和在所述电子电路层上的光敏层。所述光敏层包括多个光电二极管,所述多个光电二极管覆盖所述电子电路层。所述光电二极管中的每一个具有与所述电子电路层相邻的光敏结和由所述多个光电二极管的与所述电子电路层相对的表面限定的光接收表面。所述光接收表面包含覆盖所述光电二极管的背面中的凹陷区域的凹入表面。所述凹陷区域的尺寸和功能被设置以容纳核酸大分子。
在以上方法的一些实施方案中,每个光电二极管包括如本文所述的光电二极管。
在一些实施方案中,从所述斑点中包含的所述核酸大分子发射的所述光被一个光电二极管的所述光接收表面接收。
在一些实施方案中,从所述斑点中包含的所述核酸大分子发射的所述光从多于一个的光电二极管的所述光接收表面接收。
在一些实施方案中,提供所述电子电路层包括:沉积介电层;以及在所述介电层中形成金属布线。所述金属布线被配置为将所述多个光电二极管耦合到外部设备。
在一些实施方案中,所述方法还包括:在所述背面照射CMOS图像传感器上沉积钝化层。
在一些实施方案中,所述方法还包括:将所述多个核酸大分子中的核酸大分子附接于所述斑点中的斑点。
在一些实施方案中,所述方法还包括:使用所述多个光电二极管中的光电二极管检测从所述核酸大分子上的荧光或化学发光标记发射的光。
在一些实施方案中,所述光从与固定在所述斑点上的核酸扩增子杂交的荧光标记的寡核苷酸探针发射。
在一些实施方案中,所述光从与固定在所述斑点上的核酸扩增子杂交的荧光标记的引物延伸产物发射。
在一些实施方案中,所述核酸扩增子来自基因组DNA片段或cDNA文库。
在一些实施方案中,所述扩增子通过滚环扩增或桥聚合酶链式反应(PCR)形成。
在一些实施方案中,所述方法还包括:用激发光源照射所述核酸大分子。
根据一些实施方案,一种核酸测序方法包括迭代地执行过程,该过程包括以下步骤:
用荧光标记来标记核酸大分子,所述荧光标记识别所述核酸大分子中特定位置处的核苷酸碱基;
检测与所述核酸大分子相关的所述荧光标记,其中检测所述荧光标记包括:
用激发光照射所述核酸大分子,其中所述核酸大分子吸收所述激发光并使发射的光传输到达背面照射(BSI)互补金属氧化物半导体(CMOS)图像传感器的光电二极管上;
测量在所述光电二极管处接收的所述发射的光的至少一个参数;以及
将所述发射的光的所述至少一个参数与所述荧光标记相关联;以及
从所述核酸大分子中除去所述荧光标记。
在以上方法的一些实施方案中,每个光电二极管包括如本文所述的光电二极管。
根据一些实施方案,一种核酸测序方法包括迭代地执行过程,该过程包括以下步骤:
用化学发光标记来标记核酸大分子,所述化学发光标记识别所述核酸大分子中特定位置处的核苷酸碱基;
改变所述核酸大分子化学发光的环境,以使所述标记发射光;
其中使所发射的光传输到达背面照射(BSI)互补金属氧化物半导体(CMOS)图像传感器的光电二极管上;
测量在所述光电二极管处接收的所述发射的光的至少一个参数;以及
将所述发射的光的所述至少一个参数与所述化学发光标记相关联;以及
从所述核酸大分子中除去所述化学发光标记。
在以上方法的一些实施方案中,每个光电二极管包括如本文所述的光电二极管。
根据一些实施方案,一种生物传感器具有背面照射互补金属氧化物半导体(CMOS)图像传感器,其包括:电子电路层;以及在所述电子电路层上的光敏层。所述光敏层包括多个光电二极管,所述多个光电二极管覆盖所述电子电路层。所述光电二极管中的每一个具有与所述电子电路层相邻的光敏结和由所述多个光电二极管的与所述电子电路层相对的表面限定的光接收表面。所述光接收表面包含覆盖在所述光电二极管的背面中的凹陷区域的凹入表面。在所述光接收表面上方的保护层,其尺寸和功能被设置为包含多个核酸大分子。
在以上方法的一些实施方案中,每个光电二极管包括如本文所述的光电二极管。
上述生物或化学样品可包括许多组分中的任何一种。例如,样品可含有核酸大分子(例如模板、DNA、RNA等)、蛋白质等。可以分析样品以确定基因序列、DNA-DNA杂交、单核苷酸多态性、蛋白质相互作用、肽相互作用、抗原-抗体相互作用、葡萄糖监测、胆固醇监测等。
如上所述,在一些实施方案中,生物分子是核酸,例如DNA。参见美国专利No.8,778,849;No.8,445,194;No.9,671,344;No.7,910,354;No.9,222,132;No.6,210,891;No.6,828,100;No.6,833,246;No.6,911,345和专利申请公布No.2016/0237488,其全部内容通过引用并入本文。DNA生物分子可以是但不限于DNA纳米球(单链多联体),该DNA纳米球(单链多联体)与标记探针杂交(例如,通过附接或cPAL方法在DNB测序中)或与互补生长链杂交(例如,在通过合成方法的DNB测序中)或与两者杂交;或与单个DNA分子杂交(例如,在单分子测序中);或者与克隆的DNA分子群杂交,例如在基于桥式PCR的测序中产生的。因此,提及的“生物分子”、“DNA大分子”或“核酸大分子”可以包括多于一个分子(例如,与多个生长的互补链相关的DNB或包含数百或数千个DNA分子的克隆群的DNA簇)。用于制造DNB(例如,DNB库)和用于制造由区域间区域隔开的离散间隔区域的阵列的示例性方法在本领域中是众所周知的。参见,例如,美国专利No.8,133,719;No.8,445,196;No.8,445,197;和No.9,650,673,其全部内容通过引用并入本文。在一些实施方案中,DNB或其他大分子通过有吸引力的非共价相互作用(例如,范德华力、氢键和离子相互作用)固定在离散的间隔开的区域或斑点上。在一些实施方案中,离散的间隔开的区域包含功能性部分(例如,胺)。在一些实施方案中,离散的间隔开的区域包含附接于其上的捕获寡核苷酸,以结合模板DNA(例如,DNB)。通常,离散的间隔开的区域以直线图案布置;然而,可以使用具有其他布置的规则阵列(例如,区域的同心圆、螺旋形图案、六边形图案等)。
在一些实施方案中,核酸大分子可以是基因组DNA片段或cDNA文库的扩增子。如本文所使用的,“扩增子”可以是核酸分子扩增的产物,通常是基因组DNA片段或cDNA文库的片段。扩增的方法包括但不限于滚环扩增,如例如美国专利No.8,445,194(其全部内容通过引用并入本文)中所述,或桥式聚合酶链式反应(PCR),如例如在美国专利No.7,972,820(其全部内容通过引用并入本文)中所述。扩增可以在核酸与生物传感器接触之前进行,或者原位进行,例如,如美国专利No.7,910,354中所述,该专利其全部内容通过引用并入本文。
例如,可以将与荧光或化学发光染料缔合的生物样品(诸如DNA大分子、寡核苷酸或核苷酸)置于光电二极管上方。在荧光的情况下,可以通过来自激发光源的激发光照射染料。激发光可以对应于任何合适类型或强度的光,所述光包括例如可见光、红外光(IR)、紫外光(UV)等。激发光还可以来自任何合适的光源,例如发光二极管(LED)、灯、激光器、它们的组合等。当用特定波长的激发光照射染料时,生物样品可以吸收光,然后发射不同波长的光。例如,生物样品可以吸收具有450nm波长的激发光,但是发射具有550nm波长的光。换句话说,当染料被具有不同特征波长的光(即激发光源)照射时,可以发射具有特征波长的荧光。然而,因为激发光用于测量荧光,所以必须将其滤除以便在光电二极管112处进行精确测量。
在化学发光的情况下,光电二极管检测发射的光不需要激发光源。相反,生物样品可能由于以下原因而发光:生物样品和化学发光染料(或其他溶液)之间可能发生化学或酶促反应,导致由于破坏或形成化学键(例如,萤光素酶蛋白对萤光素底物的作用)而发光。
对于荧光和化学发光两者,光电二极管可以检测发射光的强度并将其转换成可以经由金属布线105提供给外部设备的基于该光的强度的电子信号。外部设备可以基于电子信号将电子信号与特定波长和亮度相关联。
在一些实施方案中,生物传感器的表面上的有效斑点或孔和核酸大分子可以相互配置,使得每个斑点仅结合一个核酸大分子。例如,这可以通过使表面与尺寸对应于有效斑点的扩增子(例如,直径有效地与有效斑点的直径一样大或大于有效斑点的直径的扩增子)接触来实现。参见美国专利No.8,445,194,其全部内容通过引用并入本文。替代地,有效斑点可以在化学上适合于结合单个DNA片段,然后可以扩增该片段以填充原始结合位点处和周围的较大区域。
本发明的一些实施方案可用于确定对应于不同波长的光的不同标记。标记可以是例如荧光标记、化学发光标记或生物发光标记。例如,在基因测序(或DNA测序)中,本发明的实施方案可用于确定核酸大分子(例如DNA链)内核苷酸碱基的精确顺序。可以用特定荧光标记物标记核苷酸碱基(例如腺嘌呤(A)、鸟嘌呤(G)、胞嘧啶(C)或胸腺嘧啶(T))。替代地,可以使用例如一种颜色、两种颜色或三种颜色的测序方法。
关于荧光,可以通过用激发光连续激发核酸大分子来依次确定每个核苷酸碱基。核酸大分子可以吸收激发光并将不同波长的发射光传输到生物传感器上,如本文所述。生物传感器可以测量由光电二极管接收的发射光的波长和强度。每个核苷酸(例如,荧光标记的核苷酸)当被特定波长和/或强度的激发光激发时可以向光电二极管发射特定波长和/或强度的光,从而使得能够识别在核酸大分子的特定位置存在特定的核苷酸碱基。一旦确定了特定的核苷酸碱基,就可以将其从核酸大分子中除去,从而可以根据类似的方法确定下一个连续的核苷酸碱基。
为了任何目的,核酸大分子在附接于生物传感器之前或之后,可以用一种或多种不同的荧光标记物、化学发光标记物或生物发光标记物标记。例如,核酸大分子可以与标记的寡核苷酸探针或扩增引物杂交。替代地,核酸大分子可以与未标记的寡核苷酸杂交,未标记的寡核苷酸然后可以附接到标记的探针上,或者使用标记的核苷酸类似物扩增。举例来说,可以进行标记以用于表征核酸大分子(例如,存在与疾病相关的单核苷酸多态性(SNP)),或者用于核酸大分子的全部或部分的核酸测序,如上文所述。通过探针杂交进行的DNA测序描述于例如美国专利No.8,105,771中,其全部内容通过引用并入本文。通过锚定探针附接的测序描述于例如美国专利No.8,592,150中,其全部内容通过引用并入本文。通过合成测序描述于例如美国专利No.7,883,869中,其全部内容通过引用并入本文。通常,通过合成测序是一种方法,其中将核苷酸连续地添加到与模板序列杂交的测序引物所提供的游离3'羟基上,从而导致在5'至3'方向上的核酸链的合成。在一种方法中,可以使用另一种示例性类型的SBS,焦磷酸测序技术(Ronaghi等人,1998,Science 281:363)。
在一些实施方案中,生物传感器可以可逆地耦合到流通池(未示出)。通过使生物传感器与流通池中的液体样品接触,可以将核酸大分子附接到生物传感器。流通池可包括一个或多个与反应位点流体连通的流动通道。在一个示例中,生物传感器可以流体地和电气地耦合到生物测定系统。生物测定系统可根据预定方案将试剂递送至反应位点并执行成像事件。例如,生物测定系统可以引导溶液沿着反应位点流动。该溶液可包括具有相同或不同荧光标记的四种类型的核苷酸。在一些实施方案中,然后,生物测定系统可以使用激发光源照射反应位点。激发光可以具有预定的一种或多种波长。激发的荧光标记可以提供可以由光电二极管检测到的发射信号。
用户可以通过将根据所述实施方案的生物传感器与核酸扩增子或随后扩增的核酸接触来准备测序,使得核酸大分子结合有效斑点或孔并被有效斑点或孔保留,并且可以洗去过量的核酸大分子。核酸大分子可以与标记试剂预先或原位接触。然后可以如本文所述操作生物传感器以确定在阵列上的核酸大分子上或周围发射的光。可以量化光,或者可以足以以二元方式确定表面上的哪些核酸大分子已经用在特定波长下发光的标记物标记。可以同时使用具有在不同波长下发射光的标记物的不同探针或不同核酸类似物,例如,以确定序列中特定位置的不同碱基,或对多个位置进行测序。
尽管本文关于背侧照射CMOS传感器进行了描述,但是可以预期本发明的实施方案可以类似地应用于正侧照射CMOS传感器。此外,预期本发明的实施方案可以类似地应用于任何合适的生物传感器,例如2016年11月3日提交的美国临时专利申请No.62/416,813中描述的那些生物传感器,其全部内容通过引用并入本文。
根据本发明的实施方案的生物传感器不限于特定用途。在一个方面,发现本发明的实施方案的生物传感器特别适用于大规模平行DNA测序。DNA测序技术是众所周知的(参见,例如,Drmanac et al.,2010,“Human genome sequencing using unchained basereads on self-assembling DNA nanoarrays,”Science 327:78-81;Shendure&Ji,(2008,“Next-generation DNA sequencing,”Nature Biotechnology 26:1135-45),并且因此在下面的章节中仅以一般术语进行描述。以下段落提供了对测序和相关术语的简要初步讨论,以便下面描述的生物传感器的某些特征可以被更容易理解。
已知多种DNA测序方法。在许多方式中,大分子(例如基因组DNA)被分解成许多较小的片段,每个片段具有特征性的DNA序列。在基于阵列的技术中,这些片段被分布到基板上的位置阵列,使得阵列中的每个位置包含具有单个特征序列的DNA片段。序列信息(“读数”)是同时从数千个或更通常地从数百万个位置中的每一个处的DNA获得并由计算机组装的。在大多数测序方式中,在序列测定之前扩增片段。扩增可以在片段定位在每个位置之前进行,在片段定位在每个位置之后进行,或者在定位之前和之后进行。扩增步骤产生在测序过程中用作“模板”的“扩增子”。因此,为了说明,扩增可以使用RCA在阵列上的每个位置产生单链多联体(例如,DNA纳米球)或使用桥式PCR在每个位置产生具有相同序列的DNA分子的克隆群(或簇)。
应当理解,提及“DNA大分子”等包括DNA纳米球、分支结构和成簇克隆群(即多于单个的分子)或它们的前体。另外,“DNA大分子”等可以包括辅助DNA分子,例如引物以及通过引物延伸生产的或其他过程包括的生长链。在许多测序技术中,辅助DNA分子包含(或被“标记”有)可检测的(例如荧光或化学发光)染料,其发射由生物传感器的光电二极管检测的光。因此,诸如“用激发光源照射核酸大分子并检测从大分子发射的光”之类的短语应被理解为包括“将DNA纳米球或克隆簇和相关的标记的辅助分子暴露于激发光源并检测从标记的辅助分子的染料发出的光”。
在基于阵列的测序方法和本发明实施方案的生物传感器中,DNA大分子位于在孔中或“斑点”上的基板上。孔或斑点能够接收和保留大分子。通常,斑点,有时称为“离散的间隔区域”或“垫”,包括被功能化以接收核酸大分子的基板,并且斑点被“惰性”的区域分开,“惰性”意指DNA大分子不结合这样的区域。例如但不限于,见Drmanac 2010,supra.“孔”是一种包含壁的斑点,壁形成DNA大分子的边界或屏障。除非根据上下文中显而易见,否则下面提到的“斑点”可以包括孔。
在本发明实施方案的生物传感器中,斑点通常具有均匀的尺寸并且被组织为规则(即非随机)阵列。阵列的斑点通常以直线图案组织,通常以列和行的形式组织,但是可以使用其他规则图案(例如,螺旋形)。阵列的斑点可具有特征尺寸、间距和密度。斑点本身可以是圆形、正方形、六边形或其他形状。在下面的讨论中,通常假定斑点是圆形的(即,可以描述为具有直径)。应当理解,提及的“直径”也可以指其他形状的斑点的线性尺寸(例如,对角线、长度或宽度)。因此,如本文所使用的,“线性尺寸”可以指圆的直径、正方形的宽度、对角线等。在本发明实施方案的生物传感器的背景下,斑点的大小在两种方式上有意义。首先,可以以限制对单个靶序列的占据的方式确定斑点尺寸和/或功能化斑点。这可以是单个DNA纳米球(单个靶序列的多联体)或具有单个靶序列的克隆簇。参见,例如,美国专利No.8,133,719和美国专利申请公布No.2013/0116153,两者均出于所有目的通过引用整体并入。其次,通常可以相对于下伏的光电二极管设定斑点的大小和位置,使得每个光电二极管接收来自单个斑点的发射的光。在一些实施方案中,斑点的阵列可以以1对1的相关性定位在相应光电二极管(和/或滤色器)的阵列上。也就是说,从单个斑点处的例如DNA大分子发射的光传递到下伏的滤光器,并且未被滤光器阻挡的光被与滤光器相关联的单个光电二极管检测到,或从在单个斑点处的例如DNA大分子发射的光传递到多个下伏的滤光器,每个与滤光器(特定于特定波长)相关联,每个滤光器与单个光电二极管相关联,并且未被滤光器阻挡的光被相关的光电二极管检测到。因此,如下面还讨论的,在一些实施方案中,从单个斑点发射的光可以由多于一个的光电二极管(例如,2个光电二极管、3个光电二极管、4个光电二极管等)检测。在这些实施方案中,与单个斑点相关联的多个光电二极管组可以被称为光电二极管的“单位单元”。斑点和滤光器(例如,单个滤光器或单位单元)可以布置在生物传感器中,使得单位单元中的每个光电二极管接收从相同的单个斑点发射的光。另外,在一些实施方案中,光电二极管的光接收表面的区域,或与同一斑点相关联的多个光电二极管的光接收表面的组合区域小于斑点的区域(光从该区域发射)。换句话说,斑点可以小于下伏的光电二极管,使得斑点的边界如果被投射到光电二极管的光接收表面上,则包含在光接收表面内。
众所周知,核酸测序通常涉及迭代过程,其中荧光或化学发光标记以特定方式按序列与被测序的DNA模板(扩增子)相关联,检测到该关联性,并且标记在它不再发出信号的意义上被删除。参见,例如,美国专利申请公布No.2016/0237488;美国专利申请公布No.2012/0224050;美国专利No.8,133,719;美国专利No.7,910,354;美国专利No.9,222,132;美国专利No.6,210,891;美国专利No.6,828,100,美国专利No.6,833,246;和美国专利No.6,911,345,其全部内容通过引用并入此处。因此,应当理解,例如,“用荧光标记来标记核酸大分子”可以指将标记的辅助分子与固定在斑点上的DNA模板相关联。
如上文所述,生物或化学样品可以放置在光电二极管上方的每个所述生物传感器上。生物或化学样品可以包括许多组分中的任何一种。例如,样品可含有核酸大分子(例如DNA、RNA等)、蛋白质等。可以分析样品以确定基因序列、DNA-DNA杂交、单核苷酸多态性、蛋白质相互作用、肽相互作用、抗原-抗体相互作用、葡萄糖监测、胆固醇监测等。
如上所述,在一些实施方案中,生物分子是核酸,例如DNA。DNA生物分子可以是但不限于DNA纳米球(单链多联体),该DNA纳米球(单链多联体)与标记探针杂交(例如,通过连接或cPAL方法在DNB测序中)或与互补生长链杂交(例如,在通过合成方法的DNB测序中)或与两者杂交;或与单个DNA分子杂交(例如,在单分子测序中);或者与克隆的DNA分子群杂交,例如在基于桥式PCR的测序中产生。因此,提及的“生物分子”、“DNA大分子”或“核酸大分子”可以包括多于一个的分子(例如,与多个生长的互补链相关的DNB或包含数百或数千个DNA分子的克隆群的DNA簇)。参见,例如,美国专利No.8,133,719;美国专利申请公布No.2013/0116153,美国专利申请公布No.2016/0237488;美国专利申请公布No.2012/0224050;美国专利No.8,133,719;;美国专利No.7,910,354;美国专利No.9,222,132;美国专利No.6,210,891;美国专利No.6,828,100,美国专利No.6,833,246;和美国专利No.6,911,345,在此通过引用全部并入。
为了实现高密度并有助于核酸大分子与生物传感器的光电二极管之间的对准,可以构建生物传感器的表面使得存在大小和化学功能被设定以接收核酸大分子的有效斑点或孔(例如,在图3-5中的凹陷区域),所述有效斑点或孔被核酸大分子可能不结合的表面区域包围。可以使用任何合适的表面化学过程将核酸大分子固定到与光电二极管对准的活性表面上。这可以包括非共价相互作用(例如,与带有正电荷的区域的非共价相互作用)或与附接于表面的捕获探针或寡核苷酸(其带有与核酸大分子中包含的序列互补的序列)的相互作用。参见,例如,美国专利No.8,445,194,其全部内容通过引用并入本文。
生物或化学样品可以包括许多组分中的任何一种。例如,样品可含有核酸大分子(例如DNA、RNA等)、蛋白质等。可以分析样品以确定基因序列、DNA-DNA杂交、单核苷酸多态性、蛋白质相互作用、肽相互作用、抗原-抗体相互作用、葡萄糖监测、胆固醇监测等。
尽管关于以特定顺序执行的特定数量的步骤描述了本文描述的过程,但是预期可以包括未明确示出和/或描述的附加步骤。此外,预期,在不脱离所描述的实施方案的范围的情况下,可以包括比所示出和描述的步骤更少的步骤(即,所描述的步骤中的一个或一些可以是可选的)。另外,预期本文描述的步骤可以以与所描述的顺序不同的顺序执行。
在前面的描述中,参考本申请的具体实施方案描述了本申请的各方面,但是本领域技术人员将认识到,本发明不受限于此。因此,虽然本文已经详细描述了本申请的说明性实施方案,但是应该理解,可以以其他方式不同地实施和使用本发明构思,并且所附权利要求意在被解释为包括这样的变型,除了被现有技术限制。上述发明的各种特征和方面可以单独使用或联合使用。此外,在不脱离本说明书的更广泛的精神和范围的情况下,实施方案可以在除了本文描述的那些之外的任何数量的环境和应用中利用。因此,说明书和附图应被视为说明性的而非限制性的。出于说明的目的,以特定顺序描述方法。应当理解,在替代的实施方案中,可以以与所描述的顺序不同的顺序执行所述方法。
其他变化在本公开的精神内。因此,尽管所公开的技术易于进行各种修改和替换构造,但是其某些图示的实施方案在附图中示出并且已在上面详细描述。然而,应该理解的是,并不意图将本公开限制于所公开的一种或者多种特定形式,而是相反,意图是覆盖落入如所附权利要求中所定义的本公开的精神和范围内的所有修改、替代构造和等同方案。
- 改善生物传感器光收集效率的方法和结构
- 改善CIS芯片炫光问题的晶圆级封装方法以及封装结构
