一种实时荧光恒温核酸扩增检测装置
文献发布时间:2023-06-19 12:24:27
技术领域
本发明涉及核酸检测领域,特别是涉及一种实时荧光恒温核酸扩增检测装置。
背景技术
微型全分析系统(Miniaturized Total Analysis Systems)概念自20世纪90年代首次提出,此后在微电子、微机械、生物工程和纳米技术的基础上,微流控技术迅速发展起来,成为当前世界最前沿的科技领域之一。目前其核心技术是以微流控技术为基础的微流控芯片,又称芯片实验室(Lab on chip)。微流控芯片技术(Microfluidics)是把生物、化学、医学分析过程的样品制备、反应、分离、检测等基本操作单元集成到一块微米尺度的芯片上,自动完成分析全过程。微流控芯片因为具有低消耗、低成本、高通量、自动化操作等优势,广泛用于生物医学领域,其中一个重要的应用就是基于微流控芯片的核酸检测技术。
传统的核酸检测技术以PCR技术(英文:Polymerase Chain Reaction中文:聚合酶链式反应)为主,在不同的三个温度间进行多次反复的转换,来完成核酸的迅速扩增,但对设备要求很高,且需要至少一至两小时,效率不高。而恒温扩增技术只需要一个温度,减少了设备要求,提高了效率。尽管如此,现有的恒温核酸扩增设备结构较复杂,操控复杂,对控制方面要求高,使用起来不够灵活便捷,且成本较高,仍然存在很大的优化空间。
需要说明的是,在上述背景技术部分公开的信息仅用于对本申请的背景的理解,因此可以包括不构成对本领域普通技术人员已知的现有技术的信息。
发明内容
本发明的主要目的在于克服上述背景技术的缺陷,提供一种实时荧光恒温核酸扩增检测装置。
为实现上述目的,本发明采用以下技术方案:
一种实时荧光恒温核酸扩增检测装置,包括微流控单元、温控单元、激发光单元、检测单元以及安装杆,其中,含有荧光染料的反应液在所述微流控单元中进行荧光恒温核酸扩增反应,所述温控单元向所述微流控单元提供核酸扩增所需的恒温,所述激发光单元产生激发光以激发所述微流控单元中的反应液中的荧光染料,使其产生荧光,所述检测单元对所述微流控单元中的反应液产生的荧光信息进行采集,以得到检测结果;其中,所述微流控单元、所述激发光单元、所述检测单元一同安装在所述安装杆上,所述激发光单元和所述检测单元位于所述微流控单元的上方,且至少所述检测单元在所述安装杆上相对于所述微流控单元的位置和/或角度可调。
进一步地:
所述安装杆的底部设置有起地面支撑作用的底板。
所述温控单元安装在所述安装杆上,所述微流控单元安置于所述温控单元上。
所述温控单元包括支撑板、导热外壳、加热器、温度传感器,所述支撑板与所述安装杆连接,所述导热外壳位于所述支撑板上侧,所述加热器设置在所述导热外壳中,所述微流控单元安置于所述导热外壳上,所述温度传感器紧贴所述导热外壳的靠近所述微流控单元一侧的表面,外部温度控制器与所述加热器和所述温度传感器连接以进行温度控制,来保持反应所需的恒温。
所述导热外壳包括组装在一起的下侧铝合金外壳和上侧铝合金外壳,所述加热器为胶粘连接所述下侧铝合金外壳内壁上的硅橡胶加热器,所述温度传感器用耐热胶固定连接所述上侧铝合金外壳的内表面。
所述激发光单元包括底板、第一螺钉、光源支架和激发光源装置,所述光源支架的一侧通过所述第一螺钉固定在所述安装杆上,另一侧固定所述激发光源装置,所述激发光源装置包括光源外壳、设置在所述光源外壳中的灯珠底座、灯珠、激发光滤光片以及聚光透镜,所述灯珠设置在所述灯珠底座上,所述激发光滤光片设置在所述灯珠的前侧,所述聚光透镜设置在所述激发光滤光片的前侧;优选地,所述灯珠、所述激发光滤光片、所述聚光透镜与所述微流控芯片中心的连线与竖直线的夹角为15~75°,所述聚光透镜与所述微流控芯片中心的距离为5~30cm。
所述检测单元包括第二螺钉、内圆环、上端有螺柱的外圆环、内圈有螺纹的圆柱件、结构杆件、第三螺钉、镜头支架、相机模块、第四螺钉、连接结构件、带有杆的旋钮、带有齿的长条、中间连接件及L形件,所述连接结构件通过所述第四螺钉固定在所述安装杆上,使得所述检测单元能够沿所述安装杆移动,所述旋钮设置所述连接结构件上,所述旋钮所带的杆上有齿,与所述带有齿的长条啮合以带动所述长条上下移动,所述中间连接件位于所述带有齿的长条和所述L形件之间,所述中间连接件与所述带有齿的长条连接,所述中间连接件与所述L形件的一侧连接,所述L形件的带有孔的另一侧位于所述圆柱件和所述外圆环之间,所述螺柱穿过所述孔与所述圆柱件的内圈螺纹连接,所述内圆环位于所述外圆环和所述结构杆件之间,与所述外圆环过盈配合,并与所述结构杆件之间存在间隙以使所述结构杆件可在所述内圆环内转动,所述内圆环与所述外圆环的对应位置有圆孔,所述第二螺钉与所述圆孔螺纹连接并固定所述结构杆件的位置,所述结构杆件的前端有凸起的圆柱,所述镜头支架可绕圆柱转动,并通过所述第三螺钉固定在所述凸起的圆柱上,所述相机模块安装在所述镜头支架上。
所述相机模块包括前端带有发射光滤光片的镜头以及工业相机,所述镜头安装在所述工业相机的前端,所述镜头和所述工业相机卡接在所述镜头支架的对应位置上。
所述微流控芯片包括从下至上依次层叠在一起的基底层、中间层和表面层,所述中间层包括多个加样孔、多个气孔、多个分液腔和多个反应腔及流道,所述加样孔用于加入反应液并流动至所述分液腔,所述气孔使流体能够在芯片内流动,所述分液腔通过所述流道分配反应液到多个所述反应腔。
所述中间层的材料选自用聚氯乙烯(PVC),聚乙烯(PE)、聚丙烯(PP)、聚苯乙烯(PS)、聚碳酸酯(PC)中任一种,所述基底层、所述表面层与所述中间层通过胶粘的方式键合,所述基底层与所述表面层为厚度为0.02~0.1mm的超薄胶带,所述反应腔的容积为5~10μl。
本发明具有如下有益效果:
本发明提出了一种实时荧光恒温核酸扩增检测装置,实现待检测样品中核酸恒温扩增及实时荧光检测,该装置中,将微流控单元、激发光单元、检测单元一同安装在一个安装杆上,激发光单元和检测单元位于微流控单元的上方,且至少检测单元在安装杆上相对于微流控单元的位置和/或角度可调,通过安装在同一安装杆上的各单元的配合,该装置可以实现方便、快速地实现高通量的核酸检测,且装置的结构简单,成本较低,操作与调节灵活、便捷,不仅可进行可靠的检测,而且提高了检测效率,保证检测结果的可靠、稳定及快速的获得。本发明能够很好地满足临床、疫病检测等快速检测的需求,尤其适于在资源匮乏地区应用。
附图说明
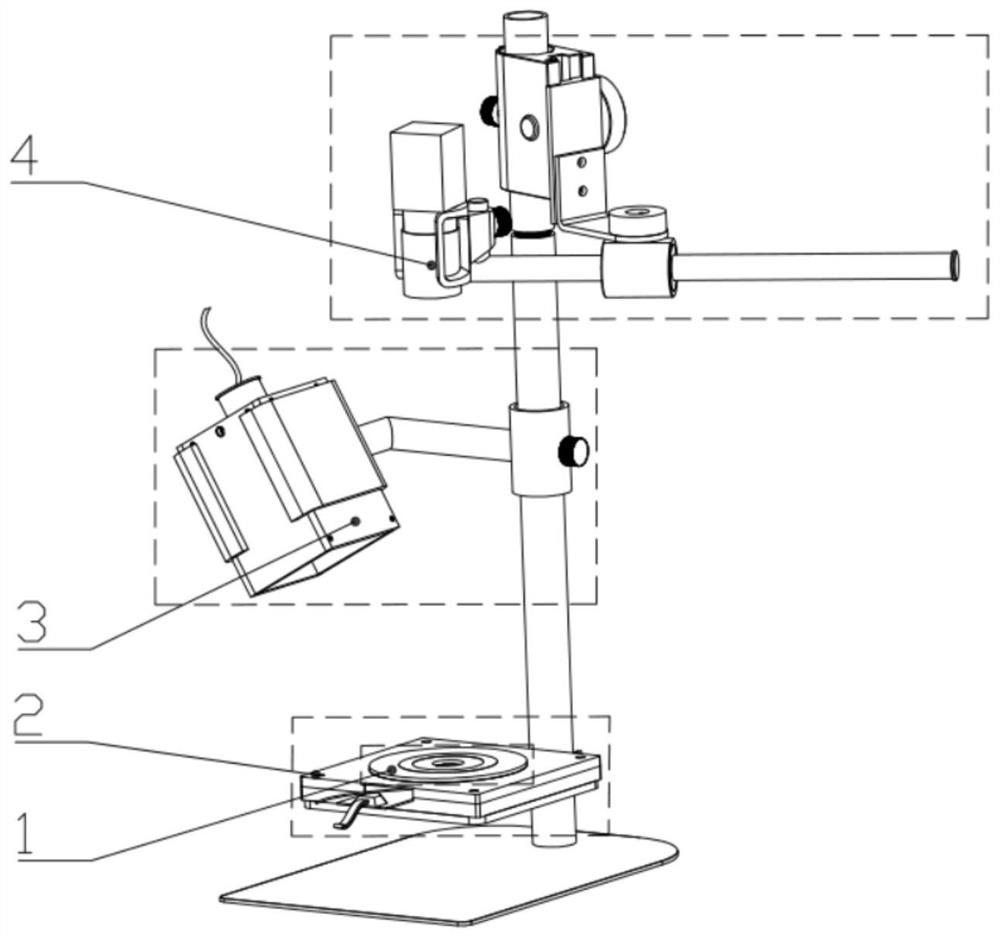
图1为本发明一种实施例的实时荧光恒温核酸扩增检测装置的结构示意图;
图2为图1中所示的微流控单元的结构示意图;
图3为图1中所示的温控单元的结构示意图;
图4为图1中所示的激发光单元的整体结构示意图;
图5为图4中所示的激发光源装置的具体结构示意图;
图6为图1中所示的检测单元的结构示意图;
图7为图1中所示的检测单元的爆炸结构示意图;
图8为本发明实施例检测的实时荧光强度曲线图。
具体实施方式
以下对本发明的实施方式做详细说明。应该强调的是,下述说明仅仅是示例性的,而不是为了限制本发明的范围及其应用。
需要说明的是,当元件被称为“固定于”或“设置于”另一个元件,它可以直接在另一个元件上或者间接在该另一个元件上。当一个元件被称为是“连接于”另一个元件,它可以是直接连接到另一个元件或间接连接至该另一个元件上。另外,连接既可以是用于固定作用也可以是用于耦合或连通作用。
需要理解的是,术语“长度”、“宽度”、“上”、“下”、“前”、“后”、“左”、“右”、“竖直”、“水平”、“顶”、“底”“内”、“外”等指示的方位或位置关系为基于附图所示的方位或位置关系,仅是为了便于描述本发明实施例和简化描述,而不是指示或暗示所指的装置或元件必须具有特定的方位、以特定的方位构造和操作,因此不能理解为对本发明的限制。
此外,术语“第一”、“第二”仅用于描述目的,而不能理解为指示或暗示相对重要性或者隐含指明所指示的技术特征的数量。由此,限定有“第一”、“第二”的特征可以明示或者隐含地包括一个或者更多该特征。在本发明实施例的描述中,“多个”的含义是两个或两个以上,除非另有明确具体的限定。
参阅图1,本发明实施例提供一种实时荧光恒温核酸扩增检测装置,该核酸扩增检测装置包括微流控单元1、温控单元2、激发光单元3、检测单元4以及安装杆18,其中,含有荧光染料的反应液在微流控单元1中进行荧光恒温核酸扩增反应,温控单元2向微流控单元1提供核酸扩增所需的恒温,激发光单元3产生激发光以激发微流控单元1中的反应液中的荧光染料,使其产生荧光,检测单元4对微流控单元1中的反应液产生的荧光信息进行采集,通过对采集的荧光信息进行分析,可以得到检测结果;其中,微流控单元1、激发光单元3、检测单元4一同安装在安装杆18上,激发光单元3和检测单元4位于微流控单元1的上方,且至少检测单元4在安装杆18上相对于微流控单元1的位置和/或角度可调。
在优选的实施例中,温控单元2安装于安装杆18上,在微流控单元1的下方提供核酸扩增所需的恒温的同时,也为微流控单元1提供支撑平台,以将微流控单元1间接安装到安装杆18上。在其他实施例中,微流控单元1也可以通过安装部件直接安装到安装杆18上,而温控单元2可以附接或不附接到安装杆18上,只要能向提供微流控单元1提供恒温反应条件即可。
本发明实施例可以方便地实现荧光恒温核酸扩增反应及检测,其操作控制灵活方便,且该检测装置结构简单,成本较低,可同时检测多项指标,保证检测结果的可靠、稳定及快速获得。
如图1所示为一个典型实施例的实时荧光恒温核酸扩增检测装置,该装置包括安装杆18以及安装在安装杆18上的微流控单元1,温控单元2,激发光单元3和检测单元4。
如图2所示为微流控单元1的结构示意图,微流控芯片由基底层5、中间层10、表面层11组成,基底层5与中间层10通过胶粘的方式进行键合,保证密封性和热稳定性;表面层11与中间层10通过胶粘的方式来密封气孔9和加样孔6,防止污染。基底层5位于下侧,中间层10位于基底层5的上侧,表面层11位于中间层10的上侧。中间层10包括多个加样孔6、多个气孔9、多个分液腔7和多个反应腔8,加样孔6用于反应液加入,气孔9的作用是离心时能使流体在芯片内流动,分液腔7通过相连的流道等分反应液到多个反应腔8,之后所述反应腔8内含有包含荧光染料的反应液,可进行核酸扩增反应。
中间层10的材料采用常见的透明医用塑料,比如聚氯乙烯(PVC),聚乙烯(PE)、聚丙烯(PP)、聚苯乙烯(PS)、聚碳酸酯PC,采用模压热塑成型、注塑成型等多种塑料成型方式;比如采用注塑成型的方法,预先加工出模具,然后将聚丙烯(PP)材料在恒温料筒220-280℃中融化,然后加压800-140MPa将融化后的PP材料注入模具,之后保压、冷却成型。基底层5与表面层11均为键合效果好的超薄胶带,厚度为0.02~0.1mm。微流控芯片内反应腔8体积为5~10μl。微流控芯片内的流体通过离心机来驱动,从分液腔7通过相连的流道流到反应腔8,完成分液。离心机的转速为1000~5000rpm,时间为10~60s,仅需离心一次。
如图3所示为温控单元2的结构示意图,位于微流控芯片的下方,用于提供恒温核酸扩增所需的温度,包括底板12、支撑板13、下侧铝合金外壳14、硅橡胶加热器15、温度传感器16、上侧铝合金外壳17、安装杆18及外部温度控制器。底板12与安装杆18通过螺纹连接,起地面支撑作用。支撑板13与安装杆18通过螺栓螺母连接,起固定支撑温控单元2,确定温控单元2位置的作用。下侧铝合金外壳14位于支撑板13上侧;上侧铝合金外壳17位于下侧铝合金外壳14上侧,起导热和提高温度均匀性的作用。硅橡胶加热器15为加热元件,紧贴下侧铝合金外壳14内壁上,通过胶粘的方式连接。温度传感器16紧贴上侧铝合金外壳17的内表面,用耐热胶固定。上侧铝合金外壳17、硅橡胶加热器15、下侧铝合金外壳14和支撑板13对应位置都开孔,可通过四个螺钉螺母固定在一起。外部温度控制器用于进行温度控制,来保持反应所需的恒温。
底板12材质为钢,位于支撑板13下侧。安装杆18材质为铝合金,安装杆18可分为两段,两段杆通过螺纹连接。支撑板13的材质为黑色耐热树脂。温度传感器16可以为K型热电偶、pt100温度传感器等类型。上侧铝合金外壳17的上表面喷涂一层漆,来增加漫反射,减少对荧光图像的影响。
温控单元2的实现流程如下:在外部温度控制器上设定扩增反应的恒温温度,然后硅橡胶加热器13加热上侧铝合金外壳17和下侧铝合金外壳14内部的空气,使得上侧铝合金外壳17上表面温度升高,然后再加热微流控芯片反应腔8内的反应液到达扩增反应的恒温,温度传感器16进行实时温度反馈,进行温度调节,使反应腔8内的反应液保持恒温,核酸扩增反应不断进行。
如图4所示为激发光单元3的整体结构示意图,激发光单元用于激发所述微流控芯片反应腔内的反应液中的荧光染料使其产生荧光,包括底板12、安装杆18、激发光源装置21、光源支架20、第一螺钉19及外部光源功率控制器。光源支架20一侧通过第一螺钉19固定在安装杆18的相应位置,另一侧固定夹紧激发光源装置19,可通过胶粘方式实现。
如图5为图4中激发光源装置21的具体结构示意图,包括灯珠底座22、灯珠23、激发光滤光片24、聚光透镜25及光源外壳26。灯珠23焊接在灯珠底座22上,产生激发光。激发光滤光片24放在灯珠23的前侧,起滤光作用。聚光透镜25放在激发光滤光片24的前侧,起聚光作用。激发光滤光片24和聚光透镜25放置在光源外壳26的相应位置。光源外壳26包含五个侧面,材质为黑色铝合金,起固定支撑及散热作用。
灯珠23的数量为1~20个,总功率为0.3~5W,激发光滤光片24与灯珠23的波长选择与荧光染料的激发光波长相适应。灯珠23、激发光滤光片24、聚光透镜25与微流控芯片中心的连线与竖直线的夹角在15~75°,聚光透镜25与微流控芯片中心的距离在5~30cm。光源外壳26各个侧面之间通过螺钉来连接。外部光源功率控制器控制灯珠23的功率。
检测单元4用于通过所述工业相机对所述微流控芯片的反应腔内的反应液产生的荧光图像信息进行采集,并进行软件分析,得到检测结果。如图6所示为检测单元4的结构示意图,图7所示为检测单元4的爆炸结构示意图,检测单元4包括第二螺钉27、塑料内圆环28、上端有螺柱的铝合金外圆环29、内圈有螺纹的圆柱件30、结构杆件31、第三螺钉32、前端带有发射光滤光片的镜头33、镜头支架34、工业相机35、第四螺钉36、连接结构件37、带有杆的旋钮38、带有齿的长条39、中间连接件40及L形件41。连接结构件37通过第四螺钉36固定在安装杆18上,使得检测单元4能够沿安装杆18移动。带有杆的旋钮38放置在连接结构件37内,杆上有齿,与带有齿的长条39啮合带动长条上下移动。中间连接件40在带有齿的长条39和L形件41之间,中间连接件40与带有齿的长条39通过螺丝螺母连接,中间连接件40与L形件41一侧通过螺钉连接。L形件41另一侧在内圈有螺纹的圆柱件30和上端有螺柱的铝合金外圆环29之间,三者的中心在同一轴线上,这使得铝合金外圆环可以转动,确定好位置后,可通过螺纹连接使三者固定。塑料内圆环28在上端有螺柱的铝合金外圆环29和结构杆件31之间,与上端有螺柱的铝合金外圆环29以过盈配合方式连接,与结构杆件31之间存在间隙。塑料内圆环28、上端有螺柱的铝合金外圆环29的对应位置有圆孔,上端有螺柱的铝合金外圆环29的对应位置内有螺纹,第二螺钉27以螺纹连接方式固定结构杆件31的位置,结构杆件31可在塑料内圆环28内转动。结构杆件31的前端有凸起的圆柱,镜头支架34可绕圆柱转动,通过第三螺钉32固定在凸起的圆柱上。前端带有发射光滤光片的镜头33安装在工业相机35前端,然后二者卡在镜头支架34对应位置上,起荧光信息采集作用。
工业相机35为CCD或CMOS类型,镜头是焦距为2.8mm~12mm的变焦镜头,镜头前端的发射光滤光片的波长选择与荧光染料的发射波长相适应。除工业相机和镜头外,其余部分的协调作用为工业相机提供了一个位置可调节的万向支架。
检测单元4用于采集激发光单元3产生的激发光照射微流控芯片内的反应腔8内反应液产生的荧光图像,然后进行荧光图像传输及图像处理,来获得多个反应腔8内的实时荧光强度信息,即检测结果,检测结果可用于判断反应液是否为阳性。
以下简述使用本发明实施例的实时荧光恒温核酸扩增检测装置进行核酸检测的过程:
1)用注射枪以200μL/min的速度从中间层10的多个加样孔6分别灌注适量反应液到多个分液腔7室中,然后将微流控芯片放到离心机上,以一定转速离心一段时间,使得分液腔7内的液体全部流到反应腔8内,之后用表面层11密封住加样孔6和气孔9;
2)将微流控芯片放在上侧铝合金外壳17表面,打开总电源,激发光单元3、温控单元2、检测单元4开始工作,设定好恒温温度,开始进行实时荧光检测,20~30min后即可得到检测结果;
3)检测完成后,关闭电源,可将微流控芯片取出。
如图8所示为实时荧光强度曲线图,即核酸检测的结果,可判断反应液是否为阳性。核酸检测装置适用的核酸扩增反应包括LAMP(环介导恒温扩增技术)、RPA(重组酶聚合酶扩增技术)等恒温核酸扩增技术。
利用本发明进行荧光核酸恒温扩增及检测,具有快速、简单、稳定、可靠、控制灵活方便等优点,能够很好地满足临床、疫病检测等快速检测的需求。
本发明的背景部分可以包含关于本发明的问题或环境的背景信息,而不一定是描述现有技术。因此,在背景技术部分中包含的内容并不是申请人对现有技术的承认。
以上内容是结合具体/优选的实施方式对本发明所作的进一步详细说明,不能认定本发明的具体实施只局限于这些说明。对于本发明所属技术领域的普通技术人员来说,在不脱离本发明构思的前提下,其还可以对这些已描述的实施方式做出若干替代或变型,而这些替代或变型方式都应当视为属于本发明的保护范围。在本说明书的描述中,参考术语“一种实施例”、“一些实施例”、“优选实施例”、“示例”、“具体示例”、或“一些示例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不必须针对的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任一个或多个实施例或示例中以合适的方式结合。在不相互矛盾的情况下,本领域的技术人员可以将本说明书中描述的不同实施例或示例以及不同实施例或示例的特征进行结合和组合。尽管已经详细描述了本发明的实施例及其优点,但应当理解,在不脱离专利申请的保护范围的情况下,可以在本文中进行各种改变、替换和变更。
- 一种实时荧光恒温核酸扩增检测装置
- 一种实时荧光核酸恒温扩增检测试剂盒及其应用
