用于消泡的改进的脂肪酶
文献发布时间:2023-06-19 13:48:08
技术领域
本申请要求2019年3月15日提交的美国临时专利申请号62/819029的优先权,所述申请的公开内容通过引用以其全文并入。
公开了涉及用于例如在碳水化合物发酵工艺中减少发泡的改进的杂交脂肪酶的组合物和方法。
背景技术
许多商业产品是在利用“细胞工厂”(通常是微生物)的发酵工艺中生产的。在此类工艺中可能产生大量泡沫,这会降低每单位发酵罐体积的有效容量,并可能导致发酵液通过通风口从发酵罐溢出。
发泡可能是在使用碳水化合物底物和酵母作为发酵生物的燃料乙醇生产中的特殊问题。当在发酵期间或发酵上游添加蛋白酶时,发泡似乎加剧。
之前已在例如WO 2004029193、WO 2008135547和WO 201875430中描述了脂肪酶用于在燃料乙醇生产中减少发泡的用途。尽管如此,仍需要成本更低的优异抑泡酶。
发明内容
本发明的组合物和方法涉及改进的变体脂肪酶多肽及其使用方法。本发明的组合物和方法的方面和实施例总结在以下分别编号的段落中:
1.在第一方面,提供了一种变体疏棉状嗜热丝孢菌(Thermomyces lanuginosus)脂肪酶,所述脂肪酶与SEQ ID NO:4的氨基酸序列具有至少95%、任选地至少98%和任选地至少99%的氨基酸序列同一性,并且在发酵工艺中与具有SEQ ID NO:5的氨基酸序列的参照脂肪酶相比具有改进的消泡活性,其中所述变体脂肪酶包含:疏棉状嗜热丝孢菌脂肪酶的基本上整个连续氨基酸序列,所述氨基酸序列参考SEQ ID NO:4包含N-末端、具有选自由以下组成的组的一个或多个取代:G91A、D96W和E99K;作为融合蛋白存在的疏棉状嗜热丝孢菌脂肪酶的基本上整个连续氨基酸序列,所述融合蛋白具有连续氨基酸序列,所述连续氨基酸序列来自具有SEQ ID NO:2的氨基酸序列的尖孢镰孢菌(Fusarium oxysporum)脂肪酶,其中所述变体脂肪酶的C-末端具有衍生自尖孢镰孢菌脂肪酶的C-末端的至少12个但少于55个氨基酸残基,并且其中所述变体脂肪酶不具有SEQ ID NO:3或SEQ ID NO:5的氨基酸序列。
2.在一些实施例中,如段落1所述的变体脂肪酶的C-末端具有衍生自尖孢镰孢菌的C-末端的至少12个但少于15个氨基酸残基。
3.在一些实施例中,如段落1或2所述的变体脂肪酶的C-末端具有衍生自尖孢镰孢菌的C-末端的12个氨基酸残基。
4.在一些实施例中,如段落1-3中任一项所述的变体脂肪酶具有取代G91A、D96W和E99K。
5.在一些实施例中,如段落1-4中任一项所述的变体脂肪酶在疏棉状嗜热丝孢菌脂肪酶的连续氨基酸序列的C-末端具有少量较少的或额外的残基。
6.在一些实施例中,如段落1-4中任一项所述的变体脂肪酶在疏棉状嗜热丝孢菌脂肪酶的连续氨基酸序列的C-末端具有残基的截短。
7.在一些实施例中,如段落1-6中任一项所述的变体脂肪酶具有SEQ ID NO:4的氨基酸序列。
8.在如段落1-7中任一项所述的变体脂肪酶的一些实施例中,在所述发酵工艺中,所述变体脂肪酶在同时糖化和发酵中具有改进的消泡活性。
9.在另一方面,提供了一种使用碳水化合物底物作为原料在乙醇生产工艺中减少发泡的改进的方法,所述方法包括在发酵步骤前或在发酵步骤期间添加如段落1-7中任一项所述的变体脂肪酶,所述变体脂肪酶在发酵工艺中与具有SEQ ID NO:5的氨基酸序列的参照脂肪酶相比具有改进的消泡活性。
10.在如段落9所述的改进的方法的一些实施例中,所述发酵工艺是糖化和/或发酵。
11.在如段落9或10所述的改进的方法的一些实施例中,所述发酵工艺是同时糖化和发酵。
12.在另一方面,提供了一种变体疏棉状嗜热丝孢菌脂肪酶,所述脂肪酶与SEQ IDNO:4的氨基酸序列具有至少95%、任选地至少98%和任选地至少99%的氨基酸序列同一性,并且在木霉属(Trichoderma)宿主中与具有SEQ ID NO:5的氨基酸序列的参照脂肪酶相比具有改进的表达,其中所述变体脂肪酶包含:疏棉状嗜热丝孢菌脂肪酶的基本上整个连续氨基酸序列,所述氨基酸序列参考SEQ ID NO:4包含N-末端、具有选自由以下组成的组的一个或多个取代:G91A、D96W和E99K;作为融合蛋白存在的疏棉状嗜热丝孢菌脂肪酶的基本上整个连续氨基酸序列,所述融合蛋白具有连续氨基酸序列,所述连续氨基酸序列来自具有SEQ ID NO:2的氨基酸序列的尖孢镰孢菌脂肪酶,其中所述变体脂肪酶的C-末端具有衍生自尖孢镰孢菌脂肪酶的C-末端的至少12个但少于55个氨基酸残基,并且其中所述变体脂肪酶不具有SEQ ID NO:3或SEQ ID NO:5的氨基酸序列。
13.在一些实施例中,如段落12所述的变体脂肪酶的C-末端具有衍生自尖孢镰孢菌的C-末端的至少12个但少于15个氨基酸残基。
14.在一些实施例中,如段落12或13所述的变体脂肪酶的C-末端具有衍生自尖孢镰孢菌的C-末端的12个氨基酸残基。
15.在一些实施例中,如段落12-14中任一项所述的变体脂肪酶具有取代G91A、D96W和E99K。
16.在一些实施例中,如段落12-15中任一项所述的变体脂肪酶在疏棉状嗜热丝孢菌脂肪酶的连续氨基酸序列的C-末端具有少量较少的或额外的残基。
17.在一些实施例中,如段落12-16中任一项所述的变体脂肪酶在疏棉状嗜热丝孢菌脂肪酶的连续氨基酸序列的C-末端具有残基的截短。
18.在一些实施例中,如段落12-17中任一项所述的变体脂肪酶具有SEQ ID NO:4的氨基酸序列。
19.在如段落11-18中任一项所述的变体脂肪酶的一些实施例中,在所述发酵工艺中,所述变体脂肪酶在同时糖化和发酵中具有改进的消泡活性。
从说明书和附图中,所述组合物和方法的这些及其他方面和实施例将是清楚的。
附图说明
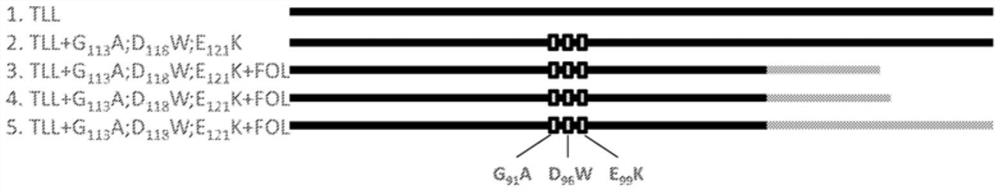
图1是描绘本文描述的脂肪酶分子的简化结构的图。黑色条带是衍生自疏棉状嗜热丝孢菌脂肪酶(TLL)的氨基酸序列。灰色条带是衍生自尖孢镰孢菌脂肪酶(FOX)的氨基酸序列。
图2是以本文描述的脂肪酶分子的样品上样的考马斯(Coomassie)染色的SDS-PAGE凝胶。
图3是显示来自表达LIP3(正方形)、LIP4(菱形)和LIP5(三角形)的细胞的培养液上清液中总蛋白浓度的图。
图4是显示LIP3(正方形)、LIP4(菱形)和LIP5(三角形)的培养液脂肪酶活性的图。
图5是显示LIP4(菱形)、LIP5(三角形)和无关的可商购脂肪酶及其截短变体(分别为形状1和形状2)的稳定性的图。pH值用+符号表示。
具体实施方式
在描述本发明的组合物和方法的各个方面和实施例之前,描述了以下定义和缩写。
1.定义和缩写
根据这一详细说明,以下缩写和定义适用。应当注意单数形式“一个/一种(a/an)”和“所述(the)”包括复数个指示物,除非上下文中另有清楚地指示。因此,例如提及“酶”包括多个此类酶,并且提及“剂量”包括提及一个或多个剂量以及本领域普通技术人员已知的其等同物,等等。
将本文件组织成若干部分以便于阅读;然而,读者将领会的是,在一个部分中进行的陈述可能适用于其他部分。以这种方式,用于本公开的不同部分的标题不应被解释为限制。
除非另有定义,否则本文使用的所有技术和科学术语具有与本领域普通技术人员通常所理解的相同的含义。下文提供了以下术语。
1.1.缩写和首字母缩略词
除非另外说明,以下缩写/首字母缩略词具有以下含义:
BSA 牛血清白蛋白
℃ 摄氏度
DCW 干细胞重量
DNA 脱氧核糖核酸
DS 溶解的固体
FFAeq 游离脂肪酸当量
g或gm 克
GA 葡糖淀粉酶
GAU/g ds 葡糖淀粉酶活性单位/克干固体
H
hr 小时
kDa 千道尔顿
kg 千克
M 摩尔
mg 毫克
min 分钟
mL和ml 毫升
mm 毫米
mM 毫摩尔
MW 分子量
ppm 百万分率,例如μg蛋白质/克干固体
REMI 限制性酶介导的整合
SDS-PAGE 十二烷基硫酸钠-聚丙烯酰胺凝胶电泳
sec 秒
sp. 物种
SSF 同时糖化和发酵
TP 总蛋白
Tris-HCl 三(羟甲基)氨基甲烷盐酸盐
U 单位
v/v 体积/体积
w/v 重量/体积
w/w 重量/重量
wt% 重量百分比
μg 微克
μL和μl 微升
μm 微米
μM 微摩尔
1.2.定义
术语“淀粉”是指由植物的复合多糖碳水化合物组成的任何材料,所述复合多糖碳水化合物由具有式(C
术语“脂肪酶”是指催化脂肪(即脂质)水解的酶。脂肪酶是酯酶的亚类。如本文使用的,术语脂肪酶旨在广泛地解释为涵盖分类为EC.3.1.1.X、尤其是EC.3.1.1.1和EC.3.1.1.2的酶。
术语“可滴定的磷脂酶单位(TIPU)”是指在30℃和pH 7.0每分钟释放1μmol游离脂肪酸当量(FFAeq)的酶的量。
术语“蛋白酶”(“protease”和“proteinase”)是指具有进行“蛋白水解”或“蛋白水解切割”的能力的酶蛋白,所述“蛋白水解”或“蛋白水解切割”是指水解将形成所述蛋白质的肽或多肽链中的氨基酸连接在一起的肽键。蛋白酶作为蛋白质消化酶的这种活性被称为“蛋白水解活性”。如本文使用的,术语脂肪酶旨在广泛地解释为涵盖分类为EC.3.4.X的酶。
术语“丝氨酸蛋白酶”是指切割蛋白质中的肽键的酶,其中酶丝氨酸在酶活性位点处充当亲核氨基酸。基于其结构将丝氨酸蛋白酶分为两大类:胰凝乳蛋白酶样(胰蛋白酶样)或枯草杆菌蛋白酶样。这些酶被分类为EC.3.4.16。
术语“葡糖淀粉酶”是指分类在EC.3.2.1.3(葡糖淀粉酶、α-1,4-D-葡聚糖葡糖水解酶)下的酶,所述酶从淀粉的非还原端除去连续的葡萄糖单元。这些酶也可以水解α-1,6和α-1,3键,但速率比水解α-1,4键慢得多。
术语“α-淀粉酶”是指分类在EC 3.2.1.1(α-D-(1→4)-葡聚糖葡聚糖水解酶)下的酶,所述酶切割淀粉中的α-D-(1→4)O-糖苷键。
关于酶的术语“热稳定的”和“热稳定性”是指酶在暴露于升高的温度后保持活性的能力。酶(例如淀粉酶)的热稳定性通过以分钟、小时或天给出的其半衰期(t1/2)来测量,在此期间酶活性的一半在限定条件下丧失。半衰期可以通过测量暴露于(即,受挑战于)升高的温度后的残余α-淀粉酶活性来计算。
关于多肽或多核苷酸的术语“野生型”、“亲本”或“参照”是指在一个或多个氨基酸或核苷酸位置处不包含人为取代、插入或缺失的天然存在的多肽。
对野生型多肽的提及应理解为包括多肽的成熟形式。“成熟”多肽或其变体是其中不存在信号序列的多肽或变体,例如,在多肽表达期间或之后从未成熟形式的多肽切割。
关于多肽的术语“变体”是指与指定的野生型、亲本或参照多肽不同的多肽,因为它包括一种或多种天然存在的或人为的氨基酸取代、插入或缺失。类似地,关于多核苷酸的术语“变体”是指在核苷酸序列中与指定的野生型、亲本或参照多核苷酸不同的多核苷酸。野生型、亲本或参照多肽或多核苷酸的特性将从上下文中显而易见。
术语“重组”当用于提及主题细胞、核酸、蛋白质或载体时,表明受试者已经从其天然状态被修饰。
术语“回收的”、“分离的”和“单独的”是指从如天然存在的与其天然相关的至少一种其他材料或组分中除去的化合物、蛋白质(多肽)、细胞、核酸、氨基酸、或者其他指定的材料或组分。
关于酶的“pH范围”是指在其下酶显示催化活性的pH值的范围。
关于酶的术语“pH稳定”和“pH稳定性”涉及在一个宽范围内的pH值下,酶保持预定时间段(例如,15min.、30min.、1小时)的活性的能力。
术语“氨基酸序列”与术语“多肽”、“蛋白质”和“肽”同义,并且可互换地使用。当此类氨基酸序列显示出活性时,它们可以被称为“酶”。使用针对氨基酸残基的常规单字母或三字母密码,采用标准氨基端-至-羧基端取向(即N→C)表示氨基酸序列。
术语“核酸”涵盖能够编码多肽的DNA、RNA、异源双链体、以及合成分子。核酸可以是单链的或双链的,并且可以含有化学修饰。术语“核酸”和“多核苷酸”可互换地使用。除非另有说明,否则核酸序列以5′-至-3′取向呈现。
关于细胞使用的术语“转化”、“稳定转化”和“转基因”意指细胞含有整合到其基因组中或作为通过多代维系的附加体的非天然(例如异源)核酸序列。
术语“发酵生物”是指适用于产生期望的发酵产物的任何生物,包括细菌和真菌生物(包括酵母和丝状真菌)。
“宿主菌株”或“宿主细胞”是已经引入了表达载体、噬菌体、病毒或其他DNA构建体,包括编码目的多肽(例如,淀粉酶)的多核苷酸的生物。术语“宿主细胞”包括从细胞产生的原生质体。
术语“丝状真菌”是指所有丝状形式的真菌亚门(Eumycotina),特别是子囊菌亚门(Pezizomycotina)物种。
关于多核苷酸或蛋白质的术语“异源”是指不是天然存在于宿主细胞中的多核苷酸或蛋白质。
关于多核苷酸或蛋白质的术语“内源”是指天然存在于宿主细胞中的多核苷酸或蛋白质。
术语“表达”是指基于核酸序列产生多肽的过程。所述过程包括转录和翻译两者。
“选择性标记”或“可选择标记”是指能够在宿主中被表达以促进选择携带所述基因的宿主细胞的基因。可选择标记的实例包括但不限于在宿主细胞上赋予代谢优势(如营养优势)的抗微生物剂(例如,潮霉素、博来霉素或氯霉素)和/或基因。
“载体”是指设计用于将核酸引入一种或多种细胞类型的多核苷酸序列。载体包括克隆载体、表达载体、穿梭载体、质粒、噬菌体颗粒、盒等。
“表达载体”是指包含编码目的多肽的DNA序列的DNA构建体,所述编码序列与能够在适合的宿主中影响DNA表达的适合控制序列有效地连接。
术语“有效地连接”意指:指定组分处于允许它们以预期方式起作用的关系(包括但不限于并列)。例如,调控序列与编码序列有效地连接,使得编码序列的表达受调控序列的控制。
“融合”多肽序列通过两个受试多肽序列之间的肽键连接,即有效地连接。
“信号序列”是与蛋白质的N-末端部分附接的氨基酸序列,所述氨基酸序列有利于蛋白质在细胞外的分泌。细胞外的蛋白质的成熟形式缺乏在分泌过程中被切除的信号序列。
术语“比活性”是指在特定条件下每单位时间通过酶或酶制剂可转化为产物的底物的摩尔数。比活性通常表示为单位(U)/mg蛋白质。
“序列同一性百分比”意指当使用具有默认参数的CLUSTAL W算法比对时,特定序列具有与指定参照序列中的氨基酸残基相同的至少一定百分比的氨基酸残基。参见Thompson等人,(1994)Nucleic Acids Res.[核酸研究]22:4673-4680。CLUSTAL W算法的默认参数是:
空位开放罚分: 10.0
空位延伸罚分: 0.05
蛋白质权重矩阵: BLOSUM系列
DNA权重矩阵: IUB
延迟发散序列%: 40
空位分隔距离: 8
DNA转换权重: 0.50
列表亲水残基: GPSNDQEKR
使用负性矩阵: 关
切换特殊残基罚分: 开
切换亲水罚分: 开
切换结束空位分隔罚分 关
短语“同时糖化和发酵(SSF)”是指生物化学品的生产工艺,其中在同一工艺步骤中存在微生物如产乙醇微生物和至少一种酶如淀粉酶。SSF包括在相同的反应容器中同时将淀粉底物(颗粒状、液化的或溶解的)水解为糖类(包括葡萄糖)和将糖类发酵为醇类或其他的生物化学品或生物材料。
术语“发酵饮料”是指通过包括发酵工艺(例如微生物发酵,如细菌和/或真菌发酵)的方法生产的任何饮料。“啤酒”是这种发酵饮料的一个实例,并且所述术语“啤酒”意指包括通过发酵/酿造含淀粉的植物材料生产的任何发酵的麦芽汁。
术语“麦芽”是指任何发芽的谷类谷粒,如发芽的大麦或小麦。
术语“麦芽汁”是指糖化醪制备期间,对谷粉进行提取后,未发酵的液体流出物(run-off)。
术语“约”是指参照值的±15%。
2.变体脂肪酶多肽
本发明的组合物和方法的一个方面是变体脂肪酶分子,包括改进其在发酵工艺中控制抑泡的性能的突变组合。
变体脂肪酶及其使用方法衍生自疏棉状嗜热丝孢菌脂肪酶(TLL;参见,例如NCBI登录号O59952.1、AOE45082.1、1DT3_A和1GT6_A),如下SEQ ID NO:1表示:
EVSQDLFNQFNLFAQYSAAAYCGKNNDAPAGTNITCTGNACPEVEKADATFLYSFEDSGVGDVTGFLALDNTNKLIVLSFRGSRSIENWIGNLNFDLKEINDICSGCRGHDGFTSSWRSVADTLRQKVEDAVREHPDYRVVFTGHSLGGALATVAGADLRGNGYDIDVFSYGAPRVGNRAFAEFLTVQTGGTLYRITHTNDIVPRLPPREFGYSHSSPEYWIKSGTLVPVTRNDIVKIEGIDATGGNNQPNIPDIPAHLWYFGLIGTCL
变体脂肪酶参考SEQ ID NO:1包含取代G91A、D96W和E99K中的一个或多个(参见,例如WO 2003/099016 A2中的SEQ ID NO:2)。在一些实施例中,变体脂肪酶包含所有三个取代G91A、D96W和E99K。
变体脂肪酶是融合蛋白并且还包含尖孢镰孢菌脂肪酶(FOX;NCBI登录号ABR12479.1)的C-末端的一部分,如下SEQ ID NO:6表示:
MLLLPLLSAITLAVASPVALDDYVNSLEERAVGVTTTDFGNFKFYIQHGAAAYCNSEAAAGSKITCSNNGCPTVQGNGATIVTSFGSKTGIGGYVATDSARKEIVVSFRGSINIRNWLTNLDFGQEDCSLVSGCGVHSGFQRAWNEISSQATAAVASARKANPSFKVISTGHSLGGAVAVLAAANLRVGGTPVDIYTYGSPRVGNVQLSAFVSNQAGGEYRVTHADDPVPRLPPLIFGYRHTTPEFWLSGGGGDTVDYTISDVKVCEGAANLGCNGGTLGLDIAAHLHYFQATDACNAGGFSWRRYRSAESVDKRATMTDAELEKKLNSYVQMDKEYVKNNQARS
在本发明的融合多肽中,基于SEQ ID NO:6的氨基酸序列,与脂肪酶的TLL部分融合的FOX的C-末端的部分不应超过FOX的最C-末端部分的50个连续氨基酸残基,且不应少于12个连续氨基酸残基。在一些实施例中,FOX的C-末端的部分不应超过FOX的最C-末端部分的15个连续氨基酸残基,且不应少于12个连续氨基酸残基。在一些实施例中,FOX的C-末端的部分是FOX的最C-末端部分的12个连续氨基酸残基。
在一些实施例中,变体脂肪酶的TLL部分的C-末端部分可能具有少量较少的残基或少量额外的残基,例如,由于为了克隆目的而使用方便的限制性位点。在一些实施例中,较少的或额外的残基的数量为10个或更少个、9个或更少个、8个或更少个、7个或更少个、6个或更少个、5个或更少个、4个或更少个、3个或更少个、2个或更少个、或者甚至1个或更少个。在特定的实施例中,较少的残基的数量是7±3个、7±2个、7±1个、或者恰好±7个。在一个特定的实施例中,较少的残基的数量是恰好-7个。
在实例中的表2中总结了多种脂肪酶分子的特征,并且在图1中提供了所述分子的图示。特定变体脂肪酶的氨基酸序列如下SEQ ID NO:4所示:
EVSQDLFNQFNLFAQYSAAAYCGKNNDAPAGTNITCTGNACPEVEKADATFLYSFEDSGVGDVTGFLALDNTNKLIVLSFRGSRSIENWIANLNFWLKKINDICSGCRGHDGFTSSWRSVADTLRQKVEDAVREHPDYRVVFTGHSLGGALATVAGADLRGNGYDIDVFSYGAPRVGNRAFAEFLTVQTGGTLYRITHTNDIVPRLPPREFGYSHSSPEYWIKSGTLVPVTRNDIVKIEGIDATGGNNQPNIPDIPAHLWYFQATDACNAGGFS
本文描述的LIP5与
在一些实施例中,本发明的脂肪酶变体具有指示的突变组合和与SEQ ID NO:4具有确定程度的氨基酸序列同源性/同一性,例如至少95%、至少96%、至少97%、至少98%、或甚至至少99%氨基酸序列同源性/同一性。优选地,变体脂肪酶不具有SEQ ID NO:3或SEQID NO:5的氨基酸序列。
本发明的脂肪酶可包括任何数量的保守氨基酸取代。示例性保守氨基酸取代列于表1中。
表1.保守氨基酸取代
读者将理解,一些前述保守突变可以通过遗传操作产生,而其他通过用遗传或其他方式将合成的氨基酸引入多肽中产生。
本发明的变体脂肪酶可以是“前体”、“未成熟”或“全长”的,在这种情况下,它们包含信号序列和/或前序列;或“成熟”的,在这种情况下,它们缺乏信号序列。成熟形式的多肽通常是最有用的。除非另有说明,否则本文使用的氨基酸残基编号是指相应变体脂肪酶多肽的成熟形式。只要所得多肽保留脂肪酶活性,本发明的脂肪酶变体多肽也可被截短以除去N-末端或C-末端。
3.金属盐
任何适合的金属盐可以与本发明的脂肪酶变体组合使用。优选的金属盐包括选自由钙、镁、钠和钾组成的组的金属盐。优选的金属盐包括二价离子,如CaCl
4.改进的变体脂肪酶的用途
本文描述的改进的抑泡脂肪酶优选地用于本领域熟知的发酵工艺中。发酵工艺通常包括包含淀粉(例如来自谷物)的原材料的液化和糖化。任何变化形式的液化或糖化都可以与本发明的发酵工艺组合使用。例如,液化和糖化可以同时或以重叠的方式进行。类似地,糖化和发酵可以单独或同时进行,如同时糖化和发酵(SSF)的情况一样。
用于发酵工艺的原材料可以从块茎、根、茎、穗轴、豆类、谷类或全谷物中获得。更具体地,可以从玉米、穗轴、小麦、大麦、黑麦、买罗高粱、西米、木薯、木薯淀粉、高粱、稻、豌豆、菜豆、香蕉、或马铃薯中获得颗粒状淀粉。
本文描述的改进的抑泡脂肪酶变体适合应用于包括研磨谷物的热糊化的发酵工艺(即“传统发酵”工艺)中,以及不包括这种热糊化的发酵工艺(即“生淀粉水解”或“冷蒸煮”工艺)中,其中在糊化温度或低于糊化温度时进行液化。可以应用本发明的抑泡系统的传统发酵工艺描述于例如WO 199628567和WO 200238787中。可以应用本发明的抑泡系统的冷蒸煮工艺描述于例如WO 2003/66816、WO 2003/66826和WO 2004/080923中。
优选地在发酵之前或发酵早期添加本发明的脂肪酶以及任选地其他酶和金属盐,其中发泡是最大的问题。通常,在糖化期间的某个时间进行添加。在SSF的情况下,通常在SSF早期进行添加。添加甚至可以在液化期间进行,只要变体脂肪酶不被热破坏。添加可以与酵母添加同时进行,并考虑与变体脂肪酶混合的酵母产品,或者甚至表达变体脂肪酶的酵母。
实例
实例1
脂肪酶表达载体的构建
构建一系列表达载体以在里氏木霉(Trichoderma reesei)中表达密码子优化的疏棉状嗜热丝孢菌脂肪酶(TLL;SEQ ID NO:1)及其变体。图1示出亲本分子和变体的特征,包括相对于亲本TLL的突变。为了编号和命名方便,LIP1为野生型TLL(即SEQ ID NO:1),并且LIP2-LIP5(SEQ ID NO:2-5)均为变体。所有四种变体都包括取代G91A、D96W和E99K(参见,例如WO 2003/099016 A2中的SEQ ID NO:2)。LIP3-LIP5还包括TLL的C-末端的小截断和与尖孢镰孢菌脂肪酶(FOX;SEQ ID NO:6)的不同长度C-末端的融合。
基于SEQ ID NO:7的密码子优化的序列,使用标准分子生物学技术制造编码变体的基因。所有基因均受天然里氏木霉cbh1启动子和终止子的转录控制(即与其有效地连接)。表达载体包括位于cbh1启动子上游的pyr2可选择标记(编码乳清酸磷酸核糖转移酶)和TLL基因。
在表2中总结了多种脂肪酶分子的特征,并且在图1中示出了所述分子的图示。应当注意,LIP5与
表2.TLL脂肪酶及其变体的特征
LIP1-LIP5的氨基酸序列和FOX的氨基酸序列以及编码TLL的密码子优化的基因的核苷酸序列如下所示。应当注意,SEQ ID NO是指成熟多肽序列(即没有信号序列),除非另外说明。
LIP1的成熟氨基酸序列如下SEQ ID NO:1所示:
EVSQDLFNQFNLFAQYSAAAYCGKNNDAPAGTNITCTGNACPEVEKADATFLYSFEDSGVGDVTGFLALDNTNKLIVLSFRGSRSIENWIGNLNFDLKEINDICSGCRGHDGFTSSWRSVADTLRQKVEDAVREHPDYRVVFTGHSLGGALATVAGADLRGNGYDIDVFSYGAPRVGNRAFAEFLTVQTGGTLYRITHTNDIVPRLPPREFGYSHSSPEYWIKSGTLVPVTRNDIVKIEGIDATGGNNQPNIPDIPAHLWYFGLIGTCL
LIP2的成熟氨基酸序列如下SEQ ID NO:2所示:
EVSQDLFNQFNLFAQYSAAAYCGKNNDAPAGTNITCTGNACPEVEKADATFLYSFEDSGVGDVTGFLALDNTNKLIVLSFRGSRSIENWIANLNFWLKKINDICSGCRGHDGFTSSWRSVADTLRQKVEDAVREHPDYRVVFTGHSLGGALATVAGADLRGNGYDIDVFSYGAPRVGNRAFAEFLTVQTGGTLYRITHTNDIVPRLPPREFGYSHSSPEYWIKSGTLVPVTRNDIVKIEGIDATGGNNQPNIPDIPAHLWYFGLIGTCL
LIP3的成熟氨基酸序列如下SEQ ID NO:3所示:
EVSQDLFNQFNLFAQYSAAAYCGKNNDAPAGTNITCTGNACPEVEKADATFLYSFEDSGVGDVTGFLALDNTNKLIVLSFRGSRSIENWIANLNFWLKKINDICSGCRGHDGFTSSWRSVADTLRQKVEDAVREHPDYRVVFTGHSLGGALATVAGADLRGNGYDIDVFSYGAPRVGNRAFAEFLTVQTGGTLYRITHTNDIVPRLPPREFGYSHSSPEYWIKSGTLVPVTRNDIVKIEGIDATGGNNQPNIPDIPAHLWYFQATDACNAGGF
LIP4的成熟氨基酸序列如下SEQ ID NO:4所示:
EVSQDLFNQFNLFAQYSAAAYCGKNNDAPAGTNITCTGNACPEVEKADATFLYSFEDSGVGDVTGFLALDNTNKLIVLSFRGSRSIENWIANLNFWLKKINDICSGCRGHDGFTSSWRSVADTLRQKVEDAVREHPDYRVVFTGHSLGGALATVAGADLRGNGYDIDVFSYGAPRVGNRAFAEFLTVQTGGTLYRITHTNDIVPRLPPREFGYSHSSPEYWIKSGTLVPVTRNDIVKIEGIDATGGNNQPNIPDIPAHLWYFQATDACNAGGFS
LIP5的成熟氨基酸序列如下SEQ ID NO:5所示:
EVSQDLFNQFNLFAQYSAAAYCGKNNDAPAGTNITCTGNACPEVEKADATFLYSFEDSGVGDVTGFLALDNTNKLIVLSFRGSRSIENWIANLNFWLKKINDICSGCRGHDGFTSSWRSVADTLRQKVEDAVREHPDYRVVFTGHSLGGALATVAGADLRGNGYDIDVFSYGAPRVGNRAFAEFLTVQTGGTLYRITHTNDIVPRLPPREFGYSHSSPEYWIKSGTLVPVTRNDIVKIEGIDATGGNNQPNIPDIPAHLWYFQATDACNAGGFSWRRYRSAESVDKRATMTDAELEKKLNSYVQMDKEYVKNNQARS
FOX脂肪酶(NCBI登录号ABR12479.1)的成熟氨基酸序列(SEQ ID NO:6):
MLLLPLLSAITLAVASPVALDDYVNSLEERAVGVTTTDFGNFKFYIQHGAAAYCNSEAAAGSKITCSNNGCPTVQGNGATIVTSFGSKTGIGGYVATDSARKEIVVSFRGSINIRNWLTNLDFGQEDCSLVSGCGVHSGFQRAWNEISSQATAAVASARKANPSFKVISTGHSLGGAVAVLAAANLRVGGTPVDIYTYGSPRVGNVQLSAFVSNQAGGEYRVTHADDPVPRLPPLIFGYRHTTPEFWLSGGGGDTVDYTISDVKVCEGAANLGCNGGTLGLDIAAHLHYFQATDACNAGGFSWRRYRSAESVDKRATMTDAELEKKLNSYVQMDKEYVKNNQARS
编码LIP1(即TLL)的密码子优化的基因的核苷酸序列如下SEQ ID NO:7所示(带下划线的是起始密码子):
CACAAGTTTGTACAAAAAAGCAGGCTCCGCGCCACC
实例2
原生质体制备和转化
将木霉属的孢子接种到50mL的YEG培养基(5g/L酵母提取物,20g/L葡萄糖)中,并且在振摇培养箱中,在28℃以180rpm在250mL摇瓶中生长过夜,移动距离(throw)为50mm。通过10-min离心(3,000g)收集发芽孢子,并用10mL的1.2MgSO
含有实例1中描述的基因的PCR产物用于转化原生质体。如果使用REMI,则与DNA一起添加5-20个单位的限制性内切核酸酶。将5-20μgDNA添加至200μL原生质体中并且在冰上孵育20min。之后,将转化混合物转移至室温,并添加2mL的25%PEG 6,000、CaCl
在补充有10mM NH
实例3
TLL分子的表达和表征
已经描述了悬浮的木霉属培养物中蛋白质的表达。将表达来自实例1的多种TLL分子的转化体接种于常规木霉属发酵培养基中,并进行标准发酵。
通过SDS-PAGE分析并使用脂肪酶活性测定来分析发酵样品的脂肪酶表达水平。考马斯染色的SDS-PAGE凝胶的图像示于图2中。LIP3-LIP5下的水平线表明两个转化体的生长需要两条凝胶泳道。LIP1、LIP3和LIP4的表达水平略高于LIP5。
在于28℃、pH 5.75-6.0以0.06g葡萄糖/g DCW/hr的糖补料速率生长的深层发酵培养物(submerged fermentation culture)中测量了总蛋白(TP)生产、磷脂酶活性和比活性。
使用将BSA作为标准的双缩脲法(Biuret method)测量了来自表达LIP3-LIP5的细胞的培养液上清液中的总蛋白浓度,并显示在图3的图中。使用Triton-X 100作为乳化剂,使用L-α-磷脂酰胆碱(Avanti 441601G,Avanti极性脂质有限公司(Avanti PolarLipids),美国)作为底物来测定磷脂酶活性,所述底物溶解在含有5mM CaCl
基于使用ImageJ软件中的凝胶分析模块分析的考马斯亮蓝染色的SDS-PAGE凝胶上条带的密度比,量化样品中脂肪酶的量作为TP的分数。计算相对于脂肪酶蛋白的比活性并总结在表3中。
表3.脂肪酶表达和比活性分析的实例
LIP4的表达比LIP3和LIP5好,其在培养液中的活性和比活性也是如此(参见,例如图4和表3)。
实例4
TLL变体的抑泡性能
使用蛋白酶处理的和未处理的液化物,在实验室规模的同时糖化和发酵(SSF)中测试脂肪酶分子LIP2-LIP5对泡沫形成和乙醇生产的影响。LIP1先前已被证明是一种较差的消泡酶(数据未显示),因此未包括在实验中。将代表商业产品的LIP5用作基准。
使用Retsch ZM200碾磨机研磨玉米仁(阿里勃洛克动物营养公司(Arie BlokAnimal Nutrition),NL-3440AA武尔登(Woerden),商品编号:377),并设置如下:3mm筛,1,0000rpm。通过向面粉中添加自来水,将所得玉米面粉用于产生34%干固体的2kg浆料批次。用H
用H
以0.5ug/g DS的剂量添加消泡剂脂肪酶至SSF。将SSF混合物分配到250mL聚丙烯分级的圆筒中。将带有泡沫阻塞的圆筒置于32℃的水浴中,并以350rpm磁力搅拌。
发酵几个小时后,泡沫开始在SSF混合物的顶部积聚,在圆筒壁上留下痕迹,痕迹即使在泡沫破裂后仍可见。孵育16h后记录SSF期间产生的泡沫水平,并以体积表示。重复样品的水平降低情况示于表3中。
表3. 16h后不同SSF混合物中的相对泡沫水平的汇总
结果表明,添加脂肪酶对控制发酵系统的泡沫水平具有积极影响,即使在使用增加的尿素和将酸性蛋白酶添加到SSF混合物中的情况下也是如此。在SSF期间,在存在和不存在热稳定的蛋白酶的情况下,LIP4均展现出最低水平的泡沫。
实例5
TLL变体的稳定性
在SSF条件下测定了LIP4、LIP5和无关的可商购脂肪酶及其截短变体的稳定性。简而言之,将50mL体积的SSF底物(表示如实例4中描述的在未调节的pH 5.5,从玉米面粉和自来水中获得的玉米液化物)与商业相关剂量的葡糖淀粉酶(
- 用于消泡的改进的脂肪酶
- 用于润滑油的消泡剂组合物及利用所述消泡剂组合物的消泡方法
