间充质干细胞疗法
文献发布时间:2023-06-19 18:35:48
优先权
本申请要求于2020年4月28日提交的美国临时申请号63/016,626的优先权,所述临时申请的内容以引用的方式整体并入本文。
技术领域
本发明部分涉及细胞,包括间充质干细胞(MSC)及其作为治疗剂的用途。
以电子方式提交的文本文件的描述
本申请含有序列表,所述序列表以ASCII格式通过EFS-Web提交并且由此以引用的方式整体并入。所述ASCII拷贝创建于2020年7月3日,名为“FAB-016PC_ST25.txt”,并且大小为18,145字节。
背景技术
间充质干细胞(MSC)有望用于各种适应症,例如,免疫相关疾病、再生医学。MSC有益地具有高可塑性、介导炎症和通过免疫调节和免疫抑制促进细胞生长、细胞分化和组织修复的能力。
天然存在的人类MSC是罕见的非造血干细胞亚群,其位于骨髓中的脉管系统和小梁周围。在过去的十年中,骨髓来源的间充质基质细胞已在各种临床环境中进行了治疗研究,所述临床环境包括移植物抗宿主病、缺血性/非缺血性心血管疾病和缺血性中风。骨髓来源的间充质基质细胞的局限性包括随着供体年龄的增加,细胞的数量和分化潜能下降,骨髓来源的间充质基质细胞产品的质量不一致,以及必要的骨髓穿刺程序的侵入性。
鉴于MSC的可能性,需要这种细胞治疗材料的改进的来源。
发明内容
因此,本发明部分涉及制备和使用来源于诱导多能干细胞(iPSC)的MSC的方法,例如通过基于mRNA的重编程。此类方法包括测定MSC的蛋白质表达和/或分泌特征的步骤,产生优异的细胞群和/或治疗效果。此外,此类方法产生了证明样品/批次之间的一致性的MSC,从而提供了治疗可靠性。
在一个方面,提供了制备包含治疗细胞的组合物的方法,所述方法包括:(a)将诱导多能干细胞(iPSC)重编程为间充质干细胞(MSC),所述重编程包括使所述iPSC与一种或多种编码重编程因子的合成RNA分子接触;(b)测定所述MSC的蛋白质分泌特征,所述蛋白质分泌特征包括一种或多种选自MIP-1α、SDF-1α、IL-27、LIF、IL-1β、IL-2、IL-5、IL-12p70、IL-13、IL-17A、IL-31、G-CSF/CSF-3、IFN-γ、TNF-α、HGF、MCP-1、IL-9、bNGF、MIP-3α、Gro-α/KC、IL-1α、IL-23、MMP-1、IL-18、M-CSF、IL-21、M-CSF、IL-21、CD40L、IL-22、VEGF-A、BLC、Tweak、ENA-78(LIX)、MCP-3、MIF和嗜酸性细胞活化趋化因子(Eotaxin)-3的蛋白质的分泌增加和/或一种或多种选自IL-6、IL-8和IL-4的蛋白质的分泌减少,其中所述分泌增加和/或减少的是相对于骨髓来源的MSC而言的;和(c)配制基本上具有用于疗法的蛋白质分泌特征的所述MSC。
在另一个方面,提供了通过本文所述的方法产生的细胞。
在另一个方面,提供了治疗炎性和/或免疫调节疾病或病症的方法,所述方法包括:(a)获得间充质干细胞(MSC),所述MSC获得自重编程诱导多能干细胞(iPSC),所述重编程包括使所述iPSC与一种或多种编码重编程因子的合成RNA分子接触,并且所述MSC具有蛋白质分泌特征,所述蛋白质分泌特征包括一种或多种选自MIP-1α、SDF-1α、IL-27、LIF、IL-1β、IL-2、IL-5、IL-12p70、IL-13、IL-17A、IL-31、G-CSF/CSF-3、IFN-γ、TNF-α、HGF、MCP-1、IL-9、bNGF、MIP-3α、Gro-α/KC、IL-1α、IL-23、MMP-1、IL-18、M-CSF、IL-21、M-CSF、IL-21、CD40L、IL-22、VEGF-A、BLC、Tweak、ENA-78(LIX)、MCP-3、MIF和嗜酸性细胞活化趋化因子-3的蛋白质的分泌增加和/或一种或多种选自IL-6、IL-8和IL-4的蛋白质的分泌减少,其中所述分泌增加和/或减少是相对于骨髓来源的MSC而言的;和(b)施用有效量基本上具有用于有需要的患者的疗法的蛋白质分泌特征的所述MSC。
在另一个方面,提供了治疗或减轻与感染相关的呼吸窘迫的方法,所述方法包括:(a)获得间充质干细胞(MSC),所述MSC获得自重编程诱导多能干细胞(iPSC),所述重编程包括使所述iPSC与一种或多种编码重编程因子的合成RNA分子接触,并且所述MSC具有蛋白质分泌特征,所述蛋白质分泌特征包括一种或多种选自MIP-1α、SDF-1α、IL-27、LIF、IL-1β、IL-2、IL-5、IL-12p70、IL-13、IL-17A、IL-31、G-CSF/CSF-3、IFN-γ、TNF-α、HGF、MCP-1、IL-9、bNGF、MIP-3α、Gro-α/KC、IL-1α、IL-23、MMP-1、IL-18、M-CSF、IL-21、M-CSF、IL-21、CD40L、IL-22、VEGF-A、BLC、Tweak、ENA-78(LIX)、MCP-3、MIF和嗜酸性细胞活化趋化因子-3的蛋白质的分泌增加和/或一种或多种选自IL-6、IL-8和IL-4的蛋白质的分泌减少,其中所述分泌增加和/或减少是相对于骨髓来源的MSC而言的;和(b)施用有效量基本上具有用于有需要的患者的疗法的蛋白质分泌特征的所述MSC。
在另一个方面,提供了治疗与SARS-CoV-2感染相关的急性呼吸窘迫综合征(ARDS)的方法,所述方法包括:(a)获得间充质干细胞(MSC),所述MSC获得自重编程诱导多能干细胞(iPSC),所述重编程包括使所述iPSC与一种或多种编码重编程因子的合成RNA分子接触,并且所述MSC具有蛋白质分泌特征,所述蛋白质分泌特征包括一种或多种选自MIP-1α、SDF-1α、IL-27、LIF、IL-1β、IL-2、IL-5、IL-12p70、IL-13、IL-17A、IL-31、G-CSF/CSF-3、IFN-γ、TNF-α、HGF、MCP-1、IL-9、bNGF、MIP-3α、Gro-α/KC、IL-1α、IL-23、MMP-1、IL-18、M-CSF、IL-21、M-CSF、IL-21、CD40L、IL-22、VEGF-A、BLC、Tweak、ENA-78(LIX)、MCP-3、MIF和嗜酸性细胞活化趋化因子-3的蛋白质的分泌增加和/或一种或多种选自IL-6、IL-8和IL-4的蛋白质的分泌减少,其中所述分泌增加和/或减少是相对于骨髓来源的MSC而言的;和(b)施用有效量基本上具有用于有需要的患者的疗法的蛋白质分泌特征的所述MSC。
在另一个方面,提供了治疗癌症的方法,所述方法包括:(a)获得间充质干细胞(MSC),所述MSC获得自重编程诱导多能干细胞(iPSC),所述重编程包括使所述iPSC与一种或多种编码重编程因子的合成RNA分子接触,并且所述MSC具有蛋白质分泌特征,所述蛋白质分泌特征包括一种或多种选自MIP-1α、SDF-1α、IL-27、LIF、IL-1β、IL-2、IL-5、IL-12p70、IL-13、IL-17A、IL-31、G-CSF/CSF-3、IFN-γ、TNF-α、HGF、MCP-1、IL-9、bNGF、MIP-3α、Gro-α/KC、IL-1α、IL-23、MMP-1、IL-18、M-CSF、IL-21、M-CSF、IL-21、CD40L、IL-22、VEGF-A、BLC、Tweak、ENA-78(LIX)、MCP-3、MIF和嗜酸性细胞活化趋化因子-3的蛋白质的分泌增加和/或一种或多种选自IL-6、IL-8和IL-4的蛋白质的分泌减少,其中所述分泌增加和/或减少是相对于骨髓来源的MSC而言的;和(b)施用有效量基本上具有用于有需要的患者的疗法的蛋白质分泌特征的所述MSC。
在实施方案中,iPSC来源于不打算接受疗法的人和/或受试者。在实施方案中,iPSC对于打算接受疗法的患者是同种异体的。
在实施方案中,MSC的特征在于炎症和/或免疫原性低或降低。在实施方案中,MSC是自我更新的、多能的、免疫抑制的,和/或适合于在免疫抑制特性显着丧失的情况下进行体外扩增。在实施方案中,MSC降低任选地选自T细胞和NK细胞的免疫细胞的增殖、数量和/或活性。在实施方案中,MSC基本上表达CD73、CD90和CD105中的一种或多种和/或基本上不表达CD14、CD34和CD45中的一种或多种。
在实施方案中,MSC已被改变以降低一种或多种MHC分子的表达和/或活性。在实施方案中,改变是通过基因编辑实现的。在实施方案中,MHC分子是MHC I类分子。在实施方案中,通过基因编辑人B2M基因(例如,NCBI参考序列:NG_012920)降低所述MHC I类分子的表达和/或活性。在实施方案中,改变是通过基因编辑实现的。在实施方案中,MHC分子是MHCII类分子。在实施方案中,通过基因编辑MHC II反式激活因子(CIITA)基因(例如,NCBI参考序列:NG_009628.1)降低所述MHC II类分子的表达和/或活性。在实施方案中,MSC已被改变以降低MHC I类和MHC II类分子的表达和/或活性。在实施方案中,通过基因编辑所述B2M基因降低所述MHC I类分子的表达和/或活性,并且通过基因编辑所述CIITA基因降低所述MHCII类分子的表达。
在实施方案中,合成RNA分子是mRNA,其中所述mRNA不包含或包含一种或多种非规范核苷酸。在实施方案中,合成RNA分子是体外转录的。
在实施方案中,重编程是非病毒的。在实施方案中,重编程因子是Oct4、Sox2、Klf4、c-Myc、l-Myc、Tert、Nanog和Lin28中的一种或多种。
在实施方案中,组合物适用于治疗各种疾病,包括感染性疾病,任选地选自病原体感染,所述病原体任选地选自细菌、病毒、真菌或寄生虫。在实施方案中,病原体是病毒。在实施方案中,病毒是流感病毒或冠状病毒科的成员。在实施方案中,病毒是SARS-CoV-2,其已引起或未引起COVID-19。在实施方案中,COVID-19的特征在于发热、咳嗽、气短、腹泻、上呼吸道症状、下呼吸道症状、肺炎和呼吸窘迫中的一种或多种。
在实施方案中,疗法在施用时预防或减轻患者急性呼吸窘迫综合征(ARDS)的发展。在实施方案中,疗法在施用时改善了患者的氧合。在实施方案中,疗法在施用时预防或减轻患者从呼吸窘迫到细胞因子失衡的转变。
在实施方案中,疗法在施用时逆转或预防可能在或可能不在患者的肺和/或全身的细胞因子风暴。在实施方案中,疗法在施用时逆转或预防患者体内一种或多种炎性细胞因子的过度产生。在实施方案中,炎性细胞因子是IL-6、IL-1、IL-1受体拮抗剂(IL-1ra)、IL-2ra、IL-10、IL-18、TNFα、干扰素-γ、CXCL10、和CCL7。在实施方案中,用选自脂多糖(LPS)、多聚(I:C)、TNF家族成员、TNF-α、干扰素和干扰素-γ的一种或多种分子启动所述细胞。在实施方案中,用一种或多种选自mRNA分子和siRNA分子的合成RNA分子启动所述细胞。在实施方案中,mRNA分子编码一种或多种免疫调节蛋白、归巢配体和归巢配体受体。在实施方案中,对所述细胞进行基因编辑以过表达一种或多种免疫调节蛋白、归巢配体和归巢配体受体。
在实施方案中,组合物被配制用于一种或多种施用途径,包括输注和注射。在实施方案中,输注是静脉输注。在实施方案中,注射是静脉注射。
在实施方案中,蛋白质分泌特征是(a)MIP-1α、SDF-1α、IL-27、LIF、IL-1β、IL-2、IL-5、IL-12p70、IL-13、IL-17A、IL-31、G-CSF/CSF-3、IFN-γ、TNF-α、HGF、MCP-1、IL-9、bNGF、MIP-3α、Gro-α/KC、IL-1α、IL-23、MMP-1、IL-18、M-CSF、IL-21、M-CSF、IL-21、CD40L、IL-22、VEGF-A、BLC、Tweak、ENA-78(LIX)、MCP-3、MIF和嗜酸性细胞活化趋化因子-3中的约5,或约10,或约15,或约20,或约25,或约30,或约35种或全部的分泌增加,和/或(b)IL-6、IL-8和/或IL-4的分泌减少。在实施方案中,蛋白质分泌特征是MIP-1α、G-CSF/CSF-3、M-CSF、BLC、Tweak、ENA-78(LIX)和MCP-3中的一种,或两种,或三种,或四种,或五种,或六种或全部的分泌。在实施方案中,蛋白质分泌特征是相对于骨髓来源的MSC的IL-6分泌而言,MIP-1α、IL-27、LIF、IL-1β、IL-2、IL-5、IL-12p70、IL-13、IL-17A、IL-31、G-CSF/CSF-3、IFN-γ、TNF-α、HGF、IL-9、bNGF、MIP-3α、Gro-α/KC、IL-1α、IL-23、IL-18、M-CSF、IL-21、M-CSF、IL-21、CD40L、IL-22、BLC、ENA-78(LIX)、MCP-3、MIF和嗜酸性细胞活化趋化因子-3中的约5,或约10,或约15,或约20,或约25,或约30种或全部的分泌减少。
附图说明
图1示出了生成本发明的MSC和骨髓来源的MSC的方法的对比。
图2示出了基于基因表达的细胞特征。
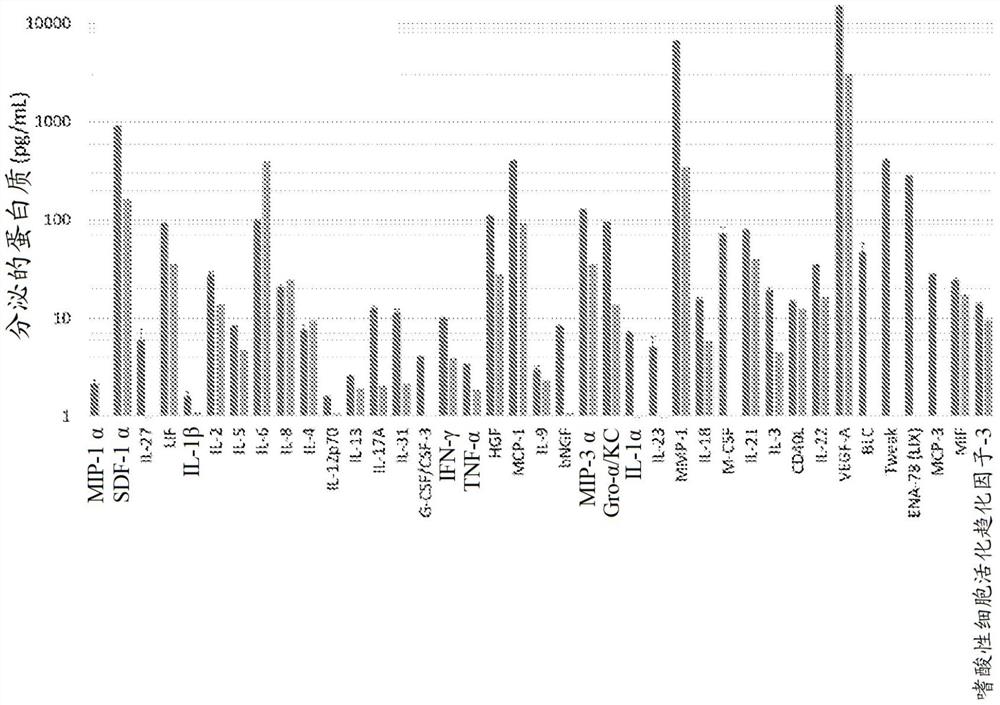
图3示出了基于蛋白质分泌的细胞特征。对于每种蛋白质(X轴),左边的条是本发明的MSC,右边的条是骨髓来源的MSC。
图4示出了接受本发明MSC(上方曲线)与对照(下方曲线)的ARDS模型绵羊的PaO
图5示出了接受本发明MSC(下方曲线)与对照(上方曲线)的ARDS模型绵羊对去甲肾上腺素的需求。
图6A至B示出了本发明MSC(下方曲线)与对照(上方曲线)ARDS模型绵羊中的肺血管损伤减少。
图7A-C示出了与ARDS模型绵羊中的对照相比的MSC治疗组中的组织细菌计数。在图7B和图7C中,左边的条是本发明MSC,并且右边的条是对照。
图8示出了mRNA电穿孔后间充质干细胞(MSC)中的细胞因子表达。在每组四个条中,从左到右的条件为TRAIL/TNFSF10、IL-7、IL-15和Flt-3配体/FLT3L。
图9示出了电穿孔和冷冻后MSC中的TRAIL表达。
图10示出了用RNA编码TRAIL对iPSC衍生的MSC进行电穿孔后的TRAIL分泌。
图11示出了用MSC上清液杀死癌细胞。
具体实施方式
本发明部分基于用于制备具有免疫抑制性并且可通过蛋白质分泌和/或基因表达特征表征的高质量MSC的方法的发现。因此,在一些方面,本发明提供获得和使用MSC的方法,所述MSC是一致产生的,具有所需特性,使得其治疗用途更可能成功。
在一个方面,提供了制备包含治疗细胞的组合物的方法,所述方法包括:(a)将诱导多能干细胞(iPSC)重编程为间充质干细胞(MSC),所述重编程包括使所述iPSC与一种或多种编码重编程因子的合成RNA分子接触;(b)测定所述MSC的蛋白质分泌特征,所述蛋白质分泌特征包括一种或多种选自MIP-1α、SDF-1α、IL-27、LIF、IL-1β、IL-2、IL-5、IL-12p70、IL-13、IL-17A、IL-31、G-CSF/CSF-3、IFN-γ、TNF-α、HGF、MCP-1、IL-9、bNGF、MIP-3α、Gro-α/KC、IL-1α、IL-23、MMP-1、IL-18、M-CSF、IL-21、M-CSF、IL-21、CD40L、IL-22、VEGF-A、BLC、Tweak、ENA-78(LIX)、MCP-3、MIF和嗜酸性细胞活化趋化因子-3的蛋白质的分泌增加和/或一种或多种选自IL-6、IL-8和IL-4的蛋白质的分泌减少,其中所述分泌增加和/或减少的是相对于骨髓来源的MSC而言的;和(c)配制基本上具有用于疗法的蛋白质分泌特征的所述MSC。
在另一个方面,提供了通过本文所述的方法产生的细胞。
在另一个方面,提供了治疗炎性和/或免疫调节疾病或病症的方法,所述方法包括:(a)获得间充质干细胞(MSC),所述MSC获得自重编程诱导多能干细胞(iPSC),所述重编程包括使所述iPSC与一种或多种编码重编程因子的合成RNA分子接触,并且所述MSC具有蛋白质分泌特征,所述蛋白质分泌特征包括一种或多种选自MIP-1α、SDF-1α、IL-27、LIF、IL-1β、IL-2、IL-5、IL-12p70、IL-13、IL-17A、IL-31、G-CSF/CSF-3、IFN-γ、TNF-α、HGF、MCP-1、IL-9、bNGF、MIP-3α、Gro-α/KC、IL-1α、IL-23、MMP-1、IL-18、M-CSF、IL-21、M-CSF、IL-21、CD40L、IL-22、VEGF-A、BLC、Tweak、ENA-78(LIX)、MCP-3、MIF和嗜酸性细胞活化趋化因子-3的蛋白质的分泌增加和/或一种或多种选自IL-6、IL-8和IL-4的蛋白质的分泌减少,其中所述分泌增加和/或减少是相对于骨髓来源的MSC而言的;和(b)施用有效量基本上具有用于有需要的患者的疗法的蛋白质分泌特征的所述MSC。
在另一个方面,提供了治疗或减轻与感染相关的呼吸窘迫的方法,所述方法包括:(a)获得间充质干细胞(MSC),所述MSC获得自重编程诱导多能干细胞(iPSC),所述重编程包括使所述iPSC与一种或多种编码重编程因子的合成RNA分子接触,并且所述MSC具有蛋白质分泌特征,所述蛋白质分泌特征包括一种或多种选自MIP-1α、SDF-1α、IL-27、LIF、IL-1β、IL-2、IL-5、IL-12p70、IL-13、IL-17A、IL-31、G-CSF/CSF-3、IFN-γ、TNF-α、HGF、MCP-1、IL-9、bNGF、MIP-3α、Gro-α/KC、IL-1α、IL-23、MMP-1、IL-18、M-CSF、IL-21、M-CSF、IL-21、CD40L、IL-22、VEGF-A、BLC、Tweak、ENA-78(LIX)、MCP-3、MIF和嗜酸性细胞活化趋化因子-3的蛋白质的分泌增加和/或一种或多种选自IL-6、IL-8和IL-4的蛋白质的分泌减少,其中所述分泌增加和/或减少是相对于骨髓来源的MSC而言的;和(b)施用有效量基本上具有用于有需要的患者的疗法的蛋白质分泌特征的所述MSC。
在另一个方面,提供了治疗急性呼吸窘迫综合征(ARDS)的方法,所述方法包括:(a)获得间充质干细胞(MSC),所述MSC获得自重编程诱导多能干细胞(iPSC),所述重编程包括使所述iPSC与一种或多种编码重编程因子的合成RNA分子接触,并且所述MSC具有蛋白质分泌特征,所述蛋白质分泌特征包括一种或多种选自MIP-1α、SDF-1α、IL-27、LIF、IL-1β、IL-2、IL-5、IL-12p70、IL-13、IL-17A、IL-31、G-CSF/CSF-3、IFN-γ、TNF-α、HGF、MCP-1、IL-9、bNGF、MIP-3α、Gro-α/KC、IL-1α、IL-23、MMP-1、IL-18、M-CSF、IL-21、M-CSF、IL-21、CD40L、IL-22、VEGF-A、BLC、Tweak、ENA-78(LIX)、MCP-3、MIF和嗜酸性细胞活化趋化因子-3的蛋白质的分泌增加和/或一种或多种选自IL-6、IL-8和IL-4的蛋白质的分泌减少,其中所述分泌增加和/或减少是相对于骨髓来源的MSC而言的;和(b)施用有效量基本上具有用于有需要的患者的疗法的蛋白质分泌特征的所述MSC。在一个实施方案中,ARDS与SARS-CoV-2感染相关。
在一些方面,提供了制备包含治疗细胞的组合物的方法,所述方法包括配制基本上具有用于疗法的所需蛋白质分泌特征的MSC,所述蛋白质分泌特征包括一种或多种选自MIP-1α、SDF-1α、IL-27、LIF、IL-1β、IL-2、IL-5、IL-12p70、IL-13、IL-17A、IL-31、G-CSF/CSF-3、IFN-γ、TNF-α、HGF、MCP-1、IL-9、bNGF、MIP-3α、Gro-α/KC、IL-1α、IL-23、MMP-1、IL-18、M-CSF、IL-21、M-CSF、IL-21、CD40L、IL-22、VEGF-A、BLC、Tweak、ENA-78(LIX)、MCP-3、MIF和嗜酸性细胞活化趋化因子-3的蛋白质的分泌增加和/或一种或多种选自IL-6、IL-8和IL-4的蛋白质的分泌减少,其中所述分泌增加和/或减少是相对于骨髓来源的MSC而言的,和/或所述MSC经过重编程来源于诱导多能干细胞(iPSC),所述重编程包括使iPSC与具有一种或多种编码重编程因子的合成RNA分子接触。
成熟的分化细胞可以被重编程和去分化成胚胎样细胞,具有胚胎干细胞样特性。成纤维细胞可以通过例如某些转录因子的逆转录病毒转导转变为多能性,从而产生iPSC。在一些实施方案中,iPSC由各种组织生成,包括成纤维细胞、角质形成细胞、黑素细胞血细胞、骨髓细胞、脂肪细胞和组织驻留祖细胞。在一些实施方案中,iPSC通过Oct3/4、Sox2和Klf4的转导生成。
iPSC的生成依赖于通过载体将特定转录因子转导到体细胞基因组中进行重编程。
在一些实施方案中,在iPSC生成后,通过多能性测定评估细胞,所述测定包括形态学和组织学分析,以及某些基因表达谱,证明细胞分化成来源于三个胚层和畸胎瘤形成的组织的能力。在一些实施方案中,畸胎瘤测定涉及将iPSC注射到免疫功能低下的实验动物中,并随后进行组织分析以评估畸胎瘤的形成。
在实施方案中,iPSC来源于人。在实施方案中,iPSC来源于不打算接受疗法的受试者。在实施方案中,iPSC对于打算接受疗法的患者是同种异体的。在实施方案中,iPSC来自主细胞库。
干细胞具有自我更新和分化成多种细胞类型的能力,因此在再生医学中具有应用。MSC是多能成体干细胞,能够自我更新和分化为中胚层谱系细胞,诸如骨细胞、脂肪细胞和软骨细胞。在一些实施方案中,MSC分泌促血管生成、抗细胞凋亡和/或抑制炎症、促进重塑和/或释放含有可影响疾病相关过程的微小RNA的外泌体的因子。
MSC是细胞治疗中最常用的,因为它们相对容易从一系列组织中获得,并且在离体扩增过程中很少发生自发分化。在一些实施方案中,MSC具有抗炎特性和对受损部位的归巢能力。人MSC可以从多种来源获得,包括骨髓和全身血管化组织,包括脂肪组织、胎盘、羊水、牙髓、滑膜、外周血牙周膜、子宫内膜和脐带血。然而,MSC的均匀性、有效性和分化潜力可能根据MSC的来源而异。
在治疗应用中使用自体MSC是安全的,因为这些细胞不会引发免疫反应。然而,可能难以从受试者获得大量骨髓或脂肪组织。自体MSC也可能具有降低的治疗效果,从而导致不良临床结果。此外,如果迫切需要MSC,可能没有时间从受试者身上提取和扩增自体MSC。
因此,使用同种异体MSC是有吸引力的替代方案,因为可以预先筛选供体以得到具有高治疗潜力的细胞。同种异体MSC可以在临床规模上制备,在生产后测定治疗潜力,并以可用于紧急治疗应用的可用临床剂量储存。同种异体MSC固有地具有低免疫原性,因为它们缺乏或减少了MHC II类抗原的表达。在一些实施方案中,本发明的MSC是同种异体的。
因此,通过重编程iPSC(可通过重编程人体细胞获得)获得MSC是一种有吸引力的替代方案。在一些实施方案中,获得iPSC并通过用非免疫原性信使RNA(mRNA)在确定的、无动物成分的过程中编码一种或多种重编程因子的细胞重编程生成MSC。
在一些实施方案中,使用细菌和真菌测试、支原体测试、外来病毒剂测试和致瘤性测定(核型分析、畸胎瘤形成测定、软琼脂测定、比较基因组杂交(CGH)、荧光原位杂交(FISH)和聚合酶链反应(PCR))中的一种或多种检查MSC的安全性。在一些实施方案中,通过测试MSC分化成成骨细胞、软骨细胞和/或脂肪细胞的能力来测定MSC的多向分化能力。
在实施方案中,MSC的特征在于炎症低或降低。在实施方案中,MSC的特征在于免疫原性低或降低。在实施方案中,MSC适合体外扩增而不会显著丧失免疫抑制特性。在实施方案中,MSC是自我更新的。在实施方案中,MSC是多能的。在实施方案中,MSC是免疫抑制的。
在实施方案中,MSC已被改变以减少MHC分子的表达。在实施方案中,改变是通过基因编辑实现的。在实施方案中,MHC分子是MHC I类分子。在实施方案中,通过基因编辑B2M基因来减少MHC I类分子的表达。在实施方案中,改变是通过基因编辑实现的。在实施方案中,MHC分子是MHC II类分子。在实施方案中,通过基因编辑CIITA基因来减少MHC II分子的表达。在实施方案中,MSC已被改变以减少MHC I类和MHC II类分子的表达。在实施方案中,通过基因编辑B2M基因减少MHC I类分子的表达,并且通过基因编辑CIITA基因减少MHC II类分子的表达。
在实施方案中,MSC降低任选地选自T细胞和NK细胞的免疫细胞的增殖、数量和/或活性。
在实施方案中,MSC基本上表达CD73、CD90和CD105中的一种或多种。在实施方案中,MSC基本上不表达CD14、CD34和CD45中的一种或多种。
在一些实施方案中,MSC分化为脂肪细胞、成骨细胞和软骨细胞。
每种类型的细胞,包括MSC,在细胞内、细胞表面表达特定的蛋白质组,并分泌到细胞外空间。每种细胞表达的特定蛋白质组取决于细胞的一般和即时功能。蛋白质表达与mRNA水平相关,因此可以通过分析细胞内特定mRNA的分布、数量和特征的方法进行测定。有几种定量测量mRNA的方法,包括Northern印迹法和逆转录定量PCR(RT-qPCR)。杂交微阵列还可用于生成细胞内一系列基因的表达谱或高通量分析。此外,“基于标签”的技术,诸如基因表达系列分析(SAGE)和RNA-Seq,可用于确定不同mRNA的细胞浓度的相对测量值。
在一些实施方案中,MSC的蛋白质表达通过通过northern印迹、RT-qPCR、杂交微阵列和基于标签的技术(诸如AGE和RNA-Seq)中的一种或多种确定不同mRNA的浓度来确定。
通常有两种策略用于检测细胞外环境中的蛋白质:直接方法和间接方法。直接方法包括一步染色,并且可能涉及标记的抗体(例如,FITC缀合抗血清),其直接与细胞外环境中的蛋白质反应。间接方法包括与细胞外环境中的蛋白质反应的未标记一抗和与一抗反应的标记的二抗。标记可包括放射性标记、荧光标记、半抗原标记(诸如生物素)或酶(诸如辣根过氧化物酶或碱性磷酸酶)。进行这些测定的方法是本领域所熟知的。参见例如,Harlow等人(Antibodies,Cold Spring Harbor Laboratory,NY,1988)、Harlow等人(UsingAntibodies,A Laboratory Manual,Cold Spring Harbor Laboratory,NY,1999)、Virella(Medical Immunology,第6版,Informa HealthCare,New York,2007),以及Diamandis等人(Immunoassays,Academic Press,Inc.,New York,1996)。用于进行这些测定的试剂盒可从例如Clontech Laboratories,LLC(Mountain View,CA)商购获得。在一些实施方案中,使用包括一种或多种抗体的检测方法在MSC的细胞外环境中检测蛋白质。在一些实施方案中,检测方法还包括标记,所述标记包括放射性标记、荧光标记、半抗原标记(诸如生物素),或酶(诸如辣根过氧化物酶或碱性磷酸酶)。
在一些实施方案中,流式细胞术用于确定MSC是否表达在表面上或分泌的某些蛋白质组。在一些实施方案中,对特定蛋白质具有特异性的抗体与蛋白质组学方法结合使用以确定例如MSC的蛋白质分泌特征。在一些实施方案中,使用Western印迹测定纯化的MSC组的上清液以确定可利用抗体的分泌蛋白阵列的浓度。在一些实施方案中,确定并比较来源于不同来源(诸如iPSC或骨髓)的MSC的蛋白质分泌特征。
在一些实施方案中,来源于骨髓的MSC(BM-MSC)和来源于iPSCs的MSC(iPSC-MSC)被分别纯化并以相同的细胞浓度悬浮在无血清培养基中,随后一半的BM-MSC和一半的iPSC-MSC进行选择的蛋白质表达测定以确定特定分泌蛋白质组的mRNA水平,而另一半BM-MSC和另一半iPSC-MSC使用针对特定分泌蛋白质组的抗体进行Western印迹分析,其中所述蛋白质印迹分析能够确定每个BM-MSC群体和iPSC-MSC群体关于特定分泌蛋白质组的蛋白质分泌特征。在一些实施方案中,来自蛋白质表达测定的结果用于确定MSC的mRNA水平和蛋白质分泌水平的相关性。在一些实施方案中,对照测试利用(a)在单独的场合来源于两个不同批次的骨髓并相互比较的BM-MSC,和/或(b)在单独的场合来源于两个不同批次的iPSC并相互比较的iPSC-MSC的比较分析。
在实施方案中,蛋白质分泌特征是MIP-1α、SDF-1α、IL-27、LIF、IL-1β、IL-2、IL-5、IL-12p70、IL-13、IL-17A、IL-31、G-CSF/CSF-3、IFN-γ、TNF-α、HGF、MCP-1、IL-9、bNGF、MIP-3α、Gro-α/KC、IL-1α、IL-23、MMP-1、IL-18、M-CSF、IL-21、M-CSF、IL-21、CD40L、IL-22、VEGF-A、BLC、Tweak、ENA-78(LIX)、MCP-3、MIF和嗜酸性细胞活化趋化因子-3中的约5,或约10,或约15,或约20,或约25,或约30,或约35种或全部的分泌增加。
在实施方案中,蛋白质分泌特征是IL-6、IL-8和/或IL-4的分泌减少。
在实施方案中,蛋白质分泌特征是(a)MIP-1α、SDF-1α、IL-27、LIF、IL-1β、IL-2、IL-5、IL-12p70、IL-13、IL-17A、IL-31、G-CSF/CSF-3、IFN-γ、TNF-α、HGF、MCP-1、IL-9、bNGF、MIP-3α、Gro-α/KC、IL-1α、IL-23、MMP-1、IL-18、M-CSF、IL-21、M-CSF、IL-21、CD40L、IL-22、VEGF-A、BLC、Tweak、ENA-78(LIX)、MCP-3、MIF和嗜酸性细胞活化趋化因子-3中的约5,或约10,或约15,或约20,或约25,或约30,或约35种或全部的分泌增加,和(b)IL-6、IL-8和/或IL-4的分泌减少。
在实施方案中,蛋白质分泌特征是MIP-1α、G-CSF/CSF-3、M-CSF、BLC、Tweak、ENA-78(LIX)和MCP-3中的一种,或两种,或三种,或四种,或五种,或六种或全部的分泌。
在实施方案中,蛋白质分泌特征是相对于骨髓来源的MSC的IL-6分泌而言,MIP-1α、IL-27、LIF、IL-1β、IL-2、IL-5、IL-12p70、IL-13、IL-17A、IL-31、G-CSF/CSF-3、IFN-γ、TNF-α、HGF、IL-9、bNGF、MIP-3α、Gro-α/KC、IL-1α、IL-23、IL-18、M-CSF、IL-21、M-CSF、IL-21、CD40L、IL-22、BLC、ENA-78(LIX)、MCP-3、MIF和嗜酸性细胞活化趋化因子-3中的约5,或约10,或约15,或约20,或约25,或约30种或全部的分泌减少。
在实施方案中,蛋白质分泌特征是以下约5,或约10,或约15,或约20,或约25,或约30,或约35种,或全部的分泌增加:
1.MIP-1α:
2.SDF-1α,其分泌任选地是骨髓来源MSC的SDF-1α分泌的约3倍,或约4倍,或约5倍,或约6倍,或约7倍;
3.IL-27,其分泌任选地是骨髓来源MSC的IL-27分泌的约8倍,或约9倍,或约10倍,或约11倍,或约12倍;
4.LIF,其分泌任选地是骨髓来源MSC的LIF分泌的约1.5倍,或约2倍,或约2.5倍,或约3倍,或约3.5倍;
5.IL-1β,其分泌任选地是骨髓来源MSC的IL-1β分泌的约1.1倍,或约1.3倍,或约1.5倍,或约1.7倍,或约1.9倍;
6.IL-2,其分泌任选地是骨髓来源MSC的IL-2分泌的约1.2倍,或约1.6倍,或约2倍,或约2.4倍,或约2.8倍;
7.IL-5,其分泌任选地是骨髓来源MSC的IL-5分泌的约1.2倍,或约1.5倍,或约1.8倍,或约2.1倍,或约2.4倍;
8.IL-12p70,其分泌任选地是骨髓来源MSC的IL-12p70分泌的约1.1倍,或约1.3倍,或约1.5倍,或约1.7倍,或约1.9倍;
9.IL-13,其分泌任选地是骨髓来源MSC的IL-13分泌的约1.2倍,或约1.3倍,或约1.4倍,或约1.5倍,或约1.6倍;
10.IL-17A,其分泌任选地是骨髓来源MSC的IL-17A分泌的约4倍,或约5倍,或约6倍,或约7倍,或约8倍;
11.IL-31,其分泌任选地是骨髓来源MSC的IL-31分泌的约4倍,或约5倍,或约6倍,或约7倍,或约8倍;
12.G-CSF/CSF-3;
13.IFN-γ,其分泌任选地是骨髓来源MSC的IFN-γ分泌的约1.5倍,或约2倍,或约2.5倍,或约3倍,或约3.5倍;
14.TNF-α,其分泌任选地是骨髓来源MSC的TNF-α分泌的约1.2倍,或约1.6倍,或约2倍,或约2.4倍,或约2.8倍;
15.HGF,其分泌任选地是骨髓来源MSC的HGF分泌的约2倍,或约3倍,或约4倍,或约5倍,或约6倍;
16.MCP-1,其分泌任选地是骨髓来源MSC的MCP-1分泌的约2倍,或约3倍,或约4倍,或约5倍,或约6倍;
17.IL-9,其分泌任选地是骨髓来源MSC的IL-9分泌的约1.1倍,或约1.2倍,或约1.3倍,或约1.4倍,或约1.5倍;
18.bNGF,其分泌任选地是骨髓来源MSC的bNGF分泌的约6倍,或约7倍,或约8倍,或约9倍,或约10倍;
19.MIP-3α,其分泌任选地是骨髓来源MSC的MIP-3α分泌的约2倍,或约3倍,或约4倍,或约5倍,或约6倍;
20.Gro-α/KC,其分泌任选地是骨髓来源MSC的Gro-α/KC分泌的约5倍,或约6倍,或约7倍,或约8倍,或约9倍;
21.IL-1α,其分泌任选地是骨髓来源MSC的IL-1α分泌的约11倍,或约12倍,或约13倍,或约14倍,或约15倍;
22.IL-23,其分泌任选地是骨髓来源MSC的IL-23分泌的约5倍,或约6倍,或约7倍,或约8倍,或约9倍;
23.MMP-1,其分泌任选地是骨髓来源MSC的MMP-1分泌的约14倍,或约16倍,或约18倍,或约20倍,或约22倍;
24.IL-18,其分泌任选地是骨髓来源MSC的IL-18分泌的约1.5倍,或约2倍,或约2.5倍,或约3倍,或约3.5倍;
25.M-CSF;
26.IL-21,其分泌任选地是骨髓来源MSC的IL-21分泌的约1.2倍,或约1.6倍,或约2倍,或约2.4倍,或约2.8倍;
27.IL-3,其分泌任选地是骨髓来源MSC的IL-3分泌的约2倍,或约3倍,或约4倍,或约5倍,或约6倍;
28.CD40L,其分泌任选地是骨髓来源MSC的CD40L分泌的约1.1倍,或约1.15倍,或约1.2倍,或约1.25倍,或约1.3倍;
29.IL-22,其分泌任选地是骨髓来源MSC的IL-22分泌的约1.2倍,或约1.6倍,或约2倍,或约2.4倍,或约2.8倍;
30.VEGF-A,其分泌任选地是骨髓来源MSC的VEGF-A分泌的约3倍,或约4倍,或约5倍,或约6倍,或约7倍;
31.BLC;
32.Tweak;
33.ENA-78(LIX);
34.MCP-3;
35.MIF,其分泌任选地是骨髓来源MSC的MIF分泌的约1.2倍,或约1.3倍,或约1.4倍,或约1.5倍,或约1.6倍;以及
36.嗜酸性细胞活化趋化因子-3,其分泌任选地是骨髓来源MSC的嗜酸性细胞活化趋化因子-3分泌的约1.3倍,或约1.4倍,或约1.5倍,或约1.6倍,或约1.7倍。
在实施方案中,蛋白质分泌特征是相对于骨髓来源MSC的IL-6分泌而言,约5,或约10,或约15,或约20,或约25,或约30种,或所有以下的分泌减少。在实施方案中,蛋白质分泌特征是以下约5,或约10,或约15,或约20,或约25,或约30种,或全部的分泌减少:
1.MIP-1α,任选地是骨髓来源MSC的IL-6分泌的约1/160,或约1/170,或约1/180,或约1/190,或约1/200;
2.IL-27,任选地是骨髓来源MSC的IL-6分泌的约1/55,或约1/60,或约1/65,或约1/70,或约1/75;
3.LIF,任选地是骨髓来源MSC的IL-6分泌的约1/2,或约1/3,或约1/4,或约1/5,或约1/6;
4.IL-1β,任选地是骨髓来源MSC的IL-6分泌的约1/210,或约1/230,或约1/250,或约1/270,或约1/290;
5.IL-2,任选地是骨髓来源MSC的IL-6分泌的约1/11,或约1/13,或约1/15,或约1/17,或约1/19;
6.IL-5,任选地是骨髓来源MSC的IL-6分泌的约1/35,或约1/40,或约1/45,或约1/50,或约1/55;
7.IL-6,任选地是骨髓来源MSC的IL-6分泌的约1/2,或约1/3,或约1/4,或约1/5,或约1/6;
8.IL-8,任选地是骨髓来源MSC的IL-6分泌的约1/14,或约1/16,或约1/18,或约1/20,或约1/22;
9.IL-4,任选地是骨髓来源MSC的IL-6分泌的约1/40,或约1/45,或约1/50,或约1/55,或约1/60;
10.IL-12p70,任选地是骨髓来源MSC的IL-6分泌的约1/210,或约1/230,或约1/250,或约1/270,或约1/290;
11.IL-13,任选地是骨髓来源MSC的IL-6分泌的约1/130,或约1/140,或约1/150,或约1/160,或约1/170;
12.IL-17A,任选地是骨髓来源MSC的IL-6分泌的约1/20,或约1/25,或约1/30,或约1/35,或约1/40;
13.IL-31,任选地是骨髓来源MSC中的IL-6分泌的约1/25,或约1/30,或约1/35,或约1/40,或约1/45;
14.G-CSF/CSF-3,任选地是骨髓来源MSC的IL-6分泌的约1/80,或约1/90,或约1/100,或约1/110,或约1/120;
15.IFN-γ,任选地是骨髓来源MSC中的IL-6分泌的约1/30,或约1/35,或约1/40,或约1/45,或约1/50;
16.TNF-α,任选地是骨髓来源MSC的IL-6分泌的约1/100,或约1/110,或约1/120,或约1/130,或约1/140;
17.HGF,任选地是骨髓来源MSC的IL-6分泌的约1/2.5,或约1/3,或约1/3.5,或约1/4,或约1/4.5;
18.IL-9,任选地是骨髓来源MSC的IL-6分泌的约1/110,或约1/120,或约1/130,或约1/140,或约1/150;
19.bNGF,任选地是骨髓来源MSC的IL-6分泌的约1/40,或约1/45,或约1/50,或约1/55,或约1/60;
20.MIP-3α,任选地是骨髓来源MSC的IL-6分泌的约1/2,或约1/2.5,或约1/3,或约1/3.5,或约1/4;
21.Gro-α/KC,任选地是骨髓来源MSC的IL-6分泌的约1/3,或约1/3.5,或约1/4,或约1/4.5,或约1/5;
22.IL-1α,任选地是骨髓来源MSC的IL-6分泌的约1/45,或约1/50,或约1/55,或约1/60,或约1/65;
23.IL-23,任选地是骨髓来源MSC的IL-6分泌的约1/65,或约1/70,或约1/75,或约1/80,或约1/85;
24.IL-18,任选地是骨髓来源MSC的IL-6分泌的约1/20,或约1/22.5,或约1/25,或约1/27.5,或约1/30;
25.M-CSF,任选地是骨髓来源MSC的IL-6分泌的约1/4.5,或约1/5,或约1/5.5,或约1/6,或约1/6.5;
26.IL-21,任选地是骨髓来源MSC的IL-6分泌的约1/4,或约1/4.5,或约1/5,或约1/5.5,或约1/6;
27.IL-3,任选地是骨髓来源MSC的IL-6分泌的约1/15,或约1/17.5,或约1/20,或约1/22.5,或约1/25;
28.CD40L,任选地是骨髓来源MSC的IL-6分泌的约1/20,或约1/22.5,或约1/25,或约1/27.5,或约1/30;
29.IL-22,任选地是骨髓来源MSC的IL-6分泌的约1/9,或约1/10,或约1/11,或约1/12,或约1/13;
30.BLC,任选地是骨髓来源MSC的IL-6分泌的约1/6,或约1/7,或约1/8,或约1/9,或约1/10;
31.ENA-78(LIX),任选地是骨髓来源MSC的IL-6分泌的约1/1.2,或约1/1.3,或约1/1.4,或约1/1.5,或约1/1.6;
32.MCP-3,任选地是骨髓来源MSC的IL-6分泌的约1/12,或约1/13,或约1/14,或约1/15,或约1/16;
33.MIF,任选地是骨髓来源MSC的IL-6分泌的约1/14,或约1/15,或约1/16,或约1/17,或约1/18;以及
34.嗜酸性细胞活化趋化因子-3,任选地是骨髓来源MSC的IL-6分泌的约1/24,或约1/26,或约1/28,或约1/30,或约1/32;
在实施方案中,蛋白质分泌特征如表1所示。在实施方案中,表1的任何值在蛋白质分泌特征的上下文中可变化约5%,或约10%,或约15%。
在各种实施方案中,本发明涉及使用非病毒、基于RNA的方式将iPSC重编程为MSC。iPSC,即多能或分化程度较低的细胞,可以由非多能或分化细胞(包括成纤维细胞、角质形成细胞、黑素细胞血细胞、骨髓细胞、脂肪细胞和组织驻留祖细胞)重编程而得。
在一些实施方案中,用于重编程非多能细胞的方法包括:(a)提供非多能细胞;(b)培养非多能细胞;和(c)用一种或多种合成RNA分子转染非多能细胞,其中所述一种或多种合成RNA分子包括至少一种编码选自由Oct4蛋白、Sox2蛋白、Klf4蛋白、c-Myc蛋白、l-Myc蛋白、Tert蛋白、Nanog蛋白和Lin28蛋白组成的组的一种或多种重编程因子的RNA分子;其中转染导致细胞表达一种或多种重编程因子以导致细胞被重编程;并且其中步骤(c)在含有支持分化细胞重编程为低分化状态的成分的培养基存在下发生。
在一些实施方案中,用于将分化细胞重编程为低分化状态的方法包括:(a)提供分化细胞;(b)培养分化细胞;和(c)用一种或多种合成RNA分子转染分化细胞,其中所述一种或多种合成RNA分子包括至少一种编码选自由Oct4蛋白、Sox2蛋白、Klf4蛋白、c-Myc蛋白、l-Myc蛋白、Tert蛋白、Nanog蛋白和Lin28蛋白组成的组的一种或多种重编程因子的RNA分子;其中转染导致细胞表达一种或多种重编程因子以导致细胞被重编程为低分化状态;并且其中步骤(c)在含有支持分化细胞重编程为低分化状态的成分的培养基存在下发生。
在一些实施方案中,用于将分化细胞重编程为低分化状态的方法包括:(a)提供分化细胞;(b)培养分化细胞;和(c)用一种或多种合成RNA分子转染分化细胞,其中所述一种或多种合成RNA分子包括至少一种编码一种或多种重编程因子的RNA分子;其中转染导致细胞表达一种或多种重编程因子;并且其中步骤(c)进行至少两次,并且在一次或多次后期转染中转染的一种或多种合成RNA分子的量大于在一次或多次前期转染中转染的量以导致细胞被重编程为低分化状态,并且这在含有支持分化细胞重编程为低分化状态的成分的培养基存在下发生。
在一些实施方案中,用于重编程非多能细胞的方法包括:(a)提供非多能细胞;(b)培养非多能细胞;和(c)用一种或多种合成RNA分子转染非多能细胞,其中所述一种或多种合成RNA分子包括至少一种编码一种或多种重编程因子的RNA分子;其中转染导致细胞表达一种或多种重编程因子以导致细胞被重编程;并且其中步骤(c)在不使用辐照人新生儿成纤维细胞饲养层细胞的情况下进行,并且在含有支持细胞重编程的成分的培养基存在下发生。
在一些实施方案中,用于将分化细胞重编程为低分化状态的方法包括:(a)提供分化细胞;(b)培养分化细胞;和(c)用一种或多种合成RNA分子转染分化细胞,其中所述一种或多种合成RNA分子包括至少一种编码一种或多种重编程因子的RNA分子;其中转染导致细胞表达一种或多种重编程因子以导致细胞被重编程为低分化状态;并且其中步骤(c)在不使用辐照人新生儿成纤维细胞饲养层细胞的情况下进行,并且在含有支持细胞重编程为低分化状态的成分的培养基存在下发生。
在一些实施方案中,用于重编程非多能细胞的方法包括:(a)提供非多能细胞;(b)培养非多能细胞;(c)用一种或多种合成RNA分子转染非多能细胞,其中所述一种或多种合成RNA分子包括至少一种编码一种或多种重编程因子的RNA分子,并且其中转染导致细胞表达一种或多种重编程因子;和(d)在连续5天内重复步骤(c)至少两次,其中在一次或多次后期转染中转染的一种或多种合成RNA分子的量大于在一次或多次前期转染中转染的量以导致非多能细胞被重编程,其中步骤(c)和(d)在含有支持非多能细胞重编程的成分的培养基存在下发生。
在一些实施方案中,用于将分化细胞重编程为低分化状态的方法包括:(a)提供分化细胞;(b)培养分化细胞;(c)用一种或多种合成RNA分子转染分化细胞,其中所述一种或多种合成RNA分子包括至少一种编码一种或多种重编程因子的RNA分子,并且其中转染导致细胞表达一种或多种重编程因子;和(d)在连续5天内重复步骤(c)至少两次,其中在一次或多次后期转染中转染的一种或多种合成RNA分子的量大于在一次或多次前期转染中转染的量以导致细胞被重编程为低分化状态,其中步骤(c)和(d)在含有支持将分化细胞重编程为低分化状态的成分的培养基存在下发生。
在一些实施方案中,用于重编程非多能细胞的方法包括:(a)提供非多能细胞,所述非多能细胞来源于人类受试者的活检;(b)培养非多能细胞;和(c)用合成RNA分子转染非多能细胞,其中:合成RNA分子编码一种或多种选自由Oct4蛋白、Sox2蛋白、Klf4蛋白、c-Myc蛋白、I-Myc蛋白、Tert蛋白、Nanog蛋白和Lin28蛋白组成的组的重编程因子,转染导致非多能细胞表达一种或多种重编程非多能细胞的重编程因子;并且步骤(c)在不使用辐照人新生儿成纤维细胞饲养层细胞的情况下进行,并且在含有支持非多能细胞重编程的成分的培养基存在下发生。
在一些实施方案中,用于将细胞重编程为低分化状态的方法包括:(a)提供非多能细胞;(b)培养所述细胞;和(c)用合成RNA分子转染细胞,其中:RNA分子编码一种或多种选自由Oct4蛋白、Sox2蛋白、Klf4蛋白、c-Myc蛋白、I-Myc蛋白、Tert蛋白、Nanog蛋白和Lin28蛋白组成的组的重编程因子,转染导致细胞表达一种或多种将细胞重编程为低分化状态的重编程因子;并且步骤(c)在不使用辐照人新生儿成纤维细胞饲养层细胞的情况下进行,并且在含有支持将细胞重编程为低分化状态的成分的培养基存在下发生。
在一些实施方案中,用于将细胞重编程为低分化状态的方法包括:(a)提供非多能细胞;(b)在含有支持将细胞重编程为低分化状态的成分的培养基中培养所述细胞;和(c)用合成RNA分子转染细胞,其中:合成RNA分子编码一种或多种选自由Oct4蛋白、Sox2蛋白、Klf4蛋白、c-Myc蛋白、I-Myc蛋白、Tert蛋白、Nanog蛋白和Lin28蛋白组成的组的重编程因子,转染导致细胞表达一种或多种将细胞重编程为低分化状态的重编程因子;并且步骤(c)在不使用辐照人新生儿成纤维细胞饲养层细胞的情况下进行,并且在饲养细胞条件培养基存在下发生。
在一些实施方案中,用于将细胞重编程为低分化状态的方法包括:(a)提供非多能细胞;(b)在含有支持将细胞重编程为低分化状态的成分和白蛋白的培养基中培养所述细胞,其中用离子交换树脂和活性炭处理所述白蛋白;(c)用合成RNA分子转染细胞,其中RNA分子编码一种或多种选自由Oct4蛋白、Sox2蛋白、Klf4蛋白、c-Myc蛋白、I-Myc蛋白、Tert蛋白、Nanog蛋白和Lin28蛋白组成的组的重编程因子,其中转染导致细胞表达一种或多种将细胞重编程为低分化状态的重编程因子。
在一些实施方案中,用于将细胞重编程为低分化状态的方法包括:(a)用重编程培养基培养分化细胞;(b)用一种或多种合成RNA分子转染细胞,其中所述一种或多种合成RNA分子包括至少一种编码一种或多种重编程因子的RNA分子,并且其中转染导致细胞表达一种或多种重编程因子;和(c)在连续5天内重复步骤(b)至少两次,其中在一次或多次后期转染中转染的一种或多种合成RNA分子的量大于在一次或多次前期转染中转染的量以导致细胞被重编程为低分化状态,其中步骤(a)-(c)在不使用饲养细胞的情况下进行,并且在饲养细胞条件培养基存在下发生。
在一些实施方案中,用于将细胞重编程为低分化状态的方法包括:a.用含有白蛋白的重编程培养基培养分化细胞,其中用离子交换树脂或活性炭处理所述白蛋白;b.用一种或多种合成RNA分子转染细胞,其中一种或多种合成RNA分子包括至少一种编码一种或多种重编程因子的RNA分子,并且其中转染导致细胞表达一种或多种重编程因子;和c.在连续5天内重复步骤(b)至少两次以导致细胞被重编程为低分化状态。
在一些实施方案中,用于将细胞重编程为低分化状态的方法包括:a.用含有白蛋白的重编程培养基培养分化细胞,其中用辛酸钠处理白蛋白;将白蛋白温度升至至少40℃;并用离子交换树脂或活性炭处理白蛋白;b.用一种或多种合成RNA分子转染细胞,其中一种或多种合成RNA分子包括至少一种编码一种或多种重编程转录因子的RNA分子,并且其中转染导致细胞表达一种或多种合成RNA分子;和c.在连续约5天内重复步骤(b)至少两次以导致细胞被重编程为低分化状态。
在实施方案中,重编程是非病毒的。在实施方案中,重编程因子是Oct4、Sox2、Klf4、c-Myc、l-Myc、Tert、Nanog和Lin28中的一种或多种。
在一些实施方案中,获得iPSC并通过用非免疫原性信使RNA(mRNA)在确定的、无动物成分的过程中编码一种或多种重编程因子的细胞重编程生成MSC。在一些实施方案中,所述过程无免疫抑制剂。在一些实施方案中,所述过程无动物成分。在一些实施方案中,定义了所述过程。
在一些实施方案中,iPSC是使用基于mRNA的高效、无免疫抑制剂的方案由成人皮肤成纤维细胞生成的,然后使用21天高产单层方案将iPSC分化成MSC。在一些实施方案中,分化的MSC的特征在于Nanog和Oct4的下调和/或CD73和CD105的上调,例如,相对于源细胞。在一些实施方案中,rtPCR分析用于表征MSC。在一些实施方案中,MSC的多能性通过分化成脂肪细胞、成骨细胞和软骨细胞来证实。在一些实施方案中,如通过末端限制性片段的Southern分析所测量的,本发明的MSC的特征在于具有大约13kb长的端粒,而骨髓来源的MSC(BM MSC)的端粒长7kb。
在一些实施方案中,在连续传代时,本发明的MSC在衰老前经历>70次群体倍增,而BM MSC的群体倍增<20次。在一些实施方案中,本发明的MSC在衰老前能够经历大于约25,或大于约30,或大于约35,或大于约40,或大于约45,或大于约50,或大于约55,或大于约60,或大于约65,或大于约70,或大于约75次倍增。
可以通过将细胞暴露于特定的细胞外信号和/或通过特定蛋白质、microRNA等的异位表达来重编程细胞。虽然先前已经描述了几种重编程方法,但大多数依赖异位表达的方法都需要引入外源DNA,这可能带来突变风险。已经报道了基于直接递送重编程蛋白的无DNA重编程方法。然而,这些方法对于商业用途来说效率太低且不可靠。此外,已经描述了基于RNA的重编程方法(参见,例如,Angel.MIT Thesis.2008.1-56;Angel等人PLoSONE.2010.5,107;Warren等人Cell Stem Cell.2010.7,618-630;Angel.MITThesis.2011.1-89;和Lee等人,Cell.2012.151,547-558;所述文献的所有内容以引用的方式并入本文)。然而,现有的基于RNA的重编程方法在成体细胞上进行时速度慢、不可靠且效率低,需要多次转染(导致大量费用和出错机会),只能重编程有限数量的细胞类型,只能重编程有限数量的细胞类型的细胞,需要使用免疫抑制剂,并且需要使用多种人类来源的成分,包括血液来源的HSA和人成纤维细胞饲养层。先前公开的基于RNA的重编程方法的许多缺点使它们不适合研究、治疗或美容用途。
在一些实施方案中,通过用一种或多种编码一种或多种重编程因子的核酸转染细胞来进行重编程,所述重编程因子包括但不限于Oct4蛋白、Sox2蛋白、Klf4蛋白、c-Myc蛋白、l-Myc蛋白、TERT蛋白、Nanog蛋白、Lin28蛋白、Utf1蛋白、Aicda蛋白、miR200微RNA、miR302微RNA、miR367微RNA、miR369微RNA及其生物活性片段、类似物、变体和家族成员。在一些实施方案中,重编程细胞在体内进行。在一个实施方案中,通过用一种或多种编码一种或多种重编程因子的核酸转染细胞来对体内细胞进行重编程。在一个实施方案中,所述一种或多种核酸包括编码Oct4蛋白的RNA分子。在另一个实施方案中,所述一种或多种核酸还包括编码Sox2蛋白、Klf4蛋白和c-Myc蛋白的一种或多种RNA分子。在又一个实施方案中,所述一种或多种核酸还包括编码Lin28蛋白的RNA分子。在一个实施方案中,细胞是人皮肤细胞,并且所述人皮肤细胞被重编程为多能干细胞。在另一个实施方案中,细胞是人皮肤细胞,并且人皮肤细胞被重编程为葡萄糖反应性胰岛素产生细胞。可被重编程的其他细胞和细胞可被重编程为的其他细胞的实例包括但不限于皮肤细胞、多能干细胞、MSC、β-细胞、视网膜色素上皮细胞、造血细胞、心肌细胞、气道上皮细胞、神经干细胞、神经元、神经胶质细胞、骨细胞、血细胞和牙髓干细胞。在一个实施方案中,所述细胞与支持所述重编程细胞的培养基接触。在一个实施方案中,所述培养基还支持所述细胞。
重要的是,据报道,用编码Oct4、Sox2、Klf4和c-Myc的病毒感染皮肤细胞与在支持心肌细胞生长的培养基中培养细胞结合会导致皮肤细胞重编程为心肌细胞,而无需先将皮肤细胞重编程为多能干细胞(参见Efs等人Nat Cell Biol.2011;13:215-22,其内容以引用的方式并入本文)。在某些情况下,可能需要直接重编程(将一种体细胞重编程为另一种体细胞,而无需先将体细胞重编程为多能干细胞,也称为“转分化”),部分是因为培养多能干细胞可能耗时并且昂贵,建立和表征稳定的多能干细胞系所涉及的额外处理可能会增加污染的风险,并且与首次生产多能干细胞相关的额外培养时间可能会增加基因组不稳定和获得突变的风险,所述突变包括点突变、拷贝数变化和核型异常。因此,某些实施方案涉及用于体内重编程体细胞的方法,其中将细胞重编程为体细胞,并且其中不产生特征化的多能干细胞系。
在实施方案中,与根据其他方法相比,根据本发明的方法重编程细胞可能需要更少的总转染。因此,某些实施方案涉及用于体内重编程细胞的方法,其中在约连续20天内进行约1至约12次转染,或在约连续15天内进行约4至约10次转染,或在约连续10天内进行约4至约8次转染。认识到当细胞与含有核酸分子的培养基接触时,细胞可能同时或在不同时间接触和/或内化多于一种核酸分子。因此,即使细胞仅与含有核酸的培养基接触一次,细胞也可以与核酸接触一次以上,例如重复接触。
值得注意的是,核酸可以含有一个或多个如本文所述的非规范或“修饰”残基。例如,本文所述的任何非规范核苷酸可用于本发明的重编程方法。在一个实施方案中,假尿苷-5'-三磷酸可以在体外转录反应中取代尿苷-5'-三磷酸以产生合成RNA,其中合成RNA高达100%的尿苷残基可以被假尿苷残基替代。即使当假尿苷和5-甲基胞苷分别完全替代尿苷和胞苷时,体外转录也可以产生具有残留免疫原性的RNA,(参见,例如,Angel.Reprogramming Human Somatic Cells to Pluripotency Using RNA[DoctoralThesis].Cambridge,MA:MIT;2011,其内容以引用的方式并入本文)。因此,在用RNA转染细胞时,通常会在转染培养基中添加免疫抑制剂。在某些情况下,可能不希望在转染培养基中添加免疫抑制剂,部分是因为最常用于此目的的重组免疫抑制剂B18R可能很昂贵且难以制造。在实施方案中,根据本发明的方法在体内转染和/或重编程细胞,而不使用B18R或任何其他免疫抑制剂。在实施方案中,根据本发明的方法在体内重编程细胞而不使用免疫抑制剂可以是快速的、有效的和可靠的。因此,某些实施方案涉及用于在体内转染细胞的方法,其中转染培养基不含免疫抑制剂。其他实施方案涉及用于在体内重编程细胞的方法,其中转染培养基不含免疫抑制剂。在某些情况下,例如当使用高细胞密度时,向转染培养基中添加免疫抑制剂可能是有益的。因此,某些实施方案涉及用于在体内转染细胞的方法,其中转染培养基含有免疫抑制剂。其他实施方案涉及用于在体内重编程细胞的方法,其中转染培养基含有免疫抑制剂。在一个实施方案中,免疫抑制剂是B18R或其生物活性片段、类似物、变体或家族成员,或地塞米松或其衍生物。在一个实施方案中,转染培养基不含免疫抑制剂,并且选择核酸剂量以预防过度毒性。在另一个实施方案中,组织的核酸剂量小于约1mg/cm
根据本发明的某些实施方案产生的重编程细胞适用于治疗和/或美容应用,因为它们不含不合需要的外源DNA序列,并且它们不暴露于可能未定义的并且可能含有有毒和/或致病性污染物动物来源或人类来源产品。此外,本发明的某些实施方案的高速、高效和可靠性可以降低突变和其他染色体异常的获得和积累的风险。因此,本发明的某些实施方案可用于生成具有足以用于治疗和/或美容应用的安全特性的细胞。例如,使用RNA和本发明的培养基重编程细胞,其中培养基不含动物或人类来源成分,可以产生未暴露于同种异体材料的细胞。因此,某些实施方案涉及具有所需安全特性的重编程细胞。在一个实施方案中,重编程细胞具有正常核型。在另一个实施方案中,重编程细胞相对于患者基因组具有少于约5个拷贝数变异(CNV),诸如相对于患者基因组少于约3个拷贝数变异,或相对于患者基因组没有拷贝数变异。在又一个实施方案中,重编程细胞具有正常核型,和在编码区中相对于患者基因组少于约100个单核苷酸变体,或相对于患者基因组在编码区中少于约50个单核苷酸变体,或相对于患者基因组在编码区中少于约10个单核苷酸变体。
内毒素和核酸酶可以共纯化和/或与其他蛋白质(诸如血清白蛋白)结合。特别是重组蛋白,通常可能具有高水平的相关内毒素和核酸酶,部分是因为在其产生过程中可能发生细胞溶解。内毒素和核酸酶可以通过本发明的许多方法来减少、去除、替代或以其他方式灭活,包括例如,通过乙酰化、通过添加稳定剂诸如辛酸钠随后热处理、通过向白蛋白溶液和/或培养基添加和酸酶抑制剂、通过结晶、通过与一种或多种离子交换树脂接触、通过与活性炭接触、通过制备电泳或通过亲和色谱法。在实施方案中,提供了从培养基和/或从培养基的一种或多种组分的部分或完全减少、去除、替换或以其他方式灭活内毒素和/或核酸酶,这可以提高细胞转染和重编程的效率。因此,某些实施方案涉及用一种或多种核酸在体内转染细胞的方法,其中处理转染培养基以部分或完全减少、去除、替代或以其他方式灭活一种或多种内毒素和/或核酸酶。其他实施方案涉及引起核酸最小降解的培养基。在一个实施方案中,培养基含有小于约1EU/mL,或小于约0.1EU/mL,或小于约0.01EU/mL。
在某些情况下,基于蛋白质的脂质载体诸如血清白蛋白可以用非基于蛋白质的脂质载体诸如甲基-β-环糊精替代。本发明的培养基也可以在没有脂质载体的情况下使用,例如,当使用可能不需要或可能不会受益于脂质载体的存在的方法(例如,使用一种或多种基于脂质的转染试剂、基于聚合物的转染试剂或基于肽的转染试剂或使用电穿孔)进行转染时。许多蛋白质缔合分子,诸如金属,可能对体内细胞有剧毒。这种毒性可导致活力降低,以及获得突变。因此某些实施方案具有产生不含毒性分子的细胞的额外益处。
可以通过将蛋白质悬浮在溶液中并测量溶液的电导率来测量蛋白质的缔合分子成分。因此,某些实施方案涉及含有蛋白质的培养基,其中蛋白质在水中的约10%溶液具有小于约500μmho/cm的电导率。在一个实施方案中,溶液具有小于约50μmho/cm的电导率。在另一个实施方案中,小于约0.65%的蛋白质干重包含脂质和/或小于约0.35%的蛋白质干重包含游离脂肪酸。
可以增加递送至体内细胞的核酸量以增加核酸的所需效果。然而,增加递送至体内细胞的核酸量超过某一点时会引起细胞活力降低,部分是因为转染试剂的毒性。在实施方案中,核酸以固定体积被递送至体内细胞群(例如,组织区域中的细胞),并且递送至每个细胞的核酸量可取决于递送至细胞群的核酸总量和细胞密度,细胞密度越高导致递送至每个细胞的核酸越少。在某些实施方案中,用一种或多种核酸转染体内细胞一次以上。在某些条件下,例如当细胞增殖时,细胞密度从一次转染到下一次转染可能会变化。因此,某些实施方案涉及用核酸在体内转染细胞的方法,其中细胞被转染一次以上,并且其中递送至细胞的核酸的量对于两次转染是不同的。在一个实施方案中,细胞在两次转染之间增殖,并且两次转染中的第二次递送至细胞的核酸量大于两次转染中的第一次的核酸量。在另一个实施方案中,细胞被转染两次以上,并且三次转染中的第二次递送至细胞的核酸量大于相同三次转染中的第一次的核酸量,并且相同三次转染中的第三次递送至细胞的核酸量大于相同三次转染中的第二次的核酸量。在又一个实施方案中,细胞被转染一次以上,并且在每次转染期间递送至细胞的核酸最大量足够低以产生至少两次连续转染的至少约80%的活力。
在实施方案中,提供了其中调节在一系列转染中递送至体内增殖细胞群的核酸量可导致核酸作用增加和细胞活力增加的方法。在实施方案中,当体内细胞在一系列转染中与编码一种或多种重编程因子的一种或多种核酸接触时,对于一系列转染的至少一部分,当后期转染中递送的核酸量大于前期转染中递送的核酸量时,重编程的效率可被增加。因此,某些实施方案涉及用于在体内重编程细胞的方法,其中在一系列转染中将一种或多种核酸重复递送至细胞,并且至少一次后期转染的递送至细胞的核酸的量大于至少一次前期转染的核酸量。在一个实施方案中,细胞被转染约2至约10次,或约3至约8次,或约4至约6次。在另一个实施方案中,一种或多种核酸包括至少一种RNA分子,细胞被转染约2至约10次,并且在每次转染中递送至细胞的核酸量等于或大于在最近的前一次转染中递送到细胞的核酸量。在又一个实施方案中,在第一次转染中递送至细胞的核酸量在约20ng/cm
某些实施方案涉及用核酸在体内转染细胞的方法,其中通过测量细胞密度来确定核酸量,并且基于细胞密度的测量选择转染的核酸量。在一个实施方案中,通过光学方式测量细胞密度。在另一个实施方案中,细胞被重复转染,细胞密度在两次转染之间增加,并且两次转染中的第二次转染的核酸量大于两次转染中的第一次转染的核酸量。
在实施方案中,与本发明的培养基接触的细胞的体内转染效率和活力可以通过调整培养基来提高。因此,某些实施方案涉及一种用于调整培养基的方法。其他实施方案涉及经调整的培养基。在一个实施方案中,饲养层是成纤维细胞,并且培养基被调整大约24小时。其他实施方案涉及用于体内转染细胞的方法,其中转染培养基是经调整的。其他实施方案涉及用于体内重编程细胞的方法,其中培养基是经调整的。在一个实施方案中,饲养层被有丝分裂灭活,例如,通过暴露于诸如丝裂霉素-C的化学物质或通过暴露于γ辐射。在某些实施方案中,仅使用自体材料可能是有益的,部分例如并且不受理论束缚,避免疾病从饲养层传播到细胞或患者的风险。因此,某些实施方案涉及用于体内转染细胞的方法,其中转染培养基是经调整的,并且其中饲养层来源于与被转染的细胞相同的个体。其他实施方案涉及用于体内重编程细胞的方法,其中培养基是经调整的,并且其中饲养层来源于与被重编程的细胞相同的个体。
可以通过调整将几种分子添加到培养基中。因此,某些实施方案涉及补充有一种或多种存在于条件培养基中的分子的培养基。在一个实施方案中,培养基补充有Wnt1、Wnt2、Wnt3、Wnt3a或其生物活性片段、类似物、变体、激动剂或家族成员。在另一个实施方案中,培养基补充有TGF-β或其生物活性片段、类似物、变体、激动剂或家族成员。在又一个实施方案中,根据本发明的方法重编程体内细胞,其中培养基在约1至约5天不补充TGF-β,然后补充TGF-β至少约2天。在又一个实施方案中,培养基补充有IL-6、IL-6R或其生物活性片段、类似物、变体、激动剂或家族成员。在又一个实施方案中,培养基补充有鞘脂或脂肪酸。在又一个实施方案中,鞘脂是溶血磷脂酸、溶血鞘磷脂、鞘氨醇-1-磷酸或其生物活性类似物、变体或衍生物。
除了使细胞灭活有丝分裂外,在某些条件下,辐照可以改变细胞的基因表达,导致细胞产生的某些蛋白质比未辐照的细胞少,并且某些其他蛋白质比未辐照的细胞多,所述蛋白质例如Wnt蛋白家族的成员。此外,Wnt蛋白家族的某些成员可以促进细胞的生长和转化。在实施方案中,通过使体内细胞与使用辐照的饲养层而不是丝裂霉素c处理的饲养层进行调整的培养基接触,可以大大提高重编程效率。在实施方案中,当使用经辐照的饲养层时观察到的重编程效率的增加部分是由饲养层分泌的Wnt蛋白引起的。因此,某些实施方案涉及用于体内重编程细胞的方法,其中使细胞与Wnt1、Wnt2、Wnt3、Wnt3a或其生物活性片段、类似物、变体、家族成员或激动剂接触,包括Wnt蛋白下游靶标的激动剂和/或模拟Wnt蛋白的一种或多种生物学效应的剂,例如2-氨基-4-[3,4-(亚甲基二氧)苄氨基]-6-(3-甲氧基苯基)嘧啶。
因为许多基于DNA的重编程方法效率低,这些方法可能难以或不可能用于来源于患者样品的细胞,这些样品可能仅包含少量细胞。相比之下,本发明的某些实施方案的高效率可以允许对少量细胞(包括单个细胞)进行可靠的重编程。某些实施方案涉及用于重编程少量细胞的方法。其他实施方案涉及用于重编程单个细胞的方法。在一个实施方案中,细胞与一种或多种酶接触。在另一个实施方案中,酶是胶原酶。在另一个实施方案中,胶原酶无动物成分。在一个实施方案中,胶原酶以约0.1mg/mL至约10mg/mL,或约0.5mg/mL至约5mg/mL的浓度存在。在另一个实施方案中,细胞是血细胞。在又一个实施方案中,使细胞与含有一种或多种来源于患者血液的蛋白质的培养基接触。在又一个实施方案中,使细胞与包含以下的培养基接触:DMEM/F12+2mM L-丙氨酰-L-谷氨酰胺+约5%至约25%的患者来源血清,或约10%至约20%的患者血清来源血清,或约20%的患者来源血清。
在实施方案中,使用本发明的培养基用编码Oct4、Sox2、Klf4和c-Myc的RNA混合物在体内转染细胞可引起细胞增殖速率增加。当递送至细胞的RNA量太低而无法确保所有细胞都被转染时,只有一小部分细胞可能显示出增殖速率增加。在某些情况下,诸如在生成个性化治疗剂时,可能需要增加细胞的增殖速率,部分是因为这样做可以减少生成治疗剂所需的时间,因此可以减少治疗剂的成本。因此,某些实施方案涉及用于用编码Oct4、Sox2、Klf4和c-Myc的RNA的混合物在体内转染细胞的方法。在一个实施方案中,细胞表现出增加的增殖速率。在另一个实施方案中,细胞被重编程。
虽然本文提供了用于产生特定类型的细胞和用于产生包含特定类型细胞的治疗剂的详细实施例,但应认识到本发明的方法可用于产生许多其他类型的细胞,和产生包含许多其他类型细胞中的一种或多种的治疗剂,例如,通过根据本发明的方法重编程细胞,并通过提供与在发育过程中的细胞微环境中存在的条件相似的条件在模拟发育的一个或多个方面的条件下培养细胞。
其他实施方案涉及用于在体内重编程细胞的方法。在一个实施方案中,通过使细胞与一种或多种核酸接触来重编程细胞。在一个实施方案中,使细胞与编码Oct4蛋白、Sox2蛋白、Klf4蛋白、c-Myc蛋白、Lin28蛋白中的至少一种或其生物活性片段、变体或衍生物的多种核酸接触。在另一个实施方案中,使细胞与编码多种蛋白质的多种核酸接触,所述多种蛋白质包括:Oct4蛋白、Sox2蛋白、Klf4蛋白和c-Myc蛋白或其一种或多种生物活性片段、变体或衍生物。
示例性受试者或患者是指任何脊椎动物,包括但不限于人类和其他灵长类动物(例如,黑猩猩和其他猿类和猴子物种)、家畜(例如,牛、绵羊、猪、山羊和马)、家养哺乳动物(例如,狗和猫)、实验室动物(例如,啮齿动物诸如小鼠、大鼠和豚鼠)和鸟类(例如,家禽、野禽和猎鸟,诸如鸡、火鸡和其他鸡类、鸭、鹅等)。在一些实施方案中,受试者是哺乳动物。在一些实施方案中,受试者是人类。
在一些实施方案中,合成RNA分子被用于将iPSC重编程为MSC。在实施方案中,合成RNA分子是mRNA。在实施方案中,合成RNA分子是体外转录的。
在一些实施方案中,合成RNA分子含有一种或多种非规范核苷酸,在为嘧啶的情况下在2C和/或4C和/或5C位置包含一个或多个取代基或在为嘌呤的情况下在6C和/或7N和/或8C位置包含一个或多个取代基可能比仅含有规范核苷酸的合成RNA分子毒性低,部分是因为这些位置的取代干扰检测外源核酸的蛋白质对合成RNA分子的鉴定的能力,此外,这些位置的取代对合成RNA分子翻译为蛋白质的效率影响最小,部分是因为这些位置的取代缺乏碱基配对和碱基堆叠相互作用的干扰。
在实施方案中,合成RNA分子是包含一种或多种非规范核苷酸的mRNA,所述核苷酸选自2-硫代尿苷、5-氮杂尿苷、假尿苷、4-硫尿苷、5-甲基尿苷、5-甲基假尿苷、5-氨基尿苷、5-氨基假尿苷、5-羟基尿苷、5-羟基假尿苷、5-甲氧基尿苷、5-甲氧基假尿苷、5-乙氧基尿苷、5-乙氧基假尿苷、5-羟甲基尿苷、5-羟甲基假尿苷、5-羧基尿苷、5-羧基假尿苷、5-甲酰基尿苷、5-甲酰基假尿苷、5-甲基-5-氮杂尿苷、5-氨基-5-氮杂尿苷、5-羟基-5-氮杂尿苷、5-甲基假尿苷、5-氨基假尿苷、5-羟基假尿苷、4-硫代-5-氮杂尿苷、4-硫代假尿苷、4-硫代-5-甲基尿苷、4-硫代-5-氨基尿苷、4-硫代-5-羟基尿苷、4-硫代-5-甲基-5-氮杂尿苷、4-硫代-5-氨基-5-氮杂尿苷、4-硫代-5-羟基-5-氮杂尿苷、4-硫代-5-甲基假尿苷、4-硫代-5-氨基假尿苷、4-硫代-5-羟基假尿苷、2-硫代胞苷、5-氮杂胞苷、假异胞苷、N4-甲基胞苷、N4-氨基胞苷、N4-羟基胞苷、5-甲基胞苷、5-氨基胞苷、5-羟基胞苷、5-甲氧基胞苷、5-乙氧基胞苷、5-羟甲基胞苷、5-羧基胞苷、5-甲酰基胞苷、5-甲基-5-氮杂胞苷、5-氨基-5-氮杂胞苷、5-羟基-5-氮杂胞苷、5-甲基假异胞苷、5-氨基假异胞苷、5-羟基假异胞苷、N4-甲基-5-氮杂胞苷、N4-甲基假异胞苷、2-硫代-5-氮杂胞苷、2-硫代假异胞苷、2-硫代-N4-甲基胞苷、2-硫代-N4-氨基胞苷、2-硫代-N4-羟基胞苷、2-硫代-5-甲基胞苷、2-硫代-5-氨基胞苷、2-硫代-5-羟基胞苷、2-硫代-5-甲基-5-氮杂胞苷、2-硫代-5-氨基-5-氮杂胞苷、2-硫代-5-羟基-5-氮杂胞苷、2-硫代-5-甲基假异胞苷、2-硫代-5-氨基假异胞苷、2-硫代-5-羟基假异胞苷、2-硫代-N4-甲基-5-氮杂胞苷、2-硫代-N4-甲基假异胞苷、N4-甲基-5-甲基胞苷、N4-甲基-5-氨基胞苷、N4-甲基-5-羟基胞苷、N4-甲基-5-甲基-5-氮杂胞苷、N4-甲基-5-氨基-5-氮杂胞苷、N4-甲基-5-羟基-5-氮杂胞苷、N4-甲基-5-甲基假异胞苷、N4-甲基-5-氨基假异胞苷、N4-甲基-5-羟基假异胞苷、N4-氨基-5-氮杂胞苷、N4-氨基假异胞苷、N4-氨基-5-甲基胞苷、N4-氨基-5-氨基胞苷、N4-氨基-5-羟基胞苷、N4-氨基-5-甲基-5-氮杂胞苷、N4-氨基-5-氨基-5-氮杂胞苷、N4-氨基-5-羟基-5-氮杂胞苷、N4-氨基-5-甲基假异胞苷、N4-氨基-5-氨基假异胞苷、N4-氨基-5-羟基假异胞苷、N4-羟基-5-氮杂胞苷、N4-羟基假异胞苷、N4-羟基-5-甲基胞苷、N4-羟基-5-氨基胞苷、N4-羟基-5-羟基胞苷、N4-羟基-5-甲基-5-氮杂胞苷、N4-羟基-5-氨基-5-氮杂胞苷、N4-羟基-5-羟基-5-氮杂胞苷、N4-羟基-5-甲基假异胞苷、N4-羟基-5-氨基假异胞苷、N4-羟基-5-羟基假异胞苷、2-硫代-N4-甲基-5-甲基胞苷、2-硫代-N4-甲基-5-氨基胞苷、2-硫代-N4-甲基-5-羟基胞苷、2-硫代-N4-甲基-5-甲基-5-氮杂胞苷、2-硫代-N4-甲基-5-氨基-5-氮杂胞苷、2-硫代-N4-甲基-5-羟基-5-氮杂胞苷、2-硫代-N4-甲基-5-甲基假异胞苷、2-硫代-N4-甲基-5-氨基假异胞苷、2-硫代-N4-甲基-5-羟基假异胞苷、2-硫代-N4-氨基-5-氮杂胞苷、2-硫代-N4-氨基假异胞苷、2-硫代-N4-氨基-5-甲基胞苷、2-硫代-N4-氨基-5-氨基胞苷、2-硫代-N4-氨基-5-羟基胞苷、2-硫代-N4-氨基-5-甲基-5-氮杂胞苷、2-硫代-N4-氨基-5-氨基-5-氮杂胞苷、2-硫代-N4-氨基-5-羟基-5-氮杂胞苷、2-硫代-N4-氨基-5-甲基假异胞苷、2-硫代-N4-氨基-5-氨基假异胞苷、2-硫代-N4-氨基-5-羟基假异胞苷、2-硫代-N4-羟基-5-氮杂胞苷、2-硫代-N4-羟基假异胞苷、2-硫代-N4-羟基-5-甲基胞苷、N4-羟基-5-氨基胞苷、2-硫代-N4-羟基-5-羟基胞苷、2-硫代-N4-羟基-5-甲基-5-氮杂胞苷、2-硫代-N4-羟基-5-氨基-5-氮杂胞苷、2-硫代-N4-羟基-5-羟基-5-氮杂胞苷、2-硫代-N4-羟基-5-甲基假异胞苷、2-硫代-N4-羟基-5-氨基假异胞苷、2-硫代-N4-羟基-5-羟基假异胞苷、N6-甲基腺苷、N6-氨基腺苷、N6-羟基腺苷、7-脱氮腺苷、8-氮杂腺苷、N6-甲基-7-脱氮腺苷、N6-甲基-8-氮杂腺苷、7-脱氮-8-氮杂腺苷、N6-甲基-7-脱氮-8-氮杂腺苷、N6-氨基-7-脱氮腺苷、N6-氨基-8-氮杂腺苷、N6-氨基-7-脱氮-8-氮杂腺苷、N6-羟基腺苷、N6-羟基-7-脱氮腺苷、N6-羟基-8-氮杂腺苷、N6-羟基-7-脱氮-8-氮杂腺苷、6-硫代鸟苷、7-脱氮鸟苷、8-氮杂鸟苷、6-硫代-7-脱氮鸟苷、6-硫代-8-氮杂鸟苷、7-脱氮-8-氮杂鸟苷和6-硫代-7-脱氮-8-氮杂鸟苷。
在一些实施方案中,一种或多种非规范核苷酸选自5-羟基胞苷、5-甲基胞苷、5-羟甲基胞苷、5-羧基胞苷、5-甲酰基胞苷、5-甲氧基胞苷、5-羟基尿苷、5-羟基甲基尿苷、5-羧基尿苷、5-甲酰基尿苷、5-甲氧基尿苷、假尿苷、5-羟基假尿苷、5-甲基假尿苷、5-羟甲基假尿苷、5-羧基假尿苷、5-甲酰基假尿苷和5-甲氧基假尿苷。在一些实施方案中,至少50%,或至少55%,或至少60%,或至少65%,或至少70%,或至少75%,或至少80%,或至少85%,或至少90%,或至少95%,或100%的非规范核苷酸是5-羟基胞苷、5-甲基胞苷、5-羟甲基胞苷、5-羧基胞苷、5-甲酰基胞苷、5-甲氧基胞苷、5-羟基尿苷、5-甲基尿苷、5-羟甲基尿苷、5-羧基尿苷、5-甲酰基尿苷、5-甲氧基尿苷、假尿苷、5-羟基假尿苷、5-甲基假尿苷、5-羟甲基假尿苷、5-羧基假尿苷、5-甲酰基假尿苷和5-甲氧基假尿苷中的一种或多种。
在一些实施方案中,至少约50%,或至少约55%,或至少60%,或至少65%,或至少70%,或至少75%,或至少80%,或至少至少85%,或至少90%,或至少95%,或100%的胞苷残基是选自5-羟基胞苷、5-甲基胞苷、5-羟甲基胞苷、5-羧基胞苷、5-甲酰基胞苷、5-甲氧基胞苷的非规范核苷酸。
在一些实施方案中,至少约20%,或约30%,或约40%,或约50%,或至少约55%,或至少60%,或至少65%,或至少70%,或至少75%,或至少80%,或至少85%,或至少90%,或至少95%,或100%的尿苷残基是选自5-羟基尿苷、5-甲基尿苷、5-羟甲基尿苷、5-羧基尿苷、5-甲酰基尿苷、5-甲氧基尿苷、假尿苷、5-羟基假尿苷、5-甲基假尿苷、5-羟甲基假尿苷、5-羧基假尿苷、5-甲酰基假尿苷和5-甲氧基假尿苷的非规范核苷酸。
在一些实施方案中,至少约10%(例如10%,或约20%,或约30%,或约40%,或约50%)的鸟苷残基是非规范核苷酸,并且所述非规范核苷酸任选地是7-脱氮鸟苷。在一些实施方案中,RNA含有不超过约50%的代替鸟苷残基的7-脱氮鸟苷。
在一些实施方案中,合成RNA分子不含代替腺苷残基的非规范核苷酸。
需注意,某些非规范核苷酸存在替代命名方案。例如,在某些情况下,5-甲基假尿苷可以被称为“3-甲基假尿苷”或“N3-甲基假尿苷”或“1-甲基假尿苷”或“N1-甲基假尿苷”。含有前缀“氨基”的核苷酸可以指含有与核苷酸的所述位置处的原子结合的氮原子的任何核苷酸,例如,5-氨基胞苷可以指5-氨基胞苷、5-甲基氨基胞苷和5-硝基胞苷。类似地,含有前缀“甲基”的核苷酸可以指含有与核苷酸的所述位置处的原子结合的碳原子的任何核苷酸,例如,5-甲基胞苷可以指5-甲基胞苷、5-乙基胞苷和5-羟甲基胞苷,含有前缀“硫代”的核苷酸可以指含有与核苷酸的给定位置处的原子结合的硫原子的任何核苷酸,并且含有前缀“羟基”的核苷酸可以指含有与核苷酸的给定位置处的原子结合的氧原子的任何核苷酸,例如,5-羟基尿苷可以指5-羟基尿苷和具有与氧原子结合的甲基的尿苷,其中氧原子与位于尿苷的5C位置处的原子结合。
通过通常用于体外转录的RNA聚合酶,某些非规范核苷酸可以比其他非规范核苷酸更有效地并入RNA分子中,部分是因为这些特定非规范核苷酸参与标准碱基-配对相互作用和碱基堆叠相互作用的趋势,和以类似于相应的规范核苷酸与RNA聚合酶相互作用的方式与RNA聚合酶相互作用。结果,含有一种或多种非规范核苷酸的某些核苷酸混合物可能是有益的,部分是因为含有这些核苷酸混合物的体外转录反应可以产生大量RNA。因此,某些实施方案涉及含有一种或多种核苷酸的核苷酸混合物,所述核苷酸在为嘧啶的情况下在2C和/或4C和/或5C位置处包含一个或多个取代基,或在为嘌呤的情况下在6C和/或7N和/或8C位置处包含一个或多个取代基。核苷酸混合物包括但不限于(每个核苷酸前面的数字表示在体外转录反应中非规范核苷酸三磷酸的示例性分数,例如,0.2假异胞苷是指含有腺苷-5'-三磷酸、鸟苷-5'-三磷酸、尿苷-5'-三磷酸、胞苷-5'-三磷酸和假异胞苷-5'-三磷酸的反应,其中假异胞苷-5'-三磷酸以大约等于存在于反应中的假异胞苷-5'-三磷酸+胞苷-5'-三磷酸的总量的0.2倍的量存在于反应中,所述量在摩尔或质量的基础上测量,并且其中核苷前面的多于一个数字表示示例性分数的范围):1.0假尿苷、0.1–0.8 2-硫代尿苷、0.1–0.8 5-甲基尿苷、0.2–1.0 5-羟基尿苷、0.2–1.0 5-甲氧基尿苷、0.1–1.0 5-氨基尿苷、0.1–1.0 4-硫代尿苷、0.1–1.0 2-硫代尿苷、0.1–1.0 4-硫代假尿苷、0.1–1.0 5-羟基假尿苷、0.2–1 5-甲基假尿苷、0.2–1.0 5-甲氧基假尿苷、0.1–1.0 5-氨基假尿苷、0.2–1.02-硫代胞苷、0.1–0.8假异胞苷、0.2-1.0 5-甲基胞苷、0.2–1.0 5-羟基胞苷、0.2–1.0 5-羟甲基胞苷、0.2–1.0 5-甲氧基胞苷、0.1–1.0 5-氨基胞苷、0.2–1.0 N4-甲基胞苷、0.2–1.05-甲基假异胞苷、0.2–1.0 5-羟基假异胞苷、0.2-1.0 5-氨基假异胞苷、0.2-1.0N4-甲基假异胞苷、0.2-1.0 2-硫代假异胞苷、0.2-1.0 7-脱氮鸟苷、0.2-1.0 6-硫代鸟苷、0.2-1.06-硫代-7-脱氮杂鸟苷、0.2-1.0 8-氮杂鸟苷、0.2-1.0 7-脱氮-8-氮杂鸟苷、0.2-1.0 6-硫代-8-氮杂鸟苷、0.1-0.5 7-多氮杂鸟苷和0.1-0.5N6-甲基腺苷。
在一些实施方案中,包含一种或多种非规范核苷酸组分或合成多核苷酸组分(例如,其可通过体外转录制备)的RNA在遗传密码中具有腺嘌呤或“A”的位置处基本上或完全含有规范核苷酸。在上下文中,术语“基本上”是指至少90%。在这些实施方案中,RNA组合物或合成多核苷酸组合物还可以在遗传密码中具有“G”的位置处含有(例如,由以下组成)7-脱氮鸟苷以及相应的规范核苷酸“G”,并且在具有G的位置处的规范和非规范核苷酸可以在5:1至1:5的范围内,或在一些实施方案中在2:1至1:2的范围内。在这些实施方案中,RNA组合物或合成多核苷酸组合物还可以在遗传密码中具有“C”的位置处含有(例如,由以下组成)5-羟基胞苷、5-甲基胞苷、5-羟甲基胞苷、5-羧基胞苷、5-甲酰基胞苷、5-甲氧基胞苷中的一种或多种(例如,两种、三种或四种)以及规范核苷酸“C”,并且在具有C的位置处的规范和非规范核苷酸可以在5:1至1:5的范围内,或在一些实施方案中在2:1至1:2的范围内。在一些实施方案中,在“C”的位置处的非规范核苷酸的水平如前一段所述。在这些实施方案中,RNA组合物或合成多核苷酸组合物还可以在遗传密码中具有“U”的位置处含有(例如,由以下组成)5-羟基尿苷、5-甲基尿苷、5-羟甲基尿苷、5-羧基尿苷、5-甲酰基尿苷、5-甲氧基尿苷、假尿苷、5-羟基假尿苷、5-甲基假尿苷、5-羟甲基假尿苷、5-羧基假尿苷、5-甲酰基假尿苷和5-甲氧基假尿苷中的一种或多种(例如,两种、三种或四种)以及规范核苷酸“U”,并且在具有“U”的位置处的规范和非规范核苷酸可以在5:1至1:5的范围内,或在一些实施方案中在2:1至1:2的范围内。在一些实施方案中,在“U”的位置处的非规范核苷酸的水平如前一段所述。
在实施方案中,组合某些非规范核苷酸可能是有益的,部分是因为非规范核苷酸对降低RNA分子毒性的贡献可以是累加的。因此,某些实施方案涉及核苷酸混合物,其中核苷酸混合物含有多于一种以上列出的非规范核苷酸,例如,核苷酸混合物含有假异胞苷和7-脱氮鸟苷两者,或核苷酸混合物含有N4-甲基胞苷和7-脱氮鸟苷两者等。在一个实施方案中,核苷酸混合物含有多于一种以上列出的非规范核苷酸,并且每种非规范核苷酸以以上列出的分数存在于混合物中,例如,核苷酸混合物含有0.1-0.8假异胞苷和0.2-1.0 7-脱氮鸟苷或核苷酸混合物含有0.2-1.0 N4-甲基胞苷和0.2-1.0 7-脱氮鸟苷等。
在某些情况下,例如,当可能不需要或不希望使体外转录反应的产量最大化时,可以使用除上文给出的那些之外的核苷酸分数。上面列出的示例性分数和分数范围涉及典型纯度(大于90%纯度)的核苷酸三磷酸溶液。通过使用更高纯度(例如,大于约95%纯度或大于约98%纯度或大于约99%纯度或大于约99.5%纯度)的核苷酸-三磷酸盐溶液,可以使用更大分数的这些和其他核苷酸,这可以例如通过使用现有的化学纯化技术诸如高压液相色谱(HPLC)纯化核苷酸三磷酸溶液或通过其他方式来实现。在一个实施方案中,纯化具有多种异构体的核苷酸以富集所需异构体。
在一些实施方案中,一种或多种非规范核苷酸避免了显著的细胞毒性。
在一些实施方案中,非规范核苷酸包括5-羟基胞苷、5-甲基胞苷、5-羟甲基胞苷、5-羧基胞苷、5-甲酰基胞苷、5-甲氧基胞苷、假尿苷、5-羟基尿苷、5-甲基尿苷、5-羟甲基尿苷、5-羧基尿苷、5-甲酰基尿苷、5甲氧基尿苷、5-羟基假尿苷、5-甲基假尿苷、5-羟甲基假尿苷、5-羧基假尿苷、5-甲酰基假尿苷和5-甲氧基假尿苷中的一种或多种,任选地为非规范核苷酸的至少50%,或至少60%,或至少70%,或至少80%,或至少90%,或100%的量。
在一些实施方案中,至少约50%的胞苷残基是非规范核苷酸,并且其选自5-羟基胞苷、5-甲基胞苷、5-羟甲基胞苷、5-羧基胞苷、5-甲酰基胞苷和5-甲氧基胞苷。
在一些实施方案中,至少约75%或至少约90%的胞苷残基是非规范核苷酸,并且所述非规范核苷酸选自5-羟基胞苷、5-甲基胞苷、5-羟甲基胞苷、5-羧基胞苷、5-甲酰基胞苷和5-甲氧基胞苷。
在一些实施方案中,至少约20%的尿苷,或至少约40%,或至少约50%,或至少约75%,或至少约90%的尿苷残基是非规范核苷酸,并且所述非规范核苷酸选自假尿苷、5-羟基尿苷、5-甲基尿苷、5-羟甲基尿苷、5-羧基尿苷、5-甲酰基尿苷、5-甲氧基尿苷、5-羟基假尿苷、5-甲基假尿苷、5-羟甲基假尿苷、5-羧基假尿苷、5-甲酰基假尿苷和5-甲氧基假尿苷。
在一些实施方案中,至少约40%,或至少约50%,或至少约75%,或至少约90%的尿苷残基是非规范核苷酸,并且所述非规范核苷酸选自假尿苷、5-羟基尿苷、5-甲基尿苷、5-羟甲基尿苷、5-羧基尿苷、5-甲酰基尿苷、5-甲氧基尿苷、5-羟基假尿苷、5-甲基假尿苷、5-羟甲基假尿苷、5-羧基假尿苷、5-甲酰基假尿苷和5-甲氧基假尿苷。
在一些实施方案中,至少约10%的鸟嘌呤残基是非规范核苷酸,并且所述非规范核苷酸任选地是7-脱氮鸟苷。在一些实施方案中,合成RNA包含不超过约50%的代替鸟苷残基的7-脱氮鸟苷。在一些实施方案中,合成RNA不包含代替腺苷残基的非规范核苷酸。
在一些实施方案中,合成RNA包含5'帽子结构。在一些实施方案中,合成RNA包含Kozak共有序列。在一些实施方案中,合成RNA包含5'-UTR,其包含增加RNA体内稳定性的序列,并且5'-UTR任选地包含α-珠蛋白或β-珠蛋白5'-UTR。在一些实施方案中,合成RNA包含3'-UTR,其包含增加RNA体内稳定性的序列,并且3'-UTR任选地包含α-珠蛋白或β-珠蛋白3'-UTR。在一些实施方案中,合成RNA包含5'-UTR,其包含以细胞类型特异下方式调节RNA稳定性的微小RNA结合位点。在一些实施方案中,合成RNA包含3'-UTR,其包含以细胞类型特异下方式调节RNA稳定性的微小RNA结合位点。在一些实施方案中,合成RNA包含3'多聚(A)尾。在一些实施方案中,合成RNA包含3'多聚(A)尾,其包含约20个核苷酸至约250个核苷酸。
在一些实施方案中,合成RNA包含约200个核苷酸至约5000个核苷酸。在一些实施方案中,合成RNA包含约500至约2000个核苷酸,或约500至约1500个核苷酸,或约500至约1000个核苷酸。
在各种实施方案中,本发明的方法和组合物可用在治疗、预防或改善疾病、病症和/或病状的方法中。例如,在一些实施方案中,所述体内递送方法,包括施用策略和制剂被用在治疗方法中。在一些方法中,所述方法减轻与疾病相关的症状。在一些实施方案中,所述方法消除了疾病的根本原因。在一些实施方案中,所述方法用于治疗需要免疫抑制的疾病。在一些实施方案中,所述方法减少炎症。在一些实施方案中,所述方法减少免疫反应。
在实施方案中,所公开的组合物适用于治疗肌萎缩侧索硬化(ALS)、脊髓损伤、退行性椎间盘疾病、冠状动脉疾病、急性心肌梗死、酒精性肝硬化、丙型肝炎病毒(HCV)诱导的肝硬化、多发性硬化症(MS)、骨关节炎(OA)、膝骨关节炎、肾同种异体移植物、严重肢体缺血、缺血性心肌病、克罗恩氏病(Crohn's disease)、特发性肺纤维化、肛瘘、脊髓损伤、系统性红斑狼疮(SLE)、急性呼吸窘迫综合征(ARDS)、急性移植物抗宿主病(aGvHD)、早产儿支气管肺发育不良(BPD)、自闭症非缺血性心力衰竭和/或2型糖尿病。
在实施方案中,本方法涉及在自身免疫性疾病或病症中的治疗用途。
可被本发明治疗或预防的自身免疫性疾病或病症的实例包括但不限于斑秃、强直性脊柱炎、抗磷脂综合征、自身免疫性阿狄森氏病(autoimmune Addison's disease)、肾上腺自身免疫性疾病、自身免疫性溶血性贫血、自身免疫性肝炎、自身免疫性卵巢炎和睾丸炎、自身免疫性血小板减少症、贝切特氏病(Behcet's disease)、大疱性类天疱疮、心肌病、乳糜泻皮炎、慢性疲劳免疫功能异常综合征(CFIDS)、慢性炎性脱髓鞘性周围神经病、Churg-Strauss综合征、疤痕性类天疱疮、CREST综合征、冷凝集素病、克罗恩氏病、盘状狼疮、原发性混合型冷球蛋白血症、纤维肌痛-纤维肌炎、肾小球肾炎、格雷夫斯病(Graves'disease)、格-巴二氏综合征(Guillain-Barre syndrome)、桥本甲状腺炎(Hashimoto'sthyroiditis)、特发性肺纤维化、特发性血小板减少性紫癜(ITP)、肠易激综合征(IBD)、IgA神经病、幼年型关节炎、扁平苔藓、红斑狼疮、美尼尔病(Meniere's disease)、混合型结缔组织病、多发性硬化、1型或免疫介导糖尿病、重症肌无力、寻常性天疱疮、恶性贫血、结节性多动脉炎、多毛症、多腺体综合征、风湿性多肌痛、多肌炎和皮肌炎、原发性低丙种球蛋白血症、原发性胆汁性肝硬化、牛皮癣、牛皮癣性关节炎、雷诺现象(Raynaud's phenomena)、莱特尔综合征(Reiter's syndrome)、类风湿关节炎、结节病、硬皮病、僵人综合征、系统性红斑狼疮、红斑狼疮、大动脉炎、颞动脉炎、巨细胞性动脉炎、溃疡性结肠炎、葡萄膜炎、白癜风和多发性肉芽肿病(Wegener's granulomatosis)。优选地,可通过本发明组合物治疗或预防的自身免疫性病症包括类风湿性关节炎、1型糖尿病、多发性硬化、系统性红斑狼疮和特应症。
在实施方案中,本方法涉及在退行性疾病或病症中的治疗用途。
退行性疾病或病症是受影响的组织或器官的功能或结构将随着时间逐渐恶化的疾病。可以用本发明治疗或预防的退行性疾病的实例包括肌萎缩侧索硬化症(ALS)、阿尔茨海默氏病、帕金森病、多系统萎缩、尼曼匹克病(Niemann Pick disease)、动脉粥样硬化、进行性核上性麻痹、泰萨克斯病(Tay-Sachs Disease)、糖尿病、心脏疾病、圆锥形角膜、炎症性肠病(IBD)、前列腺炎、骨关节炎、骨质疏松症、类风湿性关节炎、亨廷顿氏病、慢性创伤性脑病、癫痫、痴呆、肾衰竭、多发性硬化症、疟疾伴CNS变性、神经-AIDS、溶酶体贮积病、病毒性、细菌性或自身免疫源性脑膜炎。
在实施方案中,本方法涉及在肺部疾病或病症中的治疗用途。
在实施方案中,肺部疾病或病症是将从抑制肺中的免疫反应治疗上受益的肺部疾病或病症。在一些实施方案中,炎症与肺部疾病或病症相关。
在一些实施方案中,肺部疾病或病症选自石棉沉着病、哮喘、支气管扩张、支气管炎、慢性咳嗽、慢性阻塞性肺疾病(COPD)、普通感冒、哮吼、囊性纤维化、汉坦病毒、特发性肺纤维化、流感、肺癌、大流行性流感、百日咳、胸膜炎、肺炎、肺栓塞、肺性高血压、呼吸道合胞病毒(RSV)、结节病、睡眠呼吸暂停、肺活量测定、婴儿猝死综合征(SIDS)和结核病。
在一些实施方案中,肺部病或病症是慢性阻塞性肺疾病(COPD)、反应性气道疾病诸如哮喘、细支气管炎、急性肺损伤、肺同种异体移植物排斥(急性或慢性)、肺纤维化、间质性肺病或高敏性肺炎。在实施方案中,疾病或病症是急性肺损伤(ALI)。在实施方案中,ALI是可以通过吸入化学物质(化学物质诱发的急性肺损伤)或其他方式(例如感染)直接诱发或可以通过系统性损伤(例如感染)间接诱发的肺部病症。急性肺损伤包括呼吸窘迫综合征的亚类,包括婴儿呼吸窘迫综合征(IRDS)、透明膜病(HMD)、新生儿呼吸窘迫综合征(NRDS)、新生儿呼吸窘迫综合征(RDSN)、表面活性物质缺乏症(SDD)、急性呼吸窘迫综合征(ARDS)、全身炎症反应综合征(SIRS)引起的呼吸系统并发症或严重急性呼吸综合征(SARS)。
在实施方案中,本发明涉及本发明的MSC用于治疗与病毒感染相关的一种或多种症状的治疗用途。
在实施方案中,组合物适用于治疗感染性疾病,任选地选自病原体感染,所述病原体任选地选自细菌、病毒、真菌或寄生虫。
在实施方案中,病原体是病毒。在实施方案中,病毒是:(a)流感病毒,任选地选自A型、B型、C型和D型流感病毒,或(b)冠状病毒科的成员,任选地选自(i)β冠状病毒,其任选地选自严重急性呼吸综合征冠状病毒2(SARS-CoV-2)、SARS-CoV、中东呼吸综合征冠状病毒(MERS-CoV)、HCoV-HKU1和HCoV-OC43或(ii)α冠状病毒,任选地选自HCoV-NL63和HCoV-229E。
在实施方案中,病毒是SARS-CoV-2。在实施方案中,病毒是SARS-CoV-2,其已引起COVID-19。在实施方案中,COVID-19的特征在于发热、咳嗽、气短、腹泻、上呼吸道症状、下呼吸道症状、肺炎和呼吸窘迫中的一种或多种。
在一些实施方案中,组合物适用于治疗感染,其中所述感染是冠状病毒感染。在一些实施方案中,冠状病毒感染是严重急性呼吸综合征冠状病毒2(SARS-CoV-2)、SARS-CoV、中东呼吸综合征冠状病毒(MERS-CoV)、HCoV-HKU1、HCoV-OC43、HCoV-NL63和HCoV-229E中的一种或多种。在各种实施方案中,冠状病毒感染是SARS或COVID-19。在另一实施方案中,受试者被SARS-CoV-2感染。
在实施方案中,疗法在施用时预防或减轻患者急性呼吸窘迫综合征(ARDS)的发展。在实施方案中,疗法在施用时改善了患者的氧合。在实施方案中,疗法在施用时改善患者的全身血压氧合,例如减少或减轻休克,例如需要较少的加压支持。在实施方案中,疗法在施用时改善了患者的肺和/或肺泡渗透性。
在实施方案中,疗法在施用时预防或减轻患者从呼吸窘迫到细胞因子失衡的转变。在实施方案中,疗法在施用时逆转或预防患者体内的细胞因子风暴。在实施方案中,疗法在施用时逆转或预防患者的肺中或全身的细胞因子风暴。在实施方案中,细胞因子风暴选自全身炎症反应综合征、细胞因子释放综合征、巨噬细胞活化综合征和噬血细胞性淋巴组织细胞增多症中的一种或多种。
在实施方案中,疗法在施用时逆转或预防患者体内一种或多种炎性细胞因子的过度产生。在实施方案中,炎性细胞因子是IL-6、IL-1、IL-1受体拮抗剂(IL-1ra)、IL-2ra、IL-10、IL-18、TNFα、干扰素-γ、CXCL10、和CCL7。
在实施方案中,本发明涉及本发明的MSC用于治疗与冠状病毒感染相关的一种或多种症状的治疗用途。
冠状病毒(CoV)是冠状病毒科的成员,包括β冠状病毒和α冠状病毒,其为最近才知道会侵入人类的呼吸道病原体。冠状病毒科包括此类β冠状病毒,如严重急性呼吸综合征冠状病毒2(SARS-CoV-2)、SARS-CoV、中东呼吸综合征冠状病毒(MERS-CoV)、HCoV-HKU1和HCoV-OC43。α冠状病毒包括例如HCoV-NL63和HCoV-229E。在实施方案中,本发明涉及本发明的MSC用于治疗严重急性呼吸综合征冠状病毒2(SARS-CoV-2)、SARS-CoV、中东呼吸综合征冠状病毒(MERS-CoV)、HCoV-HKU1和HCoV-OC43中任一种感染的一种或多种症状的治疗用途。α冠状病毒包括例如HCoV-NL63和HCoV-229E。
不受理论的束缚,冠状病毒通过利用其“尖峰”表面糖蛋白侵入细胞,所述糖蛋白负责病毒识别血管紧张素转换酶2(ACE2),血管紧张素转换酶2(ACE2)是哺乳动物宿主上促进病毒进入宿主细胞的跨膜受体。(Zhou等人,A pneumonia outbreak associated with anew coronavirus of probable bat origin,Nature 2020)。
与冠状病毒感染相关的症状包括但不限于发热、疲倦、干咳、疼痛、气短和其他呼吸困难、腹泻、上呼吸道症状(例如打喷嚏、流鼻涕、鼻充血、咳嗽、喉咙痛)和/或肺炎。在实施方案中,本发明的组合物和方法可用于治疗或减轻任何这些症状。
在实施方案中,本发明涉及本发明的MSC在治疗SARS-CoV-2感染(包括由SARS-CoV-2(例如,2019-nCoV)引起的冠状病毒感染2019(COVID-19))的一种或多种症状中的治疗用途。
在某些情况下,包括患有冠状病毒感染的受试者,肺部病毒感染的发病率和死亡率可能与过度或压倒性的炎症反应有关。在不同的临床情况下,这种反应可被描述为“细胞因子反应综合征”、“细胞因子风暴”或“继发性噬血细胞性淋巴组织细胞增多症”(sHLH)。在实施方案中,本发明的组合物和方法可用于治疗或减轻任何这些过度的或压倒性的炎症反应。总的来说,据推测,这些高度促炎状态可导致因肺萎陷诸如急性呼吸窘迫综合征(ARDS)或影响器官诸如肝脏、肾脏、心脏和大脑的全身性多器官衰竭引发的死亡。在实施方案中,本发明的MSC治疗或减轻“细胞因子反应综合征”、“细胞因子风暴”或“继发性噬血细胞性淋巴组织细胞增多症”(sHLH)。
在实施方案中,COVID-19的特征部分在于白介素2(IL-2)、白介素7(IL-7)、粒细胞集落刺激因子(GCSF)、干扰素-γ诱导蛋白10、单核细胞趋化蛋白-1(MCP-1)、巨噬细胞炎症蛋白1-α(MIP1a)和肿瘤坏死因子-α(TNFa)的升高。在实施方案中,本发明的组合物和方法可用于治疗或减轻任何这些症状的增加。
在实施方案中,本发明的MSC预防COVID-19患者患上从呼吸窘迫发展为细胞因子风暴的疾病。
在实施方案中,本发明的MSC治疗或减轻ARDS。
在一些实施方案中,细胞因子风暴与COVID-19相关,并通过包括向有需要的受试者施用有效量的MSC的方法治疗或减轻,所述有效量的MSC对治疗冠状病毒感染和/或与冠状病毒感染有关的细胞因子风暴有效,其中受试者具有IL-6、IL-1、TNF、干扰素-γ、CXCL10、CCL7、IL-1受体拮抗剂(IL-1ra)、IL-2ra、IL-10、IL-18、CCL2/MCP-1、CCL5/RANTES、CCL7/MCP-3、MCP-2、肿瘤坏死因子-α(TNFa)、干扰素-γ(IFNg)、CXCL10、CXC3、粒细胞集落刺激因子(GCSF)、巨噬细胞炎症蛋白1α(MIP-1a)、IL-22和干扰素γ诱导蛋白10(IP-10)中的一种或多种的异常(例如增加或减少)表达或活性。
在一些实施方案中,受试者具有IL-6、IL-1、TNF、干扰素-γ、CXCL10、CCL7、IL-1受体拮抗剂(IL-1ra)、IL-2ra、IL-10、IL-18、CCL2/MCP-1、CCL5/RANTES、CCL7/MCP-3、MCP-2、肿瘤坏死因子-α(TNFa)、干扰素-γ(IFNg)、CXCL10、CXC3、粒细胞集落刺激因子(GCSF)、巨噬细胞炎症蛋白1α(MIP-1a)、IL-22和干扰素γ诱导蛋白10(IP-10)中的一种或多种的已调节的(例如减少或增加)表达或活性。
在一个方面,提供了治疗癌症的方法,所述方法包括:(a)获得间充质干细胞(MSC),所述MSC获得自重编程诱导多能干细胞(iPSC),所述重编程包括使所述iPSC与一种或多种编码重编程因子的合成RNA分子接触,并且所述MSC具有蛋白质分泌特征,所述蛋白质分泌特征包括一种或多种选自MIP-1α、SDF-1α、IL-27、LIF、IL-1β、IL-2、IL-5、IL-12p70、IL-13、IL-17A、IL-31、G-CSF/CSF-3、IFN-γ、TNF-α、HGF、MCP-1、IL-9、bNGF、MIP-3α、Gro-α/KC、IL-1α、IL-23、MMP-1、IL-18、M-CSF、IL-21、M-CSF、IL-21、CD40L、IL-22、VEGF-A、BLC、Tweak、ENA-78(LIX)、MCP-3、MIF和嗜酸性细胞活化趋化因子-3的蛋白质的分泌增加和/或一种或多种选自IL-6、IL-8和IL-4的蛋白质的分泌减少,其中所述分泌增加和/或减少是相对于骨髓来源的MSC而言的;和(b)施用有效量基本上具有用于有需要的患者的疗法的蛋白质分泌特征的所述MSC。
在实施方案中,MSC被进一步工程化改造以表达和/或分泌可溶性蛋白质。在实施方案中,可溶性蛋白质是TNF家族受体配体,任选地选自TRAIL/TNFSF10和TNFα。在实施方案中,可溶性蛋白是白介素,任选地选自IL-2、IL-6、IL-7、IL-12、IL-15、IL-18和IL-21,包括其在内或其嵌合蛋白(例如与甘氨酸/丝氨酸接头或自切割肽连接)。在实施方案中,可溶性蛋白质是Flt-3配体。
在实施方案中,癌症是基底细胞癌、胆管癌;膀胱癌;骨癌;大脑或中枢神经系统癌;乳腺癌;腹膜癌;宫颈癌;绒毛膜癌;结直肠癌;结缔组织癌;消化系统癌;子宫内膜癌;食道癌;眼癌;头颈部癌;胃癌(包括胃肠道癌);胶质母细胞瘤;肝癌;上皮内肿瘤;肾癌;喉癌;白血病;肝癌;肺癌(例如,小细胞肺癌、非小细胞肺癌、肺腺癌和肺鳞状癌);黑色素瘤;骨髓瘤;神经母细胞瘤;口腔(唇、舌、口和咽)癌;卵巢癌;胰腺癌;前列腺癌;视网膜母细胞瘤;横纹肌肉瘤;直肠癌;呼吸系统癌;唾液腺癌;肉瘤;皮肤癌;鳞状细胞癌;胃癌;睾丸癌;甲状腺癌;子宫或子宫内膜癌;泌尿系统癌;外阴癌;淋巴瘤(包括霍奇金淋巴瘤和非霍奇金淋巴瘤)以及B细胞淋巴瘤(包括低度恶性/滤泡性非霍奇金淋巴瘤(NHL));小淋巴细胞(SL)NHL;中级/滤泡性NHL;中级弥漫性NHL;高级免疫母细胞性NHL;高级淋巴母细胞NHL;高级小无核裂细胞NHL;大病NHL(bulky disease NHL);套细胞淋巴瘤;AIDS相关淋巴瘤;和Waldenstrom巨球蛋白血症;慢性淋巴细胞白血病(CLL);急性淋巴细胞白血病(ALL);多毛细胞白血病;慢性粒细胞白血病;以及其他癌和肉瘤;和移植后淋巴组织增殖性疾病(PTLD),以及与瘢痣病、水肿和梅格斯综合征(Meigs’syndrome)相关的异常血管增生中的一种或多种。
在实施方案中,iPSC来源于人。在实施方案中,iPSC来源于不打算接受疗法的受试者。在实施方案中,iPSC对于打算接受疗法的患者是同种异体的。在实施方案中,iPSC来自主细胞库。在实施方案中,MSC的特征在于炎症低或降低。在实施方案中,MSC的特征在于免疫原性低或降低。在实施方案中,MSC是自我更新的。在实施方案中,MSC是多能的。在实施方案中,MSC是免疫抑制的。在实施方案中,MSC适合体外扩增而不会显著丧失免疫抑制特性。在实施方案中,MSC基本上表达CD73、CD90和CD105中的一种或多种。在实施方案中,MSC基本上不表达CD14、CD34和CD45中的一种或多种。
在实施方案中,合成RNA分子是mRNA。在实施方案中,合成RNA分子是包含一种或多种非规范核苷酸的mRNA,所述核苷酸选自2-硫代尿苷、5-氮杂尿苷、假尿苷、4-硫尿苷、5-甲基尿苷、5-甲基假尿苷、5-氨基尿苷、5-氨基假尿苷、5-羟基尿苷、5-羟基假尿苷、5-甲氧基尿苷、5-甲氧基假尿苷、5-乙氧基尿苷、5-乙氧基假尿苷、5-羟甲基尿苷、5-羟甲基假尿苷、5-羧基尿苷、5-羧基假尿苷、5-甲酰基尿苷、5-甲酰基假尿苷、5-甲基-5-氮杂尿苷、5-氨基-5-氮杂尿苷、5-羟基-5-氮杂尿苷、5-甲基假尿苷、5-氨基假尿苷、5-羟基假尿苷、4-硫代-5-氮杂尿苷、4-硫代假尿苷、4-硫代-5-甲基尿苷、4-硫代-5-氨基尿苷、4-硫代-5-羟基尿苷、4-硫代-5-甲基-5-氮杂尿苷、4-硫代-5-氨基-5-氮杂尿苷、4-硫代-5-羟基-5-氮杂尿苷、4-硫代-5-甲基假尿苷、4-硫代-5-氨基假尿苷、4-硫代-5-羟基假尿苷、2-硫代胞苷、5-氮杂胞苷、假异胞苷、N4-甲基胞苷、N4-氨基胞苷、N4-羟基胞苷、5-甲基胞苷、5-氨基胞苷、5-羟基胞苷、5-甲氧基胞苷、5-乙氧基胞苷、5-羟甲基胞苷、5-羧基胞苷、5-甲酰基胞苷、5-甲基-5-氮杂胞苷、5-氨基-5-氮杂胞苷、5-羟基-5-氮杂胞苷、5-甲基假异胞苷、5-氨基假异胞苷、5-羟基假异胞苷、N4-甲基-5-氮杂胞苷、N4-甲基假异胞苷、2-硫代-5-氮杂胞苷、2-硫代假异胞苷、2-硫代-N4-甲基胞苷、2-硫代-N4-氨基胞苷、2-硫代-N4-羟基胞苷、2-硫代-5-甲基胞苷、2-硫代-5-氨基胞苷、2-硫代-5-羟基胞苷、2-硫代-5-甲基-5-氮杂胞苷、2-硫代-5-氨基-5-氮杂胞苷、2-硫代-5-羟基-5-氮杂胞苷、2-硫代-5-甲基假异胞苷、2-硫代-5-氨基假异胞苷、2-硫代-5-羟基假异胞苷、2-硫代-N4-甲基-5-氮杂胞苷、2-硫代-N4-甲基假异胞苷、N4-甲基-5-甲基胞苷、N4-甲基-5-氨基胞苷、N4-甲基-5-羟基胞苷、N4-甲基-5-甲基-5-氮杂胞苷、N4-甲基-5-氨基-5-氮杂胞苷、N4-甲基-5-羟基-5-氮杂胞苷、N4-甲基-5-甲基假异胞苷、N4-甲基-5-氨基假异胞苷、N4-甲基-5-羟基假异胞苷、N4-氨基-5-氮杂胞苷、N4-氨基假异胞苷、N4-氨基-5-甲基胞苷、N4-氨基-5-氨基胞苷、N4-氨基-5-羟基胞苷、N4-氨基-5-甲基-5-氮杂胞苷、N4-氨基-5-氨基-5-氮杂胞苷、N4-氨基-5-羟基-5-氮杂胞苷、N4-氨基-5-甲基假异胞苷、N4-氨基-5-氨基假异胞苷、N4-氨基-5-羟基假异胞苷、N4-羟基-5-氮杂胞苷、N4-羟基假异胞苷、N4-羟基-5-甲基胞苷、N4-羟基-5-氨基胞苷、N4-羟基-5-羟基胞苷、N4-羟基-5-甲基-5-氮杂胞苷、N4-羟基-5-氨基-5-氮杂胞苷、N4-羟基-5-羟基-5-氮杂胞苷、N4-羟基-5-甲基假异胞苷、N4-羟基-5-氨基假异胞苷、N4-羟基-5-羟基假异胞苷、2-硫代-N4-甲基-5-甲基胞苷、2-硫代-N4-甲基-5-氨基胞苷、2-硫代-N4-甲基-5-羟基胞苷、2-硫代-N4-甲基-5-甲基-5-氮杂胞苷、2-硫代-N4-甲基-5-氨基-5-氮杂胞苷、2-硫代-N4-甲基-5-羟基-5-氮杂胞苷、2-硫代-N4-甲基-5-甲基假异胞苷、2-硫代-N4-甲基-5-氨基假异胞苷、2-硫代-N4-甲基-5-羟基假异胞苷、2-硫代-N4-氨基-5-氮杂胞苷、2-硫代-N4-氨基假异胞苷、2-硫代-N4-氨基-5-甲基胞苷、2-硫代-N4-氨基-5-氨基胞苷、2-硫代-N4-氨基-5-羟基胞苷、2-硫代-N4-氨基-5-甲基-5-氮杂胞苷、2-硫代-N4-氨基-5-氨基-5-氮杂胞苷、2-硫代-N4-氨基-5-羟基-5-氮杂胞苷、2-硫代-N4-氨基-5-甲基假异胞苷、2-硫代-N4-氨基-5-氨基假异胞苷、2-硫代-N4-氨基-5-羟基假异胞苷、2-硫代-N4-羟基-5-氮杂胞苷、2-硫代-N4-羟基假异胞苷、2-硫代-N4-羟基-5-甲基胞苷、N4-羟基-5-氨基胞苷、2-硫代-N4-羟基-5-羟基胞苷、2-硫代-N4-羟基-5-甲基-5-氮杂胞苷、2-硫代-N4-羟基-5-氨基-5-氮杂胞苷、2-硫代-N4-羟基-5-羟基-5-氮杂胞苷、2-硫代-N4-羟基-5-甲基假异胞苷、2-硫代-N4-羟基-5-氨基假异胞苷、2-硫代-N4-羟基-5-羟基假异胞苷、N6-甲基腺苷、N6-氨基腺苷、N6-羟基腺苷、7-脱氮腺苷、8-氮杂腺苷、N6-甲基-7-脱氮腺苷、N6-甲基-8-氮杂腺苷、7-脱氮-8-氮杂腺苷、N6-甲基-7-脱氮-8-氮杂腺苷、N6-氨基-7-脱氮腺苷、N6-氨基-8-氮杂腺苷、N6-氨基-7-脱氮-8-氮杂腺苷、N6-羟基腺苷、N6-羟基-7-脱氮腺苷、N6-羟基-8-氮杂腺苷、N6-羟基-7-脱氮-8-氮杂腺苷、6-硫代鸟苷、7-脱氮鸟苷、8-氮杂鸟苷、6-硫代-7-脱氮鸟苷、6-硫代-8-氮杂鸟苷、7-脱氮-8-氮杂鸟苷和6-硫代-7-脱氮-8-氮杂鸟苷。在实施方案中,合成RNA分子是体外转录的。
在实施方案中,重编程是非病毒的。在实施方案中,重编程因子是Oct4、Sox2、Klf4、c-Myc、l-Myc、Tert、Nanog和Lin28中的一种或多种。
治疗性治疗包括使用一种或多种施用途径和一种或多种制剂,这些制剂被设计成以有效剂量实现治疗效果,同时使对被施用治疗的受试者的毒性最小化。
在各种实施方案中,有效剂量是基本上避免体内细胞毒性的量。在各种实施方案中,有效剂量是基本上避免人类受试者中的免疫反应的量。例如,免疫反应可以是由先天免疫系统介导的免疫反应。可以使用本领域已知的标志物(例如细胞因子、干扰素、TLR)来监测免疫反应。在一些实施方案中,有效剂量消除了以用于缓和残留毒性的免疫抑制剂(例如B18R)治疗人类受试者的需要。
当配制时,以与剂量制剂相容的方式且以治疗有效量施用溶液,如本文所述。制剂可以诸如可注射溶液等的多种剂型方便地施用。例如,对于在水溶液中的肠胃外施用,溶液通常被适当地缓冲并且液体稀释剂首先与例如足够的盐水或葡萄糖等渗。此类水溶液可用于例如静脉内、肌肉内、皮下和腹膜内施用。优选地,使用本领域技术人员已知的无菌水性介质。
药物制剂可以另外包含递送试剂(又称“转染试剂”、又称“载体”、又称“递送载体”)和/或赋形剂。药学上可接受的递送试剂、赋形剂及其制备和使用方法,包括制备药物制剂和将药物制剂施用于患者(又称“受试者”)的方法是本领域众所周知的,并且在许多出版物中阐述,包括,例如,在美国专利申请公开号US 2008/0213377中,其全部内容以引用的方式并入本文。
例如,本发明的组合物可以是药学上可接受的盐的形式。此类盐包括在例如J.Pharma.Sci.66,2-19(1977)和The Handbook of Pharmaceutical Salts;Properties,Selection,and Use.PH Stahl和CG Wermuth(eds.),Verlag,Zurich(Switzerland)2002中列出的那些,其整体以引用的方式并入本文。药学上可接受的盐的非限制性实例包括:硫酸盐、柠檬酸盐、乙酸盐、草酸盐、氯化物、溴化物、碘化物、硝酸盐、硫酸氢盐、磷酸盐、酸性磷酸盐、异烟酸盐、乳酸盐、水杨酸盐、柠檬酸盐、酒石酸盐、油酸盐、鞣酸盐、泛酸盐、酒石酸氢盐、抗坏血酸盐、琥珀酸盐、马来酸盐、龙胆酸盐、富马酸盐、葡萄糖酸盐、葡萄糖醛酸盐、糖酸盐、甲酸盐、苯甲酸盐、谷氨酸盐、甲磺酸盐、乙磺酸盐、苯磺酸盐、对甲苯磺酸盐、樟脑磺酸盐、双羟萘酸盐、苯乙酸盐、三氟乙酸盐、丙烯酸盐、氯苯甲酸盐、二硝基苯甲酸盐、羟基苯甲酸盐、甲氧基苯甲酸盐、甲基苯甲酸盐、邻乙酰氧基苯甲酸盐、萘-2-苯甲酸盐、异丁酸盐、苯丁酸盐、α-羟基丁酸盐、丁炔-1,4-二羧酸盐、己炔-1,4-二羧酸盐、癸酸盐、辛酸盐、肉桂酸盐、乙醇酸盐、庚酸盐、马尿酸盐、苹果酸盐、羟基马来酸盐、丙二酸盐、扁桃酸盐、甲磺酸盐、烟酸盐、邻苯二甲酸盐、对苯二甲酸盐、丙炔酸盐、丙酸盐、苯丙酸盐、癸二酸盐、辛二酸盐、对溴烯磺酸盐、氯苯磺酸盐、乙基磺酸盐、2-羟乙基磺酸盐、甲基磺酸盐、萘-1-磺酸盐、萘-2-磺酸盐、萘-1,5-磺酸盐、二甲苯磺酸盐、酒石酸盐、碱金属(诸如钠、钾和锂)的氢氧化物;碱土金属(诸如钙和镁)的氢氧化物;其他金属(诸如铝和锌)的氢氧化物;氨和有机胺,诸如未取代或羟基取代的单-、二-或三-烷基胺、二环己胺;三丁胺;吡啶;N-甲胺、N-乙胺;二乙胺;三乙胺;单-、双-或三-(2-OH-低级烷基胺),诸如单-、双-或三-(2-羟乙基)胺、2-羟基-叔丁胺或三-(羟甲基)甲胺、N、N-二-低级烷基-N-(羟基-低级烷基)-胺,诸如作为N,N-二甲基-N-(2-羟乙基)胺或三-(2-羟乙基)胺;N-甲基-D-葡糖胺;以及氨基酸,诸如精氨酸、赖氨酸等。
本发明的药物组合物可以包含赋形剂,包括液体诸如水和油,包括石油、动物、植物或合成来源的那些,诸如花生油、大豆油、矿物油、芝麻油等。药物赋形剂可以是例如盐水、阿拉伯树胶、明胶、淀粉糊、滑石、角蛋白、胶态二氧化硅、尿素等。另外,可使用辅助剂、稳定剂、增稠剂、润滑剂和着色剂。在一个实施方案中,药学上可接受的赋形剂在施用于受试者时是无菌的。合适的药用赋形剂还包括淀粉、葡萄糖、乳糖、蔗糖、明胶、麦芽、米、面粉、白垩、硅胶、硬脂酸钠、单硬脂酸甘油酯、滑石、氯化钠、脱脂奶粉、丙三醇、丙烯、乙二醇、水、乙醇等。如果需要,本文所述的任何剂也可包含少量润湿剂或乳化剂,或pH缓冲剂。
在实施方案中,组合物被配制用于鞘内、病灶内、冠状动脉内、静脉内(IV)、关节内、肌肉内和支气管内施用和通过胰内血管内注射、髓核内、腰椎穿刺、心肌内、经心内膜、瘘管内、髓间间隙、硬膜内间隙和腿部注射施用中的一种或多种。
在实施方案中,组合物被配制用于输注。在一些实施方案中,组合物被配制用于输注,其中组合物通过外周线、中心线、隧道线、植入式端口和/或导管通过受试者或患者静脉中的针递送至受试者或患者的血流中。在一些实施方案中,受试者或患者还可以通过输注接受支持性药物或治疗,诸如水合作用。在一些实施方案中,组合物被配制用于静脉内输注。在一些实施方案中,输注是连续输注、二次静脉内疗法(IV)和/或IV推注。在一些实施方案中,组合物的输注可以通过使用选自输注泵、皮下注射针头、滴注室、外周插管和压力袋中的一种或多种的设备来施用。
在一些实施方案中,组合物被配制用于吸入。在一些实施方案中,吸入包括将组合物直接吸入肺中。在一些实施方案中,组合物的吸入可以通过使用一种或多种计量吸入器、干粉吸入器、喷雾器和软雾吸入器来施用。
定义
“合成RNA分子”是指在细胞外产生的RNA分子或使用生物工程在细胞内产生的RNA分子,非限制性实例为在体外转录反应中产生的RNA分子、通过直接化学合成产生的RNA分子或在基因工程化大肠杆菌(E.coli)细胞中产生的RNA分子。
“培养基”是指溶剂或包含溶剂和溶质的溶液,非限制性实例为Dulbecco改良Eagle培养基(DMEM)、DMEM+10%胎牛血清(FBS)、盐水或水。
“转染培养基”是指可用于转染的培养基,非限制性实例为Dulbecco改良Eagle培养基(DMEM)、DMEM/F12、盐水或水。
“Oct4蛋白”是指由POU5F1基因编码的蛋白,或其天然或工程化变体、家族成员、直系同源物、片段或融合构建体,非限制性实例为人Oct4蛋白(SEQ ID NO:1)、小鼠Oct4蛋白、Oct1蛋白,由POU5F1假基因2编码的蛋白、Oct4蛋白的DNA结合结构域或Oct4-GFP融合蛋白。在一些实施方案中,Oct4蛋白包含与SEQ ID NO:1具有至少70%同一性,或在其他实施方案中,与SEQ ID NO:1具有至少75%、80%、85%、90%或95%同一性的氨基酸序列。在一些实施方案中,Oct4蛋白包含相对于SEQ ID NO:1具有1至20个氨基酸插入、缺失或取代(共同地)的氨基酸序列。或在其他实施方案中,Oct4蛋白包含相对于SEQ ID NO:1具有1至15个或1至10个氨基酸插入、缺失或取代(共同地)的氨基酸序列。
SEQ ID NO:1是:
Met Ala Gly His Leu Ala Ser Asp Phe Ala Phe Ser Pro Pro Pro Gly GlyGly Gly Asp Gly Pro Gly Gly Pro Glu Pro Gly Trp Val Asp Pro Arg Thr Trp LeuSer Phe Gln Gly Pro Pro Gly Gly Pro Gly Ile Gly Pro Gly Val Gly Pro Gly SerGlu Val Trp Gly Ile Pro Pro Cys Pro Pro Pro Tyr Glu Phe Cys Gly Gly Met AlaTyr Cys Gly Pro Gln Val Gly Val Gly Leu Val Pro Gln Gly Gly Leu Glu Thr SerGln Pro Glu Gly Glu Ala Gly Val Gly Val Glu Ser Asn Ser Asp Gly Ala Ser ProGlu Pro Cys Thr Val Thr Pro Gly Ala Val Lys Leu Glu Lys Glu Lys Leu Glu GlnAsn Pro Glu Glu Ser Gln Asp Ile Lys Ala Leu Gln Lys Glu Leu Glu Gln Phe AlaLys Leu Leu Lys Gln Lys Arg Ile Thr Leu Gly Tyr Thr Gln Ala Asp Val Gly LeuThr Leu Gly Val Leu Phe Gly Lys Val Phe Ser Gln Thr Thr Ile Cys Arg Phe GluAla Leu Gln Leu Ser Phe Lys Asn Met Cys Lys Leu Arg Pro Leu Leu Gln Lys TrpVal Glu Glu Ala Asp Asn Asn Glu Asn Leu Gln Glu Ile Cys Lys Ala Glu Thr LeuVal Gln Ala Arg Lys Arg Lys Arg Thr Ser Ile Glu Asn Arg Val Arg Gly Asn LeuGlu Asn Leu Phe Leu Gln Cys Pro Lys Pro Thr Leu Gln Gln Ile Ser His Ile AlaGln Gln Leu Gly Leu Glu Lys Asp Val Val Arg Val Trp Phe Cys Asn Arg Arg GlnLys Gly Lys Arg Ser Ser Ser Asp Tyr Ala Gln Arg Glu Asp Phe Glu Ala Ala GlySer Pro Phe Ser Gly Gly Pro Val Ser Phe Pro Leu Ala Pro Gly Pro His Phe GlyThr Pro Gly Tyr Gly Ser Pro His Phe Thr Ala Leu Tyr Ser Ser Val Pro Phe ProGlu Gly Glu Ala Phe Pro Pro Val Ser Val Thr Thr Leu Gly Ser Pro Met His SerAsn
“Sox2蛋白”是指由SOX2基因编码的蛋白,或其天然或工程化变体、家族成员、直系同源物、片段或融合构建体,非限制性实例为人Sox2蛋白(SEQ ID NO:2)、小鼠Sox2蛋白、Sox2蛋白的DNA结合结构域或Sox2-GFP融合蛋白。在一些实施方案中,Sox2蛋白包含与SEQID NO:2具有至少70%同一性,或在其他实施方案中,与SEQ ID NO:2具有至少75%、80%、85%、90%或95%同一性的氨基酸序列。在一些实施方案中,Sox2蛋白包含相对于SEQ IDNO:2具有1至20个氨基酸插入、缺失或取代(共同地)的氨基酸序列。或在其他实施方案中,Sox2蛋白包含相对于SEQ ID NO:2具有1至15个或1至10个氨基酸插入、缺失或取代(共同地)的氨基酸序列。
SEQ ID NO:2是:
Met Tyr Asn Met Met Glu Thr Glu Leu Lys Pro Pro Gly Pro Gln Gln ThrSer Gly Gly Gly Gly Gly Asn Ser Thr Ala Ala Ala Ala Gly Gly Asn Gln Lys AsnSer Pro Asp Arg Val Lys Arg Pro Met Asn Ala Phe Met Val Trp Ser Arg Gly GlnArg Arg Lys Met Ala Gln Glu Asn Pro Lys Met His Asn Ser Glu Ile Ser Lys ArgLeu Gly Ala Glu Trp Lys Leu Leu Ser Glu Thr Glu Lys Arg Pro Phe Ile Asp GluAla Lys Arg Leu Arg Ala Leu His Met Lys Glu His Pro Asp Tyr Lys Tyr Arg ProArg Arg Lys Thr Lys Thr Leu Met Lys Lys Asp Lys Tyr Thr Leu Pro Gly Gly LeuLeu Ala Pro Gly Gly Asn Ser Met Ala Ser Gly Val Gly Val Gly Ala Gly Leu GlyAla Gly Val Asn Gln Arg Met Asp Ser Tyr Ala His Met Asn Gly Trp Ser Asn GlySer Tyr Ser Met Met Gln Asp Gln Leu Gly Tyr Pro Gln His Pro Gly Leu Asn AlaHis Gly Ala Ala Gln Met Gln Pro Met His Arg Tyr Asp Val Ser Ala Leu Gln TyrAsn Ser Met Thr Ser Ser Gln Thr Tyr Met Asn Gly Ser Pro Thr Tyr Ser Met SerTyr Ser Gln Gln Gly Thr Pro Gly Met Ala Leu Gly Ser Met Gly Ser Val Val LysSer Glu Ala Ser Ser Ser Pro Pro Val Val Thr Ser Ser Ser His Ser Arg Ala ProCys Gln Ala Gly Asp Leu Arg Asp Met Ile Ser Met Tyr Leu Pro Gly Ala Glu ValPro Glu Pro Ala Ala Pro Ser Arg Leu His Met Ser Gln His Tyr Gln Ser Gly ProVal Pro Gly Thr Ala Ile Asn Gly Thr Leu Pro Leu Ser His Met
“Klf4蛋白”是指由KLF4基因编码的蛋白,或其天然或工程化变体、家族成员、直系同源物、片段或融合构建体,非限制性实例为人Klf4蛋白(SEQ ID NO:3)、小鼠Klf4蛋白、Klf4蛋白的DNA结合结构域或Klf4-GFP融合蛋白。在一些实施方案中,Klf4蛋白包含与SEQID NO:3具有至少70%同一性,或在其他实施方案中,与SEQ ID NO:13具有至少75%、80%、85%、90%或95%同一性的氨基酸序列。在一些实施方案中,Klf4蛋白包含相对于SEQ IDNO:3具有1至20个氨基酸插入、缺失或取代(共同地)的氨基酸序列。或在其他实施方案中,Klf4蛋白包含相对于SEQ ID NO:3具有1至15个或1至10个氨基酸插入、缺失或取代(共同地)的氨基酸序列。
SEQ ID NO:3是:
Met Arg Gln Pro Pro Gly Glu Ser Asp Met Ala Val Ser Asp Ala Leu LeuPro Ser Phe Ser Thr Phe Ala Ser Gly Pro Ala Gly Arg Glu Lys Thr Leu Arg GlnAla Gly Ala Pro Asn Asn Arg Trp Arg Glu Glu Leu Ser His Met Lys Arg Leu ProPro Val Leu Pro Gly Arg Pro Tyr Asp Leu Ala Ala Ala Thr Val Ala Thr Asp LeuGlu Ser Gly Gly Ala Gly Ala Ala Cys Gly Gly Ser Asn Leu Ala Pro Leu Pro ArgArg Glu Thr Glu Glu Phe Asn Asp Leu Leu Asp Leu Asp Phe Ile Leu Ser Asn SerLeu Thr His Pro Pro Glu Ser Val Ala Ala Thr Val Ser Ser Ser Ala Ser Ala SerSer Ser Ser Ser Pro Ser Ser Ser Gly Pro Ala Ser Ala Pro Ser Thr Cys Ser PheThr Tyr Pro Ile Arg Ala Gly Asn Asp Pro Gly Val Ala Pro Gly Gly Thr Gly GlyGly Leu Leu Tyr Gly Arg Glu Ser Ala Pro Pro Pro Thr Ala Pro Phe Asn Leu AlaAsp Ile Asn Asp Val Ser Pro Ser Gly Gly Phe Val Ala Glu Leu Leu Arg Pro GluLeu Asp Pro Val Tyr Ile Pro Pro Gln Gln Pro Gln Pro Pro Gly Gly Gly Leu MetGly Lys Phe Val Leu Lys Ala Ser Leu Ser Ala Pro Gly Ser Glu Tyr Gly Ser ProSer Val Ile Ser Val Ser Lys Gly Ser Pro Asp Gly Ser His Pro Val Val Val AlaPro Tyr Asn Gly Gly Pro Pro Arg Thr Cys Pro Lys Ile Lys Gln Glu Ala Val SerSer Cys Thr His Leu Gly Ala Gly Pro Pro Leu Ser Asn Gly His Arg Pro Ala AlaHis Asp Phe Pro Leu Gly Arg Gln Leu Pro Ser Arg Thr Thr Pro Thr Leu Gly LeuGlu Glu Val Leu Ser Ser Arg Asp Cys His Pro Ala Leu Pro Leu Pro Pro Gly PheHis Pro His Pro Gly Pro Asn Tyr Pro Ser Phe Leu Pro Asp Gln Met Gln Pro GlnVal Pro Pro Leu His Tyr Gln Glu Leu Met Pro Pro Gly Ser Cys Met Pro Glu GluPro Lys Pro Lys Arg Gly Arg Arg Ser Trp Pro Arg Lys Arg Thr Ala Thr His ThrCys Asp Tyr Ala Gly Cys Gly Lys Thr Tyr Thr Lys Ser Ser His Leu Lys Ala HisLeu Arg Thr His Thr Gly Glu Lys Pro Tyr His Cys Asp Trp Asp Gly Cys Gly TrpLys Phe Ala Arg Ser Asp Glu Leu Thr Arg His Tyr Arg Lys His Thr Gly His ArgPro Phe Gln Cys Gln Lys Cys Asp Arg Ala Phe Ser Arg Ser Asp His Leu Ala LeuHis Met Lys Arg His Phe
“c-Myc蛋白”是指由MYC基因编码的蛋白,或其天然或工程化变体、家族成员、直系同源物、片段或融合构建体,非限制性实例为人c-Myc蛋白(SEQ ID NO:4)、小鼠c-Myc蛋白、l-Myc蛋白、c-Myc(T58A)蛋白、c-Myc蛋白的DNA结合结构域或c-Myc-GFP融合蛋白。在一些实施方案中,c-Myc蛋白包含与SEQ ID NO:4具有至少70%同一性,或在其他实施方案中,与SEQ ID NO:4具有至少75%、80%、85%、90%或95%同一性的氨基酸序列。在一些实施方案中,c-Myc蛋白包含相对于SEQ ID NO:4具有1至20个氨基酸插入、缺失或取代(共同地)的氨基酸序列。或在其他实施方案中,c-Myc蛋白包含相对于SEQ ID NO:4具有1至15个或1至10个氨基酸插入、缺失或取代(共同地)的氨基酸序列。
SEQ ID NO:4是:
Met Asp Phe Phe Arg Val Val Glu Asn Gln Gln Pro Pro Ala Thr Met ProLeu Asn Val Ser Phe Thr Asn Arg Asn Tyr Asp Leu Asp Tyr Asp Ser Val Gln ProTyr Phe Tyr Cys Asp Glu Glu Glu Asn Phe Tyr Gln Gln Gln Gln Gln Ser Glu LeuGln Pro Pro Ala Pro Ser Glu Asp Ile Trp Lys Lys Phe Glu Leu Leu Pro Thr ProPro Leu Ser Pro Ser Arg Arg Ser Gly Leu Cys Ser Pro Ser Tyr Val Ala Val ThrPro Phe Ser Leu Arg Gly Asp Asn Asp Gly Gly Gly Gly Ser Phe Ser Thr Ala AspGln Leu Glu Met Val Thr Glu Leu Leu Gly Gly Asp Met Val Asn Gln Ser Phe IleCys Asp Pro Asp Asp Glu Thr Phe Ile Lys Asn Ile Ile Ile Gln Asp Cys Met TrpSer Gly Phe Ser Ala Ala Ala Lys Leu Val Ser Glu Lys Leu Ala Ser Tyr Gln AlaAla Arg Lys Asp Ser Gly Ser Pro Asn Pro Ala Arg Gly His Ser Val Cys Ser ThrSer Ser Leu Tyr Leu Gln Asp Leu Ser Ala Ala Ala Ser Glu Cys Ile Asp Pro SerVal Val Phe Pro Tyr Pro Leu Asn Asp Ser Ser Ser Pro Lys Ser Cys Ala Ser GlnAsp Ser Ser Ala Phe Ser Pro Ser Ser Asp Ser Leu Leu Ser Ser Thr Glu Ser SerPro Gln Gly Ser Pro Glu Pro Leu Val Leu His Glu Glu Thr Pro Pro Thr Thr SerSer Asp Ser Glu Glu Glu Gln Glu Asp Glu Glu Glu Ile Asp Val Val Ser Val GluLys Arg Gln Ala Pro Gly Lys Arg Ser Glu Ser Gly Ser Pro Ser Ala Gly Gly HisSer Lys Pro Pro His Ser Pro Leu Val Leu Lys Arg Cys His Val Ser Thr His GlnHis Asn Tyr Ala Ala Pro Pro Ser Thr Arg Lys Asp Tyr Pro Ala Ala Lys Arg ValLys Leu Asp Ser Val Arg Val Leu Arg Gln Ile Ser Asn Asn Arg Lys Cys Thr SerPro Arg Ser Ser Asp Thr Glu Glu Asn Val Lys Arg Arg Thr His Asn Val Leu GluArg Gln Arg Arg Asn Glu Leu Lys Arg Ser Phe Phe Ala Leu Arg Asp Gln Ile ProGlu Leu Glu Asn Asn Glu Lys Ala Pro Lys Val Val Ile Leu Lys Lys Ala Thr AlaTyr Ile Leu Ser Val Gln Ala Glu Glu Gln Lys Leu Ile Ser Glu Glu Asp Leu LeuArg Lys Arg Arg Glu Gln Leu Lys His Lys Leu Glu Gln Leu Arg Asn Ser Cys Ala
通过以下非限制性实施例进一步说明本发明。
序列
在实施方案中,例如涉及进一步工程化改造MSC以表达和/或分泌可溶性蛋白质的实施方案中,将MSC细胞用以下序列或与以下序列具有约95%,或至少约97%,或至少约98%的同一性的序列中的一种或多种或其密码子优化版本转导或电穿孔。
>TRAIL
ATGGCCATGATGGAAGTGCAGGGTGGGCCCTCCCTCGGGCAGACGTGCGTGCTCATAGTCATTTTCACCGTGCTCCTCCAGAGCCTGTGCGTCGCCGTCACGTACGTGTACTTCACCAACGAGCTGAAGCAGATGCAGGACAAGTACAGCAAGTCGGGGATCGCCTGCTTCCTGAAGGAGGACGACTCCTACTGGGACCCGAACGACGAGGAGTCCATGAACTCCCCGTGCTGGCAGGTCAAGTGGCAGCTGCGGCAGCTGGTCCGCAAGATGATCCTCCGGACCAGCGAGGAGACTATCAGCACCGTCCAGGAGAAGCAGCAGAACATCTCCCCGCTCGTCCGGGAGCGAGGTCCCCAGCGGGTAGCGGCTCATATCACCGGCACCCGCGGGAGGTCGAACACGCTCAGCTCGCCGAACTCCAAGAACGAGAAGGCCCTCGGCCGCAAGATCAACTCCTGGGAGAGCTCGCGGAGCGGGCACTCGTTCCTGTCGAACCTGCATCTGCGGAACGGCGAGCTCGTGATCCACGAGAAGGGCTTCTACTACATCTACAGCCAGACCTACTTCCGGTTCCAGGAGGAGATCAAGGAGAACACCAAGAACGACAAGCAGATGGTGCAGTACATCTACAAGTACACCAGCTACCCCGACCCGATCCTCCTGATGAAGTCCGCCCGCAACAGCTGCTGGAGCAAGGACGCGGAGTACGGCCTGTACAGCATCTACCAGGGCGGCATCTTCGAGCTCAAGGAGAACGACCGCATCTTCGTGAGCGTGACGAACGAGCACCTGATCGACATGGACCACGAGGCCTCCTTCTTCGGGGCGTTCCTGGTCGGTTGA(SEQ ID NO:5)
>FLT3LG
ATGACAGTGCTGGCGCCCGCCTGGTCCCCCACAACCTACCTCCTCCTGCTGCTGTTGCTGTCGTCGGGCCTGAGCGGGACGCAGGACTGCTCGTTCCAGCACAGCCCGATCTCCTCCGACTTCGCGGTCAAGATCCGGGAGCTGAGCGACTACCTGTTGCAGGACTACCCCGTCACCGTCGCCTCCAACCTGCAGGACGAGGAGCTCTGCGGTGGCTTGTGGCGTCTGGTGTTGGCTCAGCGCTGGATGGAGCGGCTCAAGACGGTCGCGGGGTCCAAGATGCAGGGCCTGCTCGAGCGCGTGAACACGGAGATCCACTTCGTCACCAAGTGCGCCTTCCAGCCGCCACCCAGCTGCCTGCGGTTCGTCCAGACCAACATCTCCCGCCTCCTGCAGGAGACATCCGAGCAGCTGGTGGCGCTGAAGCCCTGGATCACGCGCCAGAACTTCTCCCGATGCCTGGAGCTGCAGTGCCAGCCTGACTCCTCAACCCTGCCACCTCCATGGAGTCCCCGGCCTTTGGAGGCCACCGCGCCCACTGCTCCGCAGCCCCCACTCCTCTTGCTACTCCTGCTCCCCGTAGGCCTTCTACTGCTGGCCGCAGCCTGGTGCCTACATTGGCAAAGAACGCGGCGACGTACACCCCGCCCTGGGGAGCAGGTGCCCCCAGTCCCCAGTCCCCAGGACCTGCTGCTTGTGGAGCACTGA(SEQ ID NO:6)
>IL7-(G4S)2-IL15
ATGTTCCACGTGTCGTTCCGGTACATCTTCGGCCTCCCGCCGCTCATCCTGGTCCTGCTCCCCGTGGCGTCCTCGGACTGCGACATCGAGGGCAAGGACGGGAAGCAGTACGAGTCGGTGCTGATGGTGTCCATCGACCAGCTGCTCGACTCCATGAAGGAGATCGGGTCGAACTGCCTCAACAACGAGTTCAACTTCTTCAAGCGCCACATCTGCGACGCGAACAAGGAGGGGATGTTCCTCTTCCGGGCGGCCCGCAAGCTCCGGCAGTTCCTCAAGATGAACAGCACGGGGGACTTCGACCTGCACCTGCTGAAGGTGTCGGAGGGCACCACCATCCTCCTCAACTGCACCGGCCAGGTCAAGGGCCGGAAGCCCGCCGCCCTGGGCGAGGCGCAGCCCACGAAGTCCCTCGAGGAGAACAAGTCCCTCAAGGAGCAGAAGAAGCTCAACGACCTGTGCTTCCTCAAGCGGCTCCTCCAGGAGATCAAGACCTGCTGGAACAAGATCCTCATGGGCACCAAGGAGCACGGGGGCGGCGGGAGCGGCGGGGGTGGCTCCAACTGGGTGAACGTCATCTCGGACCTCAAGAAGATCGAGGACCTGATCCAGAGCATGCACATCGACGCCACGCTCTACACCGAGTCGGACGTCCACCCGTCGTGCAAGGTCACCGCCATGAAGTGCTTCCTCCTGGAGCTGCAGGTCATCTCGCTGGAGTCCGGCGACGCCAGCATCCACGACACGGTCGAGAACCTCATCATCCTCGCGAACAACTCCCTCAGCTCGAACGGCAACGTGACGGAGAGCGGGTGCAAGGAGTGCGAGGAGCTGGAGGAGAAGAACATCAAGGAGTTCCTGCAGAGCTTCGTGCACATCGTGCAGATGTTCATCAACACCAGCTGA(SEQ ID NO:7)。
实施例
获得诱导多能干细胞(iPSC)并通过用非免疫原性信使RNA(mRNA)在确定的、无动物成分的过程中编码一种或多种重编程因子的细胞重编程生成MSC。
iPSC是使用基于mRNA的高效、无免疫抑制剂的方案由成人皮肤成纤维细胞生成的。然后使用21天高产单层方案将iPSC分化为MSC。rtPCR分析显示分化的MSC中Nanog和Oct4的下调以及CD73和CD105的上调。通过分化成脂肪细胞、成骨细胞和软骨细胞来证实多能性,并如通过末端限制性片段的Southern分析所测量的,iPSC MSC具有大约13kb长的端粒,而骨髓来源的MSC(BM MSC)的端粒长7kb。在连续传代时,iPSC MSC在衰老前经历>70次群体倍增,而BM MSC的群体倍增<20次。参见图1。
对实施例1的MSC的基因和分泌蛋白特征进行了表征。
图2显示了基于基因表达的细胞特征。供体来源的MSC(BM-MSC)模拟免疫惰性成纤维细胞。相比之下,本发明的MSC聚集在一起(多批次,早期和晚期传代)。这表明本发明的MSC具有免疫活性。
图3示出了基于蛋白质分泌的细胞特征。本发明的MSC显示出相对于骨髓来源的MSC而言的MIP-1α、SDF-1α、IL-27、LIF、IL-1β、IL-2、IL-5、IL-12p70、IL-13、IL-17A、IL-31、G-CSF/CSF-3、IFN-γ、TNF-α、HGF、MCP-1、IL-9、bNGF、MIP-3α、Gro-α/KC、IL-1α、IL-23、MMP-1、IL-18、M-CSF、IL-21、M-CSF、IL-21、CD40L、IL-22、VEGF-A、BLC、Tweak、ENA-78(LIX)、MCP-3、MIF和嗜酸性细胞活化趋化因子-3的分泌增加。本发明的MSC显示出相对于骨髓来源的MSC而言的IL-6、IL-8和IL-4的分泌减少。分泌数据的定量另外参见表1。
在绵羊急性呼吸窘迫综合征(ARDS)模型中评估了本发明的MSC的体内功效。在此严重ARDS的绵羊模型中,接受MSC的动物在几个参数(包括氧合;全身血压;和肺/肺泡渗透性)上表现出相对于对照动物的明显改善。
获得体重30至40kg的成年美利奴母绵羊。对于此研究,一个20只母绵羊;使用N=8只绵羊/组。此研究是随机的,并在大型动物重症监护环境中进行。每只绵羊的研究持续时间为48小时,并且给药方案为2剂MSC(10,000,000cell/kg)或对照(PlasmaLite A)。在急性肺损伤后1小时和24小时施用NC-MSC或对照。在损伤后1小时开始通过IV输注(中心线)施用MSC或对照1小时,并在损伤后24小时以类似的方式重复给药。
在至少14天的隔离时间后,对绵羊进行手术准备,测量心率、全身动脉压、肺动脉压(包括心输出量)、肺动脉楔压、左心房压和中心静脉压。在一些绵羊的尾侧纵隔淋巴结的传出血管插管,用于肺血管内液体流量评估。这些仪器程序是在异氟醚麻醉下通过气管导管进行的。
手术恢复5至7天后,在清醒、未麻醉的绵羊中以30min的间隔进行两次呼吸和血流动力学变量的基线测量。基线变量包括心肺血流动力学和动脉和静脉血气分析。
在深度麻醉(静脉注射10至15mg/kg的氯胺酮)和镇痛(0.1至0.27mg/kg的丁丙诺啡SR)下,放置气管造口管,并通过吸入异氟醚(2%至5%)支持麻醉。在咳嗽反射被抑制时,通过支气管镜将铜绿假单胞菌滴入肺部。将活的铜绿假单胞菌(总共2.5至3.5x 1011CFU)悬浮在30mL的0.9%生理盐水中,并通过纤维支气管镜以直接观察的方式将其滴入肺的右中叶、右下叶和左下叶(各10ml)。细菌滴注后,用异氟醚继续麻醉大约10分钟,以预防通过咳嗽将滴入的细菌过早咳出。
此外,将Foley导管插入膀胱并采集基线尿液样本。
损伤后,将绵羊放置在机械呼吸机上(Avea APVcmv模式:RR 20b/m,TV 12mL/kg,PEEP 5cmH
治疗后的研究评估以与基线变量相同的方式进行。研究评估包括血流动力学监测、肺气体交换和全血细胞计数、肺淋巴流量及其蛋白质等。
安乐死后(在达到安乐死标准或完成48小时研究期时进行),取出肺组织并在左肺中进行支气管肺泡灌洗。
PaO
图5示出了接受本发明的MSC与对照的ARDS模型绵羊对去甲肾上腺素的需求。此数据表明与对照组相比,MSC治疗组的全身血压得到改善,例如更少的休克/更少的加压支持。
图6A至B示出了与对照相比,MSC治疗组的肺血管损伤减少。具体地,图6A示出了了肺淋巴流量。图6B示出了肺淋巴蛋白丢失。肺/肺泡通透性。因此,图6A至B尤其示出了过量肺淋巴流量产生和相关蛋白质损失的减少。
图7A-C示出了ARDS模型绵羊中与对照组相比,MSC治疗组中的组织细菌计数。图7A示出了MSC中与支气管肺泡灌洗液(BALF)、肺和脾脏的对照设置相比的细菌生长。图7B示出了与对照组相比,MSC治疗组中的BALF细菌负荷计数。图7C示出了与对照组相比,MSC治疗组的脾脏细菌负荷计数。
MSC被工程化改造以表达和分泌所需的蛋白质,例如用于癌症治疗。
图8示出了mRNA电穿孔后间充质干细胞(MSC)中的细胞因子表达。用2μg RNA对200,000个间充质干细胞进行电穿孔,所述RNA编码:TRAIL、IL7-(G
图9示出了电穿孔和冷冻后MSC中的TRAIL表达。用编码TRAIL的mRNA(1μg RNA/100,000个细胞)对来源于诱导多能干细胞的2,000,000(2M)和6,000,000(6M)个MSC进行电穿孔并立即冷冻。将细胞解冻、铺板并放置24小时,然后使用兔抗hTRAIL一抗(C92B9,CellSignaling Technology)和AlexaFluor 488驴抗兔二抗(A21206,Invitrogen)固定和染色。
图10示出了用编码TRAIL的RNA对iPSC来源的MSC进行电穿孔后的TRAIL分泌。用1μg RNA/100,000个细胞对2×10
图11Calu3人肺腺癌细胞生长至约80%融合并使用TrypLE Select CTS解离。将细胞颗粒化并重悬在400μL来自于在MSC培养基(Mesencult,Stem Cell Technologies)、MSC培养基或Calu3培养基(αMEM+10% FBS)中以指定条件,用重组hTRAIL(310-04,Peprotech)电穿孔的MSC的上清液中。将细胞铺板24h,用TrypLE Select CTS解离,用膜联蛋白V和碘化丙啶染色以鉴定凋亡和坏死细胞。通过流式细胞术对细胞进行计数。星号表示相对于使用非配对双边t检验确定的Calu3培养基样品的显著性。*P<0.05;**P<0.01;***P<0.005
等效方案
尽管已经结合其具体的实施方案描述本发明,但应理解本发明能够具有另外的修改,并且本申请旨在涵盖大体上符合本发明原理的、包括虽然不属于本发明所公开内容范围但属于本发明所属领域的公知技术或常用的技术手段并可以应用于上文中阐述和所附权利要求的范围所列出的必要特征中的任何变型、用途或者变更。
本领域技术人员将认识到或将能够确定仅使用常规实验的本文具体描述的特定实施方案的许多等效物。此类等效方案意图包含于下列权利要求中。
以引用的方式并入
本文所引用的所有专利和出版物以全部引用的方式并入本文中。
本文所讨论的公布仅针对它们在本申请提交日之前的公开内容而提供。本文没有任何内容被解释为承认本发明没有资格先于现有发明的这种出版物。
如本文所用,所有标题仅用于组织并且不旨在以任何方式限制公开内容。任何单个部分的内容可能同样适用于所有部分。
序列表
<110> 菲克特生物科学股份有限公司(Factor Bioscience Inc.)
安格尔·马修(ANGEL, Matthew)
罗德·克里斯托弗 (ROHDE, Christopher)
哈里斯·贾斯敏(HARRIS, Jasmine)
<120> 间充质干细胞疗法
<130> FAB-016PC/107541-5016
<150> US 63/016,626
<151> 2020-04-28
<160> 7
<170> PatentIn version 3.5
<210> 1
<211> 360
<212> PRT
<213> 人工序列(Artificial Sequence)
<220>
<223> 合成聚合物
<400> 1
Met Ala Gly His Leu Ala Ser Asp Phe Ala Phe Ser Pro Pro Pro Gly
1 5 10 15
Gly Gly Gly Asp Gly Pro Gly Gly Pro Glu Pro Gly Trp Val Asp Pro
20 25 30
Arg Thr Trp Leu Ser Phe Gln Gly Pro Pro Gly Gly Pro Gly Ile Gly
35 40 45
Pro Gly Val Gly Pro Gly Ser Glu Val Trp Gly Ile Pro Pro Cys Pro
50 55 60
Pro Pro Tyr Glu Phe Cys Gly Gly Met Ala Tyr Cys Gly Pro Gln Val
65 70 75 80
Gly Val Gly Leu Val Pro Gln Gly Gly Leu Glu Thr Ser Gln Pro Glu
85 90 95
Gly Glu Ala Gly Val Gly Val Glu Ser Asn Ser Asp Gly Ala Ser Pro
100 105 110
Glu Pro Cys Thr Val Thr Pro Gly Ala Val Lys Leu Glu Lys Glu Lys
115 120 125
Leu Glu Gln Asn Pro Glu Glu Ser Gln Asp Ile Lys Ala Leu Gln Lys
130 135 140
Glu Leu Glu Gln Phe Ala Lys Leu Leu Lys Gln Lys Arg Ile Thr Leu
145 150 155 160
Gly Tyr Thr Gln Ala Asp Val Gly Leu Thr Leu Gly Val Leu Phe Gly
165 170 175
Lys Val Phe Ser Gln Thr Thr Ile Cys Arg Phe Glu Ala Leu Gln Leu
180 185 190
Ser Phe Lys Asn Met Cys Lys Leu Arg Pro Leu Leu Gln Lys Trp Val
195 200 205
Glu Glu Ala Asp Asn Asn Glu Asn Leu Gln Glu Ile Cys Lys Ala Glu
210 215 220
Thr Leu Val Gln Ala Arg Lys Arg Lys Arg Thr Ser Ile Glu Asn Arg
225 230 235 240
Val Arg Gly Asn Leu Glu Asn Leu Phe Leu Gln Cys Pro Lys Pro Thr
245 250 255
Leu Gln Gln Ile Ser His Ile Ala Gln Gln Leu Gly Leu Glu Lys Asp
260 265 270
Val Val Arg Val Trp Phe Cys Asn Arg Arg Gln Lys Gly Lys Arg Ser
275 280 285
Ser Ser Asp Tyr Ala Gln Arg Glu Asp Phe Glu Ala Ala Gly Ser Pro
290 295 300
Phe Ser Gly Gly Pro Val Ser Phe Pro Leu Ala Pro Gly Pro His Phe
305 310 315 320
Gly Thr Pro Gly Tyr Gly Ser Pro His Phe Thr Ala Leu Tyr Ser Ser
325 330 335
Val Pro Phe Pro Glu Gly Glu Ala Phe Pro Pro Val Ser Val Thr Thr
340 345 350
Leu Gly Ser Pro Met His Ser Asn
355 360
<210> 2
<211> 317
<212> PRT
<213> 人工序列(Artificial Sequence)
<220>
<223> 合成聚合物
<400> 2
Met Tyr Asn Met Met Glu Thr Glu Leu Lys Pro Pro Gly Pro Gln Gln
1 5 10 15
Thr Ser Gly Gly Gly Gly Gly Asn Ser Thr Ala Ala Ala Ala Gly Gly
20 25 30
Asn Gln Lys Asn Ser Pro Asp Arg Val Lys Arg Pro Met Asn Ala Phe
35 40 45
Met Val Trp Ser Arg Gly Gln Arg Arg Lys Met Ala Gln Glu Asn Pro
50 55 60
Lys Met His Asn Ser Glu Ile Ser Lys Arg Leu Gly Ala Glu Trp Lys
65 70 75 80
Leu Leu Ser Glu Thr Glu Lys Arg Pro Phe Ile Asp Glu Ala Lys Arg
85 90 95
Leu Arg Ala Leu His Met Lys Glu His Pro Asp Tyr Lys Tyr Arg Pro
100 105 110
Arg Arg Lys Thr Lys Thr Leu Met Lys Lys Asp Lys Tyr Thr Leu Pro
115 120 125
Gly Gly Leu Leu Ala Pro Gly Gly Asn Ser Met Ala Ser Gly Val Gly
130 135 140
Val Gly Ala Gly Leu Gly Ala Gly Val Asn Gln Arg Met Asp Ser Tyr
145 150 155 160
Ala His Met Asn Gly Trp Ser Asn Gly Ser Tyr Ser Met Met Gln Asp
165 170 175
Gln Leu Gly Tyr Pro Gln His Pro Gly Leu Asn Ala His Gly Ala Ala
180 185 190
Gln Met Gln Pro Met His Arg Tyr Asp Val Ser Ala Leu Gln Tyr Asn
195 200 205
Ser Met Thr Ser Ser Gln Thr Tyr Met Asn Gly Ser Pro Thr Tyr Ser
210 215 220
Met Ser Tyr Ser Gln Gln Gly Thr Pro Gly Met Ala Leu Gly Ser Met
225 230 235 240
Gly Ser Val Val Lys Ser Glu Ala Ser Ser Ser Pro Pro Val Val Thr
245 250 255
Ser Ser Ser His Ser Arg Ala Pro Cys Gln Ala Gly Asp Leu Arg Asp
260 265 270
Met Ile Ser Met Tyr Leu Pro Gly Ala Glu Val Pro Glu Pro Ala Ala
275 280 285
Pro Ser Arg Leu His Met Ser Gln His Tyr Gln Ser Gly Pro Val Pro
290 295 300
Gly Thr Ala Ile Asn Gly Thr Leu Pro Leu Ser His Met
305 310 315
<210> 3
<211> 479
<212> PRT
<213> 人工序列(Artificial Sequence)
<220>
<223> 合成聚合物
<400> 3
Met Arg Gln Pro Pro Gly Glu Ser Asp Met Ala Val Ser Asp Ala Leu
1 5 10 15
Leu Pro Ser Phe Ser Thr Phe Ala Ser Gly Pro Ala Gly Arg Glu Lys
20 25 30
Thr Leu Arg Gln Ala Gly Ala Pro Asn Asn Arg Trp Arg Glu Glu Leu
35 40 45
Ser His Met Lys Arg Leu Pro Pro Val Leu Pro Gly Arg Pro Tyr Asp
50 55 60
Leu Ala Ala Ala Thr Val Ala Thr Asp Leu Glu Ser Gly Gly Ala Gly
65 70 75 80
Ala Ala Cys Gly Gly Ser Asn Leu Ala Pro Leu Pro Arg Arg Glu Thr
85 90 95
Glu Glu Phe Asn Asp Leu Leu Asp Leu Asp Phe Ile Leu Ser Asn Ser
100 105 110
Leu Thr His Pro Pro Glu Ser Val Ala Ala Thr Val Ser Ser Ser Ala
115 120 125
Ser Ala Ser Ser Ser Ser Ser Pro Ser Ser Ser Gly Pro Ala Ser Ala
130 135 140
Pro Ser Thr Cys Ser Phe Thr Tyr Pro Ile Arg Ala Gly Asn Asp Pro
145 150 155 160
Gly Val Ala Pro Gly Gly Thr Gly Gly Gly Leu Leu Tyr Gly Arg Glu
165 170 175
Ser Ala Pro Pro Pro Thr Ala Pro Phe Asn Leu Ala Asp Ile Asn Asp
180 185 190
Val Ser Pro Ser Gly Gly Phe Val Ala Glu Leu Leu Arg Pro Glu Leu
195 200 205
Asp Pro Val Tyr Ile Pro Pro Gln Gln Pro Gln Pro Pro Gly Gly Gly
210 215 220
Leu Met Gly Lys Phe Val Leu Lys Ala Ser Leu Ser Ala Pro Gly Ser
225 230 235 240
Glu Tyr Gly Ser Pro Ser Val Ile Ser Val Ser Lys Gly Ser Pro Asp
245 250 255
Gly Ser His Pro Val Val Val Ala Pro Tyr Asn Gly Gly Pro Pro Arg
260 265 270
Thr Cys Pro Lys Ile Lys Gln Glu Ala Val Ser Ser Cys Thr His Leu
275 280 285
Gly Ala Gly Pro Pro Leu Ser Asn Gly His Arg Pro Ala Ala His Asp
290 295 300
Phe Pro Leu Gly Arg Gln Leu Pro Ser Arg Thr Thr Pro Thr Leu Gly
305 310 315 320
Leu Glu Glu Val Leu Ser Ser Arg Asp Cys His Pro Ala Leu Pro Leu
325 330 335
Pro Pro Gly Phe His Pro His Pro Gly Pro Asn Tyr Pro Ser Phe Leu
340 345 350
Pro Asp Gln Met Gln Pro Gln Val Pro Pro Leu His Tyr Gln Glu Leu
355 360 365
Met Pro Pro Gly Ser Cys Met Pro Glu Glu Pro Lys Pro Lys Arg Gly
370 375 380
Arg Arg Ser Trp Pro Arg Lys Arg Thr Ala Thr His Thr Cys Asp Tyr
385 390 395 400
Ala Gly Cys Gly Lys Thr Tyr Thr Lys Ser Ser His Leu Lys Ala His
405 410 415
Leu Arg Thr His Thr Gly Glu Lys Pro Tyr His Cys Asp Trp Asp Gly
420 425 430
Cys Gly Trp Lys Phe Ala Arg Ser Asp Glu Leu Thr Arg His Tyr Arg
435 440 445
Lys His Thr Gly His Arg Pro Phe Gln Cys Gln Lys Cys Asp Arg Ala
450 455 460
Phe Ser Arg Ser Asp His Leu Ala Leu His Met Lys Arg His Phe
465 470 475
<210> 4
<211> 454
<212> PRT
<213> 人工序列(Artificial Sequence)
<220>
<223> 合成聚合物
<400> 4
Met Asp Phe Phe Arg Val Val Glu Asn Gln Gln Pro Pro Ala Thr Met
1 5 10 15
Pro Leu Asn Val Ser Phe Thr Asn Arg Asn Tyr Asp Leu Asp Tyr Asp
20 25 30
Ser Val Gln Pro Tyr Phe Tyr Cys Asp Glu Glu Glu Asn Phe Tyr Gln
35 40 45
Gln Gln Gln Gln Ser Glu Leu Gln Pro Pro Ala Pro Ser Glu Asp Ile
50 55 60
Trp Lys Lys Phe Glu Leu Leu Pro Thr Pro Pro Leu Ser Pro Ser Arg
65 70 75 80
Arg Ser Gly Leu Cys Ser Pro Ser Tyr Val Ala Val Thr Pro Phe Ser
85 90 95
Leu Arg Gly Asp Asn Asp Gly Gly Gly Gly Ser Phe Ser Thr Ala Asp
100 105 110
Gln Leu Glu Met Val Thr Glu Leu Leu Gly Gly Asp Met Val Asn Gln
115 120 125
Ser Phe Ile Cys Asp Pro Asp Asp Glu Thr Phe Ile Lys Asn Ile Ile
130 135 140
Ile Gln Asp Cys Met Trp Ser Gly Phe Ser Ala Ala Ala Lys Leu Val
145 150 155 160
Ser Glu Lys Leu Ala Ser Tyr Gln Ala Ala Arg Lys Asp Ser Gly Ser
165 170 175
Pro Asn Pro Ala Arg Gly His Ser Val Cys Ser Thr Ser Ser Leu Tyr
180 185 190
Leu Gln Asp Leu Ser Ala Ala Ala Ser Glu Cys Ile Asp Pro Ser Val
195 200 205
Val Phe Pro Tyr Pro Leu Asn Asp Ser Ser Ser Pro Lys Ser Cys Ala
210 215 220
Ser Gln Asp Ser Ser Ala Phe Ser Pro Ser Ser Asp Ser Leu Leu Ser
225 230 235 240
Ser Thr Glu Ser Ser Pro Gln Gly Ser Pro Glu Pro Leu Val Leu His
245 250 255
Glu Glu Thr Pro Pro Thr Thr Ser Ser Asp Ser Glu Glu Glu Gln Glu
260 265 270
Asp Glu Glu Glu Ile Asp Val Val Ser Val Glu Lys Arg Gln Ala Pro
275 280 285
Gly Lys Arg Ser Glu Ser Gly Ser Pro Ser Ala Gly Gly His Ser Lys
290 295 300
Pro Pro His Ser Pro Leu Val Leu Lys Arg Cys His Val Ser Thr His
305 310 315 320
Gln His Asn Tyr Ala Ala Pro Pro Ser Thr Arg Lys Asp Tyr Pro Ala
325 330 335
Ala Lys Arg Val Lys Leu Asp Ser Val Arg Val Leu Arg Gln Ile Ser
340 345 350
Asn Asn Arg Lys Cys Thr Ser Pro Arg Ser Ser Asp Thr Glu Glu Asn
355 360 365
Val Lys Arg Arg Thr His Asn Val Leu Glu Arg Gln Arg Arg Asn Glu
370 375 380
Leu Lys Arg Ser Phe Phe Ala Leu Arg Asp Gln Ile Pro Glu Leu Glu
385 390 395 400
Asn Asn Glu Lys Ala Pro Lys Val Val Ile Leu Lys Lys Ala Thr Ala
405 410 415
Tyr Ile Leu Ser Val Gln Ala Glu Glu Gln Lys Leu Ile Ser Glu Glu
420 425 430
Asp Leu Leu Arg Lys Arg Arg Glu Gln Leu Lys His Lys Leu Glu Gln
435 440 445
Leu Arg Asn Ser Cys Ala
450
<210> 5
<211> 846
<212> DNA
<213> 人工序列(Artificial Sequence)
<220>
<223> 合成聚合物
<400> 5
atggccatga tggaagtgca gggtgggccc tccctcgggc agacgtgcgt gctcatagtc 60
attttcaccg tgctcctcca gagcctgtgc gtcgccgtca cgtacgtgta cttcaccaac 120
gagctgaagc agatgcagga caagtacagc aagtcgggga tcgcctgctt cctgaaggag 180
gacgactcct actgggaccc gaacgacgag gagtccatga actccccgtg ctggcaggtc 240
aagtggcagc tgcggcagct ggtccgcaag atgatcctcc ggaccagcga ggagactatc 300
agcaccgtcc aggagaagca gcagaacatc tccccgctcg tccgggagcg aggtccccag 360
cgggtagcgg ctcatatcac cggcacccgc gggaggtcga acacgctcag ctcgccgaac 420
tccaagaacg agaaggccct cggccgcaag atcaactcct gggagagctc gcggagcggg 480
cactcgttcc tgtcgaacct gcatctgcgg aacggcgagc tcgtgatcca cgagaagggc 540
ttctactaca tctacagcca gacctacttc cggttccagg aggagatcaa ggagaacacc 600
aagaacgaca agcagatggt gcagtacatc tacaagtaca ccagctaccc cgacccgatc 660
ctcctgatga agtccgcccg caacagctgc tggagcaagg acgcggagta cggcctgtac 720
agcatctacc agggcggcat cttcgagctc aaggagaacg accgcatctt cgtgagcgtg 780
acgaacgagc acctgatcga catggaccac gaggcctcct tcttcggggc gttcctggtc 840
ggttga 846
<210> 6
<211> 708
<212> DNA
<213> 人工序列(Artificial Sequence)
<220>
<223> 合成聚合物
<400> 6
atgacagtgc tggcgcccgc ctggtccccc acaacctacc tcctcctgct gctgttgctg 60
tcgtcgggcc tgagcgggac gcaggactgc tcgttccagc acagcccgat ctcctccgac 120
ttcgcggtca agatccggga gctgagcgac tacctgttgc aggactaccc cgtcaccgtc 180
gcctccaacc tgcaggacga ggagctctgc ggtggcttgt ggcgtctggt gttggctcag 240
cgctggatgg agcggctcaa gacggtcgcg gggtccaaga tgcagggcct gctcgagcgc 300
gtgaacacgg agatccactt cgtcaccaag tgcgccttcc agccgccacc cagctgcctg 360
cggttcgtcc agaccaacat ctcccgcctc ctgcaggaga catccgagca gctggtggcg 420
ctgaagccct ggatcacgcg ccagaacttc tcccgatgcc tggagctgca gtgccagcct 480
gactcctcaa ccctgccacc tccatggagt ccccggcctt tggaggccac cgcgcccact 540
gctccgcagc ccccactcct cttgctactc ctgctccccg taggccttct actgctggcc 600
gcagcctggt gcctacattg gcaaagaacg cggcgacgta caccccgccc tggggagcag 660
gtgcccccag tccccagtcc ccaggacctg ctgcttgtgg agcactga 708
<210> 7
<211> 906
<212> DNA
<213> 人工序列(Artificial Sequence)
<220>
<223> 合成聚合物
<400> 7
atgttccacg tgtcgttccg gtacatcttc ggcctcccgc cgctcatcct ggtcctgctc 60
cccgtggcgt cctcggactg cgacatcgag ggcaaggacg ggaagcagta cgagtcggtg 120
ctgatggtgt ccatcgacca gctgctcgac tccatgaagg agatcgggtc gaactgcctc 180
aacaacgagt tcaacttctt caagcgccac atctgcgacg cgaacaagga ggggatgttc 240
ctcttccggg cggcccgcaa gctccggcag ttcctcaaga tgaacagcac gggggacttc 300
gacctgcacc tgctgaaggt gtcggagggc accaccatcc tcctcaactg caccggccag 360
gtcaagggcc ggaagcccgc cgccctgggc gaggcgcagc ccacgaagtc cctcgaggag 420
aacaagtccc tcaaggagca gaagaagctc aacgacctgt gcttcctcaa gcggctcctc 480
caggagatca agacctgctg gaacaagatc ctcatgggca ccaaggagca cgggggcggc 540
gggagcggcg ggggtggctc caactgggtg aacgtcatct cggacctcaa gaagatcgag 600
gacctgatcc agagcatgca catcgacgcc acgctctaca ccgagtcgga cgtccacccg 660
tcgtgcaagg tcaccgccat gaagtgcttc ctcctggagc tgcaggtcat ctcgctggag 720
tccggcgacg ccagcatcca cgacacggtc gagaacctca tcatcctcgc gaacaactcc 780
ctcagctcga acggcaacgt gacggagagc gggtgcaagg agtgcgagga gctggaggag 840
aagaacatca aggagttcct gcagagcttc gtgcacatcg tgcagatgtt catcaacacc 900
agctga 906
- 一种用于直接分化多能性干细胞来源间充质干细胞的培养基、用其制备间充质干细胞的方法以及由此制备的间充质干细胞
- 评估间充质干细胞群体的伤口愈合效力的方法以及选择间充质干细胞和鉴定作为用于产生间充质干细胞群体的起始材料的组织的相关方法
